Similar presentations:
Углеводы
1. УГЛЕВОДЫ
2.
УГЛЕВОДЫПРОСТЫЕ
УГЛЕВОДЫ
(моносахариды)
СЛОЖНЫЕ
УГЛЕВОДЫ
(олиго- и полисахариды)
3. Углеводы
• По способности к гидролизу:- Моносахариды (простые сахара, монозы)
не гидролизуются с образованием более
простых углеводов.
- Олигосахариды - соединения, имеющие в
своем составе от 2 до 10 остатков
моносахаридов, связанных О–гликозидными
связями.
- Полисахариды, представляющие собой
высокомолекулярные вещества,
соединенные О–гликозидными связями, со
степенью полимеризации выше 10.
4. Моносахариды
Гетерофункциональные соединения,содержат одновременно карбонильную
и несколько гидроксильных групп:
- полигидроксиальдегиды (альдозы)
- полигидроксикетоны (кетозы)
Для них характерна неразветвлённая
углеродная цепь.
Для названий моносахаридов используют
суффикс -оза
5.
• Все моносахариды представляют собойкристаллические вещества, хорошо
растворимые в воде и обладающие, как
правило, сладким вкусом. Они дают
нейтральную реакцию на лакмус и в
растворе существуют в открытой и
циклической формах, которые
находятся в состоянии динамического
равновесия.
6.
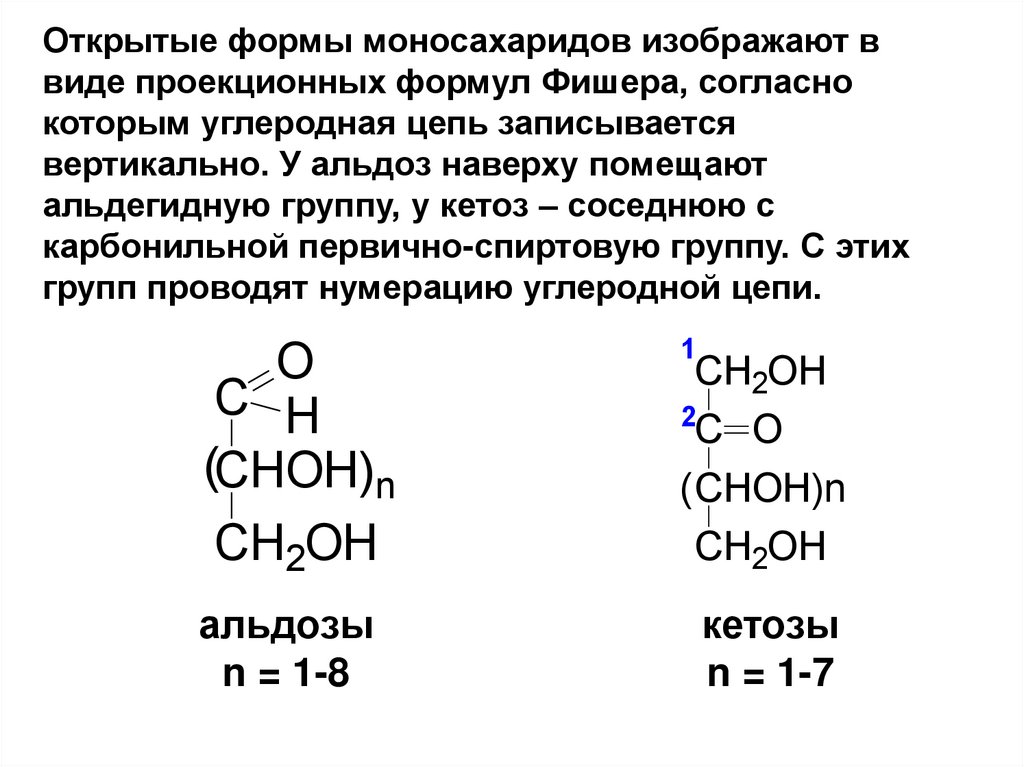
Открытые формы моносахаридов изображают ввиде проекционных формул Фишера, согласно
которым углеродная цепь записывается
вертикально. У альдоз наверху помещают
альдегидную группу, у кетоз – соседнюю с
карбонильной первично-спиртовую группу. С этих
групп проводят нумерацию углеродной цепи.
O
C H
(CHOH)n
CH2OH
CH2OH
2
C O
( CHOH)n
CH2OH
альдозы
n = 1-8
кетозы
n = 1-7
1
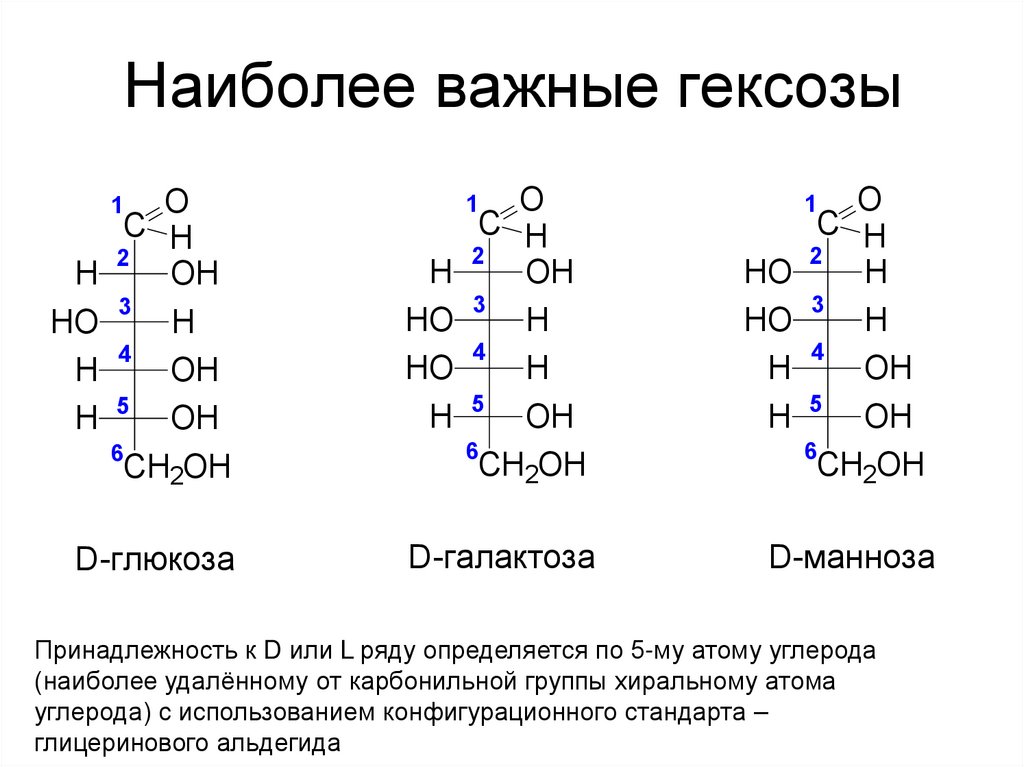
7. Наиболее важные гексозы
OC H
2
H
OH
3
HO
H
4
H
OH
H 5 OH
6
CH2OH
O
C H
2
H
OH
3
HO
H
4
HO
H
H 5 OH
6
CH2OH
O
C H
2
HO
H
3
HO
H
4
H
OH
H 5 OH
6
CH2OH
D-глюкоза
D-галактоза
D-манноза
1
1
1
Принадлежность к D или L ряду определяется по 5-му атому углерода
(наиболее удалённому от карбонильной группы хиральному атома
углерода) с использованием конфигурационного стандарта –
глицеринового альдегида
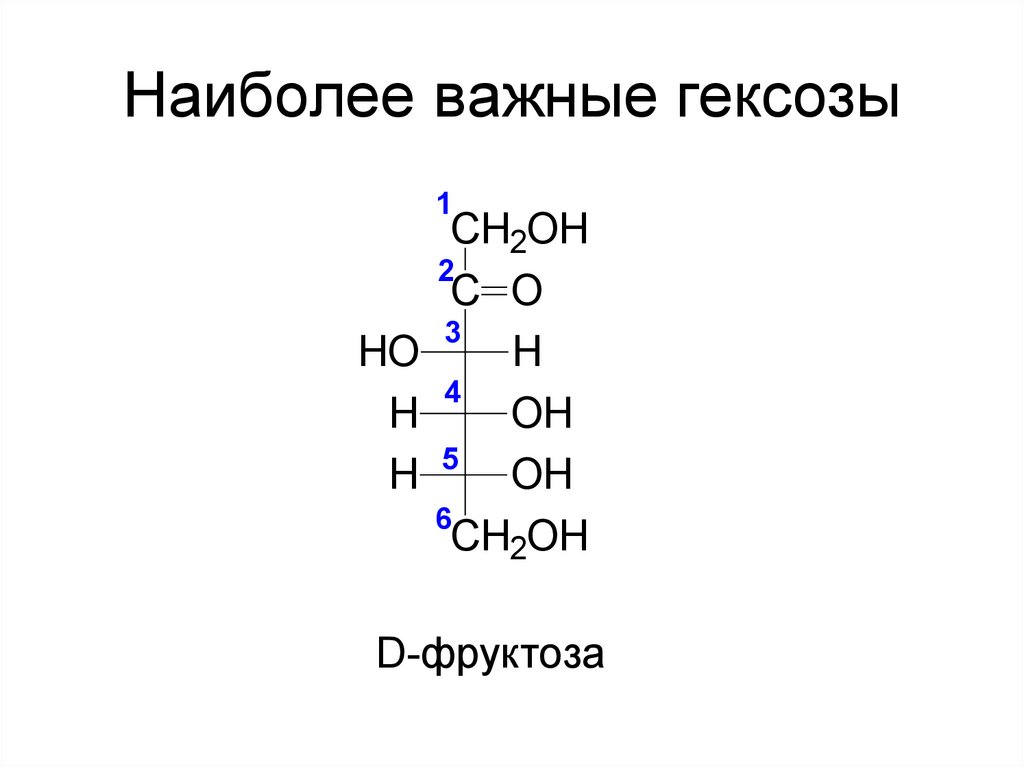
8. Наиболее важные гексозы
1CH2OH
2
C O
3
HO
H
4
H
OH
H 5 OH
6
CH2OH
D-фруктоза
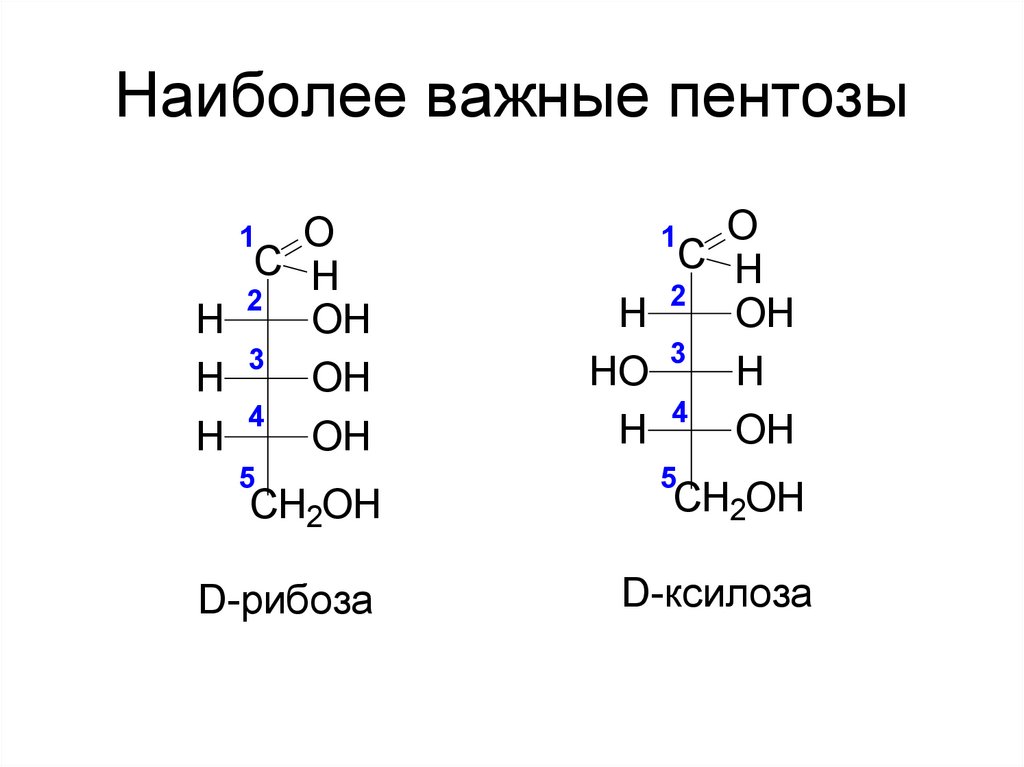
9. Наиболее важные пентозы
OC H
2
H
OH
3
H
OH
4
H
OH
1
5
CH2OH
D-рибоза
O
C H
2
H
OH
3
HO
H
4
H
OH
1
5
CH2OH
D-ксилоза
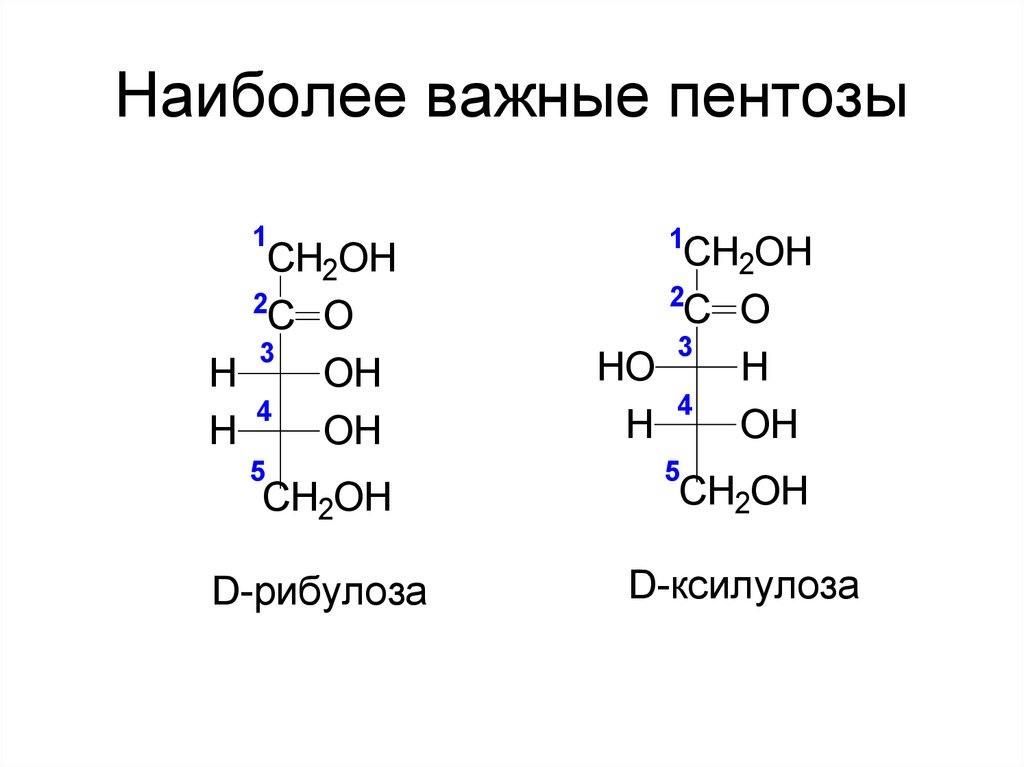
10. Наиболее важные пентозы
1CH2OH
2
C O
3
H
OH
4
H
OH
5
CH2OH
D-рибулоза
1
CH2OH
2
C O
3
HO
H
4
H
OH
5
CH2OH
D-ксилулоза
11. Циклические формы
- по химической природе являютсяциклическими полуацеталями.
Моносахариды за счет
внутримолекулярного взаимодействия
сближенных в пространстве
карбонильной и гидроксильной групп,
образуют устойчивые фуранозные
(пятичленные) или пиранозные
(шестичленные) циклы.
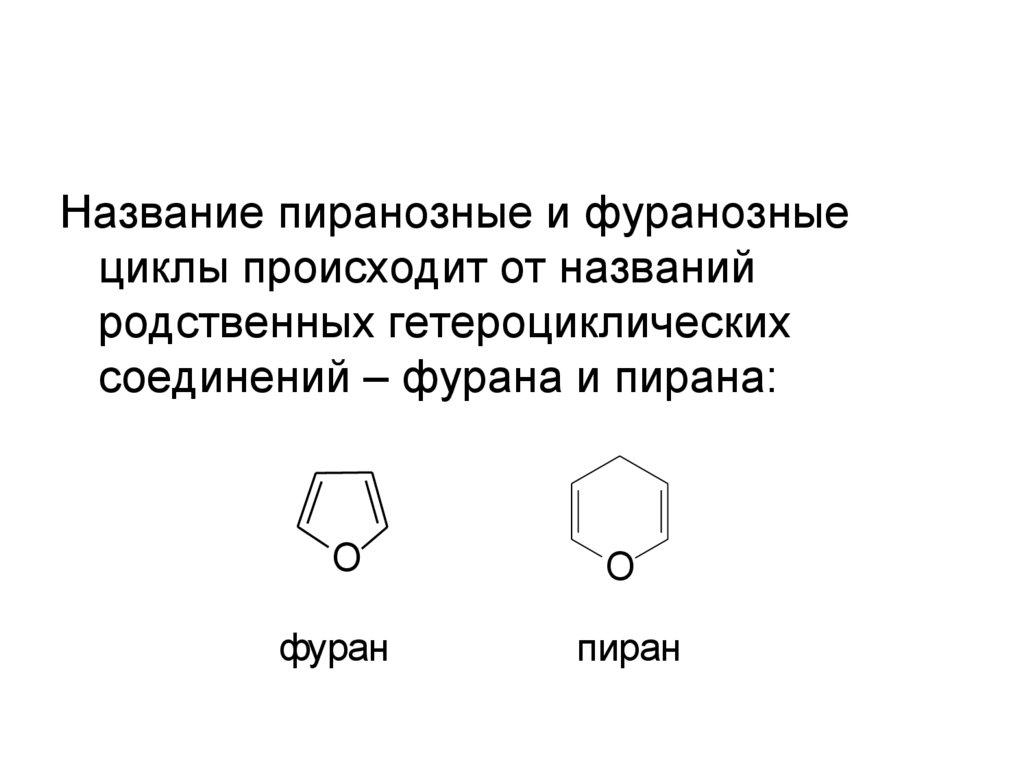
12.
Название пиранозные и фуранозныециклы происходит от названий
родственных гетероциклических
соединений – фурана и пирана:
O
O
фуран
пиран
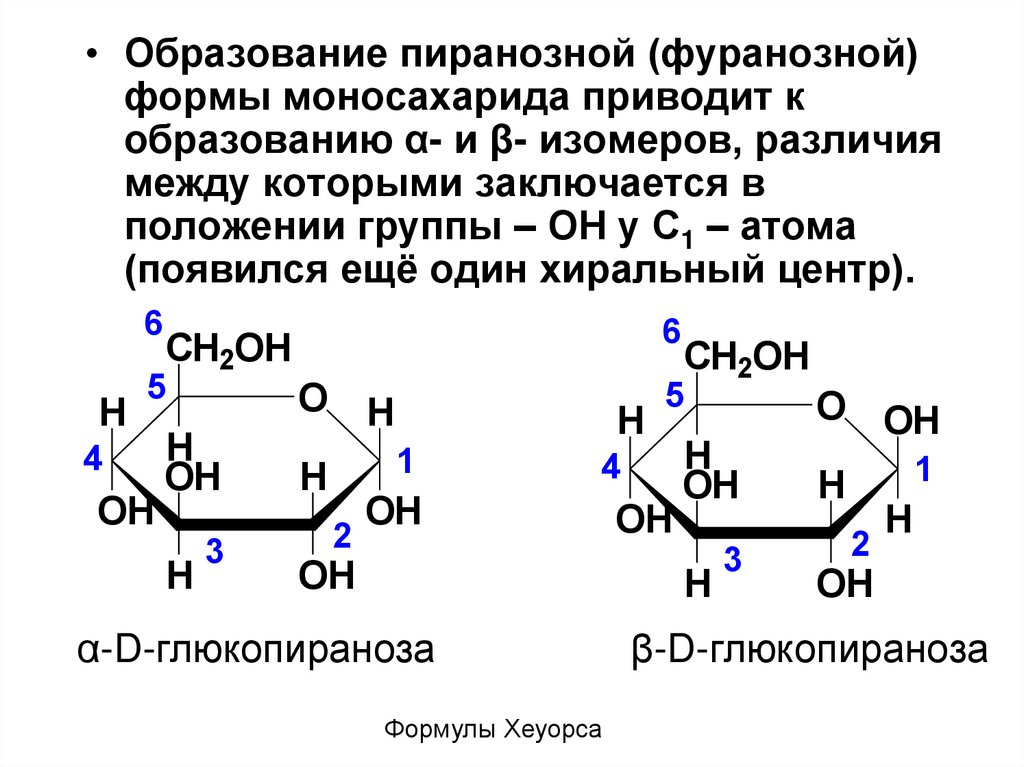
13.
• Образование пиранозной (фуранозной)формы моносахарида приводит к
образованию α- и β- изомеров, различия
между которыми заключается в
положении группы – ОН у С1 – атома
(появился ещё один хиральный центр).
6
H
5
4
OH
6
CH2OH
H
OH
H
3
O H
1
H
2
H
5
4
OH
OH
CH2OH
OH
H
OH
H
α-D-глюкопираноза
Формулы Хеуорса
3
O OH
1
H
2
H
OH
β-D-глюкопираноза
14.
• Появившаяся дополнительнаягидроксильная группа, связанная с С1 –
атомом, называется гликозидной
(полуацетальной). По свойствам она
значительно отличается от спиртовых
(гликозных) гидроксильных групп
моносахарида.
15.
• В растворах сахаров при стояниинаблюдается изменение угла
отклонения плоскости поляризованного
света, т.е. изменение оптической
активности – мутаротация.
• Объясняется установлением
равновесия между циклической и
нециклической формами , а также
между α- и β- формами. После
установления равновесия угол
отклонения ППС принимает
определённое значение.
16. ХИМИЧЕСКИЕ СВОЙСТВА МОНОСАХАРИДОВ
• I. Химические реакции с участиемгидроксильных групп.
I.1. Полуацетальный гидроксил непрочно
связан с атомом углерода и может
достаточно легко вступать во
взаимодействие со спиртами,
фенолами, карбоновыми кислотами,
аминами и т.д. (как правило, в условиях
кислотного катализа)
17.
CH2OHH
OH
H
OH
H
- H2O
OH
H
OH
OH
- H2O
CH2OH
CH2OH
H
OH
H
+ CH3COOH
+ CH3OH
H
O H
O H
H
H
OH
OH
OCH3
H
OH
H
O H
H
OH
CH3
O
C
O
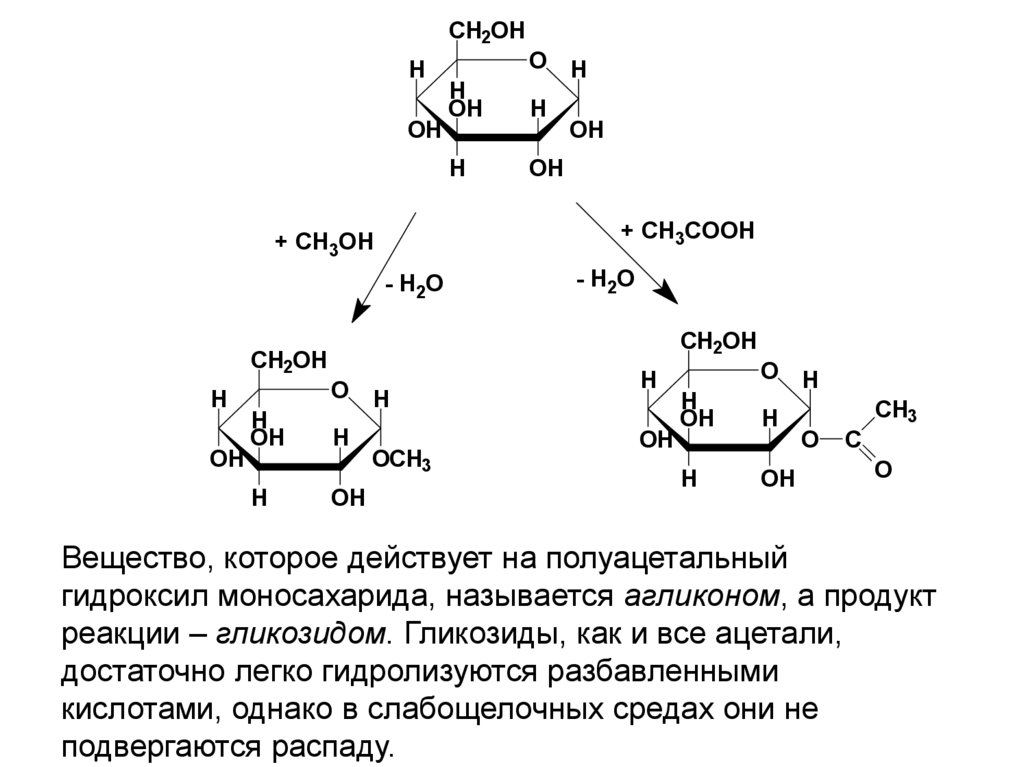
Вещество, которое действует на полуацетальный
гидроксил моносахарида, называется агликоном, а продукт
реакции – гликозидом. Гликозиды, как и все ацетали,
достаточно легко гидролизуются разбавленными
кислотами, однако в слабощелочных средах они не
подвергаются распаду.
18.
I.2. При определённых условиях вреакцию вступает не только
полуацетальный гидроксил, но и
имеющиеся в молекуле спиртовые
гидроксильные группы.
19.
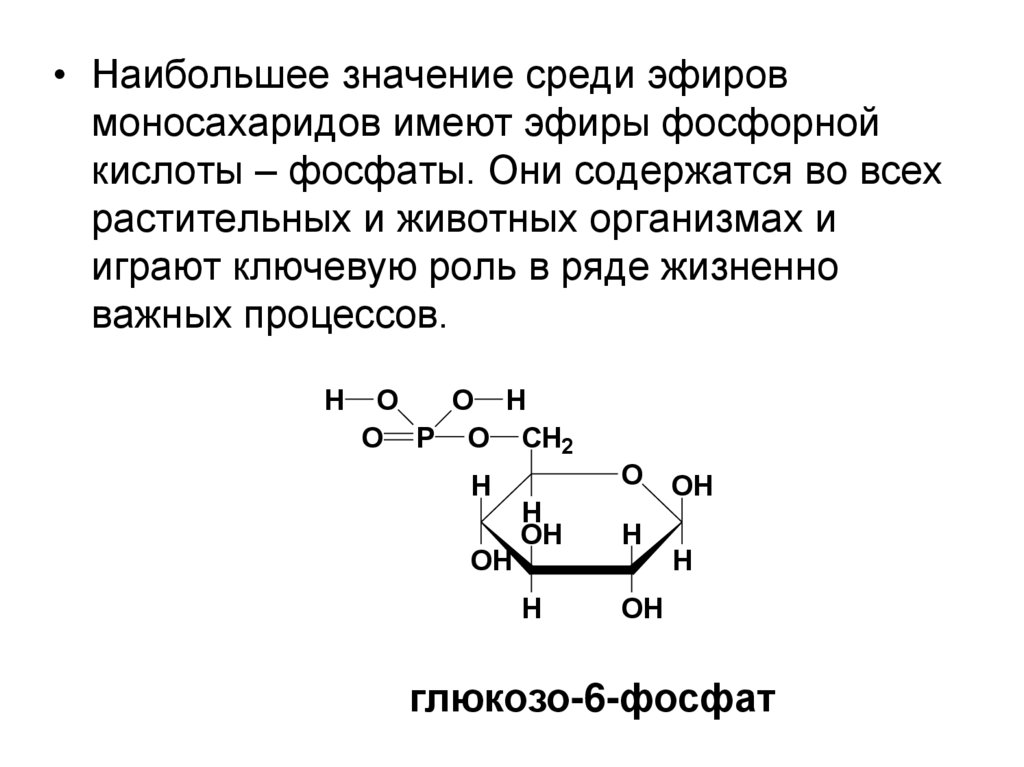
• Наибольшее значение среди эфировмоносахаридов имеют эфиры фосфорной
кислоты – фосфаты. Они содержатся во всех
растительных и животных организмах и
играют ключевую роль в ряде жизненно
важных процессов.
H
O
O H
O P O CH2
H
OH
H
OH
H
O OH
H
H
OH
глюкозо-6-фосфат
20.
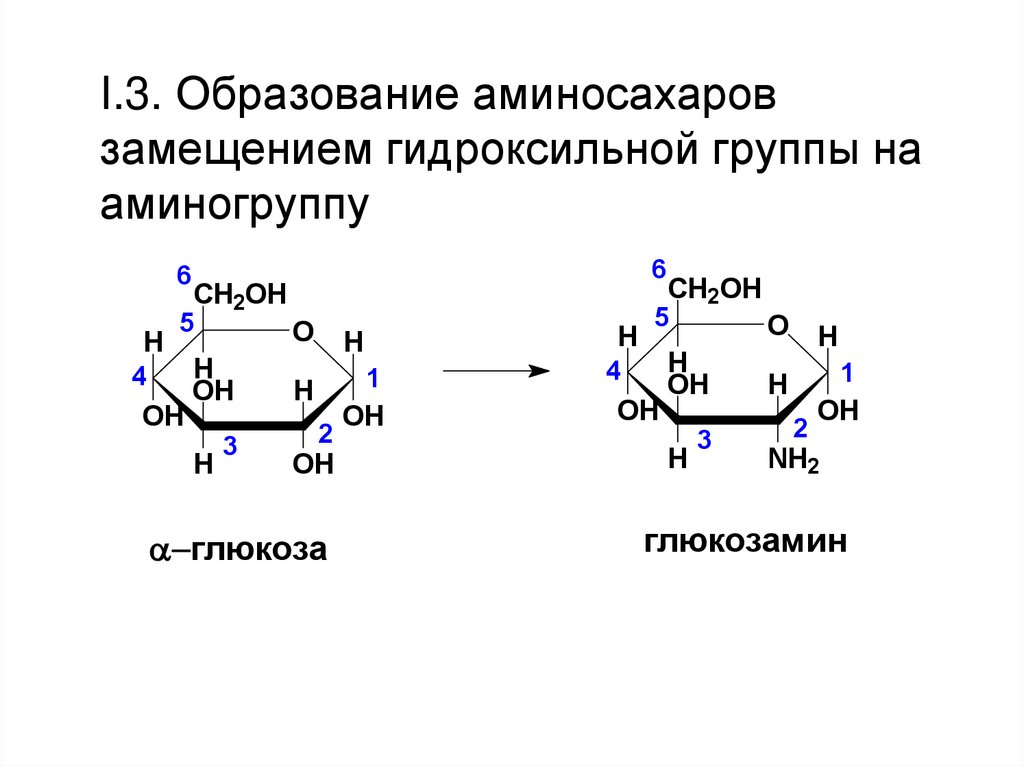
I.3. Образование аминосахаровзамещением гидроксильной группы на
аминогруппу
6
H
CH2OH
5
4
OH
6
H
OH
H
3
O H
H
1
H
2
OH
a-глюкоза
OH
CH2OH
5
4
OH
H
OH
H
3
O H
1
H
2
OH
NH2
глюкозамин
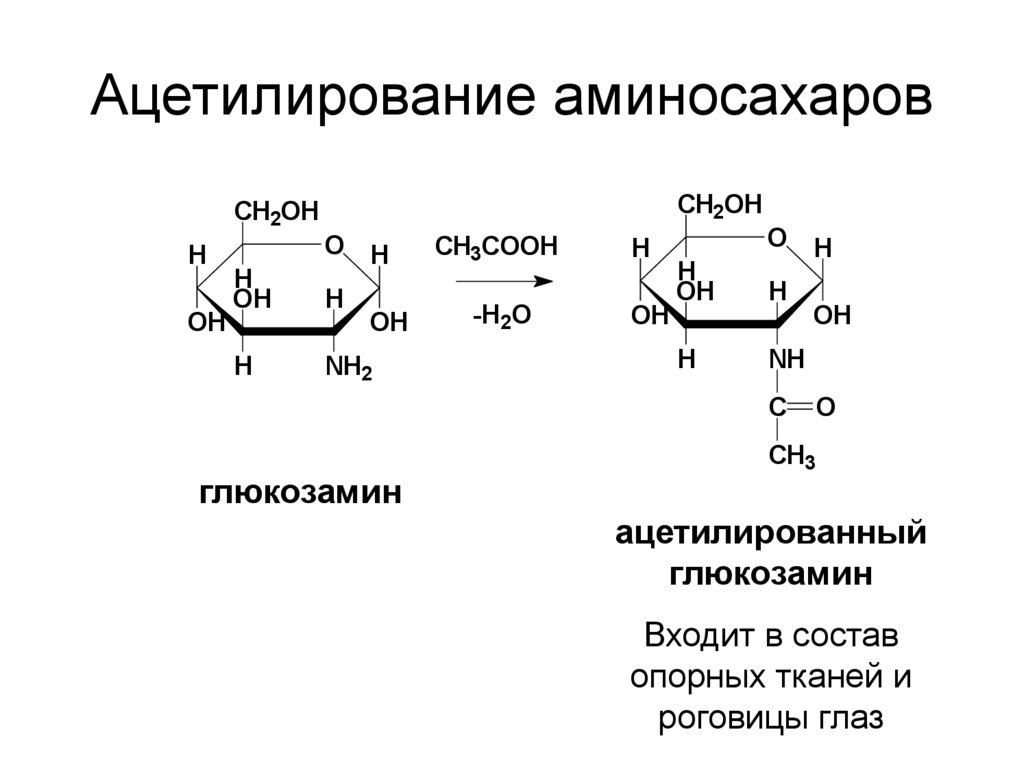
21. Ацетилирование аминосахаров
CH2OHCH2OH
H
OH
H
OH
H
O H
H
OH
NH2
CH3COOH
-H2O
H
OH
H
OH
H
O H
H
OH
NH
C
глюкозамин
O
CH3
ацетилированный
глюкозамин
Входит в состав
опорных тканей и
роговицы глаз
22.
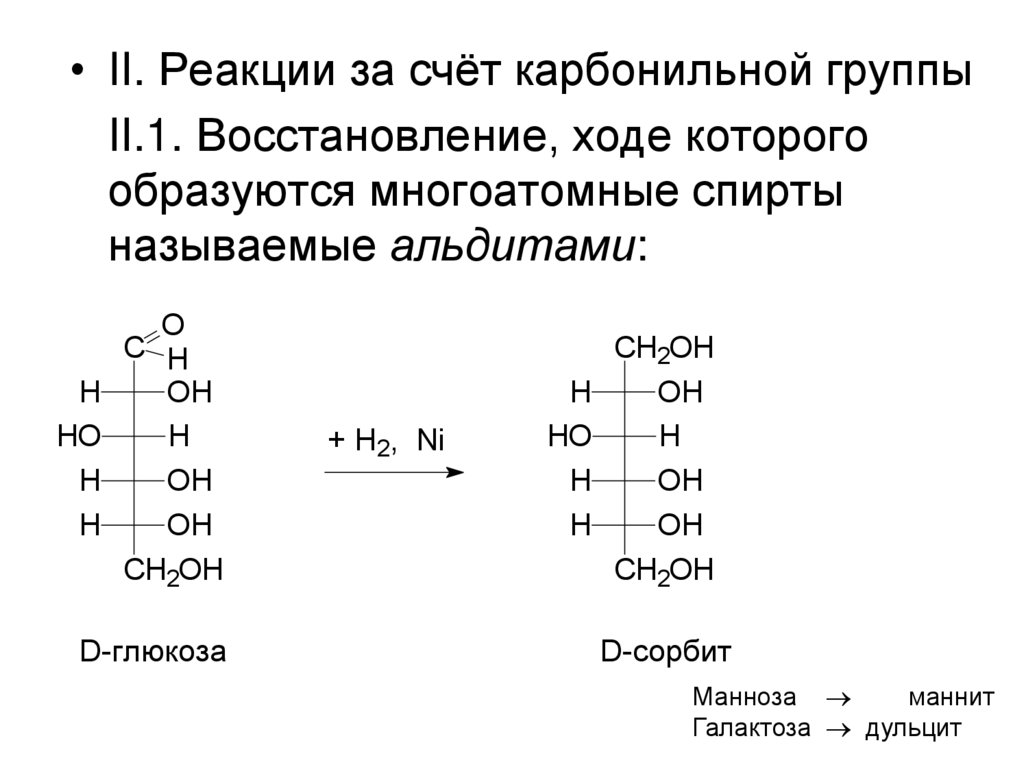
• II. Реакции за счёт карбонильной группыII.1. Восстановление, ходе которого
образуются многоатомные спирты
называемые альдитами:
O
C H
H
OH
HO
H
H
OH
H
OH
CH2OH
D-глюкоза
+ H2, Ni
CH2OH
H
OH
HO
H
H
OH
H
OH
CH2OH
D-сорбит
Манноза
маннит
Галактоза дульцит
23.
II.2. Окисление - важная реакция в химии углеводов. Егоиспользуют для получения ряда
соединений в структурных
исследованиях и биохимических
анализах.
В зависимости от условий окисления
моносахаридов образуются различные
продукты. В щелочной среде окисление
сопровождается разрушением
углеродной цепи молекулы (реакция
”серебряного зеркала”).
Окисление в нейтральной среде
позволяет сохранить углеродный
скелет.
24.
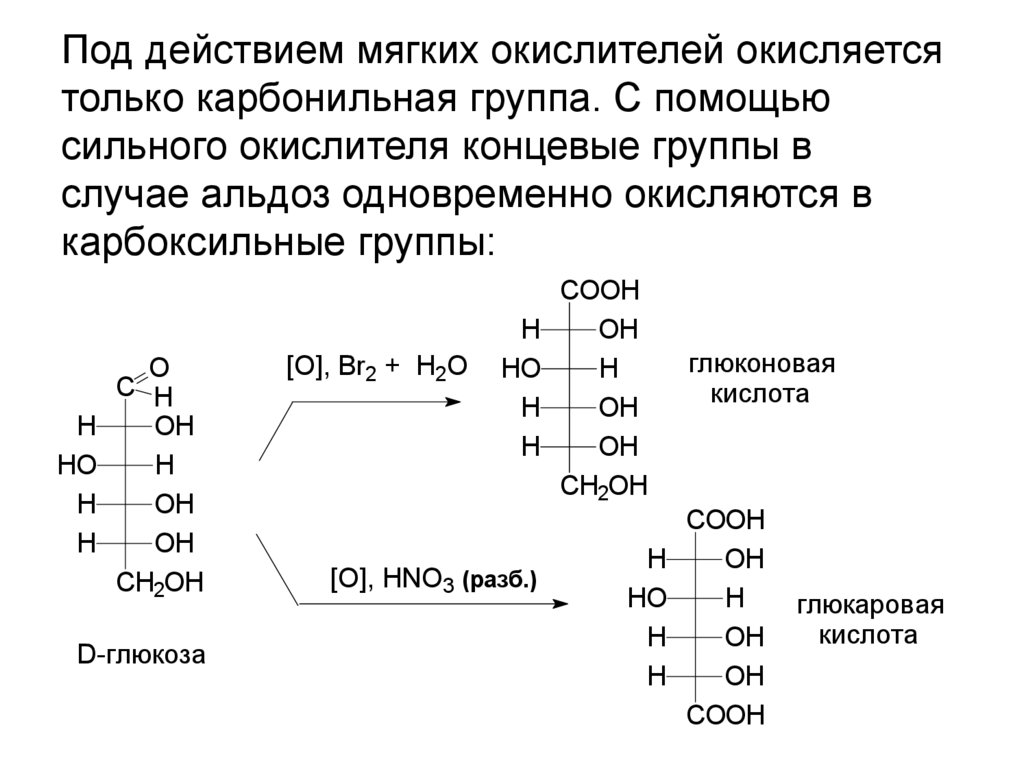
Под действием мягких окислителей окисляетсятолько карбонильная группа. С помощью
сильного окислителя концевые группы в
случае альдоз одновременно окисляются в
карбоксильные группы:
O
C H
H
OH
HO
H
H
OH
H
OH
CH2OH
D-глюкоза
[O], Br2 + H2O
COOH
H
OH
HO
H
H
OH
H
OH
CH2OH
[O], HNO3 (разб.)
глюконовая
кислота
COOH
H
OH
HO
H
H
OH
H
OH
COOH
глюкаровая
кислота
25.
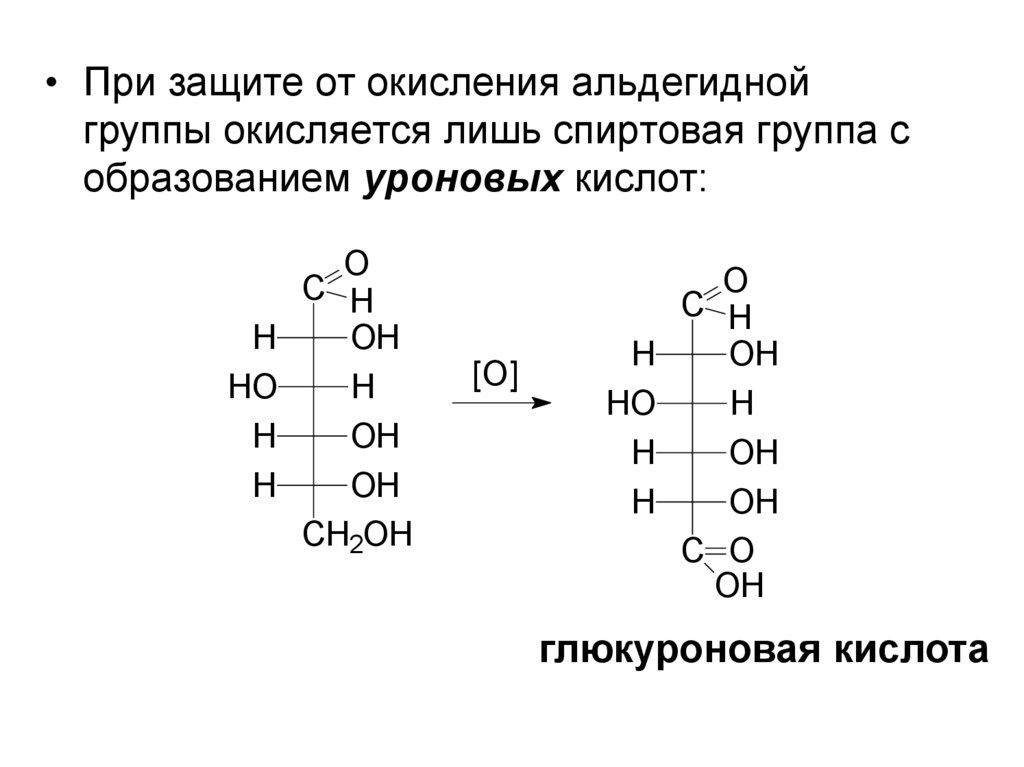
• При защите от окисления альдегиднойгруппы окисляется лишь спиртовая группа с
образованием уроновых кислот:
O
C H
H
OH
HO
H
H
OH
H
OH
CH2OH
[O]
O
C H
H
OH
HO
H
H
OH
H
OH
C O
OH
глюкуроновая кислота










 chemistry
chemistry








