Similar presentations:
Углеводы. Моносахариды
1. УГЛЕВОДЫ
2. Углеводы
• Входят в состав клеток и тканей всехрастительных и животных организмов.
• По массе составляют основную часть
органического вещества на Земле: на
долю углеводов приходится не менее
12% сухого веса любых организмов, они
составляют основную часть биомассы
растений (до 90 % сухого вещества).
3. Углеводы
• Источники энергии в метаболическихпроцессах (крахмал, гликоген)
• Структурные компоненты клеточных
стенок (целлюлоза, хитин и др.)
• Составные элементы жизненно важных
веществ (нуклеиновые кислоты и др.)
• Используются как лекарственные
средства
4. Углеводы
• Образуются в растениях в процессефотосинтеза из диоксида углерода и
воды.
• Животные организмы не способны
синтезировать углеводы и получают их
из растительных источников.
• Углеводы служат основным
ингредиентом пищи млекопитающих.
5. Углеводы
• Класс углеводов (сахаров,карбогидратов) объединяет
соединения, имеющие состав СnH2nOn и
обладающие при этом весьма
разнообразными свойствами.
6.
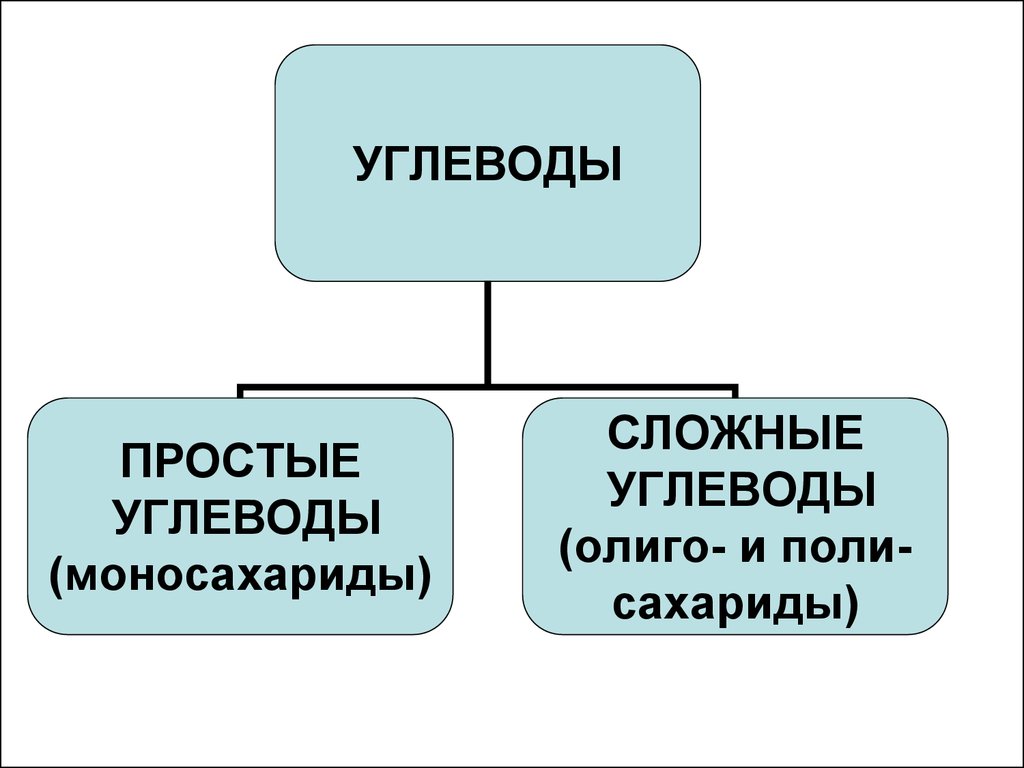
УГЛЕВОДЫПРОСТЫЕ
УГЛЕВОДЫ
(моносахариды)
СЛОЖНЫЕ
УГЛЕВОДЫ
(олиго- и полисахариды)
7. Углеводы
• По способности к гидролизу:- Моносахариды (простые сахара, монозы)
не гидролизуются с образованием более
простых углеводов.
- Олигосахариды - соединения, имеющие в
своем составе от 2 до 10 остатков
моносахаридов, связанных О–гликозидными
связями.
- Полисахариды, представляющие собой
высокомолекулярные вещества,
соединенные О–гликозидными связями, со
степенью полимеризации выше 10.
8. Моносахариды
Гетерофункциональные соединения,содержат одновременно карбонильную
и несколько гидроксильных групп:
- полигидроксиальдегиды (альдозы)
- полигидроксикетоны (кетозы)
Для них характерна неразветвлённая
углеродная цепь.
Для названий моносахаридов используют
суффикс -оза
9.
• Все моносахариды представляют собойкристаллические вещества, хорошо
растворимые в воде и обладающие, как
правило, сладким вкусом. Они дают
нейтральную реакцию на лакмус и в
растворе существуют в открытой и
циклической формах, которые
находятся в состоянии динамического
равновесия.
10.
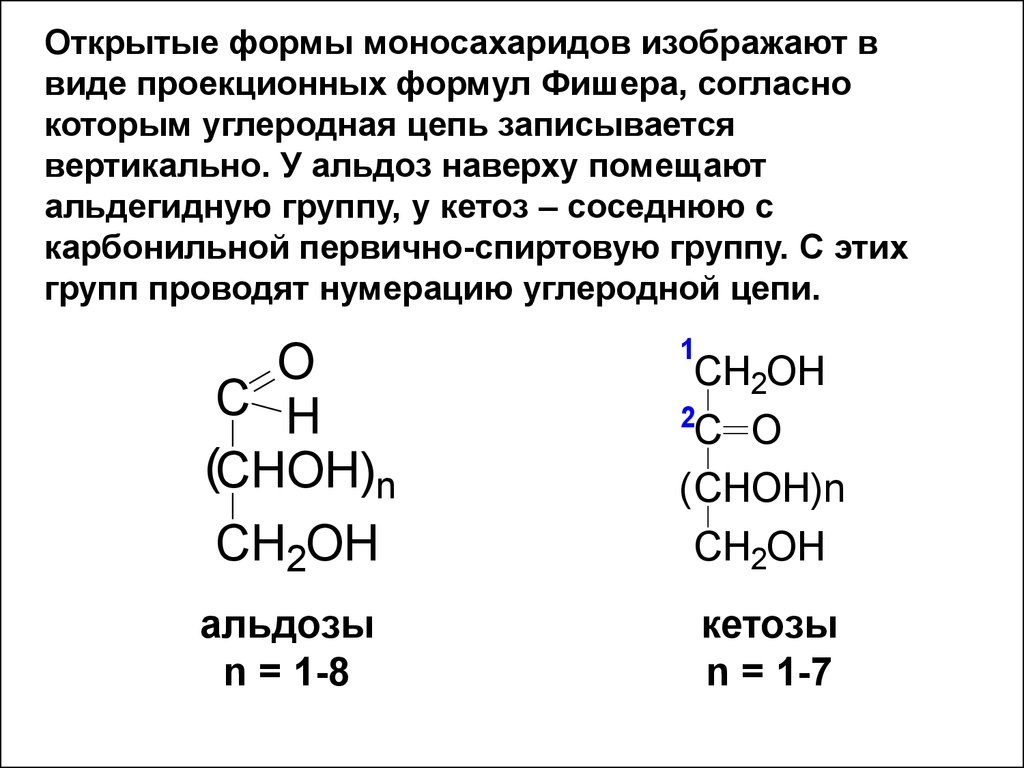
Открытые формы моносахаридов изображают ввиде проекционных формул Фишера, согласно
которым углеродная цепь записывается
вертикально. У альдоз наверху помещают
альдегидную группу, у кетоз – соседнюю с
карбонильной первично-спиртовую группу. С этих
групп проводят нумерацию углеродной цепи.
O
C H
(CHOH)n
CH2OH
альдозы
n = 1-8
1
CH2OH
2
C O
( CHOH)n
CH2OH
кетозы
n = 1-7
11. Моносахариды
• В зависимости от длины углероднойцепи (3 – 10 атомов):
- триозы
- тетрозы
- пентозы
- гексозы
- гептозы
12.
• Наличие в молекулах моносахаридовнескольких центров хиральности –
причина существования большого
числа стереоизомеров,
соответствующих одной и той же
структурной формуле.
13. Альдогексоза
HOCH2(*CHOH)4CHOчисло стереоизомеров = 24 = 16 (8 пар
энантиомеров)
В биологических средах преимущественно
распространены D-изомеры моносахаридов,
что обусловлено особенностями их
первичного синтеза в растениях. В связи с
этим, человек, животные, а также
микроорганизмы не способны усваивать Lизомеры.
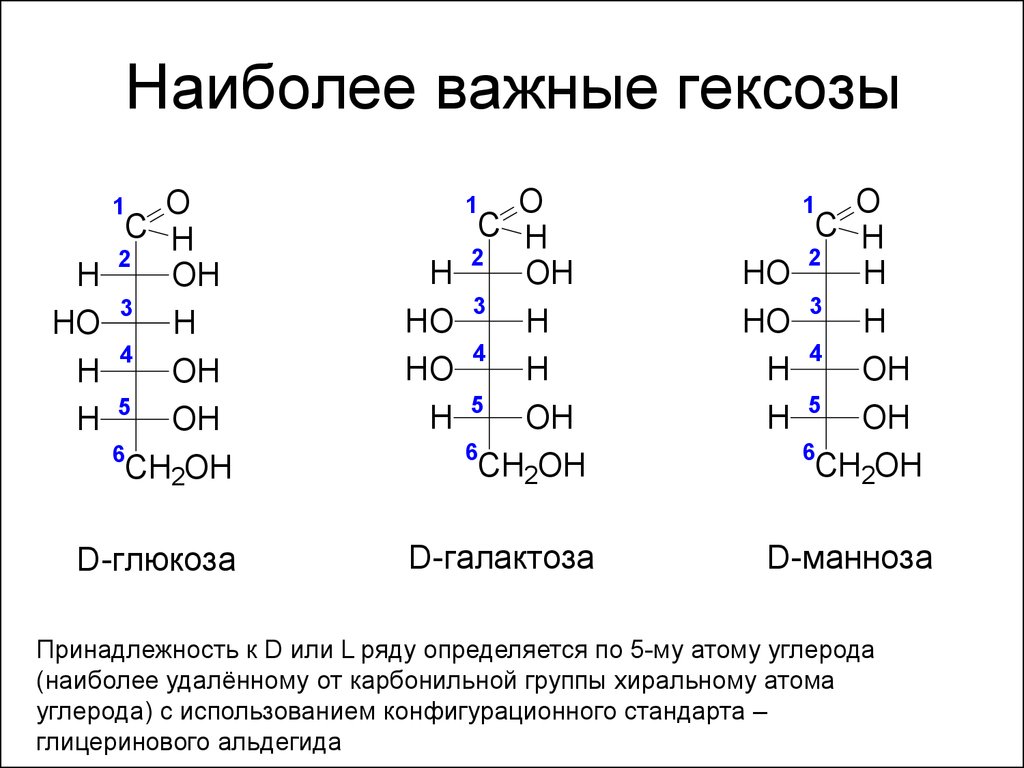
14. Наиболее важные гексозы
OC H
2
OH
3
H
4
OH
5
OH
6
CH2OH
H
HO
H
H
D-глюкоза
O
C H
2
OH
3
H
4
H
5
OH
6
CH2OH
1
1
H
HO
HO
H
D-галактоза
O
C H
2
H
3
H
4
OH
5
OH
6
CH2OH
1
HO
HO
H
H
D-манноза
Принадлежность к D или L ряду определяется по 5-му атому углерода
(наиболее удалённому от карбонильной группы хиральному атома
углерода) с использованием конфигурационного стандарта –
глицеринового альдегида
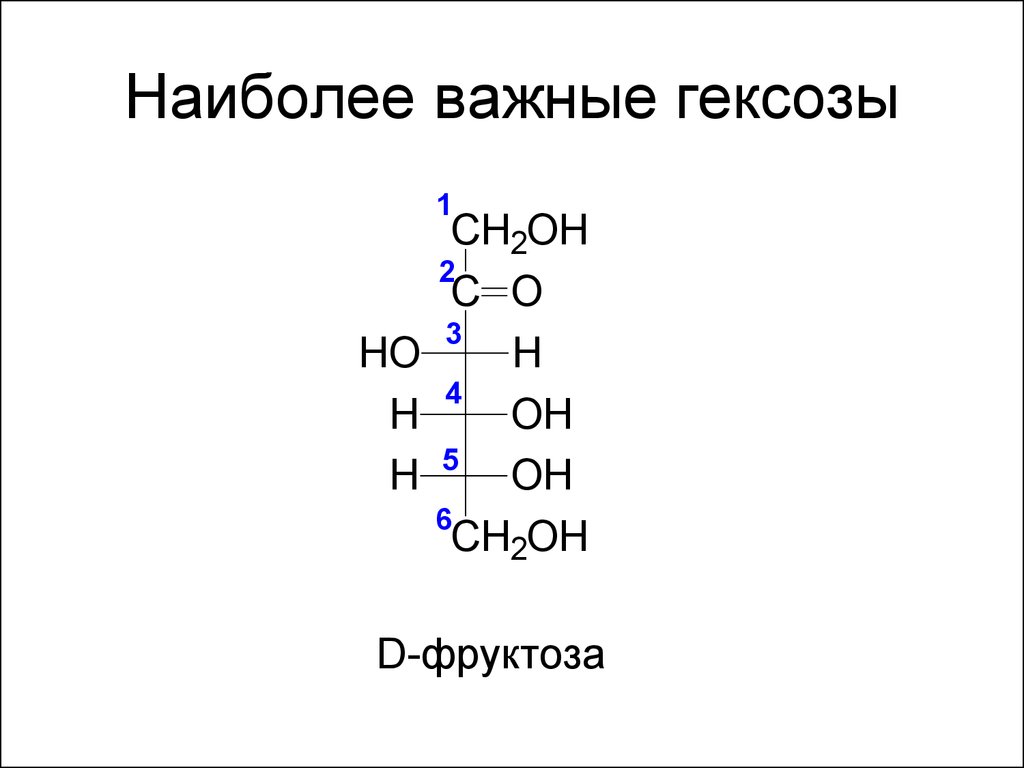
15. Наиболее важные гексозы
1CH2OH
2
C O
3
HO
H
4
H
OH
5
H
OH
6
CH2OH
D-фруктоза
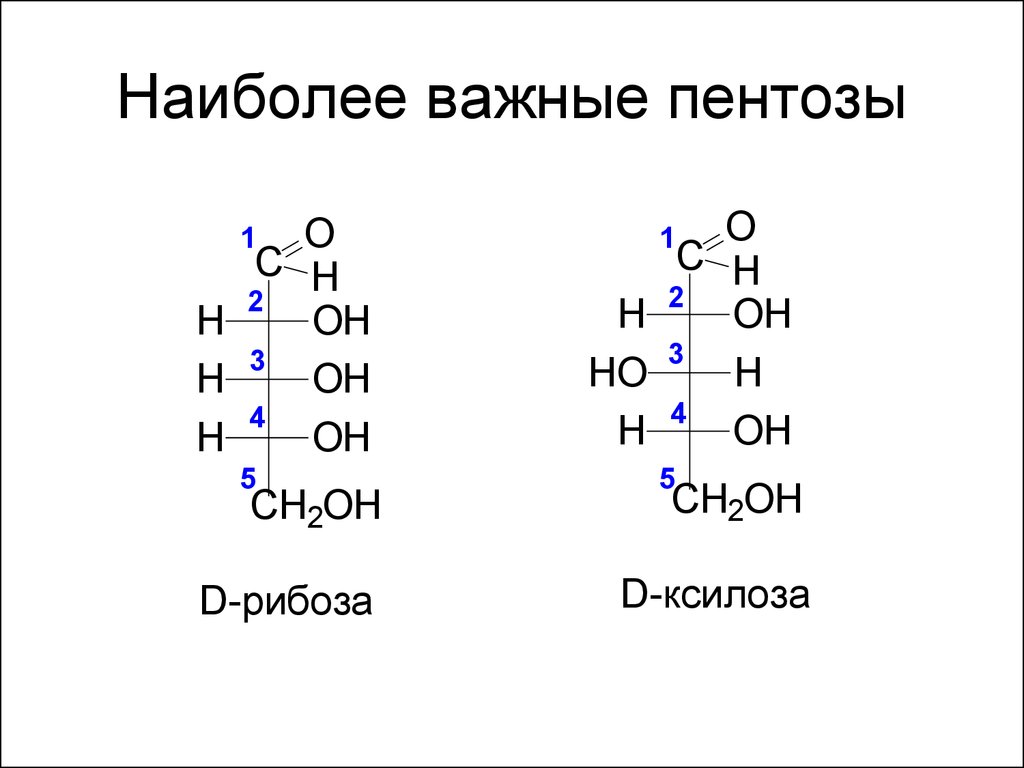
16. Наиболее важные пентозы
OC H
2
H
OH
3
H
OH
4
H
OH
1
5
CH2OH
D-рибоза
O
C H
2
H
OH
3
HO
H
4
H
OH
1
5
CH2OH
D-ксилоза
17. Наиболее важные пентозы
1CH2OH
2
C O
3
H
OH
4
H
OH
5
CH2OH
D-рибулоза
1
CH2OH
2
C O
3
HO
H
4
H
OH
5
CH2OH
D-ксилулоза
18. Циклические формы
- по химической природе являютсяциклическими полуацеталями.
Моносахариды за счет
внутримолекулярного взаимодействия
сближенных в пространстве
карбонильной и гидроксильной групп,
образуют устойчивые фуранозные
(пятичленные) или пиранозные
(шестичленные) циклы.
19.
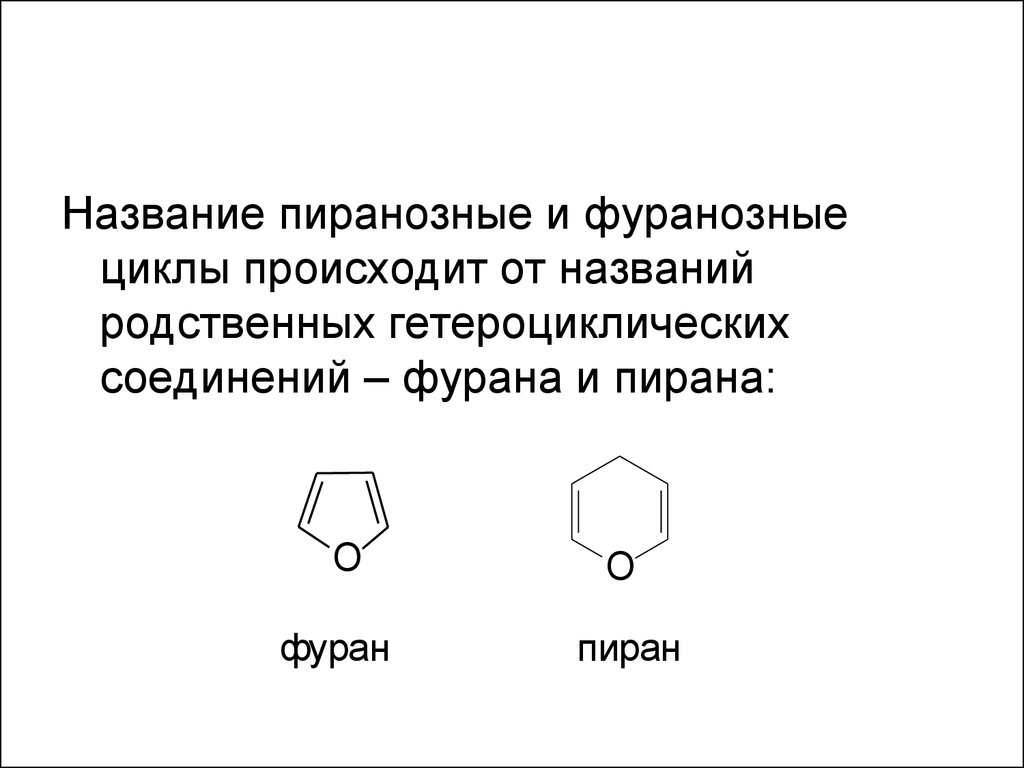
Название пиранозные и фуранозныециклы происходит от названий
родственных гетероциклических
соединений – фурана и пирана:
O
фуран
O
пиран
20.
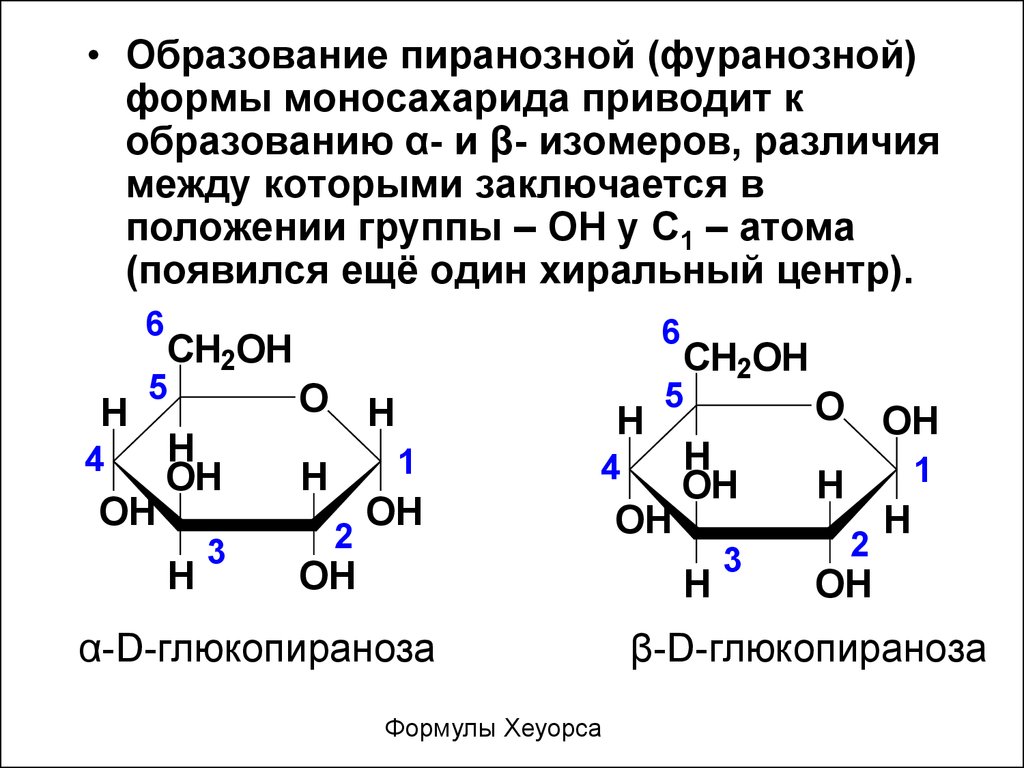
• Образование пиранозной (фуранозной)формы моносахарида приводит к
образованию α- и β- изомеров, различия
между которыми заключается в
положении группы – ОН у С1 – атома
(появился ещё один хиральный центр).
6
H
5
4
OH
6
CH2OH
H
OH
H
3
O H
1
H
2
H
5
4
OH
OH
CH2OH
OH
H
OH
H
α-D-глюкопираноза
Формулы Хеуорса
3
O OH
1
H
2
H
OH
β-D-глюкопираноза
21.
• Появившаяся дополнительнаягидроксильная группа, связанная с С1 –
атомом, называется гликозидной
(полуацетальной). По свойствам она
значительно отличается от спиртовых
(гликозных) гидроксильных групп
моносахарида.
22.
• В растворах сахаров при стояниинаблюдается изменение угла
отклонения плоскости поляризованного
света, т.е. изменение оптической
активности – мутаротация.
• Объясняется установлением
равновесия между циклической и
нециклической формами , а также
между α- и β- формами. После
установления равновесия угол
отклонения ППС принимает
определённое значение.
23. ХИМИЧЕСКИЕ СВОЙСТВА МОНОСАХАРИДОВ
• I. Химические реакции с участиемгидроксильных групп.
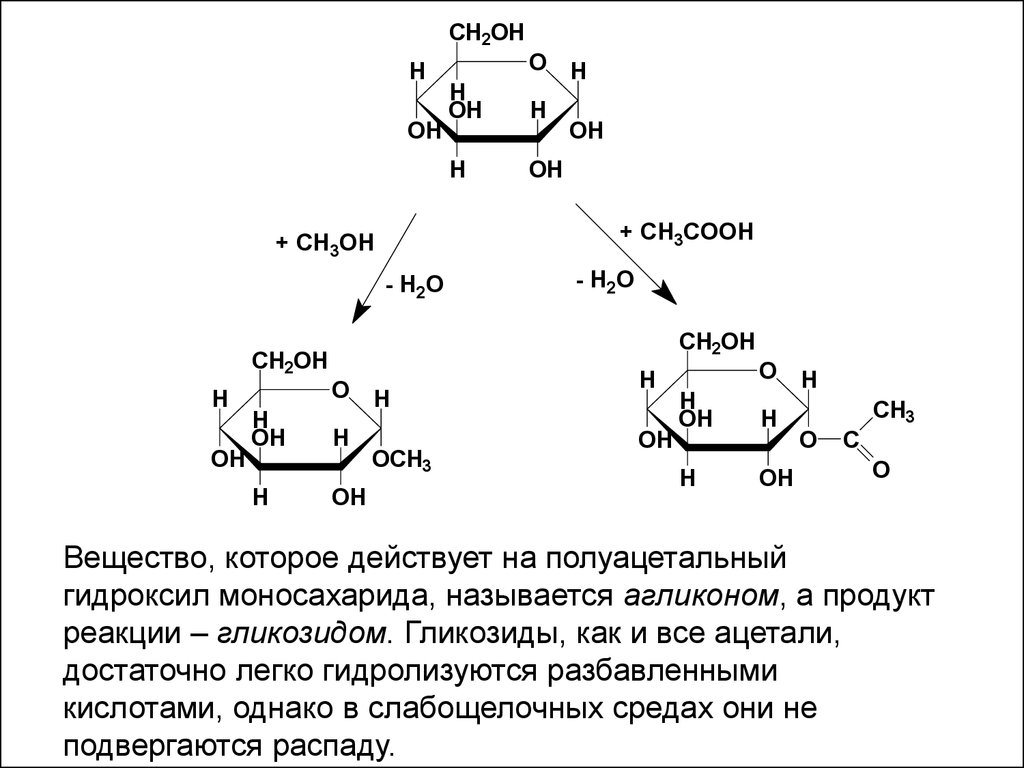
I.1. Полуацетальный гидроксил непрочно
связан с атомом углерода и может
достаточно легко вступать во
взаимодействие со спиртами,
фенолами, карбоновыми кислотами,
аминами и т.д. (как правило, в условиях
кислотного катализа)
24.
CH2OHH
OH
H
OH
H
- H2O
OH
H
OH
OH
- H2O
CH2OH
CH2OH
H
OH
H
+ CH3COOH
+ CH3OH
H
O H
O H
H
H
OH
OH
OCH3
H
OH
H
O H
H
OH
CH3
O
C
O
Вещество, которое действует на полуацетальный
гидроксил моносахарида, называется агликоном, а продукт
реакции – гликозидом. Гликозиды, как и все ацетали,
достаточно легко гидролизуются разбавленными
кислотами, однако в слабощелочных средах они не
подвергаются распаду.
25.
I.2. При определённых условиях вреакцию вступает не только
полуацетальный гидроксил, но и
имеющиеся в молекуле спиртовые
гидроксильные группы.
26.
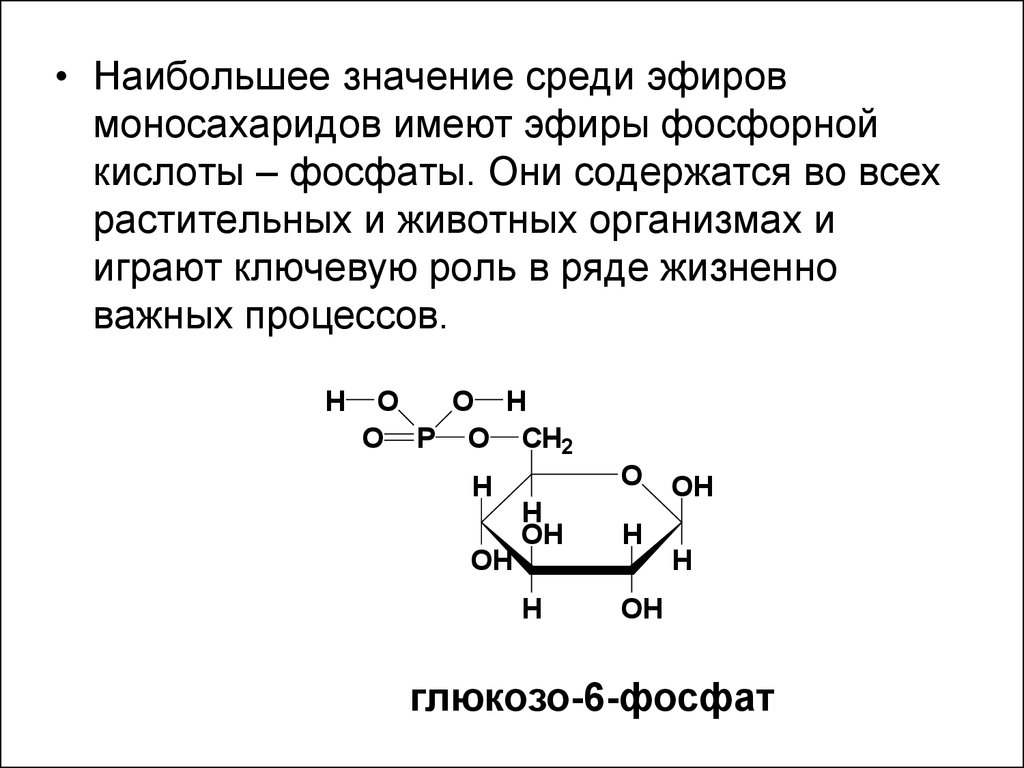
• Наибольшее значение среди эфировмоносахаридов имеют эфиры фосфорной
кислоты – фосфаты. Они содержатся во всех
растительных и животных организмах и
играют ключевую роль в ряде жизненно
важных процессов.
H
O
O H
O P O CH2
H
OH
H
OH
H
O OH
H
H
OH
глюкозо-6-фосфат
27.
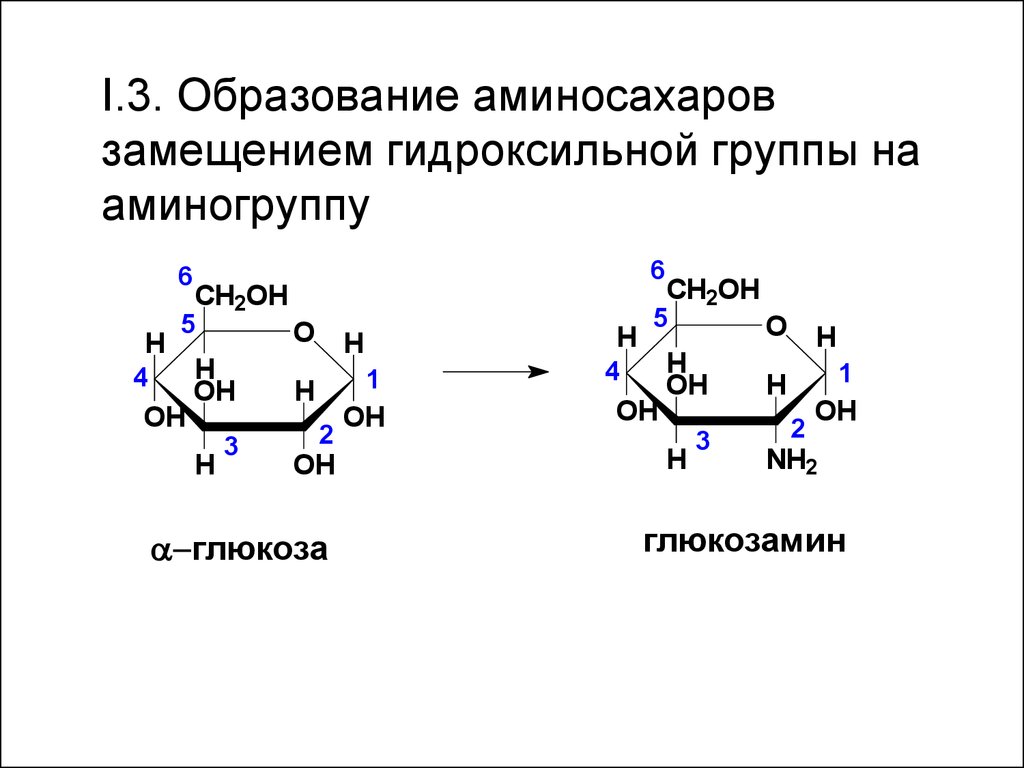
I.3. Образование аминосахаровзамещением гидроксильной группы на
аминогруппу
6
H
CH2OH
5
4
OH
6
H
OH
H
3
O H
H
1
H
2
OH
a-глюкоза
OH
CH2OH
5
4
OH
H
OH
H
3
O H
1
H
2
OH
NH2
глюкозамин
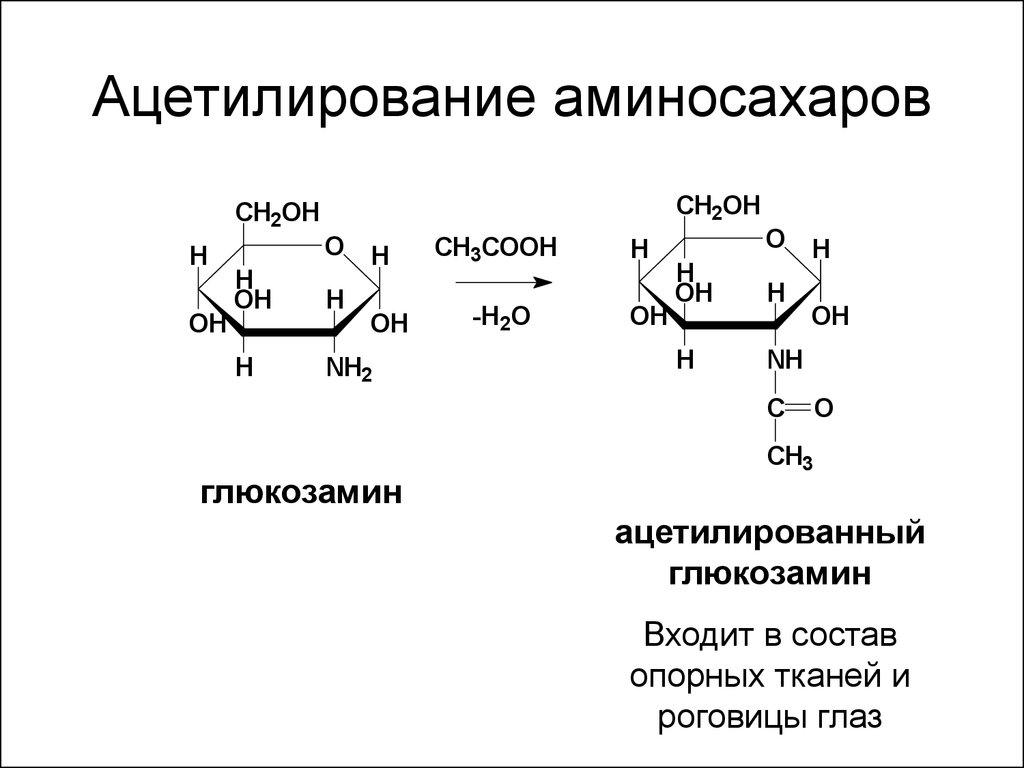
28. Ацетилирование аминосахаров
CH2OHCH2OH
H
OH
H
OH
H
O H
H
OH
NH2
CH3COOH
-H2O
H
OH
H
OH
H
O H
H
OH
NH
C
глюкозамин
O
CH3
ацетилированный
глюкозамин
Входит в состав
опорных тканей и
роговицы глаз
29.
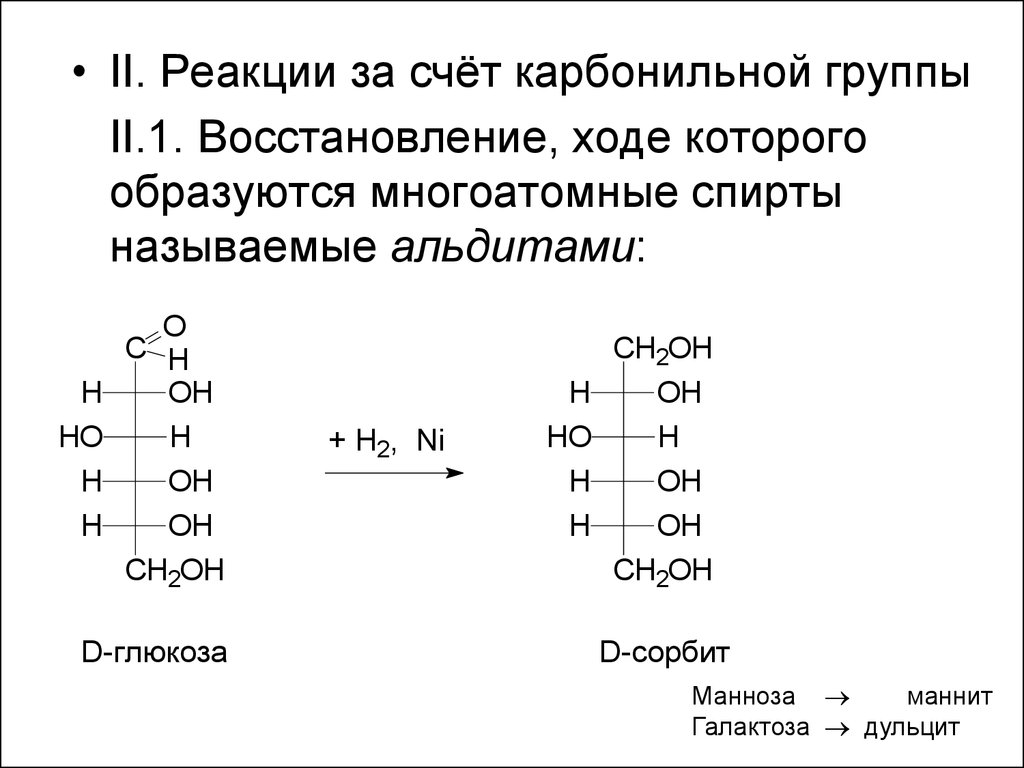
• II. Реакции за счёт карбонильной группыII.1. Восстановление, ходе которого
образуются многоатомные спирты
называемые альдитами:
H
HO
H
H
O
C H
OH
H
OH
OH
CH2OH
D-глюкоза
+ H2, Ni
H
HO
H
H
CH2OH
OH
H
OH
OH
CH2OH
D-сорбит
Манноза
маннит
Галактоза дульцит
30.
II.2. Окисление - важная реакция в химии углеводов. Егоиспользуют для получения ряда
соединений в структурных
исследованиях и биохимических
анализах.
В зависимости от условий окисления
моносахаридов образуются различные
продукты. В щелочной среде окисление
сопровождается разрушением
углеродной цепи молекулы (реакция
”серебряного зеркала”).
Окисление в нейтральной среде
позволяет сохранить углеродный
скелет.
31.
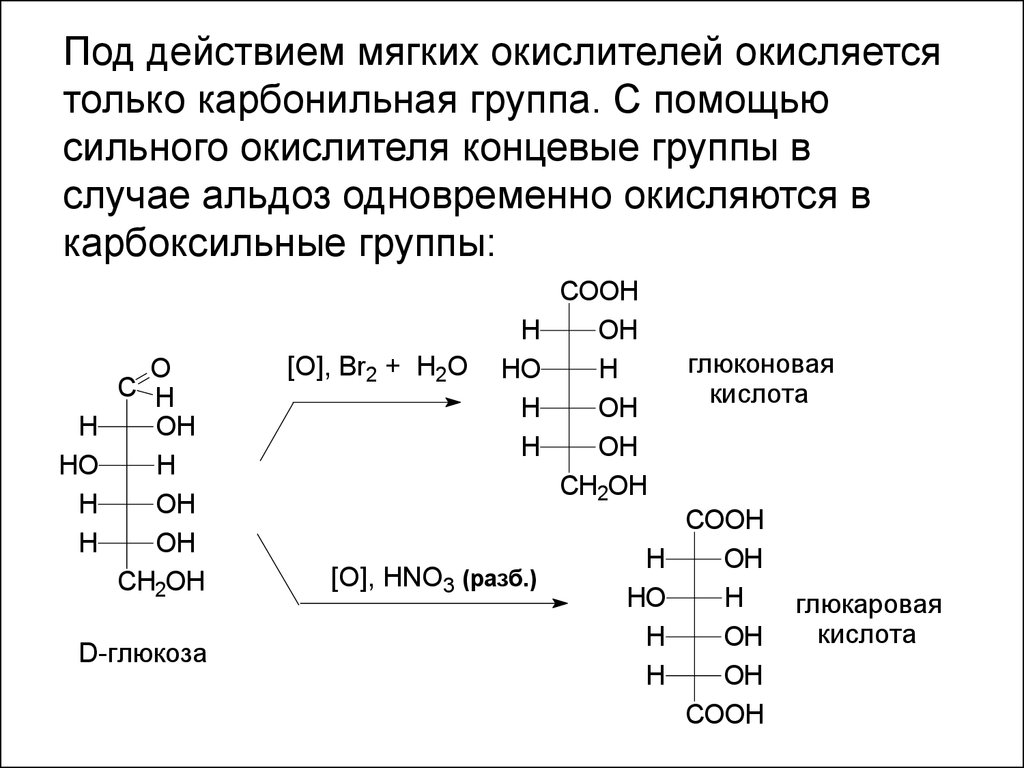
Под действием мягких окислителей окисляетсятолько карбонильная группа. С помощью
сильного окислителя концевые группы в
случае альдоз одновременно окисляются в
карбоксильные группы:
H
HO
H
H
O
C H
OH
H
OH
OH
CH2OH
D-глюкоза
[O], Br2 + H2O
H
HO
H
H
[O], HNO3 (разб.)
COOH
OH
H
OH
OH
CH2OH
H
HO
H
H
глюконовая
кислота
COOH
OH
H
OH
OH
COOH
глюкаровая
кислота
32.
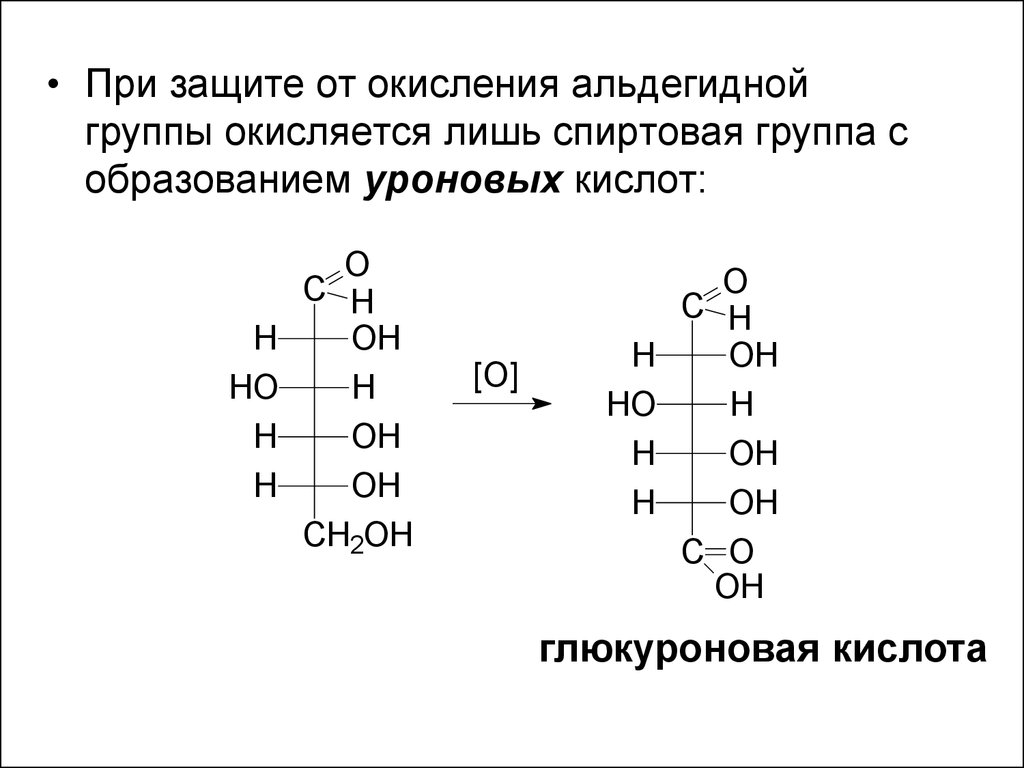
• При защите от окисления альдегиднойгруппы окисляется лишь спиртовая группа с
образованием уроновых кислот:
H
HO
H
H
O
C H
OH
H
OH
OH
CH2OH
[O]
H
HO
H
H
O
C H
OH
H
OH
OH
C O
OH
глюкуроновая кислота
33. СЛОЖНЫЕ УГЛЕВОДЫ
34. Олигосахариды
классифицируют:• в зависимости от числа
моносахаридных фрагментов,
входящих в олигосахарид (дисахариды,
трисахариды, тетрасахариды и т. д.);
• по составу моносахаридных остатков
(гомоолигосахариды,
гетероолигосахариды);
• в зависимости от порядка соединения
мономеров (линейные, разветвленные);
• на восстанавливающие и
невосстанавливающие
35.
• Из олигосахаридов в природе наиболеешироко распространены дисахариды.
Дисахариды - О-гликозиды (полные ацетали)
С гликозидной природой связана способность
дисахаридов гидролизоваться в кислой (но не в
щелочной) среде с образованием моносахаридов.
C12H22O11
мальтоза
+ H2O
D-глюкоза + D-глюкоза
целлобиоза
+ H2O
D-глюкоза + D-глюкоза
лактоза
+ H2O
D-глюкоза + D-галактоза
сахароза
+ H2O
D-глюкоза + D-фруктоза
36.
• У восстанавливающих дисахаридовсвязь между моносахаридными
остатками осуществляется за счет
спиртового и полуацетального
гидроксилов.
При этом один из моносахаридных
остатков сохраняет свободный
полуацетальный гидроксил, который
определяет восстанавливающие
свойства и реакции, свойственные
моносахаридам (сохраняется
способность к раскрытию цикла).
37.
• У невосстанавливающих дисахаридовгликозидная связь образована за счет
полуацетальных гидроксилов обоих
моносахаридов.
Они не содержат свободного
полуацетального гидроксила и не
вступают в реакции, характерные для
карбонильной группы.
38.
• Представители восстанавливающихдисахаридов:
- мальтоза,
- целлобиоза,
- лактоза
39.
• Мальтоза (солодовый сахар) являетсяосновным продуктом расщепления
крахмала под действием фермента
β-амилазы, выделяемого слюнной
железой.
В мальтозе остатки двух молекул
D-глюкопиранозы связаны
α(1→4)-гликозидной связью.
40.
CH2OHCH2OH
H
OH
H
OH
H
O H
H
OH
OH
H
OH
H
OH
H
O OH
H
OH
H
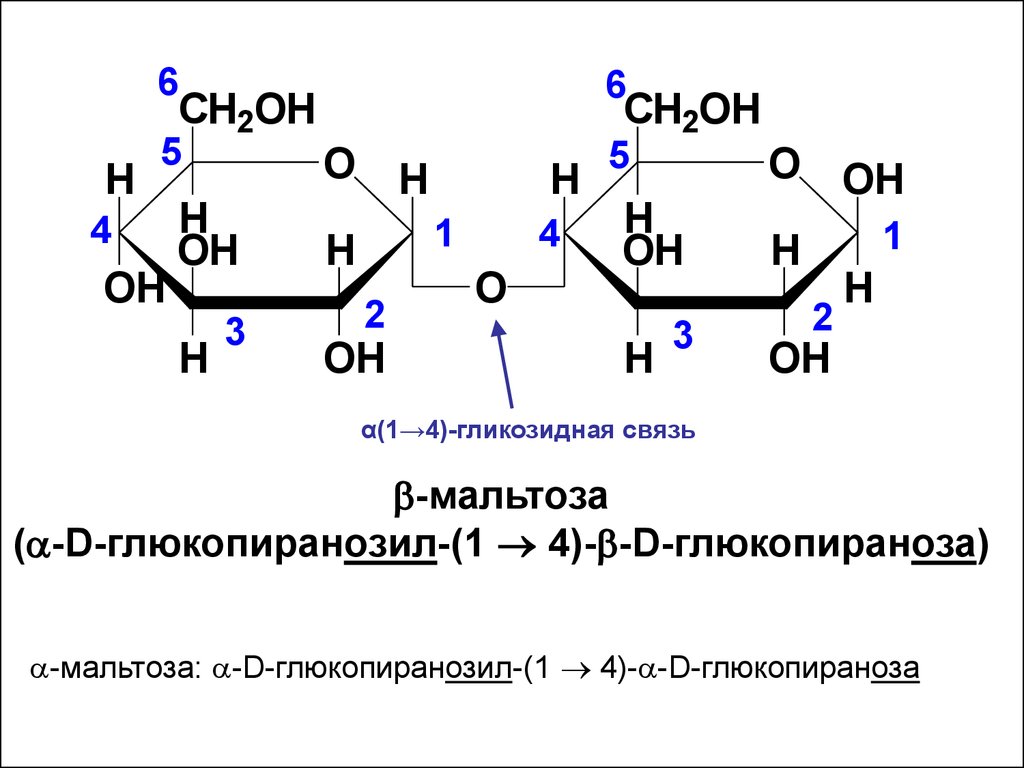
41.
66
CH2OH
H
5
4
OH
H
OH
H
3
CH2OH
O H
H
1
H
2
OH
4
O
5
H
OH
H
3
O OH
1
H
2
H
OH
α(1→4)-гликозидная связь
-мальтоза
(a-D-глюкопиранозил-(1 4)- -D-глюкопираноза)
a-мальтоза: a-D-глюкопиранозил-(1 4)-a-D-глюкопираноза
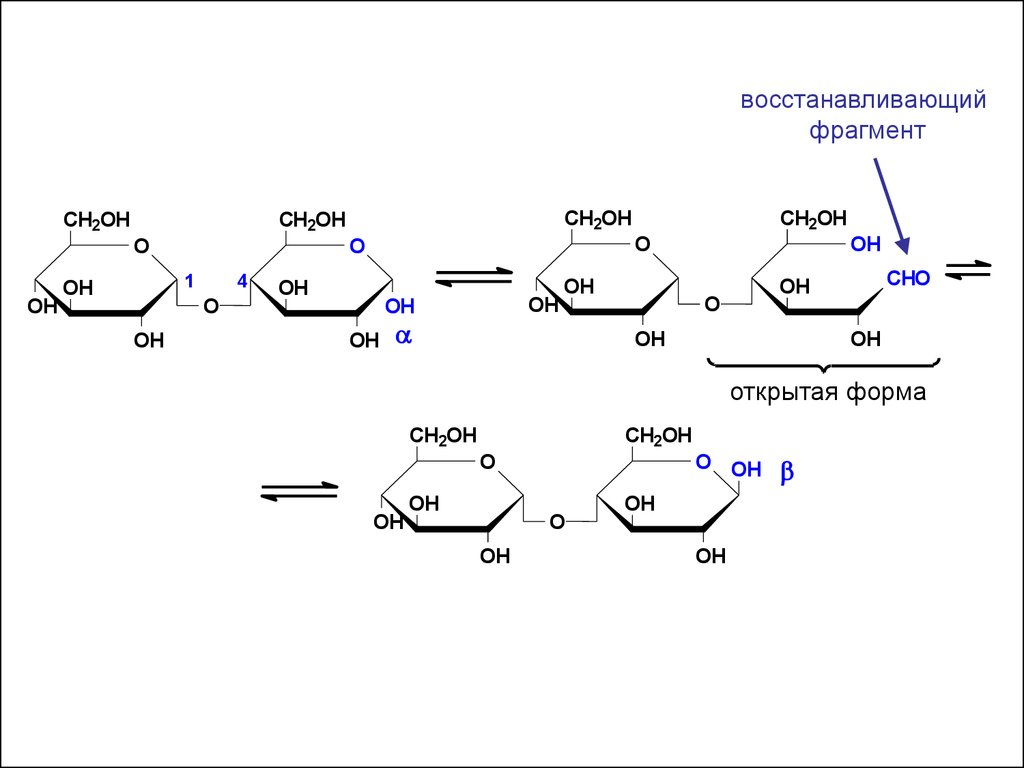
42.
восстанавливающийфрагмент
CH2OH
O
OH
CH2OH
CH2OH
4
O
OH
O
O
1
OH
CH2OH
OH
OH
OH
OH
OH
a
OH
CHO
OH
O
OH
OH
открытая форма
CH2OH
CH2OH
O
OH
OH
O OH
O
OH
OH
OH
43.
• Целлобиоза образуется при неполномгидролизе полисахарида целлюлозы.
Она также построена из двух молекул
глюкозы, но отличается от мальтозы
тем, что в одной из молекул,
образующих димер, в реакцию вступает
полуацетальный гидроксил
β-пиранозной формы.
Т.о., в целлобиозе остатки двух
молекул D- глюкопиранозы связаны
β(1→4)-гликозидной связью.
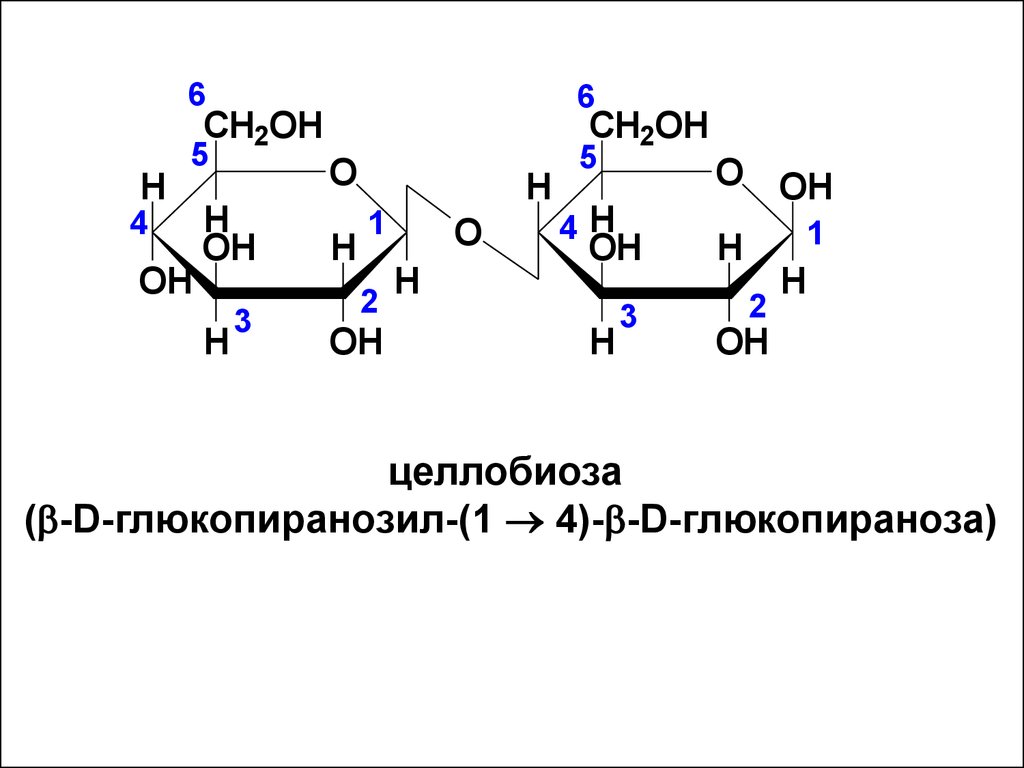
44.
66
CH2OH
H
5
4
OH
O
H
OH
H
CH2OH
3
H
H
1
2
OH
O
H
5
O OH
4H
OH
H
3
1
H
2
H
OH
целлобиоза
( -D-глюкопиранозил-(1 4)- -D-глюкопираноза)
45.
• мальтоза расщепляется в организмечеловека ферментом α-глюкозидазой
(мальтазой)
• целлобиоза расщепляется ферментом
β-глюкозидазой, который в организме
человека отсутствует
46.
• Лактоза содержится в молоке (4-5%),получают из молочной сыворотки
(молочный сахар).
Лактоза построена из остатков
D-галактопиранозы и D-глюкопиранозы,
связанных -(1 4)-гликозидной
связью.
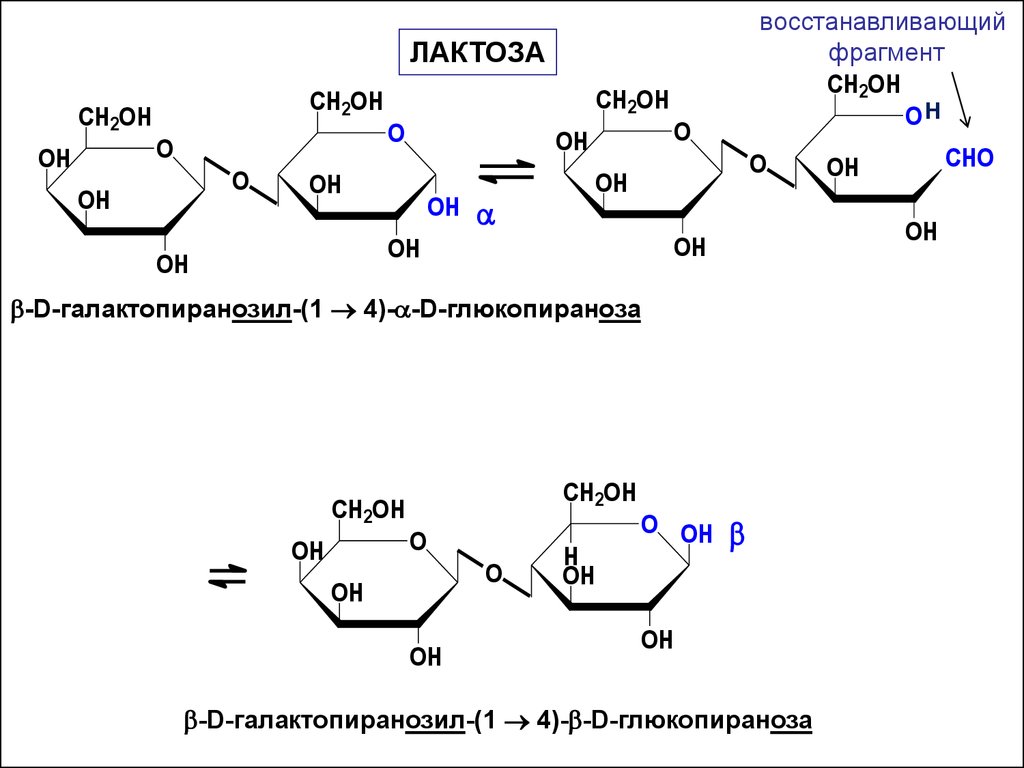
47.
восстанавливающийфрагмент
CH2OH
OH
ЛАКТОЗА
O
O
OH
CH2OH
CH2OH
CH2OH
O
OH
O
OH
OH
OH
a
OH
-D-галактопиранозил-(1 4)-a-D-глюкопираноза
CH2OH
CH2OH
O
OH
O
OH
OH
H
OH
O OH
CHO
OH
OH
OH
OH
OH
O
OH
-D-галактопиранозил-(1 4)- -D-глюкопираноза
48.
• Лактоза применяется- в фармацевтике при изготовлении
порошков и таблеток (менее
гигроскопична, чем сахар)
- питательное средство для грудных
детей (в женском молоке до 8 процентов)
49.
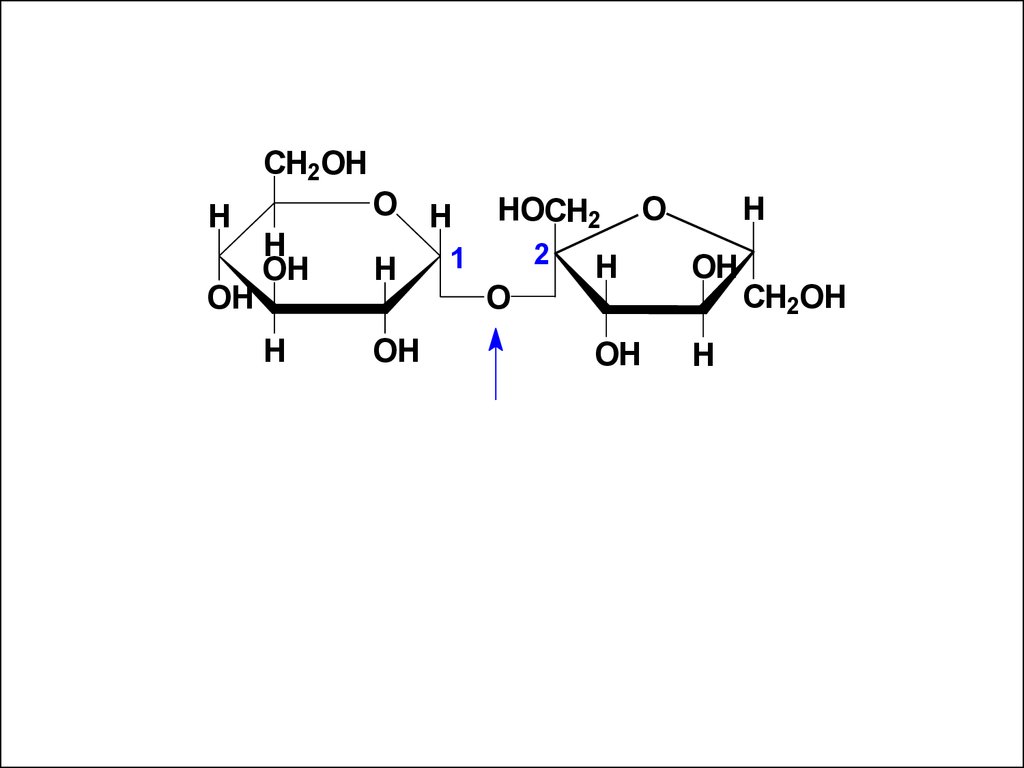
• Наиболее распространеннымневосстанавливающим дисахаридом
является сахароза. Она построена из
остатков D-глюкопиранозы и D-фруктофуранозы: CH2OH
O
OH
1
OH
OH
OH
(1 2)-гликозидная связь
O
CH2
O
OH
OH
a-êî í ô èãóðàöèÿ
2
-êî í ô èãóðàöèÿ
CH2OH
1
сахароза
(a-D-глюкопиранозил-(1 2)- -D-фруктофуранозид)
50.
CH2OHH
OH
H
OH
H
O H
H
OH
HOCH2
2
1
O
O
H
H
OH
OH
H
CH2OH
51. Химические свойства дисахаридов
• I. ВСЕ:1) подвергаются гидролизу (под
действием ферментов, в кислой среде)
2) образуют эфиры с минеральными и
органическими кислотами
3) образуют соли с гидроксидом меди
(сахараты)
52.
• II. Только ВОССТАНАВЛИВАЮЩИЕ:1) обладают мутаротацией
2) проявляют восстановительные
свойства:
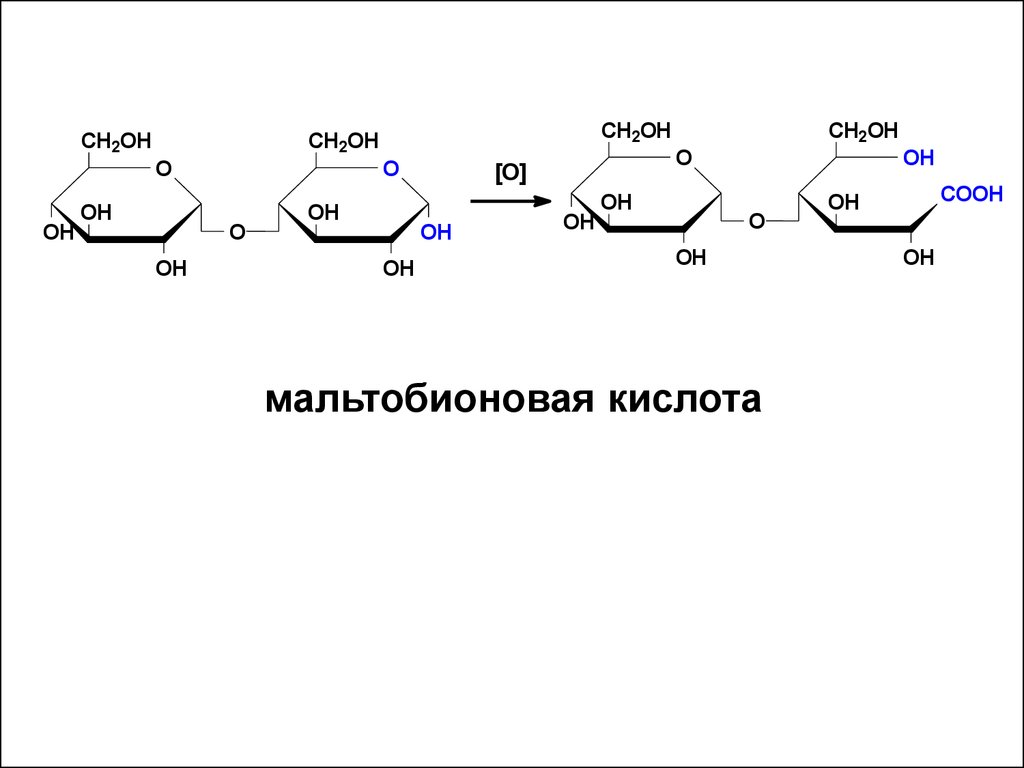
а) окисляются в гликобионовые
кислоты
53.
CH2OHO
OH
CH2OH
CH2OH
OH
O
O
OH
OH
OH
O
[O]
OH
CH2OH
OH
OH
OH
O
OH
мальтобионовая кислота
COOH
OH
OH
54.
• NB! Пробы Троммера, Фелинга и др.3) реакции альдегидной группы
55.
В отличие от большинства дисахаридовсахароза не имеет свободного
полуацетального гидроксила и, как
следствие, не обладает
восстанавливающими свойствами.
56. Полисахариды
• Полисахариды представляют собой продуктыполиконденсации моносахаридов, которые
связаны друг с другом гликозидными
связями. Таким образом, по химической
природе они являются полигликозидами
(полиацеталями). В полисахаридах
растительного происхождения в основном
присутствуют (1→4)- и (1→6)-гликозидные
связи, а в полисахаридах животного и
бактериального происхождения
дополнительно имеются (1→3)- и (1→2)гликозидные связи.
57.
• Гликозидная природа полисахаридовобусловливает их способность к
гидролизу в кислой среде. Полный
гидролиз приводит к образованию
моносахаридов и их производных, а
неполный к образованию
олигосахаридов, в том числе
дисахаридов. В щелочной среде
полисахариды обладают высокой
устойчивостью и не подвергаются
распаду.
58.
• Крахмал (резервный гомополисахаридрастений) представляет собой белое
аморфное вещество, нерастворимое в
холодной воде. При быстром нагревании
крахмала за счет содержания в нем влаги
происходит гидролитическое расщепление
полимерной цепи на более мелкие осколки,
называемые декстринами. Декстрины
растворяются в воде лучше, чем крахмал.
• Крахмал представляет собой смесь двух
полимеров, построенных из
D-глюкопиранозных остатков – амилозы (1020%) и амилопектина (80-90%).
59.
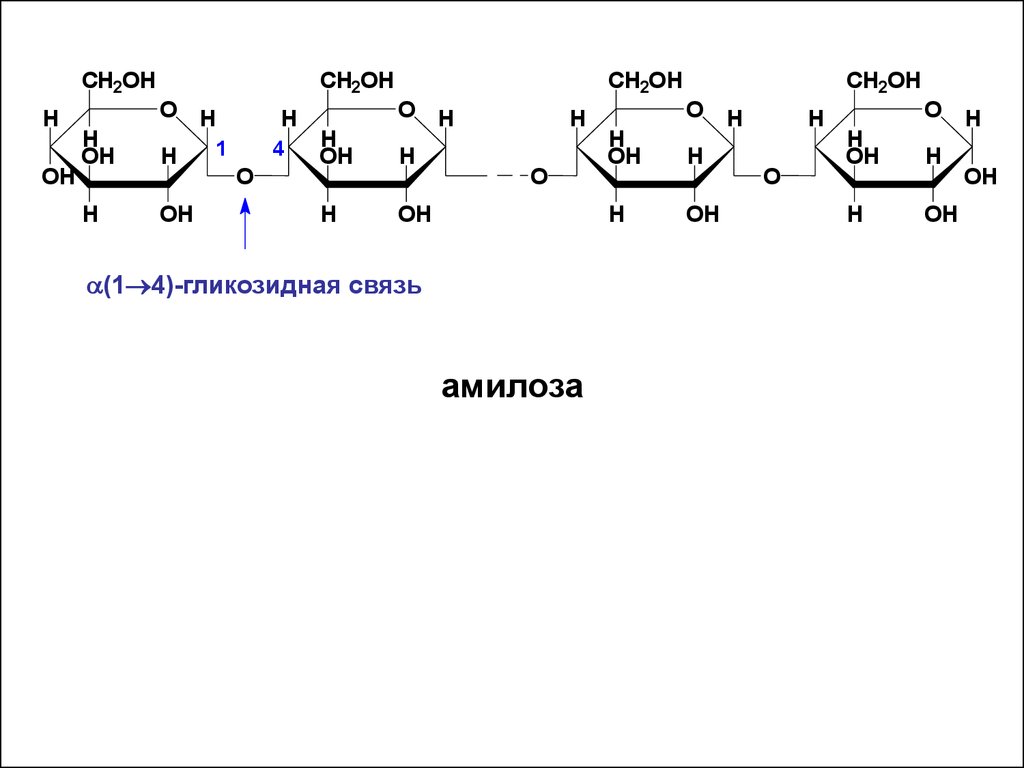
• В амилозе D-глюкопиранозные остаткисвязаны α-(1→4)-гликозидными
связями, т.е. дисахаридным
фрагментом амилозы является
мальтоза. Цепь амилозы
неразветвленная. Она включает 2001000 глюкозидных остатков.
Макромолекула амилозы свернута в
спираль. При этом на каждый виток
спирали приходится шесть
моносахаридных звеньев.
60.
CH2OHH
OH
H
OH
H
CH2OH
O H
H
OH
H
1
4
O
H
OH
H
CH2OH
O H
H
H
O
OH
H
OH
H
a(1 4)-гликозидная связь
амилоза
CH2OH
O H
H
OH
H
O
H
OH
H
O H
H
OH
OH
61.
• Амилопектин отличается от амилозывысокоразветвленным строением.
В линейных участках этого
полисахарида D-глюкопиранозные
остатки связаны α-(1→4)-гликозидными
связями, а в точках разветвления
имеются дополнительные α-(1→6)гликозидные связи. Между точками
разветвления располагаются 20-25
остатков глюкозы.
62.
CH2OHH
O H
H
OH
O
CH2OH
H
H
H
O
OH
O
H
OH
H
разветвление
H
OH
a -гликозидная связь
CH2OH
H
O
H
OH
H
CH2 O
O H
H
OH
H
O
H
OH
H
CH2OH
O H
H
H
O
OH
амилопектин
H
OH
H
O H
H
OH
63.
• Гликоген (резевный гомополисахаридживотных организмов) является
структурным и функциональным
аналогом крахмала. По строению
подобен амилопектину, но отличается
от него большей разветвленностью и
более жесткой упаковкой молекулы.
Сильное разветвление способствует
выполнению гликогеном энергетической
функции, поскольку при наличии
большого числа концевых остатков
обеспечивается быстрое отщепление
нужного количества глюкозы.
64.
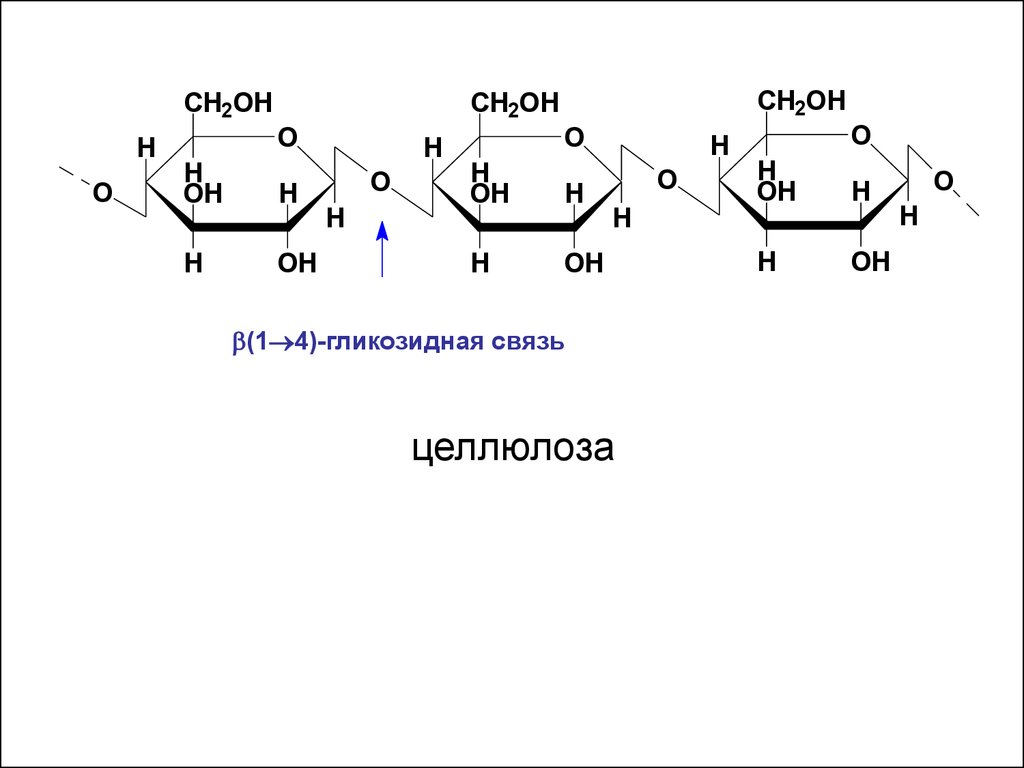
• Целлюлоза или клетчатка представляетсобой наиболее распространенный
структурный гомополисахарид растений.
Она состоит из остатков D-глюкопиранозы,
которые связанны β-(1→4)-гликозидными
связями. Т.о., дисахаридным фрагментом
целлюлозы является целлобиоза.
Полимерная цепь целлюлозы не имеет
разветвлений. В ней содержится 250012000 остатков глюкозы, что соответствует
молекулярной массе от 400000 до 1-2 млн.
65.
• Макромолекула целлюлозы имеет строголинейное строение. Благодаря этому внутри
цепи, а также между соседними цепями
образуются водородные связи. Такая
упаковка молекулы обеспечивает высокую
механическую прочность, нерастворимость в
воде и химическую инертность. Целлюлоза
не расщепляется в желудочно-кишечном
тракте, поскольку в организме отсутствует
фермент, способный гидролизовать β-(1→4)гликозидные связи. Несмотря на это, она
является необходимым балластным
веществом для нормального питания.
66.
CH2OHH
O
CH2OH
CH2OH
O
H
OH
H
H
OH
H
O
H
O
H
OH
H
H
OH
H
O
H
(1 4)-гликозидная связь
целлюлоза
O
H
OH
H
H
OH
O
H
67.
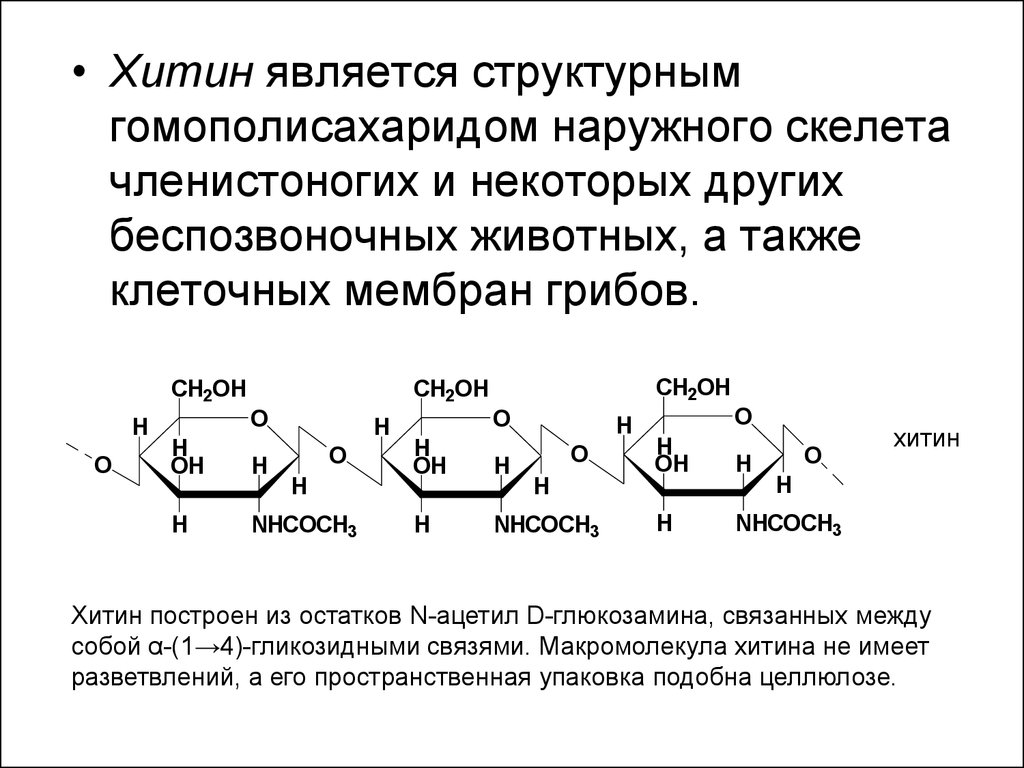
• Хитин является структурнымгомополисахаридом наружного скелета
членистоногих и некоторых других
беспозвоночных животных, а также
клеточных мембран грибов.
CH2OH
H
O
CH2OH
CH2OH
O
H
H
OH
H
H
NHCOCH3
O
H
O
H
H
OH
H
H
NHCOCH3
O
H
O
H
OH
H
H
NHCOCH3
O
хитин
H
Хитин построен из остатков N-ацетил D-глюкозамина, связанных между
собой α-(1→4)-гликозидными связями. Макромолекула хитина не имеет
разветвлений, а его пространственная упаковка подобна целлюлозе.











































 chemistry
chemistry