Similar presentations:
Азотсодержащие органические соединения. Аминокислоты (часть 2)
1.
*АМИНОКИСЛОТЫАминокислоты – соединения, содержащие
карбоксильную (COOH) и
аминогруппу (NH2).
2.
*1. Классификация*1.1. по положению аминогруппы
C C C C COOH
R CH COOH
NH2
2
3.
*1.2. По количеству карбокси- и аминогрупп*Моноаминомонокарбоновые кислоты
(глицин,
аланин, валин, лейцин, изолейцин, серин, треонин,
цистеин, фенилаланин, тирозин, метионин,
триптофан и т.д.)
*Моноаминодикарбоновые кислоты (аспарагиновая
кислота, глутаминовая кислота)
*Диаминомонокарбоновые кислоты (лизин,
аргинин)
*Диаминодикарбоновые кислоты (цистин)
4.
*1.3 Классификация по встречаемости в белках20 классических протеиногенных аминокислот, информация
о положении которых в белковой молекуле записана
цифровым трёхбуквенным кодом в ДНК и РНК
5.
Алифатические АКCH2 COOH
COOH
NH2
NH2
Тривиальноe
Рациональноe
IUPAC
Обозначниe
CH3 CH
глицин, гликокол
Аминоуксусная кислота
Аминоэтановая кислота
Gly, Гли
Аланин
-аминопропионовая кислота
2-аминопропановая кислота
Ala, Ала
CH3
CH
CH3
CH
COOH
NH2
Валин
-аминоизовалeриановая кислота
2-амино-3-мeтилбутановая кислота
Val, Вал
CH3
CH
CH CH2 CH
CH3
CH3
COOH
NH2
Лeйцин
-аминоизокапроновая кислота
2-амино-4-мeтилпeнтaновая кислота
Leu, Лeй
CH3 CH2
CH
COOH
NH2
Изолeйцин
-амино- -мeтилвалeриановая кислота
2-амино-3-мeтилпeнтaновая кислота
Ile, Илe
6.
Содержащие ОН-группуCH2 CH
OH
COOH
CH3 CH
OH
CH
COOH
NH2
NH2
Ceрин
-амино- -оксипропионовая кислота
2-амино-3-гидроксипропановая кислота
Ser, Сeр
Трeонин
-амино- -оксимасляная кислота
2-амино-3-гидроксибутановая кислота
Thr, Трe
7.
Серосодержащие АКCH2 CH
SH
COOH
S
2
NH2
CH2 CH
SH
COOH
-2e, -2H+
NH2
CH2 CH
COOH
NH2
S
CH2 CH
COOH
NH2
Цистeин
Цистеин
-амино- -тиопропионовая кислота
2-амино-3-сульфанилпропановая кислота
(2-амино-3-тиопропановая кислота,
2-амино-3-мeркаптопропановая кислота – устаревш.)
Cys, Цис
CH3 S
Цистин
CH2 CH2 CH
NH2
Мeтионин
-амино- -мeтилтиомасляная кислота
2-амино-4-метилсульфанилбутановая кислота
(2-амино-4-метилтиобутановая кислота – устаревш.)
Met, Мет.
COOH
8.
Моноаминодикарбоновые кислоты и их амидыHOOC
CH2 CH
COOH
HOOC CH2 CH2 CH
NH2
NH2
Глутаминовая кислота
-aминоглутаровая кислота
2-аминопентандиовая кислота
Glu, Глу
Аспарагиновая кислота
Аминоянтарная кислота
Аминобутандиовая кислота
Asp, Асп
O
O
C
H2N
COOH
CH2 CH
COOH
NH2
Аспарагин
Амид аспарагиновой кислоты
2,5-диамино-5-оксобутановая кислота
Asn, Асн
H2N
C CH2 CH2 CH COOH
NH2
Глутамин
Амид глутаминовой кислоты
2,6-диамино-6-оксопентановая кислота
Gln, Глн
9.
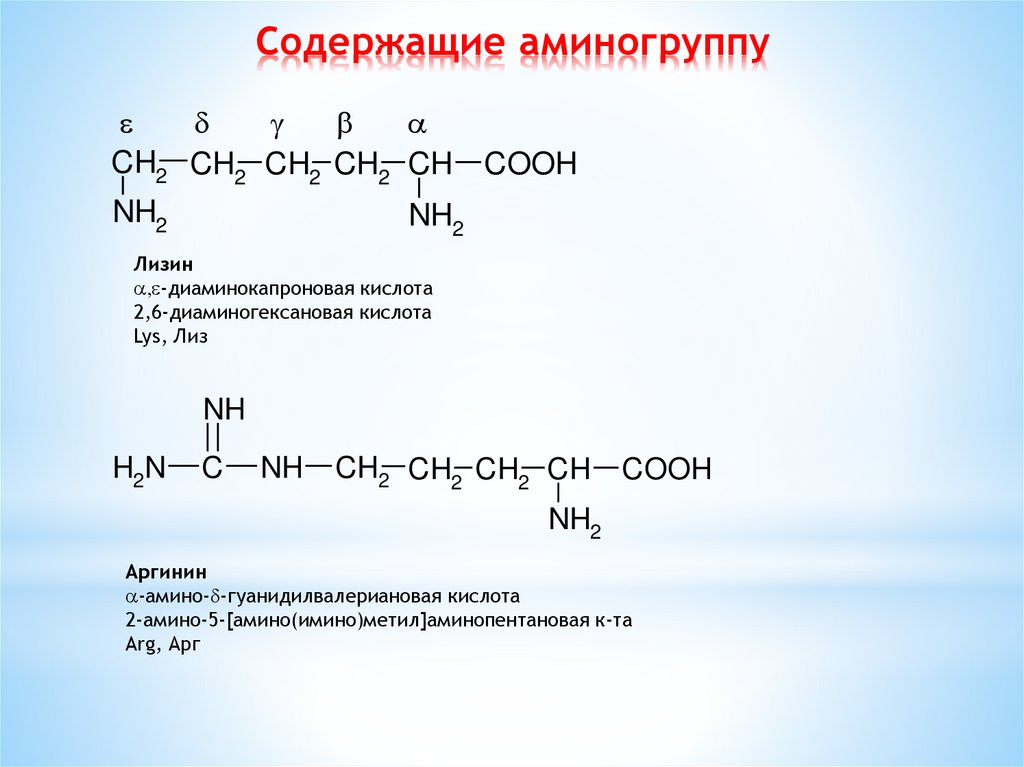
Содержащие аминогруппуCH2 CH2 CH2 CH2 CH
NH2
COOH
NH2
Лизин
, -диаминокапроновая кислота
2,6-диаминогексановая кислота
Lys, Лиз
NH
H2N
C
NH
CH2 CH2 CH2 CH
COOH
NH2
Аргинин
-амино- -гуанидилвалериановая кислота
2-амино-5-[амино(имино)метил]аминопентановая к-та
Arg, Арг
10.
Ароматические АКCH2 CH
COOH
NH2
HO
Фенилаланин
-амино- -фенилпропионовая к-та
2-амино-3-фенилпропановая к-та
Phe, Фен
CH2 CH
COOH
NH2
Тирозин
-амино- -(п-оксифенил)пропионовая к-та
2-амино-3-(4-гидроксифенил)пропановая к-та
Tyr, Тир
11.
Гетероциклические АКCH2
CH
COOH
COOH
NH2
N
N
H
Триптофан
-амино- -индолилпропионовая к-та
2-амино-3-(1H-индол-3-ил)пропановая к-та
Trp, Три
H
Пролин
Пирролидин- -карбоновая к-та
2-пирролидинкарбоновая к-та
Pro, Про
N
N
H
CH2
CH
CH3
COOH
NH2
Гистидин
-амино- -имидазолилпропионовая к-та
2-амино-3-(1H-имидазол-4-ил)пропионовая к-та
His, Гис
H
CH
COOH
N
H
Для сравнения- аланин
12.
*1. Классификация*1.1. по положению аминогруппы
C C C C COOH
R CH COOH
NH2
12
13.
*1.4. По пищевой ценности для человека*Аминокислоты делятся на
заменимые и незаменимые.
*К незаменимым аминокислотам относят:
валин, изолейцин, лейцин, триптофан,
фенилаланин, метионин, лизин, треонин.
14.
*2. Номенклатура*2.1. Тривиальная номенклатура в основном
используется для широко распространённых аминокислот.
*2.2. Рациональная и 2.3. IUPAC
CH2 CH
OH
COOH
NH2
-амино- -гидроксипропионовая кислота
2-амино-3-гидроксипропановая кислота
15.
*3. Изомерия*3.1. Структурная изомерия
CH3
CH3
CH CH2 CH
CH3
COOH
NH2
лейцин
CH3 CH COOH
NH2
аланин
CH
CH3 CH2
CH
COOH
NH2
изолейцин
CH2 CH2 COOH
NH2
-аланин
16.
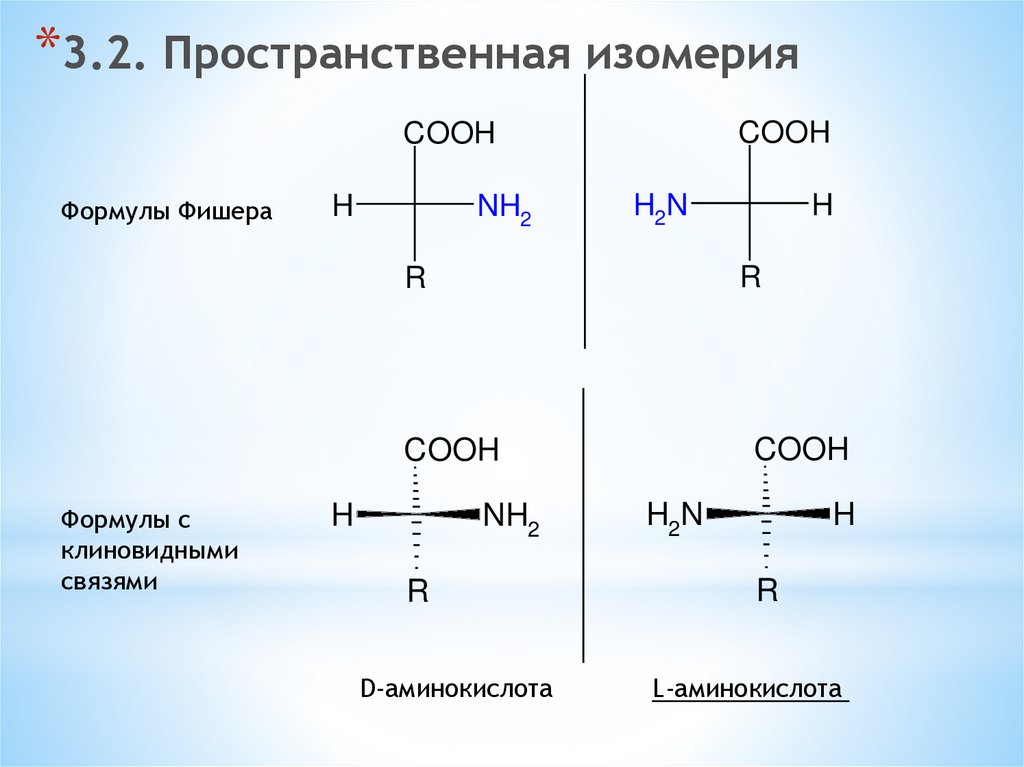
*3.2. Пространственная изомерияCOOH
COOH
Формулы Фишера
H
NH2
H2N
R
R
COOH
COOH
Формулы с
клиновидными
связями
H
H
NH2
R
D-аминокислота
H2N
H
R
L-аминокислота
17.
*4. Физические свойства*Аминокислоты, как правило,
являются
бесцветными
кристаллическими
соединениями. Большинство из них
умеренно растворимы в воде.
*Аминокислоты
являются
хиральными
соединениями, обладающими оптической
активностью
(за
некоторыми
исключениями, напр. глицин).
18.
* 5. Биологические свойства* Из остатков аминокислот построены такие важные соединения как
белки, которые участвуют практически во всех процессах in vivo.
* Биосинтез алкалоидов, порфиринов, тетрапиррольных пигментов,
мочевины и т.д.
* С нарушениями метаболизма аминокислот связаны наследственные
заболевания как фенилкетонурия и алкаптонурия.
* В медицине некоторые аминокислоты используют в качестве
лекарственных препаратов – метионин назначается при заболеваниях
печени, глицин – при заболеваниях ЦНС.
* Некоторые аминокислоты имеют сладкий вкус – например, глицин.
Интересно, что L-аспарагин безвкусен, а D-аспарагин имеет сладкий
вкус.
* L-глутаминовая кислота широко применяется как пищевая добавка –
при незначительной добавке глутамата натрия заметно усиливается
естественный вкус мясных блюд.
19.
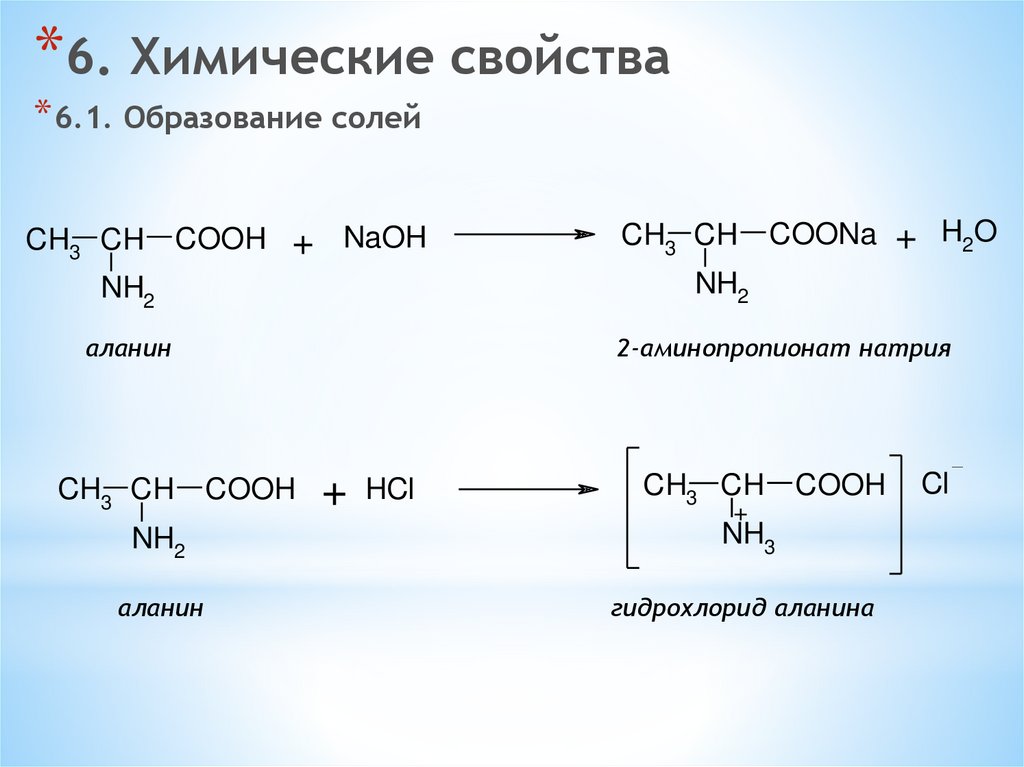
*6. Химические свойства* 6.1. Образование солей
CH3 CH
COOH
+
NaOH
COONa
+
H2O
NH2
NH2
аланин
CH3 CH
CH3 CH
2-аминопропионат натрия
COOH
+
HCl
CH3 CH
COOH
+
NH2
NH3
аланин
гидрохлорид аланина
Cl
20.
OCH3 CH C
NH2
OH
O
CH3 CH C
+
O
NH3
Аминогруппа нейтрализует карбоксильную группу,
поэтому АК в твёрдом виде и в растворе
при pH = изоэлектрической точке, находятся в виде
цвиттерионов
21.
+CH3 CH
COOH
+
NH3
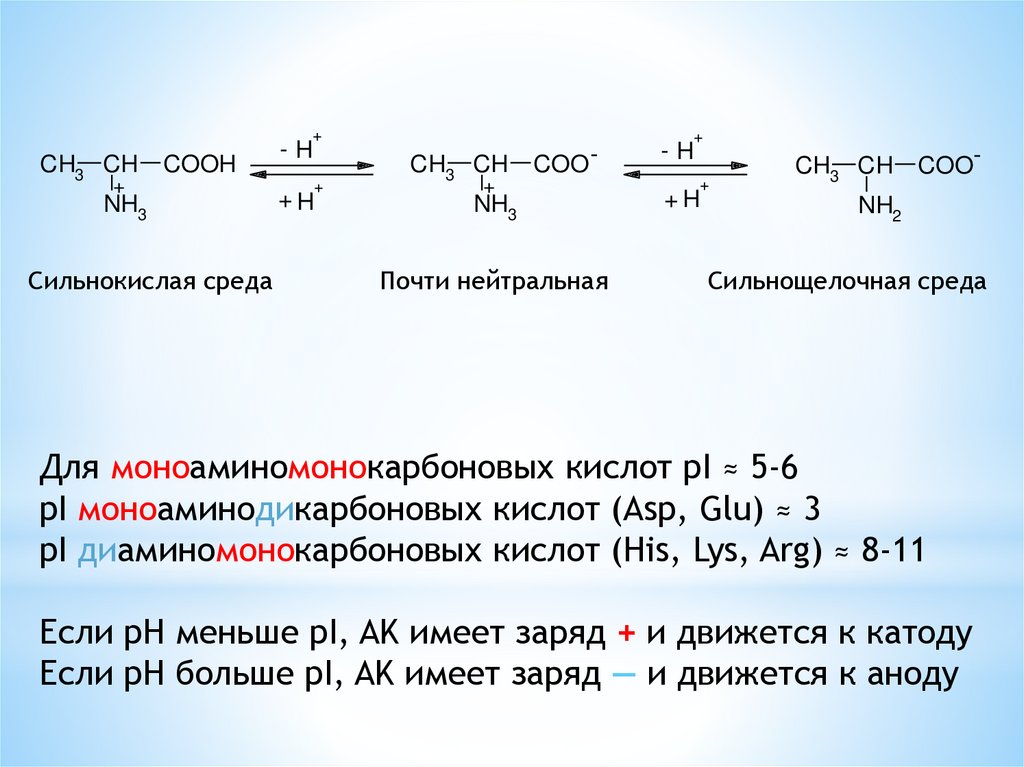
Сильнокислая среда
-H
+
+H
CH3 CH
COO -
+
NH3
Почти нейтральная
+
-H
+
+H
CH3 CH
COO-
NH2
Сильнощелочная среда
Для моноаминомонокарбоновых кислот pI ≈ 5-6
pI моноаминодикарбоновых кислот (Asp, Glu) ≈ 3
pI диаминомонокарбоновых кислот (His, Lys, Arg) ≈ 8-11
Если pH меньше pI, AK имеет заряд + и движется к катоду
Если pH больше pI, AK имеет заряд — и движется к аноду
22.
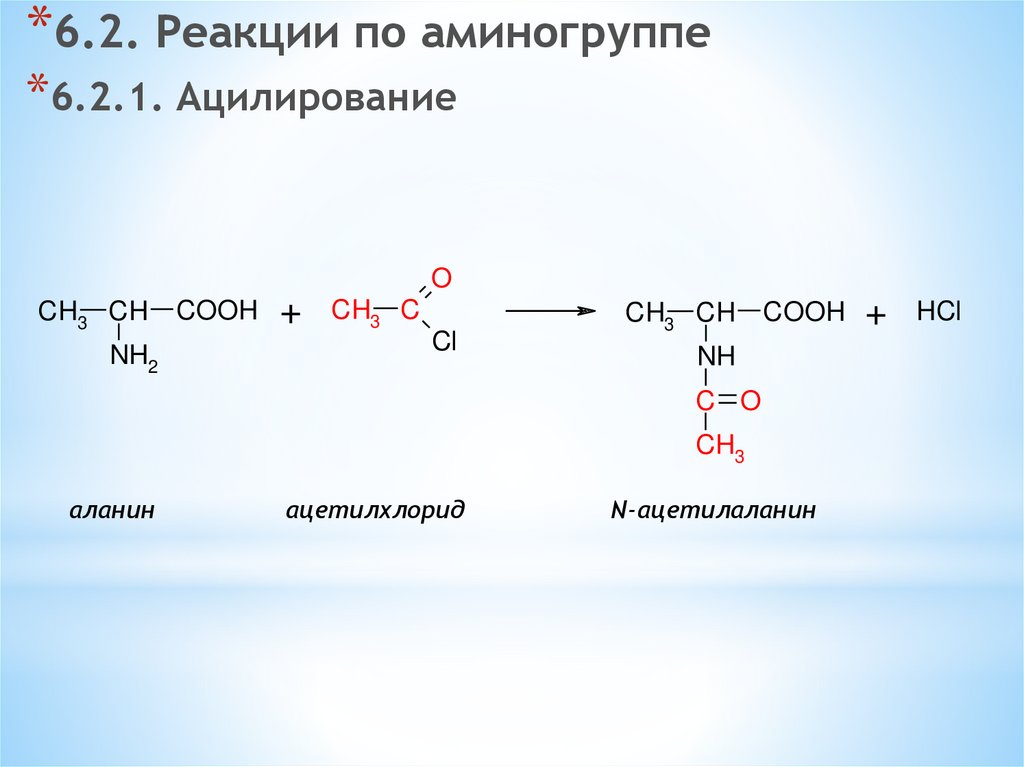
*6.2. Реакции по аминогруппе*6.2.1. Ацилирование
O
CH3 CH
NH2
COOH
+
CH3 C
Cl
CH3 CH
COOH
NH
C O
CH3
аланин
ацетилхлорид
N-ацетилаланин
+
HCl
23.
CH3R
CH
NH2
COOH
+
H3C C O C N3
CH3
R
O
CH
COOH
NH
C O
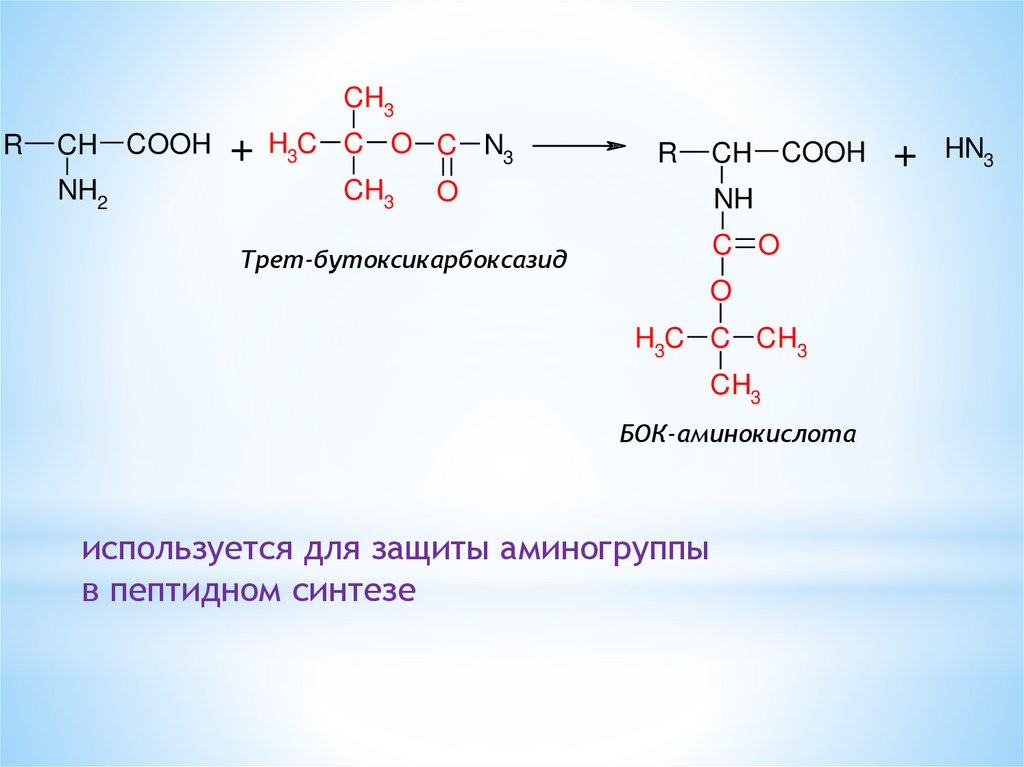
Трет-бутоксикарбоксазид
O
H3C C CH3
CH3
БОК-аминокислота
используется для защиты аминогруппы
в пептидном синтезе
+
HN3
24.
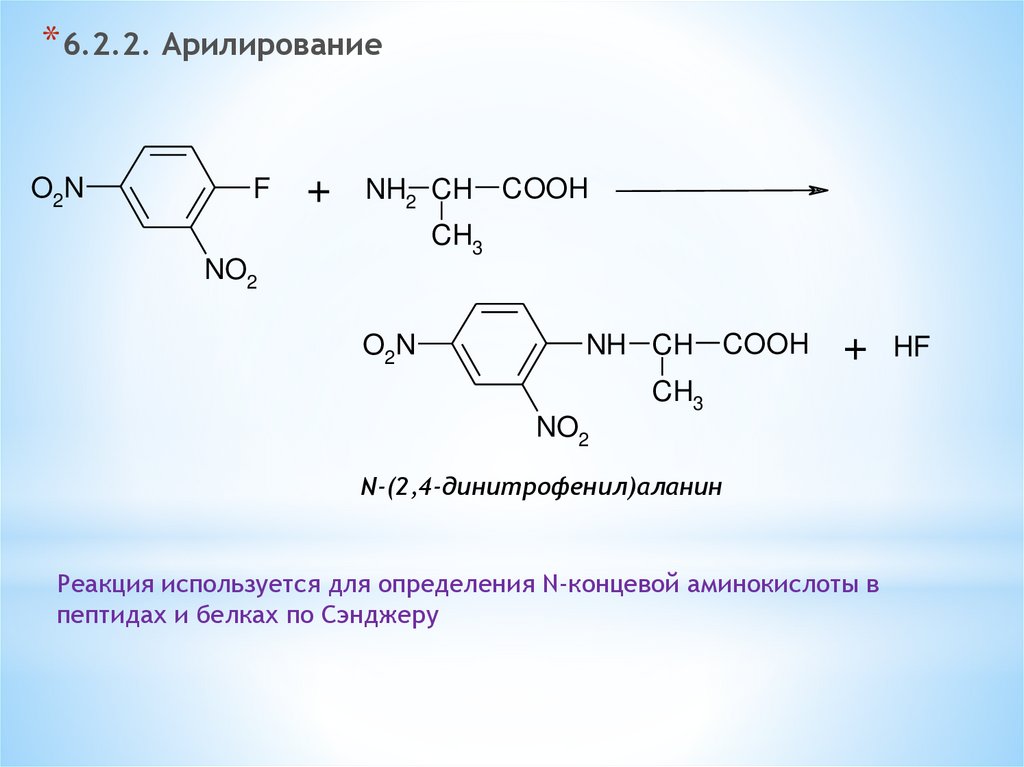
* 6.2.2. АрилированиеO2N
F
+
NH2 CH
COOH
CH3
NO2
O2N
NH CH
COOH
+
CH3
NO2
N-(2,4-динитрофенил)аланин
Реакция используется для определения N-концевой аминокислоты в
пептидах и белках по Сэнджеру
HF
25.
* 6.2.3. Взаимодействие с карбонильнымисоединениями
R
CH
COOH
1
+
R
NH2
аминокислота I
C
трансаминаза
COOH
O
кeтокислота I
R
C
COOH
O
кeтокислота II
+
1
R
CH
COOH
NH2
аминокислота II
26.
HR
CH
NH2
COOH
+
C O
H
R
CH
COOH
NH
CH2 O H
Данная реакция используется в формольном титровании
по Сёренсену: метилольные производные являются
гораздо более сильными кислотами чем аминокислоты и
они легко оттитроввываются щёлочью.
27.
* 6.2.4. Взаимодействие с азотистой кислотойR
CH
COOH
NH2
-аминокислота
+
HNO2
R
CH
COOH
+
N2
+
H2O
OH
-гидроксикислота
Реакция с азотистой кислотой используется определения
аминокислот по Ван-Сляйку: по объему выделившегося
азота легко найти количество аминокислоты.
28.
* 6.2. Реакции по карбоксильной группеR
CH
NH2
COOH
+
CH3OH
HCl газ
R
CH
COOCH3
+
H2O
NH2
Реакция используется для защиты карбоксильной группы
в синтезе пептидов
29.
* 6.2.2. ДекарбоксилированиеCH2
CH
NH2
N
COOH
CH2
декарбоксилаза
H
CO2
триптофан
триптамин
N
N
NH2
N
H
CH2
H
гистидин
CH2
CH
COOH
декарбоксилаза
N
N
NH2
CO2
CH2
H
гистамин
CH2
NH2
30.
RCH COOH
NH2
Ba(OH)2
t
-BaCO3
R
CH2
NH2
31.
* Взаимодейтсвие по обеим группам – образование хелатныхкомплексов
2 CH3 CH
COOH
+
Cu(OH)2
NH2
O
H3C
NH2
O
C
CH3
+
Cu
NH2
O
C
O
2 H2O
32.
*6.3. Поведение аминокислот при нагревании* -аминокислоты при нагревании дают дикетопиперазины
(диоксопиперазины):
H
H
O
O H
CH3 N H
H
аланин
H N
H O
CH3
O
t
O
N
CH3
+
CH3
N
2 H2O
O
H
2,5-диоксо-3,6-диметилпиперазин
33.
* -аминокислоты при нагревании отщепляют воду (реакцияэлиминирования), образуя ненасыщенные кислоты:
t
CH2 CH2 COOH
CH2 CH COOH
NH2
-аминопропионовая
кислота
пропеновая (акриловая)
кислота
+
NH3
34.
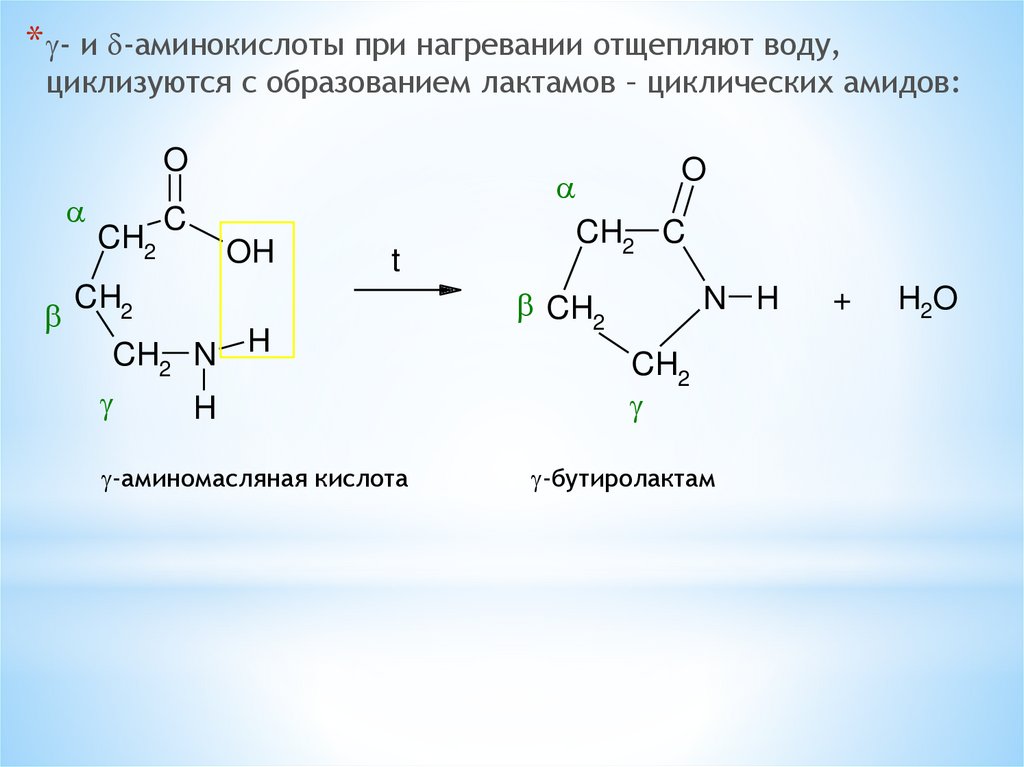
* - и -аминокислоты при нагревании отщепляют воду,циклизуются с образованием лактамов – циклических амидов:
O
CH2
O
C
OH
t
CH2
CH2 N H
H
-аминомасляная кислота
CH2 C
CH2
N H
CH2
-бутиролактам
+
H2O
35.
OO
C OH
CH2
NH2
CH
2
t
CH
2
CH2
-аминовалериановая кислота
C
CH2
CH
2
H
N
CH
2
CH2
-валеролактам
+
H2O
36.
*7. Получение аминокислот* 7.1. Выделение из белков и пептидов
Белки гидролизуют в присутствии кислот (6 М HCl) при
нагревании (110 оС) в течение длительного времени (12-72 ч.).
Используют также щелочной гидролиз и ферментативный
гидролиз.
* 7.2. Микробиологический синтез
используя патоку, аммиак и микрообранизмы Corynebacterium
glutamicum получают глутаминовую кислоту, которая
используется как пищевая добавка.
Выход глутаминовой кислоты составляет 50 кг на 100 кг
введённой глюкозы (время ферментации – 40 часов).
37.
*7.3. Пребиотический (абиогенный) синтез аминокислот*CH4, NH3, H2, H2O, HCN, H2S, CH2O
* УФ-излучение, электрический разряд, радиация и нагретый
пепел вулканов.
* аминокислоты могут образовываться и в космосе, что было
подтверждено анализом мерчисонского метеорита упавшего
1969 году в Австралии. В метеорите были обнаружены 23
рацемические аминокислоты.
38.
*7.4. Химические синтезы аминокислот* 7.4.1. Аммонолиз галогенкарбоновых кислот
CH3 CH
NH3
COOH
CH3 CH
- HCl
Cl
COOH
NH2
* 7.4.2. Синтез Штреккера
O
CH3 C
H
HCN
CH3 CH
OH
CN
NH3
гидролиз
CH3 CH
NH2
CN
CH3 CH
NH2
COOH






























 chemistry
chemistry








