Similar presentations:
Производные пиридин-4-карбоновой кислоты
1.
Производныепиридин-4-карбоновой кислоты
1
2.
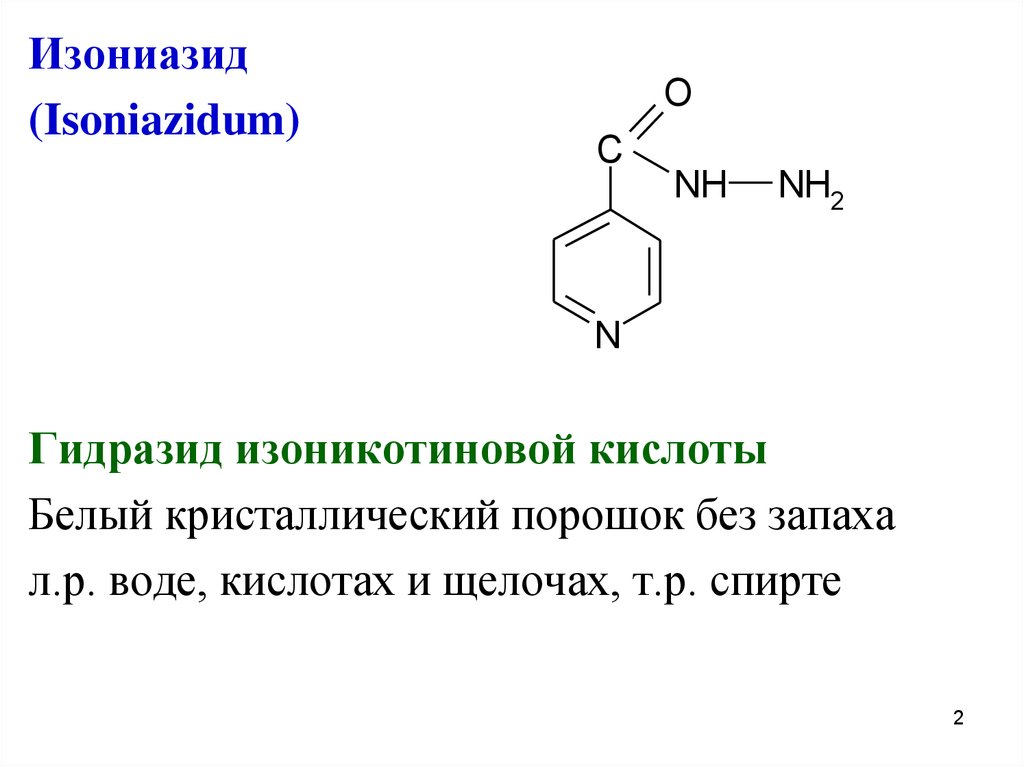
Изониазид(Isoniazidum)
O
C
NH
NH2
N
Гидразид изоникотиновой кислоты
Белый кристаллический порошок без запаха
л.р. воде, кислотах и щелочах, т.р. спирте
2
3.
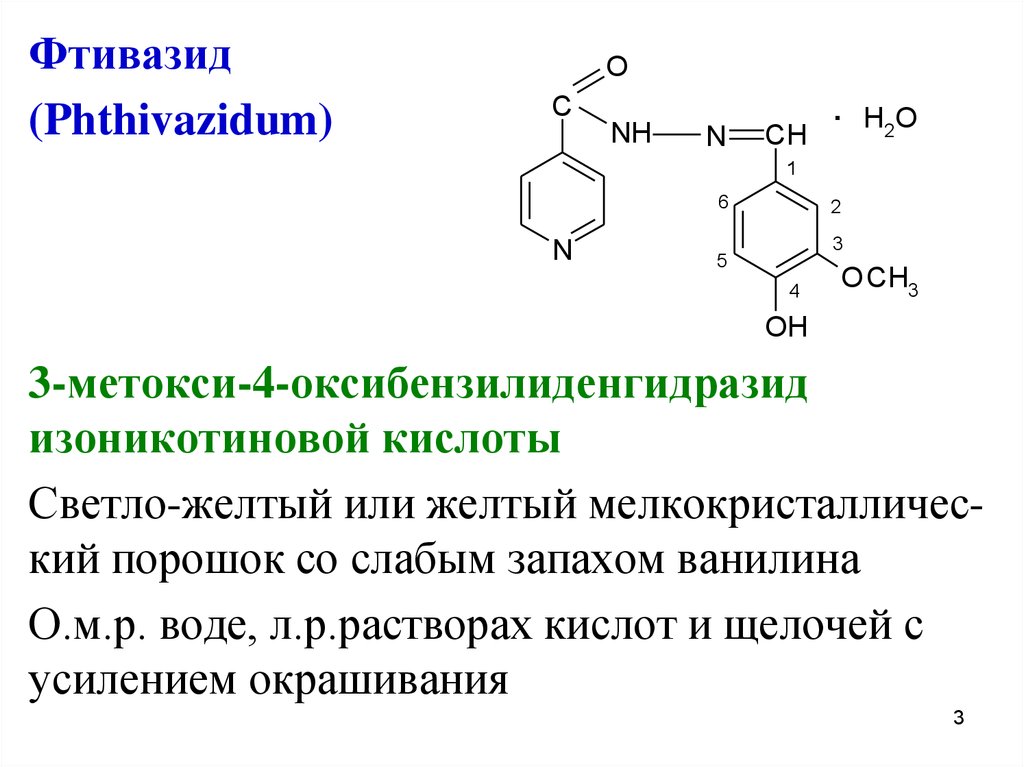
Фтивазид(Phthivazidum)
O
C
NH
N
CH
.
H2O
1
6
N
2
3
5
4
O CH3
OH
3-метокси-4-оксибензилиденгидразид
изоникотиновой кислоты
Светло-желтый или желтый мелкокристаллический порошок со слабым запахом ванилина
О.м.р. воде, л.р.растворах кислот и щелочей с
усилением окрашивания
3
4.
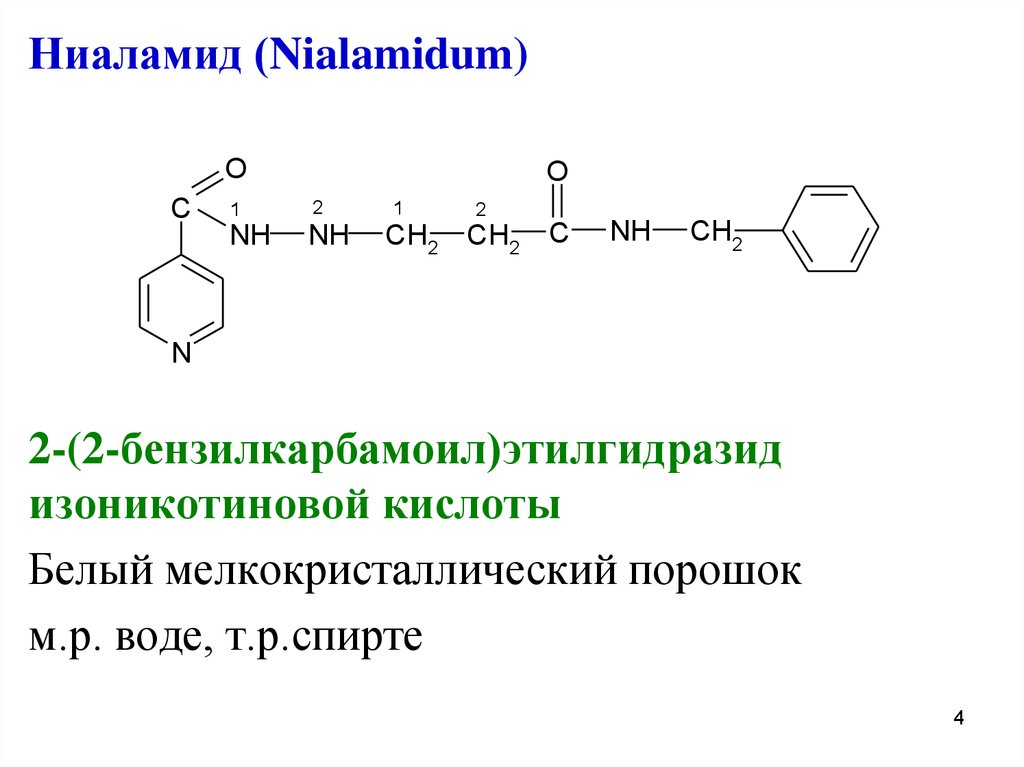
Ниаламид (Nialamidum)O
C
O
1
2
NH
NH
1
2
CH2 CH2 C
NH
CH2
N
2-(2-бензилкарбамоил)этилгидразид
изоникотиновой кислоты
Белый мелкокристаллический порошок
м.р. воде, т.р.спирте
4
5.
Этионамид(Ethionamidum)
S
C
NH2
N
C2H5
Тиоамид -этилизоникотиновой кислоты
Желтый кристаллический или мелкокристаллический порошок с легким запахом сульфидов
П.н.р. воде, р.метаноле, м.р.этаноле
5
6.
Протионамид(Prothionamidum)
S
C
NH2
N
C3H7
Тиоамид -пропилизоникотиновой кислоты
Желтый кристаллический или мелкокристаллический порошок без запаха или почти без запаха
П.н.р. воде, р.метаноле, м.р.этаноле
6
7.
Изониазид и фтивазид относятся к п/туберкулезным препаратам 1-го ряда. Наличие гидразидной группы позволяет проникать внутрь туб.палочки, образуя хелатные соединения с ионами
т.м., т.обр., угнетая деятельность ферментов и п
рекращая жизнь туб.бактерии. Изоник.к-та –
удачный носительгидразидной группы: с одной
стороны она обеспечивает проникновение
препарата в микобактерию туберкулеза с другой
– малотоксична для организма. Т.обр., изониазид
и фтивазид проявляют бактерицидный эффект.
7
8.
Этионамид и протионамид также проявляютп/туберкулезную активность
Ниаламид – антидепрессант, игибитор
моноаминооксидазы, которая дезаминирует
моноамин и т.обр. инактивирует дофамин,
норадреналин, серотонин. Под влиянием
ингибиторов МАО замедляется их метаболизм и
они накапливаются в мозге. Ф/кологичекое
действие ниаламида связано с наличием
карбамидной группы в молекуле препарата.
8
9.
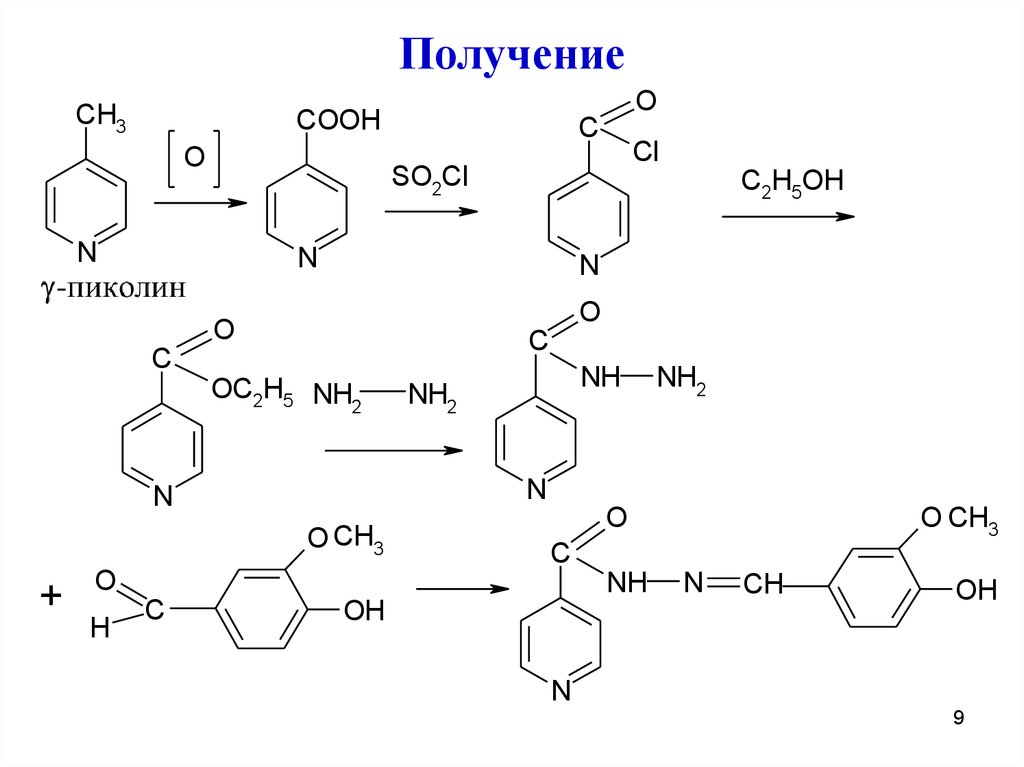
ПолучениеCH3
O
COOH
O
C
SO2Cl
N
C2H5OH
N
N
O
O
C
C
OC2H5 NH
2
NH
NH2
O CH3
O
H
O CH3
C
O
NH
C
NH2
N
N
+
Cl
OH
N
CH
OH
N
9
10.
Аналогично получают ниаламид из изониазида,присоединяя соответствующий радикал
Получение этионамида: Беликов, стр.462
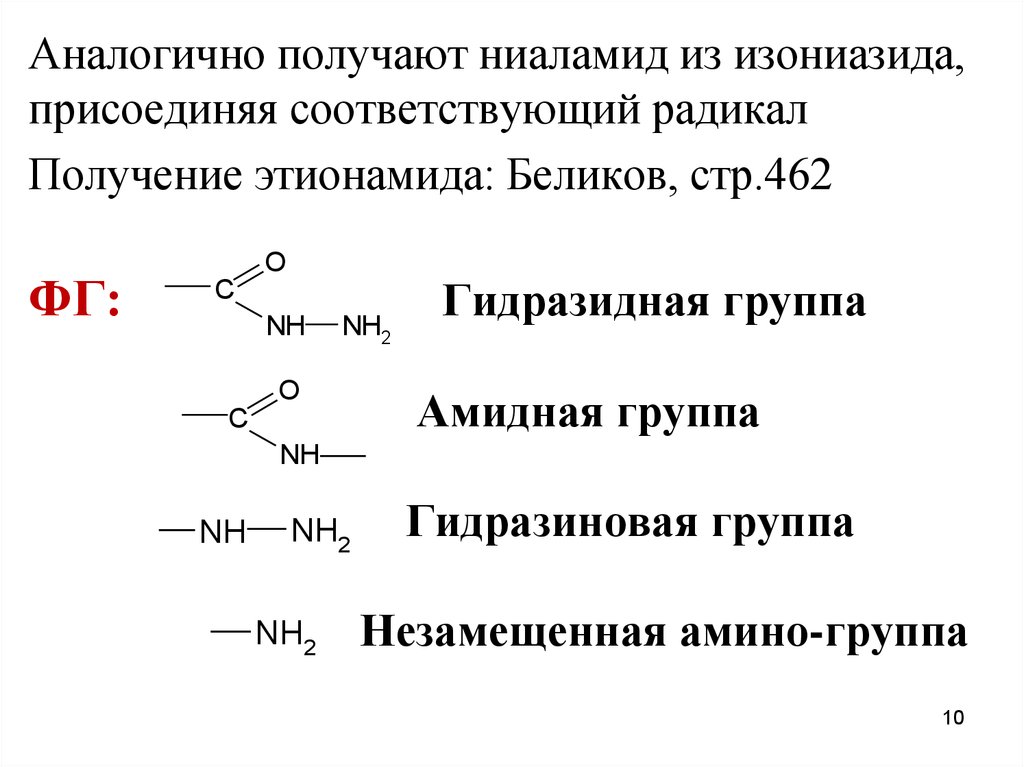
ФГ:
O
C
NH
NH2
O
C
Гидразидная группа
Амидная группа
NH
NH
NH2
NH2
Гидразиновая группа
Незамещенная амино-группа
10
11.
У фтивазида:азометиновая группа
фенольный гидроксил
У этионамида и протионамида:
тиоамидная группа
У всех – пиридиновый цикл
N CH
11
12.
Качественный анализ1. По Т плавления
2. СПФ в УФ-области спектра
3. ИК-спектроскопия
4. ТСХ, ВЭЖХ
Изониазид и фтивазид являются амфолитами:
пиридин.цикл (изониазид, фтивазид) и амино-гр
в гидразиновом фрагменте (изониазид)
обуславливают основные св-ва, кислотные св-ва
– амидная гр (изониазид) и фенол. гидроксил
(фтивазид)
12
13.
Реакции подлинности:1. Реакции на пиридиновый цикл
- Образование глутаконового альдегида
- Пирролиз
- С лимонной кислотой и уксусным ангидридом
2. На третичный ат.N – с общеалкалоидными
реактивами;
Изониазид + (NH4)2MoO4+H2SO4 бурый
Фтивазид + H2SO4 (к) желтое окрашивание
13
14.
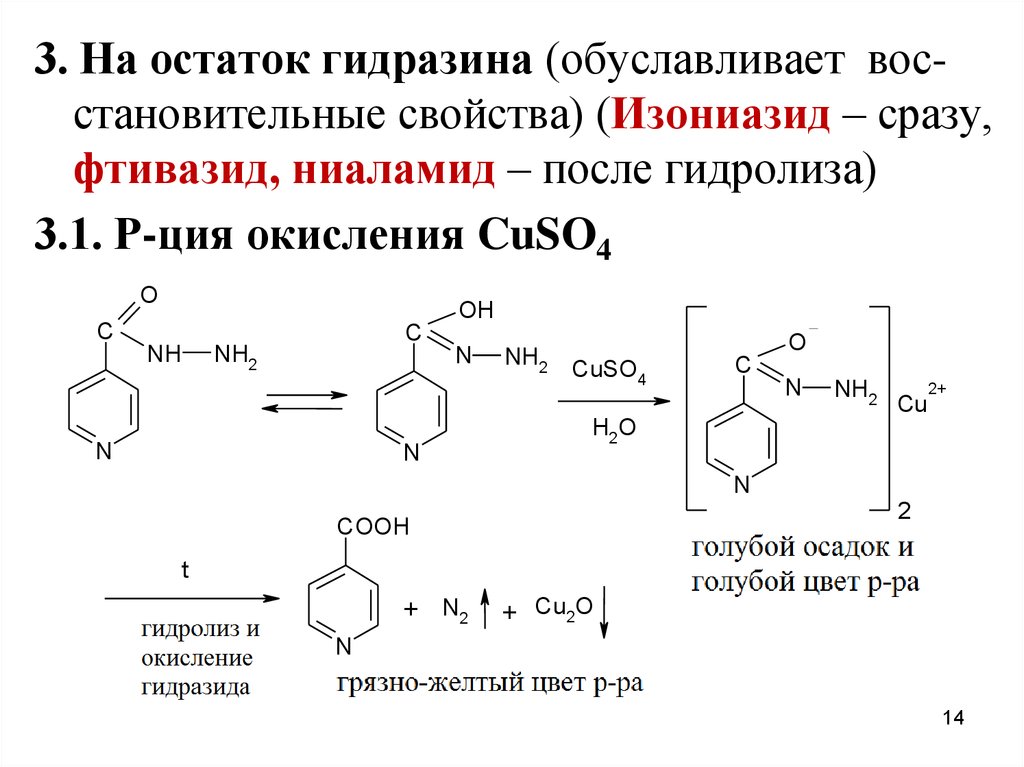
3. На остаток гидразина (обуславливает восстановительные свойства) (Изониазид – сразу,фтивазид, ниаламид – после гидролиза)
3.1. Р-ция окисления CuSO4
O
C
NH
C
NH2
OH
N
N
N
NH2
CuSO4
C
O
N
NH2
Cu
2+
H2O
N
2
COOH
t
+ N2
+ Cu2O
N
14
15.
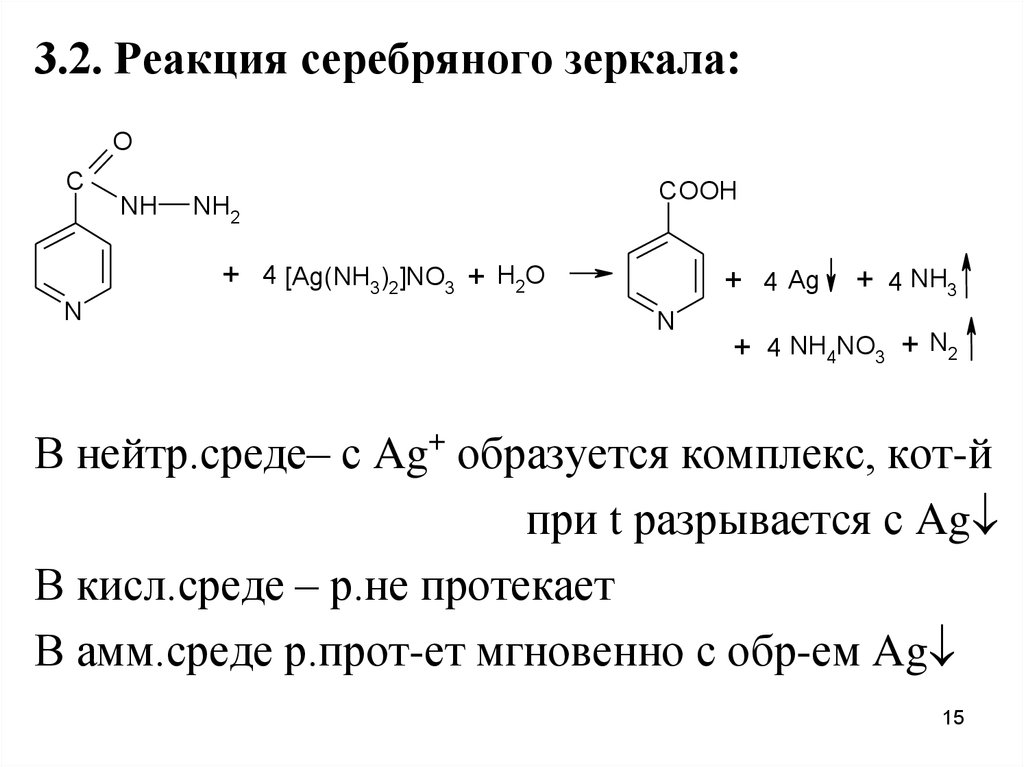
3.2. Реакция серебряного зеркала:O
C
NH
NH2
COOH
+ 4 [Ag(NH3)2]NO3 + H2O
N
+ 4 Ag
N
+ 4 NH3
+ 4 NH4NO3 + N2
В нейтр.среде– с Ag+ образуется комплекс, кот-й
при t разрывается с Ag
В кисл.среде – р.не протекает
В амм.среде р.прот-ет мгновенно с обр-ем Ag
15
16.
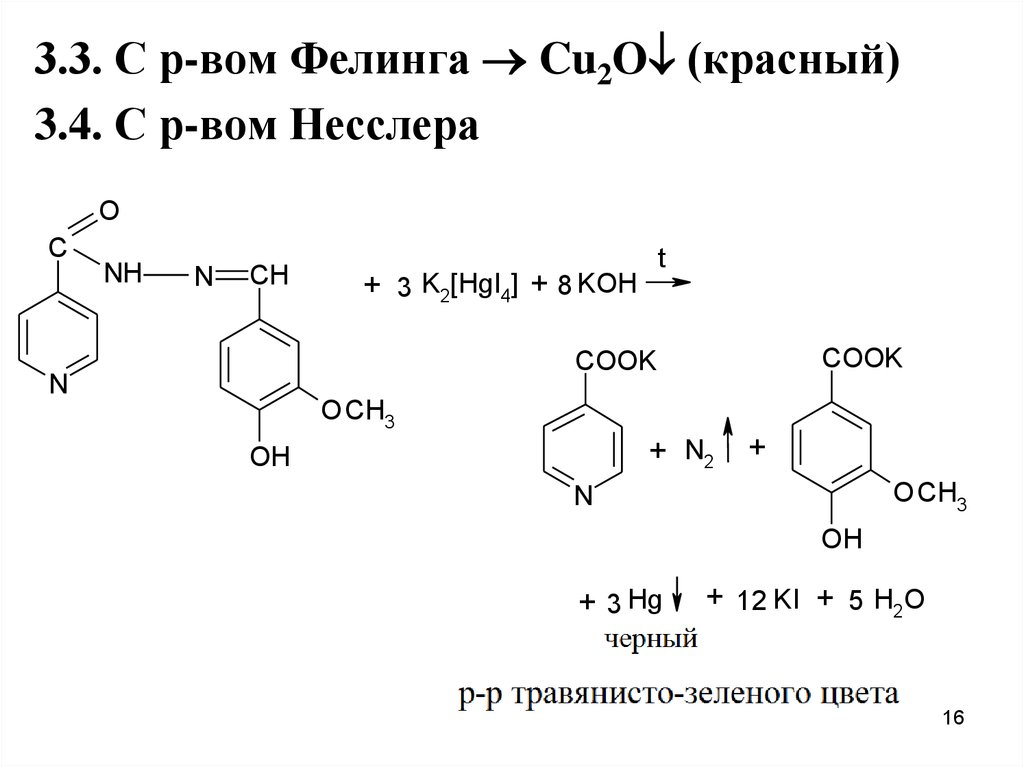
3.3. С р-вом Фелинга Cu2O (красный)3.4. С р-вом Несслера
O
C
NH
N
CH
t
+ 3 K2[HgI4] + 8 KOH
COOK
COOK
N
O CH3
+ N2
OH
+
O CH3
N
OH
+ 3 Hg
+ 12 KI + 5 H2O
16
17.
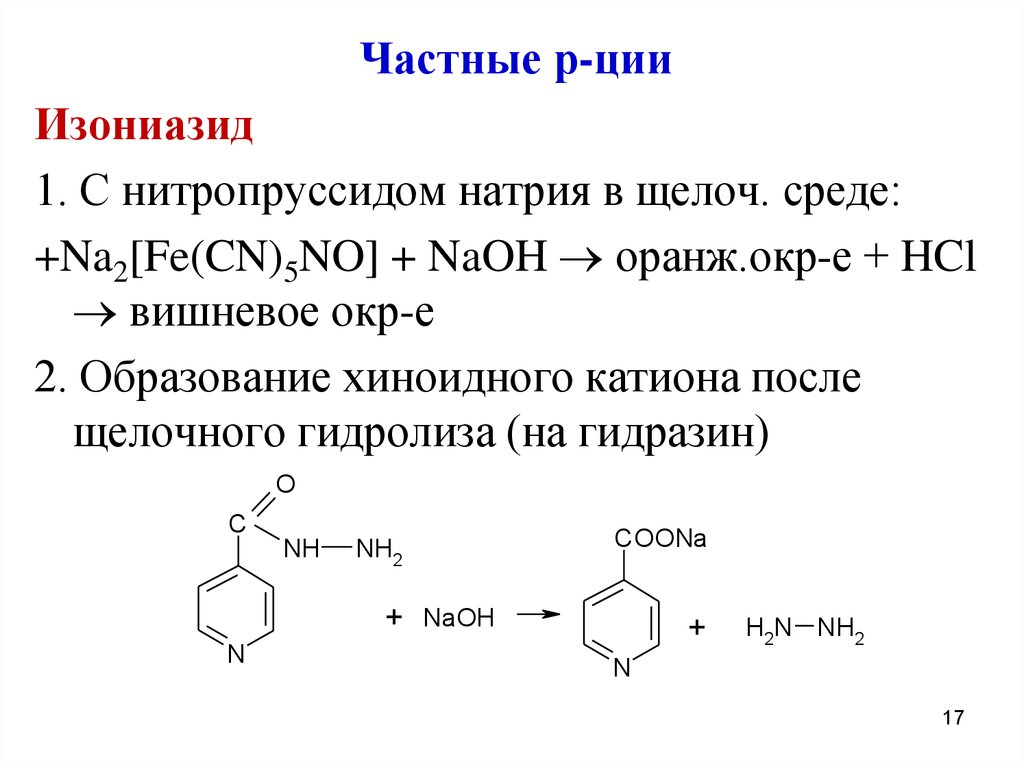
Частные р-цииИзониазид
1. С нитропруссидом натрия в щелоч. среде:
+Na2[Fe(CN)5NO] + NaOH оранж.окр-е + HCl
вишневое окр-е
2. Образование хиноидного катиона после
щелочного гидролиза (на гидразин)
O
C
NH
NH2
COONa
+ NaOH
N
+
H2N NH2
N
17
18.
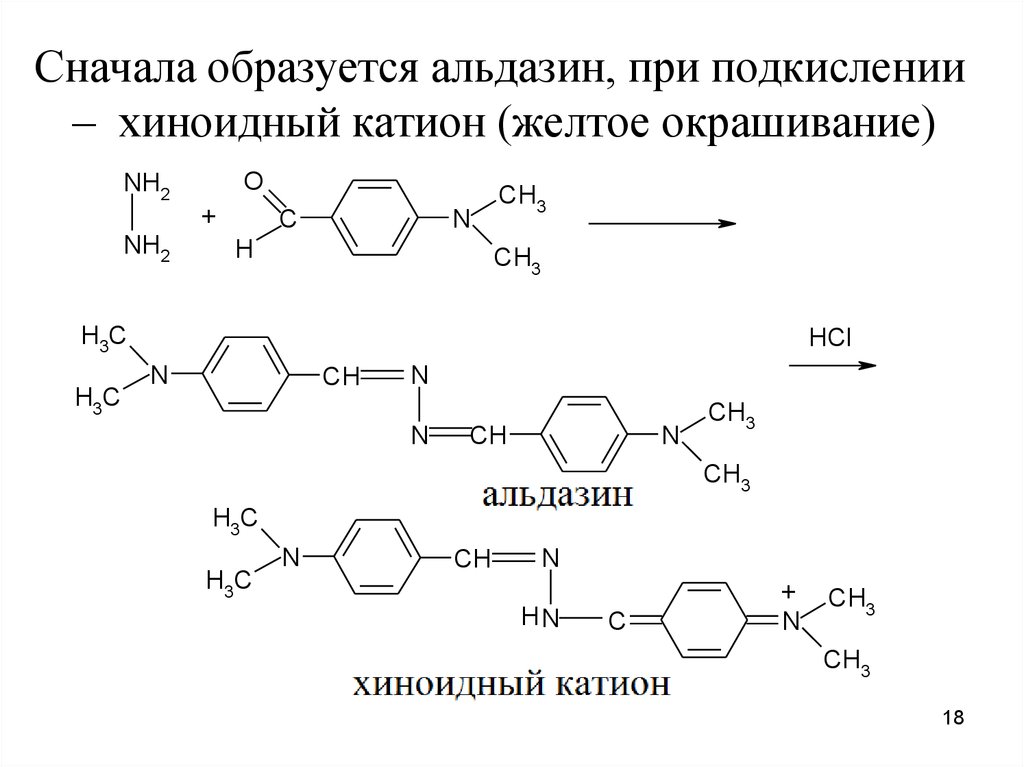
Сначала образуется альдазин, при подкислении– хиноидный катион (желтое окрашивание)
O
NH2
+
NH2
C
N
H
CH3
CH3
H3C
H3C
HCl
N
CH
N
N
CH
N
CH3
CH3
H3C
H3C
N
CH
N
HN
+
C
N
CH3
CH3
18
19.
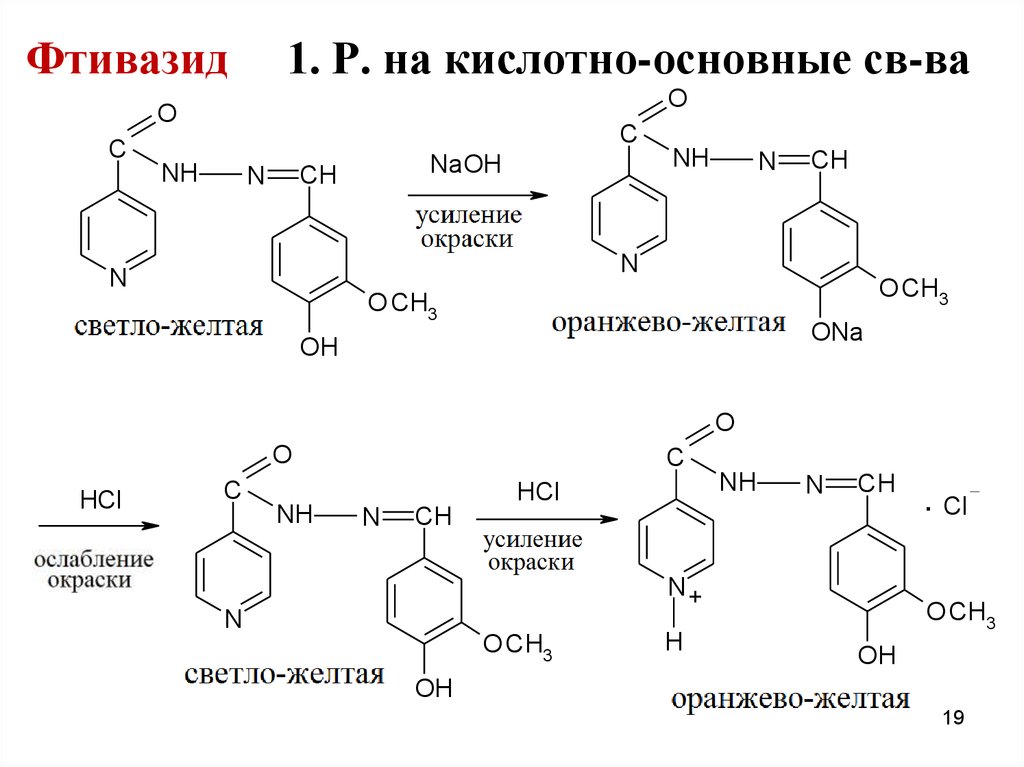
Фтивазид1. Р. на кислотно-основные св-ва
O
O
C
C
NH
NH
NaOH
CH
N
N
CH
N
N
O CH3
O CH3
ONa
OH
O
O
HCl
C
C
NH
NH
HCl
N
N
CH
CH
N+
N
O CH3
H
. Cl
O CH3
OH
OH
19
20.
2. Кислотный гидролиз по азометиновой иамидной группам
O
COOH
O
HCl
C
NH
,
C
t
NH2
CH
N
H
+
H2O
+
NH2
N
N
O CH3
OH
O CH3
OH
O
H
CH3
C
CH3
O
+
t
H2SO4
O
CH
O CH3
OH
O CH3
OH
20
21.
3. Образование хиноидного катиона послегидролиза (на гидразин)
4. На фенольный гидроксил с FeCl3 – фиол.окр.
Этионамид, протионамид
1. При нагревнии с HCl образуется H2S
H2S + (CH3COO)2Pb PbS + 2CH3COOH
Фильтр-я бумага, пропитанная (CH3COO)2Pb ,
окрашивается в черный цвет
21
22.
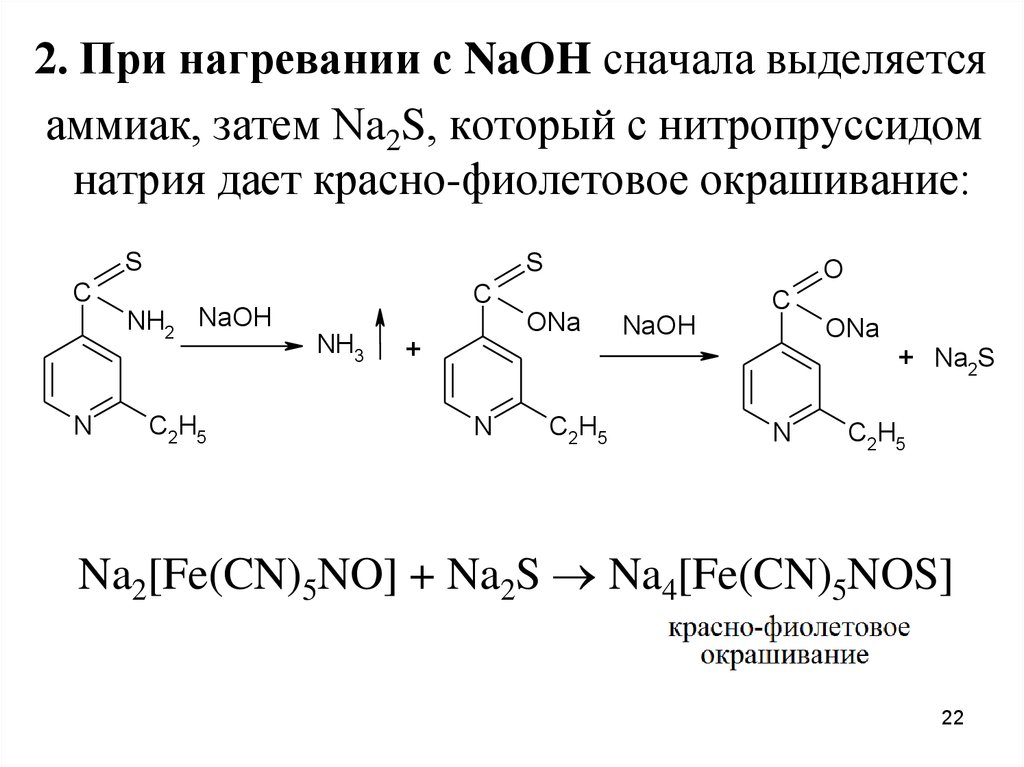
2. При нагревании с NaOH сначала выделяетсяаммиак, затем Na2S, который с нитропруссидом
натрия дает красно-фиолетовое окрашивание:
S
S
C
NH2
N
C
NaOH
C2H5
O
NH3
ONa
+
C
NaOH
ONa
+ Na2S
N
C2H5
N
C2H5
Na2[Fe(CN)5NO] + Na2S Na4[Fe(CN)5NOS]
22
23.
ПримесиФтивазид, ниаламид – не допустима примесь
изониазида
Определение: ЛВ взбалтывают с ледяной водой,
фильтруют. К фильтрату + НCl + NaNO2.
Проба, взятая через 3 мин, д. давать синее
пятно на йодкрахм.бумаге
O
Суть:
O
C
NH
C
NH2
N
NaNO2
N
N
N
HCl
+ NaCl + 2 H2O
N
23
24.
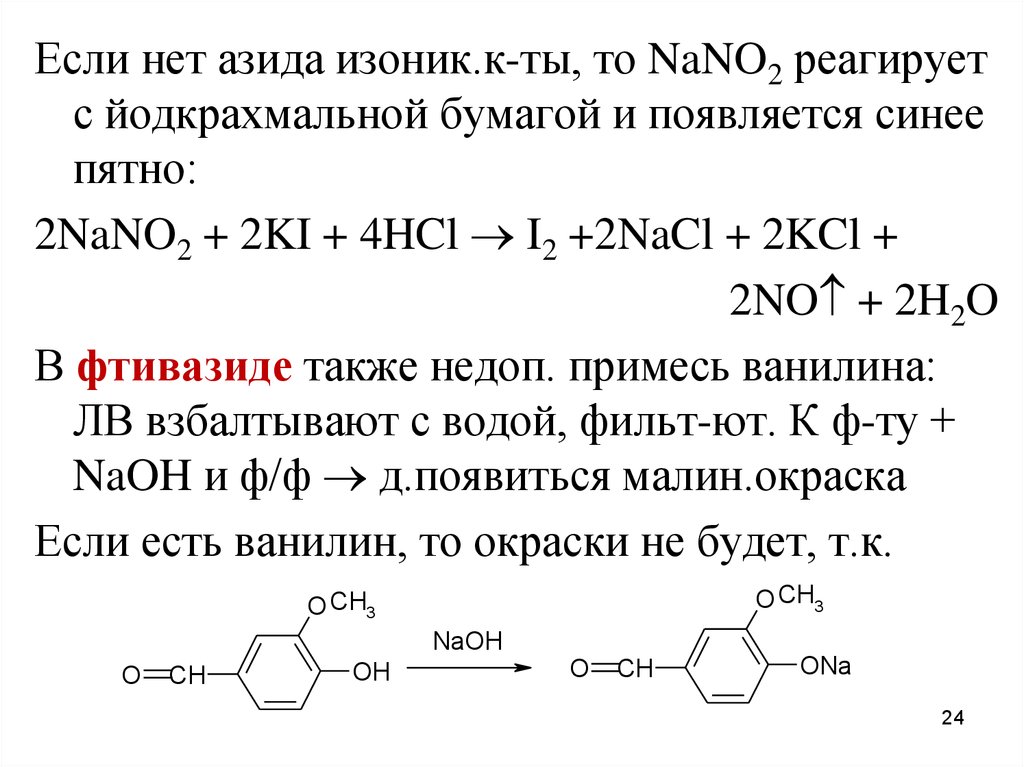
Если нет азида изоник.к-ты, то NaNO2 реагируетс йодкрахмальной бумагой и появляется синее
пятно:
2NaNO2 + 2KI + 4HCl I2 +2NaCl + 2KCl +
2NO + 2H2O
В фтивазиде также недоп. примесь ванилина:
ЛВ взбалтывают с водой, фильт-ют. К ф-ту +
NaOH и ф/ф д.появиться малин.окраска
Если есть ванилин, то окраски не будет, т.к.
O CH3
O CH3
NaOH
O
CH
OH
O
CH
ONa
24
25.
Изониазид – примесь гидразина (доп), ТСХЭтионамид, протионамид – посторонние
примеси (доп), ТСХ
25
26.
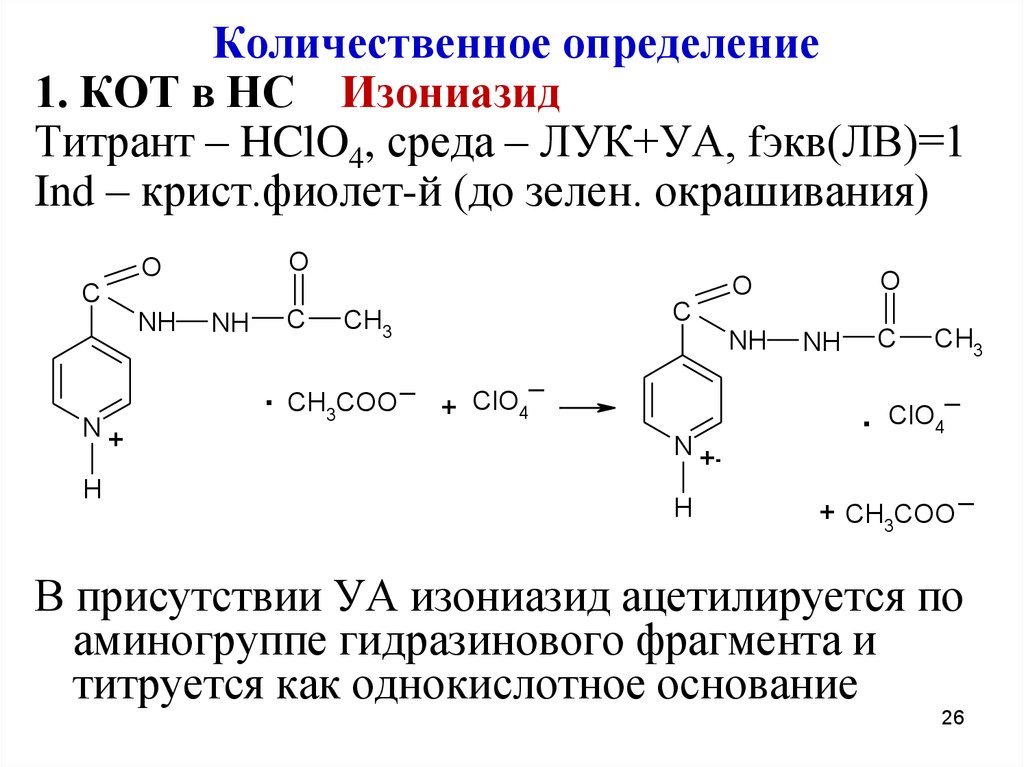
Количественное определение1. КОТ в НС Изониазид
Титрант – HClO4, среда – ЛУК+УА, fэкв(ЛВ)=1
Ind – крист.фиолет-й (до зелен. окрашивания)
O
O
NH
NH
C
H
C
CH3
. CH COO
N+
O
O
C
3
NH
_
+ ClO4
_
N+
NH
C
CH3
. ClO
_
4
+
H
+ CH3COO
_
В присутствии УА изониазид ацетилируется по
аминогруппе гидразинового фрагмента и
титруется как однокислотное основание
26
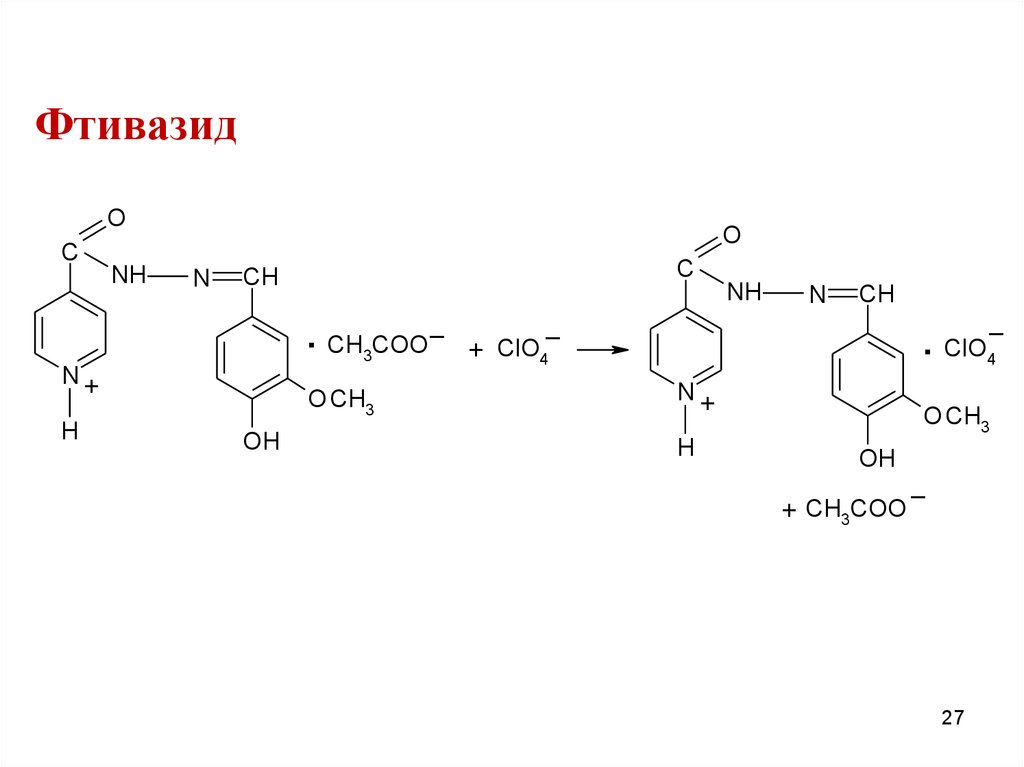
27.
ФтивазидO
O
C
NH
N
C
CH
NH
. CH COO _
3
N+
H
O CH3
OH
N
CH
_
. ClO
+ ClO4
_
4
N+
H
O CH3
OH
+ CH3COO
_
27
28.
Этионамид, протионамидТитрант – HClO4, среда – ЛУК,
fэкв(ЛВ)=1
Ind – крист.фиолетовый
28
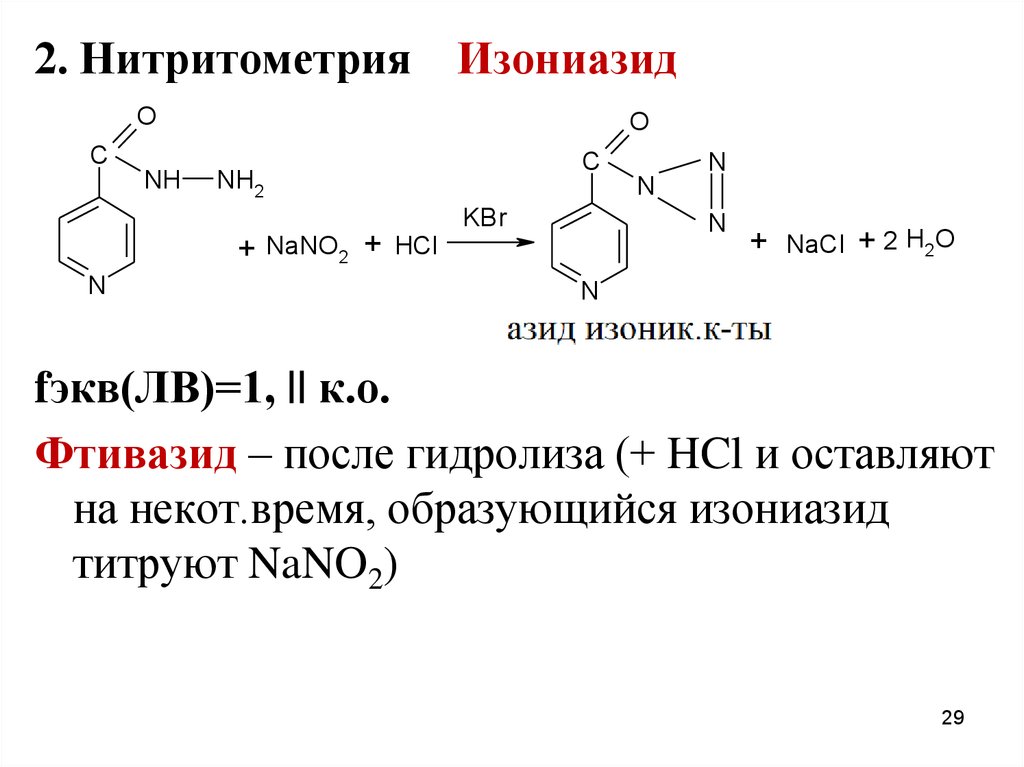
29.
2. Нитритометрия ИзониазидO
O
C
NH
C
NH2
N
KBr
N
+ NaNO2 + HCl
N
N
+ NaCl + 2 H2O
N
fэкв(ЛВ)=1, || к.о.
Фтивазид – после гидролиза (+ HCl и оставляют
на некот.время, образующийся изониазид
титруют NaNO2)
29
30.
Ниаламид – образуется нитрозопроизводноеO
O
C
NH
NH
R
+ NaNO2 + HCl
N
C
NH
KBr
N
R
N
O
+ NaCl + H2O
N
fэкв(ЛВ)=1, || к.о.
30
31.
3. Ок-вос.методы (за счет остатка гидразина)Изониазид 3.1. Иодометрия (обр. иодиметрия)
CONH NH2
COONa
+ 2 I2 + 5 NaHCO3
N
N
+ N2 + 4 NaI + 5 CO2 + 4 H2O
4NaI
I2 + 2Na2S2O3 2NaI + Na2S4O6
N22– – 4е N20
С(Na2S2O3)·M(1/4 Изн)
Т(Na2S2O3/Изн) = ——————————
1000
31
32.
Фактически окислителем является NaIO, кот-йобразуется при диспропорц-нии I2 в щелочной
среде, создаваемой NaHCO3
I2 + 2NaHCO3 NaI + NaIO + 2CO2 + H2O
CONH NH2
COOH
+ 2 NaIO
N
+ N2 + 2 NaI + H2O
N
NaIO + NaI + 2HCl I2 + 2NaCl + H2O
I2 + 2Na2S2O3 2NaI + Na2S4O6
32
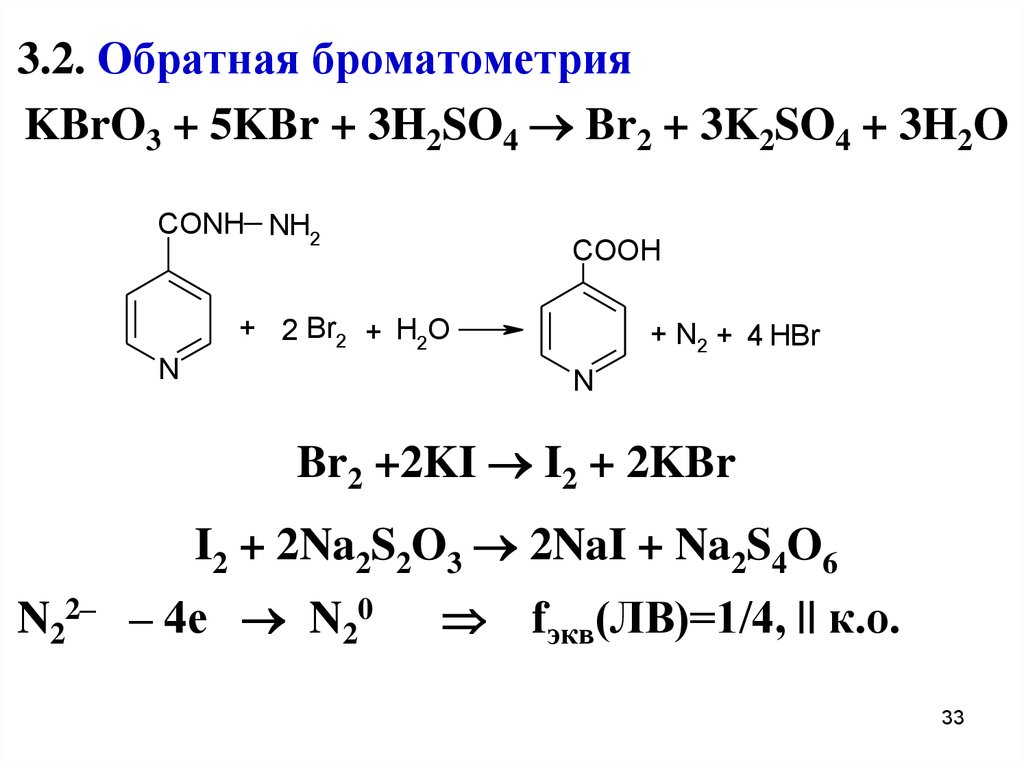
33.
3.2. Обратная броматометрияKBrO3 + 5KBr + 3H2SO4 Br2 + 3K2SO4 + 3H2O
CONH NH2
COOH
+ 2 Br2 + H2O
N
+ N2 + 4 HBr
N
Br2 +2KI I2 + 2KBr
I2 + 2Na2S2O3 2NaI + Na2S4O6
N22– – 4е N20
fэкв(ЛВ)=1/4, || к.о.
33
34.
3.3. Обратная цериметрияCONH NH2
COOH
+ 4 Ce(SO4)2 + H2O
N
+ N2 + 2 Ce2(SO4)2 + 2 H2SO4
N
Ce(SO4)2 + 2 KI
I2 + Ce2(SO4)3 + K SO
2
4
I2 + 2Na2S2O3 2NaI + Na2S4O6
Ind – крахмал, fэкв(ЛВ)=1/4, || к.о.
Фтивазид, ниаламид – м.использовать эти
методы после гидролиза
34
35.
Частные методы1. Инъекционный р-р изониазида 5%, 10%
Ацидиметрия CONH NH2
CONH NH2
. Cl
+ CaCl2 + HCl
N
N+
H
CaCl2 – усиливает основные свойства
Ind – бромфеноловый синий (до желтой окраски)
35
36.
2. Фтивазид – иодатометрия (после гидролиза)Сначала проводят кислотный гидролиз при
кипячении (образуется гидразин), р-р охл-ют и
титруют гидразин иодатом калия:
5NH2 NH2 + 4KIO3 +4HCl 5N2 + 2I2 +4KCl +
12H2O
Незадолго до конца титрования в р-р + хлф, в
котором I2 р-ется лучше, чем в воде, хлф слой
окрашивается в фиолетовый цвет и далее
титруют KIO3 до обесцвечивания хлф слоя
2I2 + KIO3 + 6HCl 5ICl + KCl + 3H2O
36
37.
Суммарная реакция:NH2 NH2 + KIO3 +2HCl N2 + ICl + KCl +
3H2O
I+5 + 4e I+1
fэкв(ЛВ)=1/4, || к.о.
4. Физ-хим. методы (СПФ, ВЭЖХ)
37
38.
ХранениеСп. Б, в ХУТ, прохл, защищ. от света, сухом месте
Применение
Изониазид, фтивазид, этионамид, протионамид
– п/туберкулезные средства, внутрь по по 0,3 г
(изон) и 0,5 г (фтив) 2-3 р/день
Этионамид, протионамид менее активны, чем
изониазид и стрептомицин, но действуют на
устойчивые к ним микобактерии
Ниаламид – в психиатрической практике при
депрессивных состояниях (тб по 0,025 г)
38
39.
и39






















 chemistry
chemistry