Similar presentations:
Функциональные производные карбоновых кислот
1. Функциональные производные карбоновых кислот
2. Цель лекции
Получить четкое представление охимическом строении и свойствах
функциональных производных
карбоновых кислот, взаимосвязи
химического строения и
биологической активности.
3. План лекции
1.2.
3.
4.
5.
6.
Классификация
Номенклатура
Физические свойства
Способы получения
Химические свойства
Медико-биологические свойства
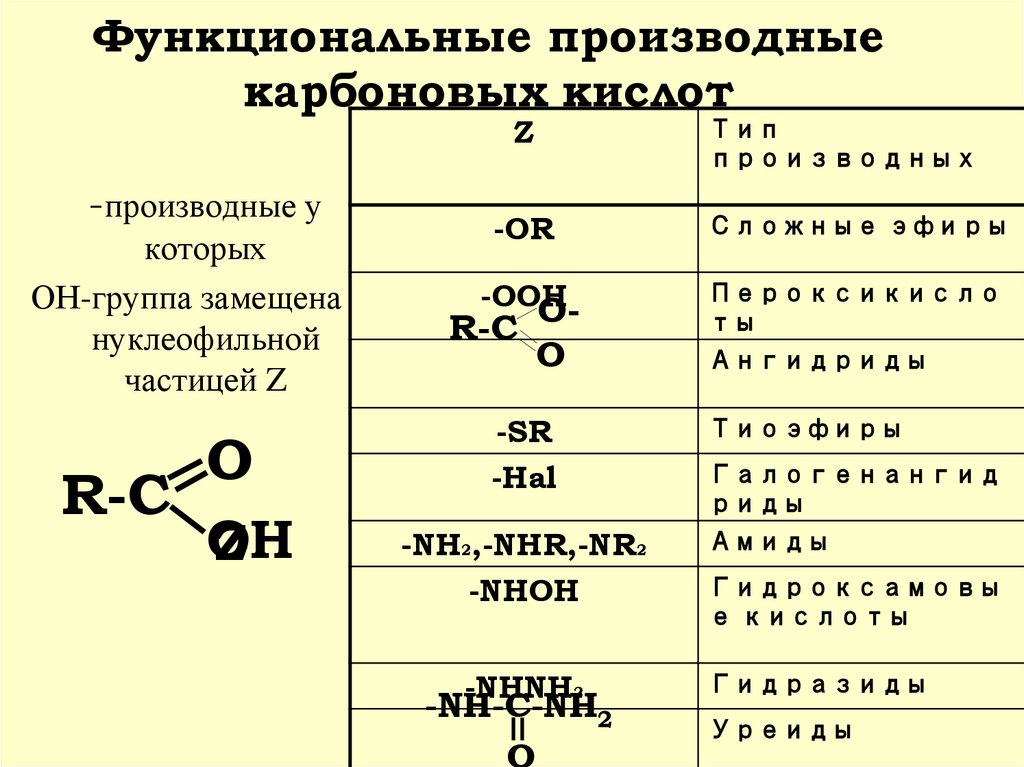
4. Функциональные производные карбоновых кислот
Z-производные у
которых
ОН-группа замещена
нуклеофильной
частицей Z
O
R-C
OH
Z
Тип
производных
-ОR
Сложные эфиры
-OOH
O-
Пероксикисло
ты
R-C
O
-SR
-Hal
-NH2,-NHR,-NR2
-NHOH
-NHNH2
-NH-C-NH2
O
Ангидриды
Тиоэфиры
Галогенангид
риды
Амиды
Гидроксамовы
е кислоты
Гидразиды
Уреиды
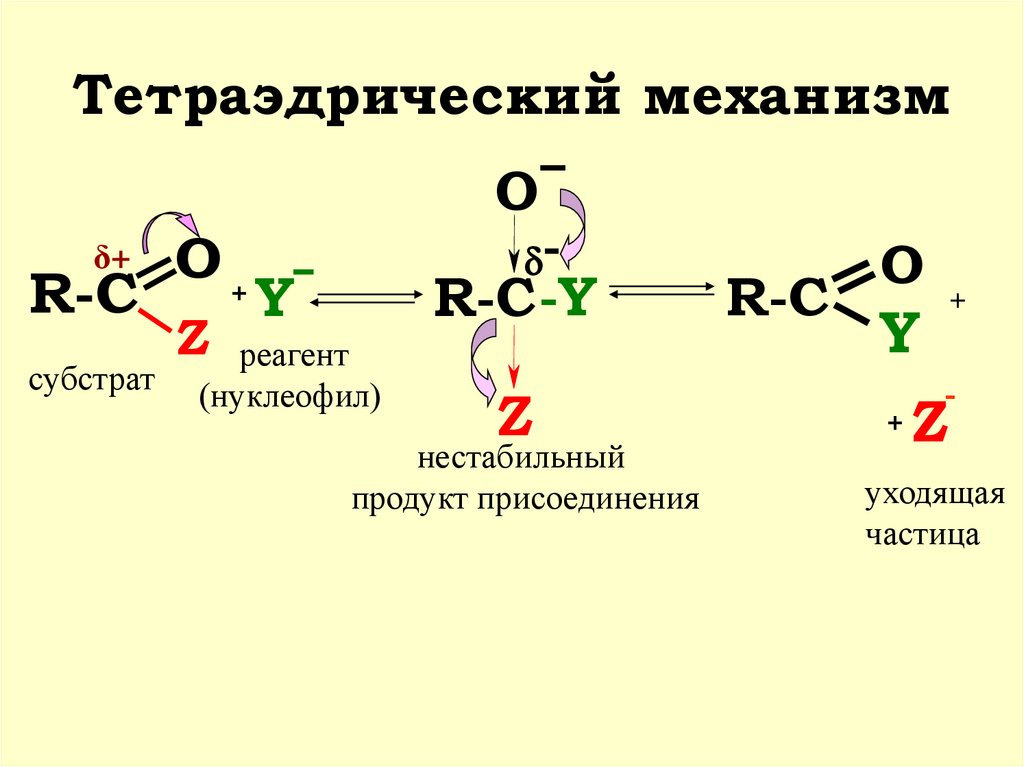
5. Тетраэдрический механизм
Oδ+
R-C
субстрат
O+
Z
R-C -Y
Y
реагент
(нуклеофил)
Z
нестабильный
продукт присоединения
R-C
O
+
Y
+
-
Z
уходящая
частица
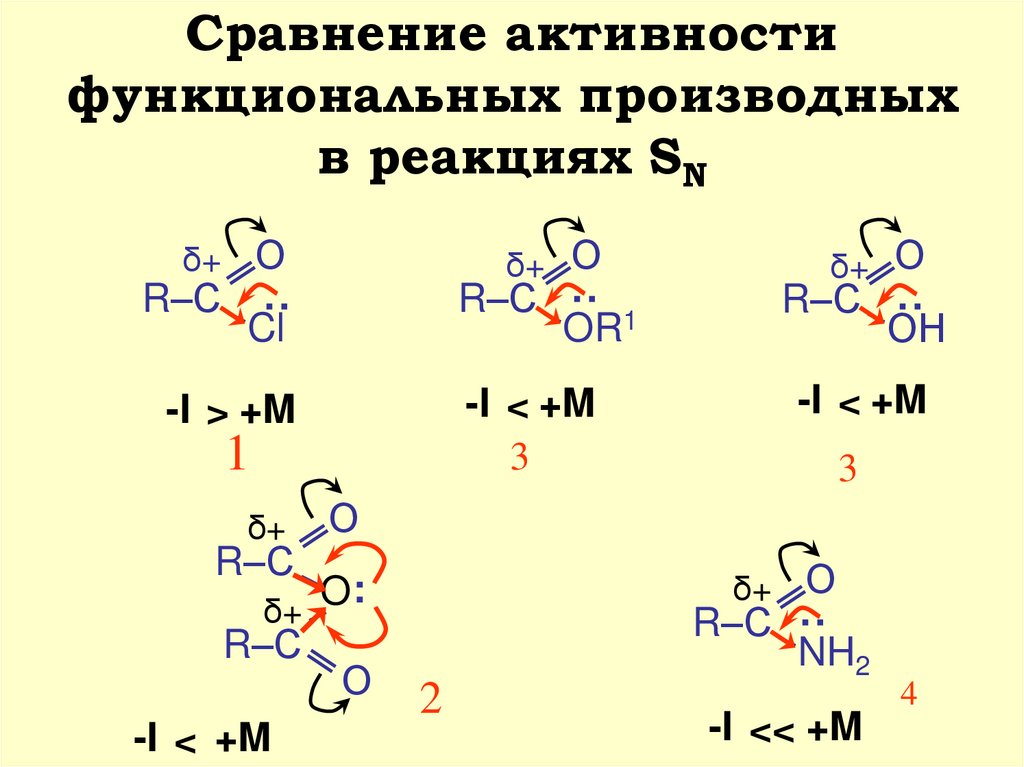
6. Сравнение активности функциональных производных в реакциях SN
Cl1
ОН
-I < +M
3
О
R–С
R–С
2
:
δ+ О
:
O
δ+
R–С
О
-I < +M
R–С
OR1
-I < +M
3
-I > +M
δ+
δ+ О
:
R–С
:
R–С
δ+ О
:
δ+ О
NH2
-I << +M
4
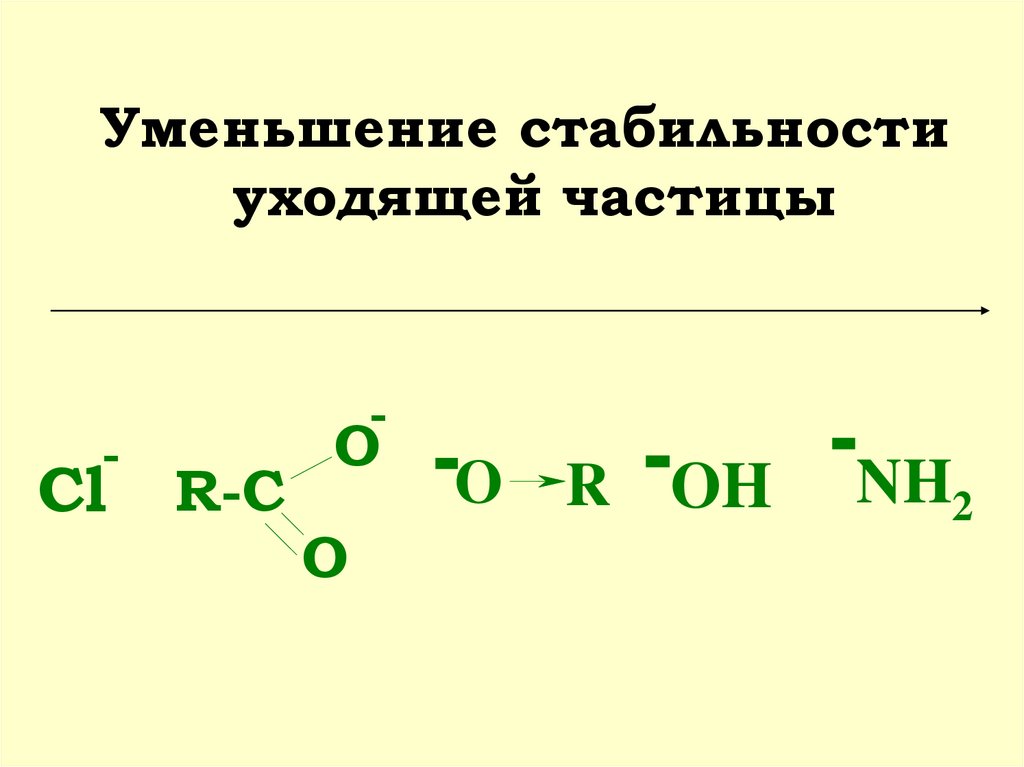
7.
Уменьшение стабильностиуходящей частицы
-
Cl
-
R-C
O
O
-O
R
-OH -NH2
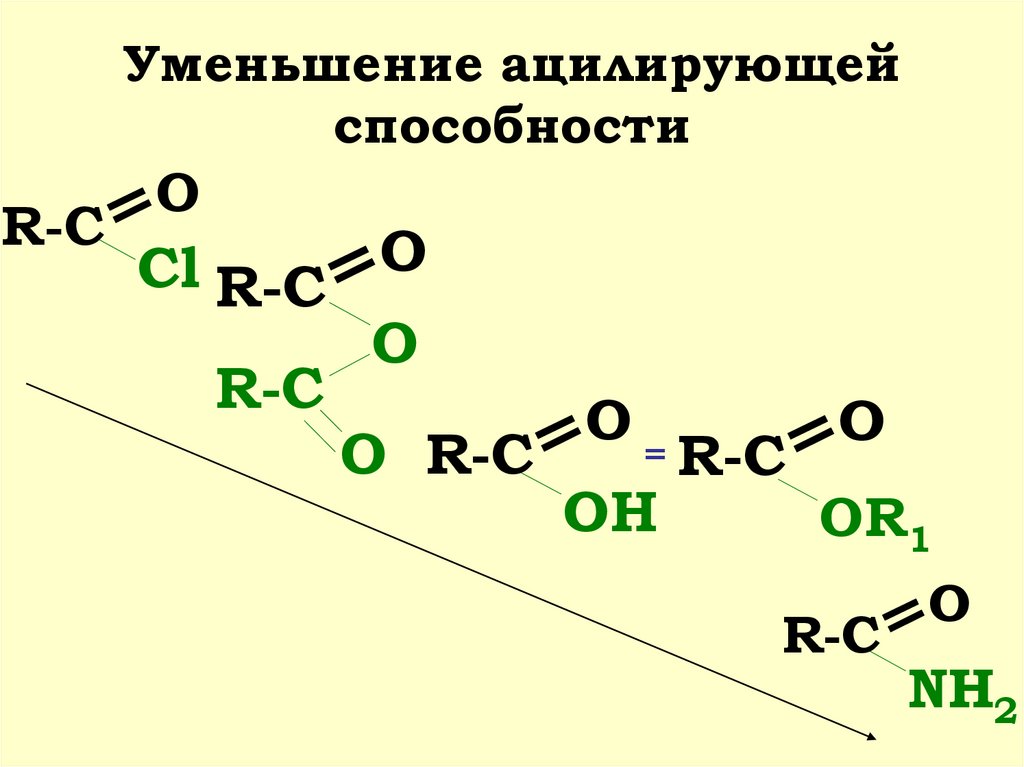
8. Уменьшение ацилирующей способности
OR-C
Cl R-C O
R-C
O
O R-C
O=
OH
R-C
O
OR1
R-C
O
NH2
9.
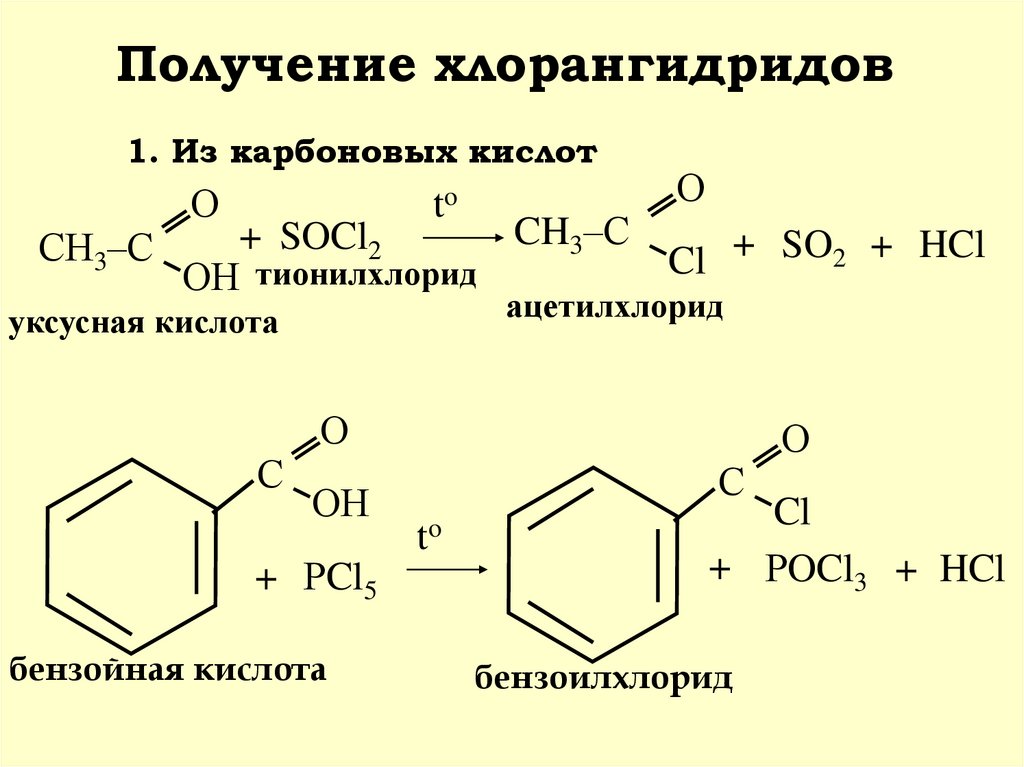
ХЛОРАНГИДРИДЫ10. Получение хлорангидридов
1. Из карбоновых кислотСН3–С
О
to
О
CH3–С
+ SOCl2
+ SO2 + HCl
Cl
ОН тионилхлорид
ацетилхлорид
уксусная кислота
С
О
ОН
+ РCl5
бензойная кислота
С
to
О
Cl
+ РOCl3 + HCl
бензоилхлорид
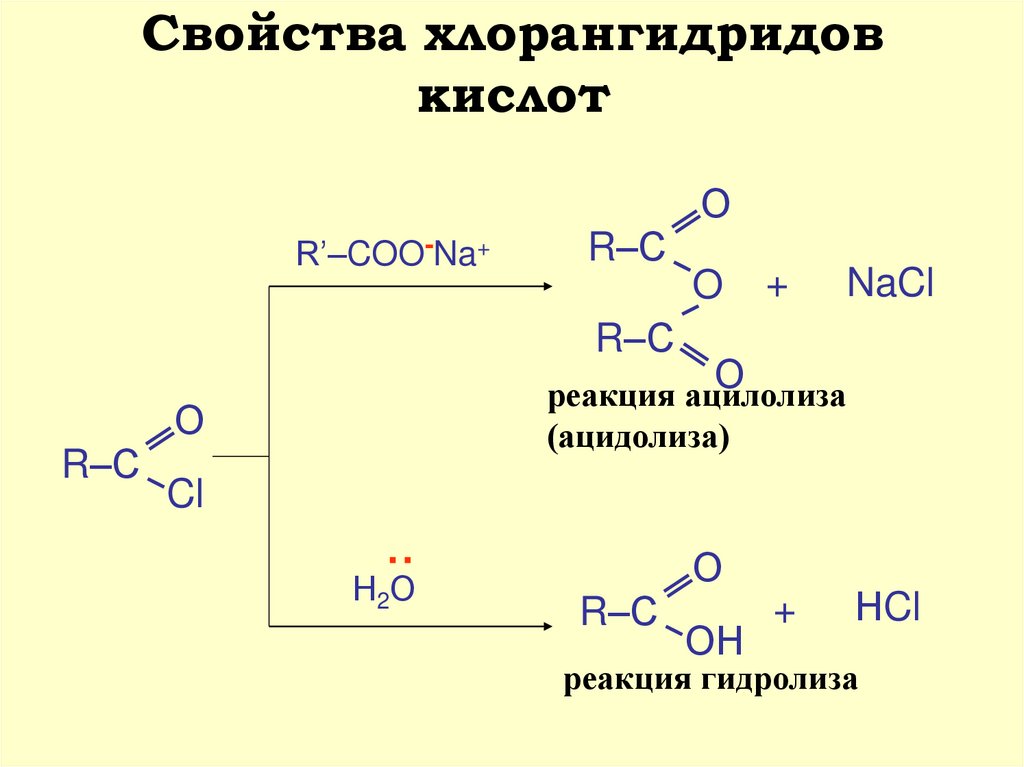
11. Свойства хлорангидридов кислот
ОR–С
O
R–С
NaCl
реакция ацилолиза
(ацидолиза)
О
Cl
О
:
R–С
+
О
R’–COO-Na+
Н2О
R–С
ОН
+
НCl
реакция гидролиза
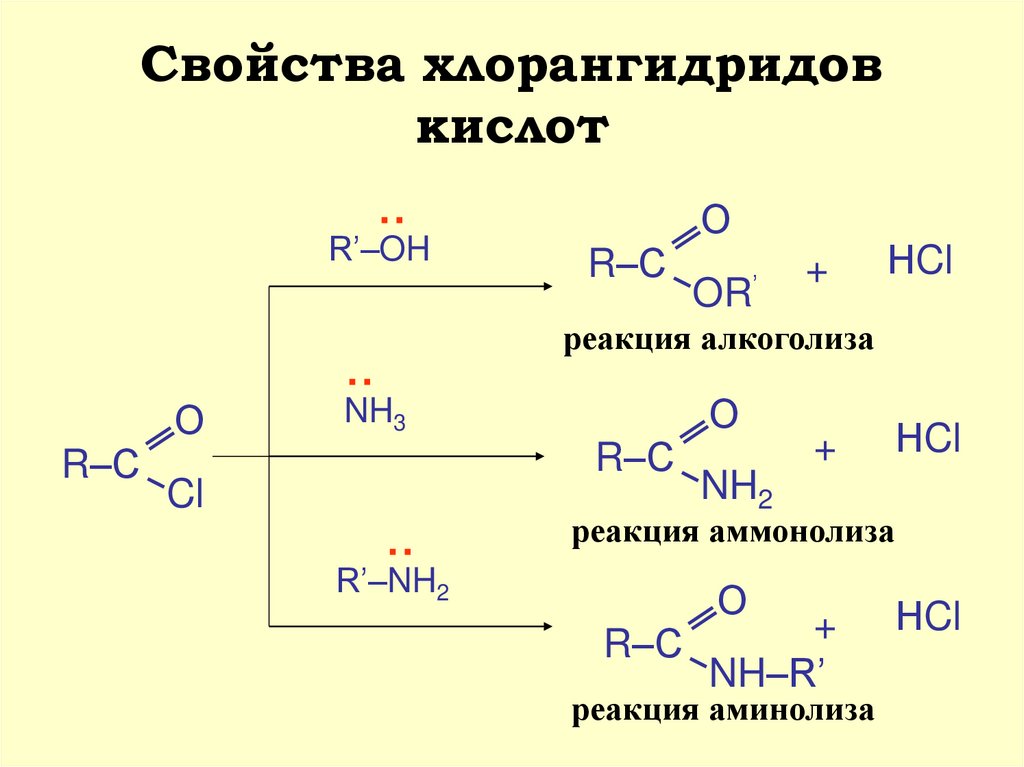
12. Свойства хлорангидридов кислот
:О
R’–OH
R–С
OR’
+
НCl
:
реакция алкоголиза
О
R–С
Cl
+
НCl
NH2
:
R–С
О
NH3
реакция аммонолиза
R’–NH2
О
+
R–С
NH–R’
реакция аминолиза
НCl
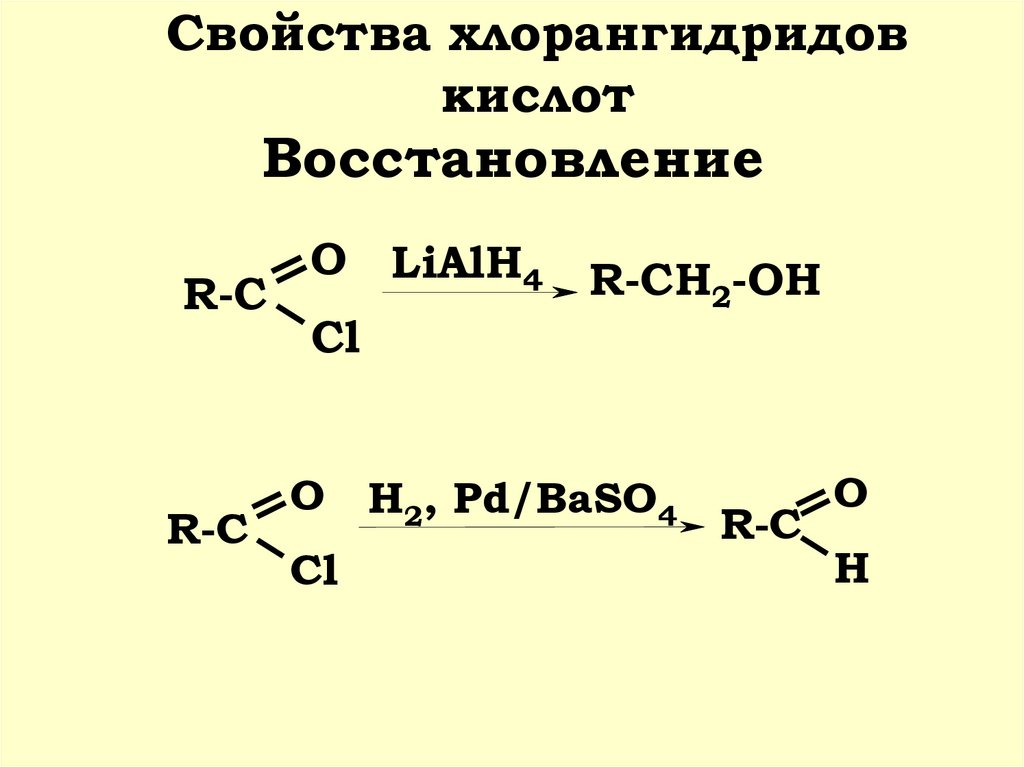
13. Восстановление
Свойства хлорангидридовкислот
Восстановление
R-C
R-C
O LiAlH4
Cl
R-CH2-OH
O H2, Pd/BaSO4
Cl
R-C
O
H
14.
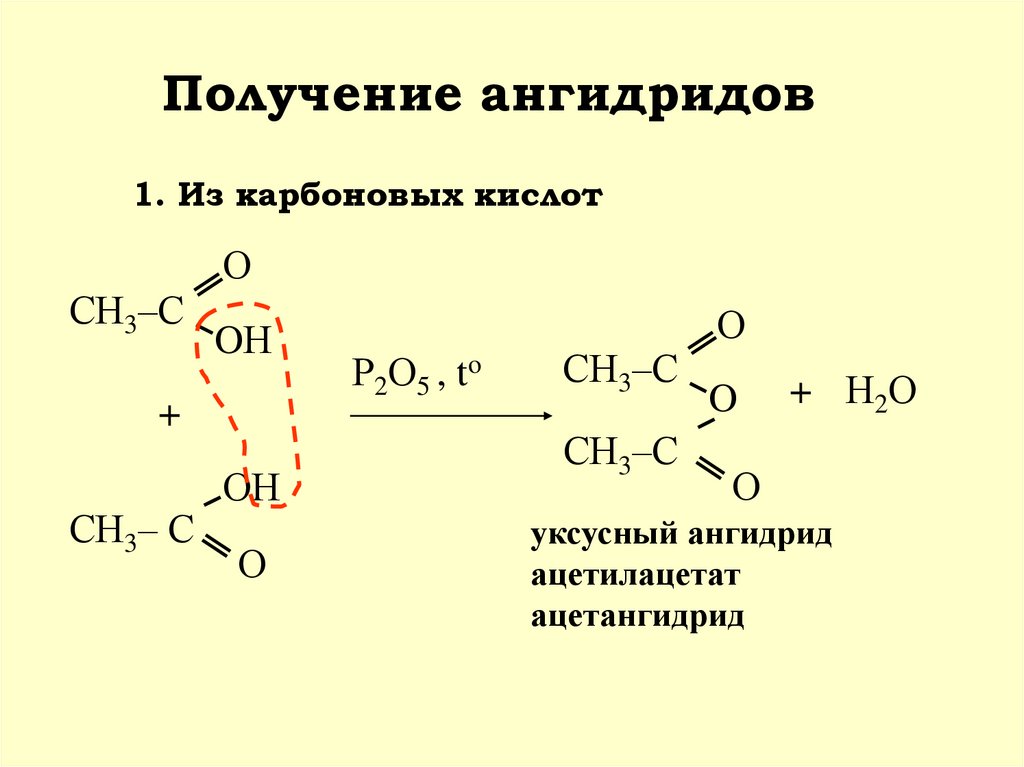
АНГИДРИДЫ15. Получение ангидридов
1. Из карбоновых кислотО
OН
+
О
СН3– С
ОН
Р2О5 , to
СН3–С
СН3–С
О
O
+ Н2О
О
СН3–С
уксусный ангидрид
ацетилацетат
ацетангидрид
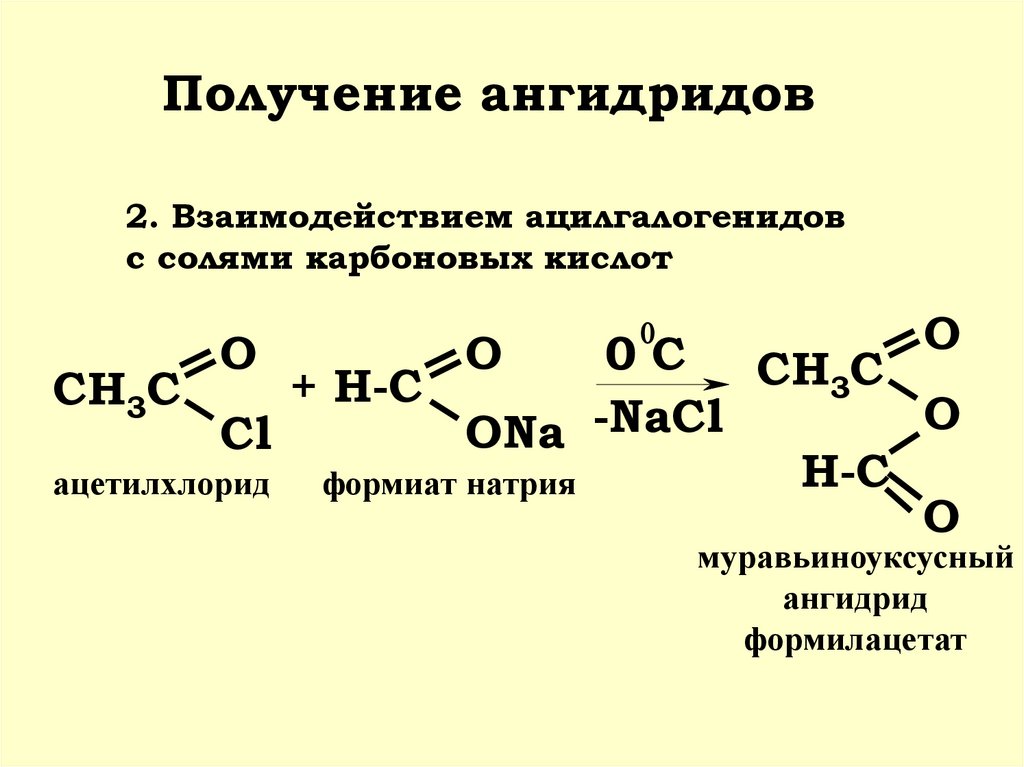
16.
Получение ангидридов2. Взаимодействием ацилгалогенидов
с солями карбоновых кислот
O
O
O
0 C CH C
3
+ H-C
CH3C
O
ONa -NaCl
Cl
H-C
ацетилхлорид
формиат натрия
O
муравьиноуксусный
ангидрид
формилацетат
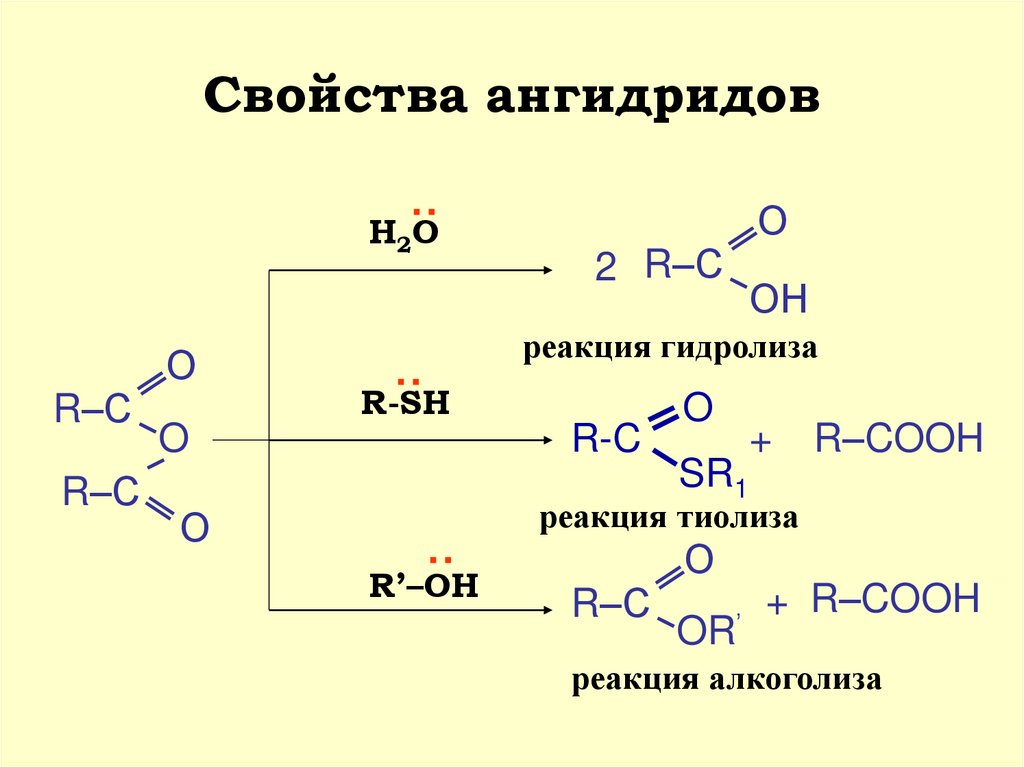
17. Свойства ангидридов
О:
Н2 О
R-SH
R-C
O
O
SR1
+
R–COOH
реакция тиолиза
О
:
R–С
реакция гидролиза
О
R–С
ОН
:
О
2 R–С
R’–OH
R–С
OR’
+ R–COOH
реакция алкоголиза
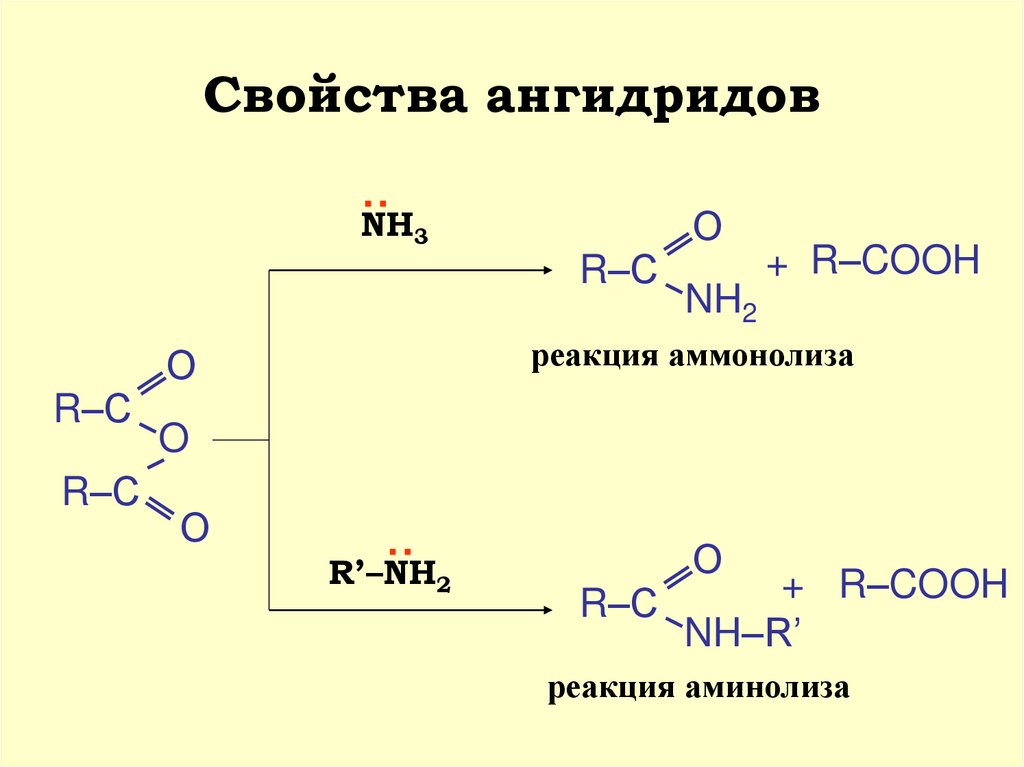
18. Свойства ангидридов
:Свойства ангидридов
NH3
О
R–С
O
О
:
О
R–С
NH2
реакция аммонолиза
О
R–С
+ R–COOH
R’–NH2
R–С
+ R–COOH
NH–R’
реакция аминолиза
19.
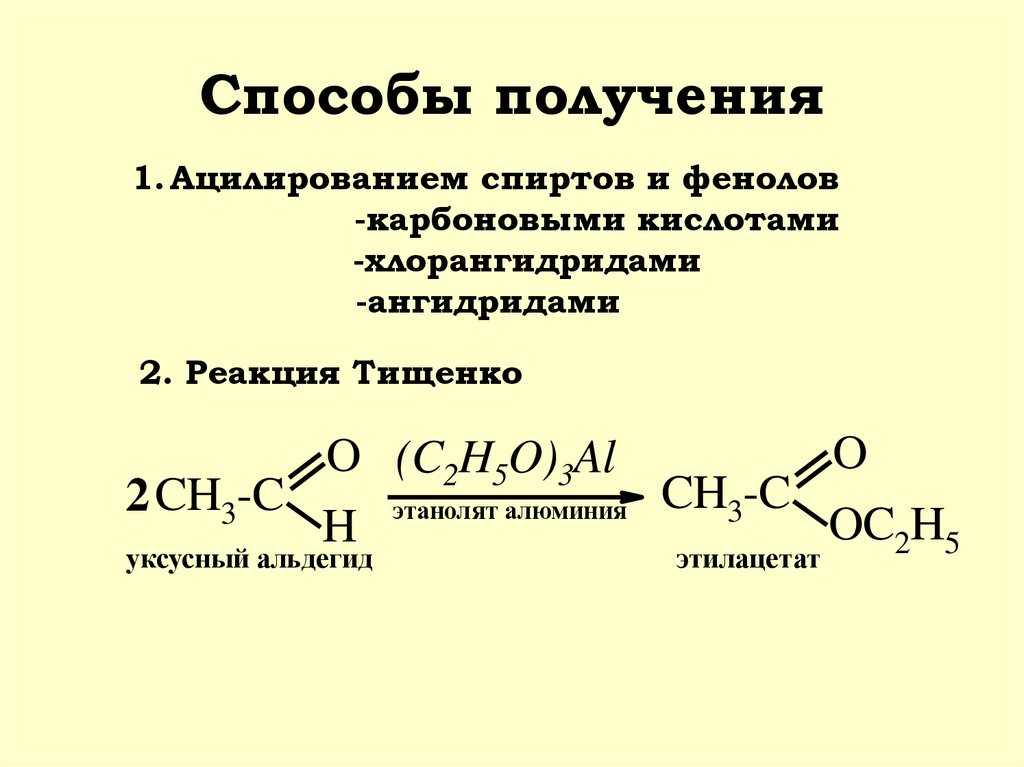
Сложные эфиры20. Способы получения
1. Ацилированием спиртов и фенолов-карбоновыми кислотами
-хлорангидридами
-ангидридами
2. Реакция Тищенко
O
O (C2H5O)3Al
2 CH3-C
этанолят алюминия CH3-C
OC2H5
H
уксусный альдегид
этилацетат
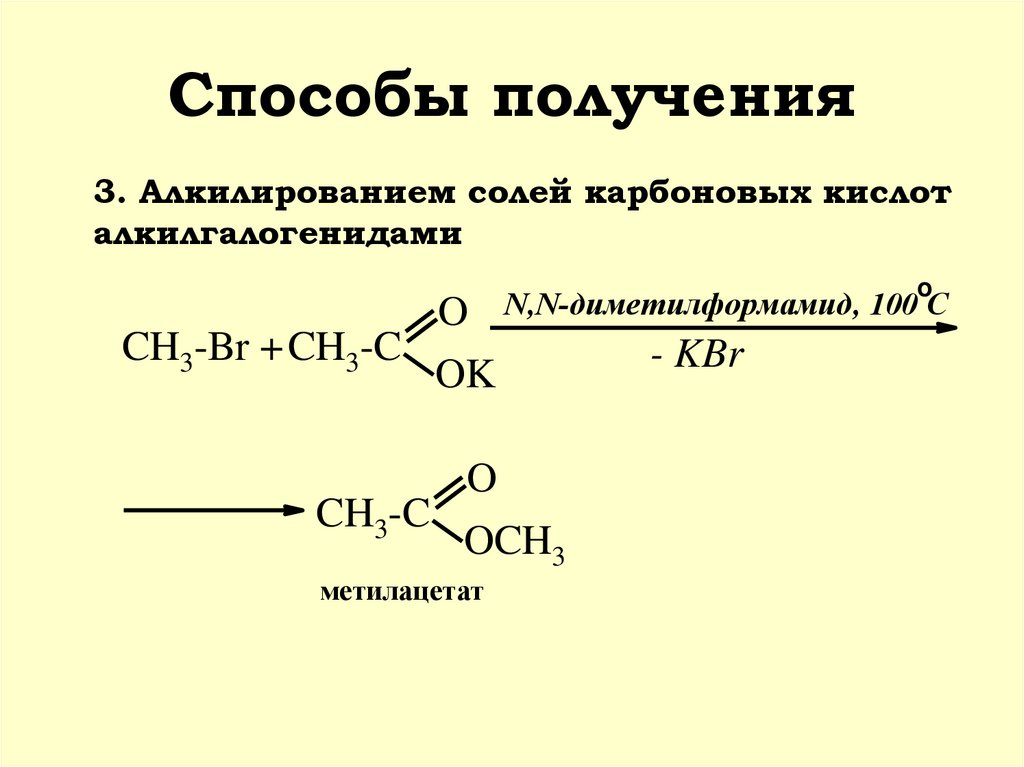
21. Способы получения
3. Алкилированием солей карбоновых кислоталкилгалогенидами
O
CH3-Br + CH3-C
OK
O
CH3-C
OCH3
метилацетат
o
N,N-диметилформамид, 100 С
- KBr
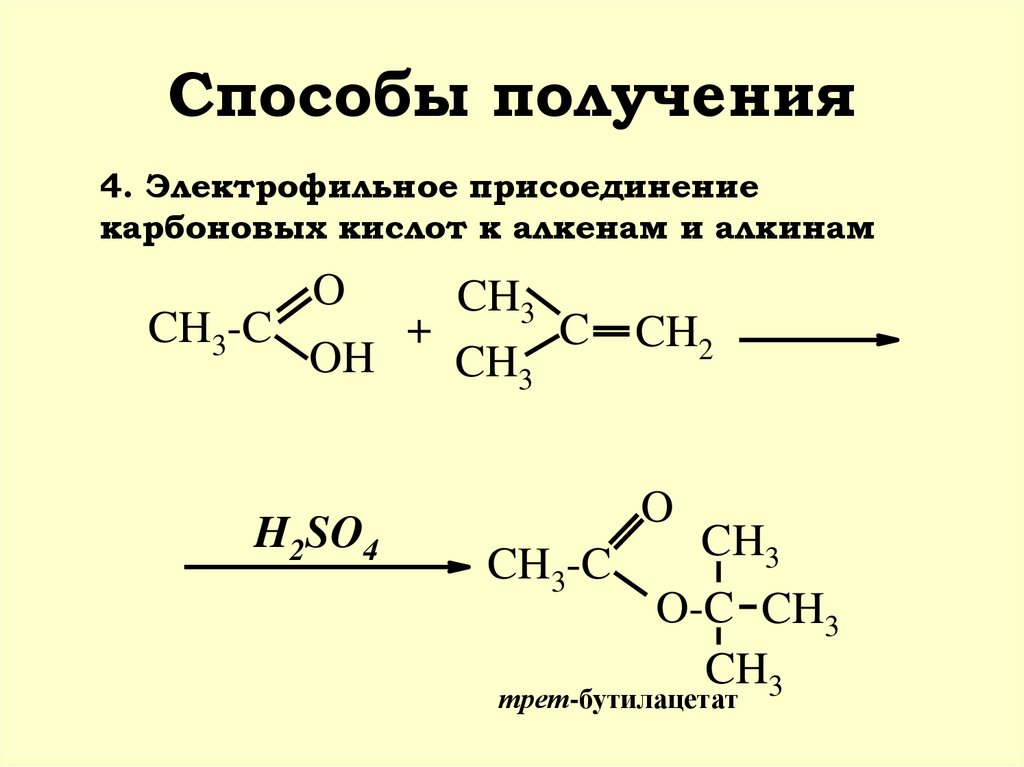
22. Способы получения
4. Электрофильное присоединениекарбоновых кислот к алкенам и алкинам
O
CH3
CH3-C
+
C
OH
CH3
H2SO4
CH2
O
CH3
CH3-C
O-C CH3
CH3
трет-бутилацетат
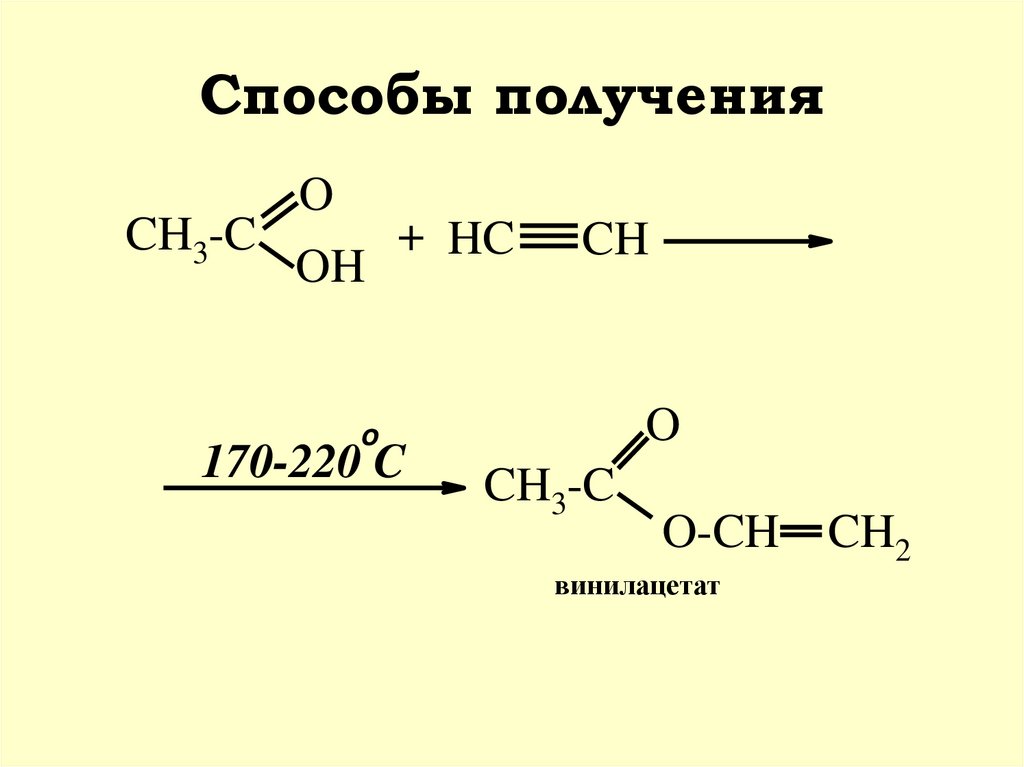
23. Способы получения
OCH3-C
+ HC
OH
CH
O
o
170-220 C
CH3-C
O-CH
винилацетат
CH2
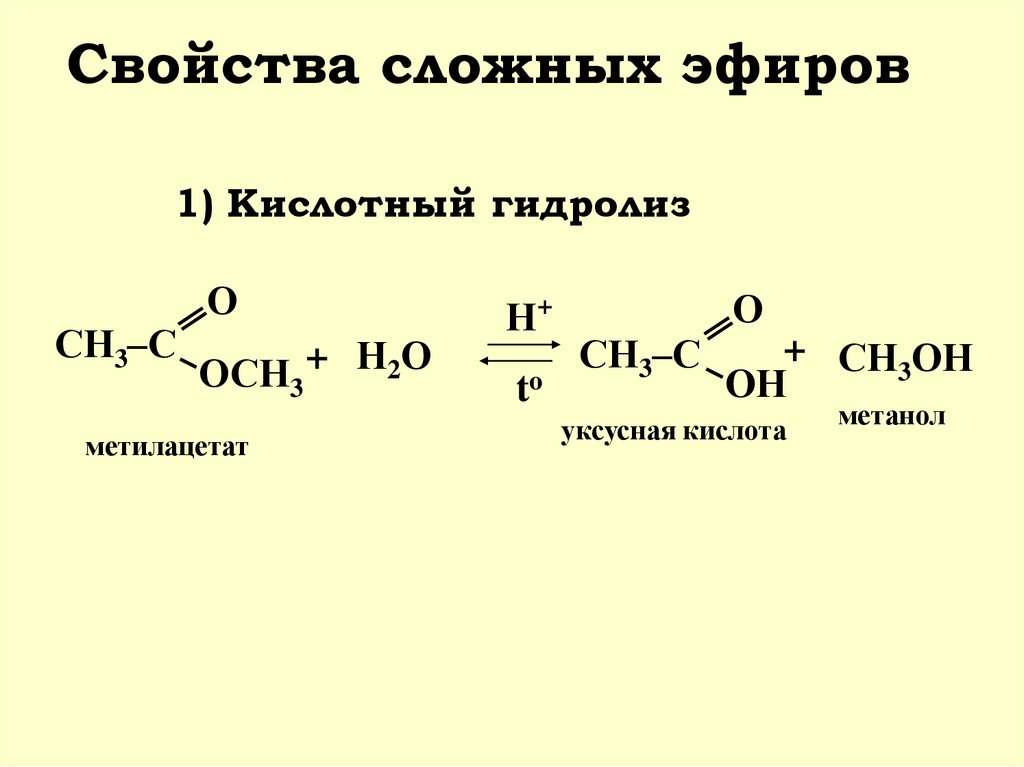
24. Свойства сложных эфиров
1) Кислотный гидролизСН3–С
О
+
Н
О
2
ОСН3
метилацетат
Н+
to
О
СН3–С
+ СН3ОН
OН
уксусная кислота
метанол
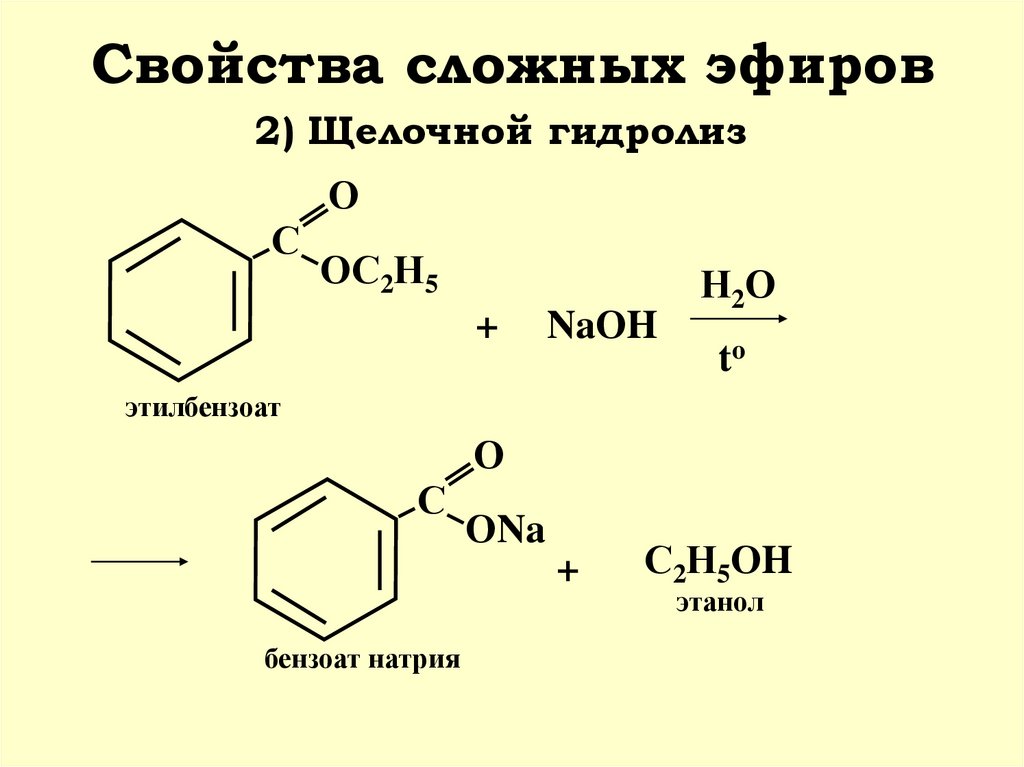
25. Свойства сложных эфиров
2) Щелочной гидролизО
С
ОС2Н5
+
NaОH
Н2О
to
этилбензоат
О
С
ОNa
+
бензоат натрия
С2Н5ОH
этанол
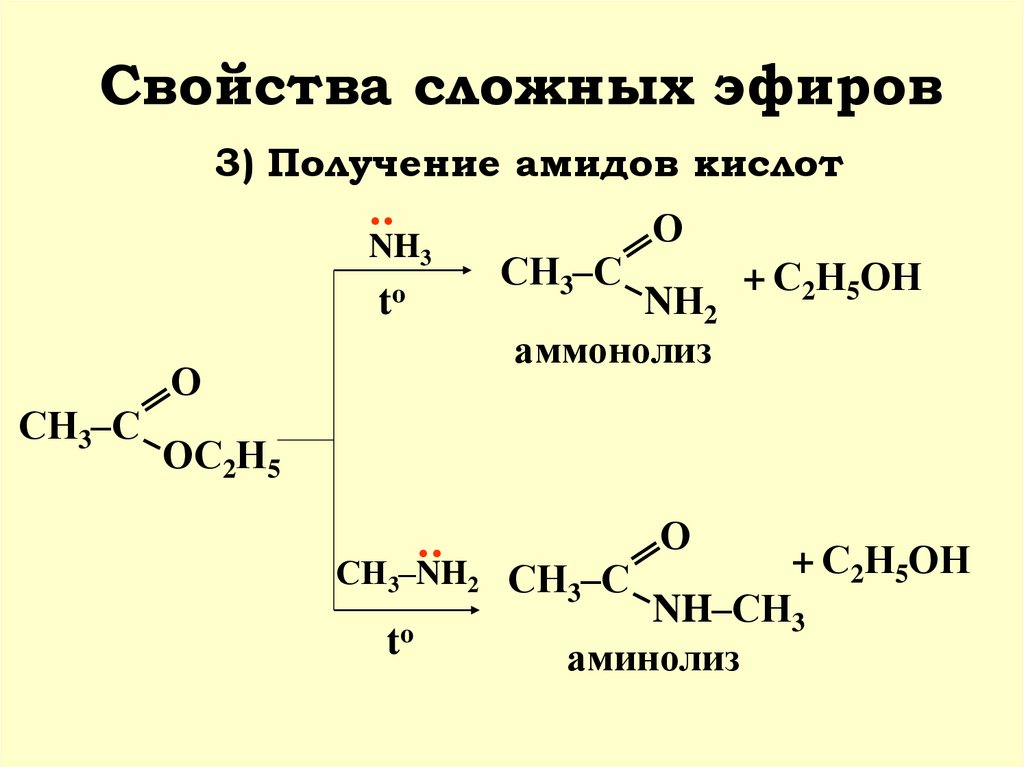
26. Свойства сложных эфиров
СН3–СО
3) Получение амидов кислот
..
О
NH3
СН3–С
+ С2Н5ОН
o
t
NН2
аммонолиз
ОС2Н5
..
+ С2Н5ОН
NH–СН3
аминолиз
СН3–NH2 СН –С
3
to
О
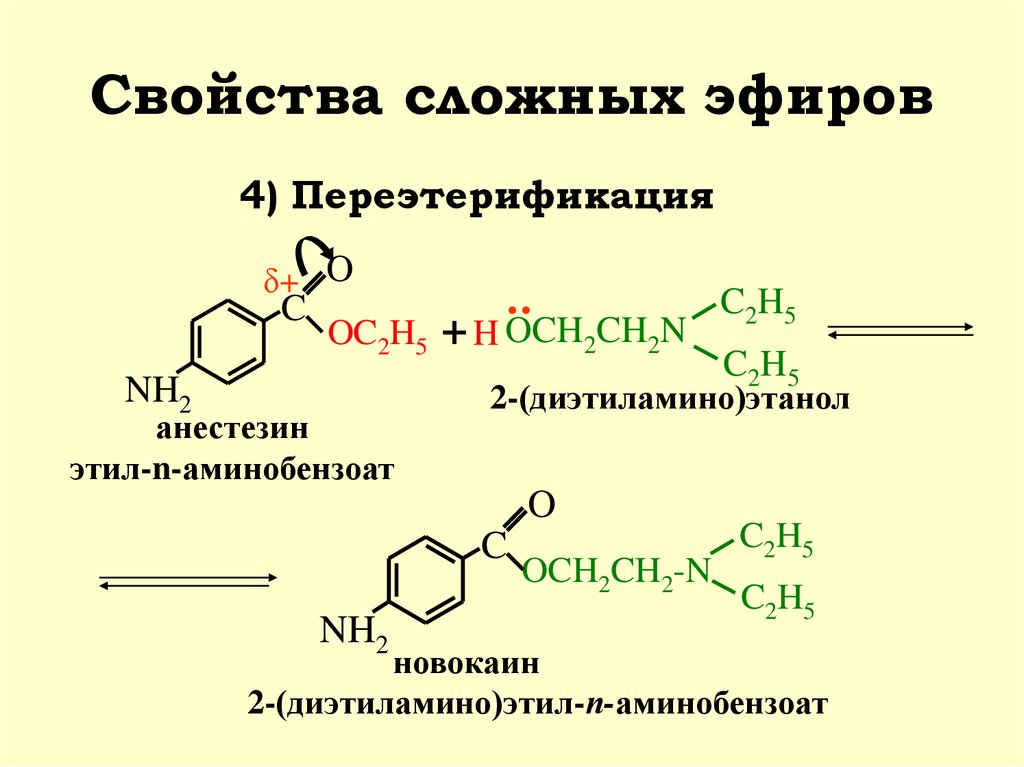
27. Свойства сложных эфиров
4) Переэтерификацияδ+ O
C
OC2H5
NH2
анестезин
этил-n-аминобензоат
..
+ H OCH2CH2N
C 2H 5
2-(диэтиламино)этанол
O
C
NH2
C 2H 5
OCH2CH2-N
C2H5
C2H5
новокаин
2-(диэтиламино)этил-п-аминобензоат
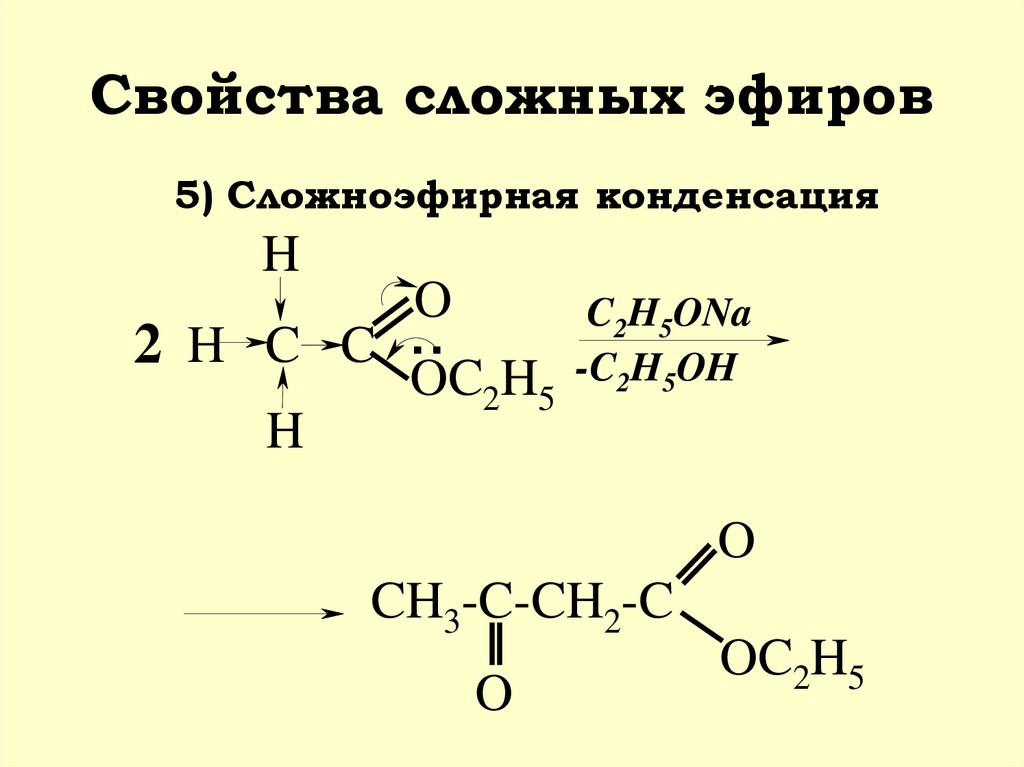
28. Свойства сложных эфиров
5) Сложноэфирная конденсацияH
O
2 H C C ..
OC2H5
H
C2H5ONa
-C2H5OH
O
CH3-C-CH2-C
O
OC2H5
29.
Механизм реакциисложноэфирной конденсации
H
H C-C
δ+
+
H
O
δ+
CH3-C
δ-
С2H5O
O
-CH -C
2
O-C2H5
O
O-C2H5
δ-
O
+
O-C2H5
O-C2H5
O
CH3-C CH2-C
O
O-C2H5
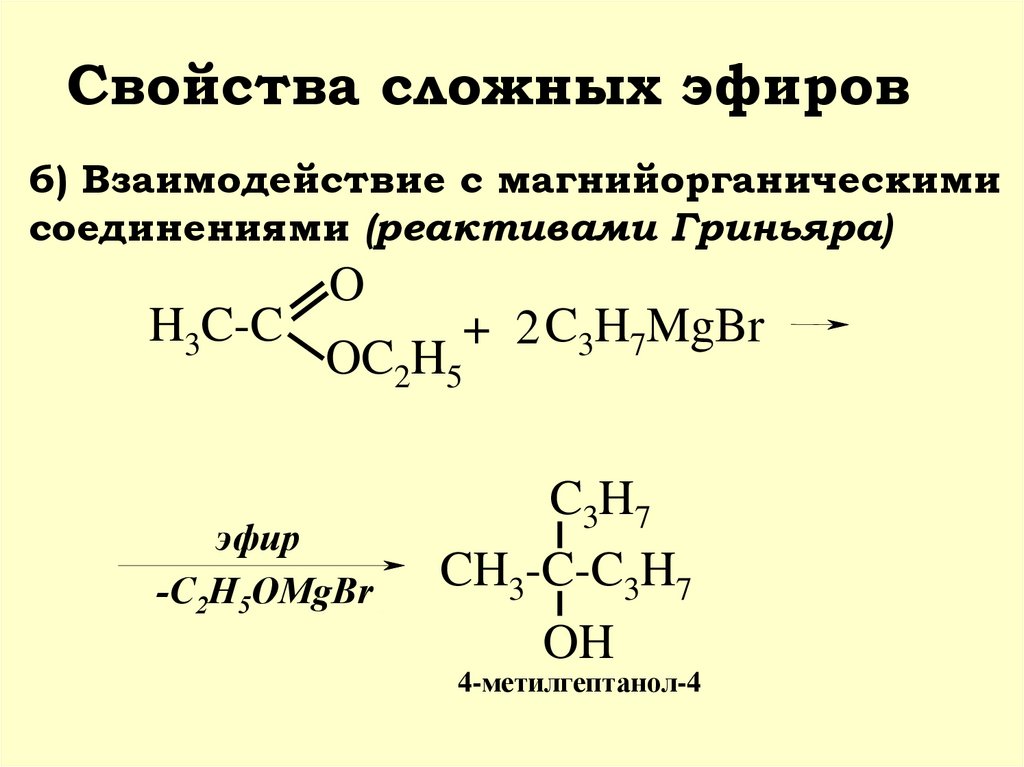
30.
Свойства сложных эфиров6) Взаимодействие с магнийорганическими
соединениями (реактивами Гриньяра)
O
H3C-C
+ 2 C3H7MgBr
OC2H5
эфир
-С2H5OMgBr
C3H7
CH3-C-C3H7
OH
4-метилгептанол-4
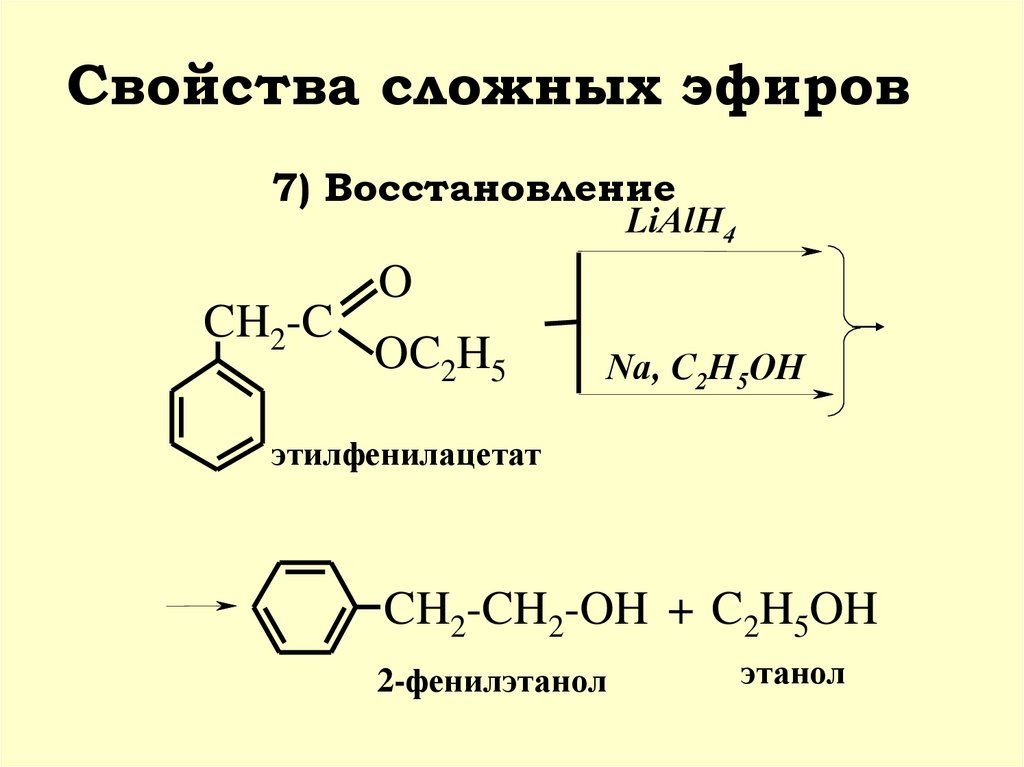
31.
Свойства сложных эфиров7) Восстановление
LiAlH4
O
CH2-C
OC2H5
Na, C2H5OH
этилфенилацетат
CH2-CH2-OH + C2H5OH
2-фенилэтанол
этанол
32.
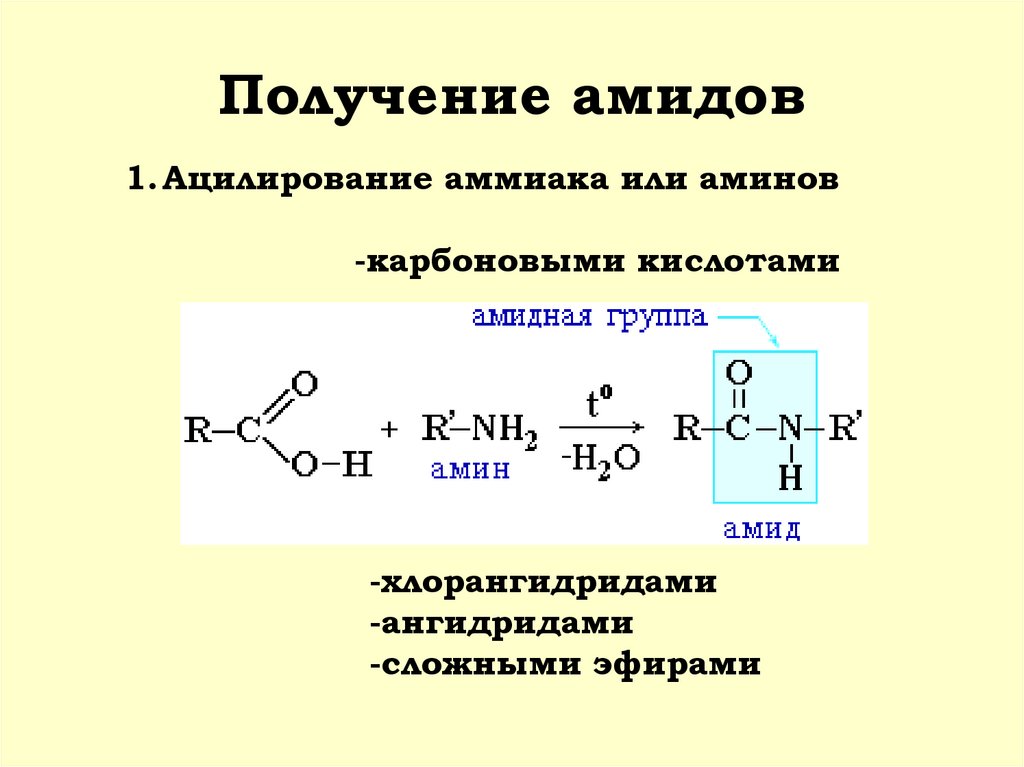
АМИДЫ33. Получение амидов
1. Ацилирование аммиака или аминов-карбоновыми кислотами
-хлорангидридами
-ангидридами
-сложными эфирами
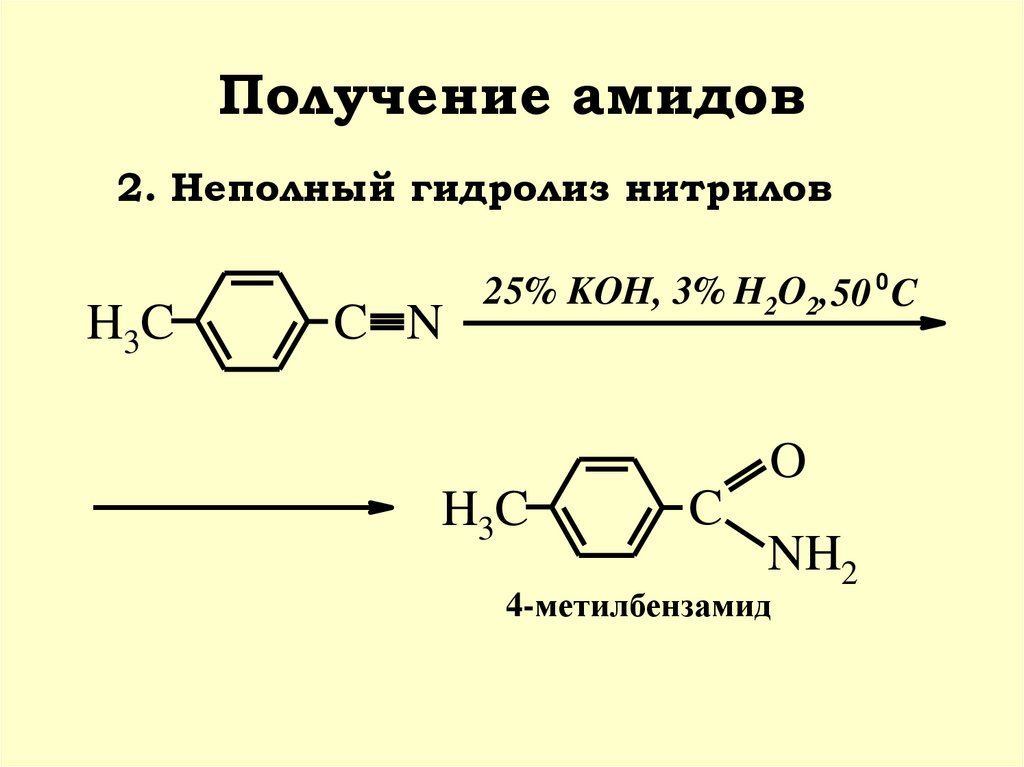
34. Получение амидов
2. Неполный гидролиз нитриловH3C
C N
25% KOH, 3% H2O2, 50 0 C
O
H3C
C
NH2
4-метилбензамид
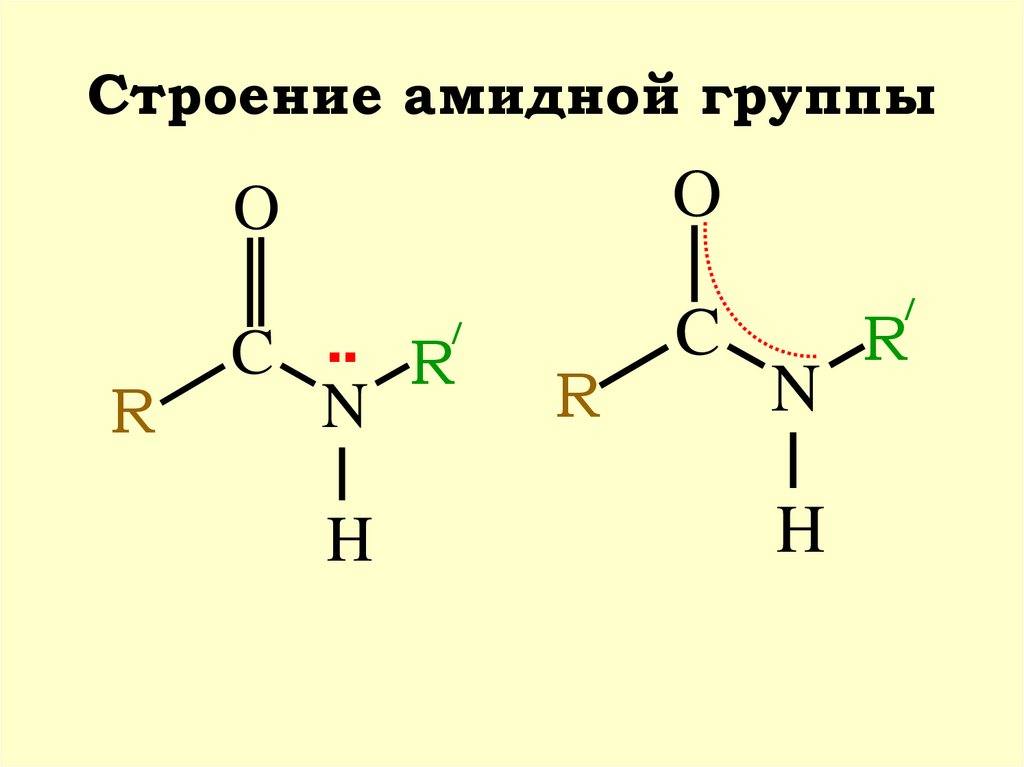
35. Строение амидной группы
OH
C
C .. R
N
O
R
/
R
H
R
C
/
N
H
R
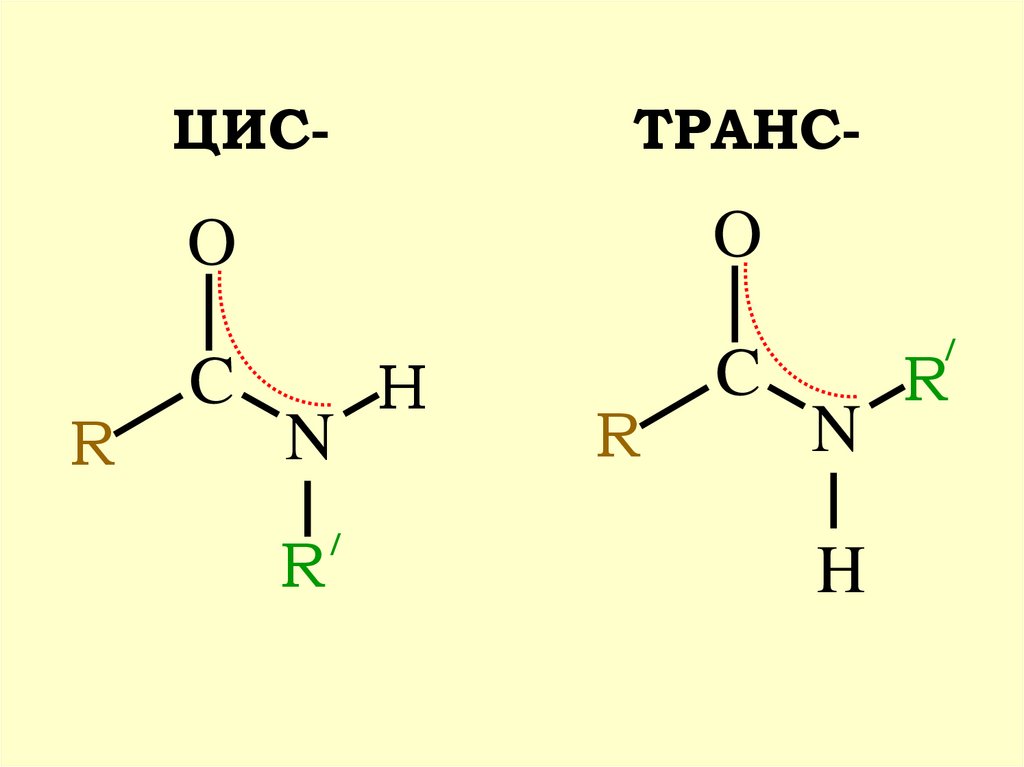
36.
ЦИС-ТРАНС-
O
O
R
C
N
/
R
H
H
R
C
/
N
H
R
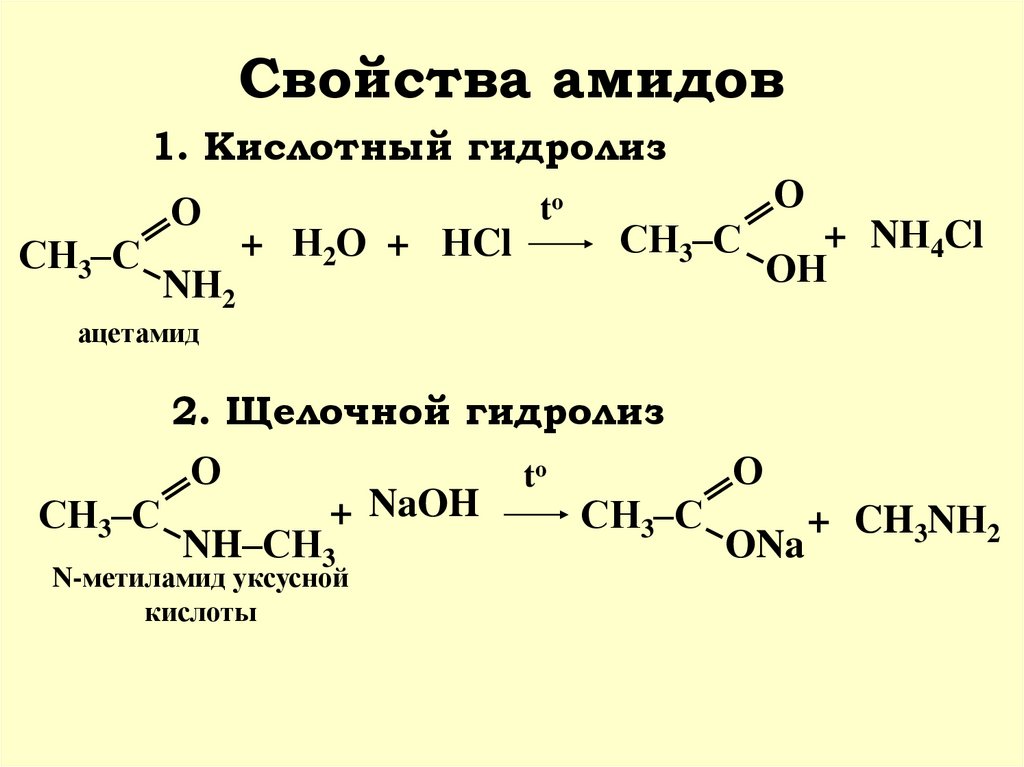
37. Свойства амидов
1. Кислотный гидролизСН3–С
О
NН2
+ Н2О + НCl
to
О
СН3–С
+ NН4Cl
OН
ацетамид
2. Щелочной гидролиз
СН3–С
О
+ NaOH
NH–СН3
N-метиламид уксусной
кислоты
to
СН3–С
О
ONa
+ CH3NН2
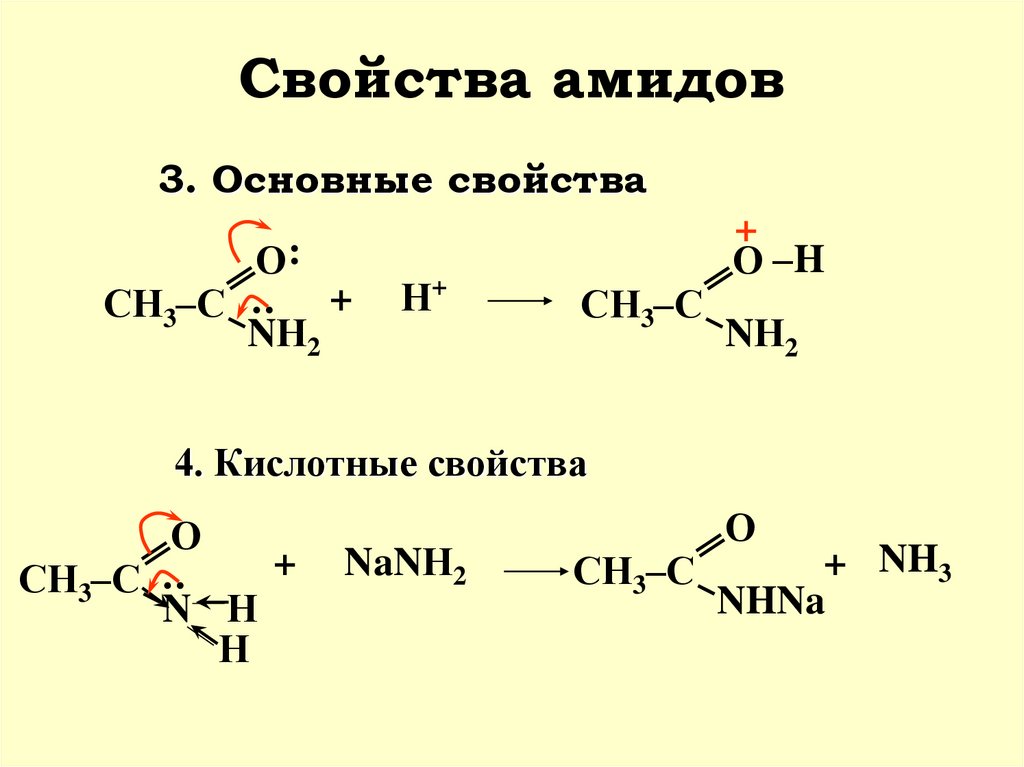
38. Свойства амидов
3. Основные свойства:
СН3–С
О:
NН2
+
Н+
СН3–С
+
О –H
NН2
4. Кислотные свойства
:
СН3–С
О
N Н
Н
+
NaNН2
СН3–С
О
+ NH3
NHNa
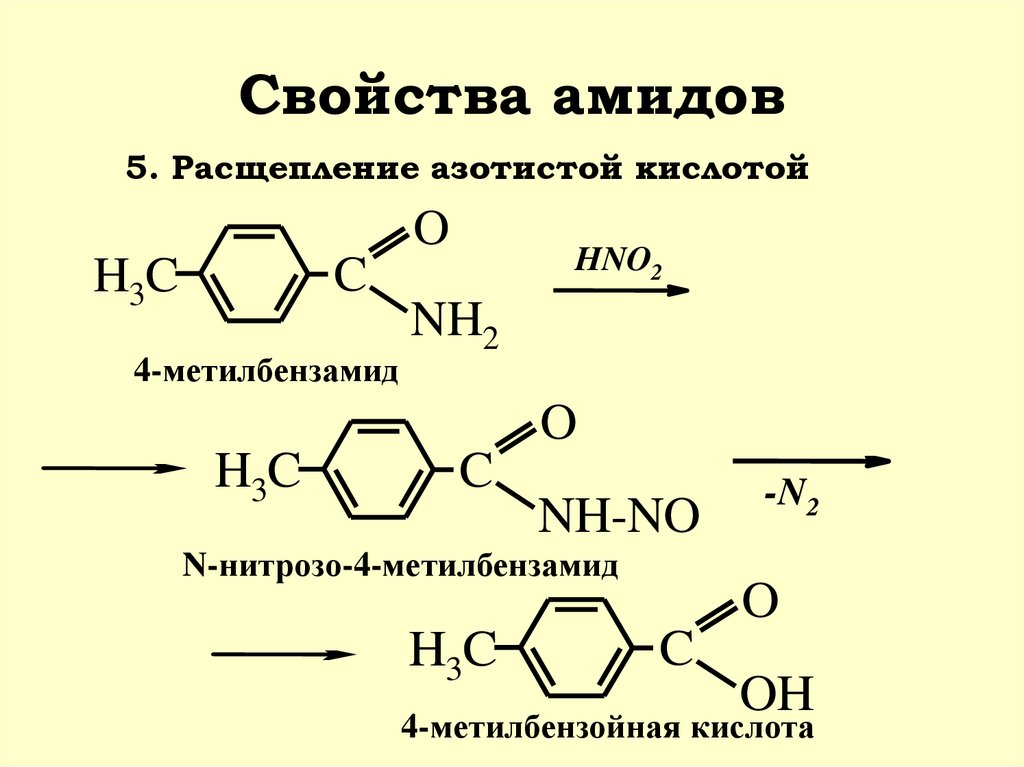
39. Свойства амидов
5. Расщепление азотистой кислотойO
C
H3C
HNO2
NH2
4-метилбензамид
O
H3C
C
NH-NO
N-нитрозо-4-метилбензамид
H3C
-N2
O
C
OH
4-метилбензойная кислота
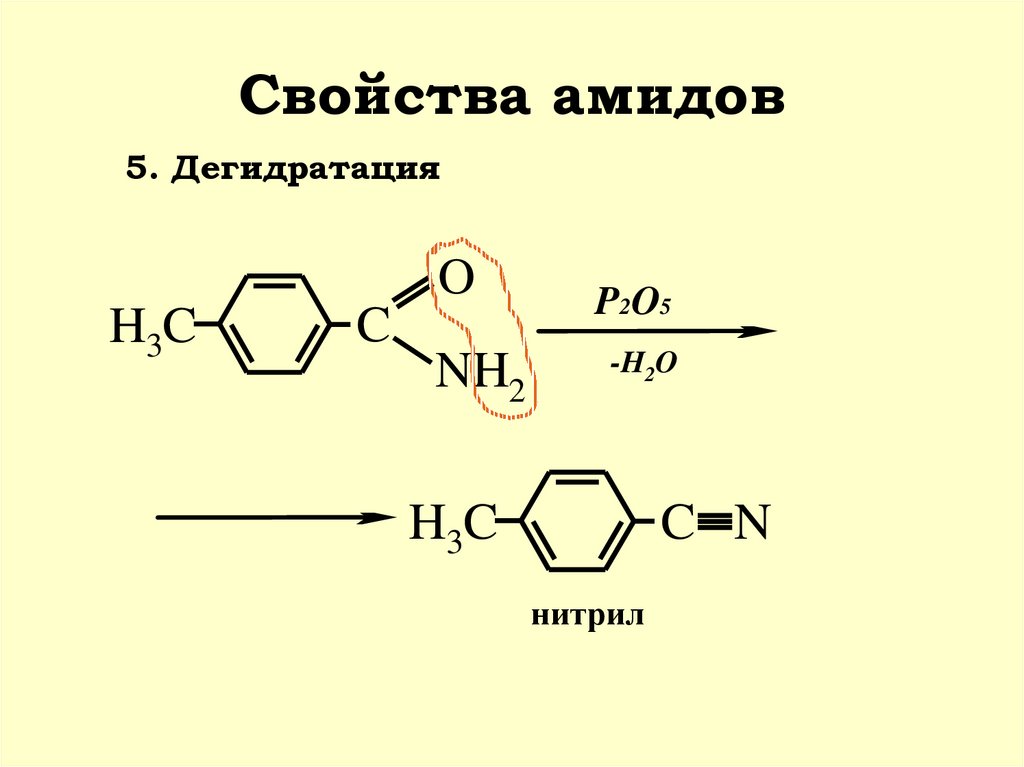
40. Свойства амидов
5. ДегидратацияO
H3C
C
NH2
P2O5
-H2O
C N
H3C
нитрил
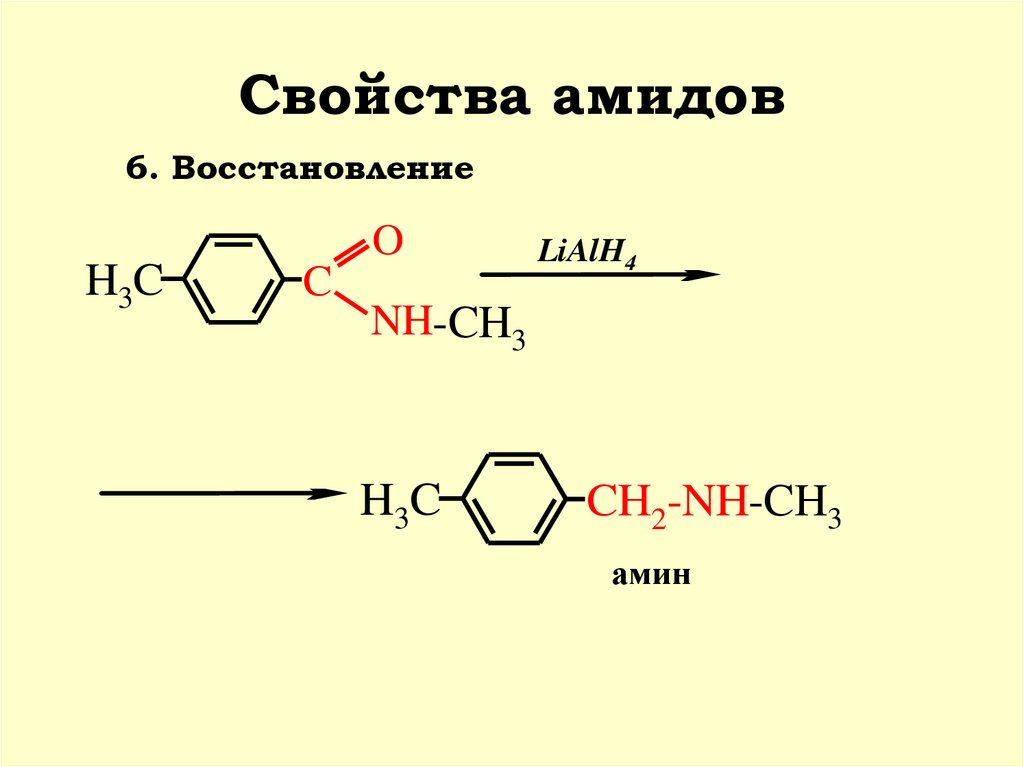
41. Свойства амидов
6. ВосстановлениеH3C
O
C
LiAlH4
NH-CH3
H3C
CH2-NH-CH3
амин
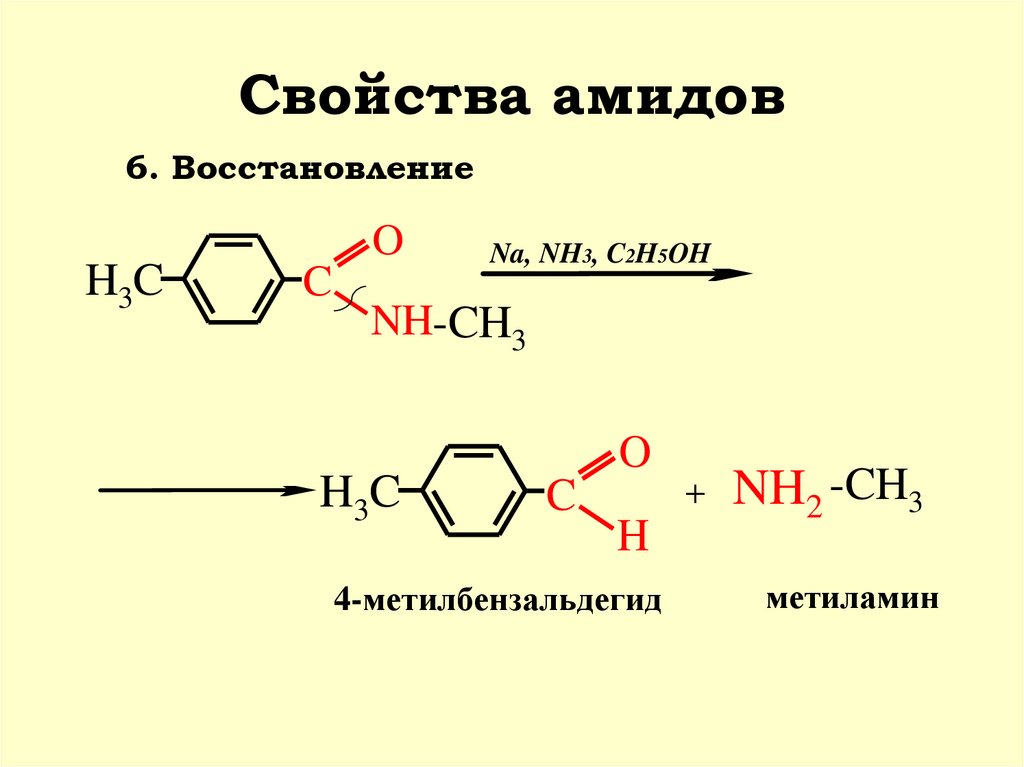
42. Свойства амидов
6. ВосстановлениеH3C
O
C
Na, NH3, C2H5OH
NH-CH3
H3C
O
C
H
4-метилбензальдегид
+
NH2 -CH3
метиламин
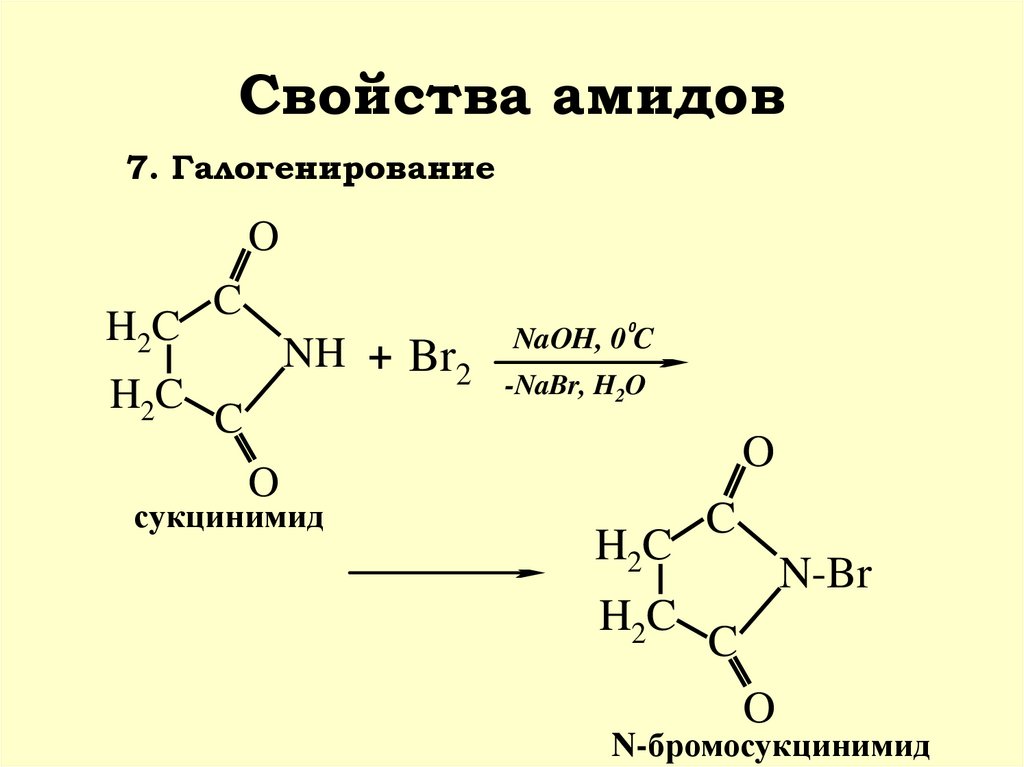
43. Свойства амидов
7. ГалогенированиеO
H2C
H2C
C
0
NH + Br2
C
NaOH, 0 C
-NaBr, H2O
O
O
сукцинимид
H2C
H2C
C
N-Br
C
O
N-бромосукцинимид
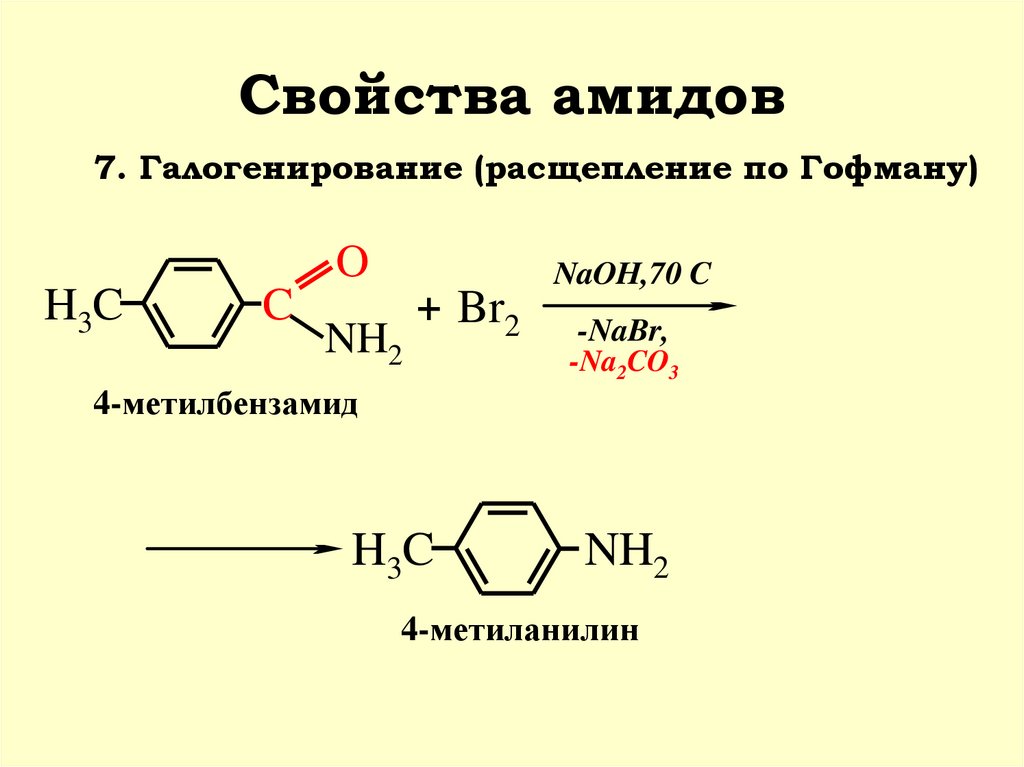
44. Свойства амидов
7. Галогенирование (расщепление по Гофману)O
H3C
C
NH2
+ Br2
NaOH,70 C
-NaBr,
-Na2CO3
4-метилбензамид
H3C
NH2
4-метиланилин
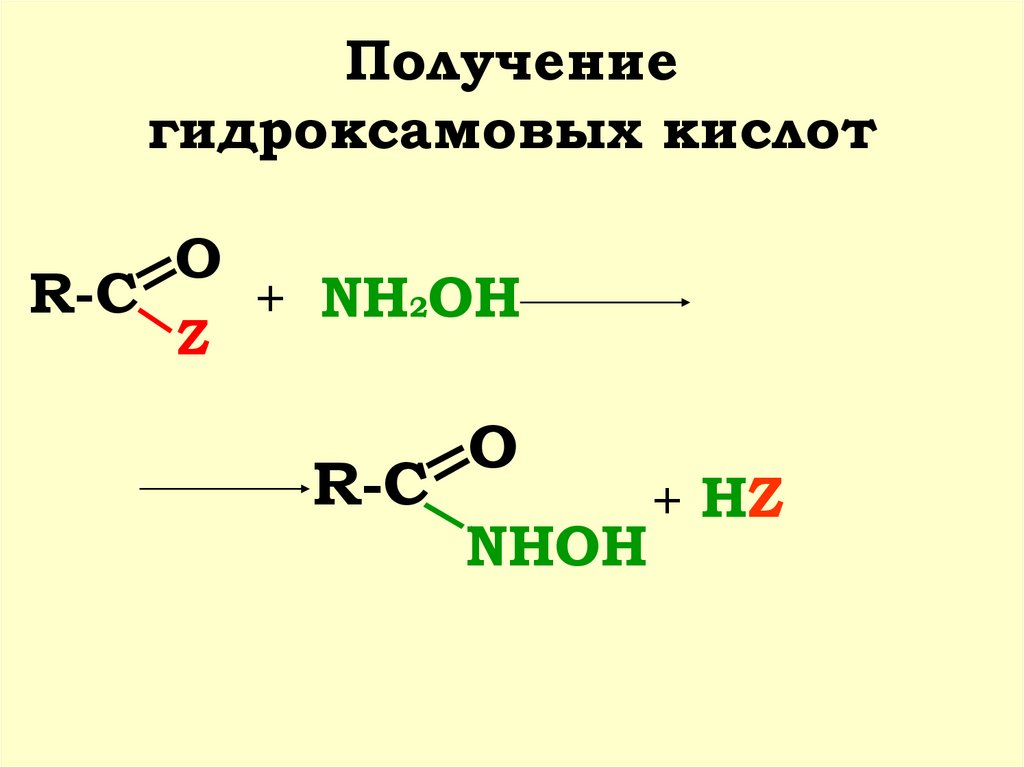
45. Получение гидроксамовых кислот
R-CO
Z
+ NH2OH
R-C
O
Z
NHOH
+ HZ
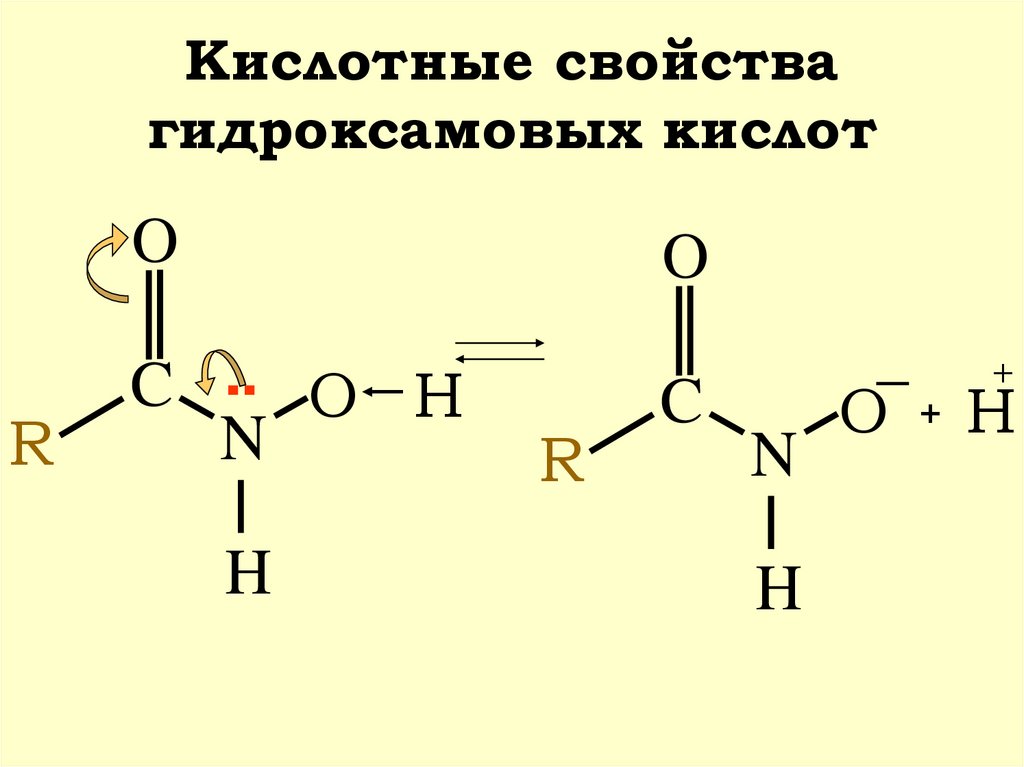
46. Кислотные свойства гидроксамовых кислот
OR
H
R
C H
C .. O
N
R
H
O
H
C
C .. O
N
H
+
R
+
H
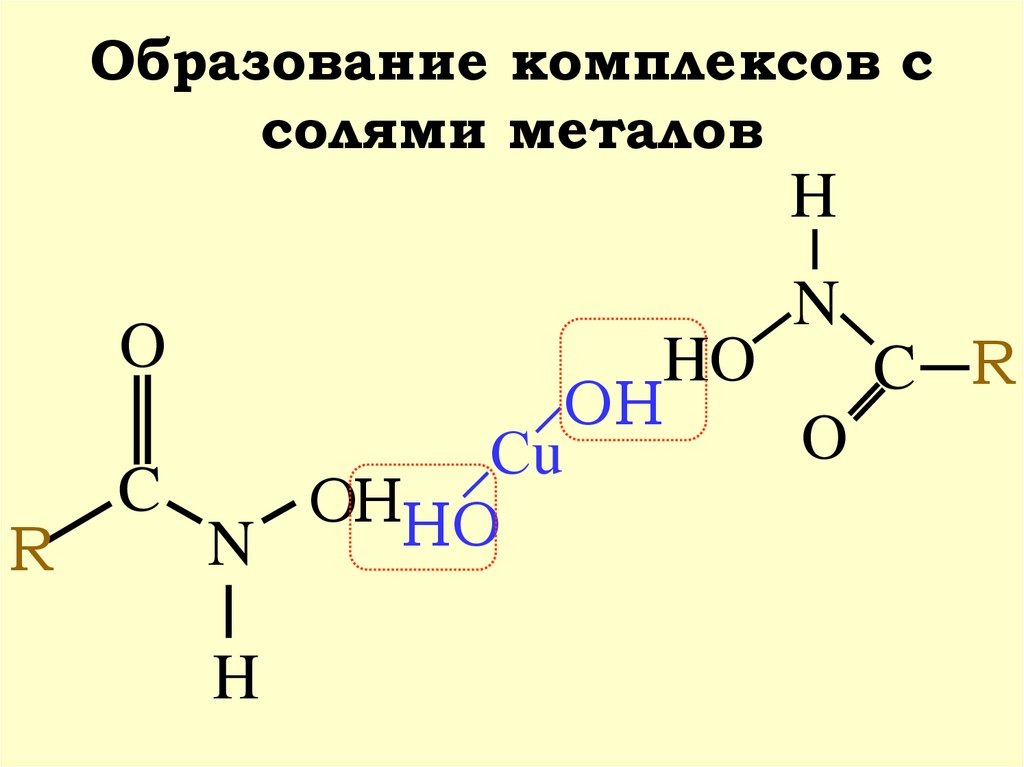
47. Образование комплексов с солями металов
HO
N
HO
C R
R OH
O
Сu
C .. C
OHHO
N
R
H
H
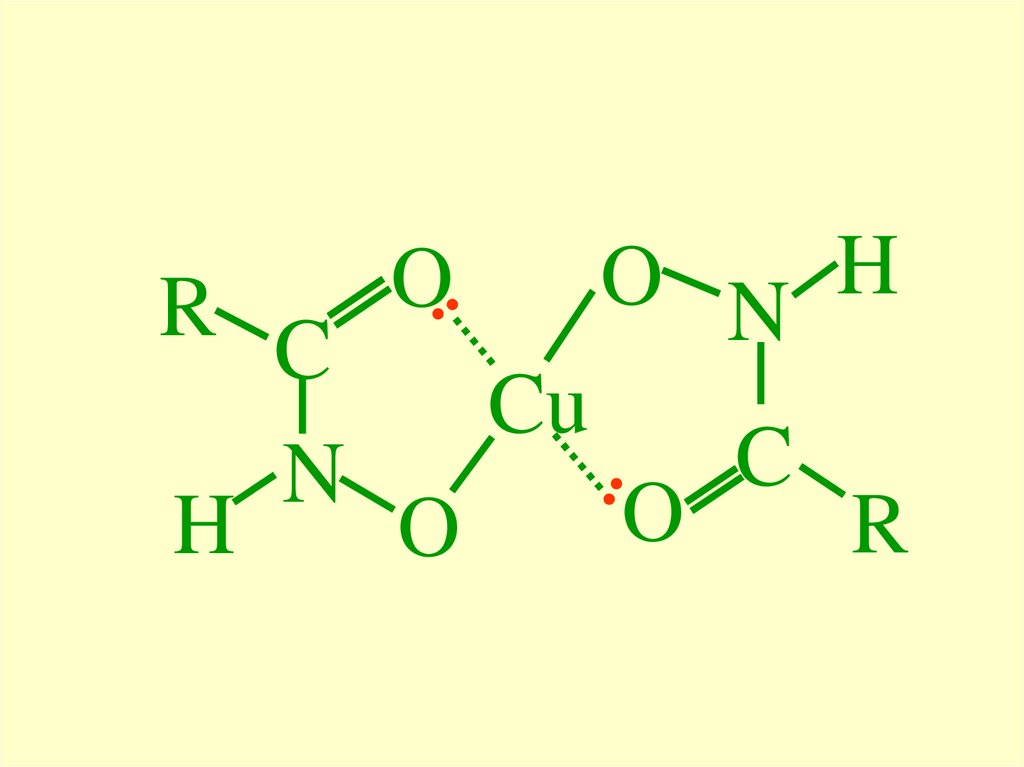
48.
OO N H
R C
Cu
C
N
O
R
H
O








 chemistry
chemistry








