Similar presentations:
Фенилхромановые соединения. Флавоноиды
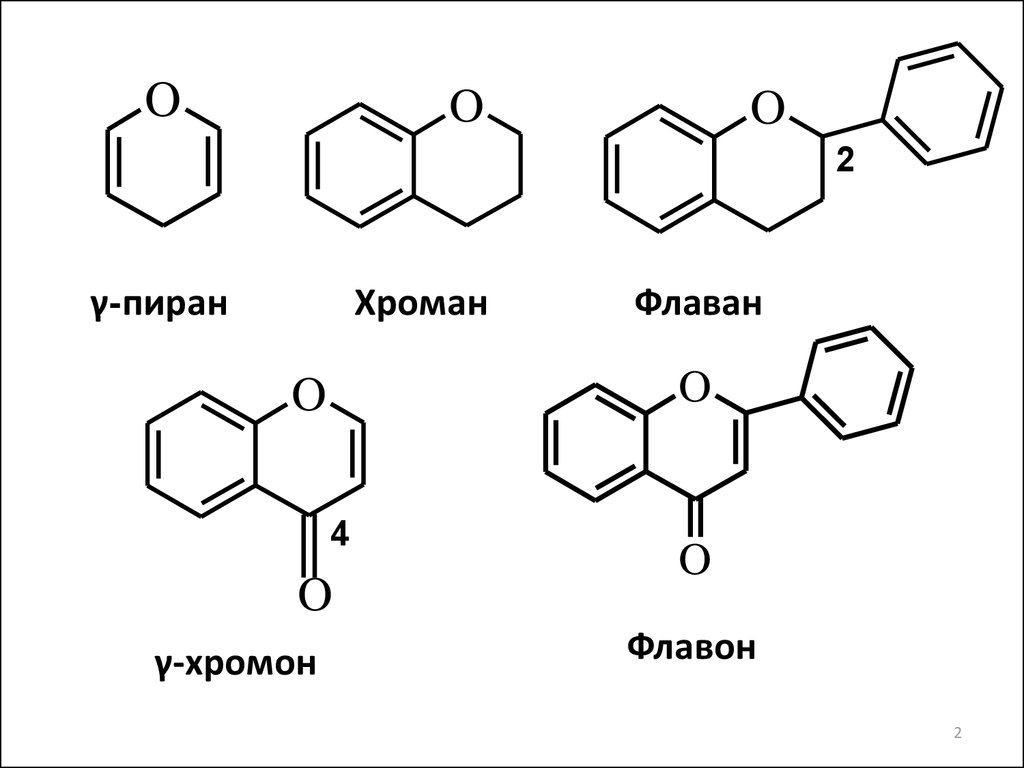
1. ФЕНИЛХРОМАНОВЫЕ СОЕДИНЕНИЯ
Лекция № 2ФЕНИЛХРОМАНОВЫЕ
СОЕДИНЕНИЯ
ФЛАВОНОИДЫ
1
2.
OO
O
2
γ-пиран
Хроман
O
O
4
O
γ-хромон
Флаван
O
Флавон
2
3. витамин Р от permeabilitus (лат.) – проникать
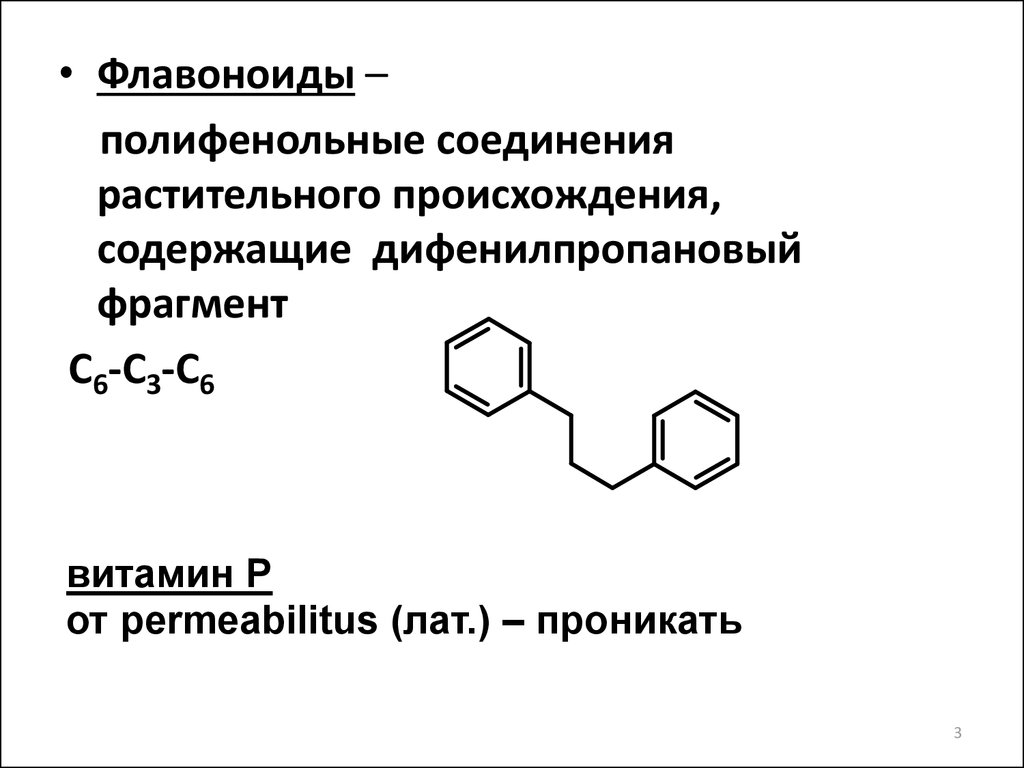
• Флавоноиды –полифенольные соединения
растительного происхождения,
содержащие дифенилпропановый
фрагмент
С6-С3-С6
витамин Р
от permeabilitus (лат.) – проникать
3
4.
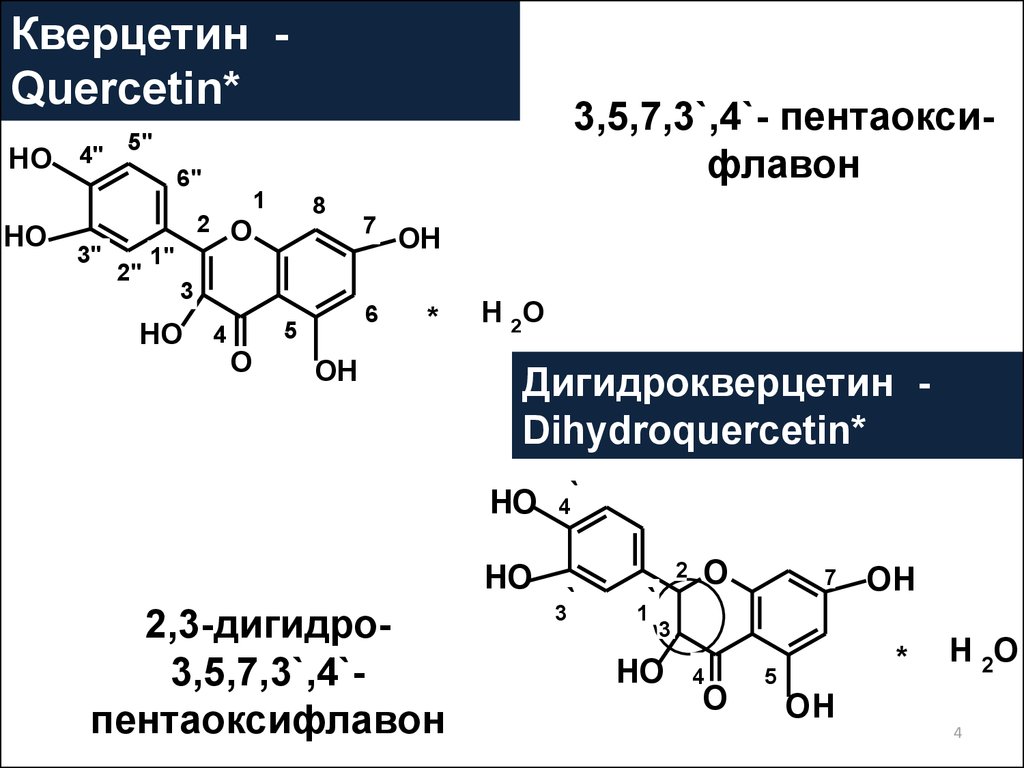
Кверцетин Quercetin*5"
HO 4"
HO
3"
6"
1
8
2 O
2"
3,5,7,3`,4`- пентаоксифлавон
7
OH
6
*
1"
3
HO
5
4
O
OH
H 2O
Дигидрокверцетин Dihydroquercetin*
HO
HO
2,3-дигидро3,5,7,3`,4`пентаоксифлавон
4`
2
3`
1`
3
HO
O
4
O
7
OH
*
5
H 2O
OH
4
5.
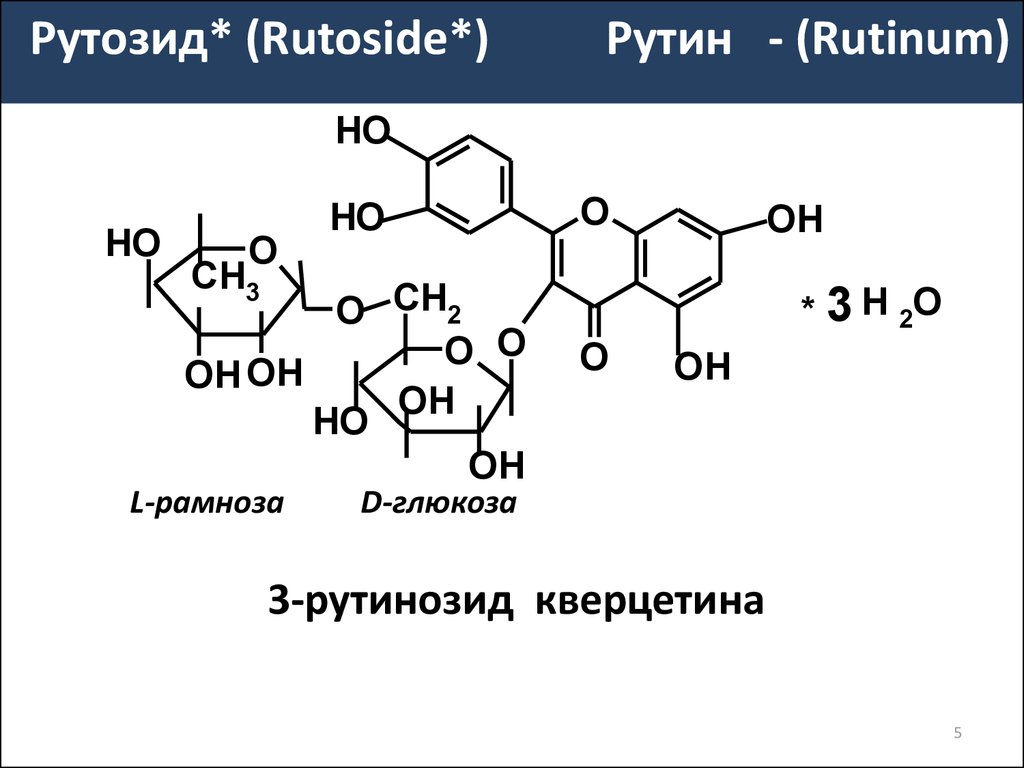
Рутозид* (Rutoside*)Рутин - (Rutinum)
HO
HO
O
HO
O
OH
CH3
O CH2
O O
OH OH
OH
HO
OH
L-рамноза
* 3 H 2O
O
OH
D-глюкоза
3-рутинозид кверцетина
5
6.
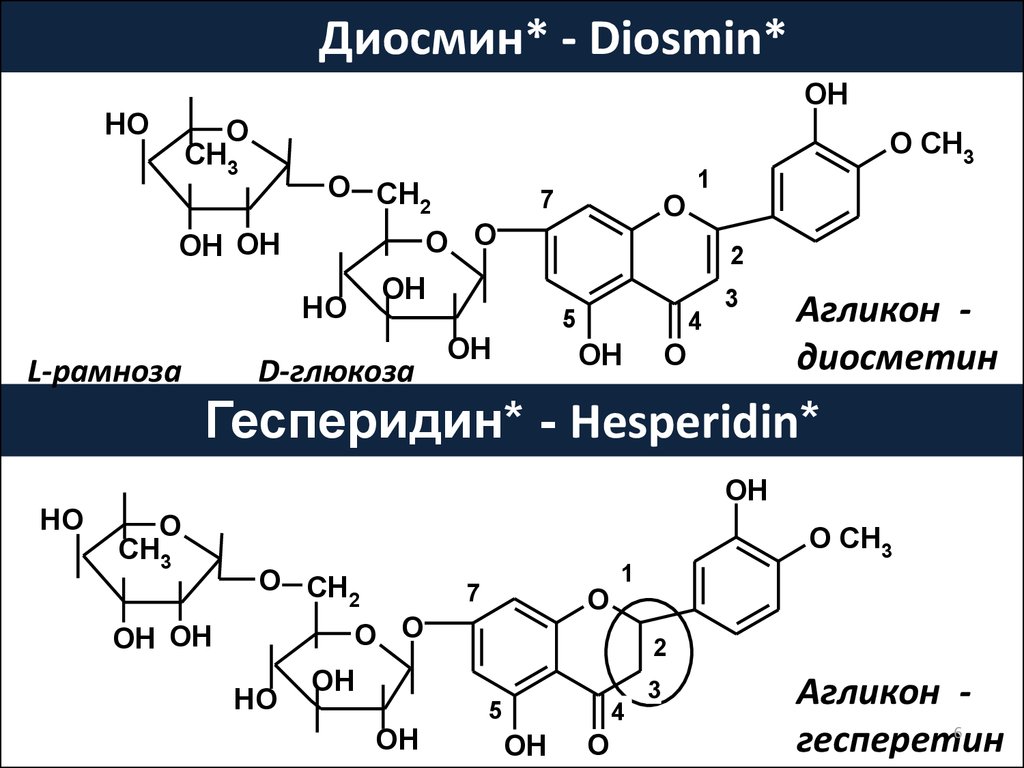
Диосмин* - Diosmin*OH
HO
O
CH3
O CH3
O CH
2
7
O
O O
OH OH
2
OH
HO
L-рамноза
1
5
D-глюкоза
OH
4
3
O
OH
Агликон диосметин
Гесперидин* - Hesperidin*
OH
HO
O
CH3
O CH3
O CH
2
1
7
O
O O
OH OH
HO
2
OH
5
OH
4
OH
O
3
Агликон 6
гесперетин
7.
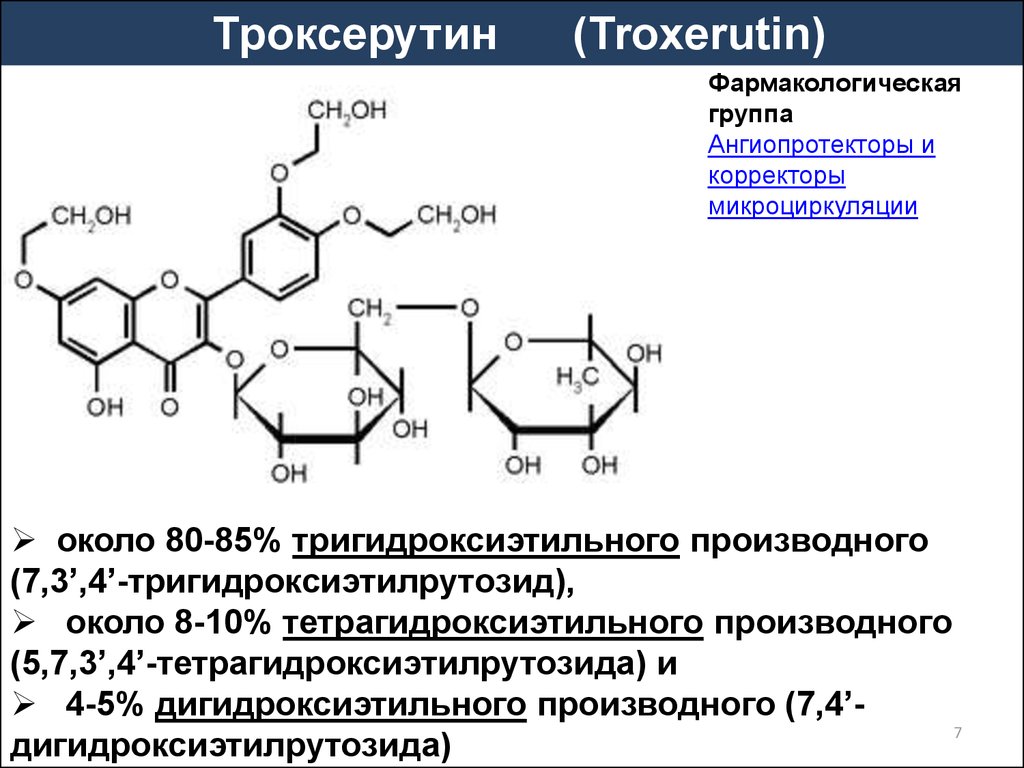
Троксерутин(Troxerutin)
Фармакологическая
группа
Ангиопротекторы и
корректоры
микроциркуляции
около 80-85% тригидроксиэтильного производного
(7,3’,4’-тригидроксиэтилрутозид),
около 8-10% тетрагидроксиэтильного производного
(5,7,3’,4’-тетрагидроксиэтилрутозида) и
4-5% дигидроксиэтильного производного (7,4’7
дигидроксиэтилрутозида)
8.
ПОЛУЧЕНИЕКверцетин получают из коры Quercus tinctoria
экстрагируют водой (гликозид кверцитрон)
гидролизуют кипячением с минеральными
кислотами (кверцетин и рамноза)
перекристаллизовывают
Рутин впервые выделен из руты пахучей (Ruta
graveolens L.) Вейссом в 1842 г.
Получают рутин из зеленой массы гречихи (1,56%):
извлекают водой
осаждают белки
перекристаллизовывают рутин
8
9.
Троксерутин получают при нагревании рутина сизбытком этиленоксида в воде в присутствии
основания, затем проводят кристаллизацию из
спирта.
Дигидрокверцетин получают из древесины
лиственницы сибирской (Larix sibirica) и л.
Гмелина (Larix gmelini) или л. даурской (L. daurica)
сем. Сосновые (Pinaceae)
Диосмин и гесперидин - из незрелых плодов сем.
Rutaceae aurantieae вида Citrus Sinesis
9
10.
Физические свойстваМелкокристаллические порошки желтого цвета,
без запаха.
Растворимость:
- в воде и хлороформе:
кверцетин, рутин, диосмин – пр. нерастворимы
дигидрокверцетин - мало растворим
- в этаноле:
дигидроквецетин – растворим
кверцетин, рутин – мало растворимы
Диосмин, троксерутин – пр. нерастворимы
- в растворах щелочей:
все ЛС растворимы (полифенолы!!!)
диосмин растворим в ДМСО
троксерутин растворим в воде, глицерине,
пропиленгликоле
10
11.
Подлинность1. Т пл. Рутин
183-194оС (с разл.)
Кверцетин 313-316оС (с разл.)
Дигидрокверцетин 220-222оС
2. ИК-спектр
3300-3100 см -1 - фенольные гидроксилы
1720-1680 см -1 - карбонильная группа
1600-1500 см -1 - ароматическая система
11
12.
3. УФ-спектр ( в этаноле)Рутин λmax 259±2 нм и 362,5±1 нм
(А1%1см = 300-330)
Кверцетин λmax 255±2 нм и 375±3 нм
Дигидрокверцетин λmax 290 нм (А1%1см = 630±60);
λmin 247 нм; плечо при 325 нм
Диосмин (в водном растворе натрия карбоната) λmax 267±2 нм и 371±2 нм
Троксерутин λmax 349 нм (А1%1см = 250);
4. ПМР-спектр (дигидрокверцетин)
5. ВЭЖХ - по времени удерживания
(дигидрокверцетин, диосмин)
12
13.
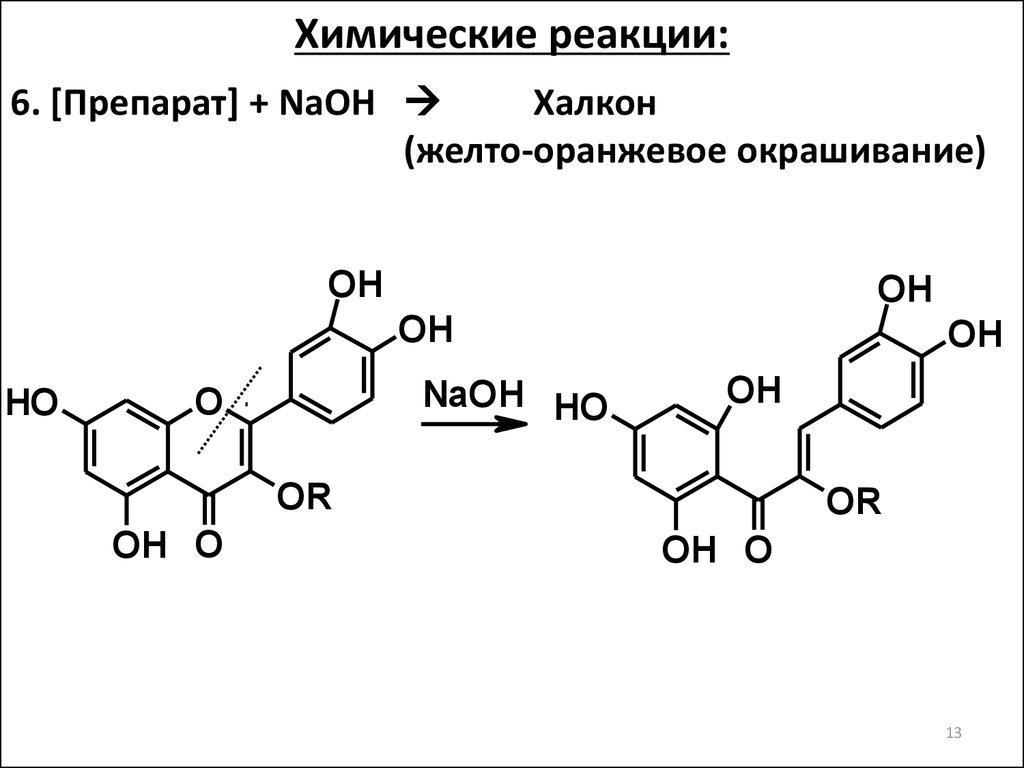
Химические реакции:6. [Препарат] + NaOH
Халкон
(желто-оранжевое окрашивание)
OH
OH
OH
HO
NaOH HO
O
OH
OH
OR
OH O
OR
OH O
13
14.
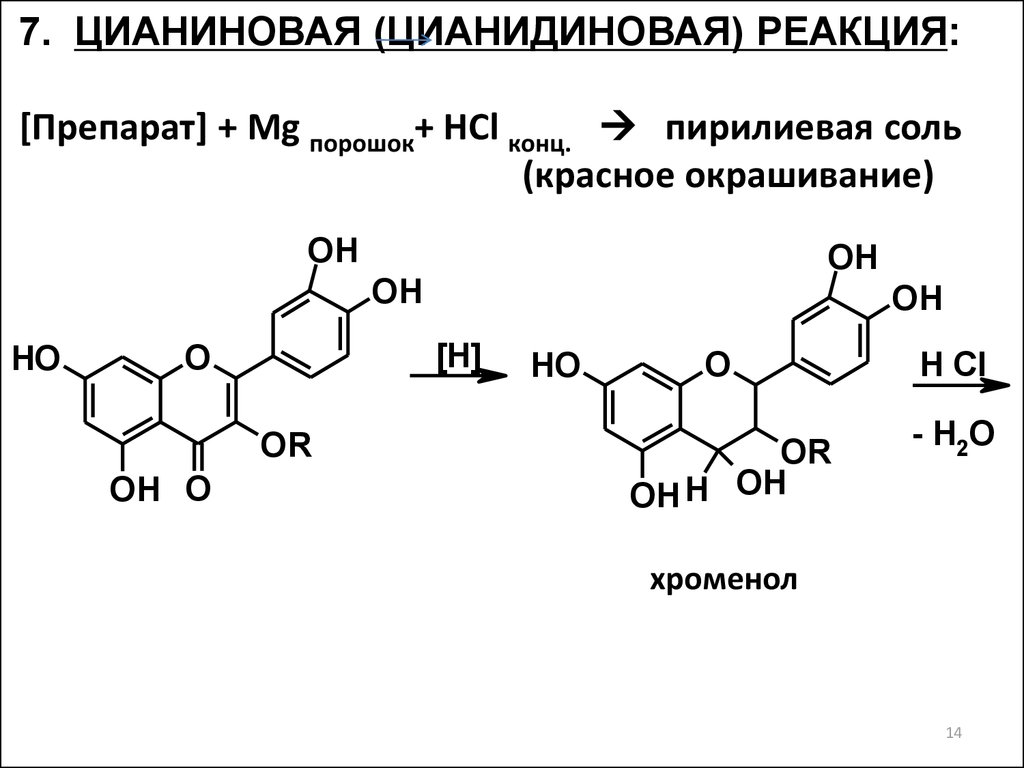
7. ЦИАНИНОВАЯ (ЦИАНИДИНОВАЯ) РЕАКЦИЯ:[Препарат] + Mg порошок+ HCl конц. пирилиевая соль
(красное окрашивание)
OH
OH
OH
HO
[H]
O
OR
OH O
OH
HO
O
OR
OH H OH
H Cl
- H2O
хроменол
14
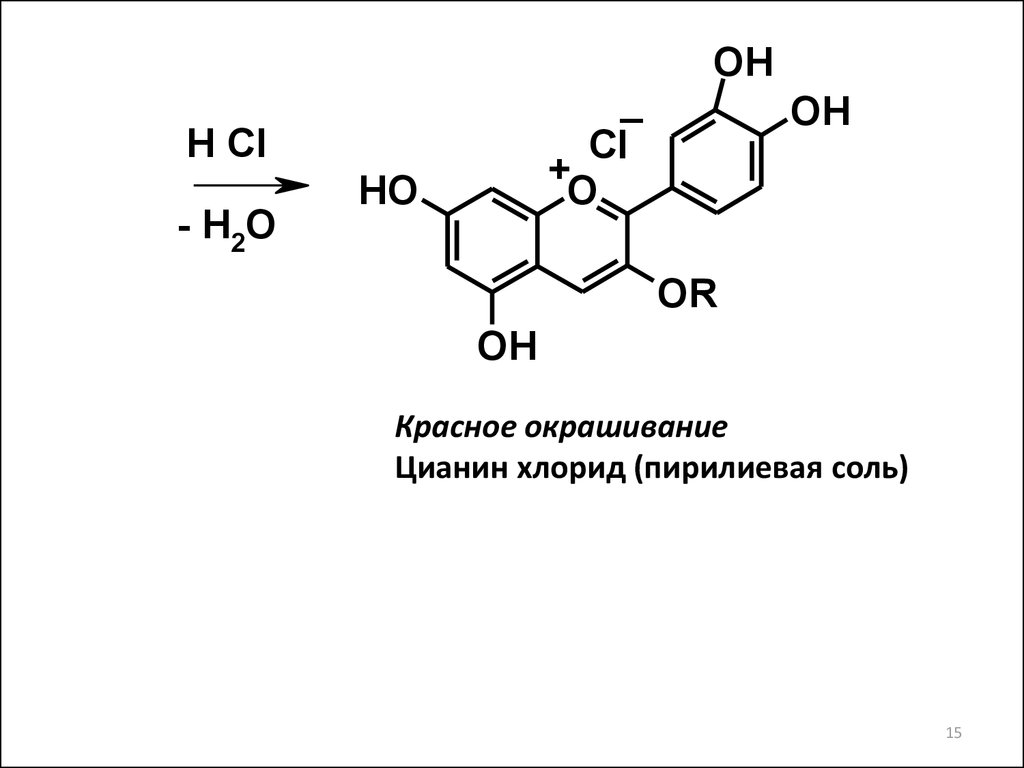
15.
OH_
Cl
+
O
H Cl
- H2O
HO
OH
OR
OH
Красное окрашивание
Цианин хлорид (пирилиевая соль)
15
16.
8. На фенольные гидроксилы:а). с FeCl3 темно-зеленое окр.
NaOH
красно-коричневое
окрашивание
б). с солями свинца оранжевый осадок
в). с солями диазония азокраситель
рутин – красно-бурого цвета;
кверцетин – красно-оранжевого цвета
г). с реактивом Марки красно-оранжевое окрашивание
16
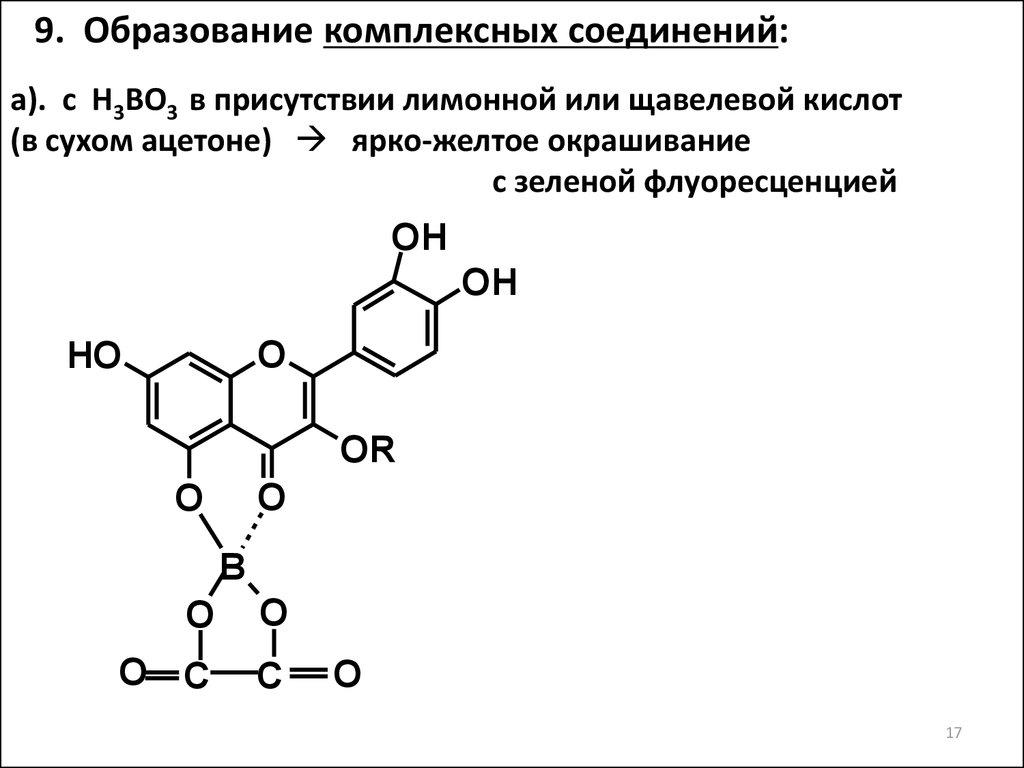
17.
9. Образование комплексных соединений:а). с Н3ВО3 в присутствии лимонной или щавелевой кислот
(в сухом ацетоне) ярко-желтое окрашивание
с зеленой флуоресценцией
OH
OH
O
HO
OR
O
O
B
O
O
O C
C
O
17
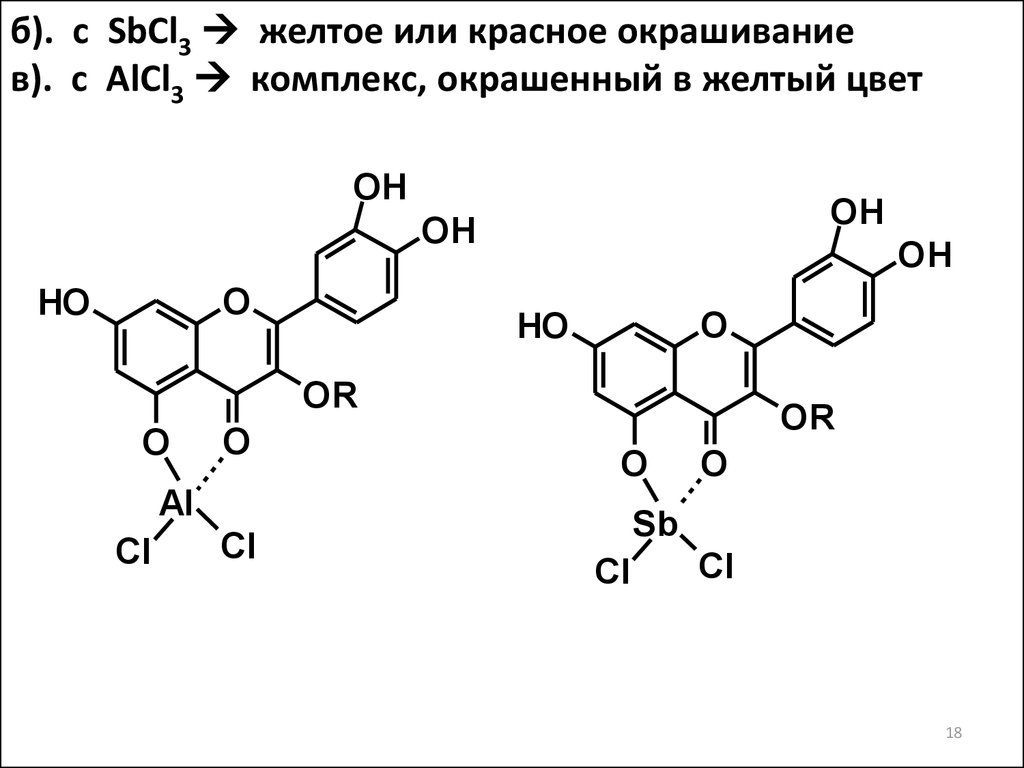
18.
б). с SbCl3 желтое или красное окрашиваниев). с AlCl3 комплекс, окрашенный в желтый цвет
OH
OH
OH
O
HO
OH
O
HO
OR
O
O
OR
O
Al
Cl
Cl
O
Sb
Cl
Cl
18
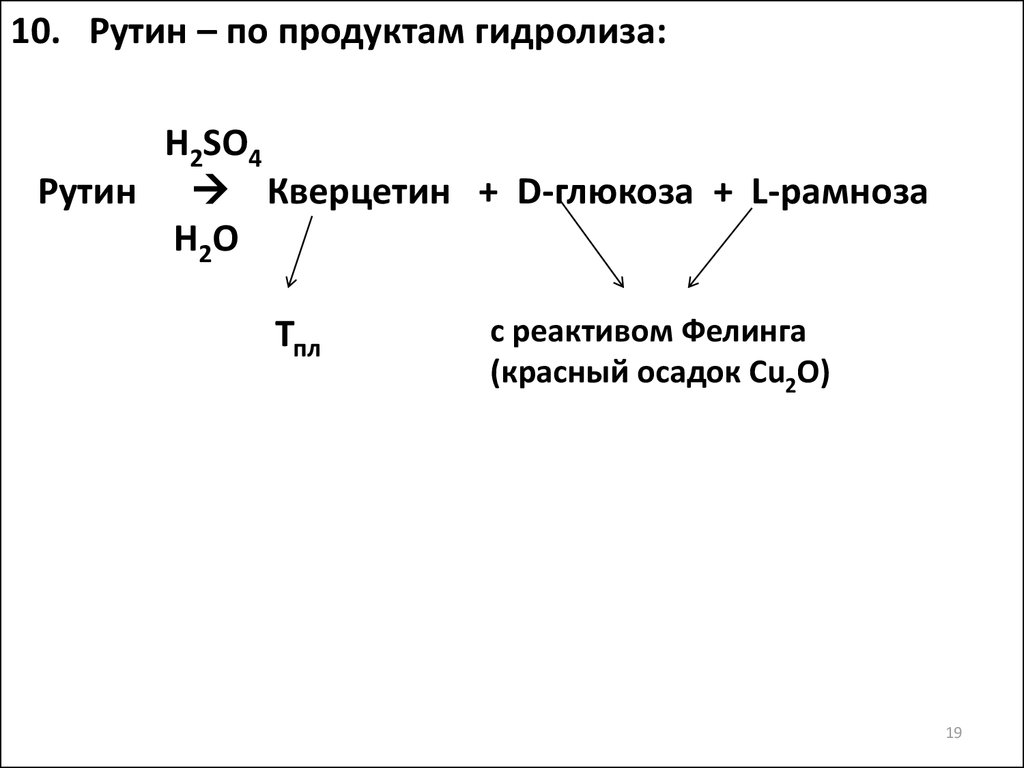
19.
10. Рутин – по продуктам гидролиза:H2SO4
Рутин Кверцетин + D-глюкоза + L-рамноза
H2O
Тпл
с реактивом Фелинга
(красный осадок Сu2O)
19
20.
Испытания на чистоту:• В кверцетине – посторонние флавоноиды - ТСХ;
• В рутине – кверцетина не более 5 % ( СФ-метрия или
БХ)
Отсутствие примесей алкалоидов; хлорофилла и
пигментов и др.
• В дигидрокверцетине – родственные примеси
(кверцетин и др.) не более 10% - ВЭЖХ
• В диосмине
– посторонние примеси – не более 10% (ВЭЖХ)
в том числе: гесперидин – не более 5%; диосметин – не
более 3%.
- содержание йода (не более 0,1%) - потенциометрически
с йодселективным электродом, после сжигания в колбе с
кислородом
Остататочные органические растворители (ГЖХ)
- в рутине – метанол
20
- в диосмине - этанол
21.
Количественное определение:•СФ-метрия
Кверцетин (λ 365 нм; в 0,002М HCl; по ГСО)
Рутин (λ 362,5 нм; в абсолютном спирте; по А1%1см)
•ФЭК (на основе цветных реакций) – в лек.формах
•ВЭЖХ
(Дигидрокверцетин, диосмин)
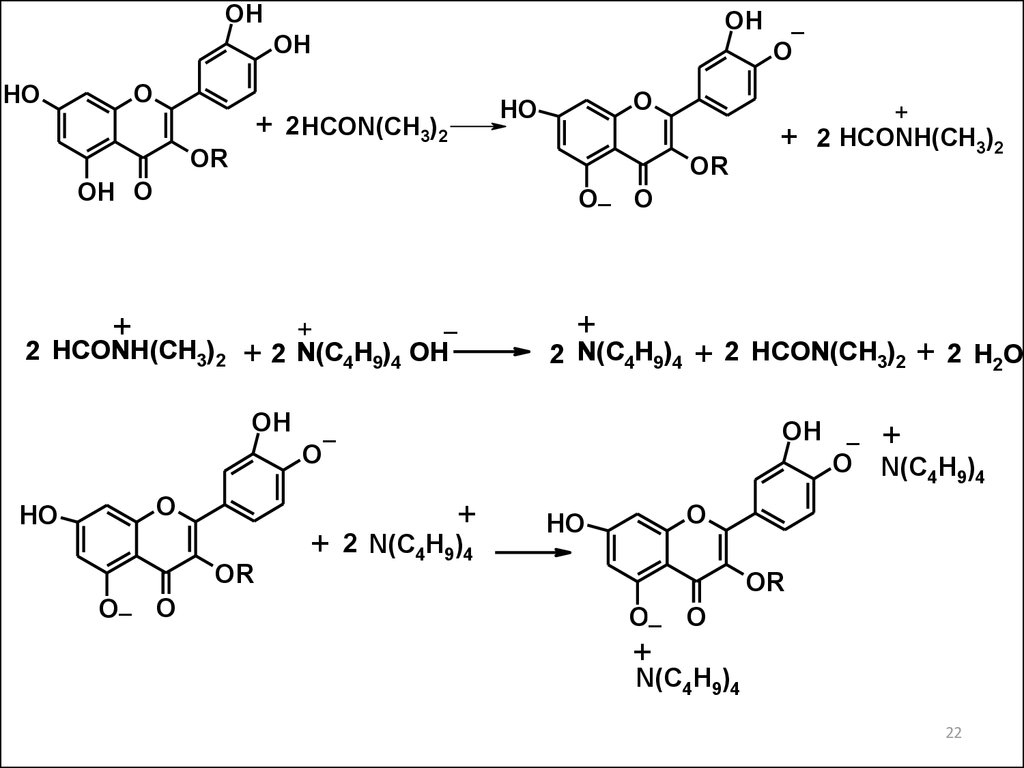
•Кислотно-основное титрование в неводных
растворителях
(Рутин – полифенол: слабые кислотные свойства)
Растворитель – ДМФА
Индикатор – тимолфталеин
Титрант – 0,1 М р-р тетрабутиламмония гидроксида
21
22.
OHOH
OH
O
O
HO
+
O
HO
2 HCON(CH3)2
+
OR
OR
OH O
+
2 HCONH(CH3)2
O_ O
+
2 HCONH(CH3)2
+
_
+
2 N(C4H9)4 OH
OH
+
2 N(C4H9)4
+2
O
+
OR
O_ O
HCON(CH3)2
+
2 H2O
OH _ +
O N(C4H9)4
_
O
HO
_
+
2 N(C4H9)4
O
HO
OR
O_ O
+
N(C4H9)4
22
23.
РУТИН (Рутозид*).Формы выпуска: таблетки, 0,02 г; поливитаминные ЛС
(Компливит, Аскорутин и др.).
ДИГИДРОКВЕРЦЕТИН
Капилар (Capilar); Таксифолин
Формы выпуска: таблетки, 0,02 г
ДИОСМИН, ГЕСПЕРИДИН
Детралекс, Флебодия, Вазокет 600
Диосмин с гесперидином — мировой стандарт для
лечения хронической венозной недостаточности
ТРОКСЕРУТИН (Троксевазин)
Формы выпуска: гель для наружного применения 2%;
капсулы 300 мг
23
24.
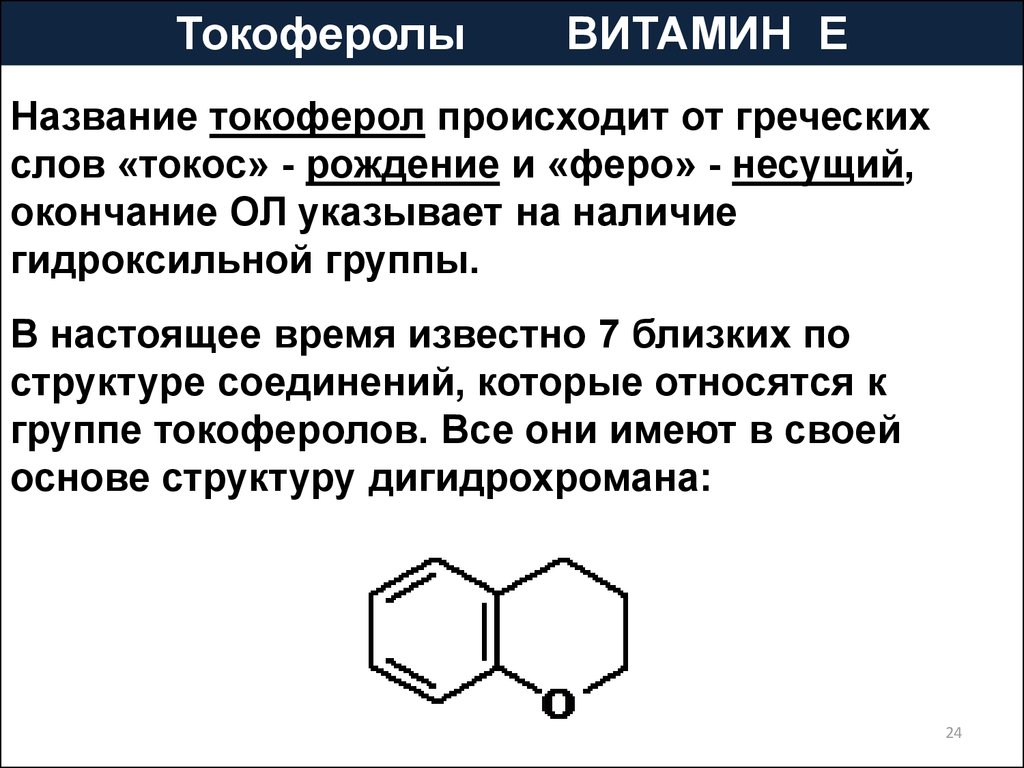
ТокоферолыВИТАМИН Е
Название токоферол происходит от греческих
слов «токос» - рождение и «феро» - несущий,
окончание ОЛ указывает на наличие
гидроксильной группы.
В настоящее время известно 7 близких по
структуре соединений, которые относятся к
группе токоферолов. Все они имеют в своей
основе структуру дигидрохромана:
24
25.
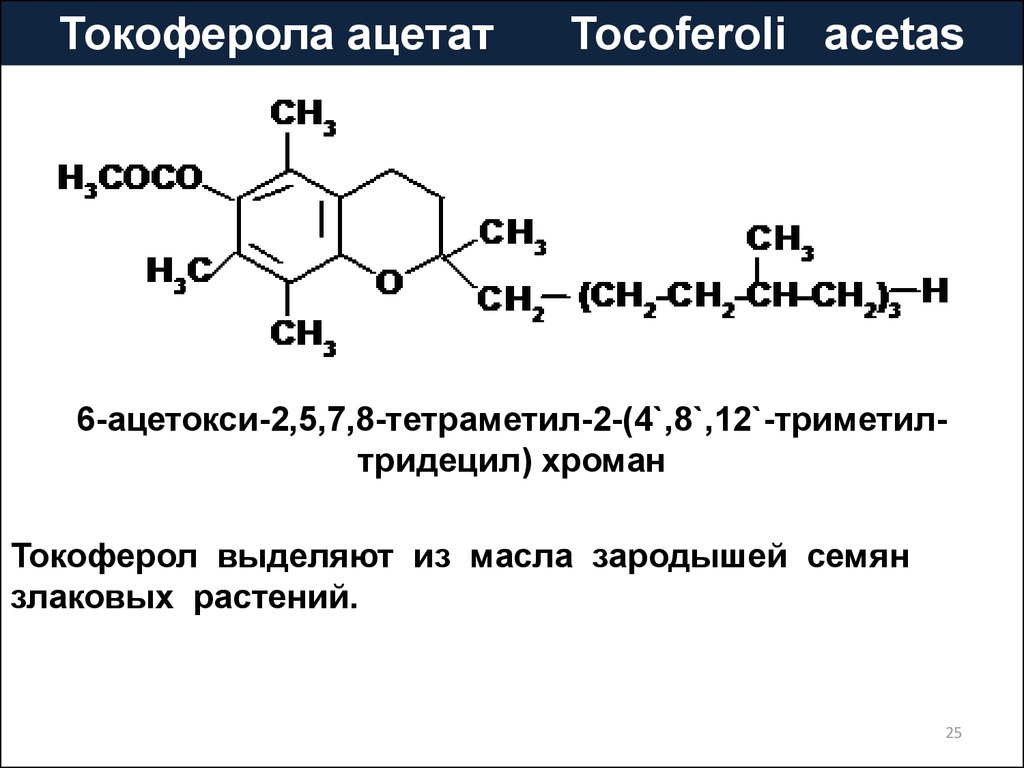
Токоферола ацетатTocoferoli acetas
6-ацетокси-2,5,7,8-тетраметил-2-(4`,8`,12`-триметилтридецил) хроман
Токоферол выделяют из масла зародышей семян
злаковых растений.
25
26.
Фармакологическое действие –восполняющее дефицит витамина E.
Обладает антиоксидантной активностью,
нормализует репродуктивную функцию;
препятствует развитию атеросклероза,
улучшает питание и сократительную способность
миокарда,
тормозит свободнорадикальные реакции,
предупреждает образование пероксидов,
повреждающих клеточные и субклеточные мембраны,
стимулирует синтез гема и гемсодержащих
ферментов — гемоглобина, миоглобина, цитохромов,
стимулирует синтез белков,
защищает от окисления витамин A.
Формы выпуска: капсулы, 100 и 200 мг;
Раствор для инъекций масляный 5%, 10% и 30% - 1,0
драже по 0,15 г
26
27.
Физические свойстваСветло-желтая прозрачная маслянистая
жидкость со слабым запахом.
На свету окисляется и темнеет.
пр. нерастворим в воде,
растворим в спирте,
очень легко – в эфире, хлороформе,
растительных маслах.
27
28.
Подлинность1. ИК-спектр
2. УФ-спектр ( в этаноле)
λmax 285 нм и λmin 254 нм
(А1%1см = 42-45)
3. n = 1,4950–1,4985
4. Химические реакции:
4.1 Реакции окисления (наличие фенольного
гидроксила)
28
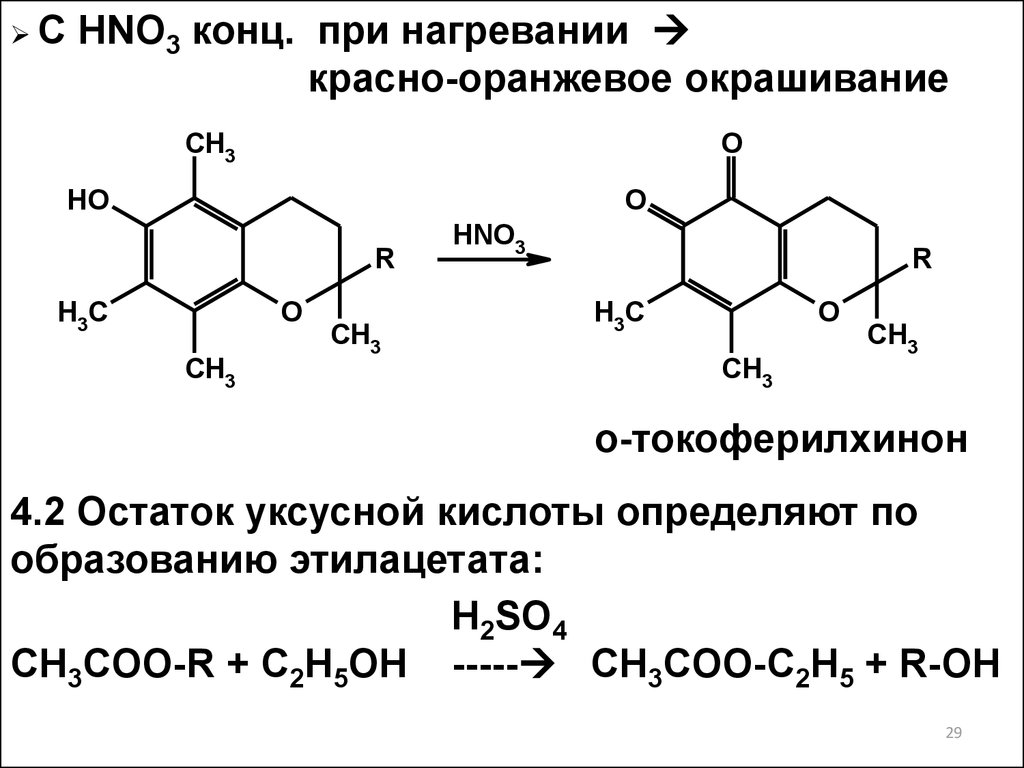
29.
СHNO3 конц. при нагревании
красно-оранжевое окрашивание
CH3
O
HO
O
R
H3C
O
CH3
CH3
HNO3
R
H3C
O
CH3
CH3
о-токоферилхинон
4.2 Остаток уксусной кислоты определяют по
образованию этилацетата:
H2SO4
CH3COO-R + C2H5OH ----- CH3COO-C2H5 + R-OH
29
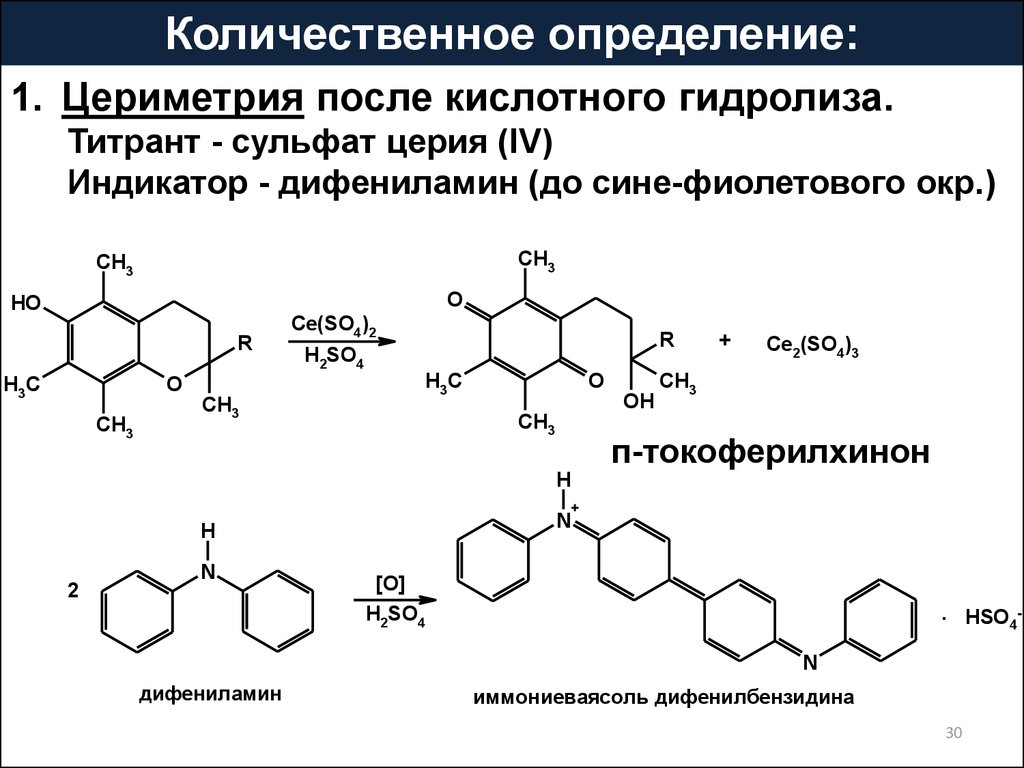
30.
Количественное определение:1. Цериметрия после кислотного гидролиза.
Титрант - сульфат церия (IV)
Индикатор - дифениламин (до сине-фиолетового окр.)
CH3
CH3
O
HO
R
H3C
O
CH3
Ce(SO4)2
H2SO4
R
H3C
CH3
O
CH3
H
OH
+
Ce2(SO4)3
CH3
п-токоферилхинон
+
N
H
2
N
[O]
H2SO4
. HSO4N
дифениламин
иммониеваясоль дифенилбензидина
30
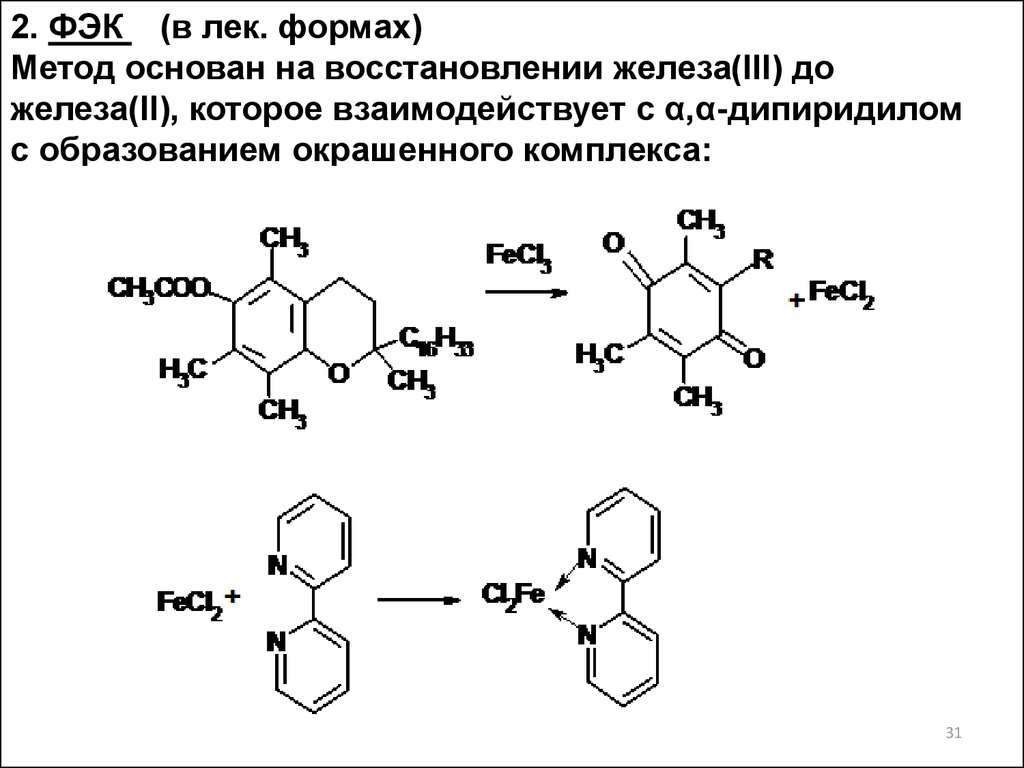
31.
2. ФЭК (в лек. формах)Метод основан на восстановлении железа(III) до
железа(II), которое взаимодействует с α,α-дипиридилом
с образованием окрашенного комплекса:
31
32.
3. ГЖХ4. ВЭЖХ
ХРАНЕНИЕ в герметически закрытых, заполненных доверху
банках
темного
стекла,
в
прохладном,
защищенном от света месте (при температуре не
выше +10 C).
32
33.
Производные бензо–γ–пирона33
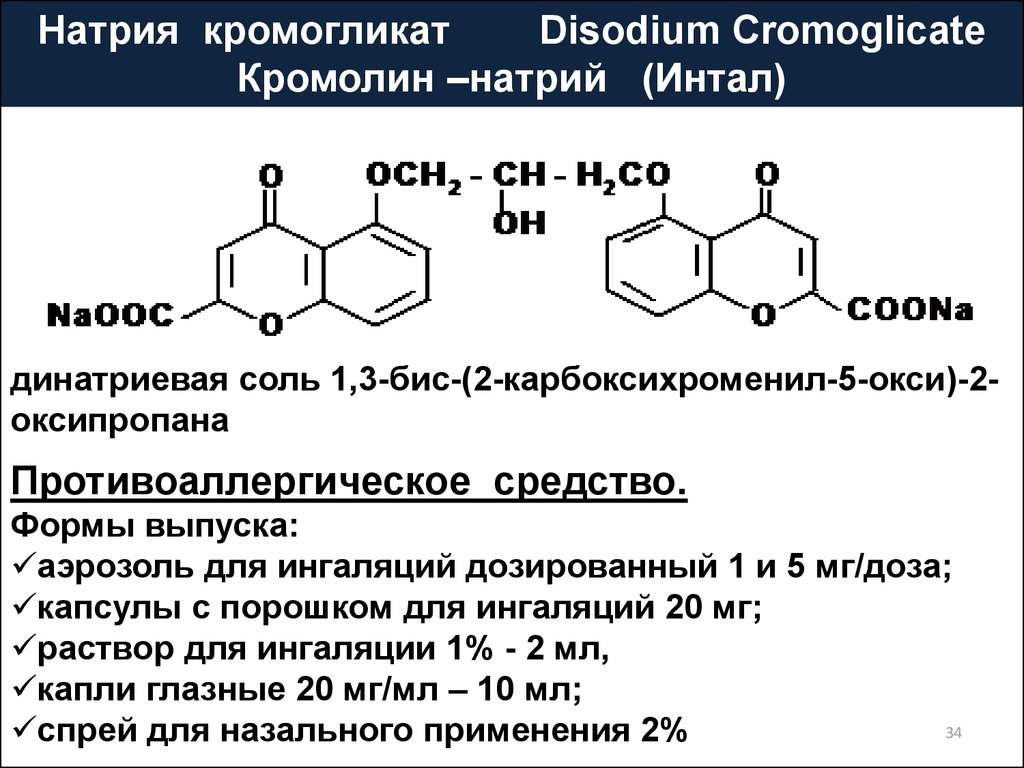
34.
Натрия кромогликатDisodium Cromoglicate
Кромолин –натрий (Интал)
динатриевая соль 1,3-бис-(2-карбоксихроменил-5-окси)-2оксипропана
Противоаллергическое средство.
Формы выпуска:
аэрозоль для ингаляций дозированный 1 и 5 мг/доза;
капсулы с порошком для ингаляций 20 мг;
раствор для ингаляции 1% - 2 мл,
капли глазные 20 мг/мл – 10 мл;
34
спрей для назального применения 2%
35.
Физические свойстваБелый кристаллический порошок.
Растворим в воде,
очень мало растворим в спирте.
Подлинность
1. ИК –спектр
2. УФ-спектр (в фосфатном буфере (рН=7,4)
λmax 238 нм и 326 нм
3. Реакции на ионы натрия
Количественное определение:
1. МЕТОД НЕВОДНОГО ТИТРОВАНИЯ слабых оснований
в смеси пропиленгликоля, изопропанола и гексана.
Титрант - 0,1 М р-р хлорной кислоты. Конец титрования
определяют потенциометрическим методом.
2. СФ
35
36.
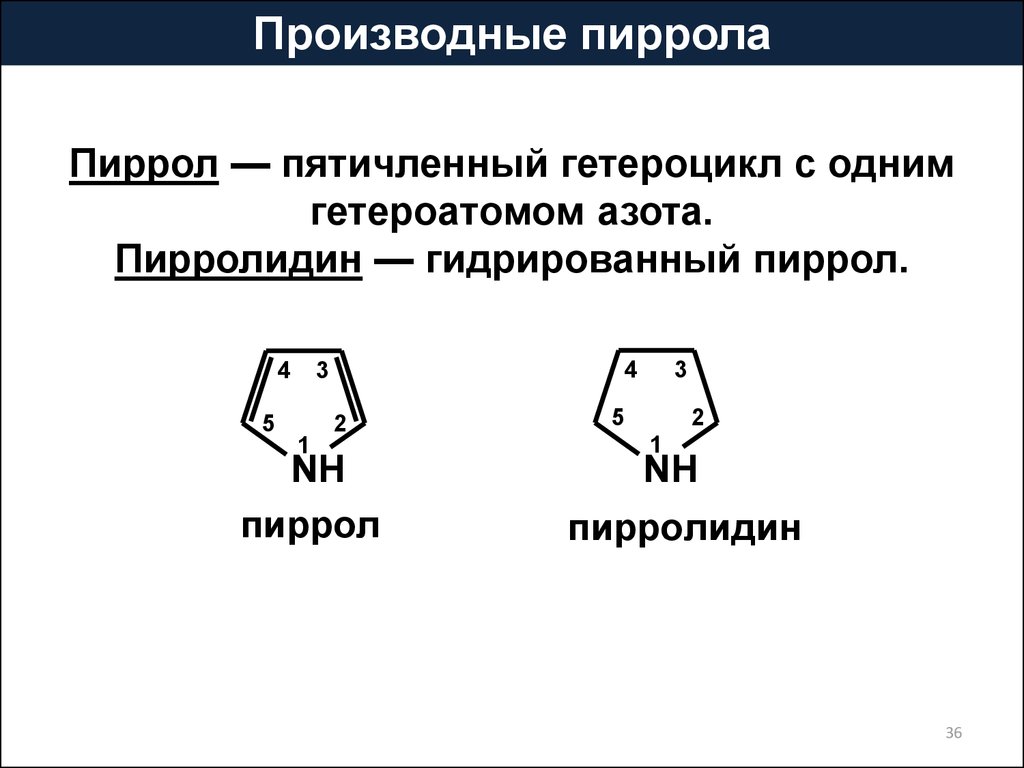
Производные пирролаПиррол — пятичленный гетероцикл с одним
гетероатомом азота.
Пирролидин — гидрированный пиррол.
4
5
4
3
1
2
NH
пиррол
3
5
2
1
NH
пирролидин
36
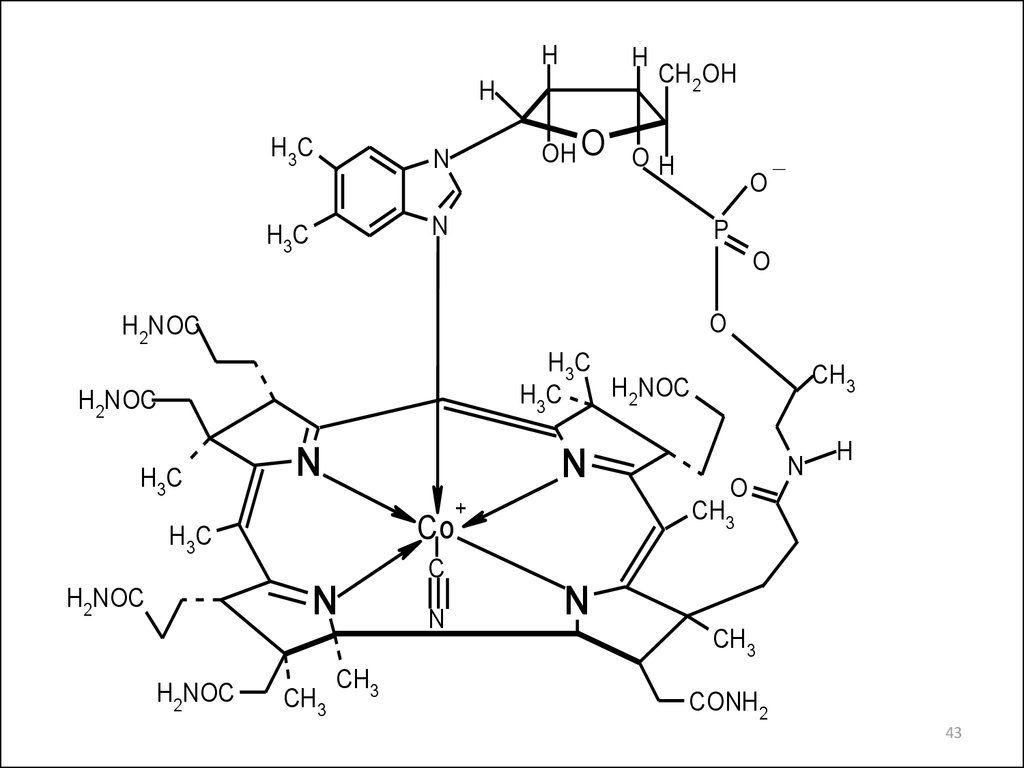
37.
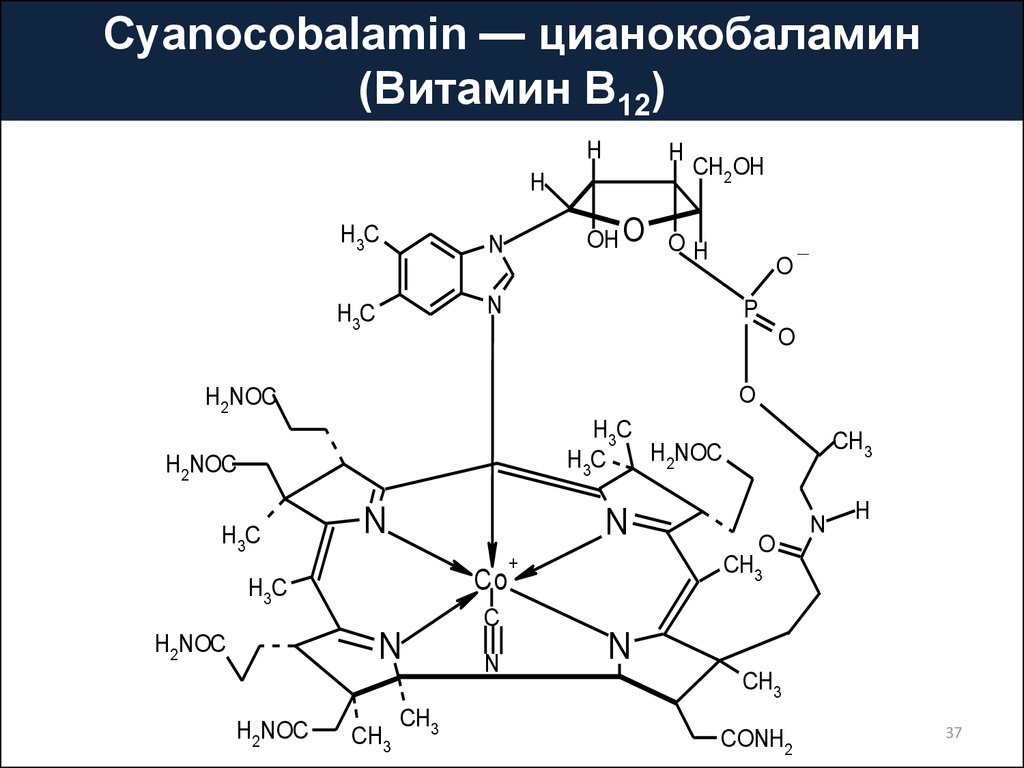
Cyanocobalamin — цианокобаламин(Витамин B12)
H
H
H
H3C
CH2 OH
OH O O H
N
O
N
H3C
P
O
O
H2NOC
H3C
H2NOC
H3C
H2NOC
H3C
N
N
Co
H3C
+
CH3
O
CH3
N
H
C
N
H2NOC
H2NOC
CH3
CH3
N
N
CH3
CONH2
37
38.
1934 г. - Джордж Уипл и Джордж Майнот получилиНобелевскую премию по медицине «за открытия,
связанные с применением печени в лечении
пернициозной анемии».
1956 г. – Дороти Кроуфут-Ходжкин установила
структуру молекулы В12 на основе данных
кристаллографии. (1964 г. - Нобелевская премия
по химии)
1973 г. – Роберт Бёрнс Вудворд разработал схему
полного химического синтеза витамина B12,
ставшую классикой для химиков-синтетиков.
38
39.
Молекула цианокобаламина состоитдвух связанных между собой частей:
кобальтового
бензимидазола
комплекса
из
нуклеотида
макроциклической корриновой системы.
39
40.
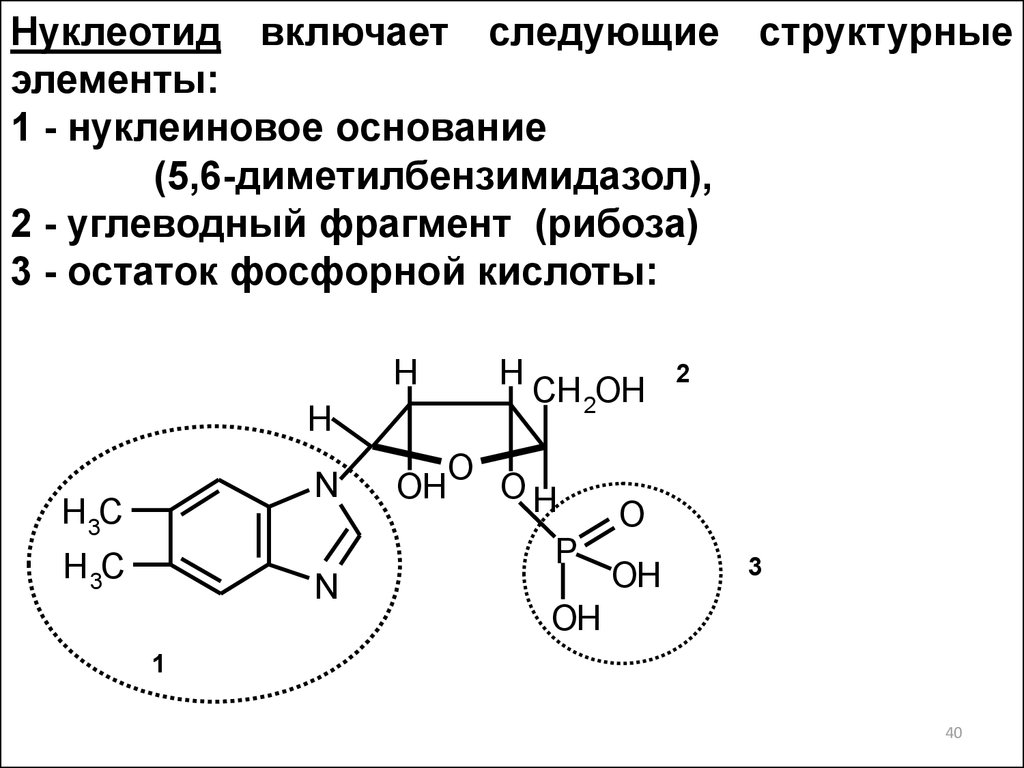
Нуклеотид включает следующие структурныеэлементы:
1 - нуклеиновое основание
(5,6-диметилбензимидазол),
2 - углеводный фрагмент (рибоза)
3 - остаток фосфорной кислоты:
H
H CH OH
2
H
N
H 3C
OH
O
OH
P
H 3C
N
2
O
OH
3
OH
1
40
41.
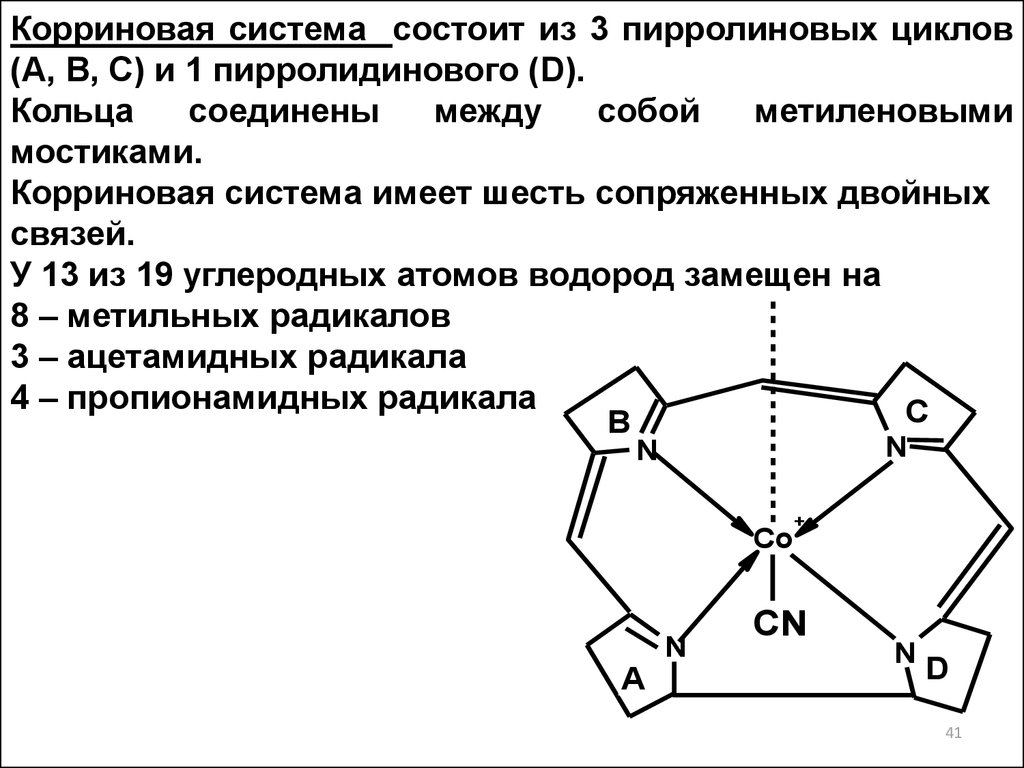
Корриновая система состоит из 3 пирролиновых циклов(А, В, С) и 1 пирролидинового (D).
Кольца
соединены
между
собой
метиленовыми
мостиками.
Корриновая система имеет шесть сопряженных двойных
связей.
У 13 из 19 углеродных атомов водород замещен на
8 – метильных радикалов
3 – ацетамидных радикала
4 – пропионамидных радикала
C
B
N
N
Co
N
A
+
CN
N
D
41
42.
Атом азота 5,6-диметилбензимидазола в положении 3связан координационной связью с атомом кобальта (III).
Кобальт
образует
хелатное
(внутрикомплексное)
соединение с цианогруппой и с атомами азота
гидрированных
пиррольных
циклов
корриновой
системы.
Таким образом, создается замкнутая циклическая
система, в центре которой находится координационный
атом кобальта (координационное число 6).
Положительный заряд иона кобальта нейтрализуется
отрицательно заряженным анионом фосфорной кислоты.
Цианокобаламин представляет собой не только
хелатное соединение, но и внутреннюю соль или диэфир
фосфорной кислоты, у которого одна связь — с рибозой,
а другая — с пропионильным остатком кобамида.
42
43.
HH
H
H3C
CH2 OH
OH O O H
N
O
N
H3C
P
O
O
H2NOC
H3C
H2NOC
H3C
H2NOC
H3C
N
N
Co
H3C
CH3
O
N
H
CH3
+
C
N
H2NOC
H2NOC
CH3
CH3
N
N
CH3
CONH2
43
44.
В.Н.Букин (СССР) - из культуральной жидкостиStreptomyces griseus
Получение
•Добавление соли кобальта
•отделение стрептомицина
•сорбция (активированный уголь)
•десорбция бутанолом
Физические свойства
Кристаллический порошок темно-красного цвета,
без запаха. Гигроскопичен. Разлагается при
температуре 200 C.
Умеренно медленно растворим в воде,
растворим в спирте,
пр. нерастворим в эфире, хлороформе.
44
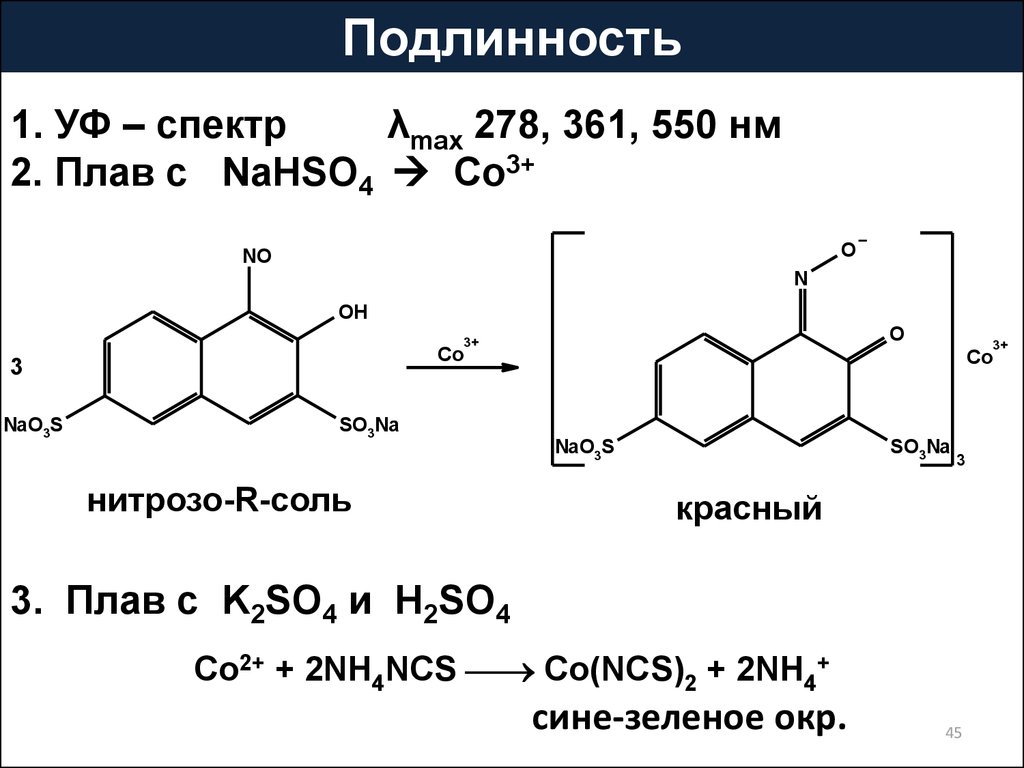
45.
Подлинность1. УФ – спектр
λmax 278, 361, 550 нм
2. Плав с NaHSO4 Co3+
O
NO
N
OH
O
3+
Co
3
NaO3S
SO3Na
нитрозо-R-соль
3+
Co
SO3Na
NaO3S
3
красный
3. Плав с K2SO4 и H2SO4
Co2+ + 2NH4NCS Co(NCS)2 + 2NH4+
сине-зеленое окр.
45
46.
4. Цианогруппа –нагревание с кислотой щавелевой
циановодородная кислота
+ бензидин + ион меди комплекс синего цвета
Посторонние примеси
1)УФ-спектрофотометрия
A361/A278 от 1,70 до 1,88 ;
A361/A550 от 3,15 до 3,40
Количественное определение:
1. Спектрофотометрия (361 нм, ГСО)
46
47.
Активное противоанемическое средство.Назначают также при заболеваниях печени,
полиневритах, дерматитах и лучевой болезни.
Потребность человека в вит. В12 ничтожна-1-5 мкг
в сутки.
Формы выпуска:
Раствор для инъекций, 100, 200, 500 мкг/мл
Таблетки 50 мкг с фолиевой кислотой 5 мкг.
Поливитамины
*Гидроксикобаламин – Со связан с ОН-группой.
*Кобамамид – Со связан с
β-5`-дезоксиаденозильным остатком.
47
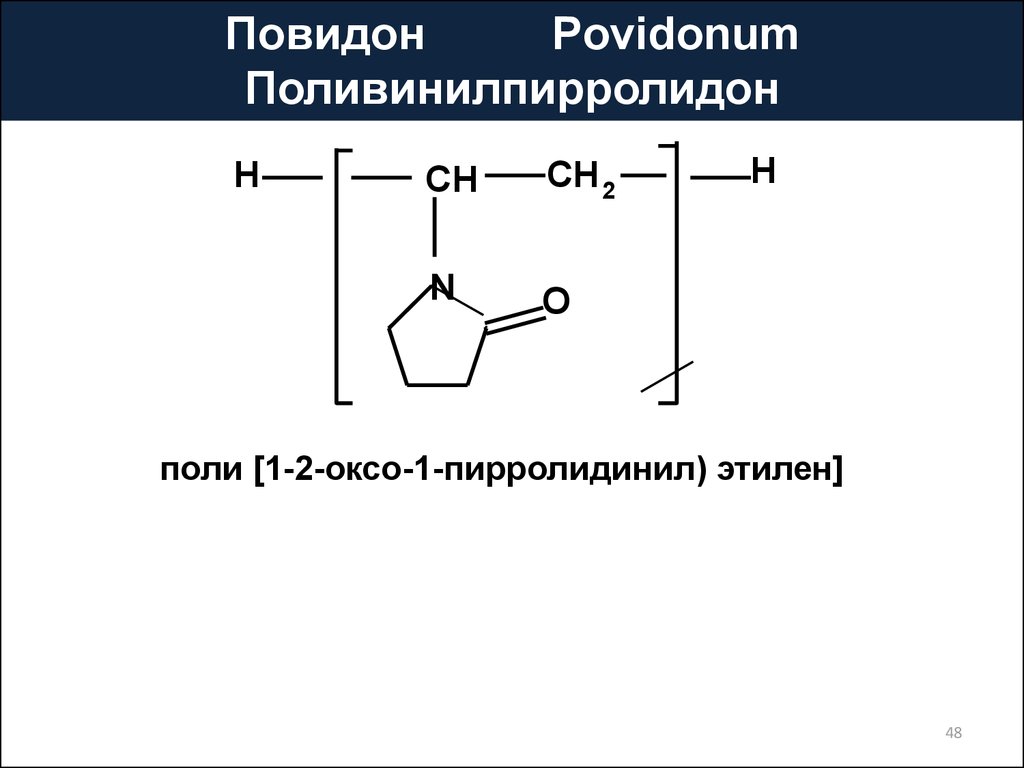
48.
ПовидонPovidonum
Поливинилпирролидон
H
CH
CH 2
N
O
H
поли [1-2-оксо-1-пирролидинил) этилен]
48
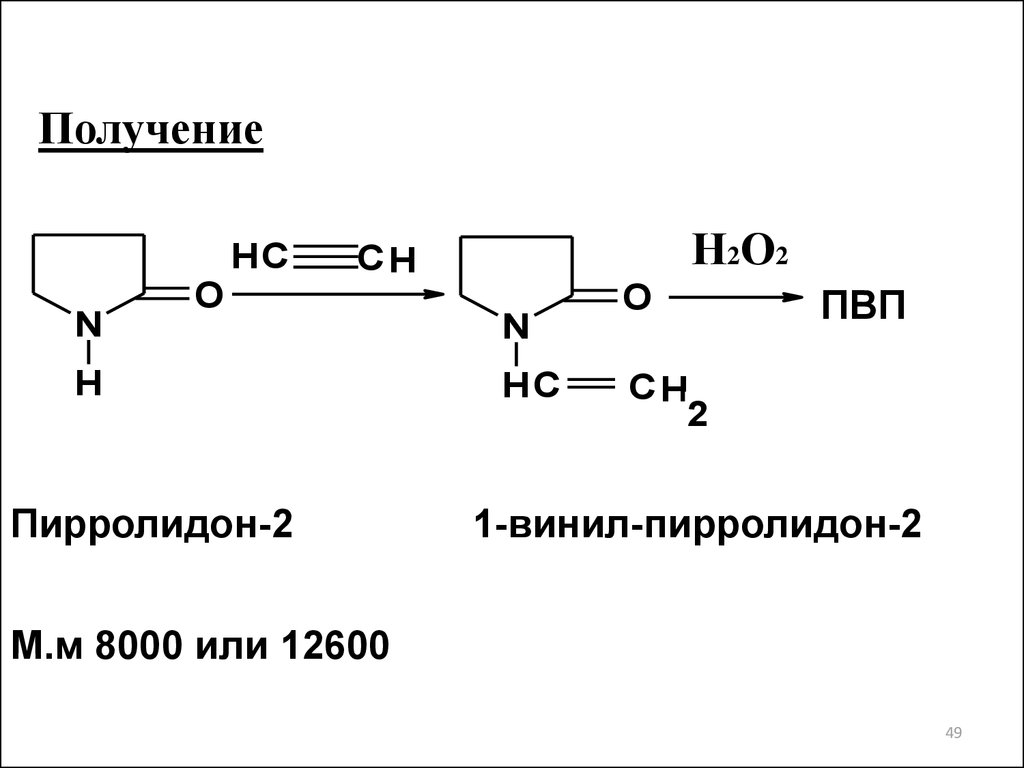
49.
ПолучениеHC
N
Н2О2
CH
O
H
Пирролидон-2
N
HC
O
ПВП
CH
2
1-винил-пирролидон-2
М.м 8000 или 12600
49
50.
Поливинилпирролидон выпускается подразличными наименованиями: повидон, калидон
и др.
Повидон – это белый или желтовато-белый
порошок, растворим в воде с образованием
коллоидного раствора, растворим в спирте.
50
51.
Подлинность1. ИК–спектр
2. + HCl + K2Cr2O7 жѐлто-оранжевый осадок.
3. +1% р-р йода в йодиде калия красное окр.
4. С р-ром n-диметиламинобензальдегида в
кислоте серной розовое окр. (при слабом
нагревании на водяной бане).
Количественное определение:
Метод Къельдаля (содержание азота 12-12,8%).
51
52.
Как лекарственное вещество повидонприменяется в качестве плазмозамещающего
средства в виде 15% раствора.
Этот раствор по физическим свойствам
сходен с синовиальной жидкостью и может
использоваться при патологии суставов
конечностей.
Выпускается в виде 15% раствора в ампулах
по 5 мл.
Повидон используется в фармацевтической
технологии в качестве вспомогательного
средства.
52
53.
ГемодезРаствор для инфузий
Состав:
повидона -12600
- 6,0 г;
ионы Nа, К, Са, Сl, Мg на 100мл.
Применение
При заболеваниях, связанных с сильной
интоксикацией. ПВП – связывает токсины и
быстро выводит их из организма.
Ионы Nа, К, Са, Мg, Cl необходимы для
поддержания солевого баланса крови.
53
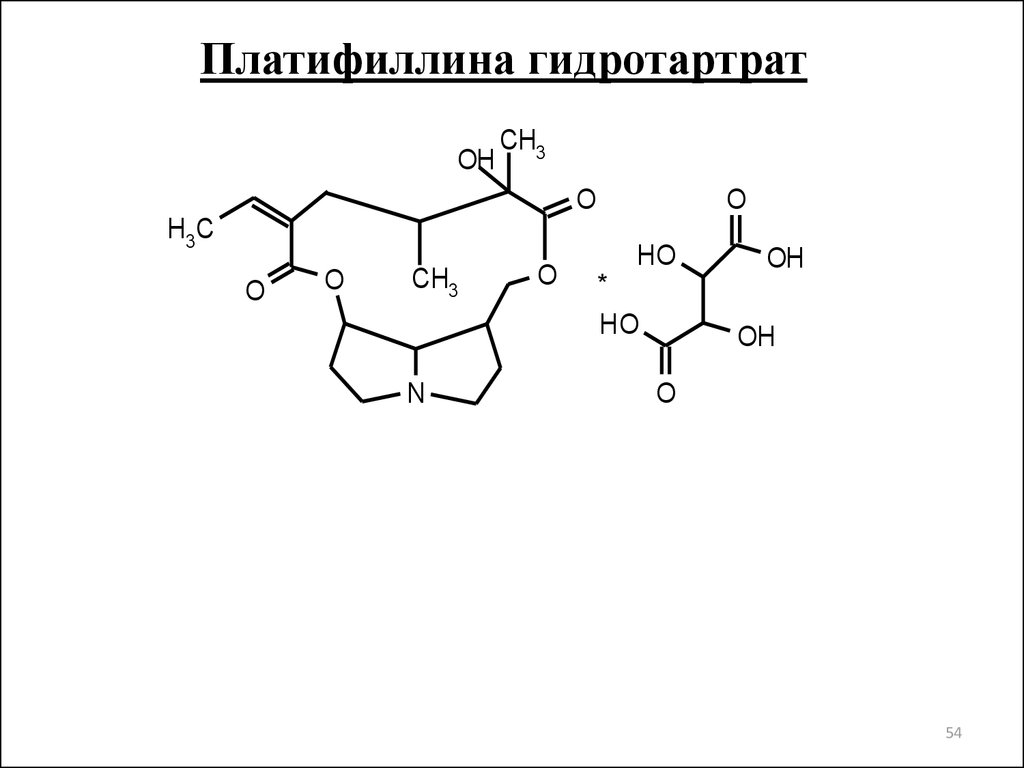
54.
Платифиллина гидротартратOH
CH3
O
O
H3C
O
O
CH3
O
HO
*
HO
N
OH
OH
O
54
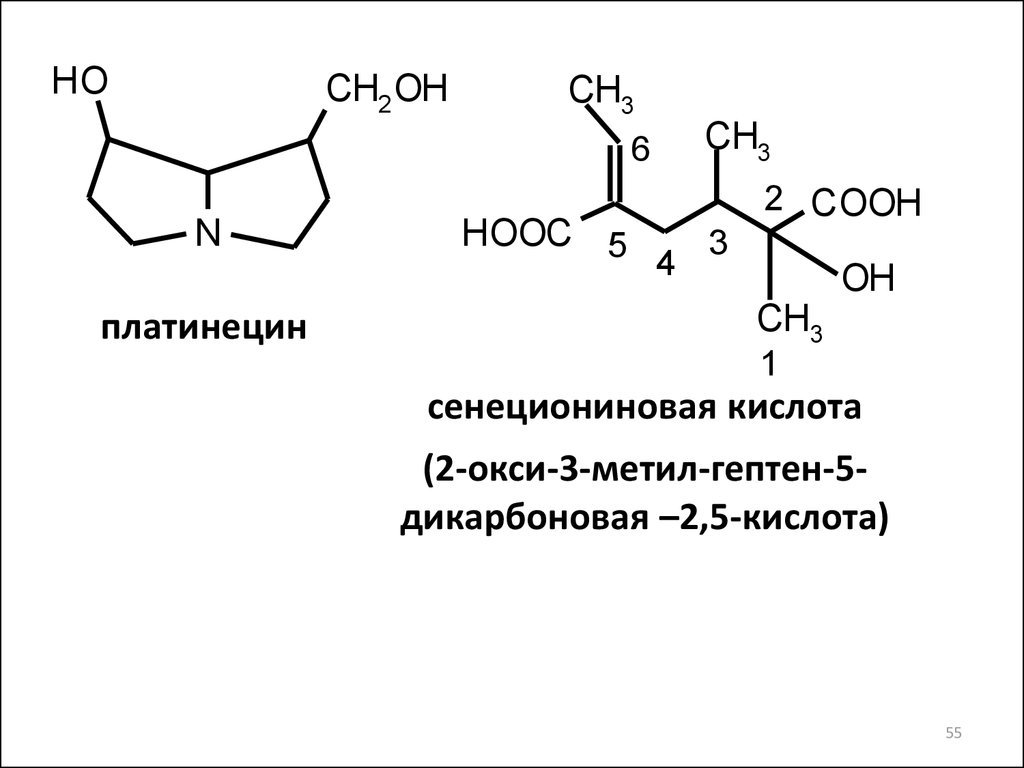
55.
HOCH2 OH
CH3
6
N
платинецин
CH3
HOOC 5
3
4
2 COOH
OH
CH3
1
сенециониновая кислота
(2-окси-3-метил-гептен-5дикарбоновая –2,5-кислота)
55
56.
Подлинностьtпл – 192-198 ˚С (с разлож.)
[α] – от 38 до 40 ˚ (5% водн. р-р)
ИК – спектр
1%
E
УФ – спектр 220 нм ( 1cm - 520) для лек. форм
ТСХ – для лек. форм
Реакции подлинности
•Основные свойства
Реактив Майера (K2HgI4)
белый осадок
•Сложноэфирные группы-гидроксамовая проба
●На тартрат-ион
с KCl
белый осадок
56
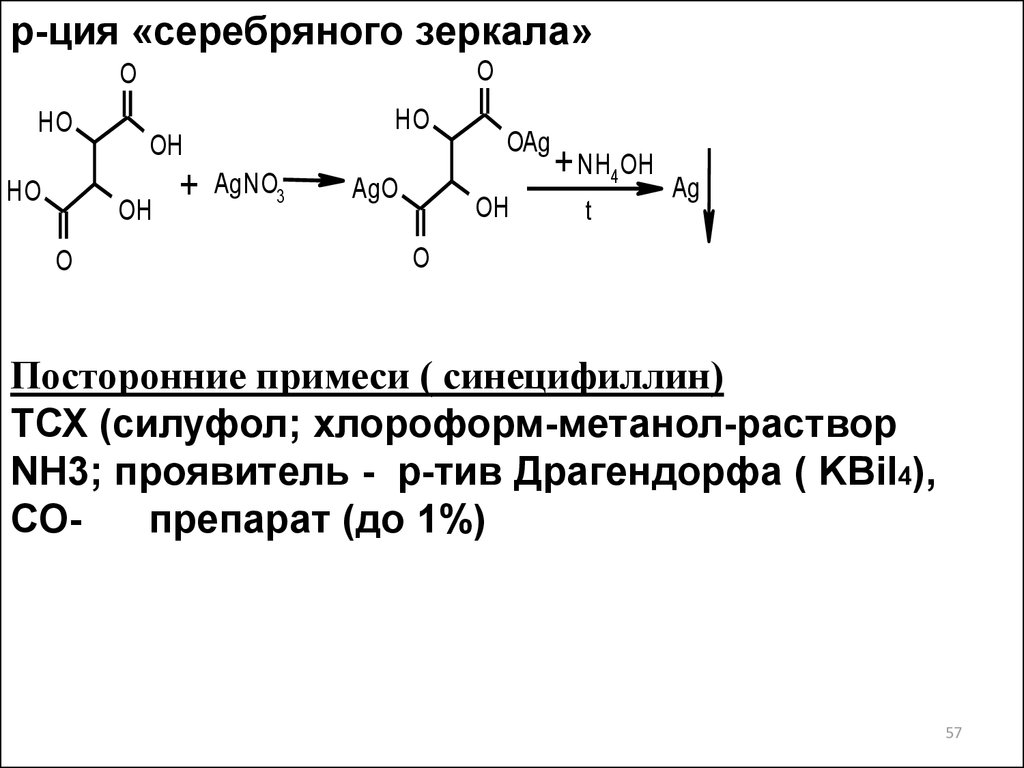
57.
р-ция «серебряного зеркала»O
O
HO
HO
OH
OH
O
HO
+
AgNO3
AgO
OAg
OH
+ NH4OH
t
Ag
O
Посторонние примеси ( синецифиллин)
ТСХ (силуфол; хлороформ-метанол-раствор
NH3; проявитель - р-тив Драгендорфа ( KBiI4),
СОпрепарат (до 1%)
57
58.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ1)Неводное титрование (ЛУК; 0,1М HClO4;
крист. фиолет.)
2)Нейтрализация по винной кислоте (в присут.
хлороформа по Ф/Ф)
3)УФ-спектрофотометрия при λ=220 нм.
табл. однородн. дозир.-в буф.р-ре с рН 6,0 ;
кол. ан. в 0,1М HCl , λ=220 нм
4.Экстракционная фотометрия по реакции с
пикриновой кислотой, тропеолином ОО
Хранение – сп. А
0, 2% растворы в ампулах;
таблетки по 0,005 г
1 и 2% растворы (глазные капли),
58
Мидриатическое и спазмолитическое средство.



























 medicine
medicine chemistry
chemistry








