Similar presentations:
Спирты. Классификация
1.
СпиртыГидроксипроизводными углеводородов
называют производные углеводородов, у
которых один или несколько атомов
водорода заменены на гидроксильные (ОН)
группы
Спирты - гидроксипроизводные
углеводородов, у которых гидроксильная
группа связана с насыщенным атомом
углерода.
1
2.
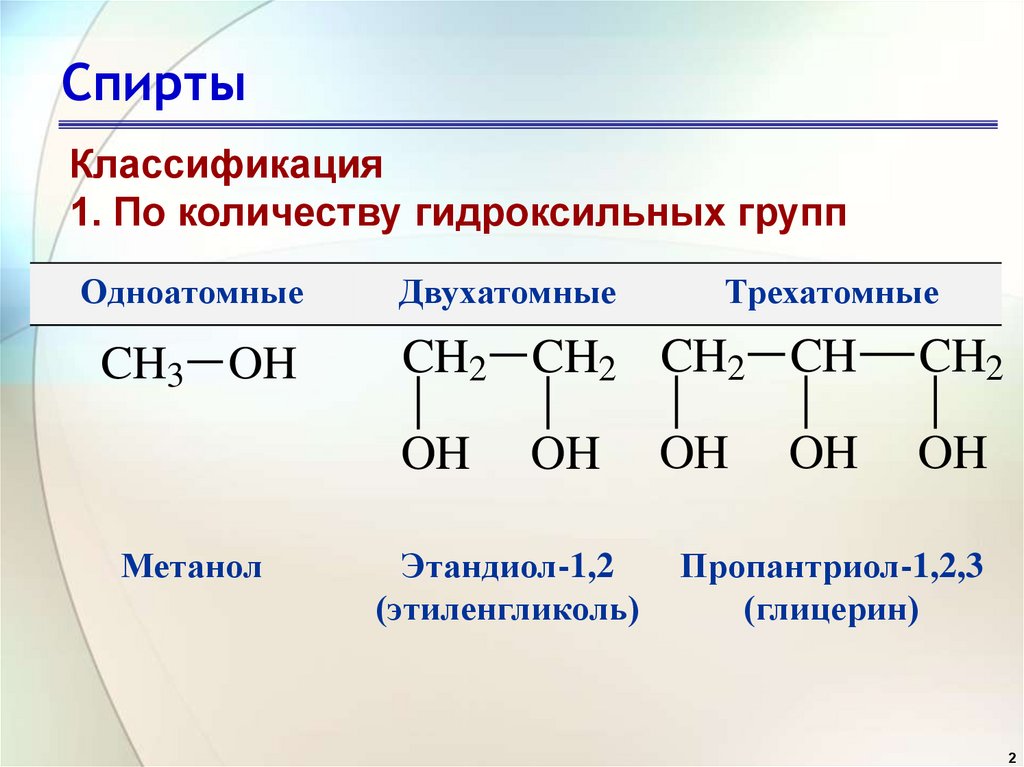
СпиртыКлассификация
1. По количеству гидроксильных групп
Одноатомные
CH3 OH
Двухатомные
CH2 CH2 CH2 CH
OH
Метанол
Трехатомные
OH
Этандиол-1,2
(этиленгликоль)
OH
OH
CH2
OH
Пропантриол-1,2,3
(глицерин)
2
3.
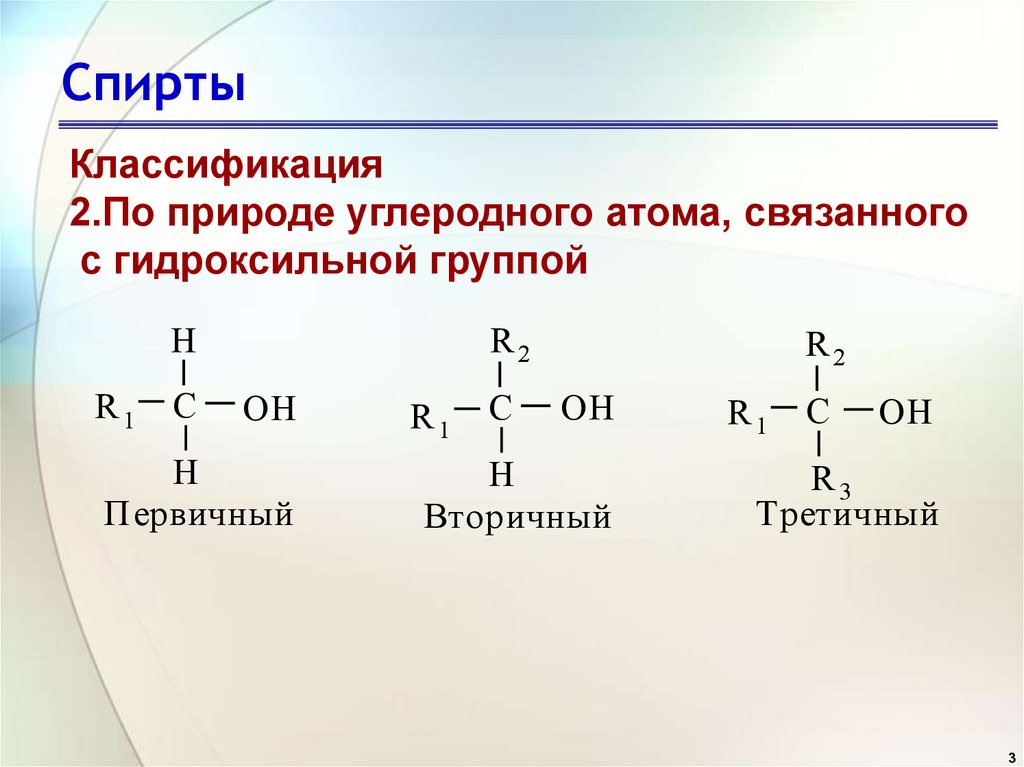
СпиртыКлассификация
2.По природе углеродного атома, связанного
с гидроксильной группой
R2
H
R1
C
OH
H
Первичный
R1
C
R2
OH
H
Вторичный
R1
C
OH
R3
Третичный
3
4.
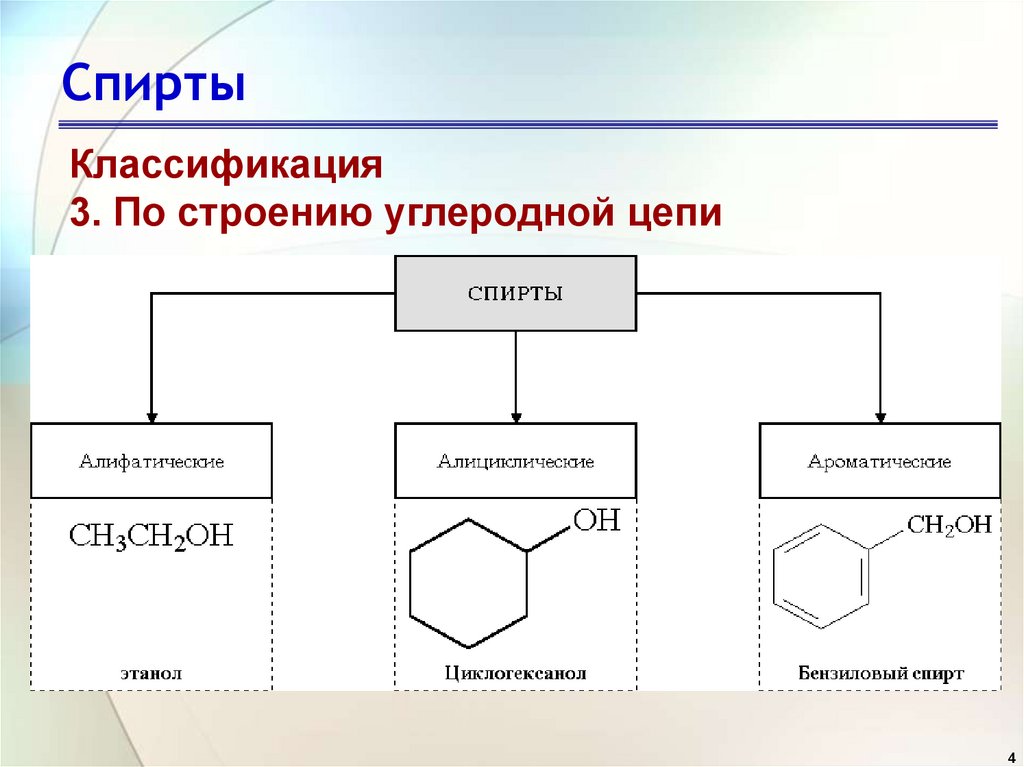
СпиртыКлассификация
3. По строению углеродной цепи
4
5.
СпиртыИзомерия
1. Измерия положения гидроксильной группы
CH3CH2CH2OH
Пропанол-1
(н-пропиловый спирт)
CH3CHCH3
OH
Пропанол-2
(изопропиловый спирт)
5
6.
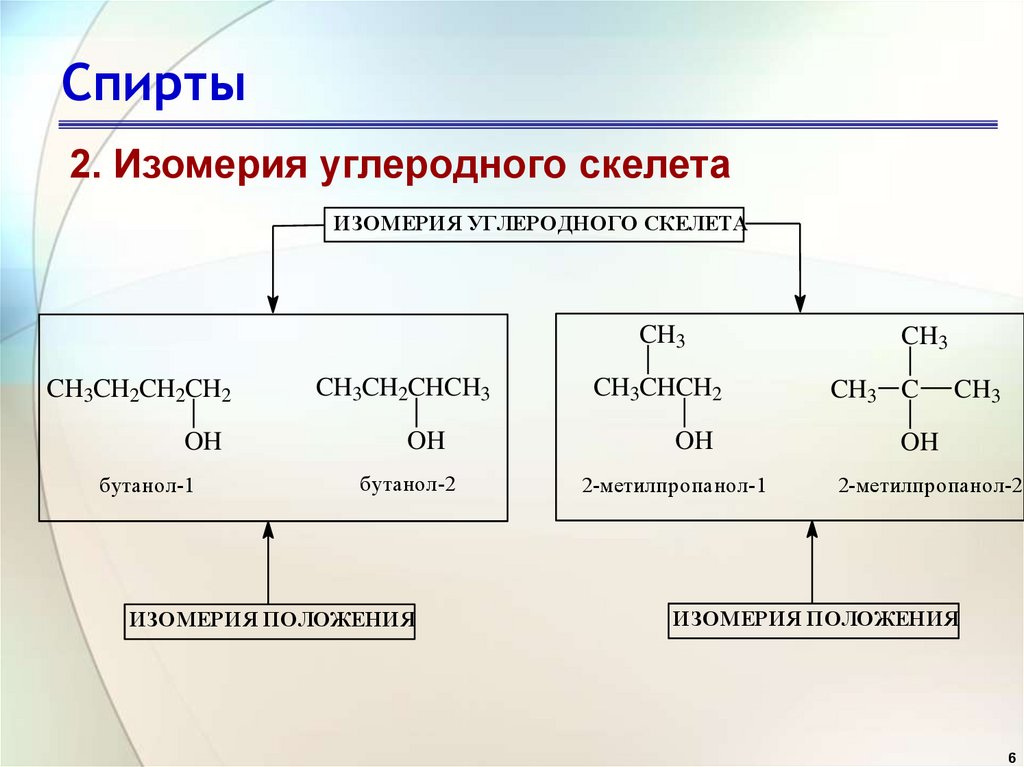
Спирты2. Изомерия углеродного скелета
ИЗОМЕРИЯ УГЛЕРОДНОГО СКЕЛЕТА
CH3
CH3CH2CH2CH2
OH
бутанол-1
CH3CH2CHCH3
OH
бутанол-2
ИЗОМЕРИЯ ПОЛОЖЕНИЯ
CH3CHCH2
OH
2-метилпропанол-1
CH3
CH3 C
CH3
OH
2-метилпропанол-2
ИЗОМЕРИЯ ПОЛОЖЕНИЯ
6
7.
СпиртыНоменклатура
1.Рациональная номенклатура
2.Радикально-функциональная номенклатура
3.Заместительная номенклатура
7
8.
СпиртыНоменклатура
1.По рациональной номенклатуре спирты
называют как производные метанола
(называется карбинол), у которого один или
несколько атомов водорода заменены на
углеводородные радикалы.
CH3CH2CH2OH
этилкарбинол
CH3CHCH3
OH
диметилкарбинол
8
9.
СпиртыНоменклатура
2.По радикально-функциональной
номенклатуре перед названием
класса соединения приводят название
углеводородного радикала
OH
CH3CH2CH2OH
Пропиловый спирт
CH3CHCH3
OH
Изопропиловый спирт
Бензиловый спирт
9
10.
СпиртыНоменклатура
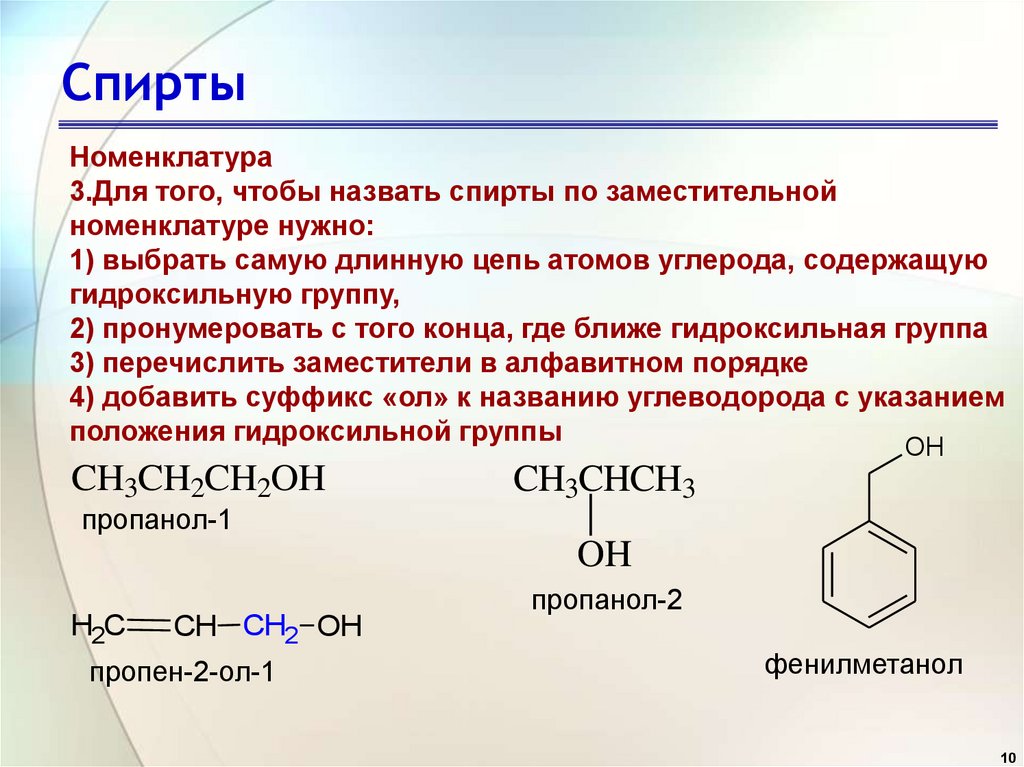
3.Для того, чтобы назвать спирты по заместительной
номенклатуре нужно:
1) выбрать самую длинную цепь атомов углерода, содержащую
гидроксильную группу,
2) пронумеровать с того конца, где ближе гидроксильная группа
3) перечислить заместители в алфавитном порядке
4) добавить суффикс «ол» к названию углеводорода с указанием
положения гидроксильной группы
OH
CH3CH2CH2OH
пропанол-1
CH3CHCH3
OH
H2C
СН CH2 OH
пропен-2-ол-1
пропанол-2
фенилметанол
10
11.
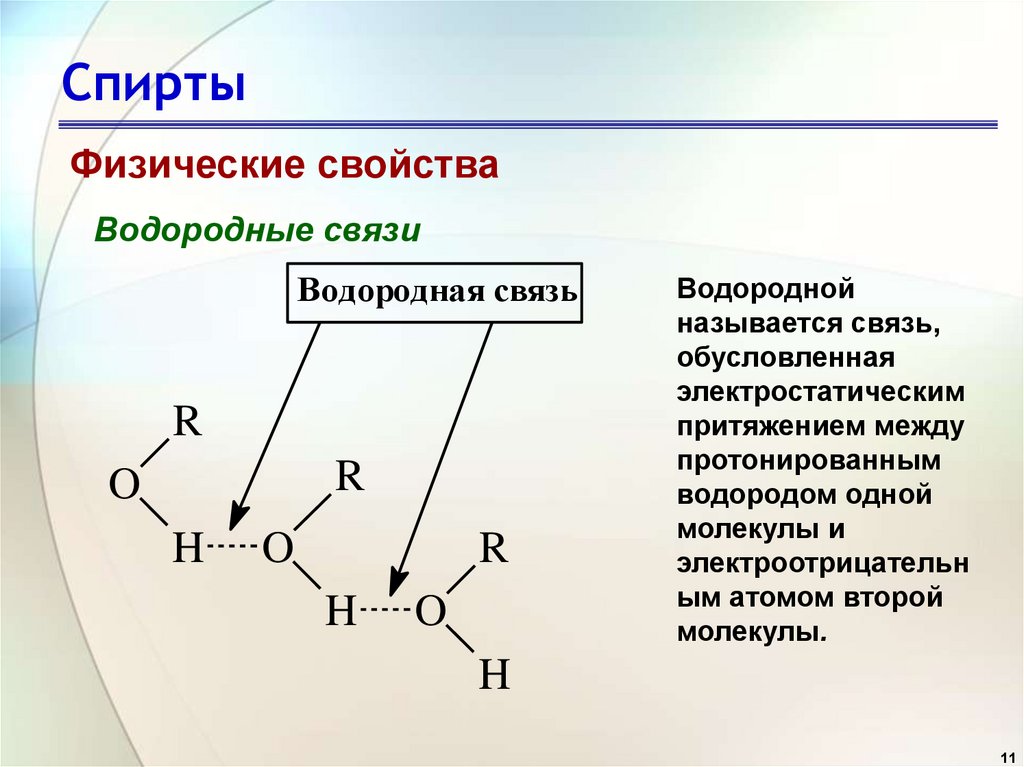
СпиртыФизические свойства
Водородные связи
Водородная связь
R
R
O
H
R
O
H
O
Водородной
называется связь,
обусловленная
электростатическим
притяжением между
протонированным
водородом одной
молекулы и
электроотрицательн
ым атомом второй
молекулы.
H
11
12.
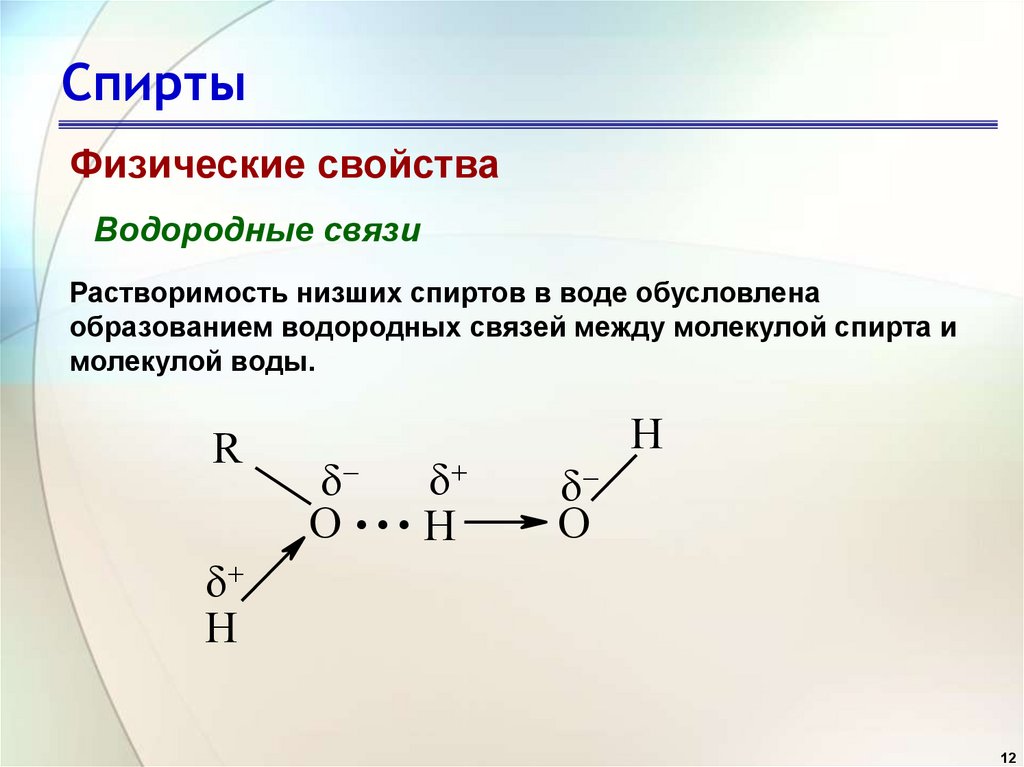
СпиртыФизические свойства
Водородные связи
Растворимость низших спиртов в воде обусловлена
образованием водородных связей между молекулой спирта и
молекулой воды.
R
O
...
H
O
H
H
12
13.
СпиртыСпособы получения
1. Гидратация алкенов (промышленный метод)
Присоединение воды к алкенам происходит в присутствии
кислых катализаторов (серная, фосфорная кислоты, оксид
алюминия или другой носитель, обработанный кислотами).
Реакция
идет
по
механизму
электрофильного
присоединения (АЕ), по правилу Марковникова
СН 2 = СН
СН 2 +
Н 2О
Н+
СН 3 СН
СН 3
ОН
13
14.
СпиртыСпособы получения
2. Брожение сахаров
Дрожжи сбраживают некоторые виды сахаров. Это сложный
каталитический многостадийный распад на спирт и диоксид
углерода
С 6Н 12О 6
2С 2Н 5ОН + 2СО 2
14
15.
СпиртыСпособы получения
3. Гидролиз галогеналканов
Гидролиз галогеналканов проводят при нагревании с водным
раствором щелочей. Реакция протекает по механизму SN1 или
SN2 в зависимости от строения галогеналкана
ОН
Br
СН 3
СН
СН 3
NaOH, Т
СН 3
CH
CH 3
+ NaBr
15
16.
СпиртыСпособы получения
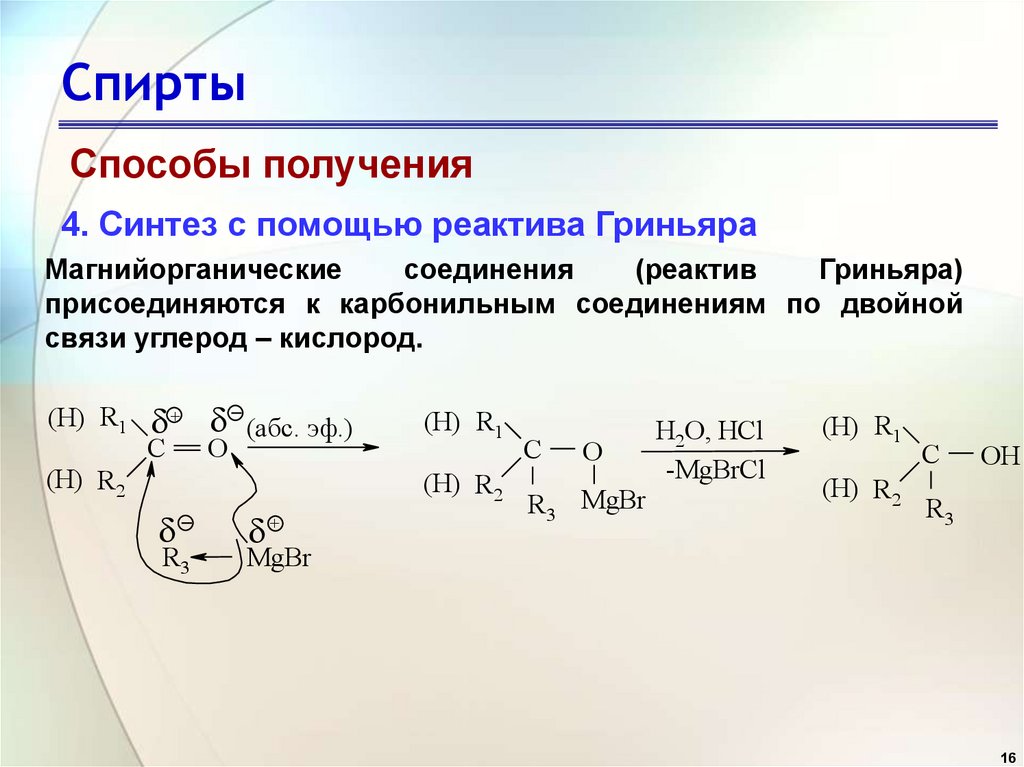
4. Синтез с помощью реактива Гриньяра
Магнийорганические
соединения
(реактив
Гриньяра)
присоединяются к карбонильным соединениям по двойной
связи углерод – кислород.
(H) R1
+
С
О
(абс. эф.)
(H) R2
(H) R1
(H) R2
R3
+
С
О
R3 MgBr
H2O, HCl
-MgBrCl
(H) R1
(H) R2
С
ОH
R3
MgBr
16
17.
СпиртыСпособы получения
4. Синтез с помощью реактива Гриньяра
Для синтеза первичных спиртов используют в качестве
карбонильного соединения муравьиный альдегид. Для
получения вторичных спиртов в качестве карбонильного
соединения используют соответствующий альдегид. В случае
синтеза третичных спиртов исходное карбонильное соединение
– кетон.
17
18.
СпиртыСпособы получения
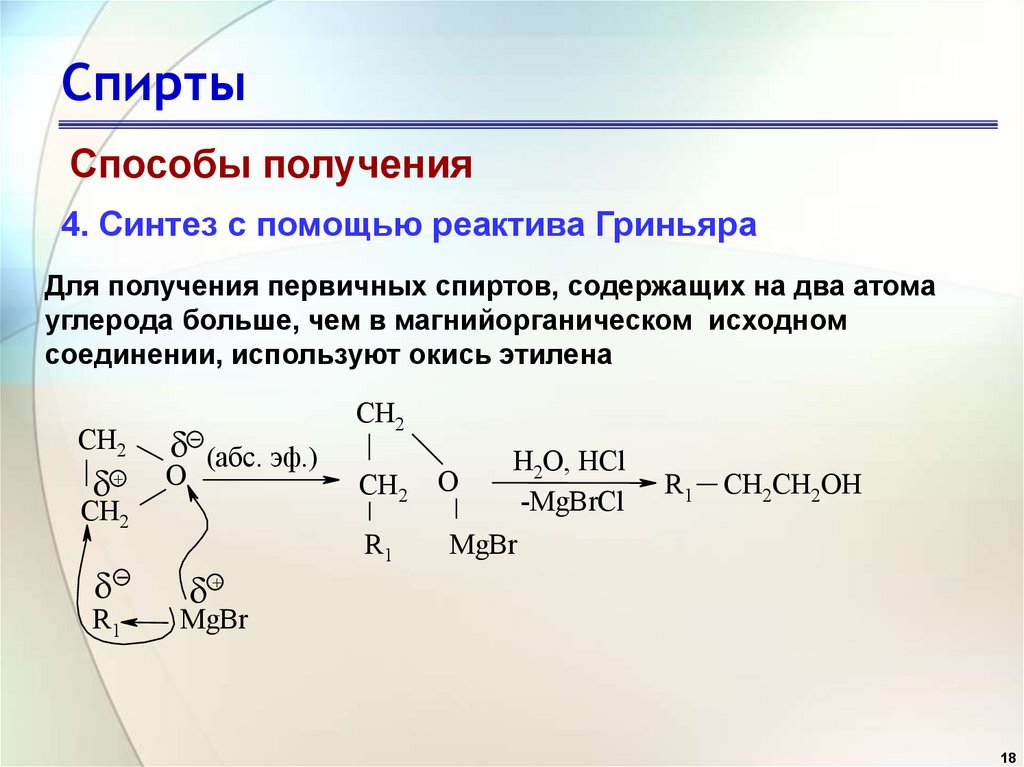
4. Синтез с помощью реактива Гриньяра
Для получения первичных спиртов, содержащих на два атома
углерода больше, чем в магнийорганическом исходном
соединении, используют окись этилена
СН2
+
О
СН2
(абс. эф.)
СН2
R1
+
СН2
R1
H2O, HCl
О
-MgBrCl
MgBr
R1
CH2СН2OH
MgBr
18
19.
СпиртыСпособы получения
5. Гидроборирование-окисление алкенов
Алкены взаимодействуют с дибораном В2Н6 с образованием
алкилборана. Диборан - димер гипотетического борана ВН3 - в
рассматриваемой реакции действует как ВН3
CH 3 CH
CH 2
ВН 3
CH 3 CH
Н
CH 2
2CH 3 CH
ВН 2
CH 2
CH 3 CH 2 CH 2 В
CH 2 CH 2 CH 3
CH 2 CH 2 CH 3
Трипропилбор
Триалкилбораны затем окисляют гидропероксидом в присутствии
щелочи
(CH 3 CH 2 CH 2)3B
H 2O 2, OH
3CH 3 CH 2 CH 2OH
+
В(ОН)3
19
20.
СпиртыСпособы получения
6. Восстановление карбонильных соединений
Альдегиды восстанавливаются в первичные спирты, кетоны –
во вторичные водородом (Ni) или с помощью алюмогидрида
лития LiAlH4, не затрагивая двойные углерод-углеродные связи.
O
CH 3 CH = CH
H 2, Ni
C
CH 3 CH 2 CH 2 CH 2OH
H
4 CH3
CH = CH
C
O
+ H
H
H
Al
+
H Li
H
OCH2
CH3
CH = CH
CH2O
Al
4 CH3
CH = CH
CH2OH
CH3
+
OCH2
OCH2
10 % H2SO4
CH = CH
CH = CH
CH = CH
+ Al+3
CH3
Li
CH3
+
Li+1
20
21.
СпиртыСпособы получения
6. Восстановление карбонильных соединений
Литийалюминийгидрид LiAlН4 – удобный, но дорогой
восстанавливающий агент, используют для синтеза спиртов,
которые менее доступны, чем карбонильные соединения.
Эта реакция представляет собой нуклеофильное присоединение:
нуклеофилом
водород, переносимый вместе с парой
..является
электронов Н
от металла на карбонильный углерод
+
С=О
H
AlH3
AN
C
H
O
3 С=О
AlH3
+
Li
C
H
+
Al Li
O
4
+
Li
Образовавшийся таким образом комплексный алкоксид алюминия подвергается
гидролитическому расщеплению
21
22.
СпиртыСпособы получения
7. Восстановление сложных эфиров
Первичные спирты также могут быть получены
восстановлением сложного эфира, при этом оба фрагмента
эфира превращаются в спирты.
H2,Ni
O
CH3(CH2)14
C
Метилпальмитат
OCH3
LiAlH4
10 % H2SO4
CH3(CH2)14
CН2ОН + СН3ОН
22
23.
СпиртыХимические свойства
1. Кислотность спиртов
В молекуле спирта содержится атом водорода, связанный с
сильно электроотрицательным кислородом, поэтому спирт
проявляет заметную кислотность.
Спирты (кроме метанола) более слабые кислоты, чем вода:
алкильная группа, проявляя электронодонорный
индукционный эффект, подает электроны на кислород R→О ,
увеличивает на нем отрицательный заряд (по сравнению с
зарядом на гидроксид-ионе) и делает алкоксид-ион R→О
(сопряженное основание) более сильным, а кислоту - более
слабой.
23
24.
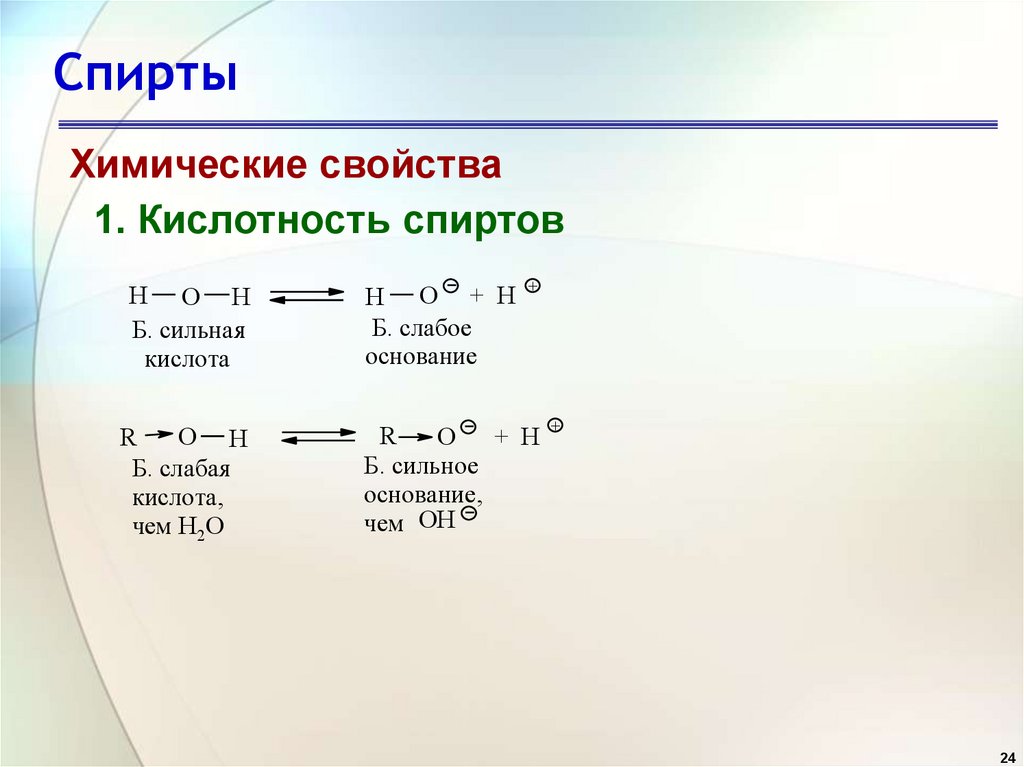
СпиртыХимические свойства
1. Кислотность спиртов
Н О Н
Б. сильнаяя
кислота
O H
R
Б. слабая
кислота,
чем Н2О
Н О + Н
Б. слабое
основание
+
R
O
+ H
Б. сильное
основание,
чем ОН
+
24
25.
СпиртыХимические свойства
1. Кислотность спиртов
Алкоксиды (алкоголяты) нельзя получить реакцией спирта с
гидроксидами металлов, их синтезируют реакцией спирта с
активным металлом (Na, K, Mg, Al и др.).
+
Na
OH
+ RO H
Б. слабое
Б. слабая
основание
кислота
R O-H
+
Na
RO
Na
Б. сильное
основание
RO
Na
+
+
Н OH
Б. сильнаяя
кислота
+
+ 1/2H 2
25
26.
СпиртыКислотность спиртов
Кислотность спиртов в водных растворах
R OH
R
O
+
pKa
трет-Бутанол
18,0
Этанол
15,9
Метанол
15,5
Вода
15,7
FCH2CH2OH
13,9
CF3CH2OH
12,4
(CF3)3COH
5,0
+
H
Ka
[RO ][H ]
[ROH]
pKa=-lgKa
26
27.
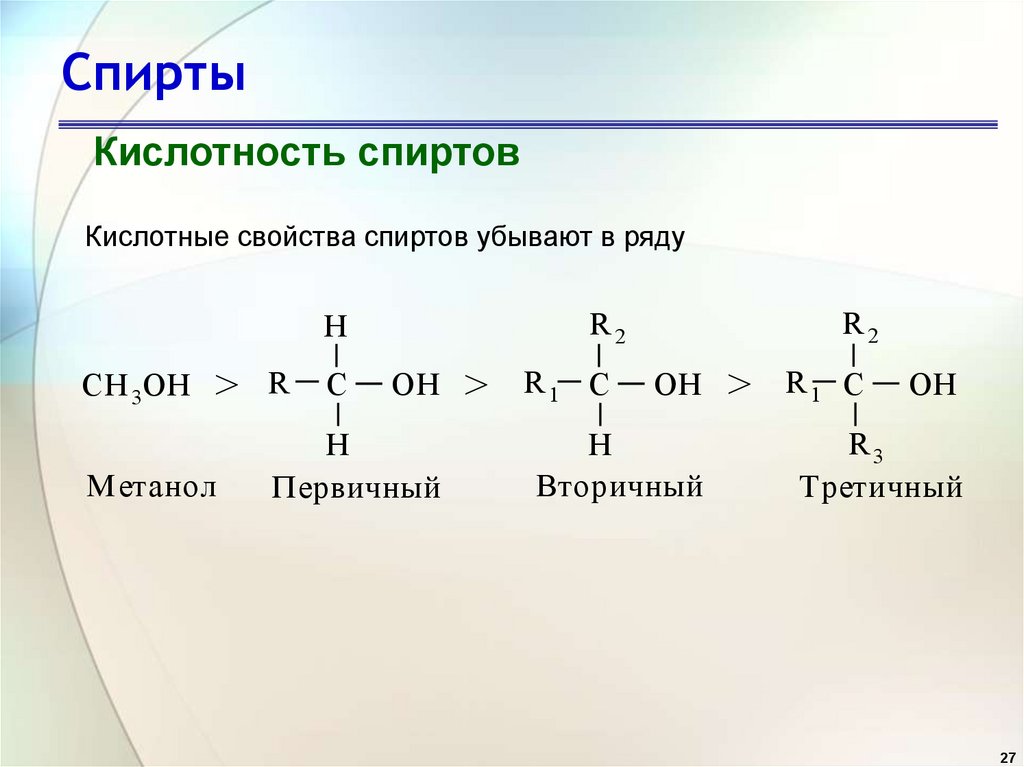
СпиртыКислотность спиртов
Кислотные свойства спиртов убывают в ряду
CH 3OH
>
Метанол
R
C
R2
R2
H
OH
H
Первичный
>
R1 C
OH
H
Вторичный
>
R1 C
OH
R3
Третичный
27
28.
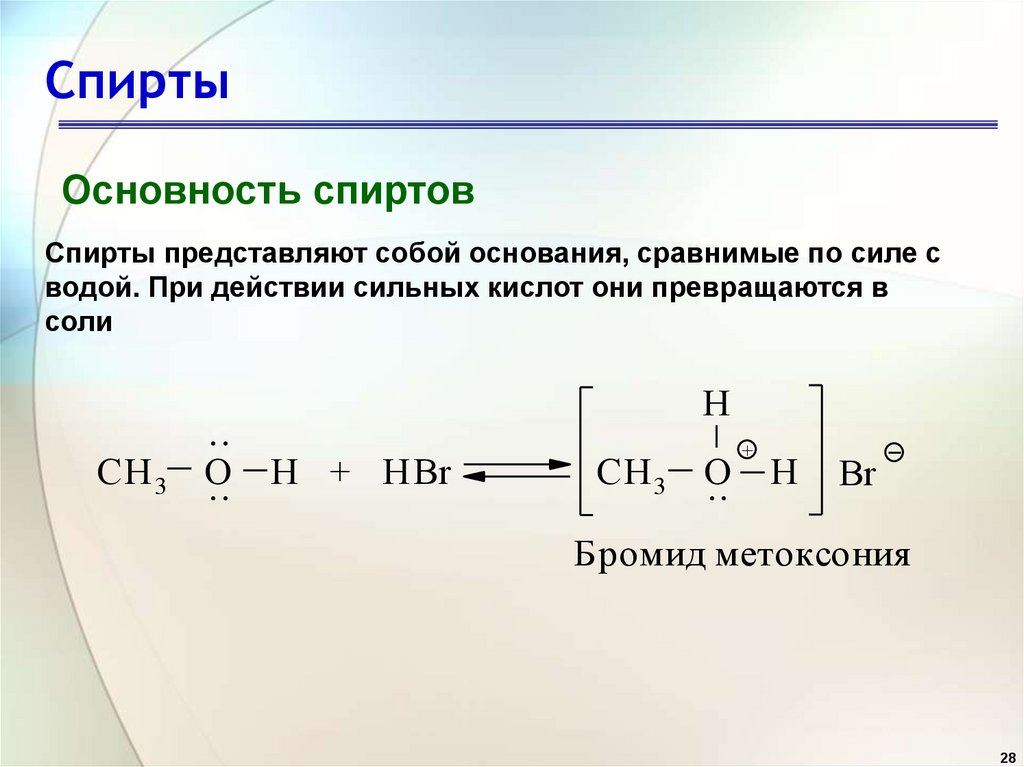
СпиртыОсновность спиртов
Спирты представляют собой основания, сравнимые по силе с
водой. При действии сильных кислот они превращаются в
соли
СН 3
..
О
.. Н + HBr
H
CH 3
O
..
+
H
Br
Бромид метоксония
28
29.
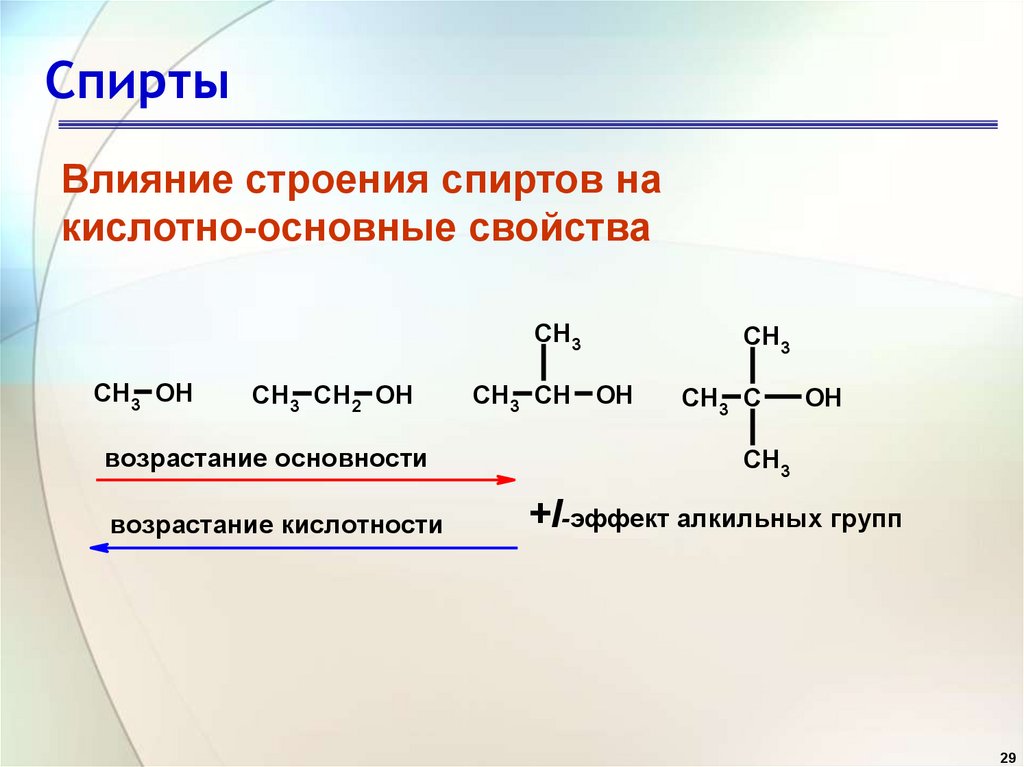
СпиртыВлияние строения спиртов на
кислотно-основные свойства
CH3
CH3 OH
CH3 CH2 OH
возрастание основности
возрастание кислотности
CH3 CH OH
CH3
CH3 C
OH
CH3
+I-эффект алкильных групп
29
30.
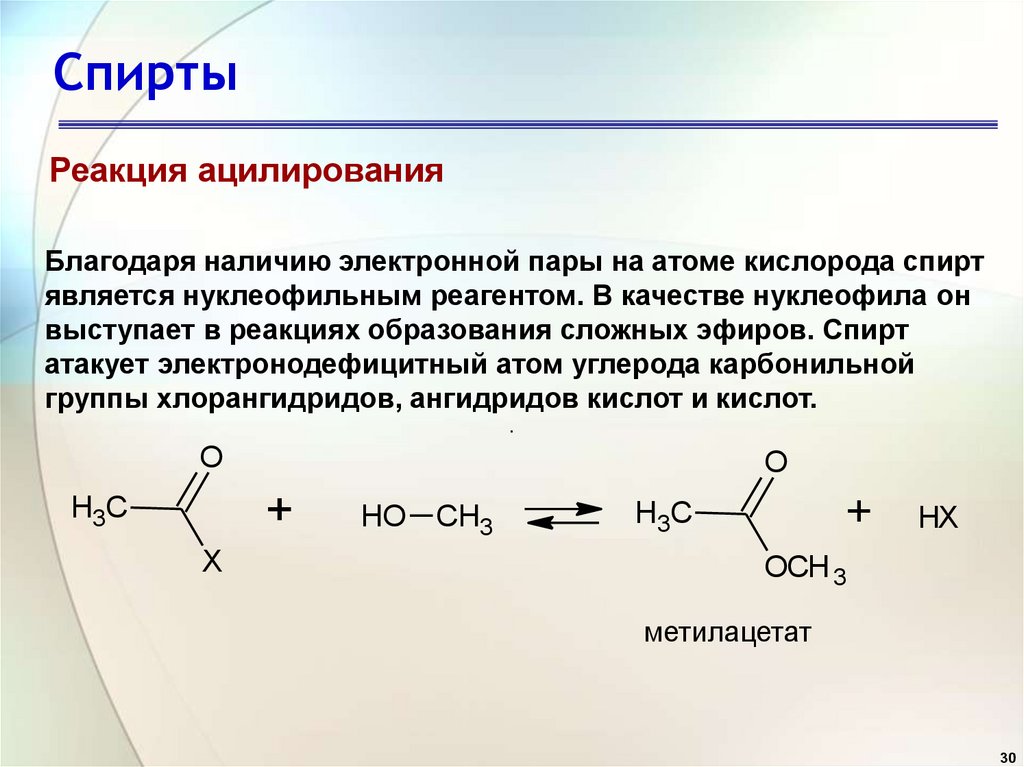
СпиртыРеакция ацилирования
Благодаря наличию электронной пары на атоме кислорода спирт
является нуклеофильным реагентом. В качестве нуклеофила он
выступает в реакциях образования сложных эфиров. Спирт
атакует электронодефицитный атом углерода карбонильной
группы хлорангидридов, ангидридов кислот и кислот.
.
O
O
+
H3C
Х
HO CH3
+
H3C
НХ
OCH 3
метилацетат
30
31.
СпиртыРеакция ацилирования
X=
-Cl
O
O C
Хлорангидриды карбоновых кислот
Ангидриды карбоновых кислот
CH3
-OH
Карбоновые кислоты
.
С карбоновыми кислотами спирты реагируют в присутствии
кислотных катализаторов, которые увеличивают поляризацию,
а, следовательно, и реакционную способность карбонильной
групп, Эта реакция называется реакцией этерификации
Это реакция нуклеофильного замещения (SN), протекающая
через стадии нуклеофильного присоединения и отщепления
(AdN, E).
31
32.
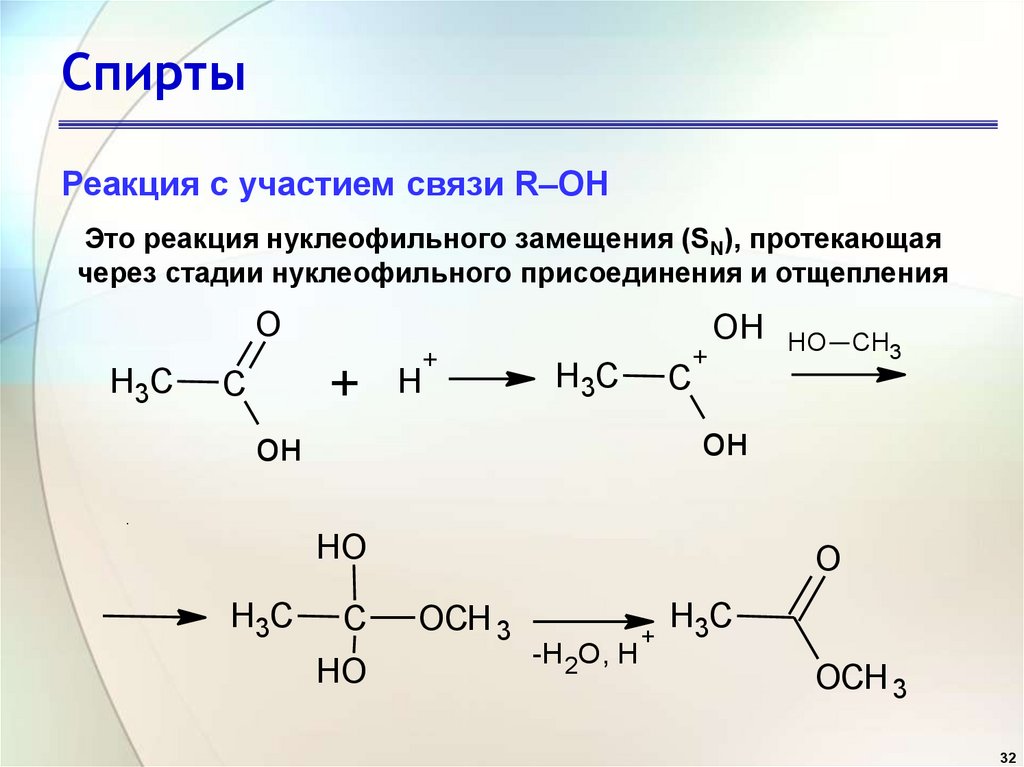
СпиртыРеакция с участием связи R–OH
Это реакция нуклеофильного замещения (SN), протекающая
через стадии нуклеофильного присоединения и отщепления
O
H3C
OH
+
C
+
H
+
H3C
HO CH3
C
он
он
.
HO
H3C
C
HO
O
OCH 3
-H 2O, H
+
H3C
OCH 3
32
33.
СпиртыРеакции нуклеофильного замещения
Реакции с галогеноводородами, образование алкилгалогенидов
Спирты легко реагируют с галогеноводородами (HCl, HBr, HI).
Реакционная способность падает в ряду
НI > HBr > HCl.
ROH
+
RХ
HX
+ H 2O
Сухой газообразный галогеноводород пропускают в спирт или спирт
нагревают с концентрированным раствором галогеноводорода.
Реакция катализируется кислотами. Спирт, присоединяя протон,
превращается в ион алкилоксония, который гораздо легче отщепляет
нейтральную молекулу воды (“хорошая” уходящая группа), чем спирт
– ион ОН (“плохая” уходящая группа).
R
..
OH
H
+
+
HX
H
X
R
..O
+
R O
.. H + X
Ион алкилоксония
H
X
R
+ H 2O
33
34.
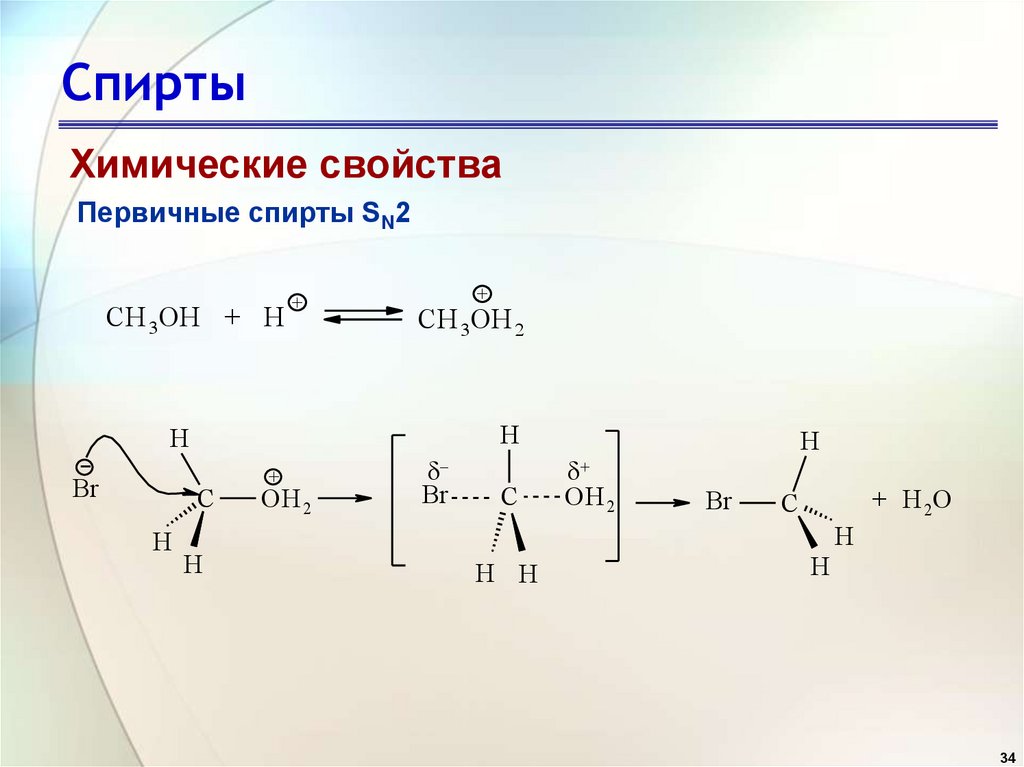
СпиртыХимические свойства
Первичные спирты SN2
CH 3OH + H
+
+
CH 3OH 2
H
H
Br
C
H
H
+
OH 2
Br
C
H
OH 2
Br
+ H 2O
C
H
H H
H
34
35.
СпиртыХимические свойства
Вторичные и третичные спирты SN1
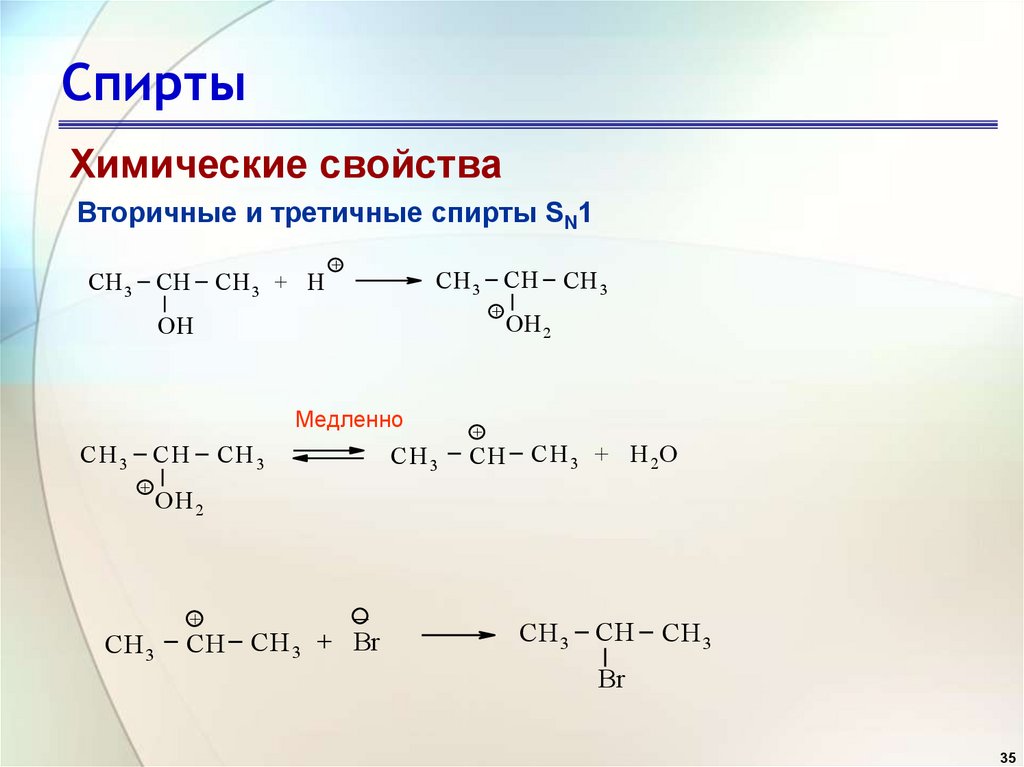
СH 3 CH
СH 3 + H
+
СH 3 CH
+
OH
Медленно
CH
СH 3
+
СH 3
СH 3
СH 3
+
СH 3
OH 2
CH
СH 3 + H 2O
OH 2
+
_
CH СH 3 + Br
СH 3 CH
СH 3
Br
35
36.
СпиртыХимические свойства
Вторичные и третичные спирты SN1
Поскольку реакции замещения у вторичных и третичных спиртов
протекают через стадию образования карбониевого иона, возможна
перегруппировка.
СH 3
СH 3
СH 3
CH
CH
СH 3
HI
OH
3-Метил-2-бутанол
C
CH 2
СH 3 + H 2O
I
2-Метил-2-иодбутан
CH 3
CH 3
CH 3
СH 3
C
CH
H
OH 2
+
CH 3
CH 3
C
+
CH
CH 3 + H 2O
CH 3
H
I
Перегруппировка CH
C
CH
CH
3
2
3
+
Перенос
Третичный карбокатион
гидрид-иона Н
более устойчив
CH 3
CH 3
C
CH 2
CH 3
I
36
37.
СпиртыХимические свойства
Реакционная способность спиртов по отношению
галогенводородам изменяется следующим образом:
к
Бензиловый, аллиловый > трет- > втор- > первичный < метанол
SN1
Устойчивость карбокатионов увеличивается,
реакционная способность
возрастает
SN2
Пространственные
препятствия для атаки
реакционного центра
уменьшаются,
реакционная
способность
увеличивается
37
38.
СпиртыРеакции нуклеофильного замещения
Реакция с галогенидами фосфора PCl5, PCl3, PBr3, PI3,
тионилхлоридом SOCl2.
Для получения алкилгалогенидов используют реакции спиртов с
галогенидами фосфора и тионилхлоридом, они не сопровождаются
перегруппировками
СН3 Br
СН3 ОН
3СН3 СН СН СН3
3-Метил-2-бутанол
+ PBr3
3СН3
СН3
+ P(OH)3
СН3 Cl
+ PCl5
СН3
СН
СН
СН3
+ POCl3 + HCl
2-Хлор-3-метилбутан
СН3 Cl
СН3 ОН
СН3 СН СН СН3
3-Метил-2-бутанол
СН
2-Бром-3-метилбутан
СН3 ОН
СН3 СН СН СН3
3-Метил-2-бутанол
СН
+ SOCl2
СН3
СН
СН
СН3
+ SO2 + HCl
2-Хлор-3-метилбутан
38
39.
СпиртыРеакции нуклеофильного замещения
Межмолекулярная дегидратация спиртов. Получение
простых эфиров
СH3СH2OH + HOCH2CH3
H
+
СH3СH2
O
CH2CH3 + H2O
Диэтиловый эфир
Межмолекулярная дегидратация спиртов в присутствии
каталитических количеств кислоты служит примером
нуклеофильного замещения, в котором субстратом является
протонированная молекула спирта, а другая молекула ROH
служит нуклеофилом
39
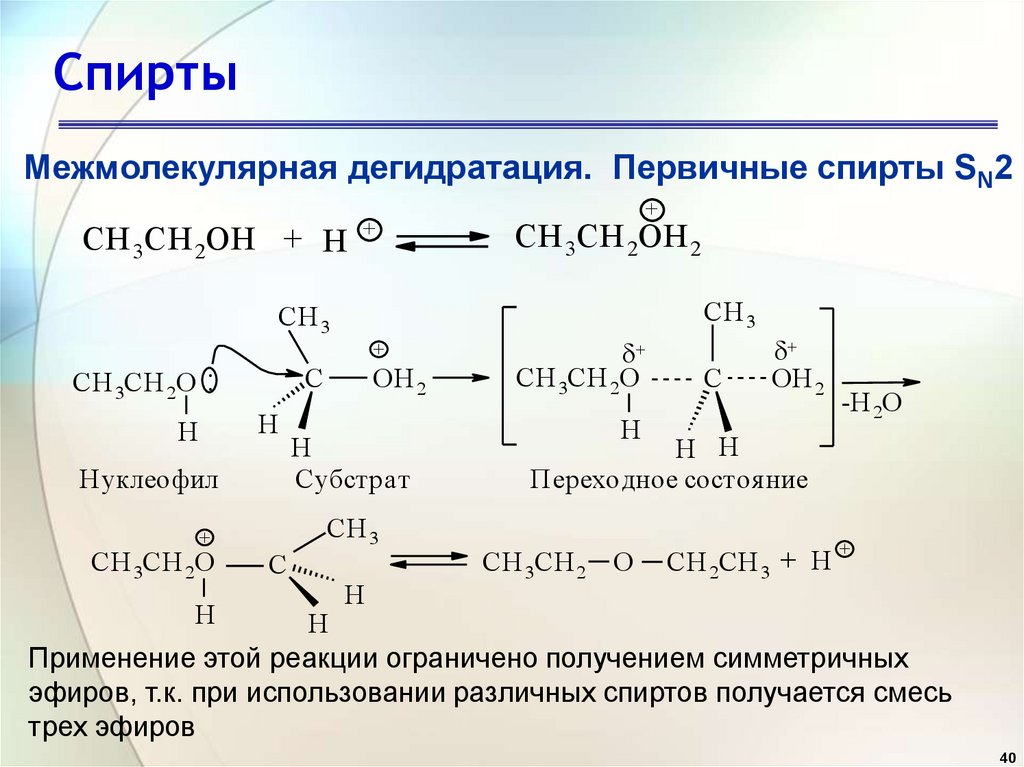
40.
СпиртыМежмолекулярная дегидратация. Первичные спирты SN2
СH 3СH 2OH + H
+
+
:
Нуклеофил
H
H
Субстрат
CH 3
+
CH 3CH 2O
OH 2
C
H
H
C
СH 3СH 2OH 2
CH 3
CH 3
CH 3CH 2O
+
H
CH 3CH 2O
C
OH 2
H
-H 2O
H H
Переходное состоя ние
CH 3CH 2
O
CH 2CH 3 + H
+
H
Применение этой реакции ограничено получением симметричных
эфиров, т.к. при использовании различных спиртов получается смесь
трех эфиров
40
41.
СпиртыПолучение простых эфиров. Синтез А.Вильямсона.
Важным методом получения простых эфиров
реакция
алкоголятов
с
алкилгалогенидами
Вильямсона) или алкилсульфатами ROSO2OR.
+
С2Н5О Na
+
+ CH3I
SN2
является
(синтез
C2H5OCH3 + NaI
Метилэтиловый
эфир
C6H5-O Na + H3C-OSO2O-C6H4CH3-п
C6H5-O-CH3 + п-CH3C6H4SO2O Na
41
42.
СпиртыОбразование алкенов – внутримолекулярная
дегидратация
Спирт превращается в алкен при температуре ~ 200 оС в
присутствии серной или фосфорной кислоты, либо при
пропускании паров спирта над окисью алюминия (Al2O3 - кислота
Льюиса) при температуре 300-350 оС.
42
43.
СпиртыОбразование алкенов – внутримолекулярная
дегидратация
Механизм дегидратации Е1
Первая стадия
CH 3
CH 3
..
CH 2OH + H
+
CH 3
H
.. +
CH 2OH
Протонированный спирт
оксоний-ион
H
.. + Медленно
CH 2OH
+
CH 3 CH 2 + H 2O
43
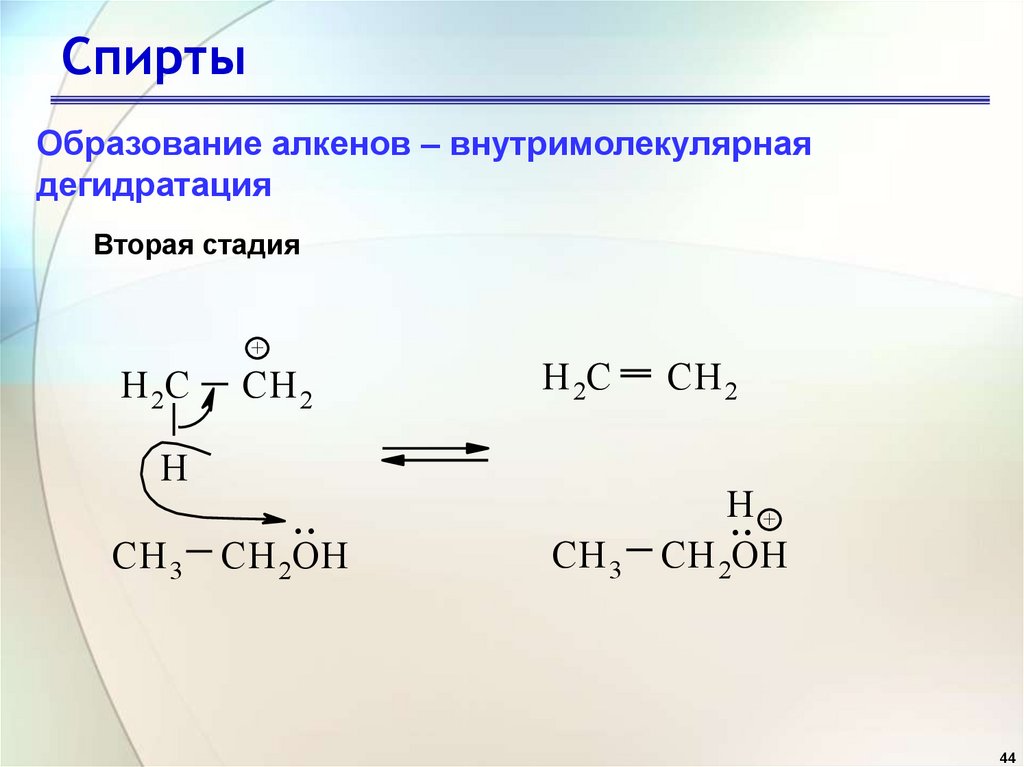
44.
СпиртыОбразование алкенов – внутримолекулярная
дегидратация
Вторая стадия
+
H 2C
CH 2
H 2C
CH 2
CH 3
H
.. +
CH 2OH
H
..
CH 3 CH 2OH
44
45.
СпиртыОбразование алкенов – внутримолекулярная
дегидратация
В отличие от галогеналканов, которые
подвергаются элиминированию в основном
по Е2-механизму, спирты реагируют только по
механизму Е1. Элиминирование Е2 требует
присутствия
сильного
основания
для
отщепления протона, но кислая среда,
необходимая для протонирования спирта, и
сильное основание не совместимы.
45
46.
СпиртыОбразование алкенов – внутримолекулярная
дегидратация
Ориентация. Элиминирование спиртов происходит с
образованием более устойчивого, т.е. более
алкилированного алкена (правило Зайцева).
CH 3
CH 2
CH
OH
CH 3
H 2SO 4, T
CH CH CH 3 + H 2O
2-Бутен
(основной продукт)
CH 3
46
47.
СпиртыОбразование алкенов – внутримолекулярная
дегидратация
Перегруппировка.
CH 3 CH 2 CH 2 CH 2 OH
+
H
+
+
CH 3 CH 2 CH 2 CH 2 OH 2
+
+
CH 3 CH 2
CH 2 CH 2 OH 2
CH 3 CH 2 CH 2 CH 2 +
Первичный карбокатион
H 2O
+
CH 3 CH
H
+
CH
CH 3
CH 3 CH
..
CH 3 CH 2 CH 2 CH 2 OH
Перегруп- CH 3 CH 2 CH CH 3
пировка Вторичный карбокатион
б. устойчив
CH CH 3
+
CH 3
CH 2 CH 2 CH 2 OH 2
47
48.
СпиртыРеакции окисления
Первичные спирты можно окислить до альдегидов действием
К2Сr2О7, если одновременно с окислением вести отгонку легко
окисляющихся альдегидов, которые кипят при более низкой
температуре, чем исходные спирты
O
Отгонка [O]
CH 3
CH CH 2
CH 2
OH
CH 3
K2 Cr2 O7 , H2 SO4
K2 Cr2 O7 , H2 SO4
CH 3
CH CH 2
COO K
СH 3
Cоль растворима в воде
C
H
СH 3
Изовалериановый альдегид
Т к = 92,5 o C
СH 3
Изопентиловый спирт
Т к = 130,5 o C
[O]
CH CH 2
+
H
O
+
CH 3
CH CH 2
C
ОH
СH 3
Изовалериановая кислота
не растворима в воде
При нагревании первичных спиртов с водным
перманганата калия получают карбоновые кислоты.
раствором
48
49.
СпиртыРеакции окисления
Вторичные спирты окисляются до кетонов действием
перманганата калия или хромовой кислотой.
CH 3 CH
CH 3
OH
Изопропиловый
спирт
[O]
K 2Cr 2O 7, H 2SO 4
CH 3 C
CH 3
O
Ацетон
Дальнейшее окисление кетона возможно только в жестких
условиях, т.к. при этом происходит разрыв углерод-углеродной
связи.
49
50.
СпиртыРеакции окисления
Третичные спирты в присутствии кислот превращаются в
алкены, которые далее легко окисляются. В щелочной и
нейтральной средах третичные спирты не окисляются.
50
51.
СпиртыДегидрирование
Превращение первичных спиртов в альдегиды, вторичных – в
кетоны можно осуществлять, нагревая пары спирта до
температуры 200-300 оС, над медным катализатором – реакция
дегидрирования.
H
CH 3
C
Н
O
Н
Сu, Т
СН 3
O
CH 3
C
+ Н 2,
Н
CH 3
C
H
O
Н
Сu, Т
CH 3
C
CH 3 + Н 2
O
51
52.
СпиртыЗамещение гидроксигруппы на водород
Спирты устойчивы к действию химических восстановителей. Они
не восстанавливаются и водородом над катализаторами.
Поэтому они часто используются в качестве растворителей при
восстановлении. Методы непрямого восстановления спиртов
основаны на превращении спиртов в соединения других классов,
способных восстанавливаться до углеводородов
CH3CH2CH2OH
R-OH
HI
H2SO4, t
R-I
HI
CH3CH=CH2
H2/ Pt
CH3CH2CH3
R-H + I2
52
53.
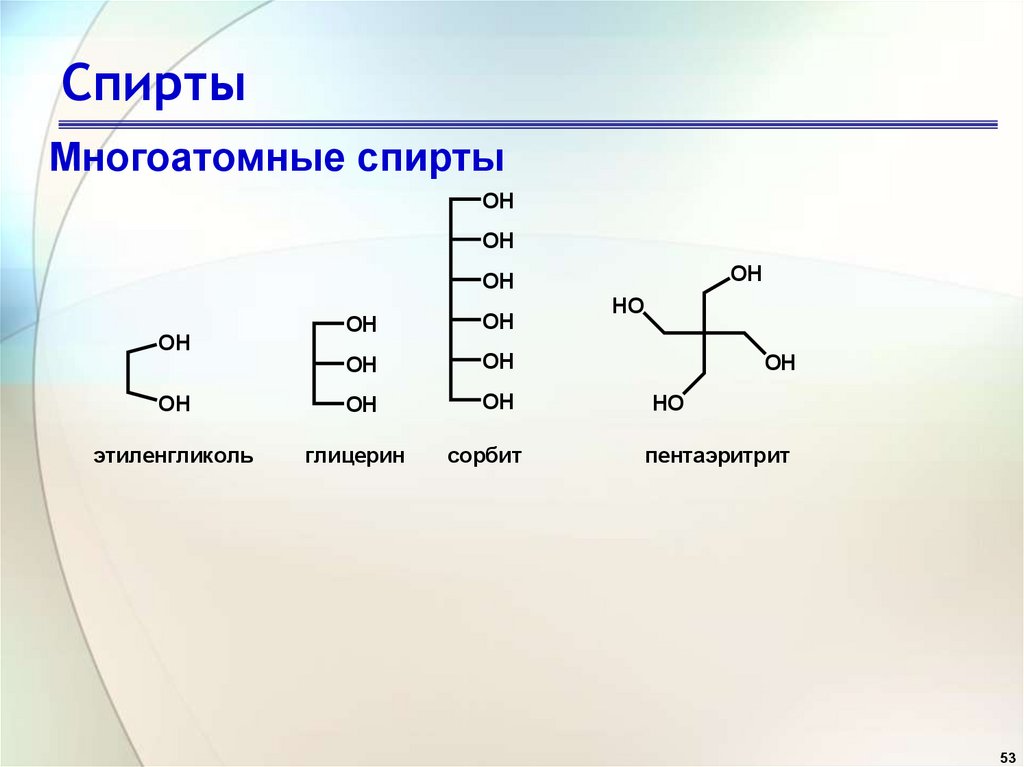
СпиртыМногоатомные спирты
OH
OH
OH
OH
OH
OH
этиленгликоль
OH
OH
OH
OH
OH
OH
глицерин
сорбит
HO
OH
HO
пентаэритрит
53
54.
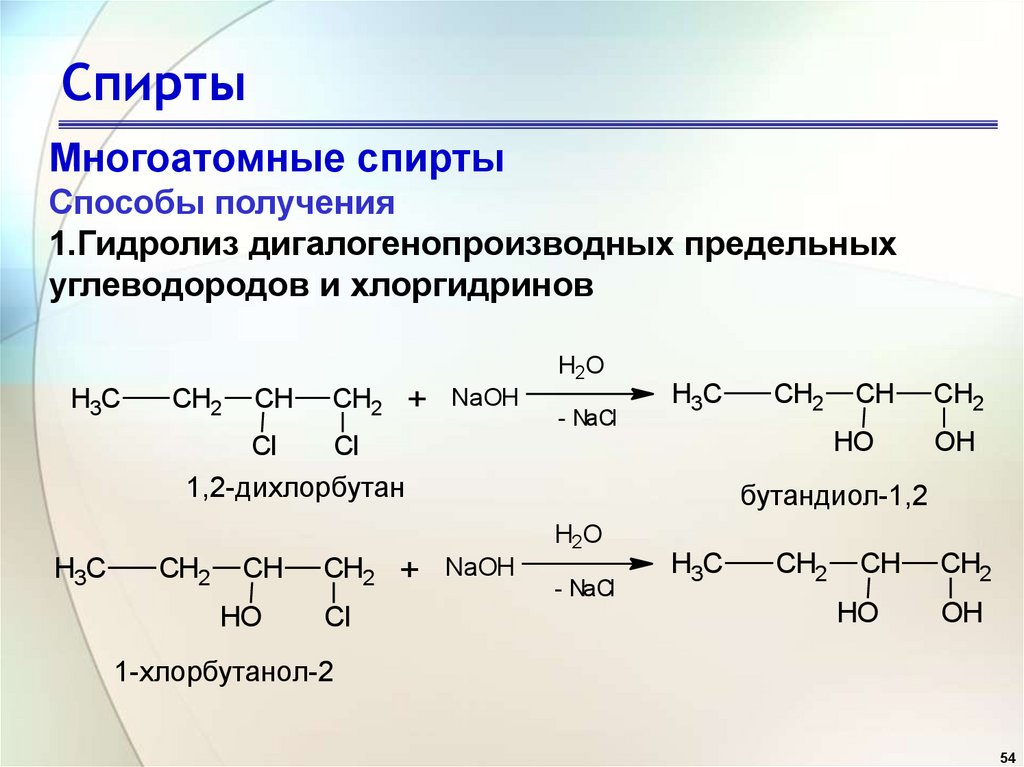
СпиртыМногоатомные спирты
Способы получения
1.Гидролиз дигалогенопроизводных предельных
углеводородов и хлоргидринов
H2O
H3C
CH2
CH
CH2 + NaOH
Cl
Cl
- NaCl
H3C
CH2
CH
HO
1,2-дихлорбутан
CH2
OH
бутандиол-1,2
H2O
H3C
CH2
CH
HO
CH2 + NaOH
Cl
- NaCl
H3C
CH2
CH
HO
CH2
OH
1-хлорбутанол-2
54
55.
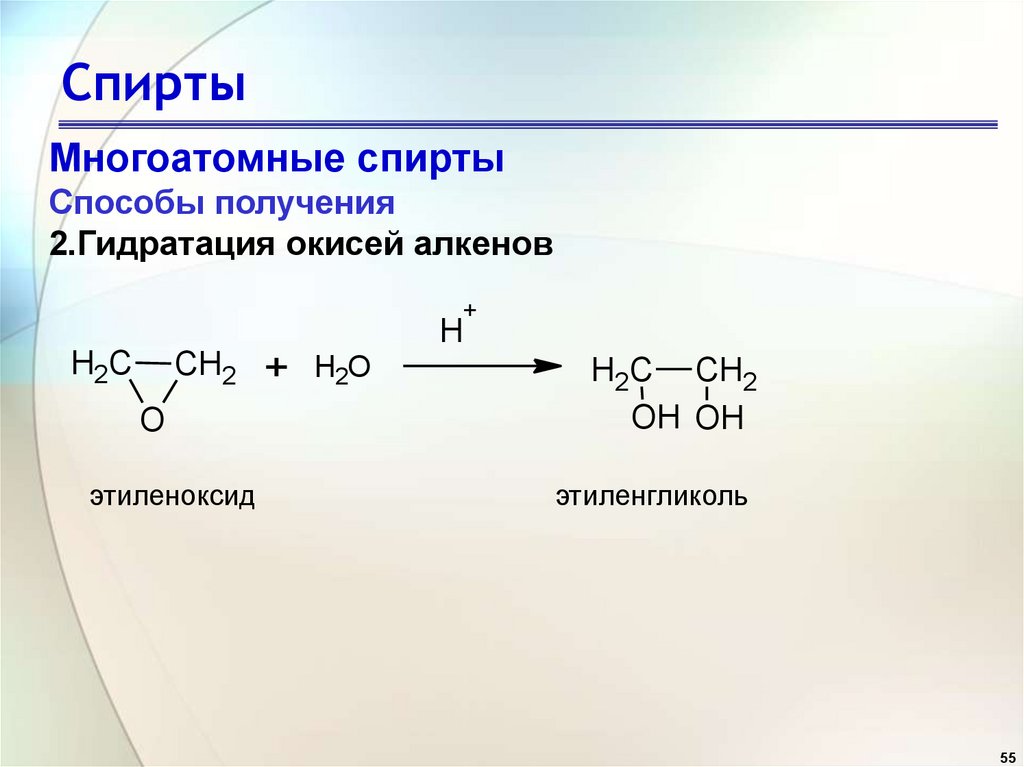
СпиртыМногоатомные спирты
Способы получения
2.Гидратация окисей алкенов
+
H
H2C
CH2 + H2O
O
этиленоксид
H2C CH2
OH OH
этиленгликоль
55
56.
СпиртыМногоатомные спирты
Способы получения
3.Окисление алкенов по Вагнеру
Под действием холодного разбавленного раствора
(5-10%) перманганата калия из алкенов получают
гликоли
R1
CH
CH
R2 + KMnO 4 + H2O
R1 HC
OH
CH
R2 + MnO 2 + KOH
OH
56
57.
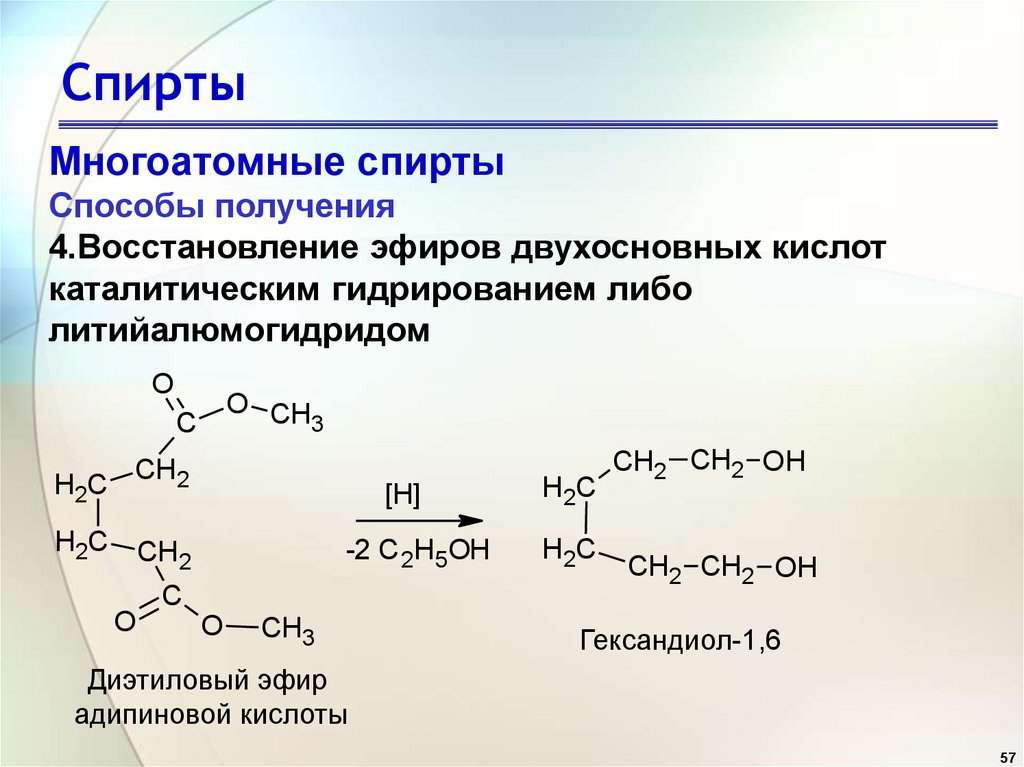
СпиртыМногоатомные спирты
Способы получения
4.Восстановление эфиров двухосновных кислот
каталитическим гидрированием либо
литийалюмогидридом
O
O CH
3
C
H2C
CH2
[H]
H2C CH
2
O
-2 C 2H5OH
C
O
CH3
H2C
H2C
CH2 CH2 OH
CH2 CH2 OH
Гександиол-1,6
Диэтиловый эфир
адипиновой кислоты
57
58.
СпиртыМногоатомные спирты
Способы получения
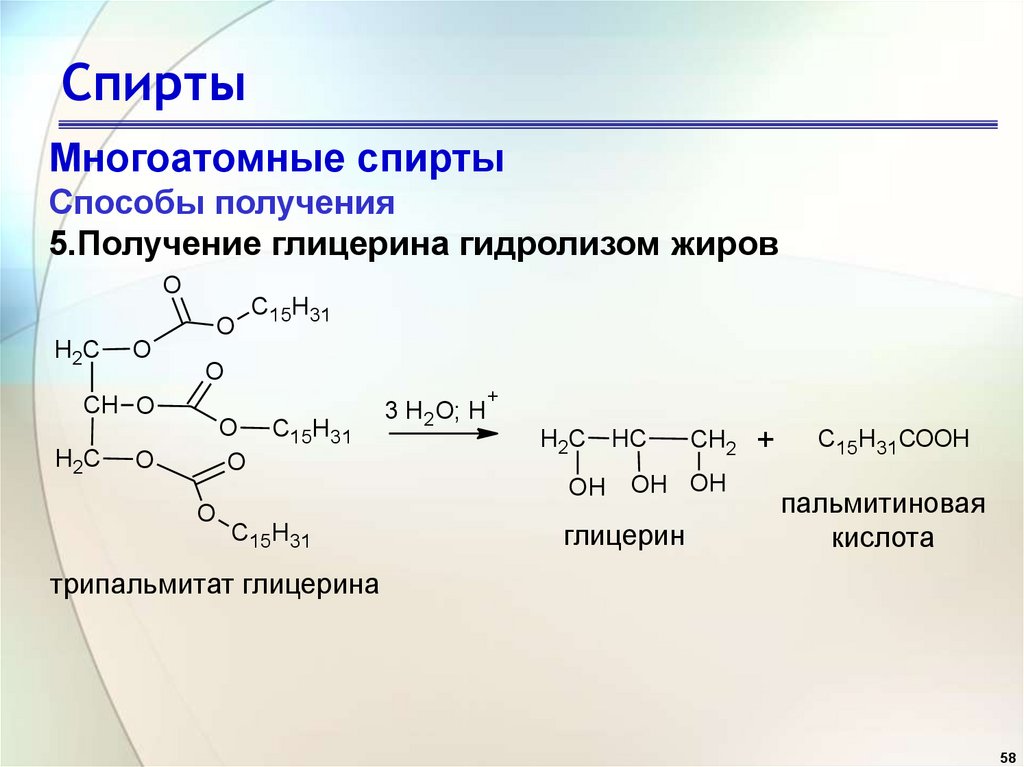
5.Получение глицерина гидролизом жиров
O
O
H2C
O
O
CH O
H2C
C15H31
O
O
O
O
C15H31
C15H31
3 H 2O; H
+
H2C
HC
CH2
OH OH OH
глицерин
+
C15H31COOH
пальмитиновая
кислота
трипальмитат глицерина
58
59.
СпиртыМногоатомные спирты
Способы получения
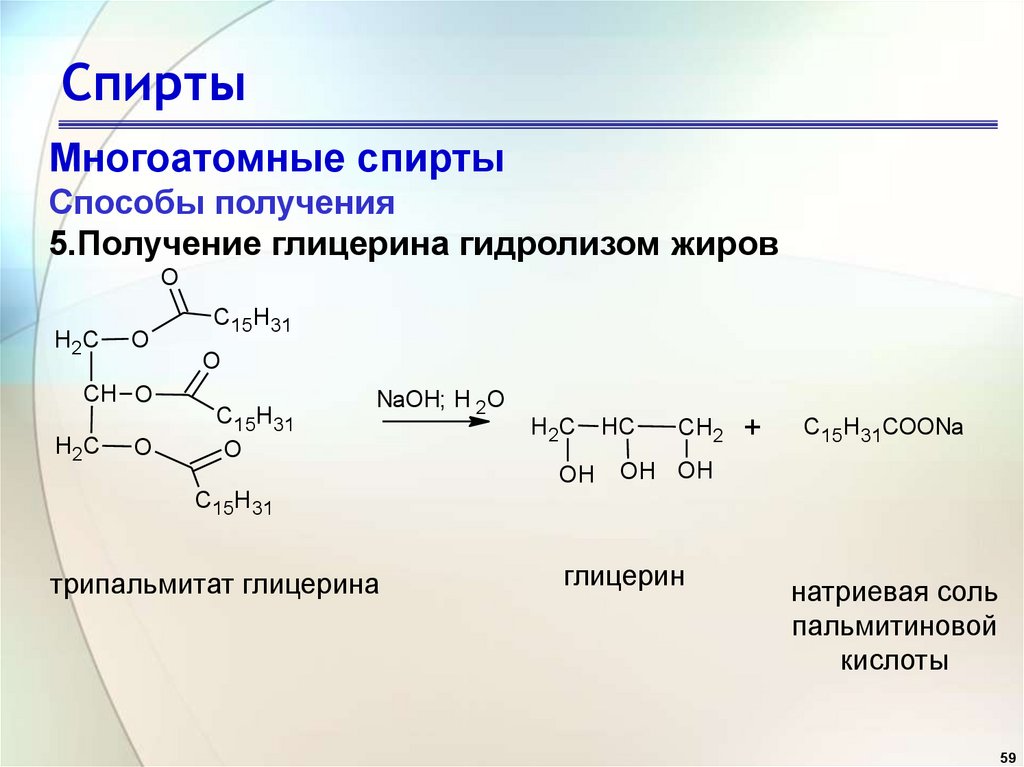
5.Получение глицерина гидролизом жиров
O
H2C
O
CH O
H2C
O
C15H31
O
C15H31
O
NaOH; H 2O
H2C
OH
HC
CH2
+
C15H31COONa
OH OH
C15H31
трипальмитат глицерина
глицерин
натриевая соль
пальмитиновой
кислоты
59
60.
СпиртыМногоатомные спирты
Получение синтетического глицерина из пропилена
CH2=CH-CH3
Cl2, 400o
NaOH, H2O
CH2=CH-CH2 Cl
хл. аллил
CH2=CH-CH2 OH
аллиловый спирт
Cl2, H2 O
CH2 Cl-CH(OH)-CH2 Cl
H2 O2, H2 O
NaOH, H2O
HOCH2 -CH(OH)-CH2 OH
Глицерин используется в пищевой и парфюмерной
промышленности, для получения полимеров и др.
60
61.
СпиртыМногоатомные спирты. Химические свойства
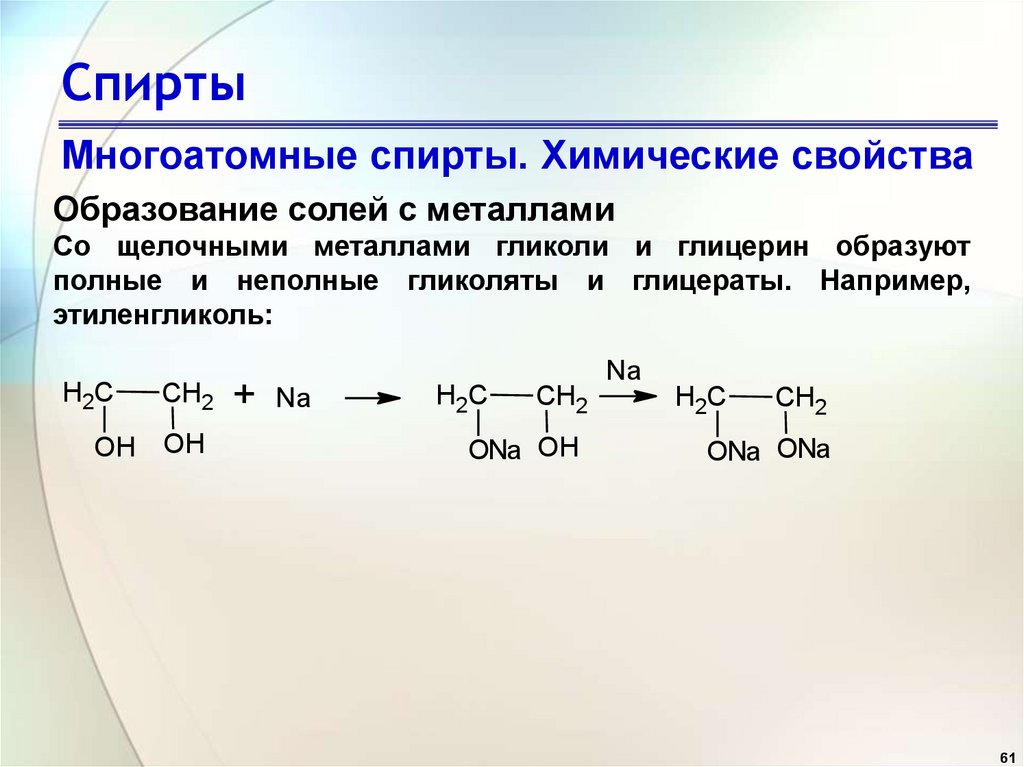
Образование солей с металлами
Со щелочными металлами гликоли и глицерин образуют
полные и неполные гликоляты и глицераты. Например,
этиленгликоль:
H2C
CH2
OH OH
+
Na
H2C
Na
CH2
ONa OH
H2C
CH2
ONa ONa
61
62.
СпиртыМногоатомные спирты. Химические свойства
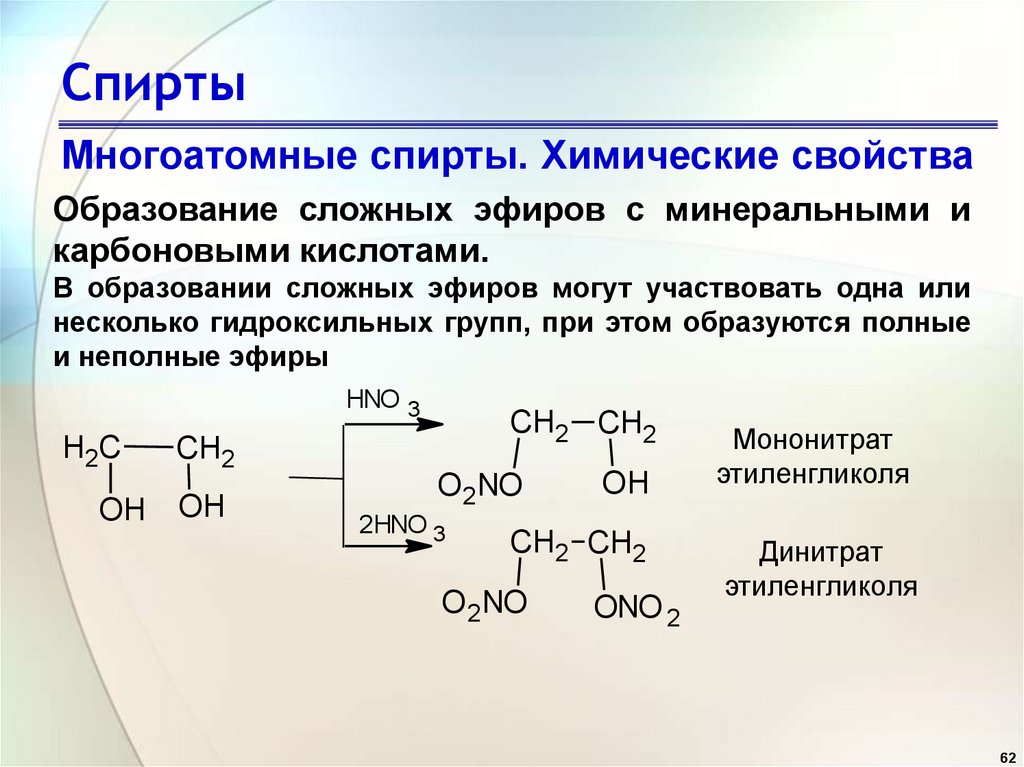
Образование сложных эфиров с минеральными и
карбоновыми кислотами.
В образовании сложных эфиров могут участвовать одна или
несколько гидроксильных групп, при этом образуются полные
и неполные эфиры
HNO 3
H2C
CH2 CH2
CH2
OH OH
O 2NO
2HNO 3
OH
CH2 CH2
O2NO
ONO 2
Мононитрат
этиленгликоля
Динитрат
этиленгликоля
62
63.
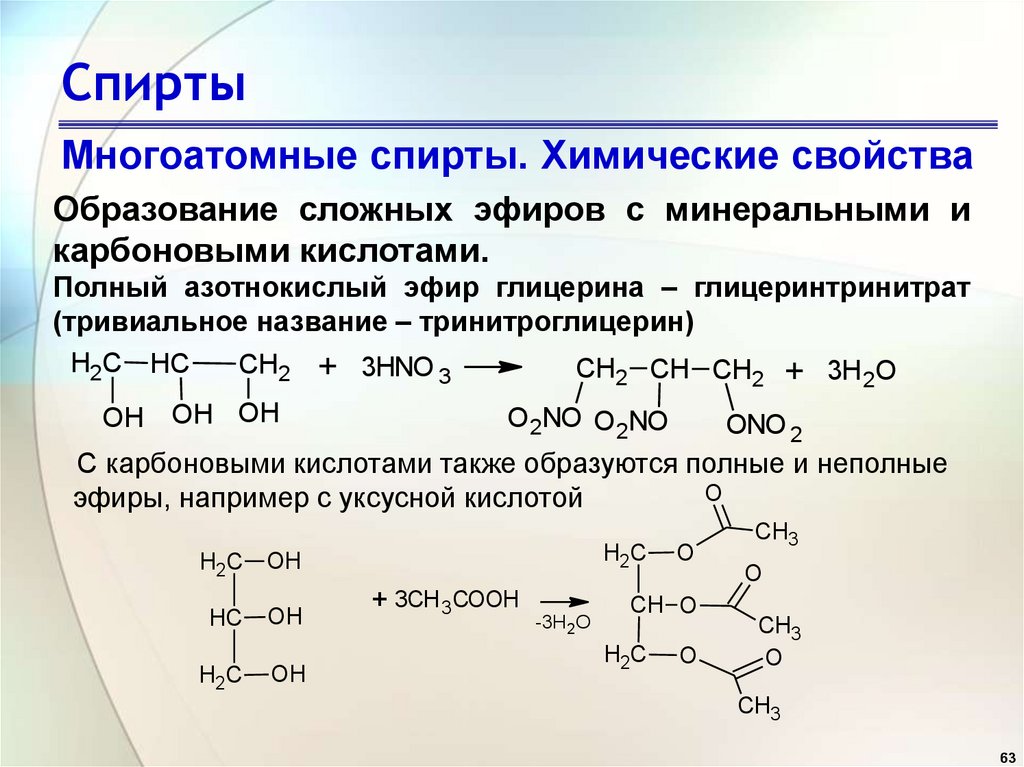
СпиртыМногоатомные спирты. Химические свойства
Образование сложных эфиров с минеральными и
карбоновыми кислотами.
Полный азотнокислый эфир глицерина – глицеринтринитрат
(тривиальное название – тринитроглицерин)
H2C HC
CH2 + 3HNO 3
CH2 CH CH2 + 3H 2O
OH OH OH
O2NO O2NO
ONO 2
С карбоновыми кислотами также образуются полные и неполные
O
эфиры, например с уксусной кислотой
H2C
OH
HC
OH
H2C
OH
H2C
+ 3CH 3COOH
-3H2O
O
CH O
H2C
O
CH3
O
CH3
O
CH3
63
64.
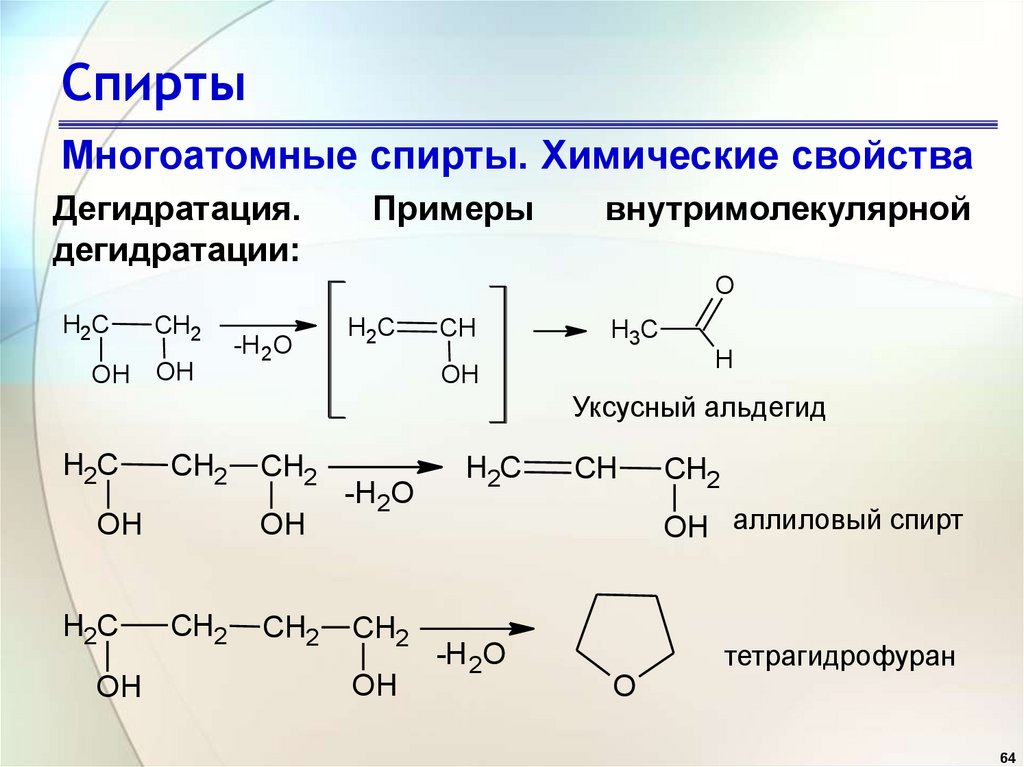
СпиртыМногоатомные спирты. Химические свойства
Дегидратация.
дегидратации:
Примеры
внутримолекулярной
O
H2C
CH2
OH OH
-H 2O
H2C
CH
H3C
H
OH
Уксусный альдегид
H2C
CH2
OH
H2C
OH
CH2
OH
CH2
CH2
-H 2O
CH2
OH
H2C
CH
CH2
OH аллиловый спирт
-H 2O
тетрагидрофуран
O
64
65.
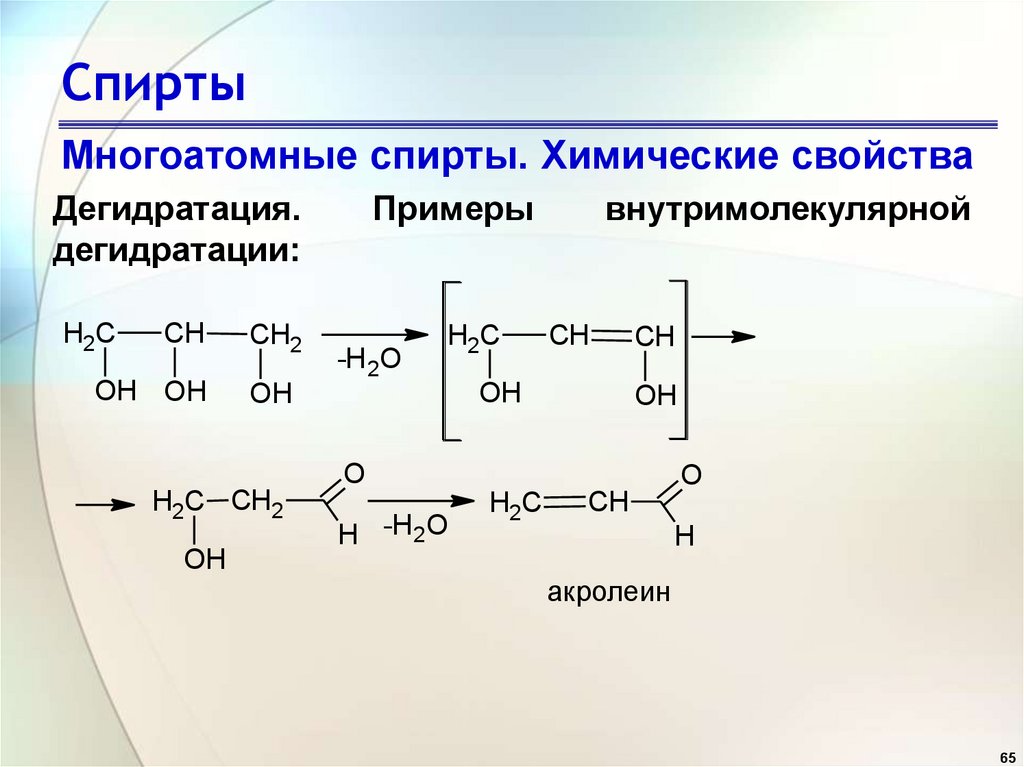
СпиртыМногоатомные спирты. Химические свойства
Дегидратация.
дегидратации:
H2C
CH
OH OH
CH2
Примеры
-H 2O
H2C
внутримолекулярной
CH
OH
OH
CH
OH
O
H2C CH2
OH
H -H 2O
O
H2C
CH
H
акролеин
65
66.
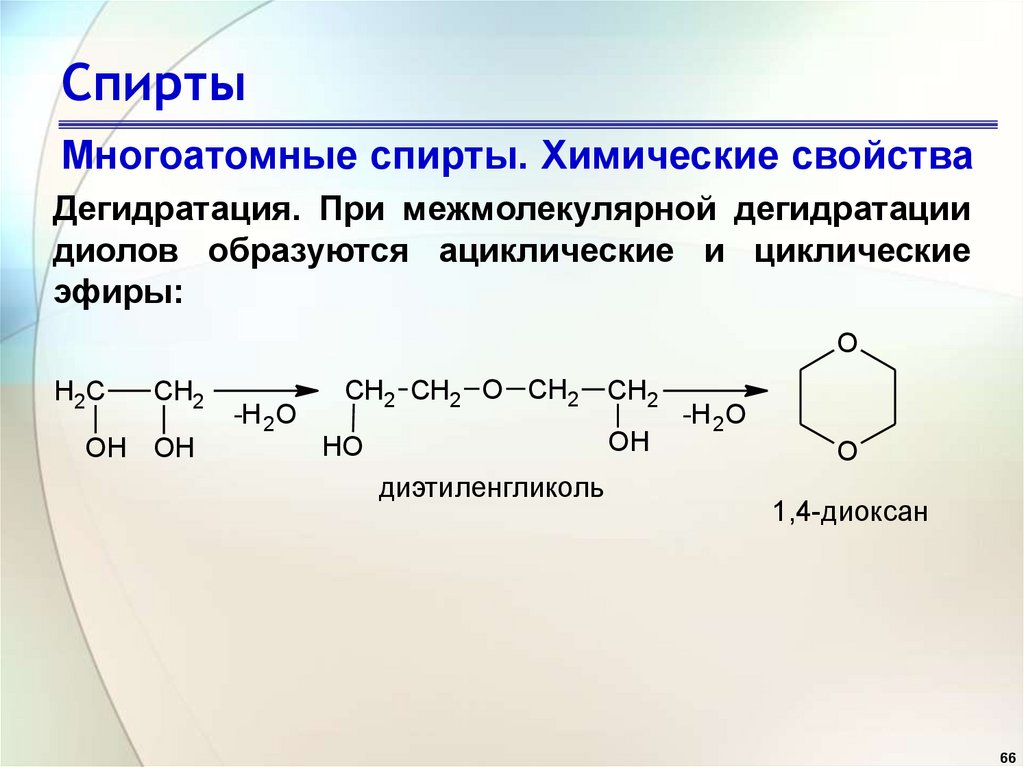
СпиртыМногоатомные спирты. Химические свойства
Дегидратация. При межмолекулярной дегидратации
диолов образуются ациклические и циклические
эфиры:
O
H2C
CH2
OH OH
-H 2O
CH2 CH2 O CH2
CH2
OH
HO
диэтиленгликоль
-H 2O
O
1,4-диоксан
66



































 chemistry
chemistry