Similar presentations:
Щелочноземельные металлы
1.
2.
29.11.2019Щелочноземельные
металлы
3.
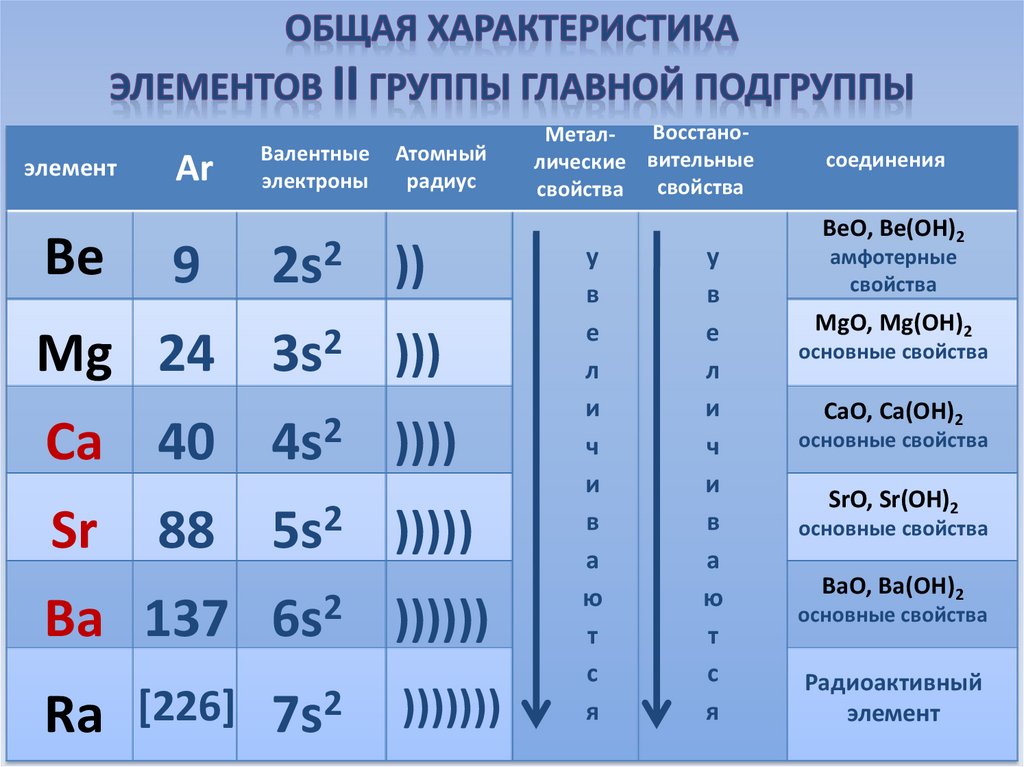
элементBe
Аr
9
Валентные
электроны
Атомный
радиус
2s2 ))
Mg 24 3s2 )))
Ca 40 4s2 ))))
Sr
88 5s2 )))))
Ba 137 6s2 ))))))
Ra [226] 7s2
)))))))
ВосстаноМеталлические вительные
свойства свойства
у
в
е
л
и
ч
и
в
а
ю
т
с
я
у
в
е
л
и
ч
и
в
а
ю
т
с
я
соединения
BeO, Be(OH)2
амфотерные
свойства
MgO, Mg(OH)2
основные свойства
CaO, Ca(OH)2
основные свойства
SrO, Sr(OH)2
основные свойства
BaO, Ba(OH)2
основные свойства
Радиоактивный
элемент
4.
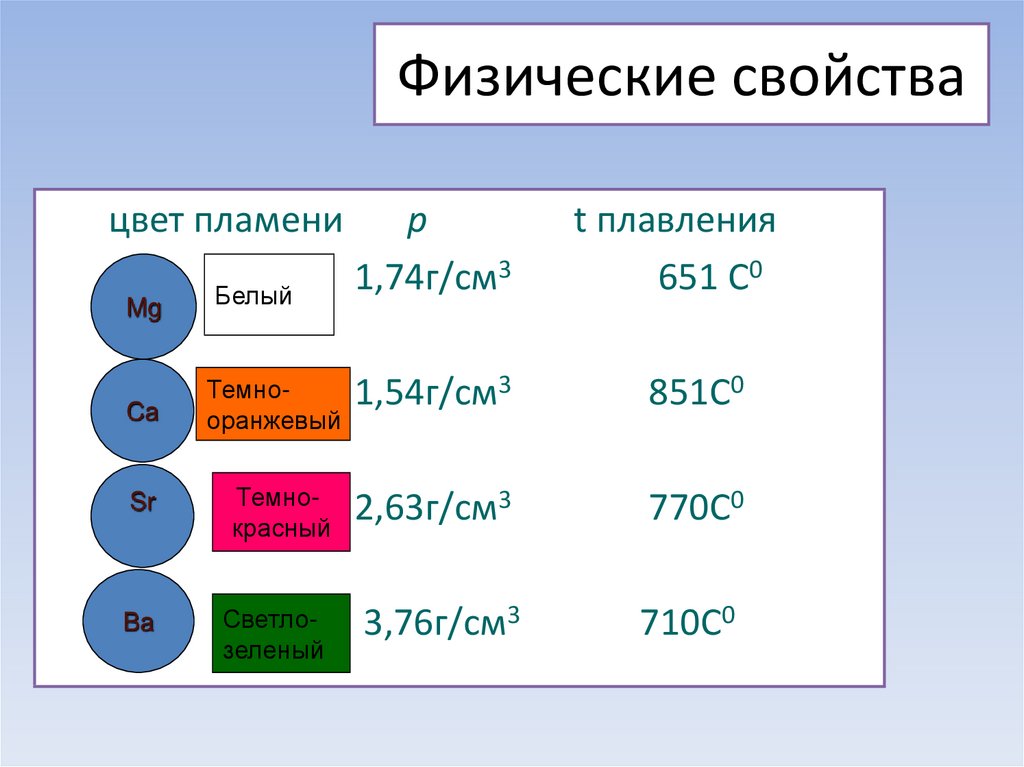
5. Физические свойства
цвет пламениMg
Белый
p
1,74г/см3
t плавления
651 С0
Ca
Темнооранжевый
1,54г/см3
851С0
Sr
Темнокрасный
2,63г/см3
770С0
Ba
Светлозеленый
3,76г/см3
710С0
6.
I.Реагируют с простымивеществами
(с неметаллами)
Me0 +Неме0 → БС
Ме + O2 → оксид
Ме + Г2 =t= галогенид
Ме + H2 =t= гидрид
Ме + S=t= сульфид
Ме+N2=t= нитрид
Mе+P=t= фосфид
II.Реагируют со сложными
веществами
1.Ме + Н2О → Ме(OH) 2 + H2
2. Ме +кислота→
Са + соляная кислота =
3 . Ме +соль→
Са + хлорид алюминия →
Са +сульфат меди(II) →
4. Ме+МехОу→стр.62
Как осуществить превращения?
Са → СаO → Ca(OH)2 → CaSO4
7.
№2. Какой объём займет водород,выделившейся при растворении в 0.5 л
воды 69 г натрия? Какова массовая доля
щелочи в полученном растворе?
8. Нахождение в природе
Бериллий: 3BeO • Al2O3 • 6SiO2– бериллМагний: MgCO3 – магнезит
MgSO4– горькая или английская соль
MgO –жжённая магнезия
Кальций: CaCO3 • MgCO3 – доломит
СаO –негашенная известь, Ca(OH)2 –гашенная известь
CaCO3 – кальцит (известняк, мрамор, мел.)
Ca3(PO4)2 – фосфат кальция
CaSO4 • 2H2O – гипс
CaSO4 • H2O – алебастр
CaF2 – плавиковый шпат (флюорит)
Стронций: SrSO4 – целестин SrCO3 – стронцианит
Барий: BaSO4 – баритова каша BaCO3 – витерит






 chemistry
chemistry








