Similar presentations:
Щелочноземельные металлы
1. Щелочноземельные металлы
1302. Положение в периодической таблице. Строение атома
В периодической системе находятся в главной подгруппе IIгруппы.
Являются сильными восстановителями, отдают 2 ē, во всех
соединениях проявляют степень окисления +2.
Mg +12 2ē, 8ē, 2ē
Ca +20 2ē, 8ē, 8 ē, 2ē
Sr +38 2ē, 8ē, 18 ē, 8ē, 2ē
Ba +56 2ē, 8ē, 18 ē, 18 ē, 8ē, 2ē
3. Физические свойства
цвет пламениMg
Ca
Sr
Ba
þ
1,74г/см3
t плавления
651 С0
1,54г/см3
851С0
2,63г/см3
770С0
3,76г/см3
710С0
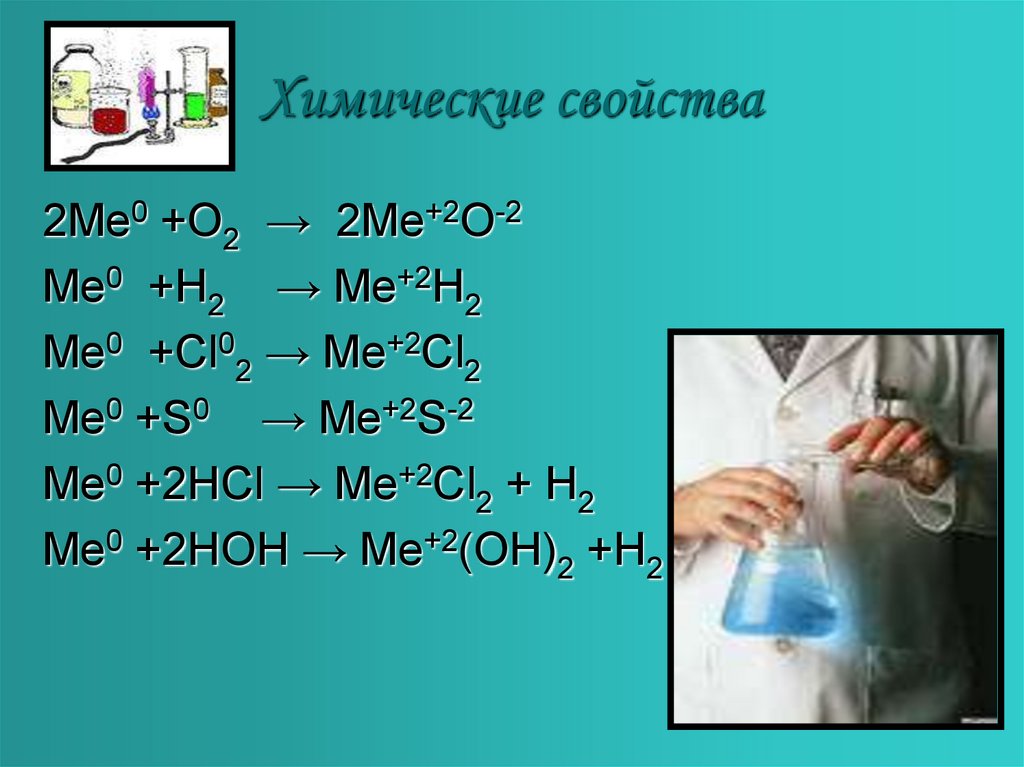
4. Химические свойства
2Me0 +O2 → 2Me+2O-2Me0 +H2 → Me+2H2
Me0 +Cl02 → Me+2Cl2
Me0 +S0 → Me+2S-2
Me0 +2HCl → Me+2Cl2 + H2
Me0 +2HOH → Me+2(OH)2 +Н2
5. Открытие щелочноземельных металлов
МеталлСтр. 105
дата
открытия
учёный,
открывший металл
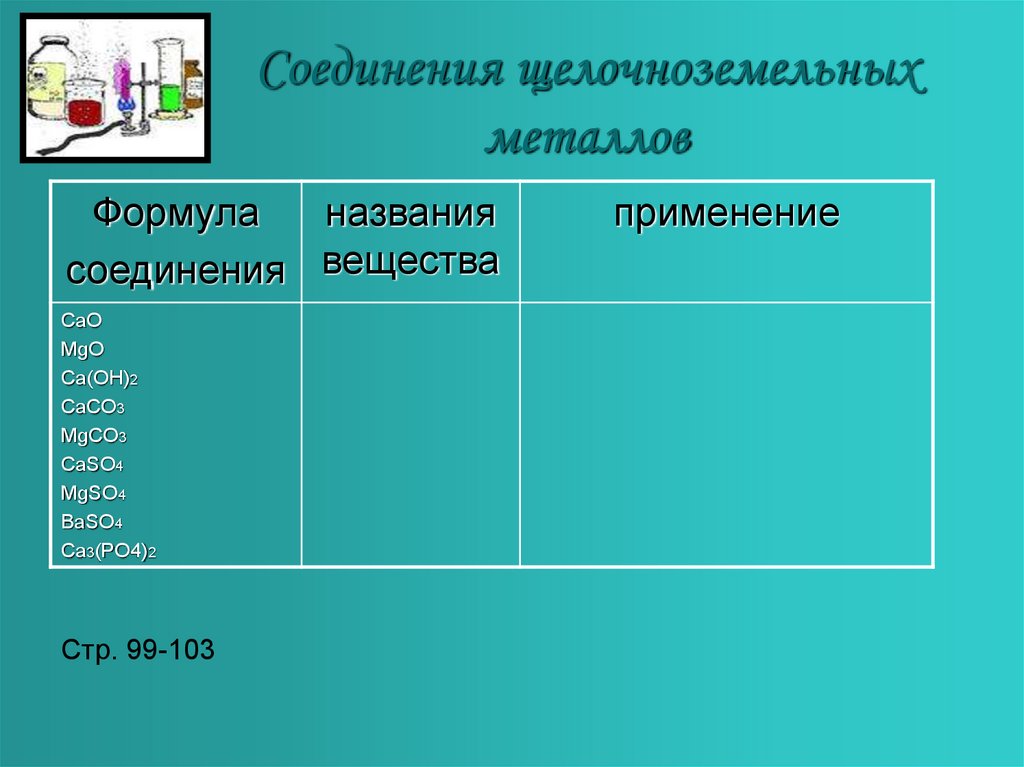
6. Соединения щелочноземельных металлов
Формуланазвания
соединения вещества
CaO
MgO
Ca(OH)2
CaCO3
MgCO3
CaSO4
MgSO4
BaSO4
Ca3(PO4)2
Стр. 99-103
применение
7. Соединения щелочноземельных металлов
Оксиды щелочноземельных металлов легкореагируют с оксидами неметаллов с образованием
соответствующих солей.
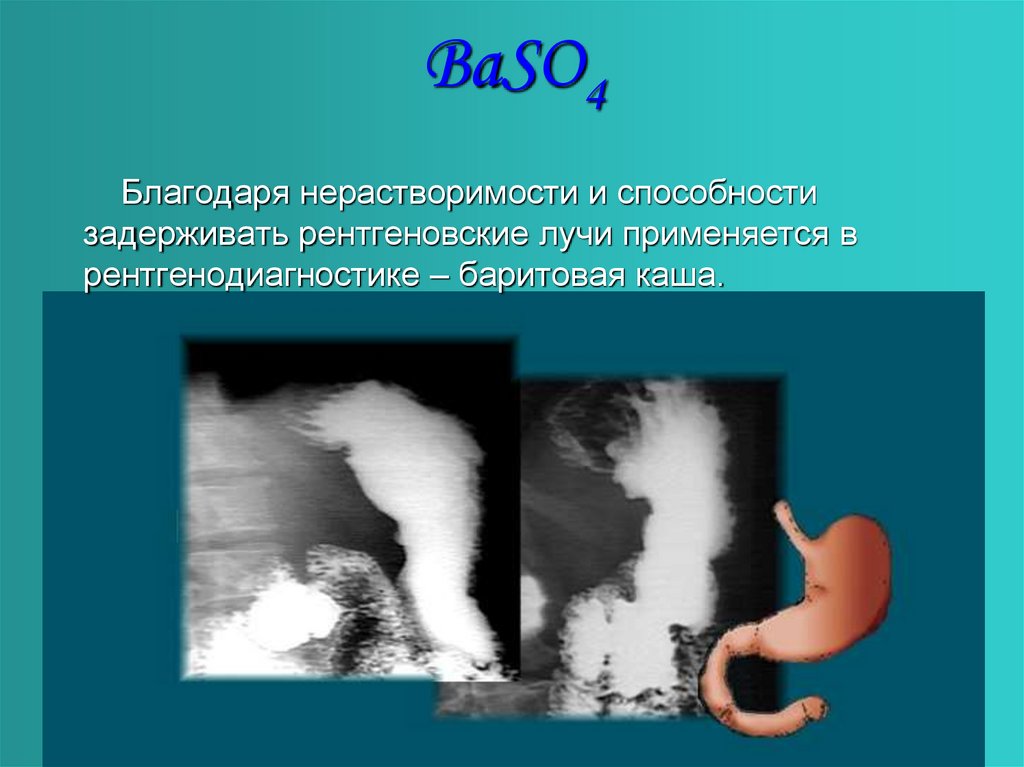
8. BaSO4
Благодаря нерастворимости и способностизадерживать рентгеновские лучи применяется в
рентгенодиагностике – баритовая каша.
9. Ca3(PO4)2
Входит в состав фосфоритов и апатитов, а также всостав костей и зубов. В организме взрослого человека
содержится 1 кг Са в виде фосфата кальция.
10. CaCO3
Карбонат кальция – одно из самыхраспространённых на Земле соединений. Его содержат
горные породы – мел, мрамор, известняк.
11. CaSO4∙ 2H2O
Встречается в природе в виде минерала гипса,представляющего собой кристаллогидрат.
Используется в строительстве, в медицине для
наложения гипсовых повязок, для получения слепков.
12. MgCO3
Широко применяется в производстве стекла,цемента, кирпича, а также в металлургии для перевода
пустой породы в шлак.
13. Са(ОН)2
Гидроксид кальция или гашёная известь с песком иводой называется известковым раствором и широко
используется в строительстве. При нагревании
разлагается на оксид и воду.
14. Домашнее задание:
§ 15Заполнить таблицу стр.105
и таблицу стр.99-103
На оценку прилагать фото конспекта
и двух таблиц.
Выполненное ДЗ отправлять в ВК
с указанием ФИ и класса
https://vk.com/maksimova2809larisa











 chemistry
chemistry








