Similar presentations:
Щелочноземельные металлы
1. Напишите уравнения химических реакций, по которым можно осуществить следующие превращения:
Где в ПСХЭ находятся щелочные металлы?Какие элементы относятся к щелочным металлам?
Почему они так называются?
Назовите общую особенность в строении атомов элементов I
группы главной подгруппы.
Как строение атомов IА определяет их свойства?
Как меняются металлические свойства элементов IА группы
с увеличением заряда их ядер?
2. ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ
3. Положение в ПСХЭ Д.И. Менделеева и строение атомов
2 группа, А- подгруппа, на внешних уровнях по2 электрона, С.О. в соединениях +2
4.
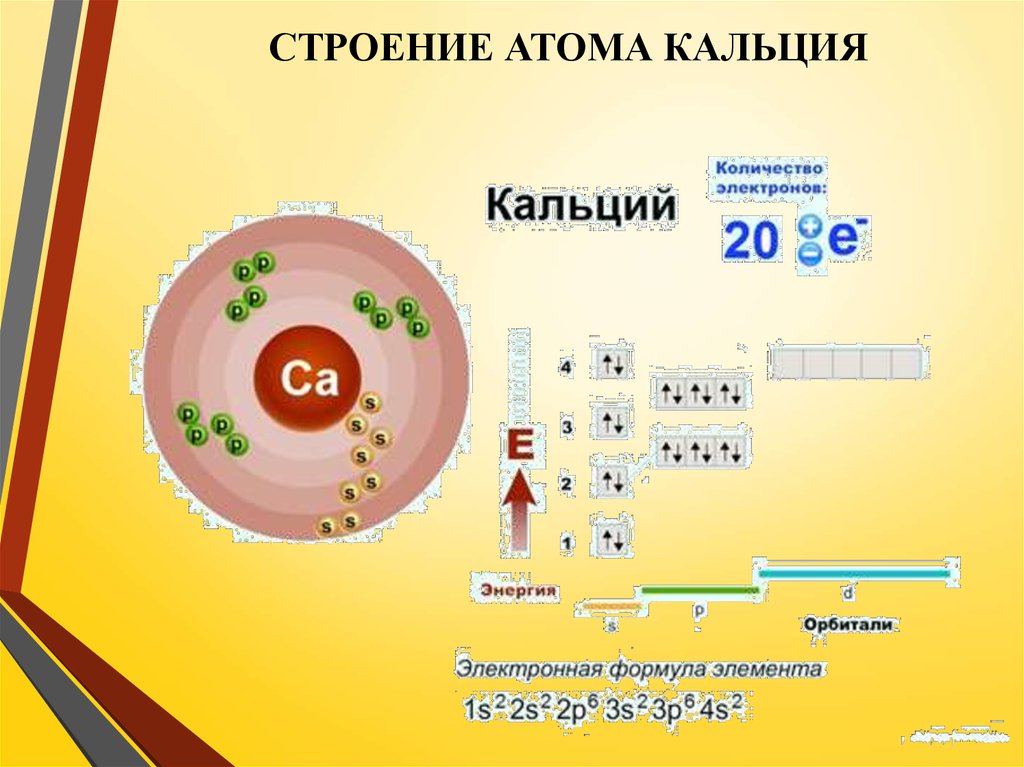
СТРОЕНИЕ АТОМА КАЛЬЦИЯ5.
ФИЗИЧЕСКИЕ СВОЙСТВАОткрыт в 1798 году французским химиком Луи Никола Вокленом,
который назвал его глюцинием. Современное название элемент
получил по предложению химиков немца Клапрота и шведа
Экеберга.
Бериллий — относительно твёрдый (5,5 баллов по Моосу), но
хрупкий металл серебристо-белого цвета. Один из самых твёрдых
металлов в чистом виде (уступает только иридию, осмию, вольфраму
и урану). На воздухе активно покрывается стойкой оксидной плёнкой
BeO. Плотность (при н. у.) 1,848 г/см³.Температура плавления 1278
°C, температура кипения 2970 °C.
В 1808 г. английский химик Гемфри Дэви с помощью электролиза увлажнённой
смеси магнезии и оксида ртути получил амальгаму неизвестного металла,
которому дал название «магнезиум», сохранившееся до сих пор во многих
странах. В России с 1831 года принято название «магний». В 1829 г.
французский химик А. Бюсси получил магний, восстанавливая его
расплавленный хлорид металлическим калием. В 1830 г. М. Фарадей получил
магний электролизом расплавленного хлорида магния.
Магний — металл серебристо-белого цвета, обладает металлическим блеском.
При обычных условиях поверхность магния покрыта довольно прочной
защитной плёнкой оксида магния MgO, которая разрушается при нагреве на
воздухе до примерно 600 °C, после чего металл сгорает с ослепительно белым
пламенем с образованием оксида и нитрида магния Mg3N2. На горящий магний
желательно смотреть только через темные очки или стекло, так как в противном
случае есть риск получить световой ожог сетчатки и на время ослепнуть.
Плотность магния при 20 °C — 1,738 г/см³, температура плавления 650 °C,
температура кипения 1090 °C. Магний высокой чистоты пластичен, хорошо
прессуется, прокатывается и поддаётся обработке резанием.
6.
Название элемента происходит от лат. calx (в родительномпадеже calcis) — «известь», «мягкий камень». Оно было
предложено английским химиком Хэмфри Дэви, в 1808 г.
выделившим металлический кальций электролитическим
методом.
Серебристый металл, плотность (при н. у.) 1,55 г/см3,
температура плавления 838,85 °C, температура кипения
1483,85 °C.
Обнаружили в минерале стронцианите, найденном в 1764 году в
свинцовом руднике близ шотландской деревни Стронти́ан[en] (англ.
Strontian, гэльск. Sron an t-Sìthein), давшей впоследствии название
новому элементу. Присутствие в этом минерале оксида нового
металла было установлено в 1787 году Уильямом Крюйкшенком и
Адером Кроуфордом. Выделен в чистом виде сэром Хемфри Дэви в
1808 году.
Стронций — мягкий серебристо-белый металл, обладает ковкостью и
пластичностью, легко режется ножом. Температура плавления: 768
°С, температура кипения: 1390 °С.
Барий был открыт в виде оксида BaO в 1774 г. Карлом Шееле
и Юханом Ганом. В 1808 году английский химик Гемфри
Дэви электролизом выделил металлический барий.
Барий — серебристо-белый ковкий металл. При резком ударе
раскалывается. Плотность 3,5 г/см³.
7.
НАХОЖДЕНИЕ В ПРИРОДЕВ земной коре содержится бериллия - 0,00053%, магния - 1,95%, кальция 3,38%, стронция - 0,014%, бария - 0,026%, радий - искусственный элемент.
Встречаются в природе только в виде соединений - силикатов,
алюмосиликатов, карбонатов, фосфатов, сульфатов и т.д.
Be
3BeO • Al2O3 • 6SiO2
или Al2[Be3(Si6O18)]
– берилл
Mg
MgCO3 – магнезит, CaCO3 • MgCO3 – доломит
KCl • MgSO4 • 3H2O – каинит, KCl • MgCl2 • 6H2O –
карналлит, MgCl2•6H2O - бишофит
8.
ХИМИЧЕСКИЕ СВОЙСТВАПОЛУЧЕНИЕ- ЭЛЕКТРОЛИЗ СОЛЕЙ
Очень реакционноспособны, сильные восстановители.
Активность металлов и их восстановительная способность
увеличивается в ряду: Be–Mg–Ca–Sr–Ba. Обладают положительной
валентностью +2. Оксиды имеют общую формулу МеО. Тенденция к
образованию пероксидов выражена слабее, чем для щелочных
металлов.
1) Взаимодействие с водой.
В обычных условиях поверхность Be и Mg покрыты инертной оксидной
пленкой, поэтому они устойчивы по отношению к воде. В отличие от
них Ca, Sr и Ba растворяются в воде с образованием гидроксидов,
которые являются сильными основаниями:
Ве + H2O → ВеO+ H2↑
Ca + 2H2O → Ca(OH)2 + H2↑
2) Взаимодействие с кислородом.
Все металлы образуют оксиды МеO, барий образует пероксид – BaO2:
2Mg + O2 → 2MgO
Ba + O2 → BaO2
9.
3) Взаимодействие с неметаллами:Be + Cl2 → BeCl2 (галогениды)
3Mg + N2 → Mg3N2 (нитриды)
Ca + 2C → CaC2 (карбиды)
Ba + S → BaS (сульфиды)
Ca + H2 → CaH2 (гидриды)
3Ba + 2P → Ba3P2 (фосфиды)
Бериллий и магний сравнительно медленно реагируют с неметаллами.
4) Взаимодействие с кислотами:
Ca + 2HCl → CaCl2 + H2
Mg + H2SO4(разб.) → MgSO4 + H2
Бериллий также растворяется в водных растворах
щелочей (амфотерные свойства):
Be + 2NaOH + 2H2O → Na2[Be(OH)4] + H2
Качественная реакция на катионы щелочноземельных
металлов – окрашивание пламени в следующие цвета:
Ca2+ - темно-оранжевый
Sr2+- темно-красный
Ba2+ - светло-зеленый
Катион Ba2+ обычно открывают обменной реакцией с серной
кислотой или ее солями: BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Ba2+ + SO42- → BaSO4↓
Сульфат бария – белый осадок, нерастворимый в минеральных
кислотах.
10.
ВАЖНЕЙШИЕ СОЕДИНЕНИЯ КАЛЬЦИЯОкси́д ка́льция (окись кальция, негашёная
и́звесть, «кипелка») формула CaO.
Получение в промышленности
Обжиг известняка:
CaCO3 t˚C→ CaO + CO2
Физические свойства
Тугоплавкое вещество белого цвета,
температура плавления 2570°С.
Химические свойства
Типичный основный оксид. Реагирует с водой, кислотными
оксидами и кислотами:
СаO + H2O → Са(OH)2 + Q; (гашение извести)
СаО + SO3 → CaSO4;
СаО + 2HCI → CaCI2 + H2O.
11.
ГИДРОКСИД КАЛЬЦИЯ (ГАШЕНАЯ ИЗВЕСТЬ, «ПУШОНКА»Получение: (гашение)
CaO+H2O→ Ca(OH)2 (гашеная известь)
Белый (иногда серый) порошок, мало
растворимый в воде, растворимость падает
с ростом температуры.
ХИМИЧЕСКИЕ СВОЙСТВА
Реакции с кислотными оксидами: Ca(OH)2 + СO2 → CaСO3↓ + H2O
ПРИМЕНЕНИЕ
•Гашёная известь — так как её получают путём «гашения» (то есть
взаимодействия с водой) «негашеной» извести (оксида кальция).
(строительство)
•Известковое молоко — взвесь (суспензия), образуемая при смешивании
избытка гашёной извести с водой. Похожа на молоко. (получение
хлорной извести, производство сахара, для борьбы с болезнями
растений)
•Известковая вода — прозрачный раствор гидроксида кальция,
получаемый при фильтровании известкового молока. (для обнаружения
углекислого газа)
12.
Написатьуравнения реакций
Л/о №10 Ознакомление со
свойствами и превращениями
карбонатов и гидрокарбонатов
13.
14.
ПРИМЕНЕНИЕ СОЛЕЙ КАЛЬЦИЯВ своей работе специалисты разных областей знаний не могут обойтись
без соединений щелочноземельных металлов.
Строитель: самый важный из минералов – известняк (карбонат
кальция), без которого не обходится ни одно строительство. Вопервых, он сам является прекрасным строительным камнем. Вовторых, это сырьё для получения цемента, гашёной и негашёной
извести, стекла и др. Известковой щебёнкой укрепляют дороги.
Природный мел представляет собой остатки раковин древних
животных. Мел применяют для побелки, а также и в школе –
школьный мел.
Агроном: среднего содержания кальция в почвах (1,37%) вполне
достаточно для обеспечения физиологических потребностей
растений. Тем не менее, соединения кальция вносят в почвы для
химической мелиорации: известковым порошком уменьшают
кислотность почв, гипсованием устраняют избыточную
щёлочность. Нитрат и фосфаты кальция используются как азотные
удобрения.
Скульптор: минерал скульпторов – мрамор (карбонат кальция).
Из него создавал свои прекрасные творения Микеланджело.
Сульфат кальция встречается в природе в виде минерала гипса.
Его используют для получения слепков. Для этого применяют
полуводный гипс – алебастр.
15.
Хирург: гипс используем и мы, медики, дляналожения фиксирующих гипсовых повязок.
Сульфат магния, известный под названием горькая
или английская соль, используют в качестве
слабительного средства. Он содержится в морской
воде и придаёт ей горький вкус. Сульфат бария
благодаря
нерастворимости
и
способности
задерживать рентгеновские лучи применяют в
рентгенодиагностике («баритовая каша») для
диагностики заболеваний желудочно-кишечного
тракта. Остальные соединения бария токсичны. Из
всех заболеваний подростков на первом месте стоят
нарушения опорно-двигательного аппарата. Одна из
причин – недостаточное содержание кальция в пище.
Замедление поступления кальция в костную ткань
вызывает деформацию костей у взрослых и рахит у
детей. Человек должен получать в день 1,5г кальция.
Наибольшее его количество содержится в сыре,
твороге, петрушке, салате. Другой хороший источник
пищевого кальция, часто не берущийся в расчет мягкие кости лосося и сардин, которые мы съедаем
при потреблении этой пищи.
16.
Стоматолог: а сколько соединений кальция в составе любойзубной пасты! Из зубной пасты доставляются кальций, фосфор и
магний. Кальций и фосфор являются основными строительными
элементами эмали зуба. На протяжении всей жизни человека они
участвуют в обменных процессах. Необходимость такой добавки
обусловлена потребностью зубов в этих элементах при кариесе, и в
еще большей степени при некариозных поражениях зубов.
Некариозные поражения зубов чаще всего связаны с нарушениями
функции
щитовидной,
поджелудочной,
половых
желез,
заболевания ЖКТ и др., а так же с влиянием внешних
неблагоприятных воздействий (ежедневная длительная - более 6
часов - работа с компьютером, экологические влияния)
вызывающих заметную убыль минеральных компонентов в тканях
зуба, ведущих в начале к повышенной чувствительности зубов, а
затем к повреждению в виде кариеса. В связи с этим местное
применение паст, содержащих фосфорно-кальциевые добавки,
позволяет не только предупредить, но и в известной степени
компенсировать потери при наличии заболевания.
Биолог: соединения кальция входят в состав скелетов
и зубов позвоночных животных. Такие скелеты
называются внутренними, и образованы они
фосфатом кальция. На долю кальция приходится
более 1,5% массы тела человека, 98% кальция
содержится в костях.
17.
Написать уравнения реакций по которым можноосуществить следующие превращения:
Ca → CaO→Ca(OH)2→CaCO3→Ca(HCO3)2→CaCO3→CaO→CaSO4
ДОМАШНЕЕ ЗАДАНИЕ
§ 44 № 5
§ 45 № 2















 chemistry
chemistry








