Similar presentations:
Альдегиды
1. Альдегиды
2.
Альдегиды - органические вещества,содержащие функциональную
альдегидную группу.
O
общая формула
R—C
H
3. Изомерия и номенклатура
Для альдегидов характерна изомерияуглеводородного радикала. Названия
альдегидов происходят от исторических
названий соответствующих органических
кислот, в которые они превращаются при
окислении. По международной номенклатуре
названия альдегидов происходят от названий
соответствующих углеводородов с
прибавлением суффикса -АЛЬ.
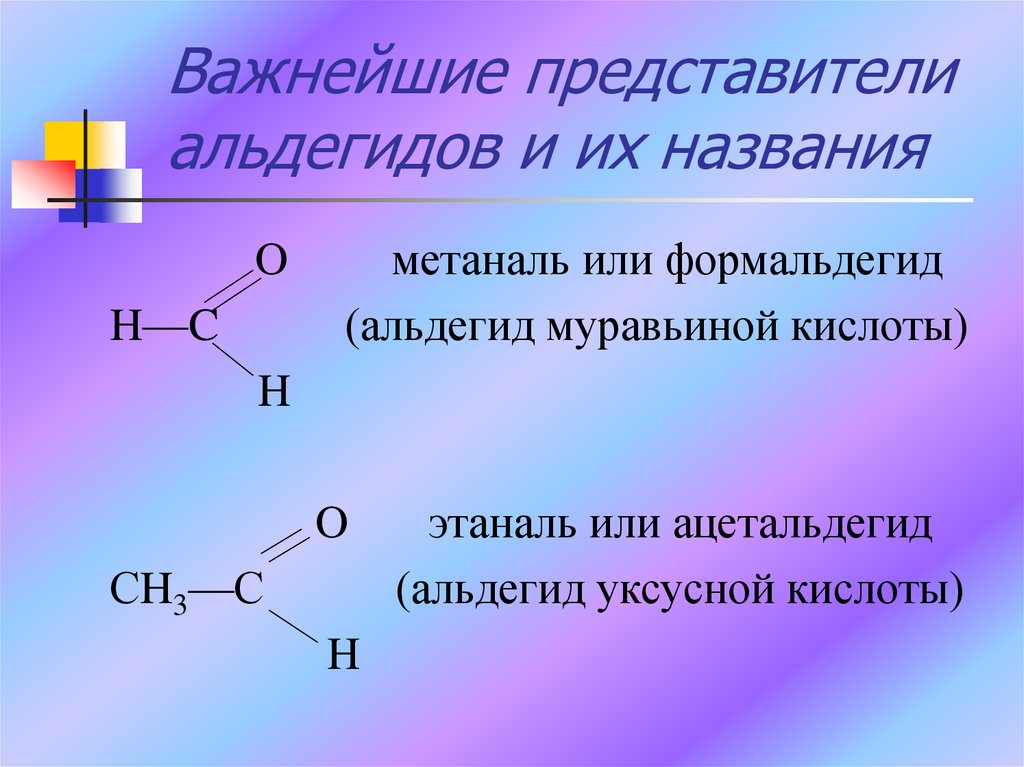
4. Важнейшие представители альдегидов и их названия
OH—C
метаналь или формальдегид
(альдегид муравьиной кислоты)
H
O
СH3—С
H
этаналь или ацетальдегид
(альдегид уксусной кислоты)
5.
OCH3—CH2—C
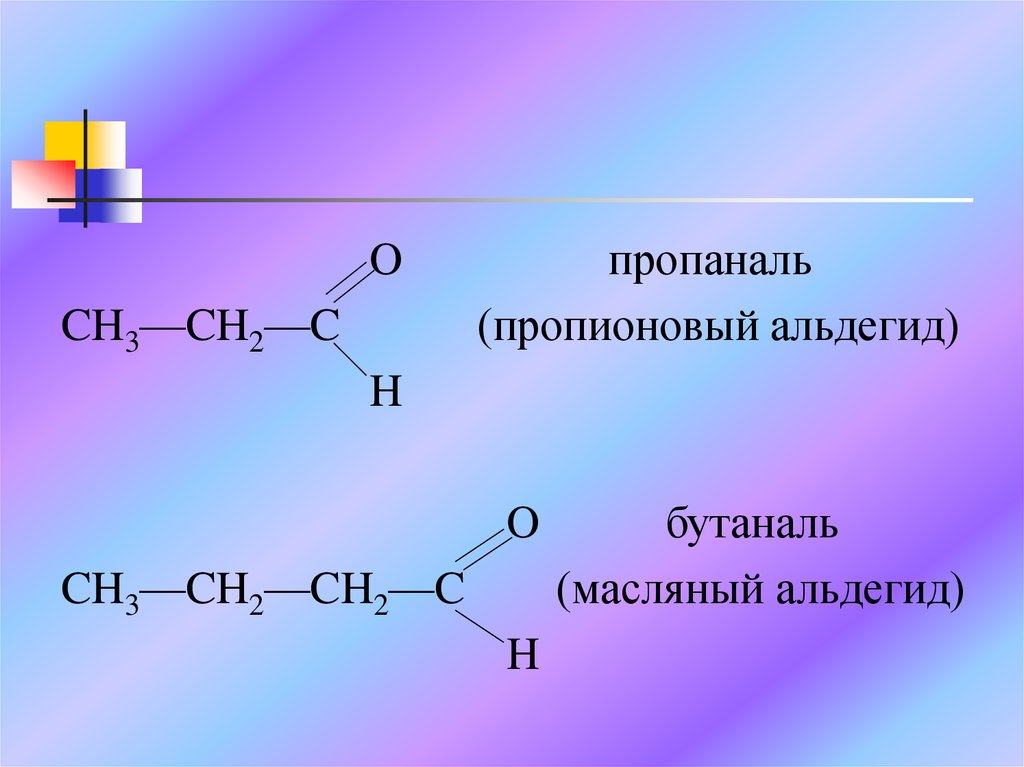
пропаналь
(пропионовый альдегид)
H
O
CH3—CH2—CH2—C
H
бутаналь
(масляный альдегид)
6.
OCH3—CH2—CH2—CH2—C
H
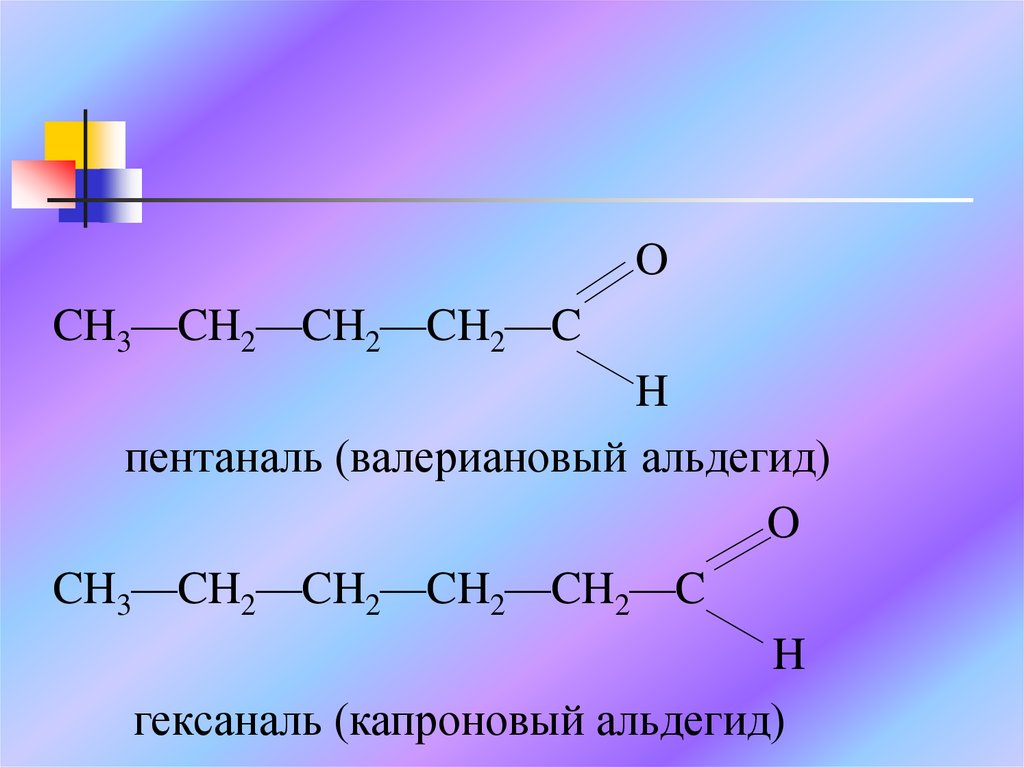
пентаналь (валериановый альдегид)
O
CH3—CH2—CH2—CH2—CH2—C
H
гексаналь (капроновый альдегид)
7. Физические свойства
Метаналь - бесцветный газ с резкимзапахом. Раствор метаналя в воде (35 40%-ный) называется формалином.
Остальные члены ряда альдегидов жидкости, а высшие альдегиды-твердые.
8. Химические свойства
1.Реакции окисления1)Качественной реакцией на альдегиды
является реакция "серебряного зеркала«
O
t, аммиачный раствор
O
R—C +Ag2O
R—C +2Ag
H
H
9.
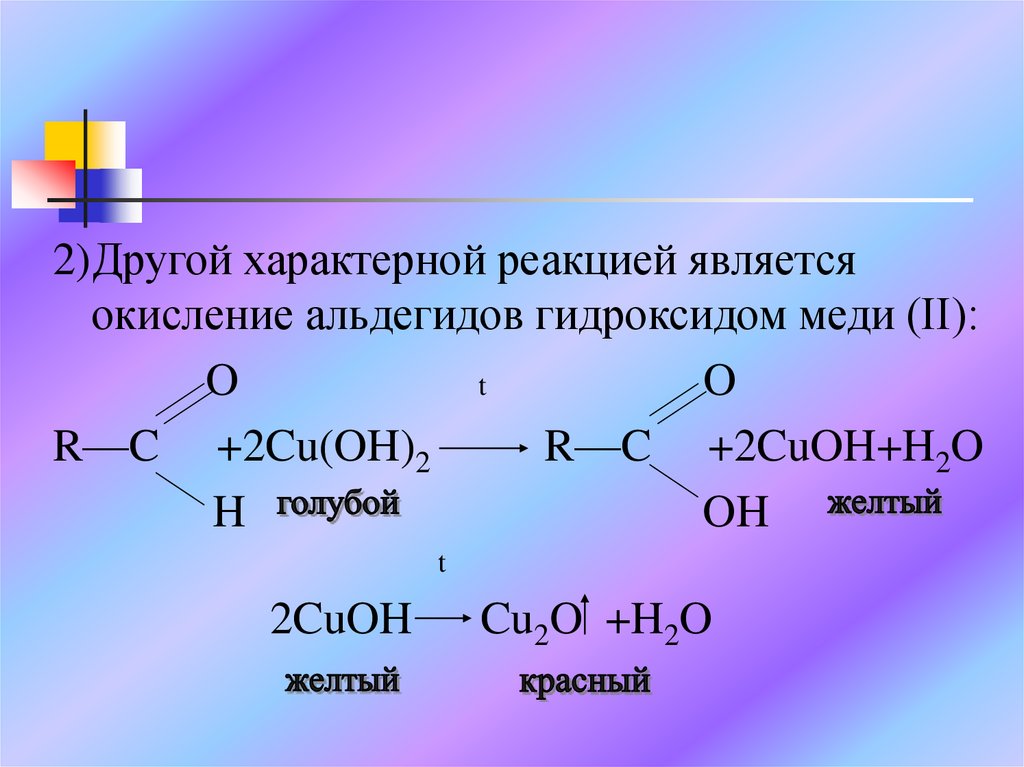
2)Другой характерной реакцией являетсяокисление альдегидов гидроксидом меди (II):
O
t
O
R—C +2Cu(OH)2
R—C +2CuOH+H2O
H
OH
t
2CuOH
Cu2O +H2O
10.
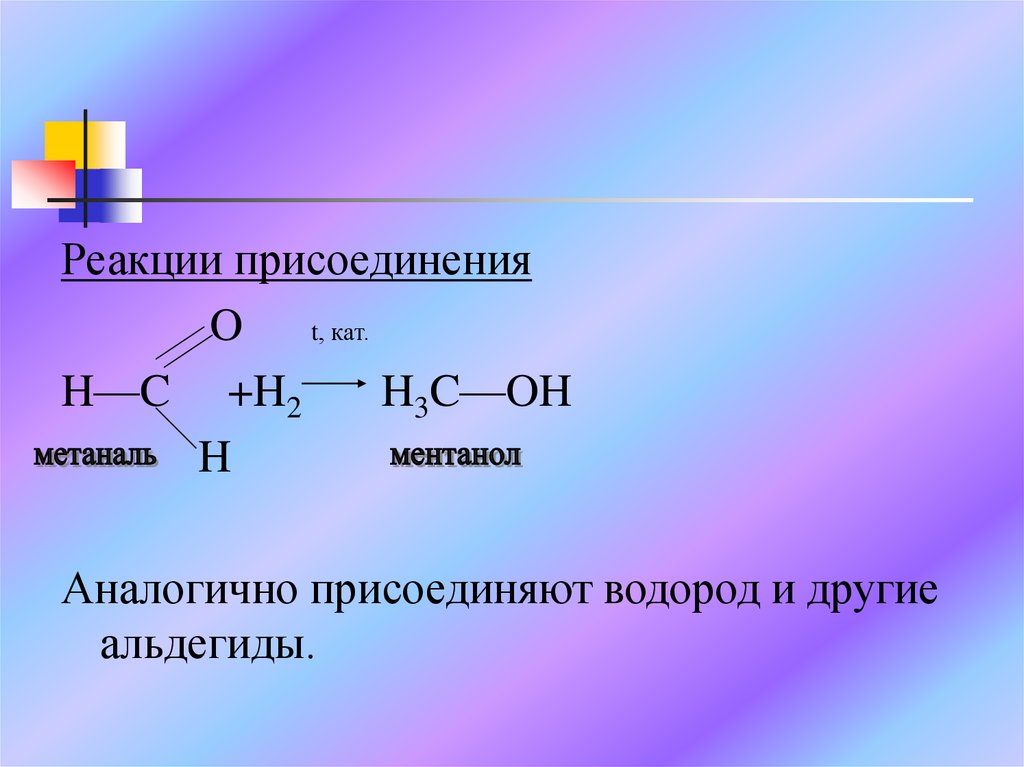
Реакции присоединенияO t, кат.
H—C +H2
H3C—OH
H
Аналогично присоединяют водород и другие
альдегиды.
11. Получение альдегидов
В лаборатории альдегиды получают окислениемпервичных спиртов. В качестве окислителей
применяют оксид меди (II), пероксид
водорода
12.
В промышленности альдегиды получаютразличными способами:
а) окислением метана кислородом воздуха
в специальном реакторе(при большой
скорости):
H
500 C, кат.
O
H—C—H+O2
H—C +H2O
H
H
0
13.
б) метаналь получают также окислениемметанола, пропуская его пары вместе с
воздухом через реактор с раскаленной медной
или серебряной сеткой:
Cu или Ag
O
2СH3OH+O2
2H—C
+2H2O
H
14.
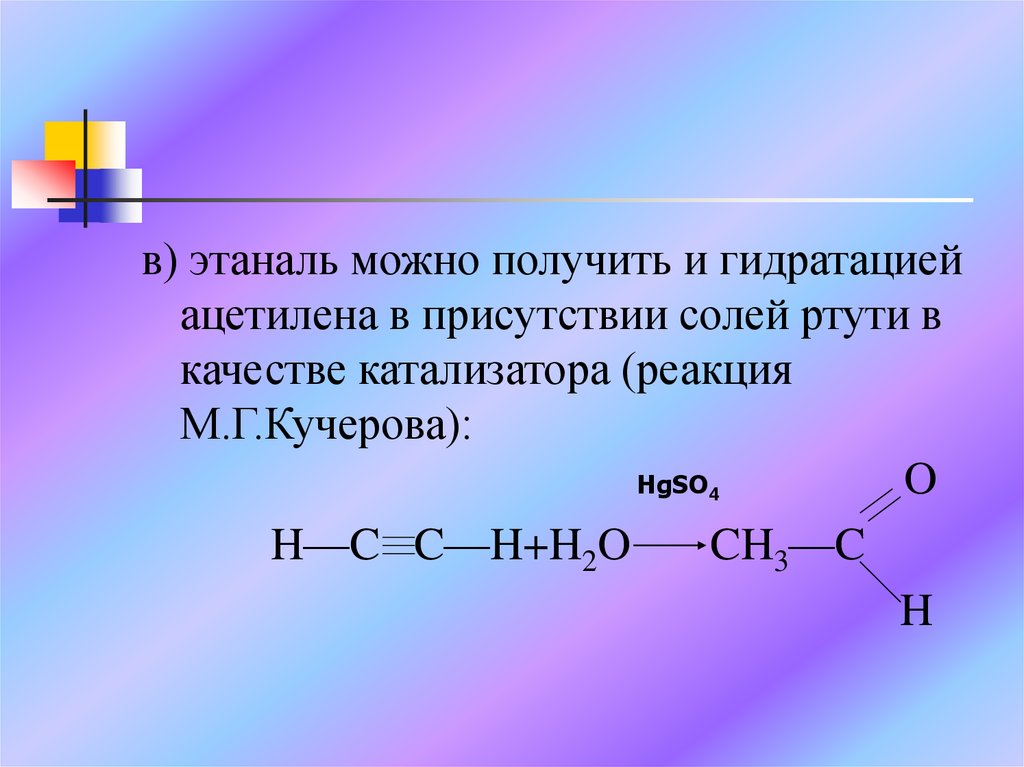
в) этаналь можно получить и гидратациейацетилена в присутствии солей ртути в
качестве катализатора (реакция
М.Г.Кучерова):
HgSO
O
H—C C—H+H2O
CH3—C
H
4
15. Применение альдегидов
Немецкий химик А.И. Байер в 1872г. изфенола и формальдегида получил
смолообразный продукт.
Бельгийский ученый Л.Х. Бакеланд
разработал способ получения этого
вещества в промышленности. Так с 1912г.
производится фенолформальдегидная смола,
названная бакелитом.
16.
Метанал используется для полученияфенолформальдегидной смолы, которая
необходима для производства различных
пластмасс, так же на производство некоторых
лекарственных веществ и красителей.










 chemistry
chemistry