Similar presentations:
Альдегиды и кетоны
1. Альдегиды
2.
Альдегиды - это карбонильные производныеуглеводородов, в молекулах которых присутствует
альдегидная группа
Альдегиды – это органические соединения, содержащие
карбонильную группу – С=О, связанную с атомом водорода
и углеводородным радикалом
Формальдегид не подпадает под это
определение, т. к. не содержит
углеводородный радикал
Название «альдегиды» объясняется сокращением слов
«алкоголь дегидрогенизированный»
3.
АльдегидыАльдегиды – это органические вещества, молекулы,
которых содержат карбонильную группу, соединенную с
углеводородным радикалом и атомом водорода
О
О
─С
─С
О
Карбонильная группа
R─ С
Н
Альдегидная группа
Н
Общая формула
4.
Альдегиды и кетоныАльдегиды
- аль
Пропаналь
CnH2nO
Кетоны
- он
СН3 – С – СН3
||
O
Пропанон
5.
АльдегидыМетаналь (формальдегид)
Этаналь (ацетальдегид)
Пропаналь
Бутаналь
Пентаналь
6.
НоменклутураO
H3 C
−
CH
|
CH3
−
CH2
− C
H
3-метил бутаналь
6
7.
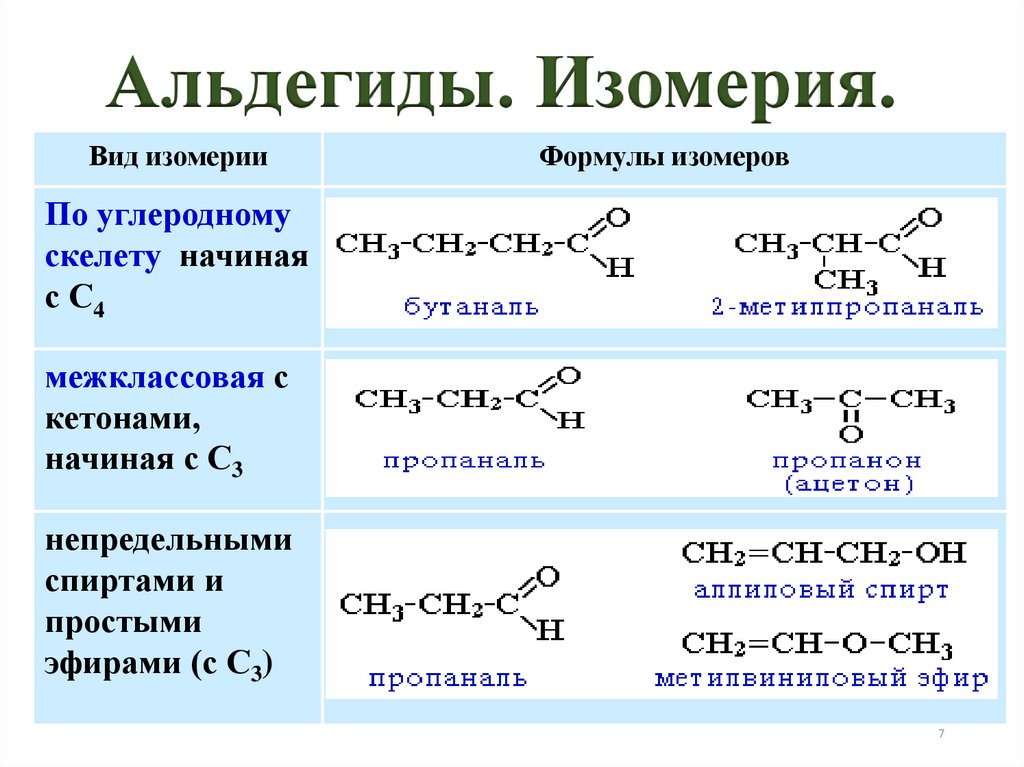
Альдегиды. Изомерия.Вид изомерии
Формулы изомеров
По углеродному
скелету начиная
с С4
межклассовая с
кетонами,
начиная с С3
непредельными
спиртами и
простыми
эфирами (с С3)
7
8. Физические свойства альдегидов определяются строением карбонильной группы >C=O.
Физические свойства альдегидов определяютсястроением карбонильной группы >C=O.
Водородная связь
t кип < tкип спиртов
С1 - газ
С2– С5 – жидкости
С6 – твердые.
9.
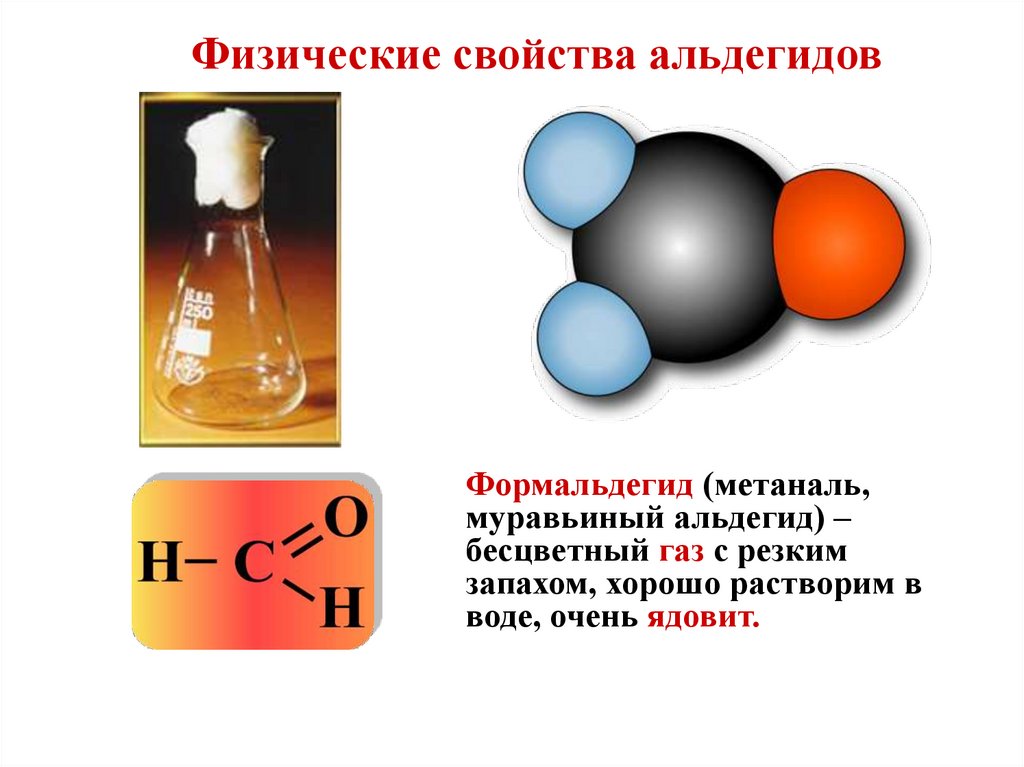
Физические свойства альдегидовФормальдегид (метаналь,
муравьиный альдегид) –
бесцветный газ с резким
запахом, хорошо растворим в
воде, очень ядовит.
10.
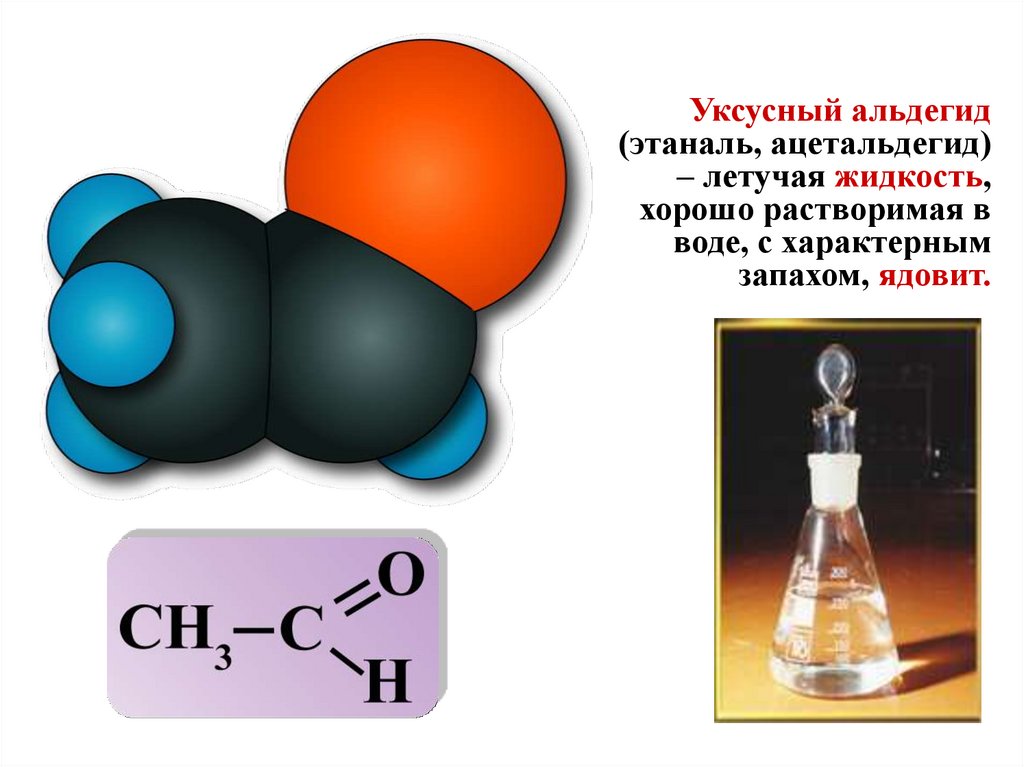
Уксусный альдегид(этаналь, ацетальдегид)
– летучая жидкость,
хорошо растворимая в
воде, с характерным
запахом, ядовит.
11.
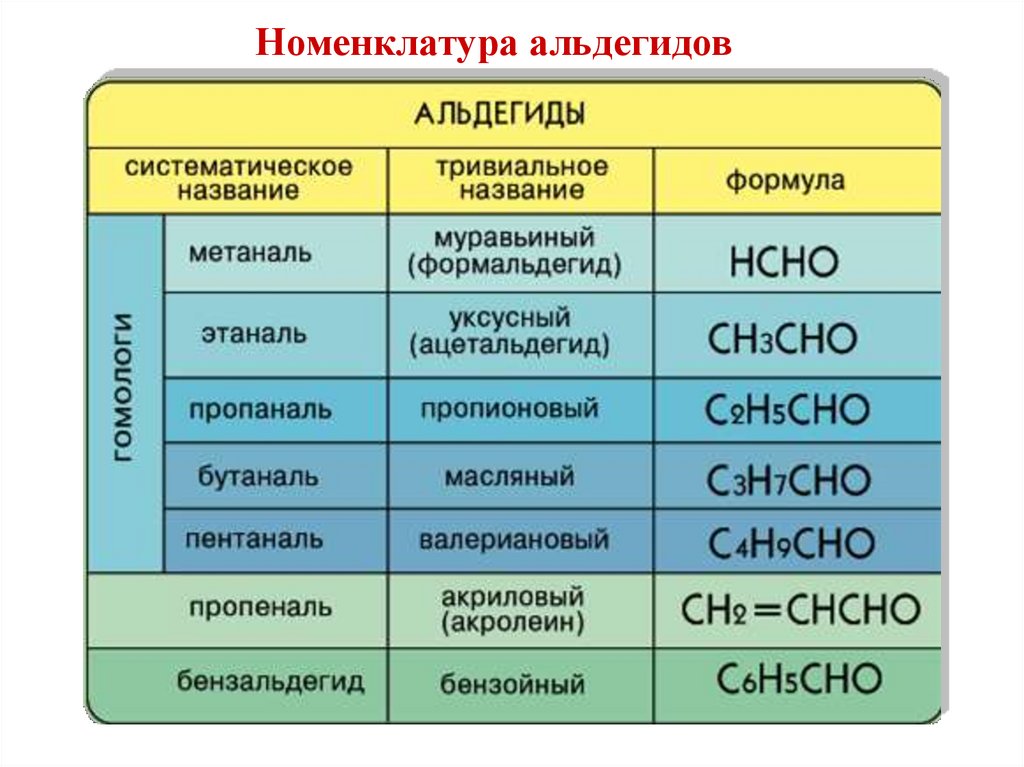
Номенклатура альдегидов12. Химические свойства альдегидов
Реакцииприсоединения
Гидрирование
Реакции
окисления
Реакция
«серебряного
зеркала»
Присоединение
NaHSO3
Реакции
поликонденсации
Реакции
полимеризации
Окисление
Cu(OH)2
13.
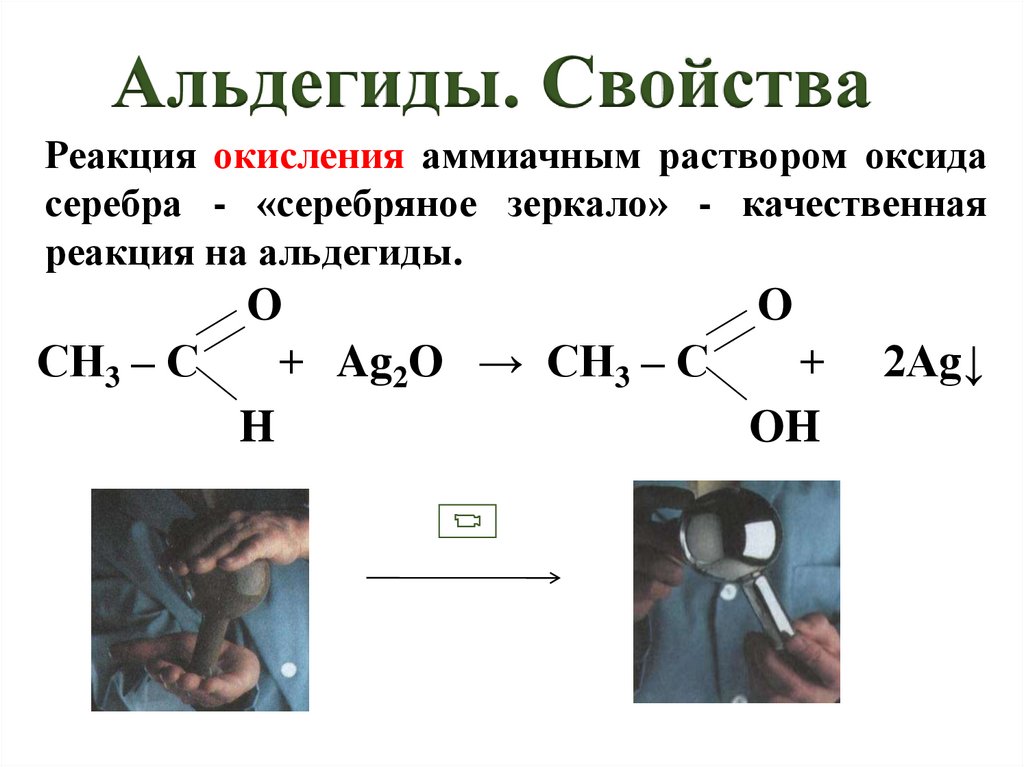
Альдегиды. СвойстваРеакция окисления аммиачным раствором оксида
серебра - «серебряное зеркало» - качественная
реакция на альдегиды.
O
O
СН3 – С
+ Ag2O → СН3 – С
+
H
OH
2Ag↓
14.
Альдегиды. СвойстваРеакция окисления гидроксидом меди (II) при
нагревании – качественная реакция на альдегиды.
O
СН3 – С
+ Cu(OH)2 → СН3 – С
H
O
+ CuOH
OH
t0
Cu2O H2O
15.
Альдегиды. СвойстваРеакция
восстановления
водородом
соответствующие спирты - гидрирование
O
СН3 – С
+
H
Н2
Кат., t0
СН3 – СН2 – ОН
в
16.
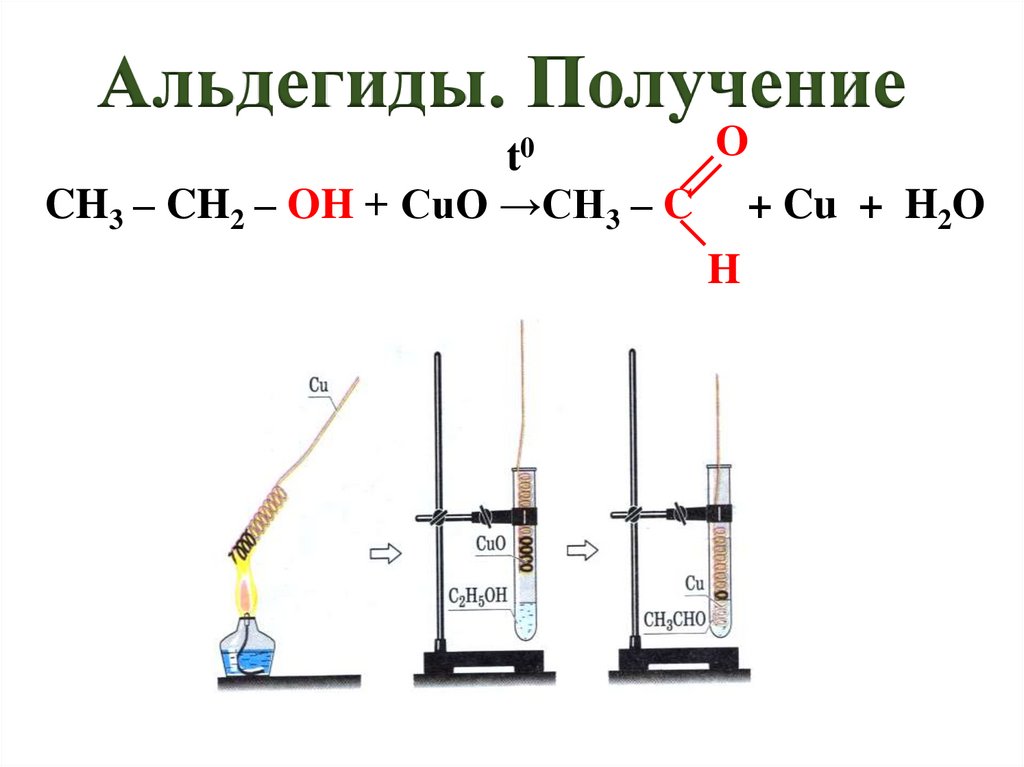
Альдегиды. ПолучениеO
t0
CH3 – CH2 – OH + CuO →CH3 – C + Cu + H2O
H
17.
Получение альдегидовКаталитическое дегидрирование первичных спиртов:
Cu, 300° C
+ H2↑
Этанол
Уксусный альдегид
По сути название «альдегид» происходит от лат. аlcohol
dehydrogenatus – спирт, от которого «отняли» водород.
Окисление первичных спиртов:
+ [О]
t
+ H2O
Уксусный альдегид
Этанол
18.
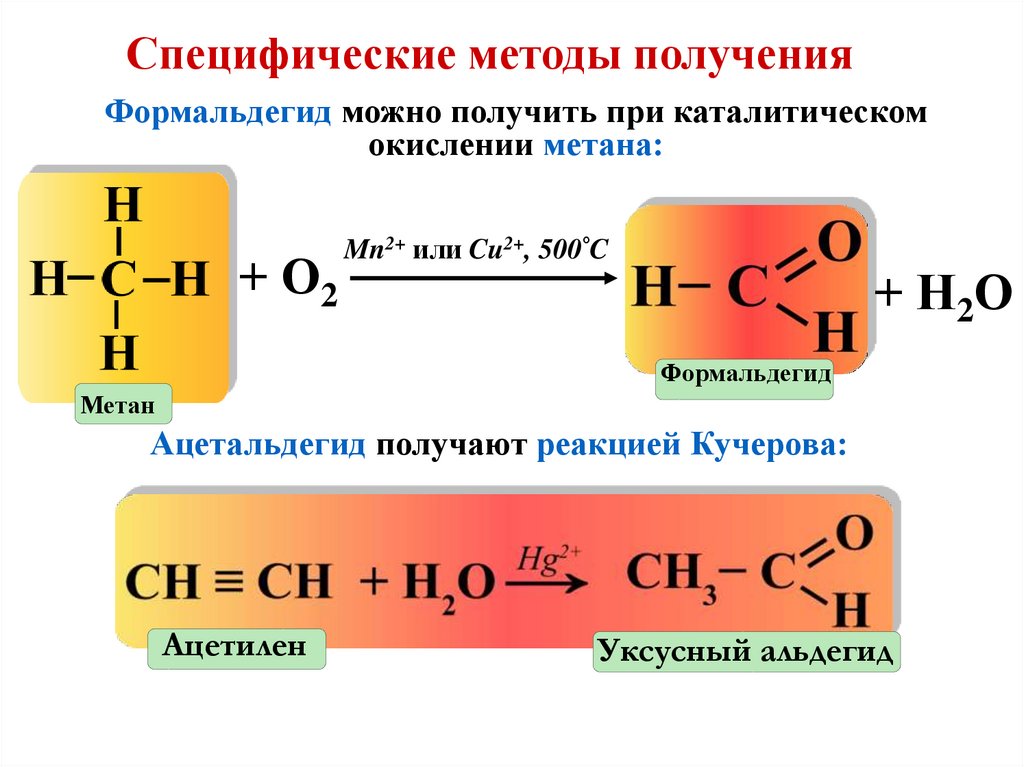
Специфические методы полученияФормальдегид можно получить при каталитическом
окислении метана:
+ О2
Mn2+ или Cu2+, 500°C
+ Н2О
Формальдегид
Метан
Ацетальдегид получают реакцией Кучерова:
Ацетилен
Уксусный альдегид
19.
20.
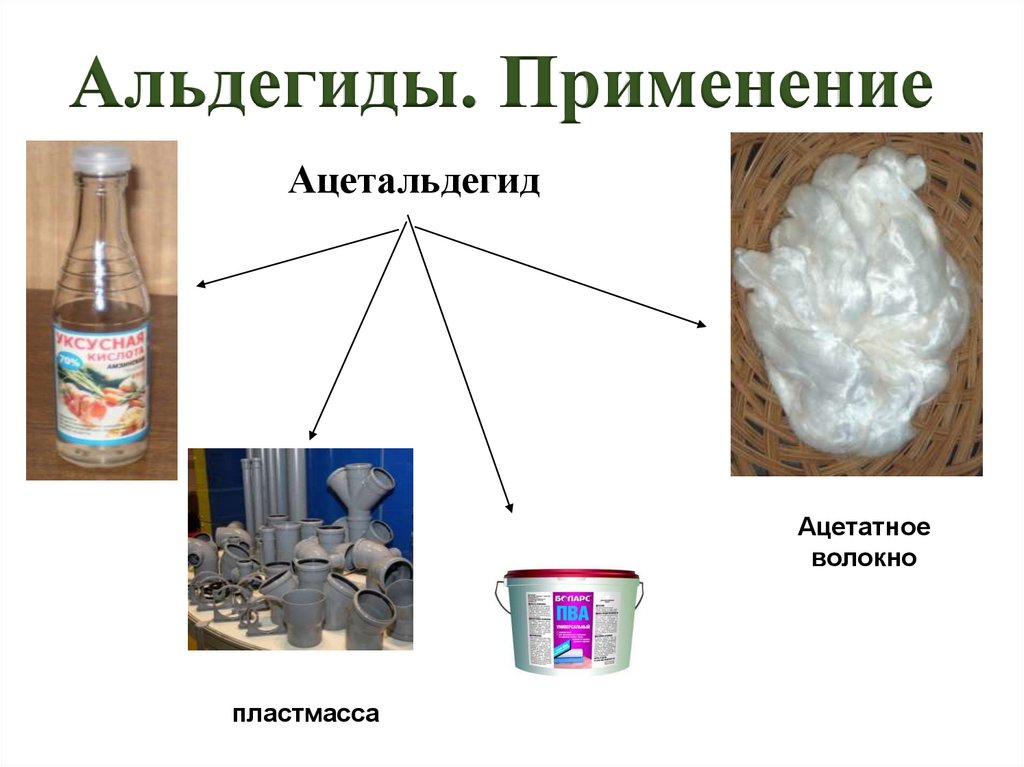
Альдегиды. ПрименениеАцетальдегид
Ацетатное
волокно
пластмасса
21.
Применение альдегидов и кетоновМетаналь (муравьиный альдегид) CH2 = O:
получение фенолформальдегидных смол;
получение мочевино-формальдегидных (карбамидных)
смол;
полиоксиметиленовые полимеры;
дезинфицирующее средство;
синтез лекарственных средств (уротропин);
консервант биологических препаратов (благодаря
способности свертывать белок).
Этаналь (уксусный альдегид, ацетальдегид
СН3СН = О:
органический синтез
производство уксусной кислоты;
Ацетон СН3– СО – СН3:
растворитель лаков, красок, ацетатов целлюлозы;
сырьё для синтеза различных органических веществ.
22.
Альдегиды в природеОтличительной чертой многих альдегидов является их
запах. Высшие альдегиды, особенно непредельные и
ароматические, входят в состав эфирных масел и содержатся
в цветах, фруктах, плодах, душистых и пряных растениях.
Их используют в пищевой промышленности и парфюмерии.
23.
Альдегиды в природеБулочки ванильные, корицы аромат,
Амаретто, шоколад
Альдегидов вкус таят
В землянике и кокосе
И в жасмине и в малине
И в духах и в еде
Альдегидов след везде.
Что за запах, что за прелесть,
И откуда эта свежесть?
Это высший альдегид
Аромат вам свой дарит.
24.
Альдегиды в природеВанилин
В плодах ванили содержится
ароматический альдегид,
который придает им
характерный запах.
Ванилин применяется в
парфюмерии, кондитерской
промышленности, для
маскировки запахов некоторых
продуктов.
25.
Альдегиды в природеЦитраль
Запах
цитрусовых
обусловлен
данным
диеновым
альдегидом. Его применяют в качестве отдушки средств
бытовой химии, косметических и парфюмерных веществ.
26.
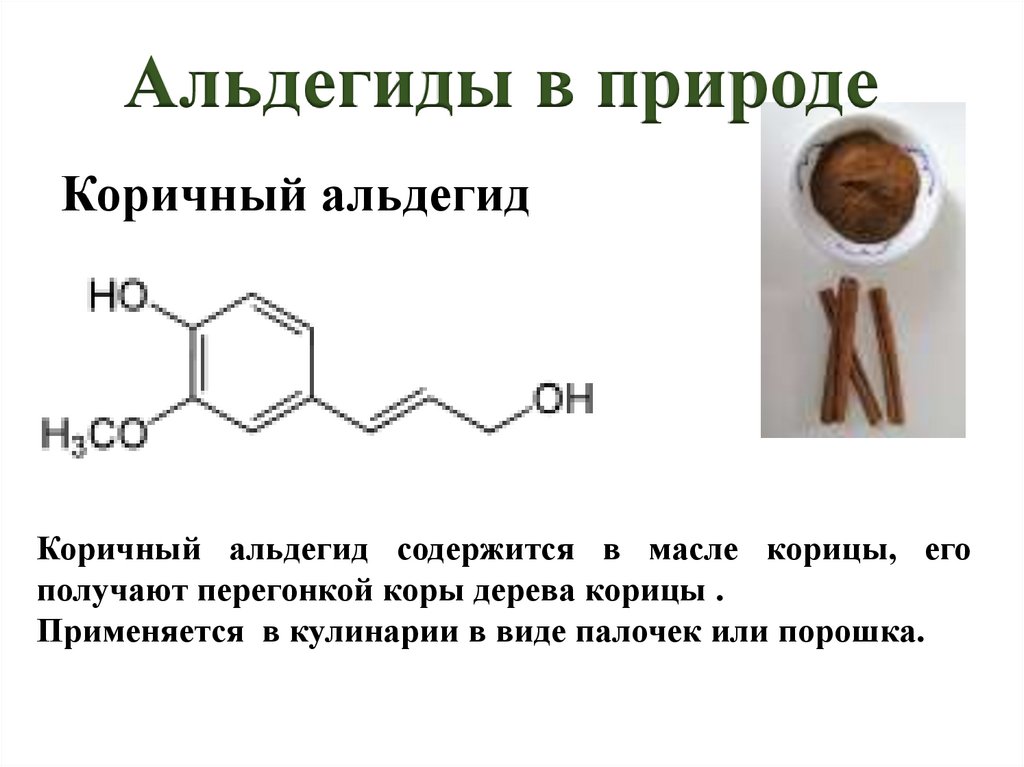
Альдегиды в природеКоричный альдегид
Коричный альдегид содержится в масле корицы, его
получают перегонкой коры дерева корицы .
Применяется в кулинарии в виде палочек или порошка.
27.
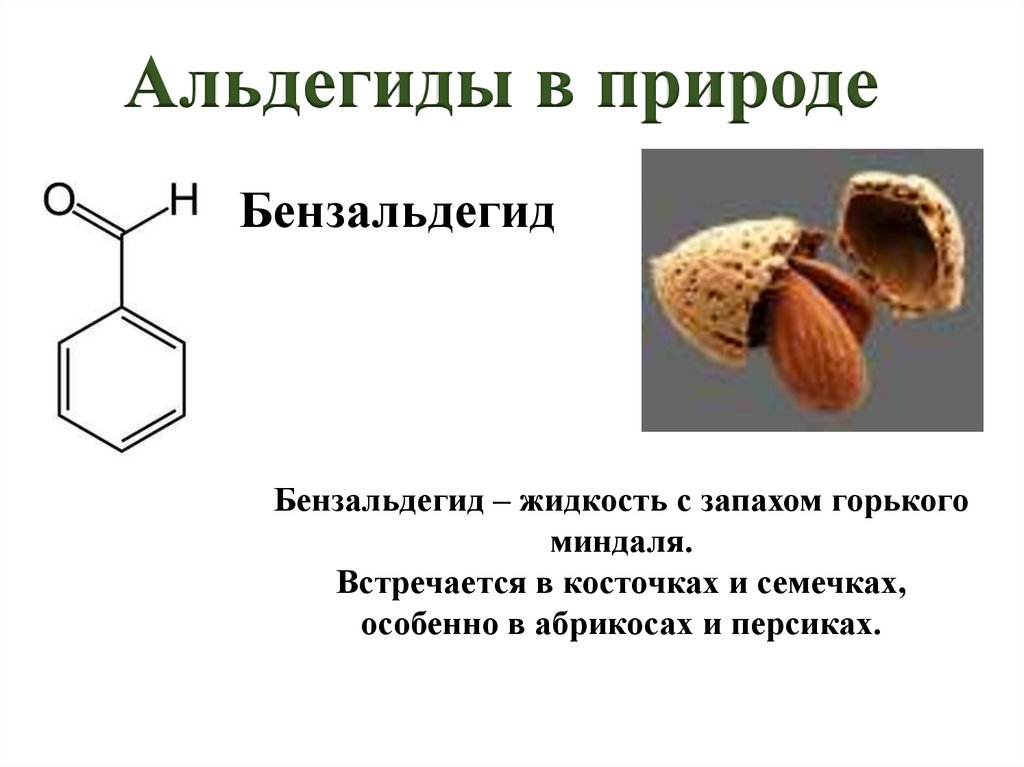
Альдегиды в природеБензальдегид
Бензальдегид – жидкость с запахом горького
миндаля.
Встречается в косточках и семечках,
особенно в абрикосах и персиках.
28.
Альдегиды в природеФенилэтаналь
Фенилэтаналь
по
сравнению
с
бензальдегидом лучше
соответствует
рецептору цветочного запаха.
Фенилэтаналь пахнет гиацинтом.
29.
Кетоны в природеГептанон-2
Это соединение представляет собой жидкость
гвоздичным запахом.
Гептаноном-2 обусловлен запах многих плодов
молочных продуктов, например, сыра «Рокфор»
с
и
30.
Кетоны в природеn-Гидроксифенилбутанон-2
Этот кетон обуславливает в основном запах
спелых ягод малины.
Его включают в состав синтетических
душистых композиций
31. Список используемых источников
•О.С. Габриелян. Учебник для общеобразовательныхучреждений. ХИМИЯ. Базовый уровень. 10 класс. –
М.: Дрофа, 2008
•О. С. Габриелян, И. Г. Остроумов. Химия 10 класс:
Настольная книга учителя. – М.: Дрофа, 2007
•О. С. Габриелян, А. В. Яшукова. Химия. 10 класс. Базовый
уровень. Методическое пособие. – М.: Дрофа, 2008.
•http://school-collection.edu.ru/collection/organic/
•http://ru.wikipedia.org/wiki/





















 chemistry
chemistry








