Similar presentations:
Углеводы (монозы, биозы)
1. Лекция № 10
УГЛЕВОДЫ(МОНОЗЫ, БИОЗЫ)
2. Биологическая роль углеводов
• Входят в состав клеток и тканей всех растительных и животныхорганизмов;
• По массе составляют основную часть органического вещества на земле
(в биосфере земли до 50% биомассы углеводов).
Углеводы образуются в процессе фотосинтеза
x CO2 + y H2O +солнечная энергия Cx(H2O)y + x O2
Живые организмы не способны синтезировать углеводы, поэтому их
получают из растительных источников .
Важнейшая биологическая роль углеводов – энергетическая
Cx(H2O)y + x O2 x CO2 + y H2O + 38 АТФ
Биологическое окисление (дегидрирование субстрата) осуществляется
посредством электронотранспортной цепи (передача 2Н+ и 2е на
конечный акцептор кислород с образованием Н2О)
3. Основные функции углеводов
• Источник энергии в метаболических процессах (врастениях – крахмал, в животных организмах –
гликоген);
• Структурные компоненты клеточных растений
(целлюлоза), бактерий (мурамин), грибов (хитин);
• Составные элементы жизненно-важных веществ
(нуклеиновых кислот, ферментов, витаминов);
• Выполняют функции структурных элементов
соединительной ткани: хондроитинсульфат (кожа
хрящи,
сухожилия),
гиалуроновая
кислота
(стекловидное тело глаза, пуповина, суставная
жидкость), гепарин (печень).
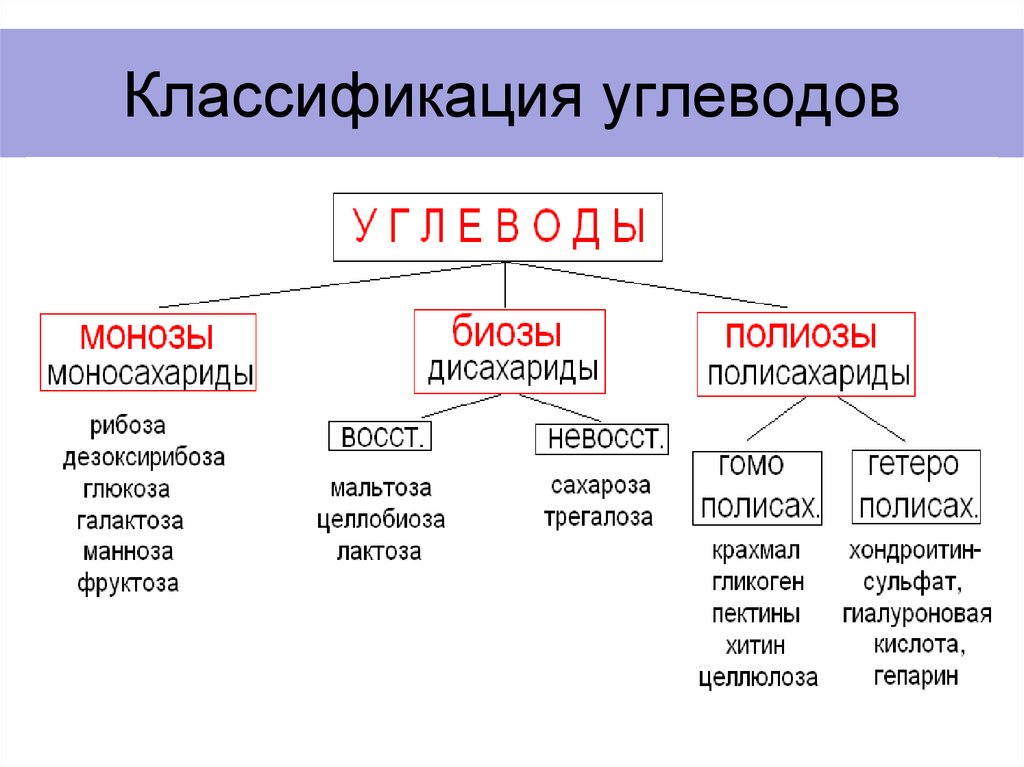
4. Классификация углеводов
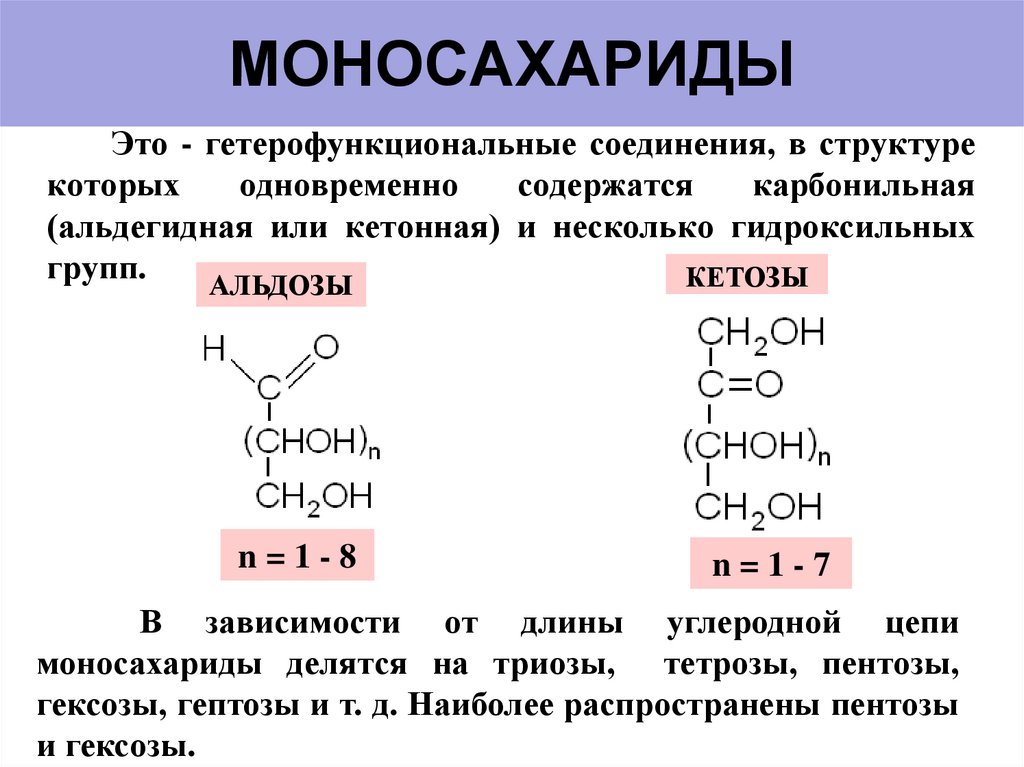
5. МОНОСАХАРИДЫ
Это - гетерофункциональные соединения, в структурекоторых
одновременно
содержатся
карбонильная
(альдегидная или кетонная) и несколько гидроксильных
групп.
КЕТОЗЫ
АЛЬДОЗЫ
n=1-8
n=1-7
В зависимости от длины углеродной цепи
моносахариды делятся на триозы, тетрозы, пентозы,
гексозы, гептозы и т. д. Наиболее распространены пентозы
и гексозы.
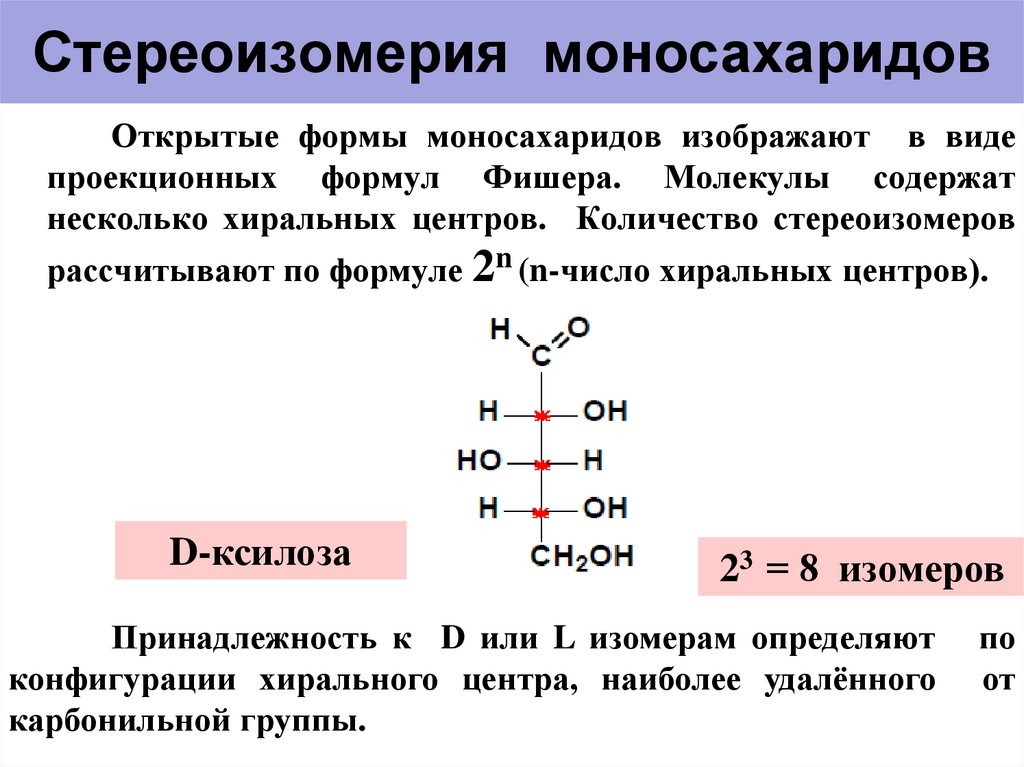
6. Стереоизомерия моносахаридов
Открытые формы моносахаридов изображают в видепроекционных формул Фишера. Молекулы содержат
несколько хиральных центров. Количество стереоизомеров
рассчитывают по формуле 2n (n-число хиральных центров).
D-ксилоза
23 = 8 изомеров
Принадлежность к D или L изомерам определяют
конфигурации хирального центра, наиболее удалённого
карбонильной группы.
по
от
7.
Энантиомеры – это стереозомеры,которые относятся друг к другу как
предмет и его зеркальное отображение.
Диастереоизомеры
не
являются
зеркальным отображением друг друга.
Эпимеры – это диастереоизомеры,
отличающиеся конфигурацией только
одного углеродного атома
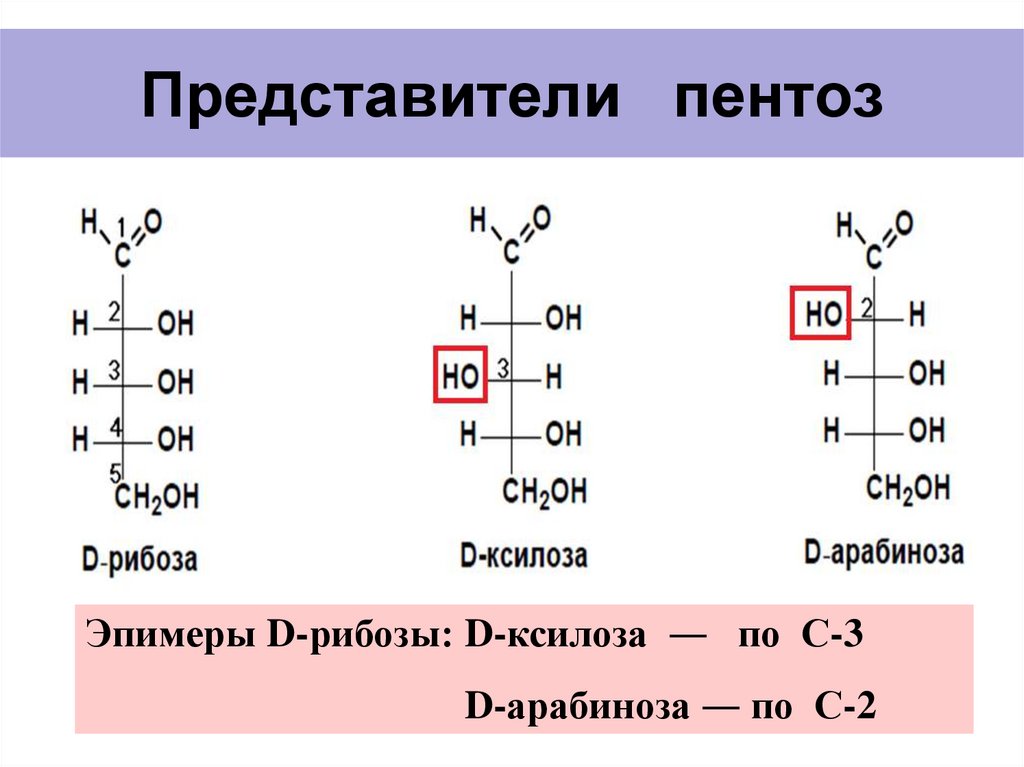
8. Представители пентоз
Эпимеры D-рибозы: D-ксилоза ― по С-3D-арабиноза ― по С-2
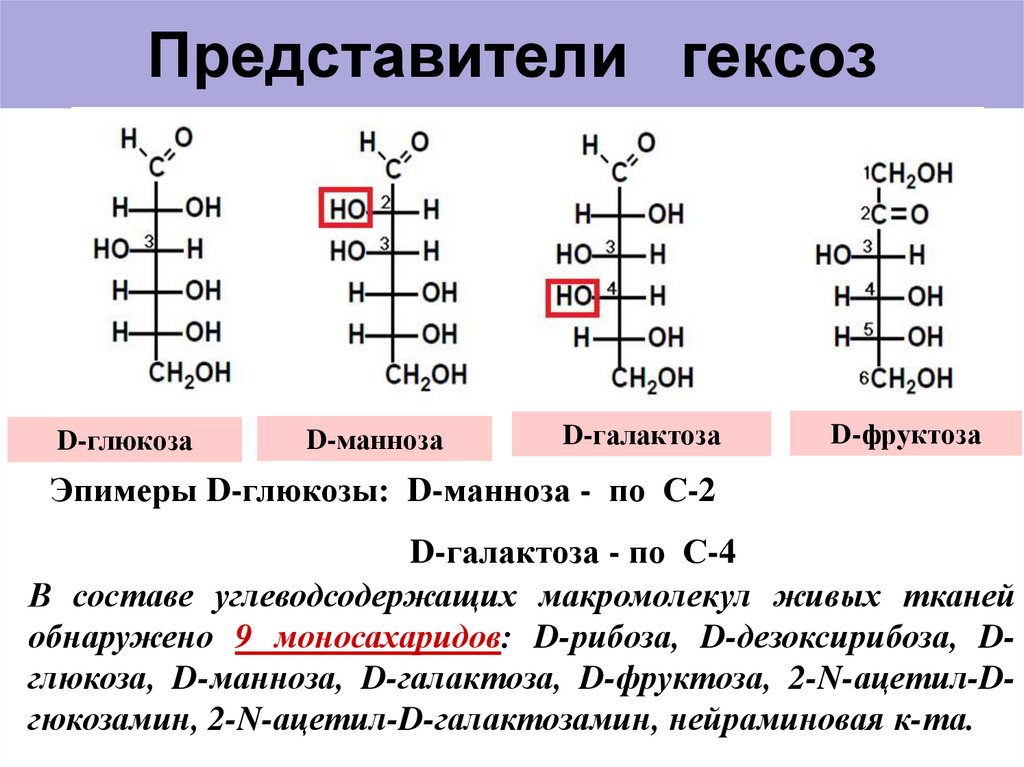
9. Представители гексоз
D-глюкозаD-манноза
D-галактоза
D-фруктоза
Эпимеры D-глюкозы: D-манноза - по С-2
D-галактоза - по С-4
В составе углеводсодержащих макромолекул живых тканей
обнаружено 9 моносахаридов: D-рибоза, D-дезоксирибоза, Dглюкоза, D-манноза, D-галактоза, D-фруктоза, 2-N-ацетил-Dгюкозамин, 2-N-ацетил-D-галактозамин, нейраминовая к-та.
10. Производные моносахаридов
1. ДезоксисахараD - дезоксирибоза
2. Аминосахара
2-амино2-дезоксиD-глюкоза
2-амино-2дезокси-Dгалактоза
2-N-ацетилD-гюкозамин
2-N-ацетил-Dгалактозамин
Нейраминовая
к-та
11.
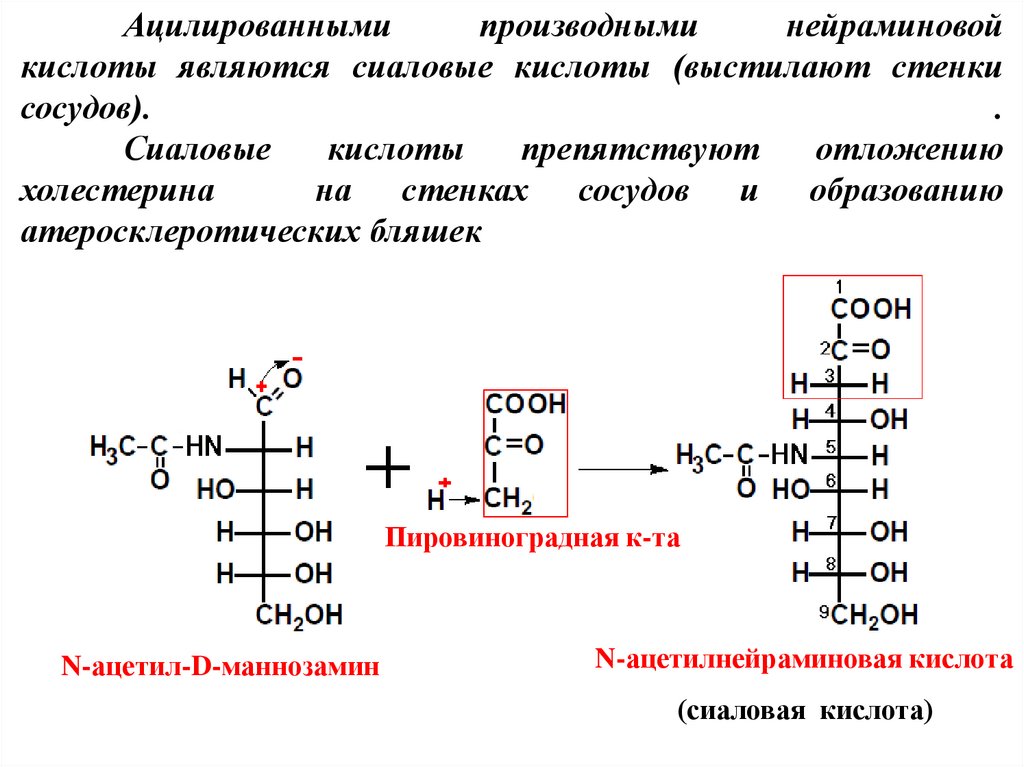
Ацилированнымипроизводными
нейраминовой
кислоты являются сиаловые кислоты (выстилают стенки
сосудов).
.
Сиаловые
кислоты
препятствуют
отложению
холестерина
на стенках сосудов и образованию
атеросклеротических бляшек
Пировиноградная к-та
N-ацетил-D-маннозамин
N-ацетилнейраминовая кислота
(сиаловая кислота)
12.
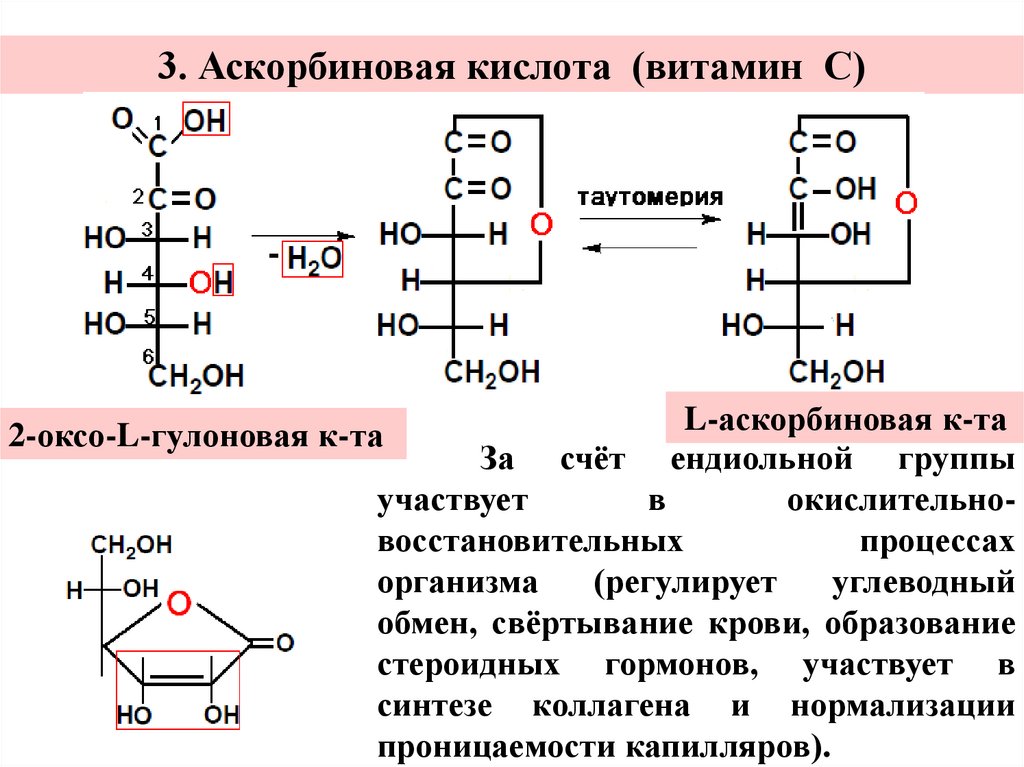
3. Аскорбиновая кислота (витамин С)L-аскорбиновая к-та
За счёт ендиольной группы
участвует
в
окислительновосстановительных
процессах
организма
(регулирует
углеводный
обмен, свёртывание крови, образование
стероидных гормонов, участвует в
синтезе коллагена и нормализации
проницаемости капилляров).
2-оксо-L-гулоновая к-та
13. Циклические формы моносахаридов (формулы Колли-Толленса)
При замыкании цикла между С-1 и С-5 углероднымиатомами образуются устойчивые пиранозные циклы
полуацетальный
гидроксил
+δ
Н
НО
Н
Н
1
С
О
-δ
Н
ОН
Н
ОН
5
ОН
СН2ОН
D - глюкоза
ОН
Н
С
Н
НО
Н
Н
Н
НО
С
ОН
Н О
ОН
+
Н
НО
Н
Н
СН2ОН
ОН
Н О
ОН
СН2ОН
α, D- глюкопираноза
β, D-глюкопираноза
аномеры
14.
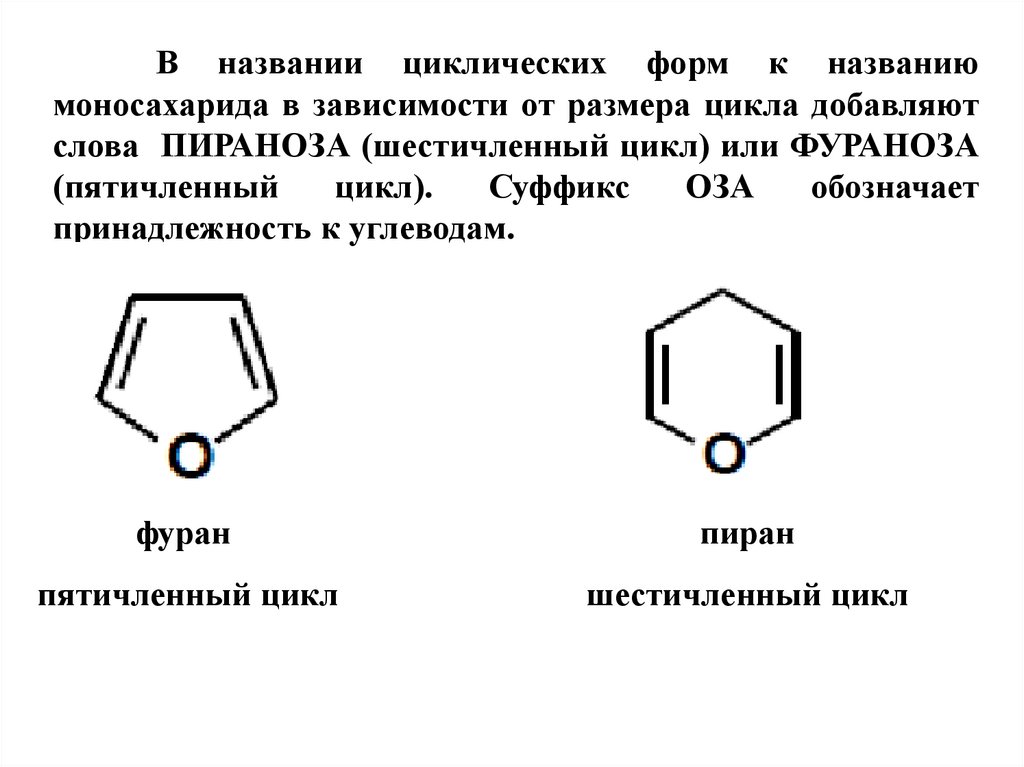
В названии циклических форм к названиюмоносахарида в зависимости от размера цикла добавляют
слова ПИРАНОЗА (шестичленный цикл) или ФУРАНОЗА
(пятичленный
цикл).
Суффикс
ОЗА
обозначает
принадлежность к углеводам.
фуран
пиран
пятичленный цикл
шестичленный цикл
15.
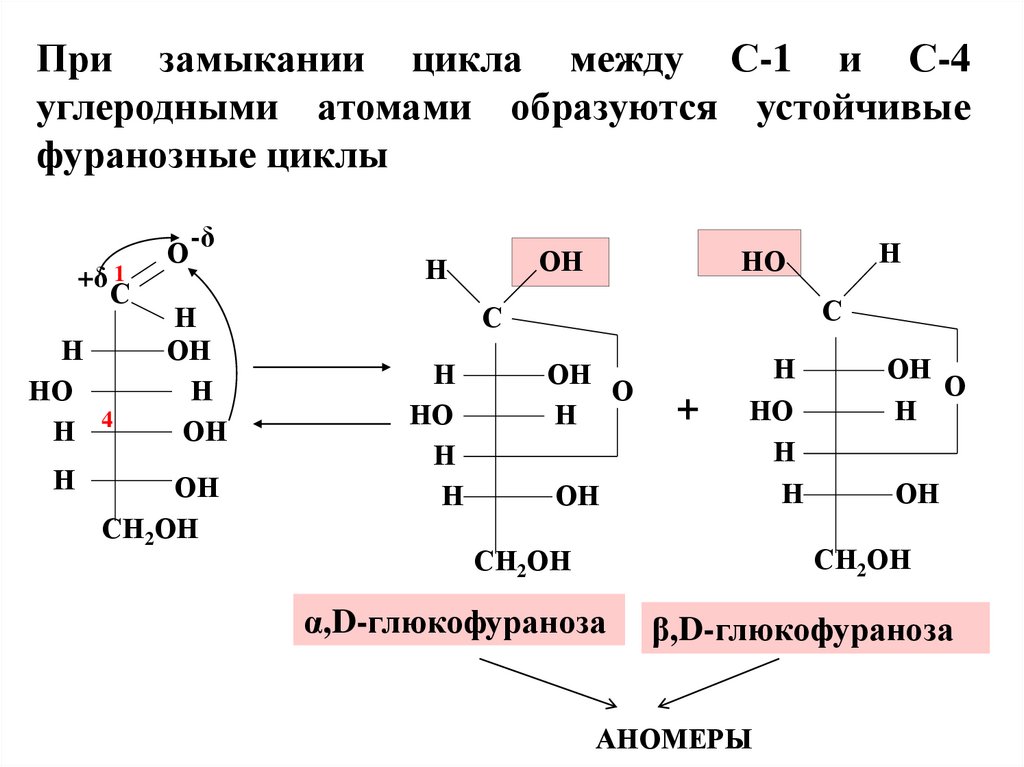
При замыкании цикла между С-1 и С-4углеродными атомами образуются устойчивые
фуранозные циклы
+δ 1
С
Н
НО
Н
Н
4
О
-δ
Н
ОН
Н
ОН
ОН
СН2ОН
ОН
Н
С
С
Н
НО
Н
Н
Н
НО
ОН
О
Н
ОН
+
Н
НО
Н
Н
ОН
О
Н
ОН
СН2ОН
СН2ОН
α,D-глюкофураноза
β,D-глюкофураноза
АНОМЕРЫ
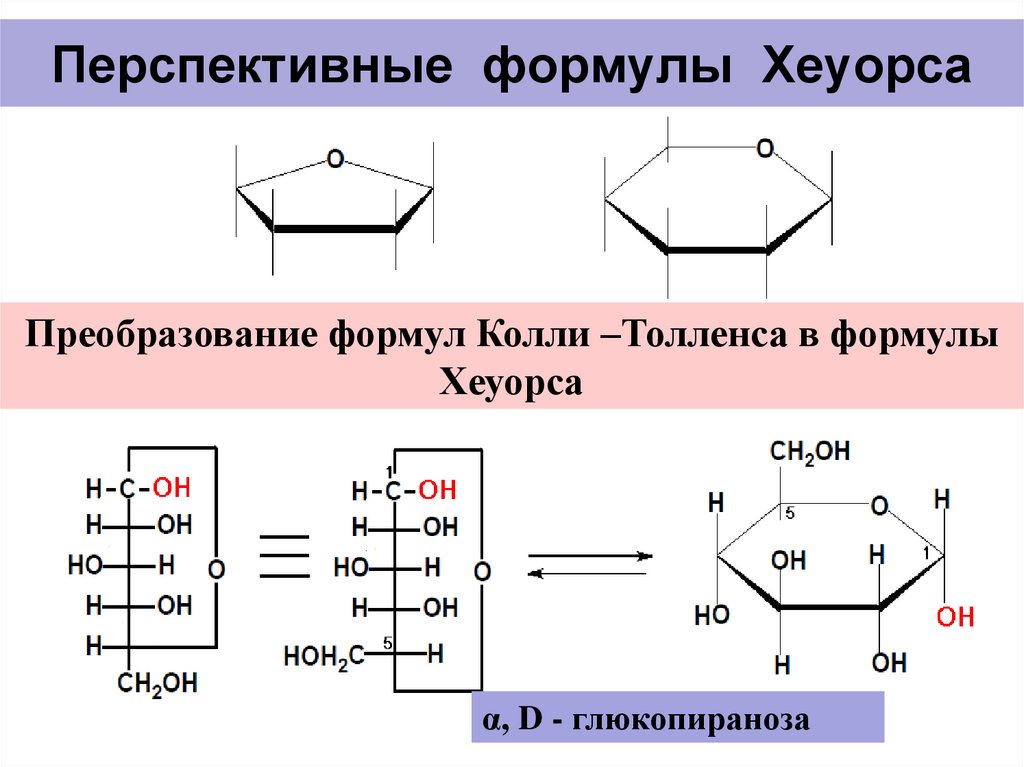
16. Перспективные формулы Хеуорса
Преобразование формул Колли –Толленса в формулыХеуорса
α, D - глюкопираноза
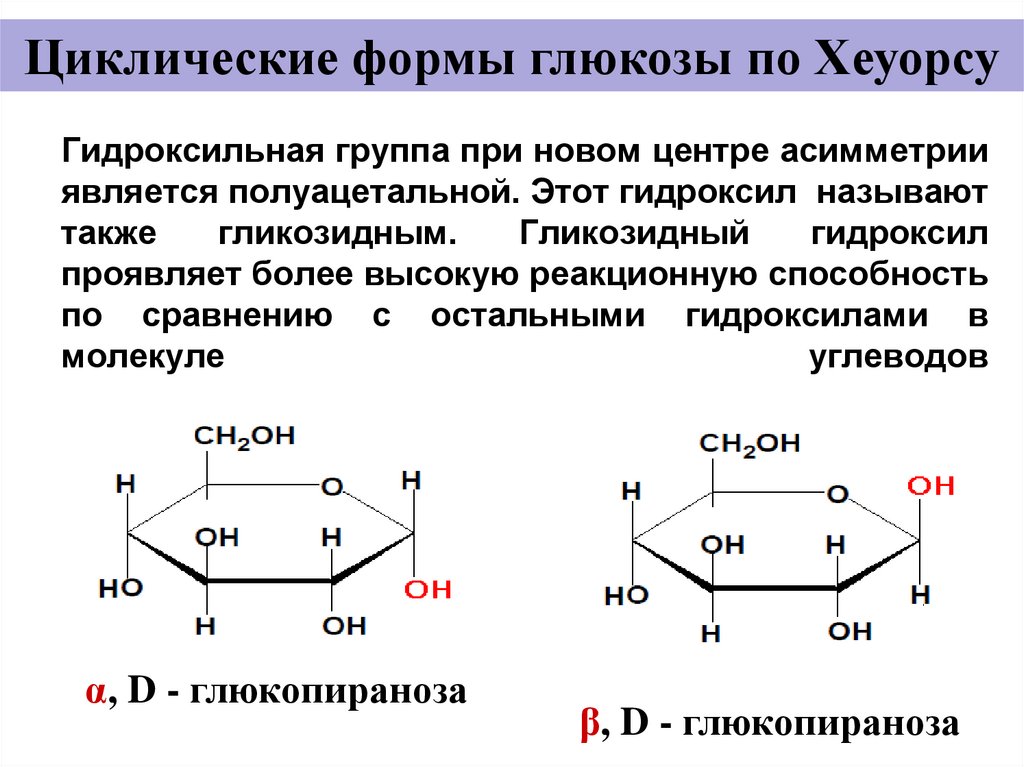
17. Гидроксильная группа при новом центре асимметрии является полуацетальной. Этот гидроксил называют также гликозидным.
Циклические формы глюкозы по ХеуорсуГидроксильная группа при новом центре асимметрии
является полуацетальной. Этот гидроксил называют
также
гликозидным.
Гликозидный
гидроксил
проявляет более высокую реакционную способность
по сравнению с остальными гидроксилами в
молекуле
углеводов
α, D - глюкопираноза
β, D - глюкопираноза
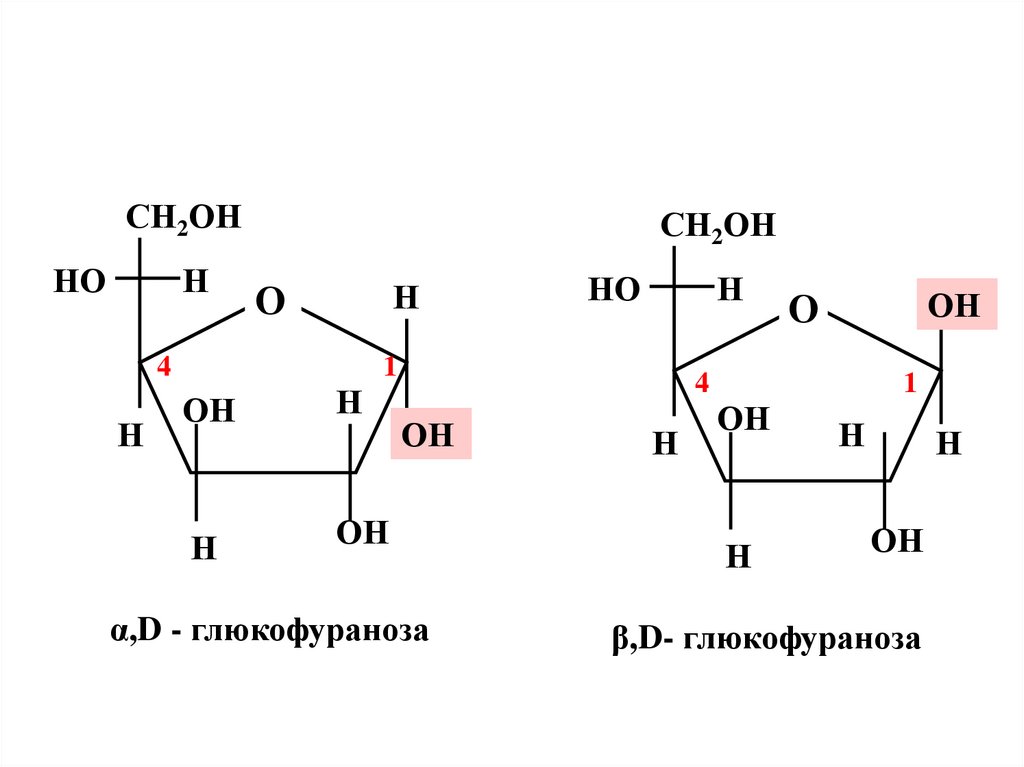
18.
СН2ОННО
Н
СН2ОН
Н
О
4
Н
НО
Н
1
ОН
Н
Н
ОН
ОН
О
4
ОН
α,D - глюкофураноза
Н
1
ОН
Н
Н
Н
ОН
β,D- глюкофураноза
19.
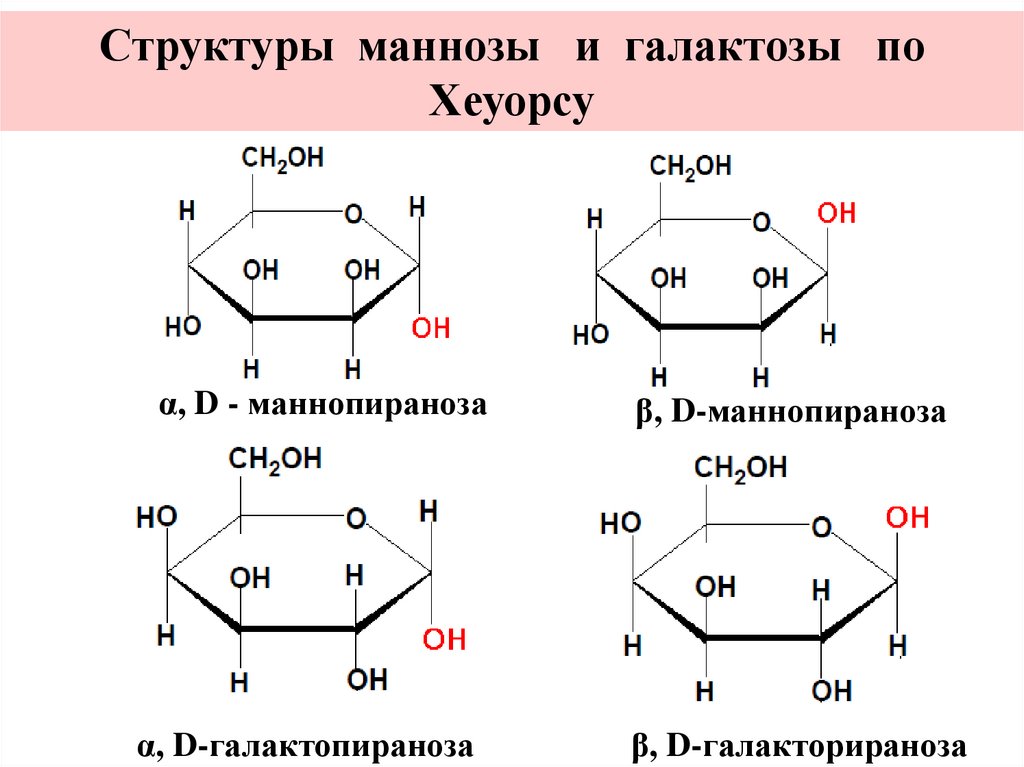
Структуры маннозы и галактозы поХеуорсу
α, D - маннопираноза
α, D-галактопираноза
β, D-маннопираноза
β, D-галакторираноза
20.
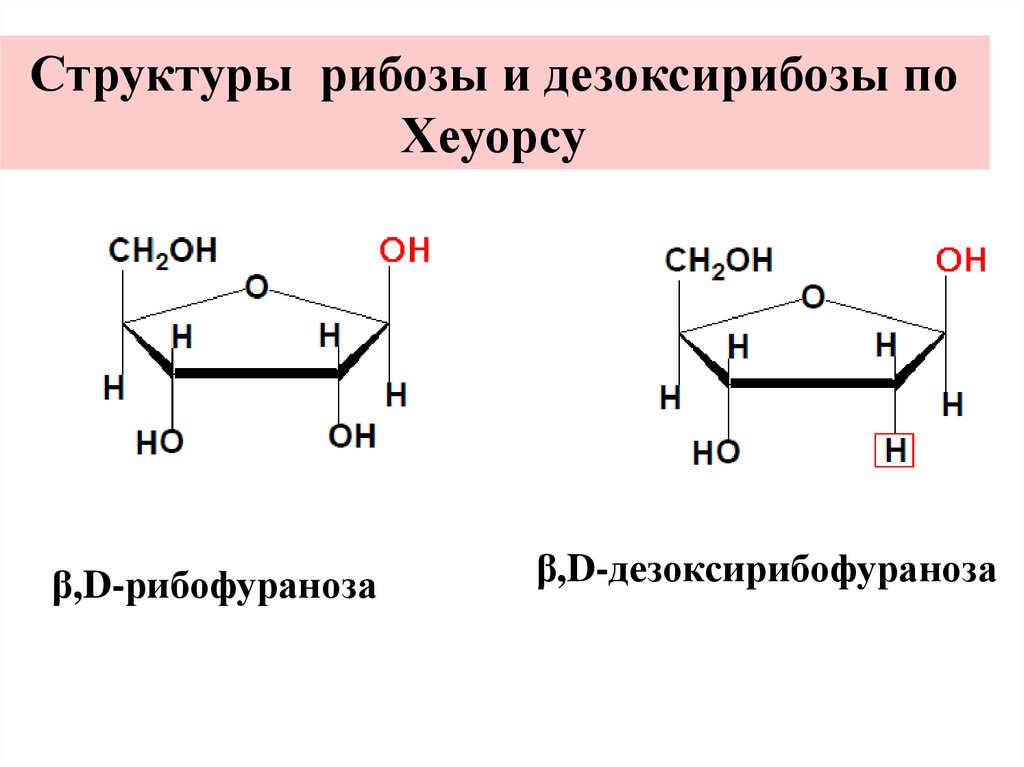
Структуры рибозы и дезоксирибозы поХеуорсу
β,D-рибофураноза
β,D-дезоксирибофураноза
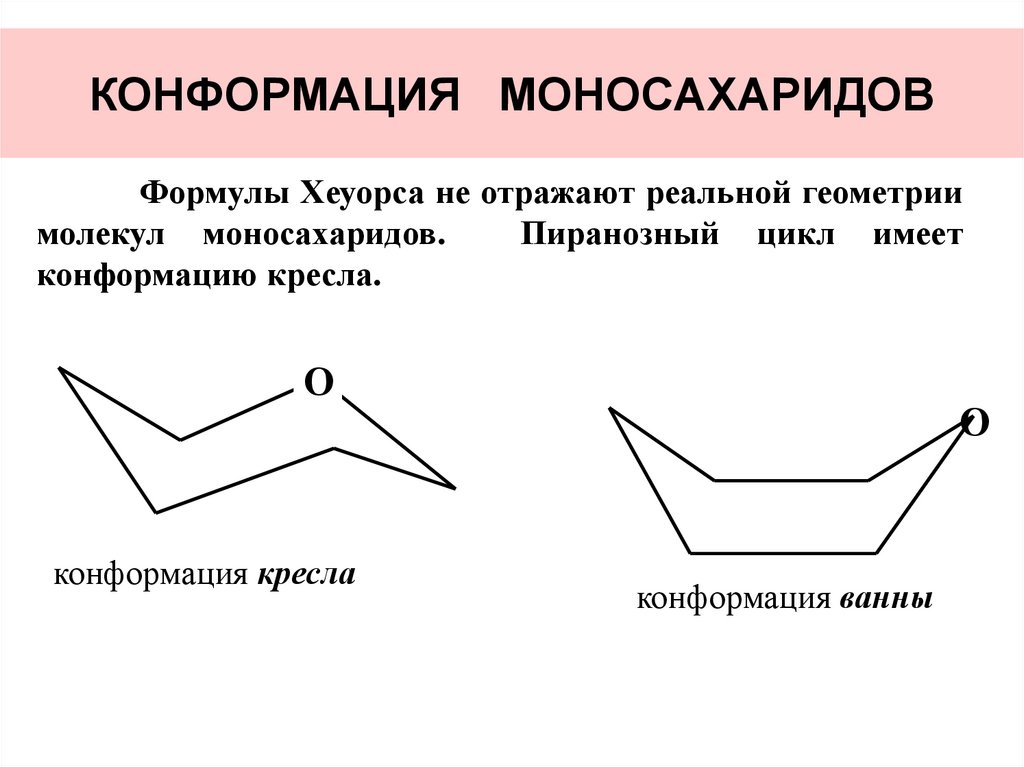
21. КОНФОРМАЦИЯ МОНОСАХАРИДОВ
Формулы Хеуорса не отражают реальной геометриимолекул моносахаридов.
Пиранозный цикл имеет
конформацию кресла.
О
конформация кресла
О
конформация ванны
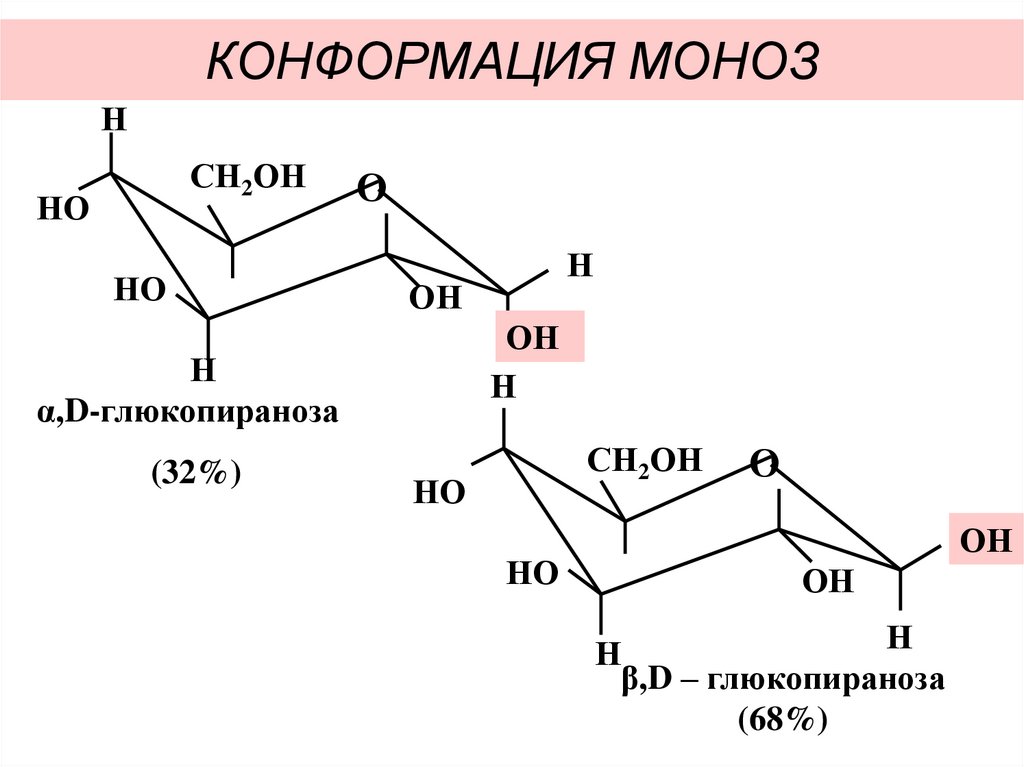
22. КОНФОРМАЦИЯ МОНОЗ
НСН2ОН
НО
НО
О
ОН
ОН
Н
Н
α,D-глюкопираноза
(32%)
Н
СН2ОН
НО
НО
О
ОН
ОН
Н
Н
β,D – глюкопираноза
(68%)
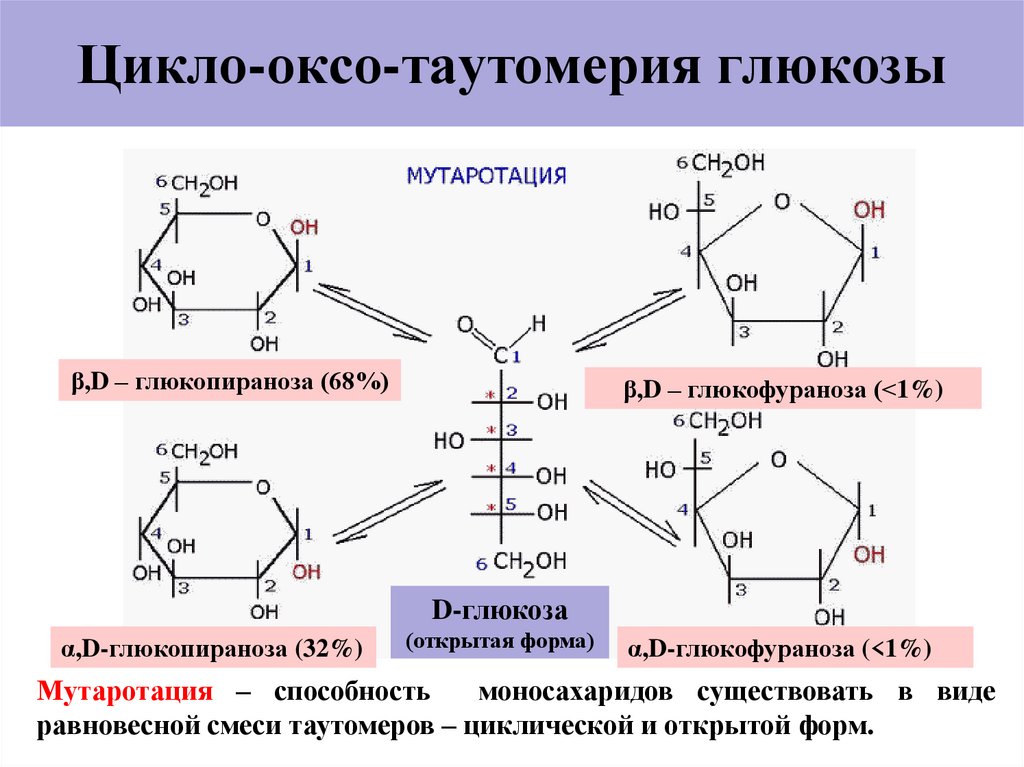
23. Цикло-оксо-таутомерия глюкозы
β,D – глюкопираноза (68%)β,D – глюкофураноза (<1%)
D-глюкоза
α,D-глюкопираноза (32%)
(открытая форма)
α,D-глюкофураноза (<1%)
Мутаротация – способность
моносахаридов существовать в виде
равновесной смеси таутомеров – циклической и открытой форм.
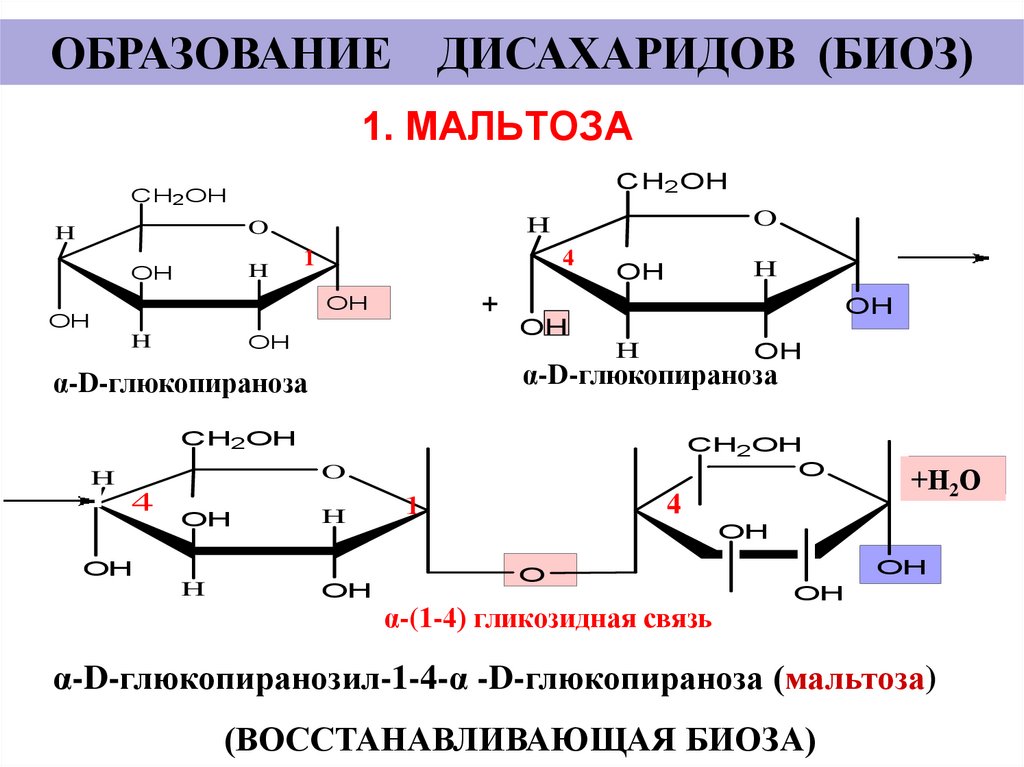
24. 1. МАЛЬТОЗА
ОБРАЗОВАНИЕ ДИСАХАРИДОВ (БИОЗ)1. МАЛЬТОЗА
CH2 OH
CH2 OH
H
OH
1
4
H
OH
+
OH
OH
H
O
H
O
H
OH
OH
OH
H
OH
α-D-глюкопираноза
α-D-глюкопираноза
CH2 OH
CH2 OH
O
O
H
4
OH
H
OH
H
OH
4
1
+Н2О
OH
OH
O
α-(1-4) гликозидная связь
OH
α-D-глюкопиранозил-1-4-α -D-глюкопираноза (мальтоза)
(ВОССТАНАВЛИВАЮЩАЯ БИОЗА)
25.
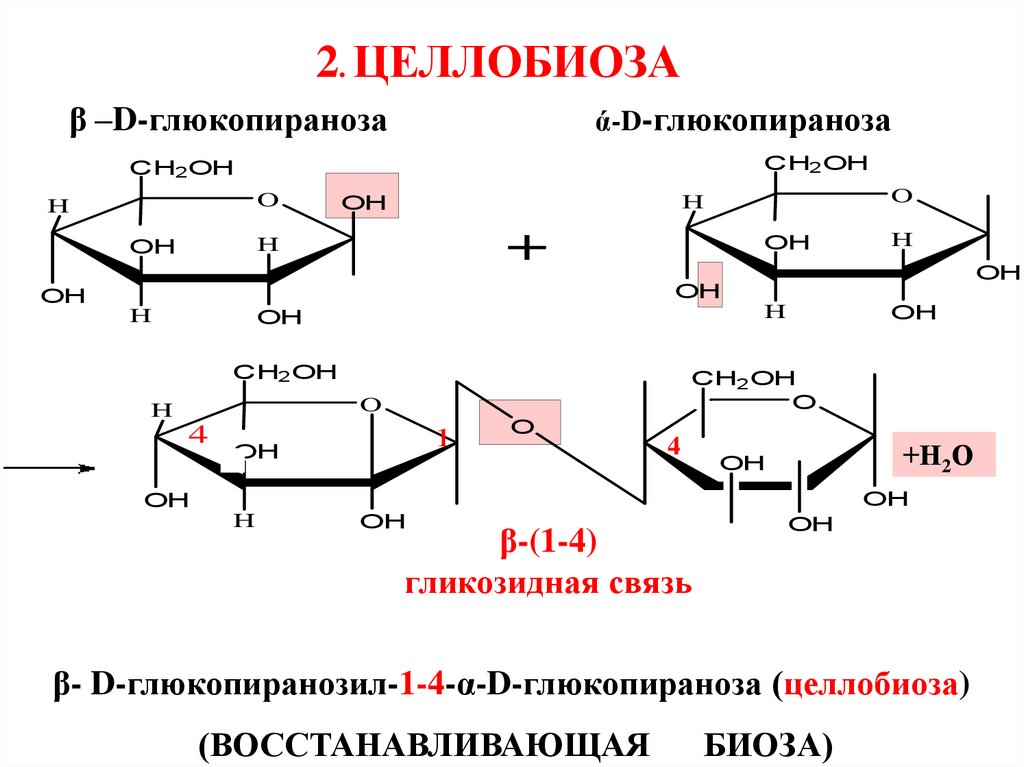
2. ЦЕЛЛОБИОЗАβ –D-глюкопираноза
ά-D-глюкопираноза
CH2 OH
CH2 OH
O
H
+
H
OH
O
H
OH
OH
H
OH
OH
OH
H
H
OH
CH2 OH
CH2 OH
O
O
H
4
OH
1
OH
O
4
+Н2О
OH
OH
OH
H
OH
β-(1-4)
гликозидная связь
OH
β- D-глюкопиранозил-1-4-α-D-глюкопираноза (целлобиоза)
(ВОССТАНАВЛИВАЮЩАЯ
БИОЗА)
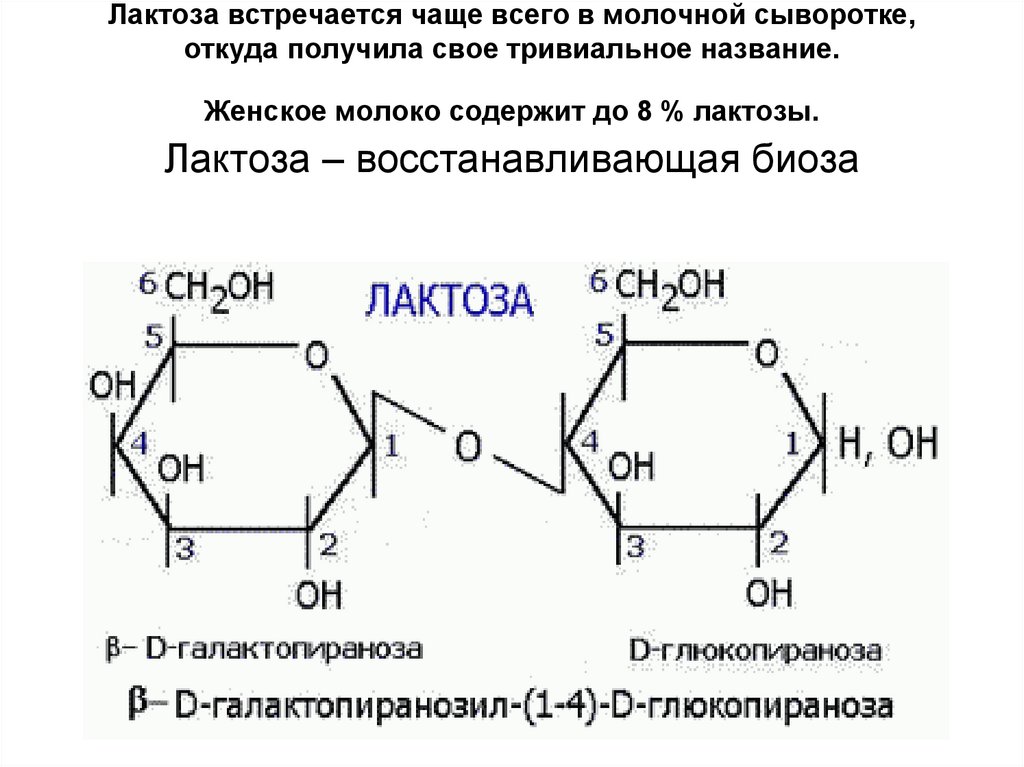
26. Лактоза встречается чаще всего в молочной сыворотке, откуда получила свое тривиальное название. Женское молоко содержит до 8 %
лактозы.Лактоза – восстанавливающая биоза
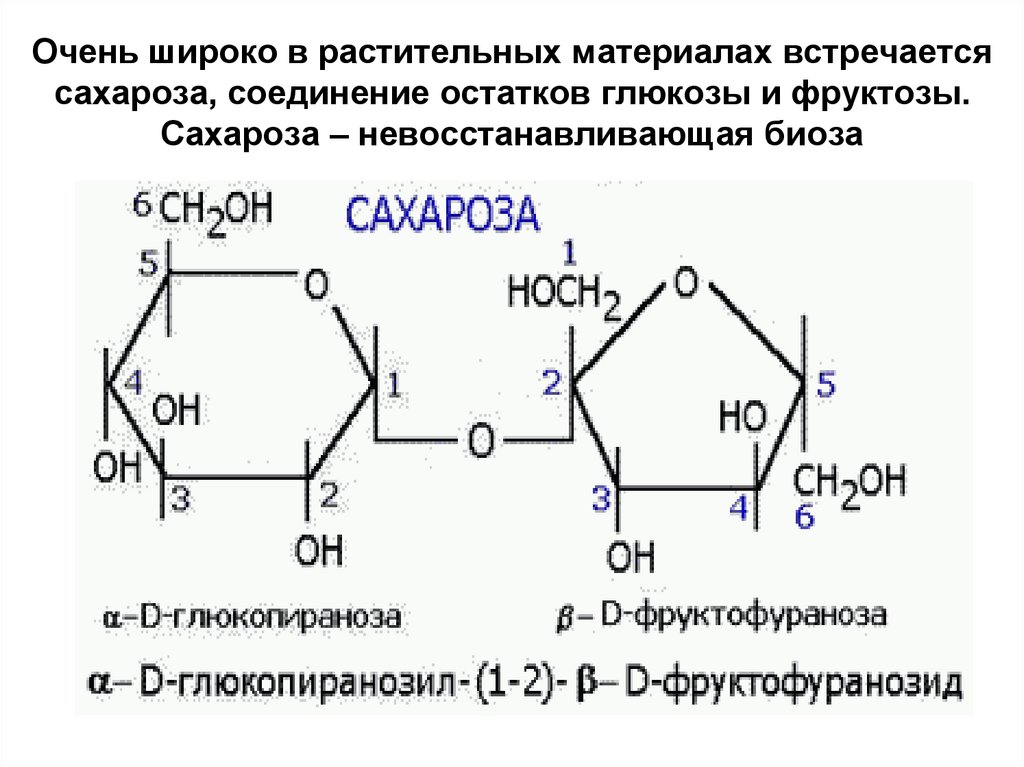
27. Очень широко в растительных материалах встречается сахароза, соединение остатков глюкозы и фруктозы. Сахароза –
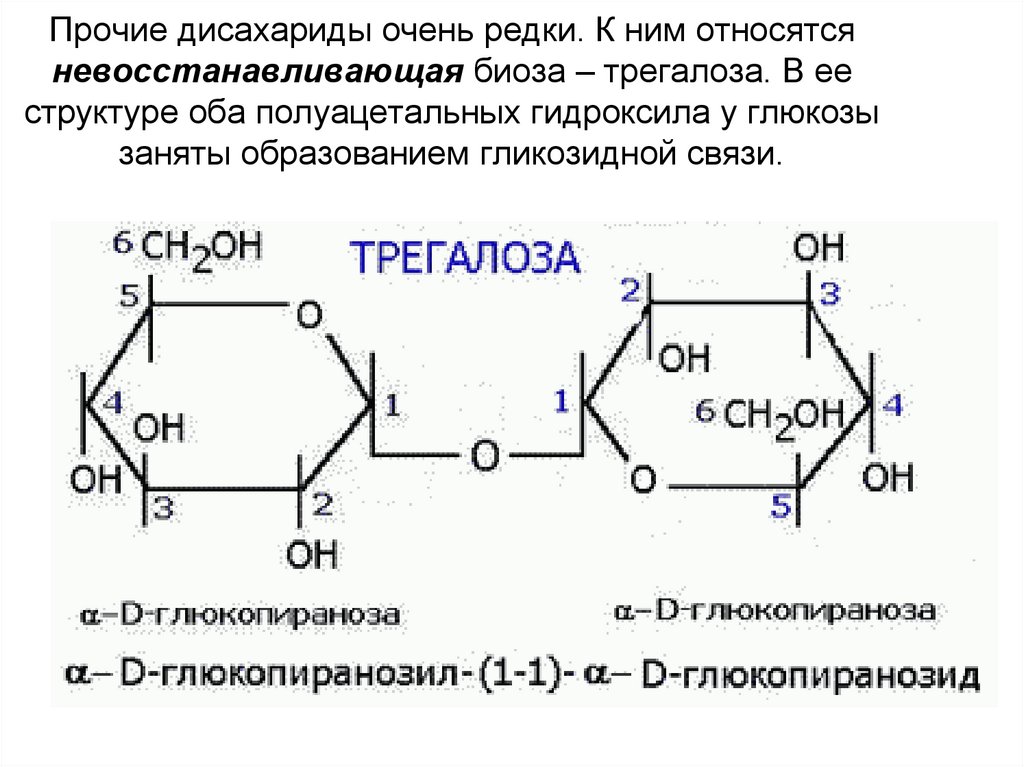
невосстанавливающая биоза28. Прочие дисахариды очень редки. К ним относятся невосстанавливающая биоза – трегалоза. В ее структуре оба полуацетальных
гидроксила у глюкозызаняты образованием гликозидной связи.
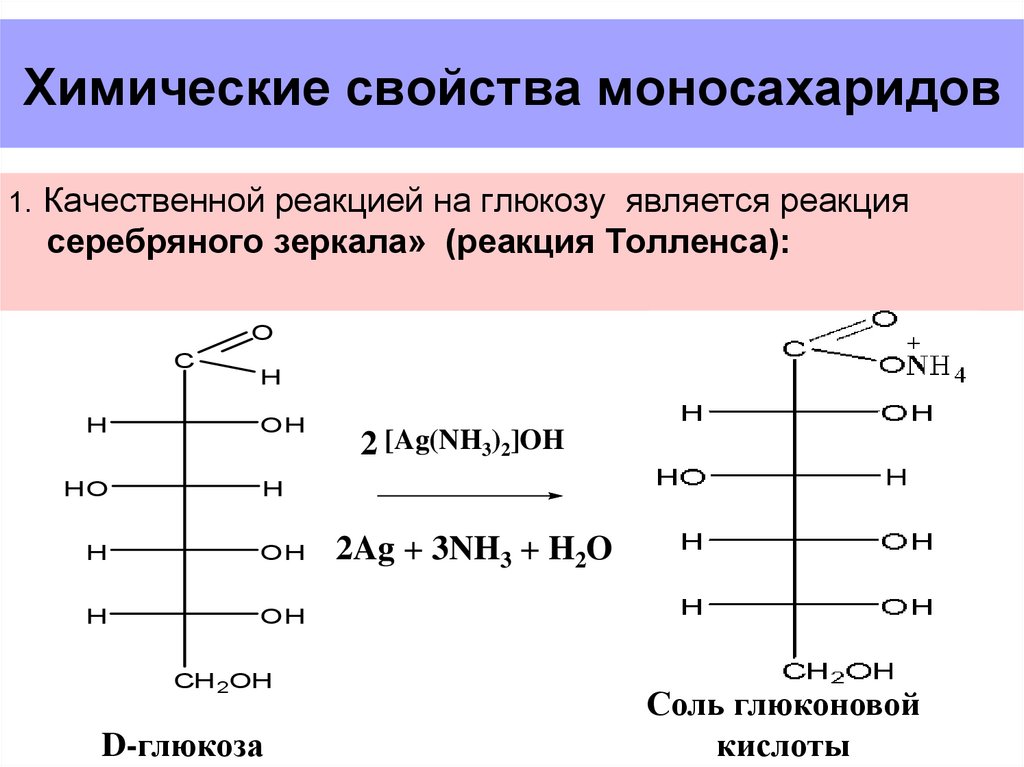
29. Химические свойства моносахаридов
1. Качественной реакцией на глюкозу является реакциясеребряного зеркала» (реакция Толленса):
O
C
H
HO
H
OH
2 [Ag(NH3)2]OH
H
H
OH
H
OH
CH 2 OH
D-глюкоза
2Ag + 3NH3 + H2O
Соль глюконовой
кислоты
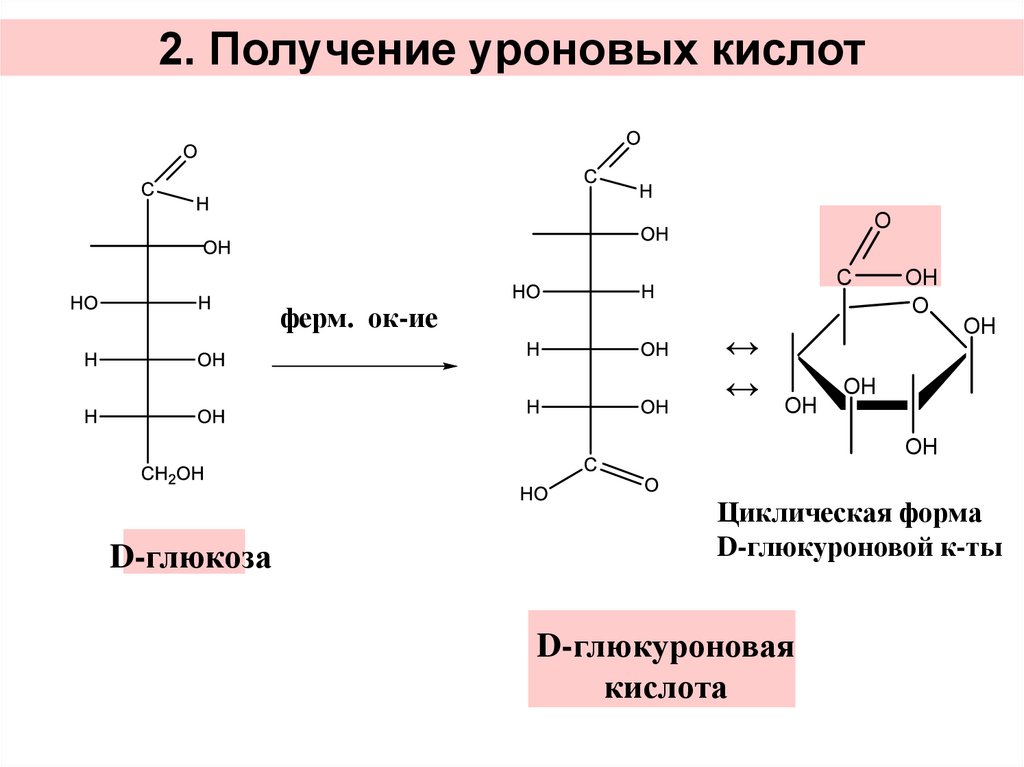
30. 2. Получение уроновых кислот
OC
ферм. ок-ие
↔
↔
OH
O
OH
OH
OH
OH
D-глюкоза
Циклическая форма
D-глюкуроновой к-ты
D-глюкуроновая
кислота
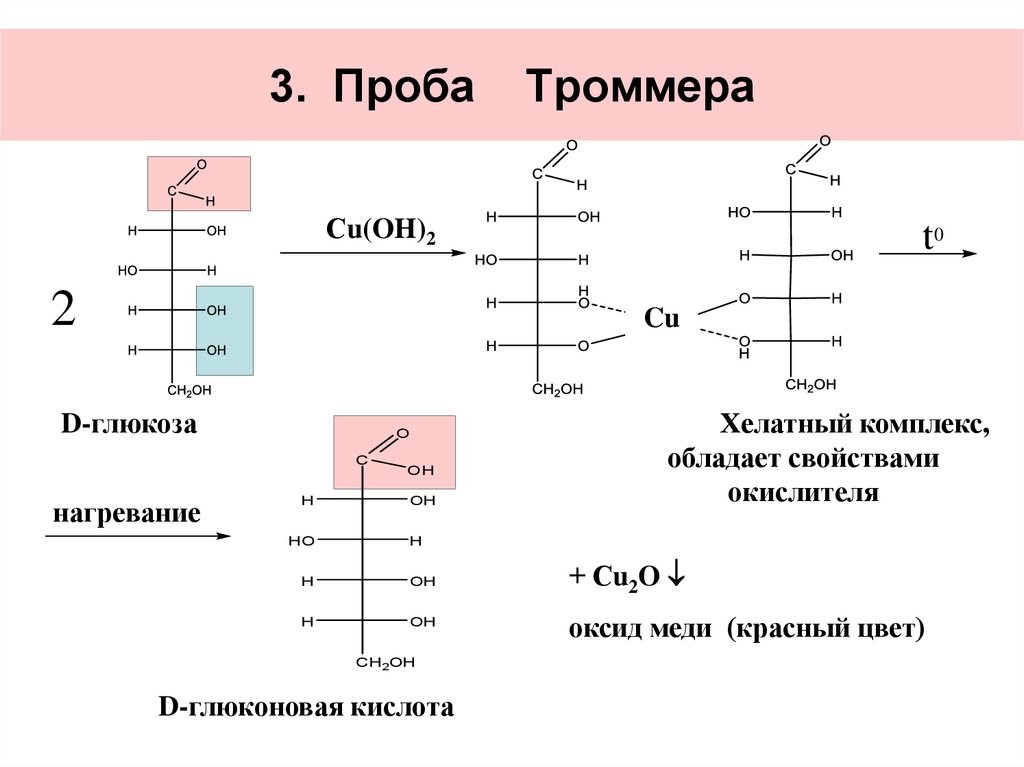
31. 3. Проба Троммера
Сu(OH)22
t0
Cu
Cu
D-глюкоза
O
C
нагревание
H
HO
OH
OH
Хелатный комплекс,
обладает свойствами
окислителя
H
H
OH
+ Сu2O
H
OH
оксид меди (красный цвет)
CH2 OH
D-глюконовая кислота
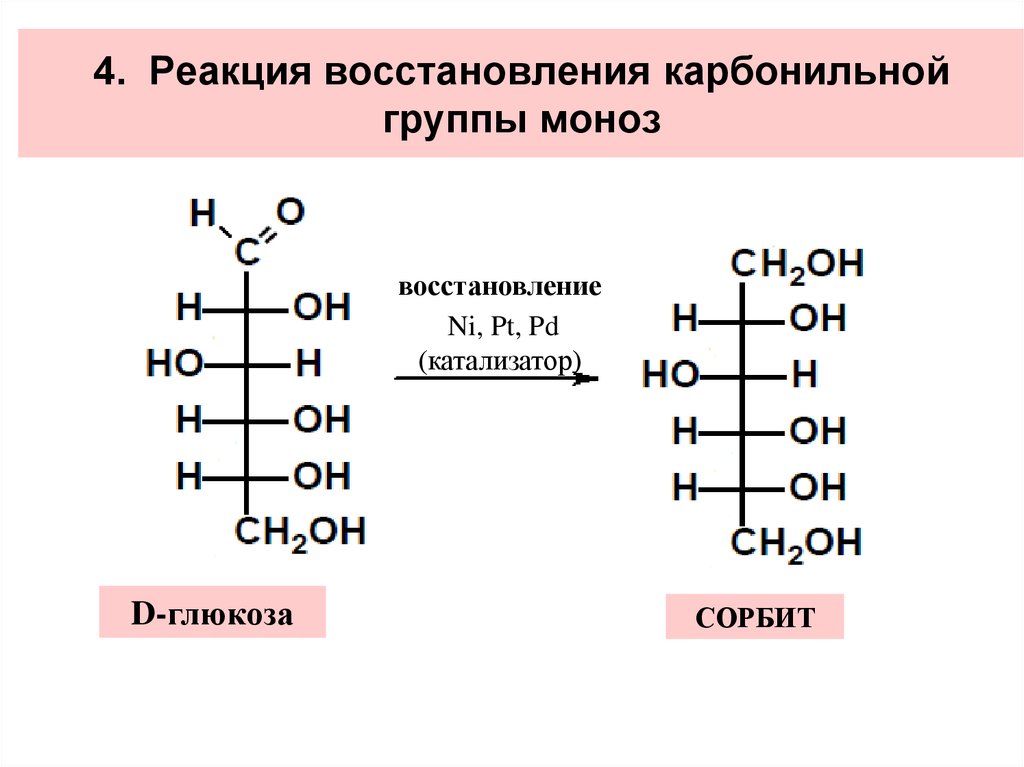
32. 4. Реакция восстановления карбонильной группы моноз
восстановлениеNi, Pt, Pd
(катализатор)
D-глюкоза
СОРБИТ
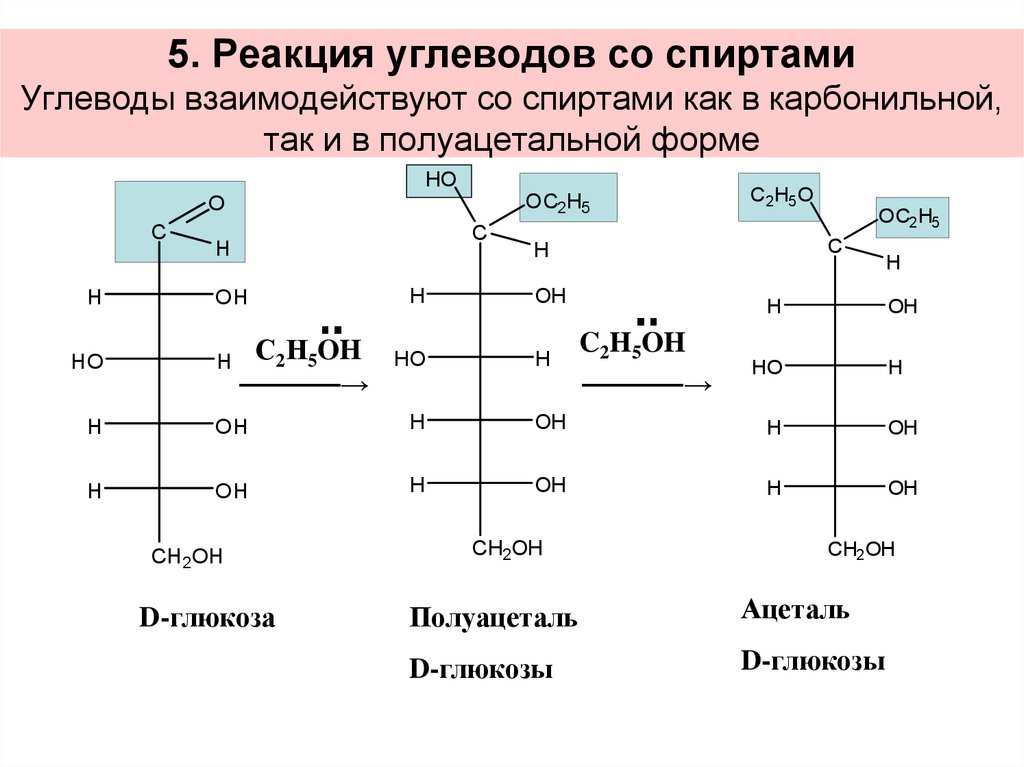
33. 5. Реакция углеводов со спиртами Углеводы взаимодействуют со спиртами как в карбонильной, так и в полуацетальной форме
HOOC2 H5
O
C
H
HO
C
H
OH
H
С2Н5OH
─────→
H
HO
C 2 H5 O
C
H
OH
H
OC2 H5
H
C2H5OH
─────→
H
OH
HO
H
H
OH
H
OH
H
OH
H
OH
H
OH
H
OH
CH 2 OH
D-глюкоза
CH2 OH
CH2 OH
Полуацеталь
Ацеталь
D-глюкозы
D-глюкозы
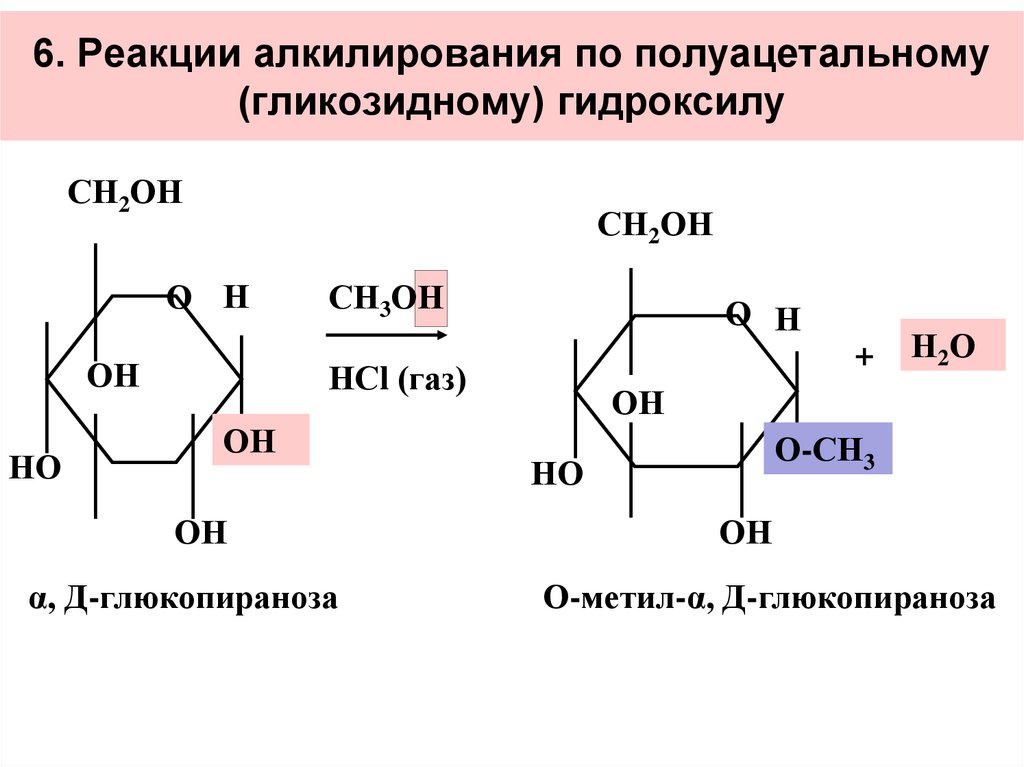
34. 6. Реакции алкилирования по полуацетальному (гликозидному) гидроксилу
СН2ОНСН2ОН
О Н
ОН
НО
СН3ОН
О Н
+
НСl (газ)
ОН
ОН
α, Д-глюкопираноза
Н2О
ОН
О-СН3
НО
ОН
О-метил-α, Д-глюкопираноза
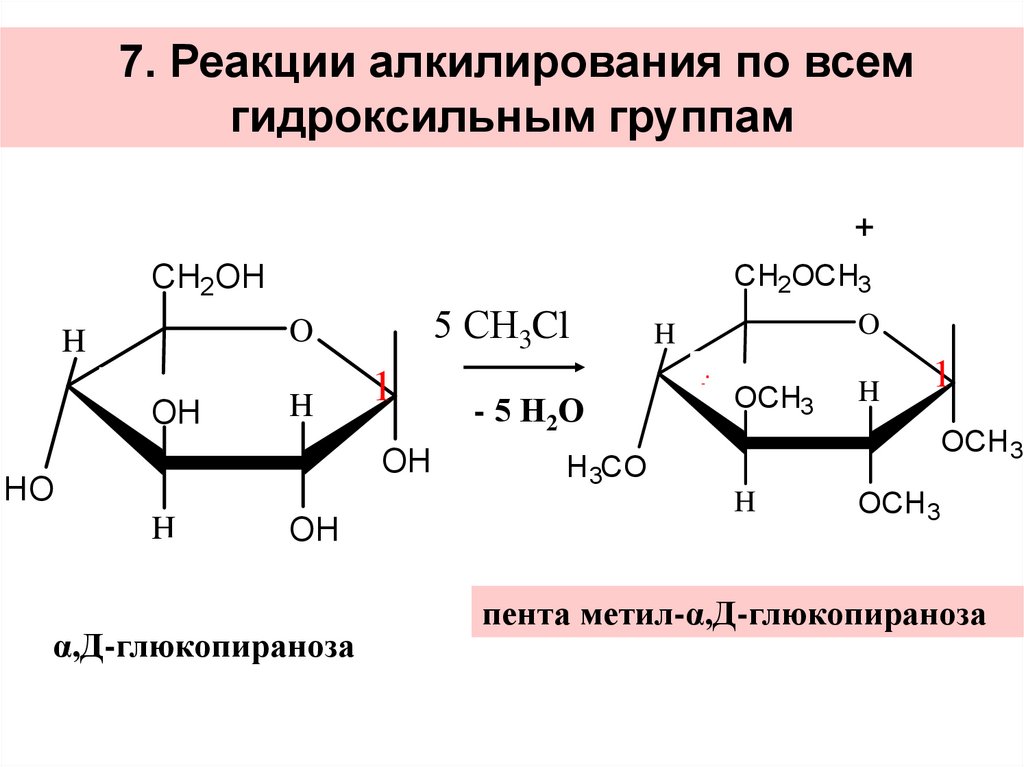
35.
7. Реакции алкилирования по всемгидроксильным группам
+
CH2 OH
CH2 OCH3
5 СН3Cl
O
H
4
OH
H
1
OH
HO
H
OH
α,Д-глюкопираноза
- 5 Н2О
O
H
4
OCH3
H
1
OCH 3
H 3CO
H
OCH 3
пента метил-α,Д-глюкопираноза
36.
8. Реакции ацилирования по всемгидроксильным группам
CH2 OH
(СН3СО)2О
O
H
4
OH
H
1
-5 СН3СООН
CH2OCOCH3
O
H
4
OCOCH3H
OH
HO
H
OH
α,Д-глюкопираноза
1
OCOCH 3
H 3COCO
H
OCOCH 3
пента ацетил-α,Д-глюкопираноза
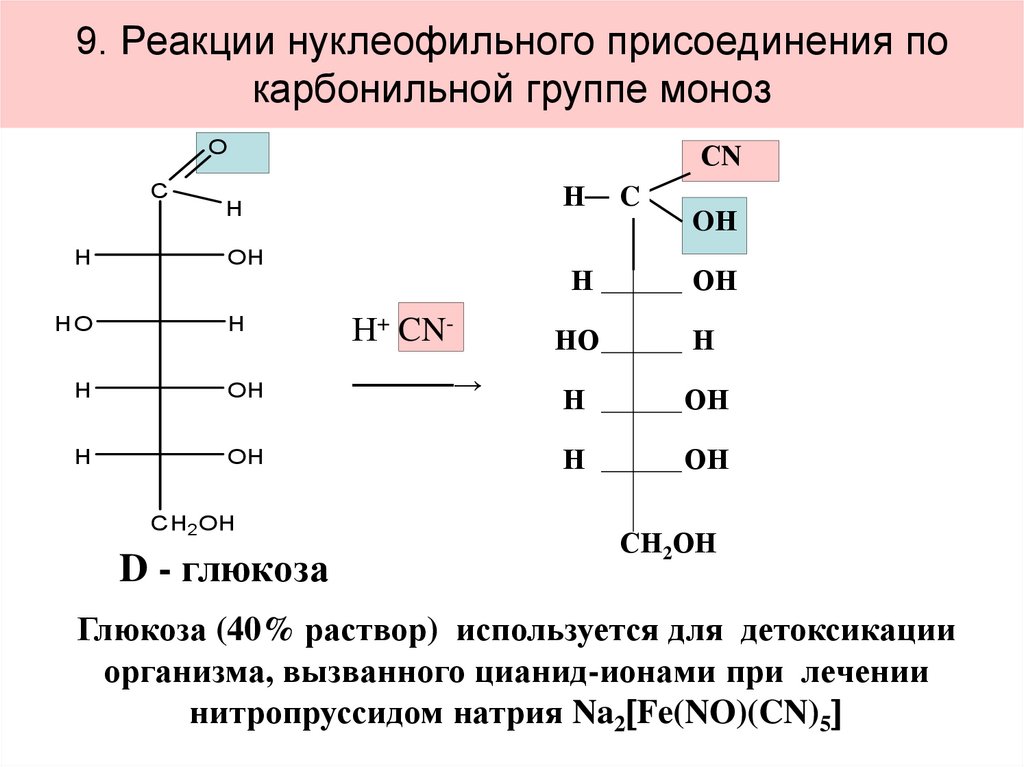
37. 9. Реакции нуклеофильного присоединения по карбонильной группе моноз
OC
H
СN
Н
H
OH
Н
H
Н+ CN-
H
OH
─────→
H
OH
HO
CH2 OH
D - глюкоза
C
OН
ОН
НО
Н
Н
ОН
Н
ОН
СН2ОН
Глюкоза (40% раствор) используется для детоксикации
организма, вызванного цианид-ионами при лечении
нитропруссидом натрия Na2 Fe(NO)(CN)5







 chemistry
chemistry