Similar presentations:
(5 колл) Ариламиновые
1. Ариламиновые красители
2.
• Хромофорная система ариламиновых красителей характеризуется наличием цепочки сопряженных двойных связей, котораяпостроена из двух ароматических остатков, способных существовать в хиноидной форме и несущих электронодонорный и
электроноакцепторный заместители, а также соединяющего их
центрального атома азота.
ЭД–Ar–N=Ar'=ЭА
ЭА=Ar=N–Ar'–ЭД
• При восстановлении ариламиновых красителей происходит
превращение хиноидного ядра в ароматическое ядро, ЭА-заместителя в ЭД-заместитель. В результате образуются бесцветные лейкосоединения, которые представляют собой производные диариламина.
ЭД–Ar–N=Ar'=ЭА + [H] ЭД–Ar–NH–Ar’-ЭД
• Поэтому этот класс красителей рассматривается как
производные диариламина, в которых центральный атом азота,
находясь в состоянии sp2-гибридизации, входит в единую
сопряженную цепочку хромофорной системы.
3.
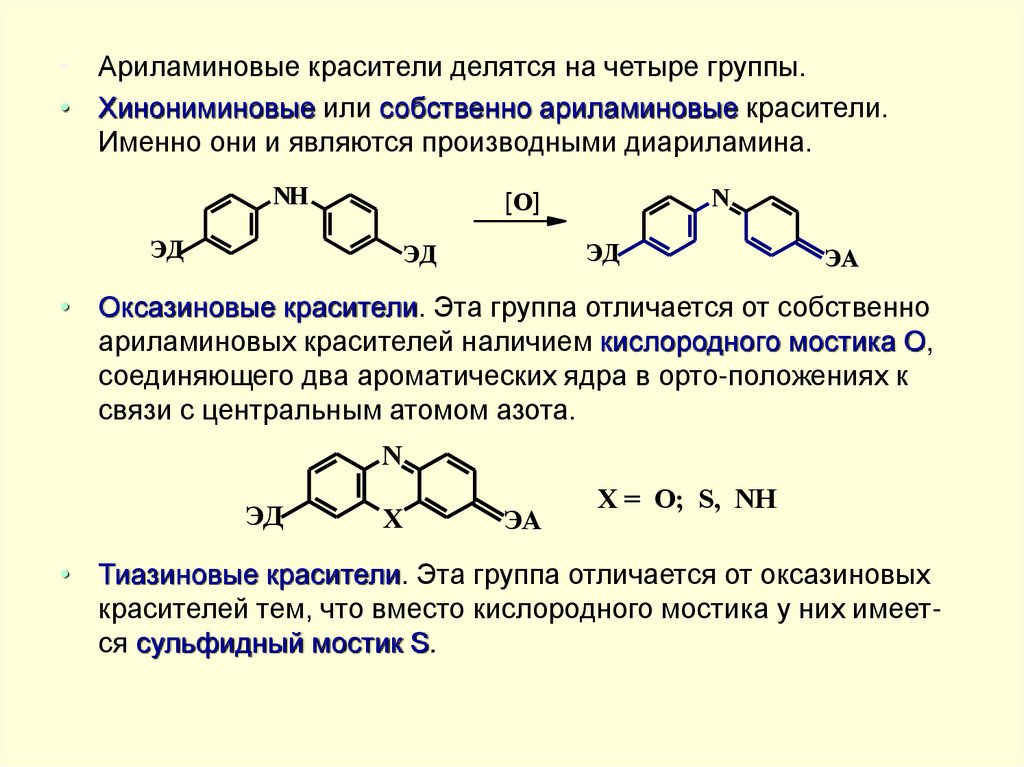
• Ариламиновые красители делятся на четыре группы.• Хинониминовые или собственно ариламиновые красители.
Именно они и являются производными диариламина.
NH
N
[O]
ЭД
ЭД
ЭД
ЭА
• Оксазиновые красители. Эта группа отличается от собственно
ариламиновых красителей наличием кислородного мостика О,
соединяющего два ароматических ядра в орто-положениях к
связи с центральным атомом азота.
N
ЭД
X
ЭА
X = O; S, NH
• Тиазиновые красители. Эта группа отличается от оксазиновых
красителей тем, что вместо кислородного мостика у них имеется сульфидный мостик S.
4.
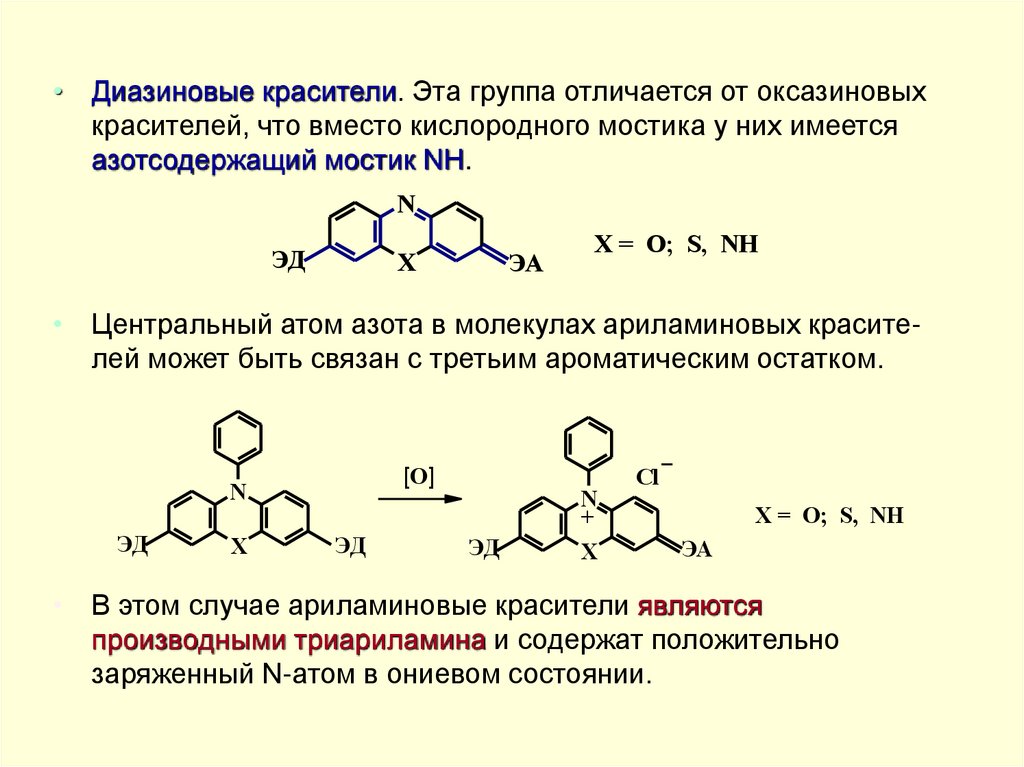
• Диазиновые красители. Эта группа отличается от оксазиновыхкрасителей, что вместо кислородного мостика у них имеется
азотсодержащий мостик NH.
N
ЭД
X
ЭА
X = O; S, NH
• Центральный атом азота в молекулах ариламиновых красителей может быть связан с третьим ароматическим остатком.
[O]
N
ЭД
X
N
Cl
-
+
ЭД
ЭД
X
X = O; S, NH
ЭА
• В этом случае ариламиновые красители являются
производными триариламина и содержат положительно
заряженный N-атом в ониевом состоянии.
5. 7.1. Хинониминовые красители
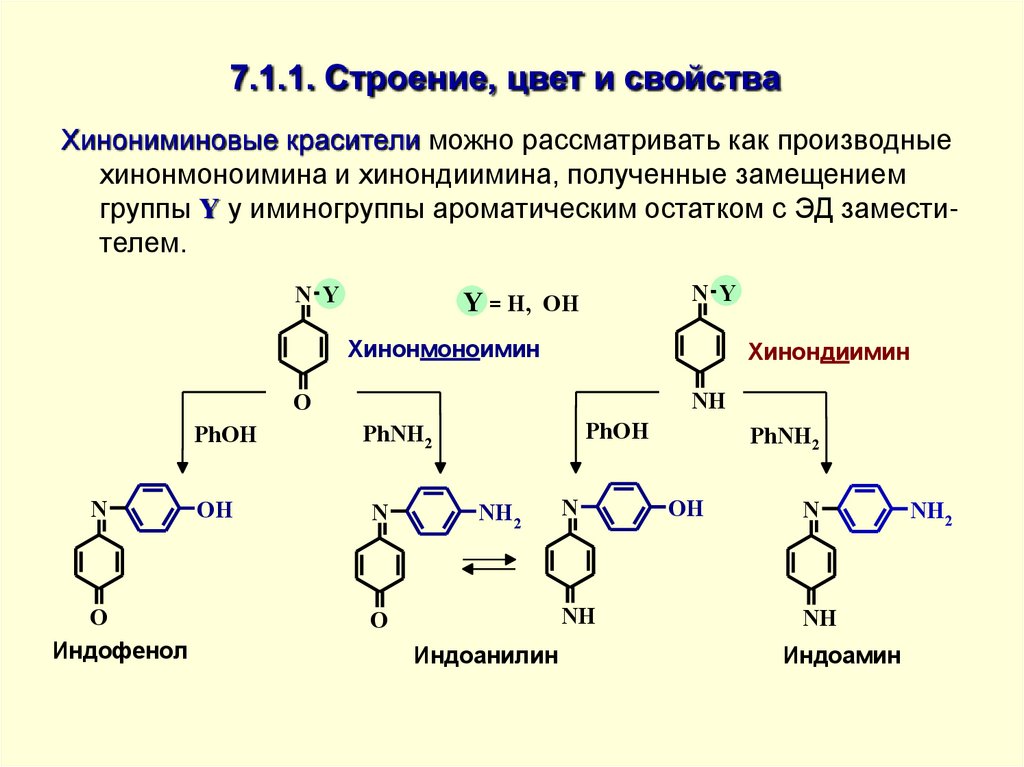
6. 7.1.1. Строение, цвет и свойства
Хинониминовые красители можно рассматривать как производныехинонмоноимина и хинондиимина, полученные замещением
группы Y у иминогруппы ароматическим остатком с ЭД заместителем.
N Y
N Y
Y = H, OH
Хинонмоноимин
Хинондиимин
NH
O
N
O
Индофенол
PhOH
PhNH2
OH
N
PhOH
NH2
N
NH
O
Индоанилин
PhNH2
OH
N
NH
Индоамин
NH2
7.
N YN Y
Y = H, OH
Хинонмоноимин
Хинондиимин
NH
O
N
O
Индофенол
PhOH
PhNH2
OH
N
PhOH
NH2
N
NH
O
Индоанилин
PhNH2
OH
N
NH2
NH
Индоамин
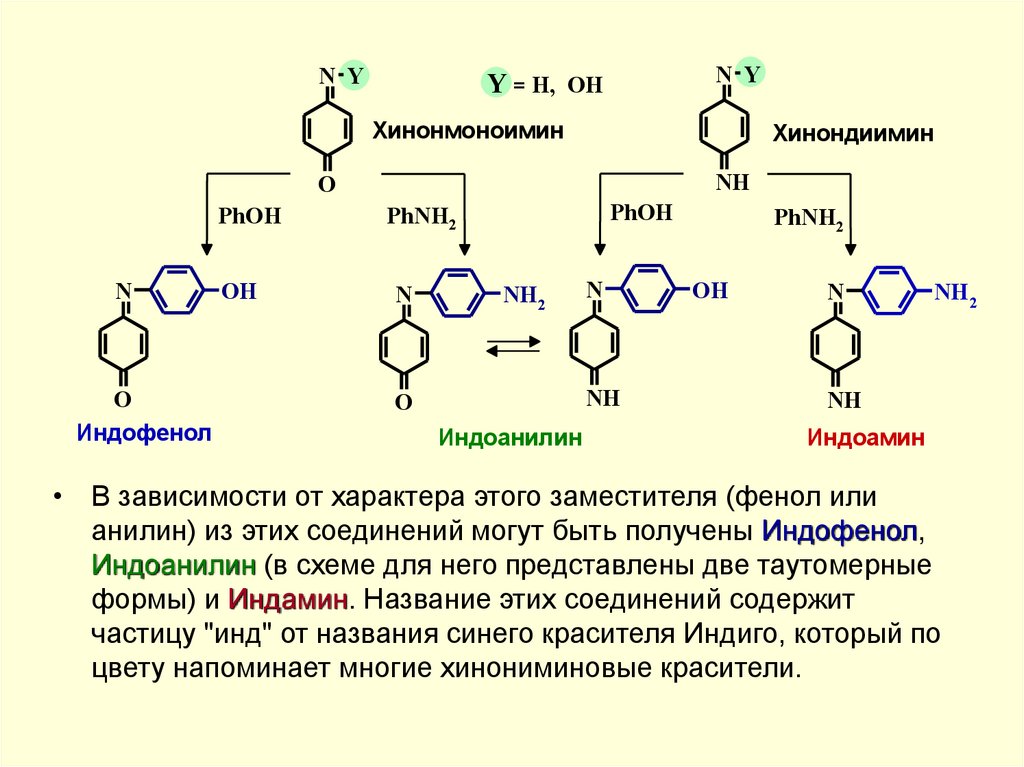
• В зависимости от характера этого заместителя (фенол или
анилин) из этих соединений могут быть получены Индофенол,
Индоанилин (в схеме для него представлены две таутомерные
формы) и Индамин. Название этих соединений содержит
частицу "инд" от названия синего красителя Индиго, который по
цвету напоминает многие хинониминовые красители.
8.
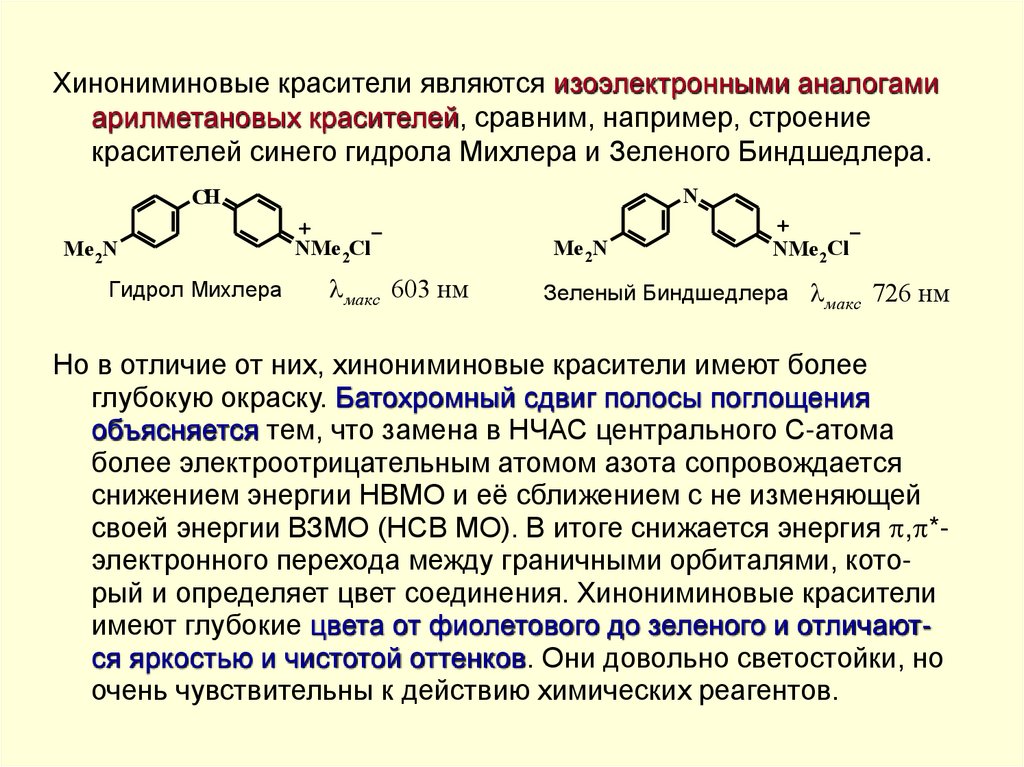
Хинониминовые красители являются изоэлектронными аналогамиарилметановых красителей, сравним, например, строение
красителей синего гидрола Михлера и Зеленого Биндшедлера.
N
CH
Me 2N
Гидрол Михлера
+
NMe 2Cl
макс 603 нм
Me 2N
+
NMe 2Cl
Зеленый Биндшедлера макс 726 нм
Но в отличие от них, хинониминовые красители имеют более
глубокую окраску. Батохромный сдвиг полосы поглощения
объясняется тем, что замена в НЧАС центрального С-атома
более электроотрицательным атомом азота сопровождается
снижением энергии НВМО и её сближением с не изменяющей
своей энергии ВЗМО (НСВ МО). В итоге снижается энергия , *электронного перехода между граничными орбиталями, который и определяет цвет соединения. Хинониминовые красители
имеют глубокие цвета от фиолетового до зеленого и отличаются яркостью и чистотой оттенков. Они довольно светостойки, но
очень чувствительны к действию химических реагентов.
9.
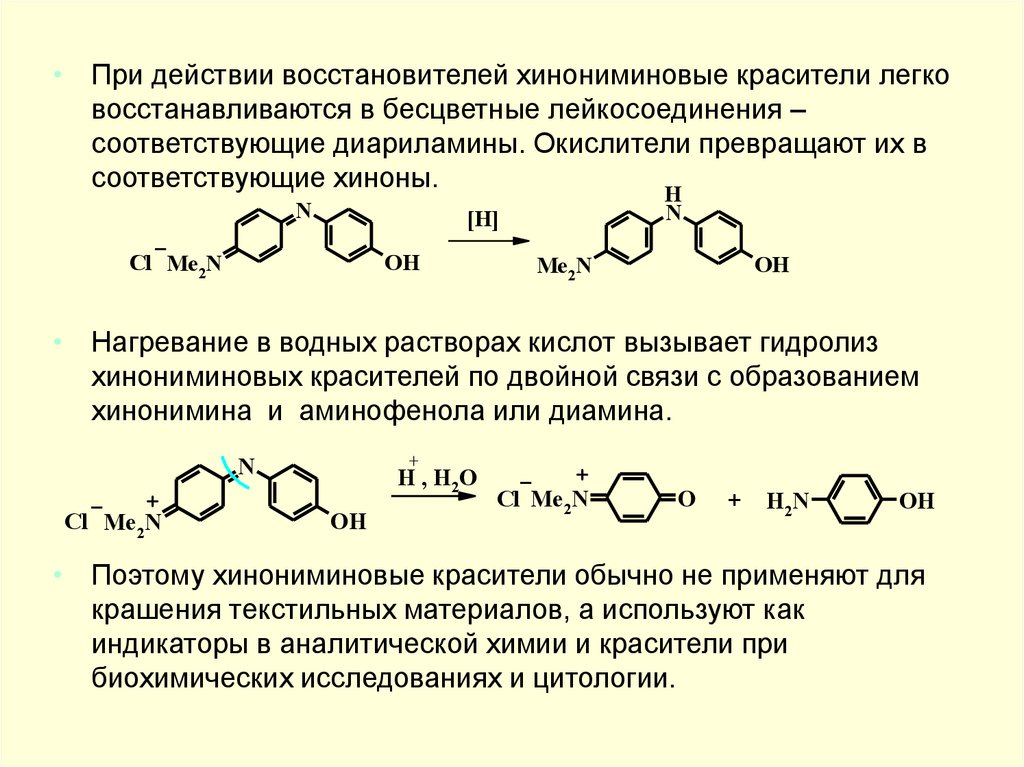
• При действии восстановителей хинониминовые красители легковосстанавливаются в бесцветные лейкосоединения –
соответствующие диариламины. Окислители превращают их в
соответствующие хиноны.
N
H
N
[H]
-
Cl Me 2N
OH
OH
Me 2N
• Нагревание в водных растворах кислот вызывает гидролиз
хинониминовых красителей по двойной связи с образованием
хинонимина и аминофенола или диамина.
+
N
+
Cl Me 2N
-
H , H2O
OH
+
Cl Me 2N
-
O
+ H2N
OH
• Поэтому хинониминовые красители обычно не применяют для
крашения текстильных материалов, а используют как
индикаторы в аналитической химии и красители при
биохимических исследованиях и цитологии.
10. 7.1.2. Методы получения хинониминовых красителей
• Существует два основных способа получения хинониминовыхкрасителей: окислительный и нитрозный.
• Окислительный способ заключается в окислении смеси
аминофенола или арилендиамина с фенолом или ариламином.
В качестве окислителей обычно применяют бихромат натрия
Na2Cr2O7 или калия K2Cr2O7 в среде минеральной кислоты, а
также гипохлорит натрия NaClO в щелочной среде.
• В зависимости от комбинации применяемых компонентов могут
быть получены:
индофенол – из аминофенола и фенола;
индоанилин – из аминофенола и амина или
диамина и фенола;
индамин
– из диамина и амина.
11.
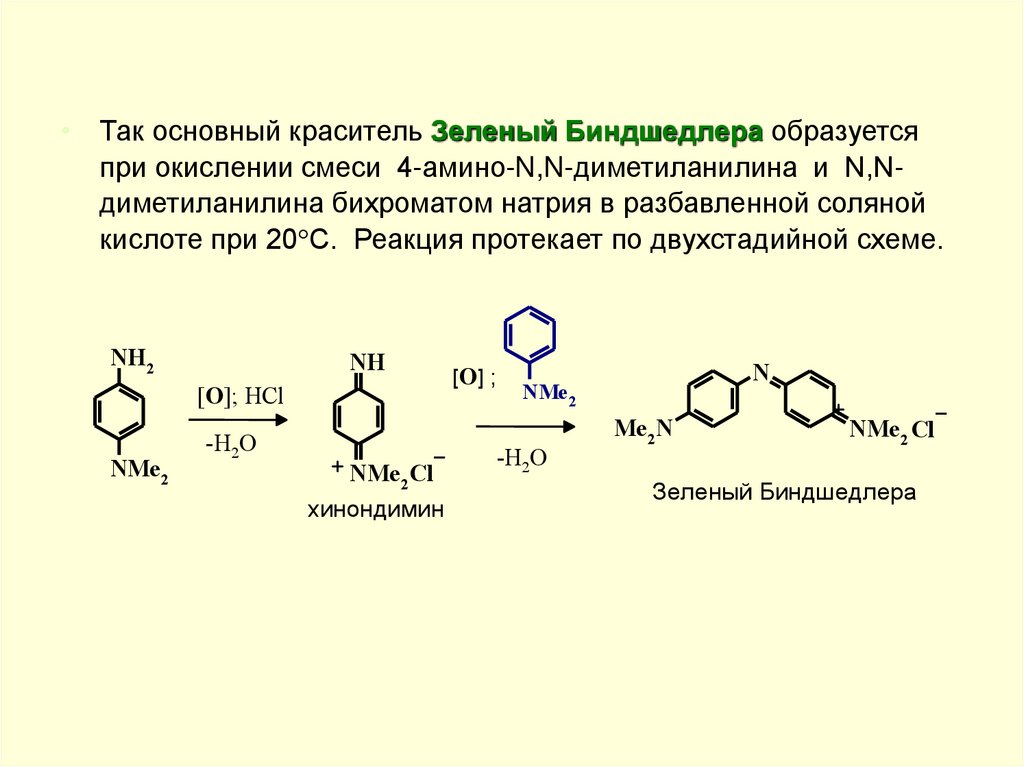
• Так основный краситель Зеленый Биндшедлера образуетсяпри окислении смеси 4-амино-N,N-диметиланилина и N,Nдиметиланилина бихроматом натрия в разбавленной соляной
кислоте при 20 С. Реакция протекает по двухстадийной схеме.
NH2
NH
[ O] ;
[O]; HCl
NMe 2
-H2O
+ NMe Cl2
хинондимин
N
NMe2
-H2O
Me 2N
+
-
NMe 2 Cl
Зеленый Биндшедлера
12.
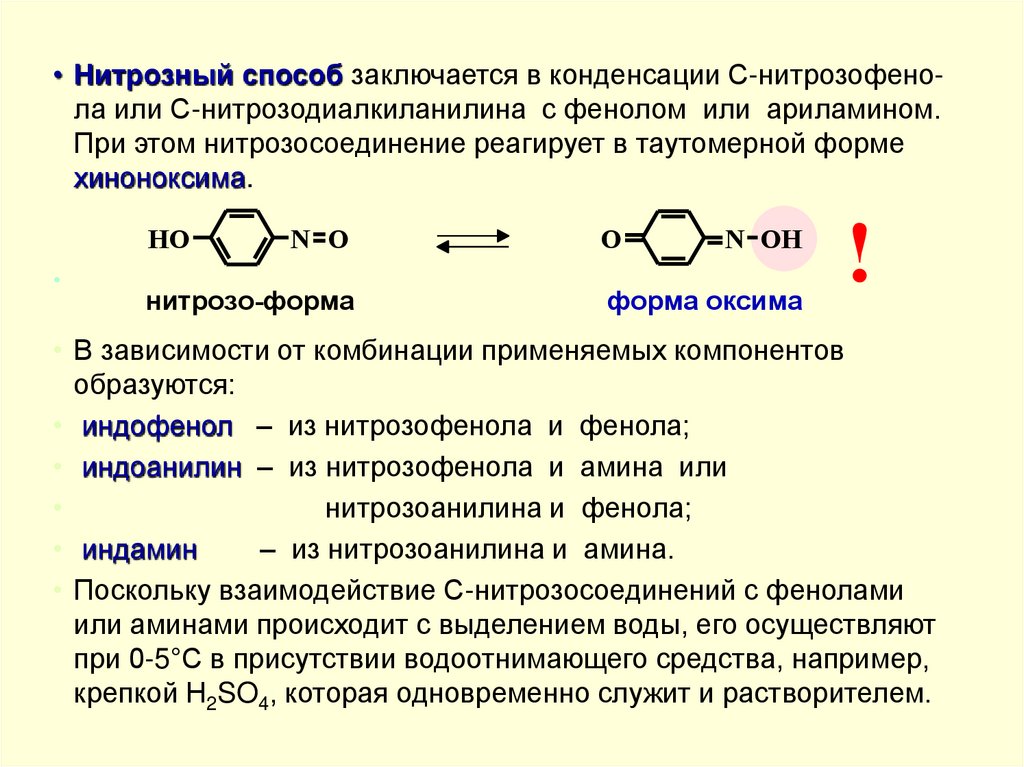
• Нитрозный способ заключается в конденсации С-нитрозофенола или С-нитрозодиалкиланилина с фенолом или ариламином.При этом нитрозосоединение реагирует в таутомерной форме
хиноноксима.
HO
N O
нитрозо-форма
O
N OH
форма оксима
!
• В зависимости от комбинации применяемых компонентов
образуются:
• индофенол – из нитрозофенола и фенола;
• индоанилин – из нитрозофенола и амина или
нитрозоанилина и фенола;
• индамин
– из нитрозоанилина и амина.
• Поскольку взаимодействие С-нитрозосоединений с фенолами
или аминами происходит с выделением воды, его осуществляют
при 0-5°С в присутствии водоотнимающего средства, например,
крепкой H2SO4, которая одновременно служит и растворителем.
13.
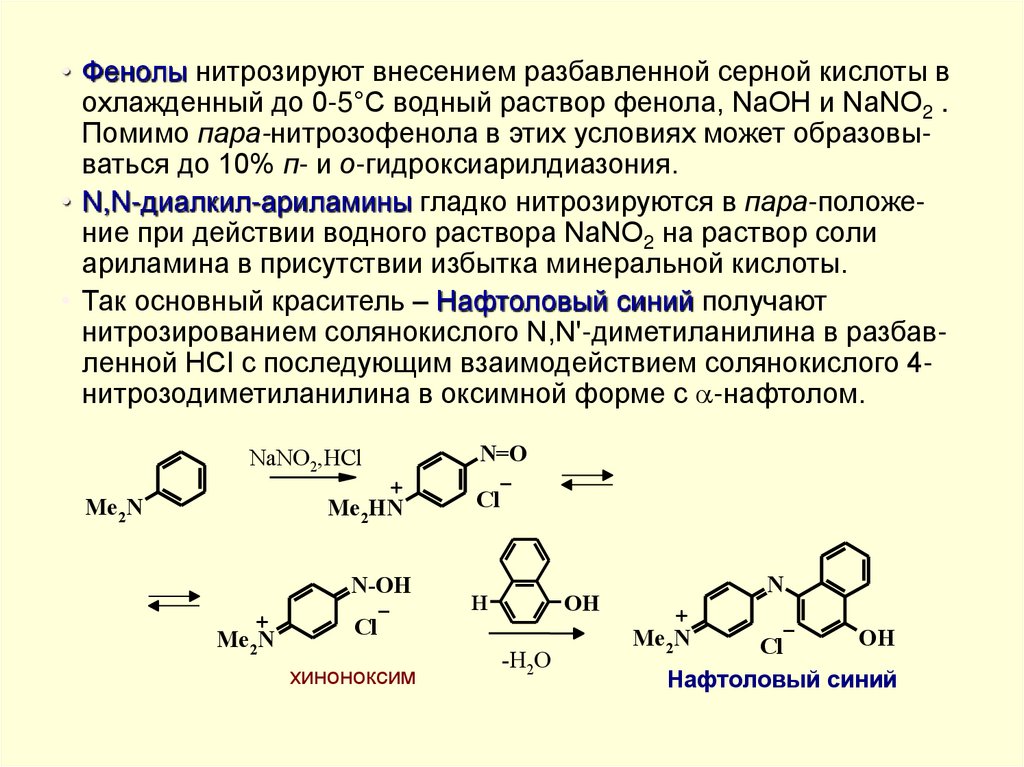
• Фенолы нитрозируют внесением разбавленной серной кислоты вохлажденный до 0-5°С водный раствор фенола, NaOH и NaNO2 .
Помимо пара-нитрозофенола в этих условиях может образовываться до 10% п- и о-гидроксиарилдиазония.
• N,N-диалкил-ариламины гладко нитрозируются в пара-положение при действии водного раствора NaNO2 на раствор соли
ариламина в присутствии избытка минеральной кислоты.
• Так основный краситель – Нафтоловый синий получают
нитрозированием солянокислого N,N'-диметиланилина в разбавленной HCl с последующим взаимодействием солянокислого 4нитрозодиметиланилина в оксимной форме с -нафтолом.
N=O
NaNO2,HCl
+
Me 2HN
Me 2N
N-OH
+
Me 2N
-
Cl
хиноноксим
-
Cl
OH
H
-H2O
N
+
Me 2N
OH
Cl
Нафтоловый синий
14. 7.1.3. Хинониминовые красители в цветной фотографии
• Самостоятельное значение некоторые хинониминовыекрасители приобрели в цветной фотографии, где с их помощью
воспроизводятся голубой цвет и на его основе зеленый, синий и
фиолетовый цвета.
• Принцип создания цветного изображения с помощью трех
красителей желтого, пурпурного и голубого цвета, которые
образуются в фотоэмульсии в результате реакции с проявителем цветного изображения, следует изучить самостоятельно в
соответствующем разделе основного учебника.
15. 7.1.4. Хинониминовые красители в качестве промежуточных продуктов
• Хинониминовые красители применяются главным образом какпромежуточные продукты при синтезе оксазиновых, тиазиновых
и диазиновых красителей. При этом используется способность
хиноидно построенного ядра присоединять нуклеофильные
частицы и превращаться в ароматические ядра в результате
восстановления.
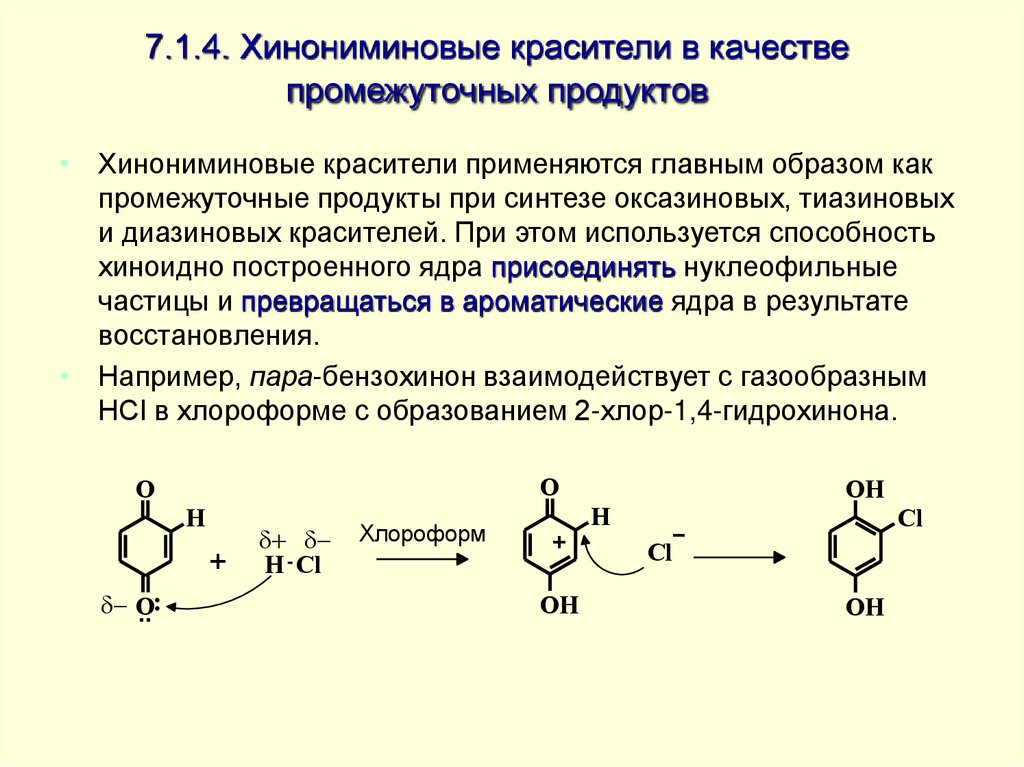
• Например, пара-бензохинон взаимодействует с газообразным
HCl в хлороформе с образованием 2-хлор-1,4-гидрохинона.
O
O
H
+
O
..
H Cl
Хлороформ
+
OH
H
OH
Cl
-
Cl
OH
16.
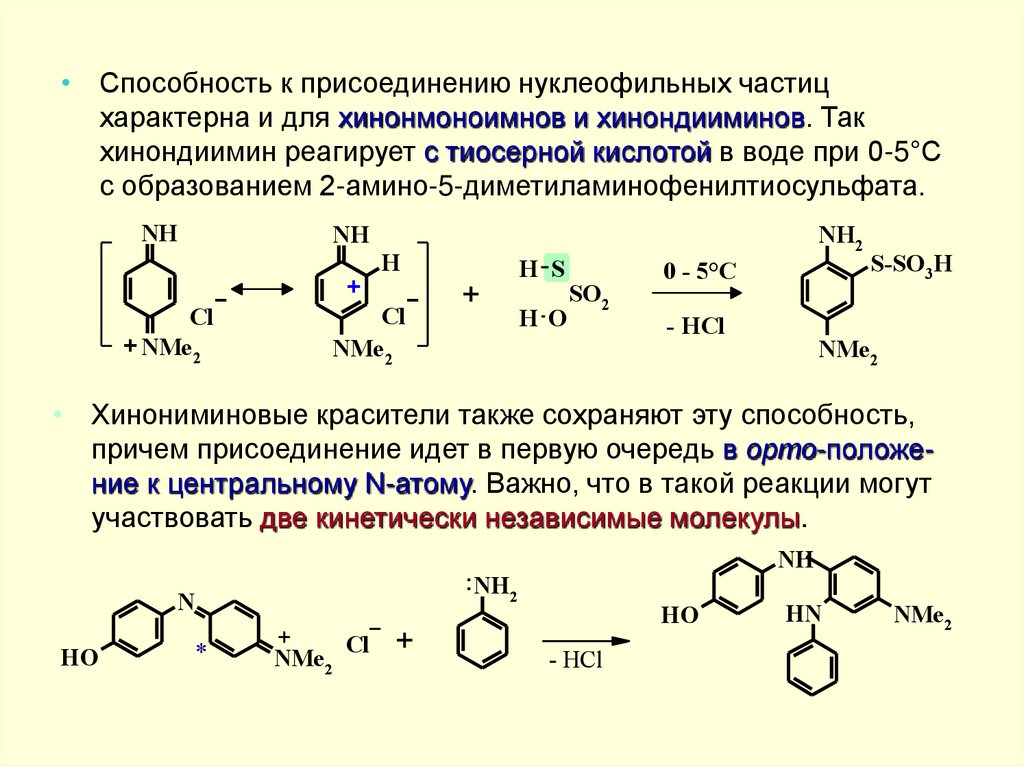
• Способность к присоединению нуклеофильных частицхарактерна и для хинонмоноимнов и хинондииминов. Так
хинондиимин реагирует с тиосерной кислотой в воде при 0-5°С
с образованием 2-амино-5-диметиламинофенилтиосульфата.
NH
NH
-
Cl
+ NMe 2
NH2
H
+
-
Cl
NMe 2
H S
+
HO
SO2
0 - 5°C
- HCl
S-SO3H
NMe 2
• Хинониминовые красители также сохраняют эту способность,
причем присоединение идет в первую очередь в орто-положение к центральному N-атому. Важно, что в такой реакции могут
участвовать две кинетически независимые молекулы.
N
HO
*
: NH
-
+
Cl
NMe 2
+
NH
2
HO
- HCl
HN
NMe 2
17.
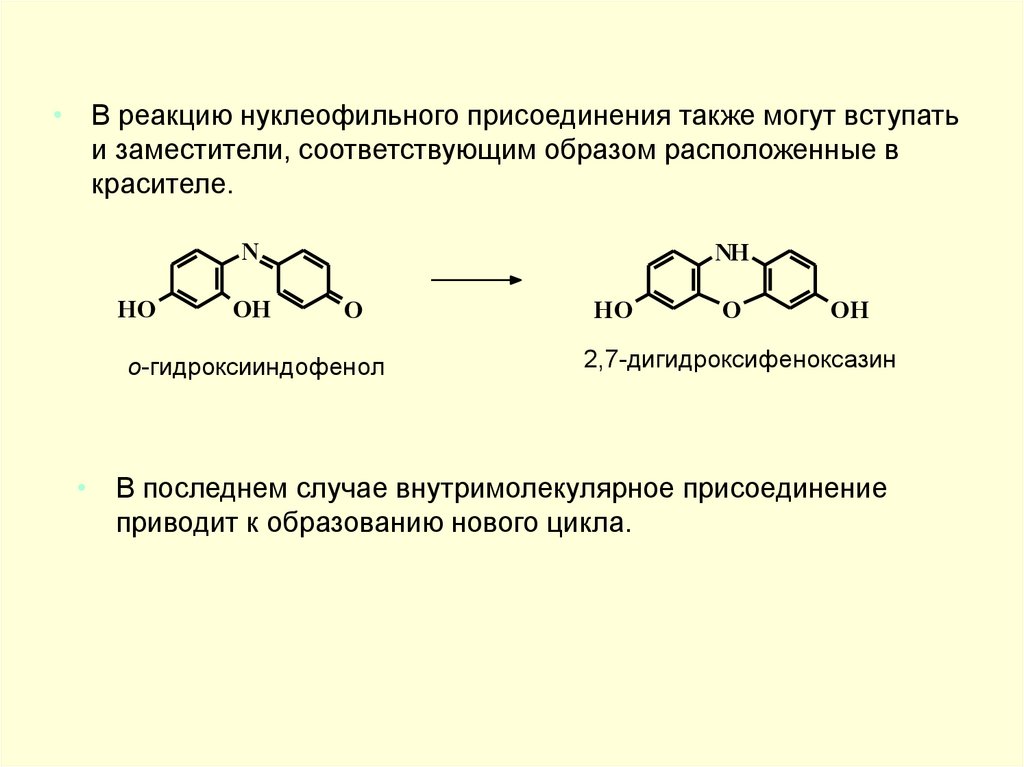
• В реакцию нуклеофильного присоединения также могут вступатьи заместители, соответствующим образом расположенные в
красителе.
N
HO
OH
NH
O
о-гидроксииндофенол
HO
O
OH
2,7-дигидроксифеноксазин
• В последнем случае внутримолекулярное присоединение
приводит к образованию нового цикла.
18. 7.2. Оксазиновые красители
19.
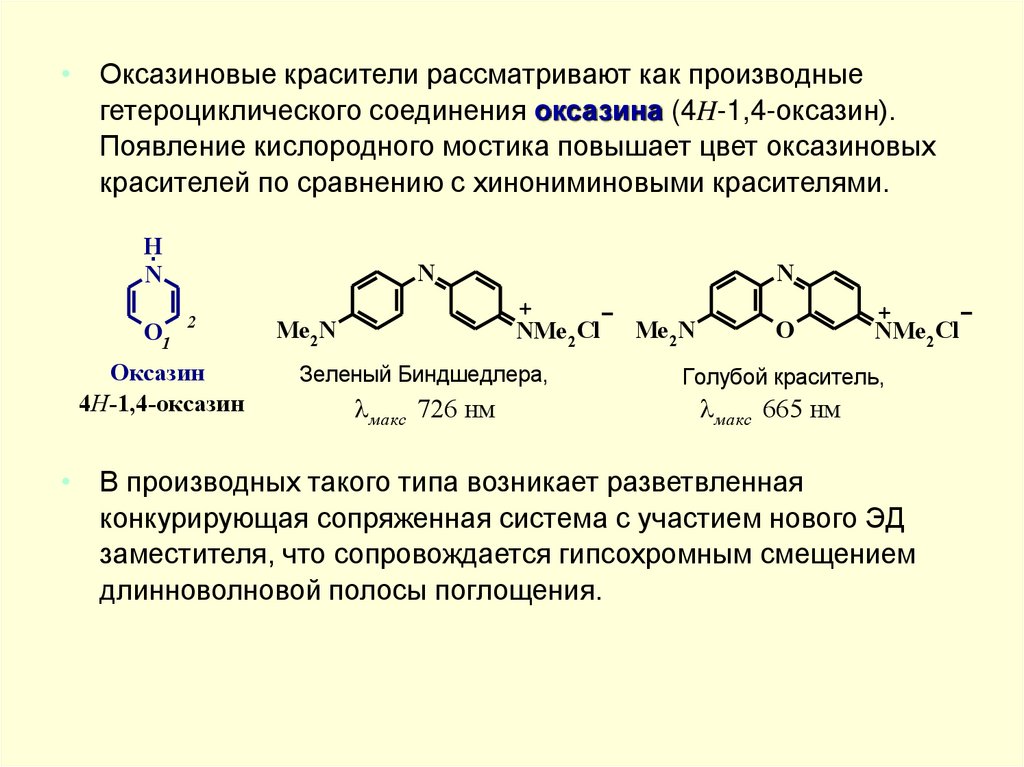
• Оксазиновые красители рассматривают как производныегетероциклического соединения оксазина (4H-1,4-оксазин).
Появление кислородного мостика повышает цвет оксазиновых
красителей по сравнению с хинониминовыми красителями.
H
N
O1
N
2
Оксазин
4H-1,4-оксазин
N
+
NMe 2Cl Me 2N
Me 2N
O
+
NMe 2Cl
Зеленый Биндшедлера,
Голубой краситель,
макс 726 нм
макс 665 нм
• В производных такого типа возникает разветвленная
конкурирующая сопряженная система с участием нового ЭД
заместителя, что сопровождается гипсохромным смещением
длинноволновой полосы поглощения.
20.
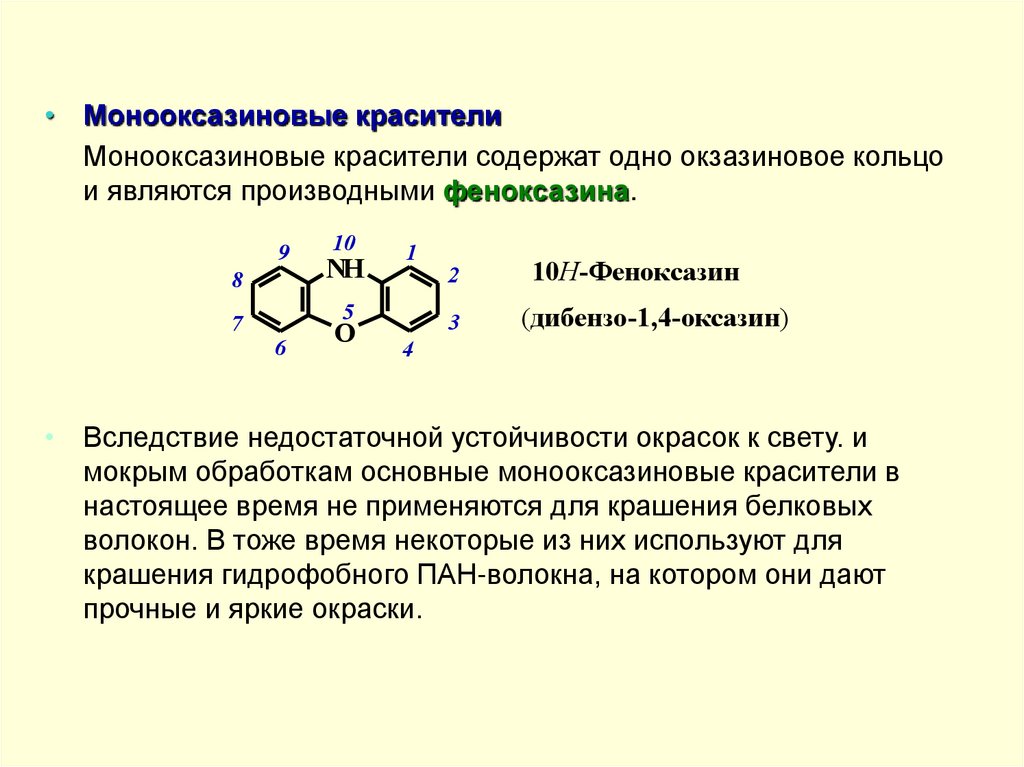
• Монооксазиновые красителиМонооксазиновые красители содержат одно окзазиновое кольцо
и являются производными феноксазина.
9
8
7
10
NH
1
5
6
O
2
10H-Феноксазин
3
(дибензо-1,4-оксазин)
4
• Вследствие недостаточной устойчивости окрасок к свету. и
мокрым обработкам основные монооксазиновые красители в
настоящее время не применяются для крашения белковых
волокон. В тоже время некоторые из них используют для
крашения гидрофобного ПАН-волокна, на котором они дают
прочные и яркие окраски.
21.
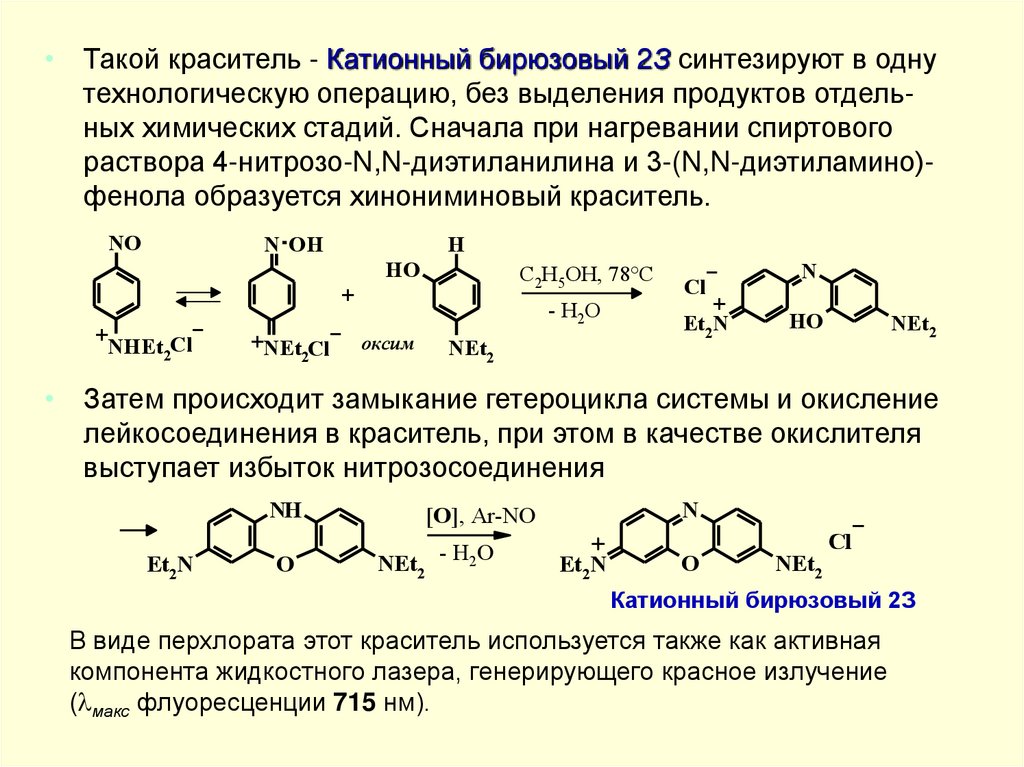
• Такой краситель - Катионный бирюзовый 2З синтезируют в однутехнологическую операцию, без выделения продуктов отдельных химических стадий. Сначала при нагревании спиртового
раствора 4-нитрозо-N,N-диэтиланилина и 3-(N,N-диэтиламино)фенола образуется хинониминовый краситель.
NO
N OH
H
+
+NHEt Cl2
HO
+NEt Cl- оксим
2
C2H5OH, 78°C
- H2O
NEt2
+
Cl
Et2N
N
HO
NEt2
• Затем происходит замыкание гетероцикла системы и окисление
лейкосоединения в краситель, при этом в качестве окислителя
выступает избыток нитрозосоединения
NH
Et2N
O
N
[O], Ar-NO
NEt2 - H2O
+
Et2N
O
-
NEt2
Cl
Катионный бирюзовый 2З
В виде перхлората этот краситель используется также как активная
компонента жидкостного лазера, генерирующего красное излучение
( макс флуоресценции 715 нм).
22.
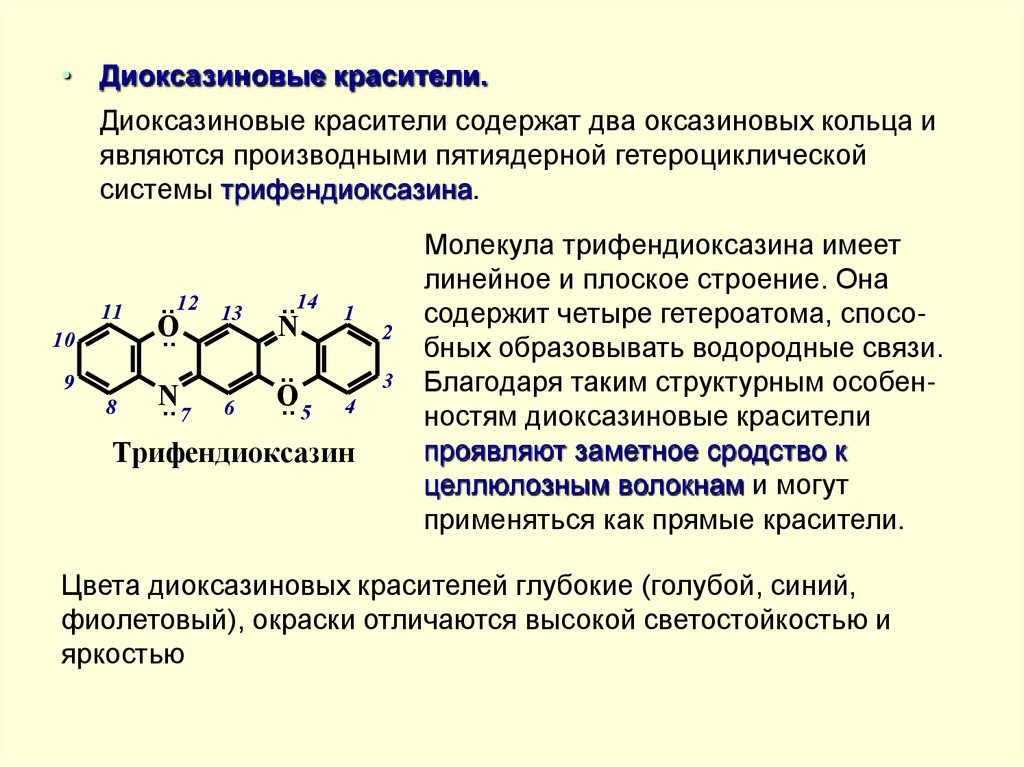
• Диоксазиновые красители.Диоксазиновые красители содержат два оксазиновых кольца и
являются производными пятиядерной гетероциклической
системы трифендиоксазина.
11
10
9
8
.. 12 13
O
..
N
2
N
..
..
O
.. 5
3
7
6
..14 1
4
Трифендиоксазин
Молекула трифендиоксазина имеет
линейное и плоское строение. Она
содержит четыре гетероатома, способных образовывать водородные связи.
Благодаря таким структурным особенностям диоксазиновые красители
проявляют заметное сродство к
целлюлозным волокнам и могут
применяться как прямые красители.
Цвета диоксазиновых красителей глубокие (голубой, синий,
фиолетовый), окраски отличаются высокой светостойкостью и
яркостью
23.
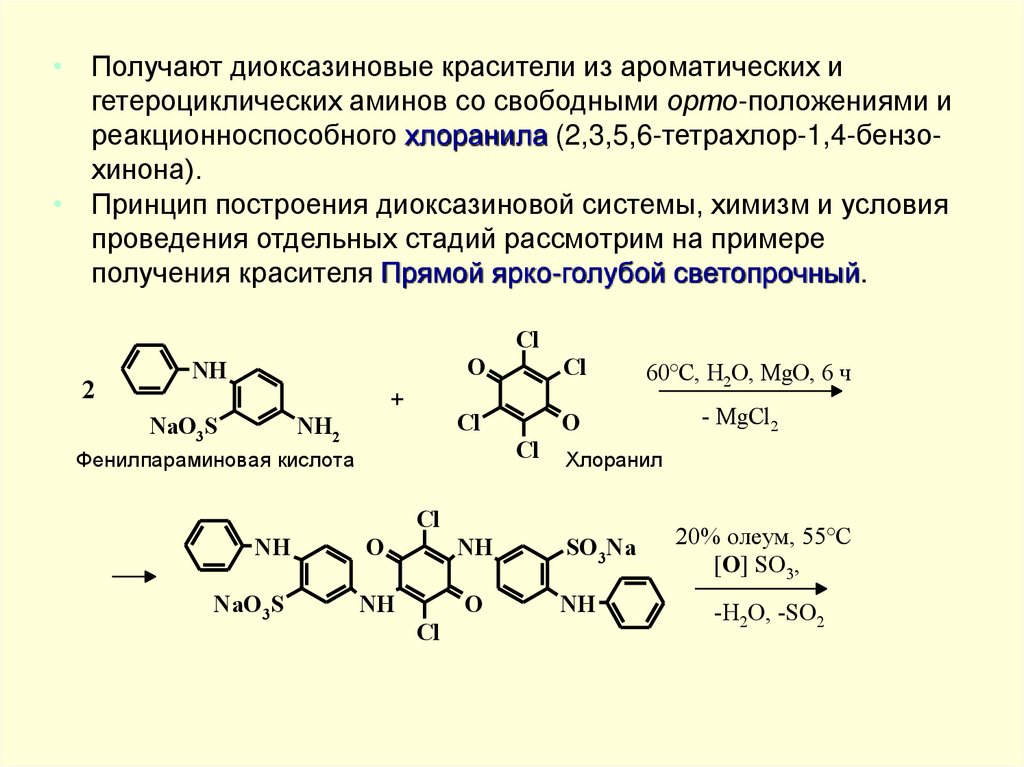
• Получают диоксазиновые красители из ароматических игетероциклических аминов со свободными орто-положениями и
реакционноспособного хлоранила (2,3,5,6-тетрахлор-1,4-бензохинона).
• Принцип построения диоксазиновой системы, химизм и условия
проведения отдельных стадий рассмотрим на примере
получения красителя Прямой ярко-голубой светопрочный.
Cl
2
NH
NaO3S
+
NH2
O
Cl
60°C, H2O, MgO, 6 ч
Cl
O
- MgCl2
Cl
Фенилпараминовая кислота
Хлоранил
Cl
NH
O
NH
SO3Na
NaO3S
NH
O
NH
Cl
20% олеум, 55°C
[O] SO3,
-H2O, -SO2
24.
[O], SO3Cl
NH
O
H HSO4
SO3Na
N
NaO3S
N
O
10% H2SO4, ~ 95°C
+
Cl
NH
сульфат красителя
Cl
NH
O
N
SO 3Na
NaO 3S
N
O
NH
Cl
Прямой ярко-голубой светопрочный
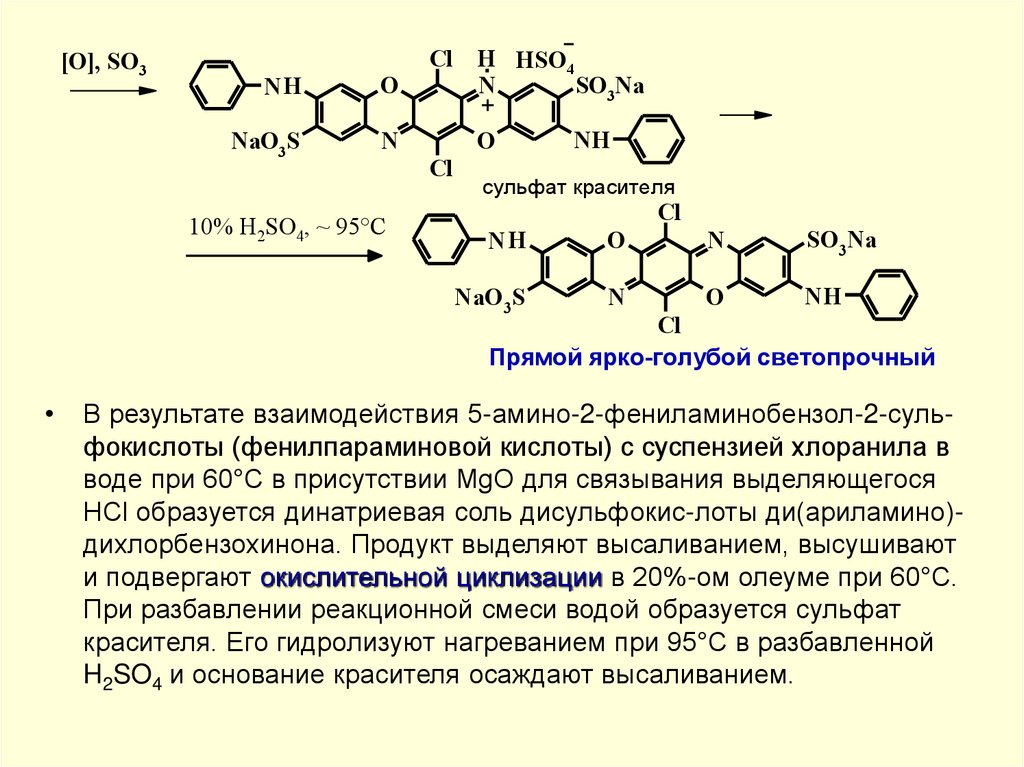
В результате взаимодействия 5-амино-2-фениламинобензол-2-сульфокислоты (фенилпараминовой кислоты) с суспензией хлоранила в
воде при 60°С в присутствии MgO для связывания выделяющегося
HCl образуется динатриевая соль дисульфокис-лоты ди(ариламино)дихлорбензохинона. Продукт выделяют высаливанием, высушивают
и подвергают окислительной циклизации в 20%-ом олеуме при 60°С.
При разбавлении реакционной смеси водой образуется сульфат
красителя. Его гидролизуют нагреванием при 95°С в разбавленной
H2SO4 и основание красителя осаждают высаливанием.
25.
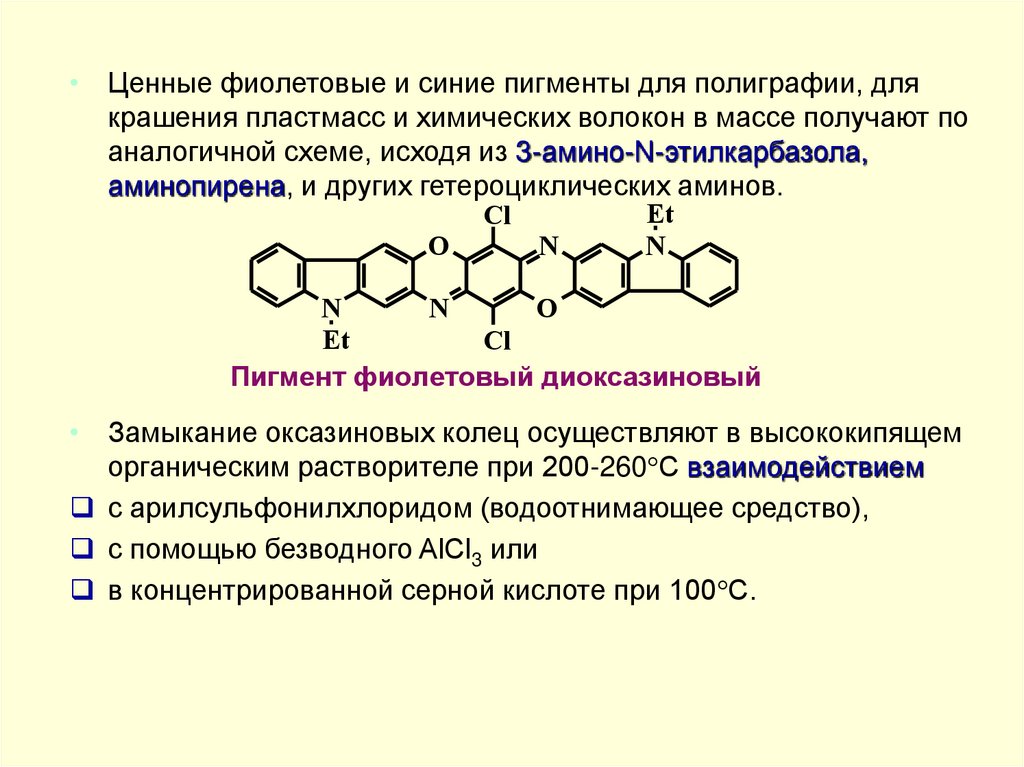
• Ценные фиолетовые и синие пигменты для полиграфии, длякрашения пластмасс и химических волокон в массе получают по
аналогичной схеме, исходя из 3-амино-N-этилкарбазола,
аминопирена, и других гетероциклических аминов.
Et
Cl
N
O
N
N
O
N
Et
Cl
Пигмент фиолетовый диоксазиновый
• Замыкание оксазиновых колец осуществляют в высококипящем
органическим растворителе при 200-260 С взаимодействием
с арилсульфонилхлоридом (водоотнимающее средство),
с помощью безводного AlCl3 или
в концентрированной серной кислоте при 100 С.
26. 7.3. Тиазиновые красители
27.
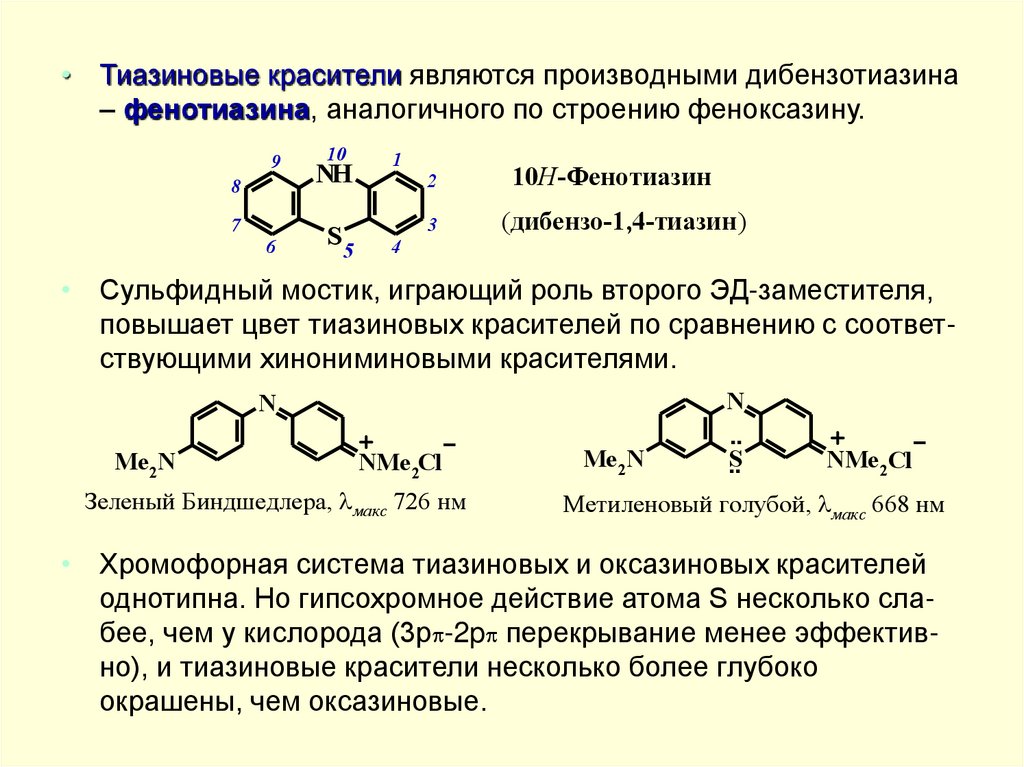
• Тиазиновые красители являются производными дибензотиазина– фенотиазина, аналогичного по строению феноксазину.
9
8
7
6
10
1
NH
S5
2
10H-Фенотиазин
3
(дибензо-1,4-тиазин)
4
• Сульфидный мостик, играющий роль второго ЭД-заместителя,
повышает цвет тиазиновых красителей по сравнению с соответствующими хинониминовыми красителями.
N
N
Me 2N
+
-
NMe 2Cl
Зеленый Биндшедлера, макс 726 нм
Me 2N
..
S
..
+
-
NMe 2Cl
Метиленовый голубой, макс 668 нм
• Хромофорная система тиазиновых и оксазиновых красителей
однотипна. Но гипсохромное действие атома S несколько слабее, чем у кислорода (3p -2p перекрывание менее эффективно), и тиазиновые красители несколько более глубоко
окрашены, чем оксазиновые.
28.
• Тиазиновые красители имеют глубокие цвета от фиолетового дозеленого. Окраски на шерсти и шелке отличаются чистотой и
яркостью оттенков, но не очень светостойки.
• Тиазиновые красители получают из соответствующих
хинониминовых красителей со свободными орто-положениями
к центральному атому азота. Создание структуры фенотиазина
можно проводить двумя способами:
постадийно, путем введения серосодержащего заместителя с
последующим замыканием тиазинового цикла в результате
внутримолекулярного присоединения;
осернением, когда нужная структура образуется в результате
нагревания с полисульфидом натрия Na2Sn , метод сернистой
"варки" или мокрого сернистого плава.
29. 7.3.1. Основные тиазиновые красители.
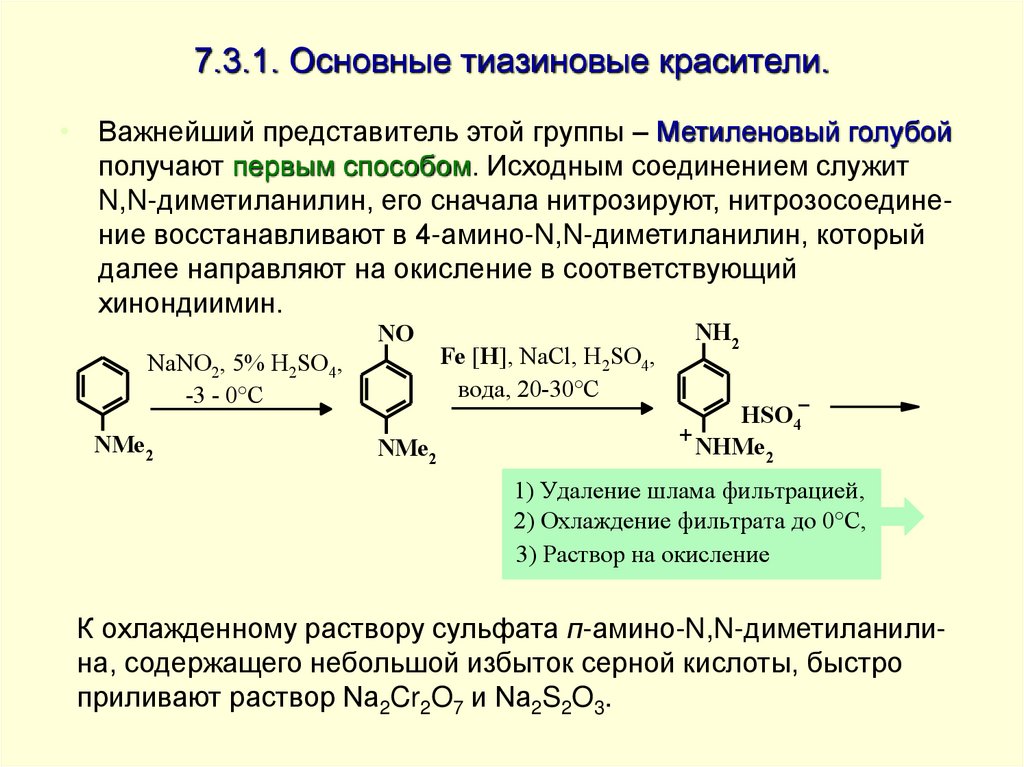
• Важнейший представитель этой группы – Метиленовый голубойполучают первым способом. Исходным соединением служит
N,N-диметиланилин, его сначала нитрозируют, нитрозосоединение восстанавливают в 4-амино-N,N-диметиланилин, который
далее направляют на окисление в соответствующий
хинондиимин.
NO
NaNO2, 5% H2SO4,
-3 - 0°C
NMe 2
NMe 2
Fe [H], NaCl, H2SO4,
вода, 20-30°C
NH2
HSO4+ NHMe
2
1) Удаление шлама фильтрацией,
2) Охлаждение фильтрата до 0°C,
3) Раствор на окисление
К охлажденному раствору сульфата п-амино-N,N-диметиланилина, содержащего небольшой избыток серной кислоты, быстро
приливают раствор Na2Cr2O7 и Na2S2O3.
30.
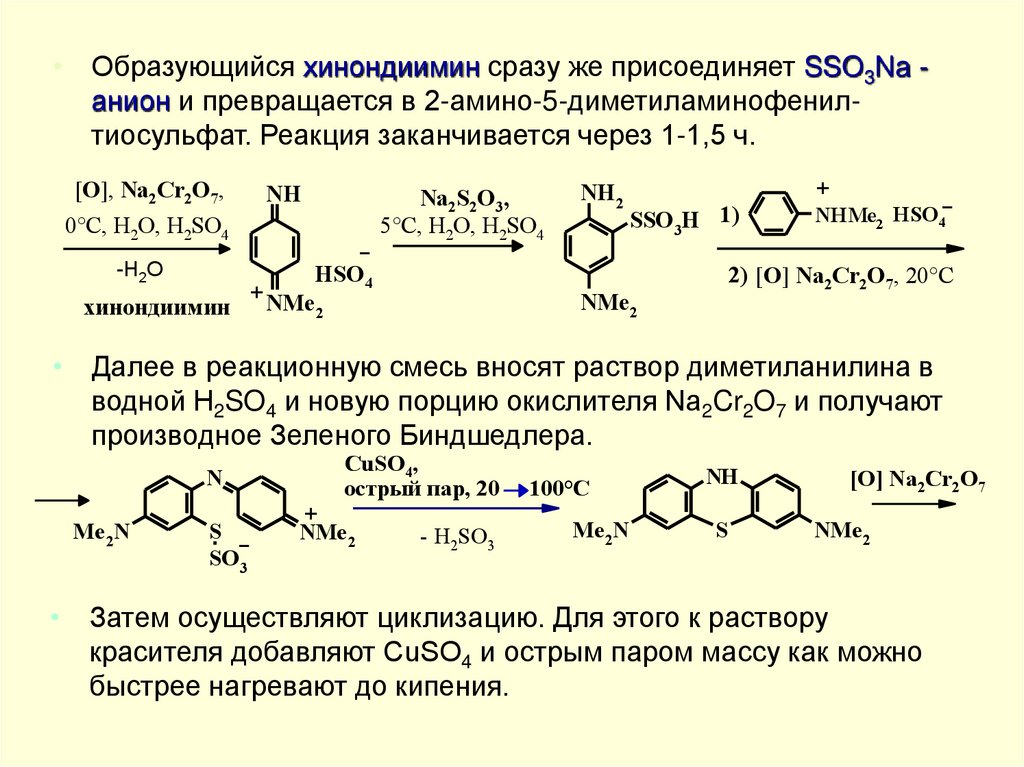
• Образующийся хинондиимин сразу же присоединяет SSO3Na анион и превращается в 2-амино-5-диметиламинофенилтиосульфат. Реакция заканчивается через 1-1,5 ч.[O], Na2Cr2O7,
NH
0°C, H2O, H2SO4
HSO4
+ NMe
хинондиимин
2
Na2S2O3,
5°C, H2O, H2SO4
NH2
SSO3H 1)
-H2O
NMe 2
+
NHMe2 HSO4-
2) [O] Na2Cr2O7, 20°C
• Далее в реакционную смесь вносят раствор диметиланилина в
водной H2SO4 и новую порцию окислителя Na2Cr2O7 и получают
производное Зеленого Биндшедлера.
CuSO4,
острый пар, 20
N
Me 2N
S
SO3
+
NMe 2
- H2SO3
100°C
Me 2N
NH
S
[O] Na2Cr2O7
NMe 2
• Затем осуществляют циклизацию. Для этого к раствору
красителя добавляют CuSO4 и острым паром массу как можно
быстрее нагревают до кипения.
31.
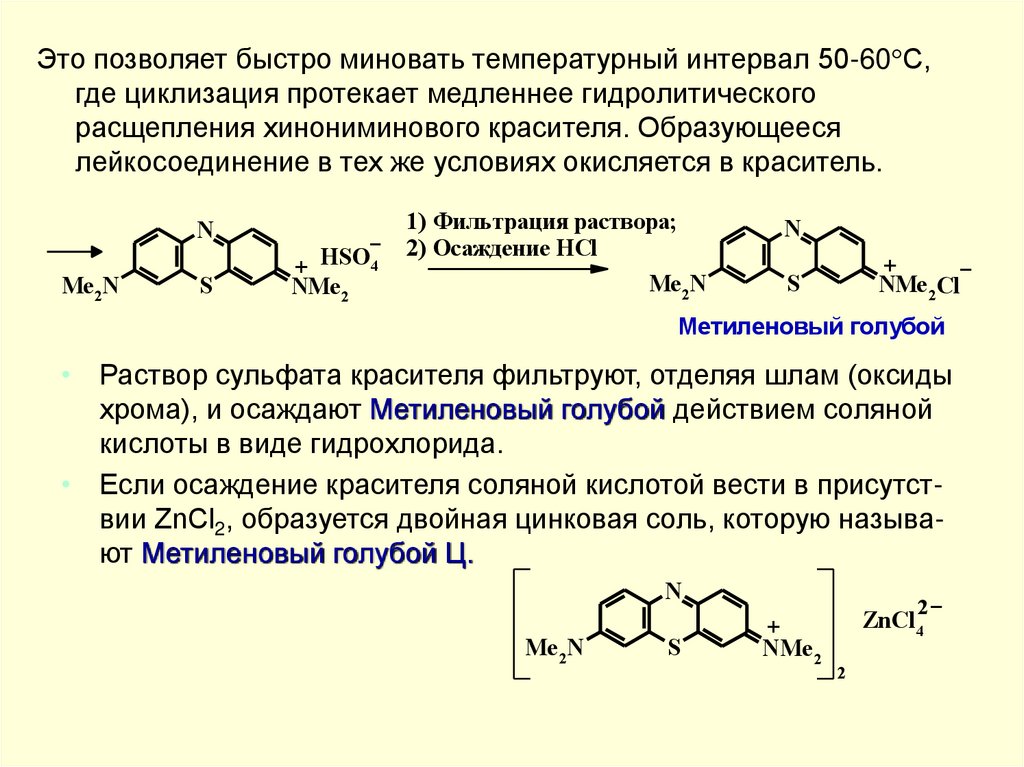
Это позволяет быстро миновать температурный интервал 50-60 С,где циклизация протекает медленнее гидролитического
расщепления хинониминового красителя. Образующееся
лейкосоединение в тех же условиях окисляется в краситель.
N
Me 2N
S
HSO4
+
NMe 2
1) Фильтрация раствора;
2) Осаждение HCl
N
Me 2N
+
S
-
NMe 2Cl
Метиленовый голубой
• Раствор сульфата красителя фильтруют, отделяя шлам (оксиды
хрома), и осаждают Метиленовый голубой действием соляной
кислоты в виде гидрохлорида.
• Если осаждение красителя соляной кислотой вести в присутствии ZnCl2, образуется двойная цинковая соль, которую называют Метиленовый голубой Ц.
N
Me 2N
S
2-
ZnCl4
+
NMe 2
2
32.
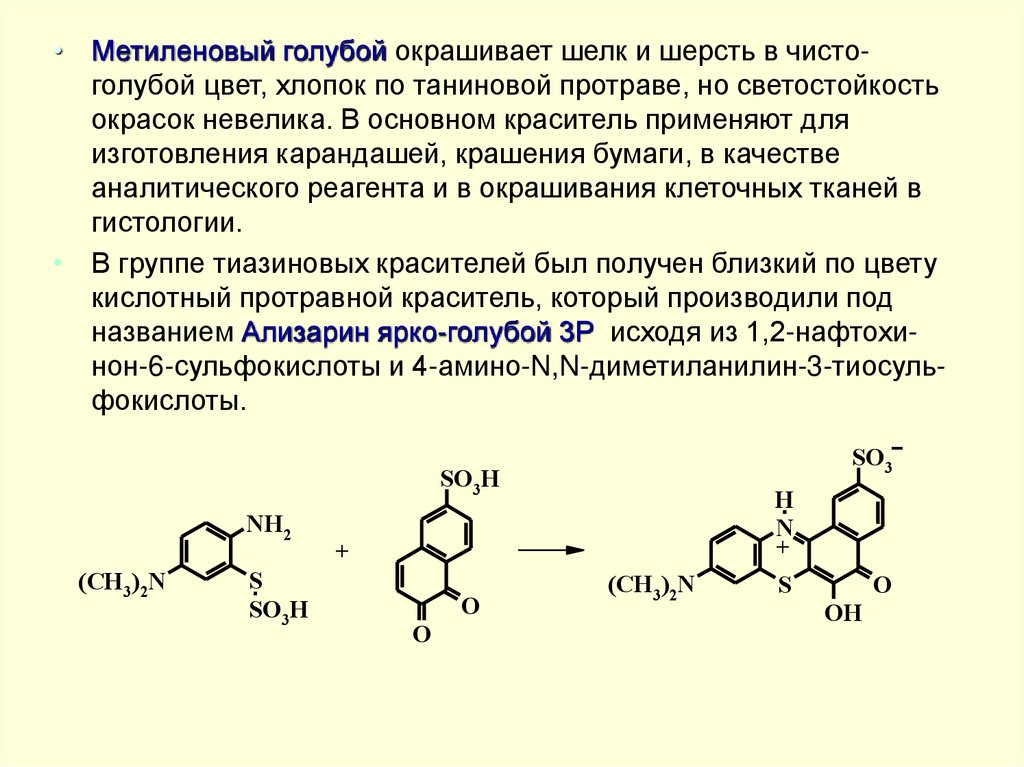
• Метиленовый голубой окрашивает шелк и шерсть в чистоголубой цвет, хлопок по таниновой протраве, но светостойкостьокрасок невелика. В основном краситель применяют для
изготовления карандашей, крашения бумаги, в качестве
аналитического реагента и в окрашивания клеточных тканей в
гистологии.
• В группе тиазиновых красителей был получен близкий по цвету
кислотный протравной краситель, который производили под
названием Ализарин ярко-голубой 3Р исходя из 1,2-нафтохинон-6-сульфокислоты и 4-амино-N,N-диметиланилин-3-тиосульфокислоты.
SO 3-
SO3H
NH2
(CH3)2N
S
SO3H
H
N
+
+
O
O
(CH 3)2N
S
O
OH
33. 7.3.2. Сернистые тиазиновые красители
Второй метод получения тиазиновых красителей – осернение
хинониминовых красителей имеет большое практическое
значение. Химические процессы, происходящие при сернистой
"варке" - нагревании хинониминовых красителей в водном
растворе Na2Sn , при 100-120°С, очень сложны.
• В реакции с красителем и продуктами его превращения
участвуют вещества, которые образуются
вследствие распада полисульфида натрия (Na2S2, Na2S, S*),
или в результате взаимодействия полисульфида натрия с
органическими молекулами и водой ( H2S, Na2S2O3 тиосульфат
натрия).
• В зависимости от строения серосодержащих молекул
могут протекать следующие реакции:
34.
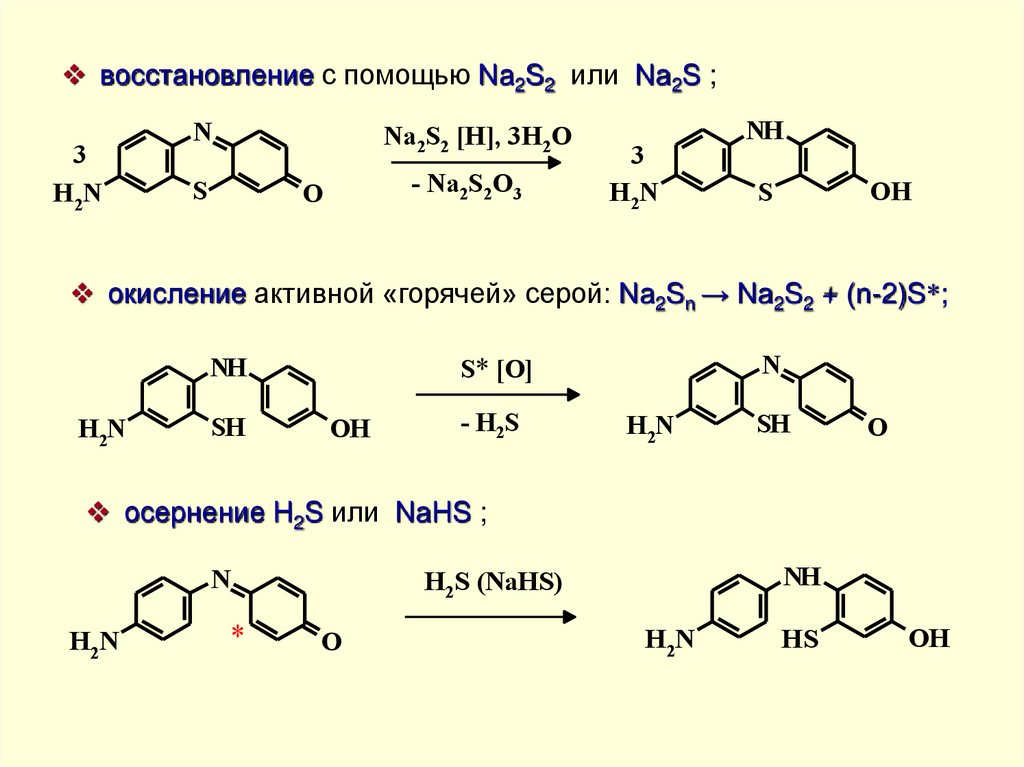
восстановление с помощью Na2S2 или Na2S ;3
H2N
N
Na2S2 [H], 3H2O
S
- Na2S2O3
O
3
H2N
NH
OH
S
окисление активной «горячей» серой: Na2Sn → Na2S2 + (n-2)S*;
H2N
SH
N
S* [O]
NH
OH
- H2S
H2N
SH
O
осернение H2S или NaHS ;
N
H2N
*
NH
H2S (NaHS)
O
H2N
HS
OH
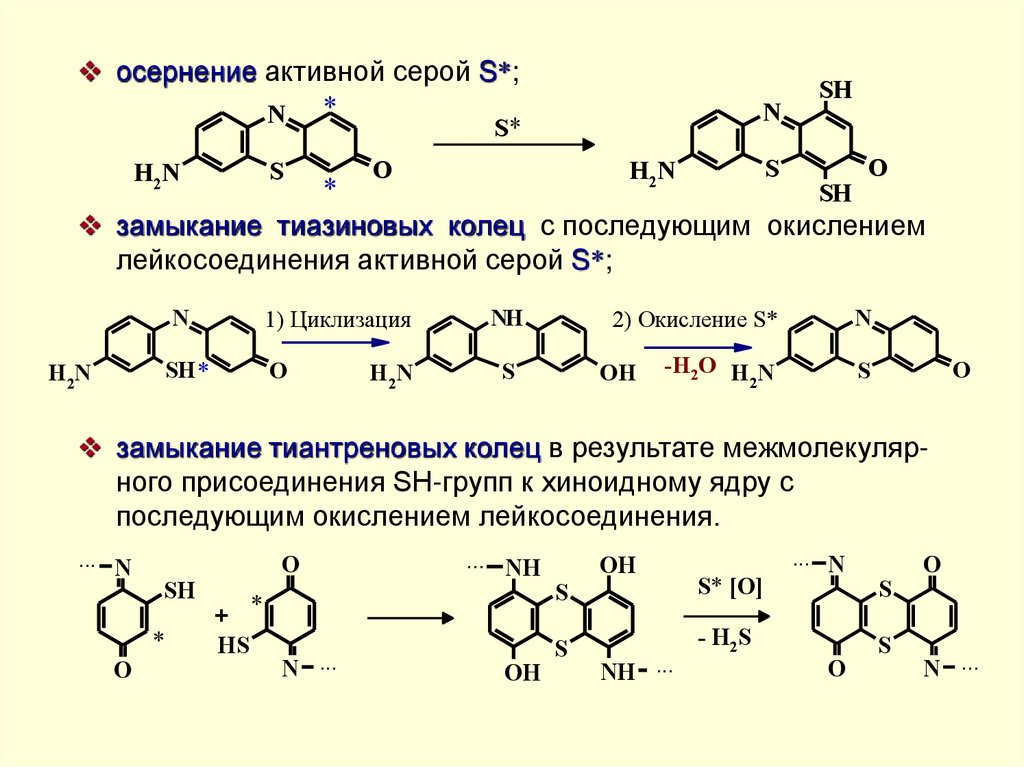
35.
осернение активной серой S*;N *
S*
S
H2N
N
O
H2N
SH
S
O
*
SH
замыкание тиазиновых колец с последующим окислением
лейкосоединения активной серой S*;
H2N
N
1) Циклизация
NH
2) Окисление S*
N
SH*
O
S
OH
-H2O H N
S
H2N
2
O
замыкание тиантреновых колец в результате межмолекулярного присоединения SH-групп к хиноидному ядру с
последующим окислением лейкосоединения.
... N
SH
*
O
O
... NH
OH
+ *
S
S* [O]
HS
S
- H2S
N ...
OH
NH ...
... N
O
S
S
O
N ...
36.
• В результате протекания перечисленных выше реакций изхинониминовых красителей образуются глубоко окрашенные
соединения с большей молекулярной массой – растворимые в
воде лейкосоединения.
• Заключительной операцией сернистой "варки" является
выделение красителя из реакционной массы. Ее осуществляют
барботированием воздуха в реакционную массу при 85-90 С
или реже добавлением окислителя (NaNO2).
• Протекающий при этом окислительный процесс необходим для
превращения содержащихся в молекулах ионогенных HS-групп
в дисульфидные –S-S– и дисульфоксидные –SO-SO – группы и
перевода водорастворимого лейкосоединения в нерастворимое
состояние.
R SNa
O2[O], CO2
- Na2CO3
R S S R
[O]
O
R S S R
O
37.
• Однако в реакционной массе сернистой варки, как правило,присутствует большой избыток полисульфида натрия. Под
действием окислителя он превращается в тиосульфат натрия и
выделяет коллоидную серу, которая загрязняет краситель и
затрудняет фильтрацию реакционной смеси.
Na2Sn + 3 [O]
Na2S2O3 + (n-2) S
• Поэтому рекомендуется при окислительной обработке лейкосоединения в массу вводить сульфит натрия Na2SO3, который
связывает "сверхдисульфидную" серу и переводит ее в водный
раствор в виде тиосульфата натрия.
Na2SO3 + S
Na2S2O3
• После фильтрации к пасте сернистого красителя добавляют до
10% NaCl, что предотвращает самовозгорание красителя при
сушке, и готовый продукт высушивают в вакууме.
38.
• Продукты сернистой "варки" получили название сернистыхкрасителей. Химизм их образования и точное строение
сернистых красителей не всегда доказаны, но установлено:
фенотиазиновые остатки входят в состав молекул сернистых
красителей;
фенотиазиновые остатки связаны между собой сульфидными
(-S-), сульфоксидными (-SO-) мостиками или посредством
тиантреновых структур;
в больших и сложных молекулах сернистых красителей
присутствуют дисульфидные связи (-S-S-) и тиокетонные группы
(C=S).
Способ крашения сернистыми красителями аналогичен крашению
кубовыми красителями. Но в отличие от них, перед крашением
сернистые красители переводят в растворимое в воде лейкосоединение нагреванием в водном растворе сульфида натрия Na2S.
39.
• Гидроксид натрия, необходимый для превращенияобразующихся тиольных групп в ионизированные тиолятные
группы, образуется вследствие гидролиза сульфида натрия.
Kp S S Kp
[H] Na2S
[O] O2
2 Kp SH
NaOH
CO2
2 Kp S Na+
Na2S + H2O = NaHS + NaOH
• После выбирания лейкосоединения целлюлозным волокном из
красильной ванны его переводят на волокне в нерастворимое
состояние окислением кислородом воздуха.
Первые сернистые красители открыли в 1873 г. французские
химики Круасан и Бретоньер. Они подвергли осернению некоторые
хинонимины и в определенных условиях получали интенсивно
окрашенные в синий и синевато-черный цвет растворы, которые
после пропитки ткани и экспозиции ее на воздухе давали прочные
окраски. Одна из их методик лежит в основе синтеза Сернистого
синего К.
40.
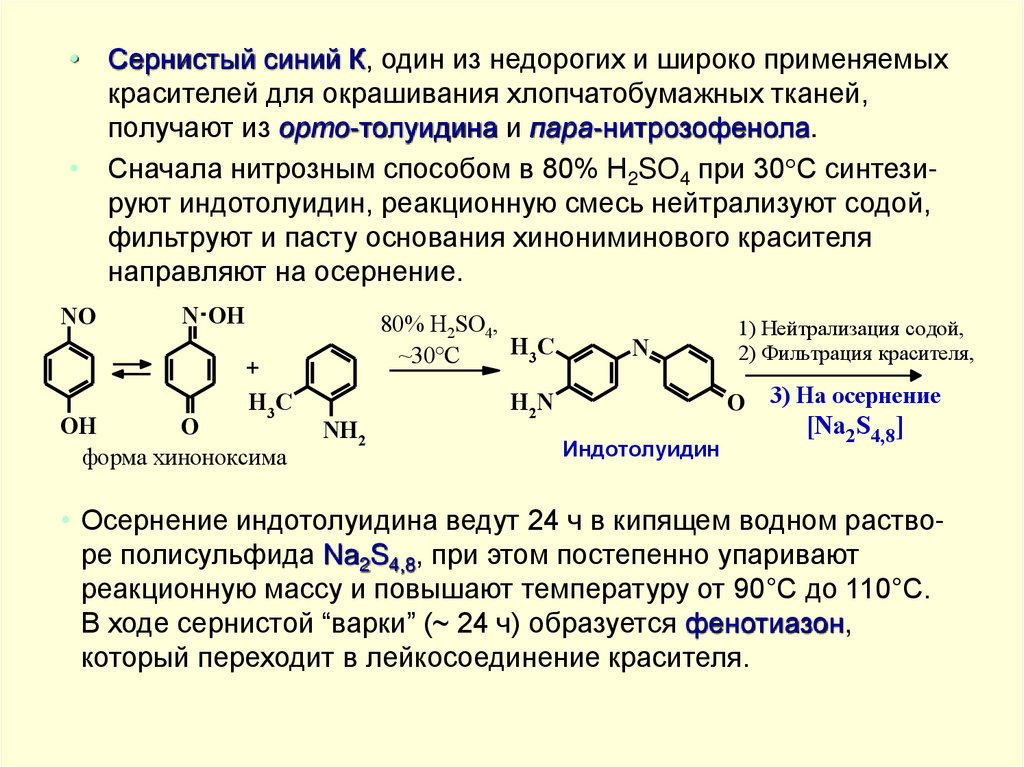
• Сернистый синий К, один из недорогих и широко применяемыхкрасителей для окрашивания хлопчатобумажных тканей,
получают из орто-толуидина и пара-нитрозофенола.
• Сначала нитрозным способом в 80% H2SO4 при 30 С синтезируют индотолуидин, реакционную смесь нейтрализуют содой,
фильтруют и пасту основания хинониминового красителя
направляют на осернение.
NO
N OH
80% H2SO4,
H3C
~30°C
+
H3C
OH
O
форма хиноноксима
NH2
N
H2N
1) Нейтрализация содой,
2) Фильтрация красителя,
O
Индотолуидин
3) На осернение
[Na2S4,8]
• Осернение индотолуидина ведут 24 ч в кипящем водном растворе полисульфида Na2S4,8, при этом постепенно упаривают
реакционную массу и повышают температуру от 90°С до 110°С.
В ходе сернистой “варки” (~ 24 ч) образуется фенотиазон,
который переходит в лейкосоединение красителя.
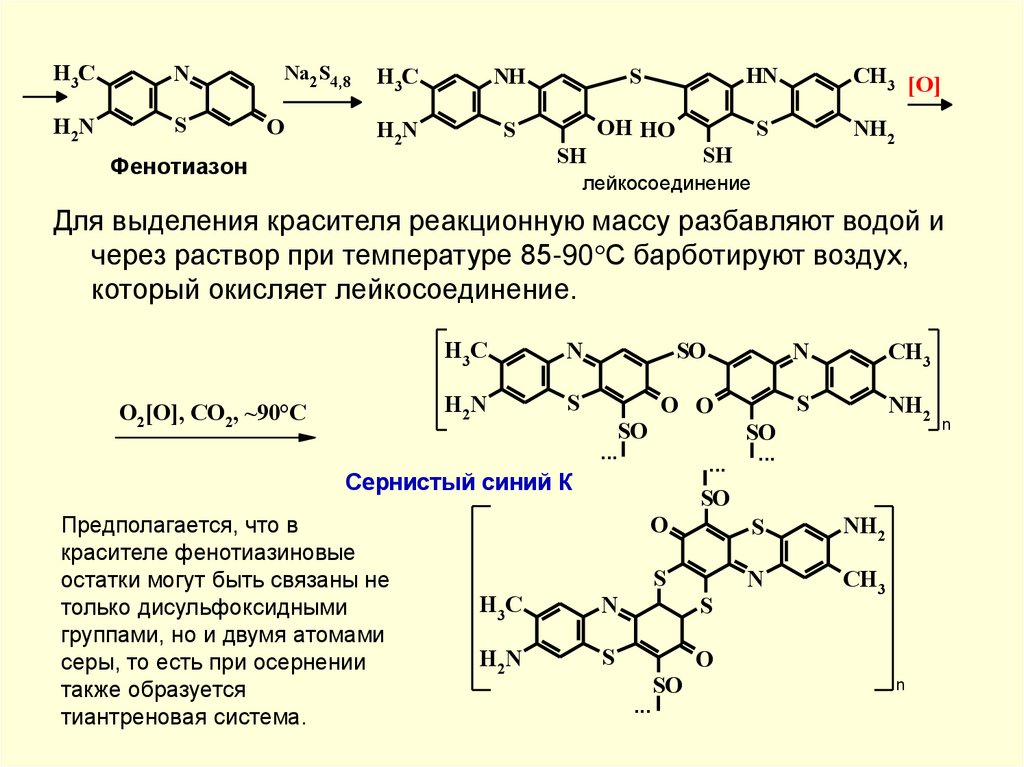
41.
H3CN
H2N
S
Na2S4,8
O
H3C
NH
S
HN
CH3 [O]
H2N
S
OH HO
S
NH2
SH
SH
Фенотиазон
лейкосоединение
Для выделения красителя реакционную массу разбавляют водой и
через раствор при температуре 85-90 С барботируют воздух,
который окисляет лейкосоединение.
O2[O], CO2, ~90°C
H3C
N
SO
N
CH3
H2N
S
O O
S
NH2
SO
SO
...
...
Сернистый синий К
Предполагается, что в
красителе фенотиазиновые
остатки могут быть связаны не
только дисульфоксидными
группами, но и двумя атомами
серы, то есть при осернении
также образуется
тиантреновая система.
...
SO
O
S
NH2
S
N
CH3
H3C
N
S
H2N
S
O
...
SO
n
n
42.
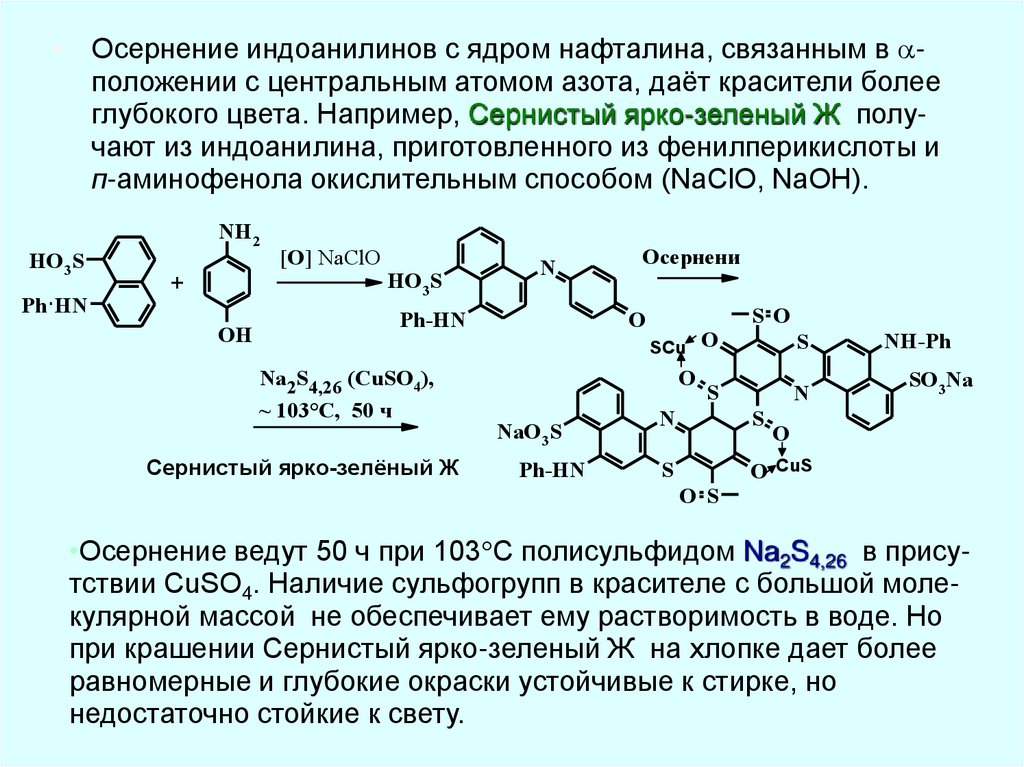
• Осернение индоанилинов с ядром нафталина, связанным в положении с центральным атомом азота, даёт красители болееглубокого цвета. Например, Сернистый ярко-зеленый Ж получают из индоанилина, приготовленного из фенилперикислоты и
п-аминофенола окислительным способом (NaClO, NaOH).
HO3S
Ph HN
NH2
+
OH
[O] NaClO
HO3S
N
Ph-HN
Осернени
е
O
SCu
Na2S4,26 (CuSO4),
~ 103°C, 50 ч
Сернистый ярко-зелёный Ж
O
NaO3S
Ph-HN
O
SO
S
S
N
N
S
S
O CuS
O S
NH-Ph
SO3Na
O
•Осернение ведут 50 ч при 103 С полисульфидом Na2S4,26 в присутствии CuSO4. Наличие сульфогрупп в красителе с большой молекулярной массой не обеспечивает ему растворимость в воде. Но
при крашении Сернистый ярко-зеленый Ж на хлопке дает более
равномерные и глубокие окраски устойчивые к стирке, но
недостаточно стойкие к свету.
43. 7.4. Диазиновые красители
44.
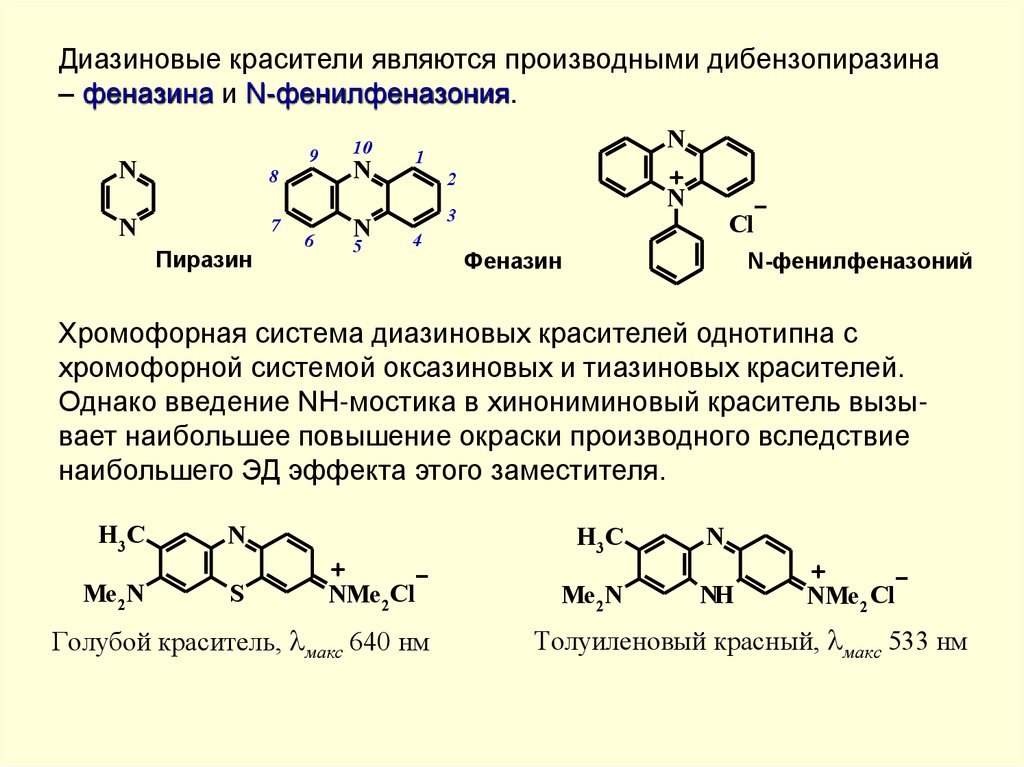
Диазиновые красители являются производными дибензопиразина– феназина и N-фенилфеназония.
10
9
N
N
8
N
7
Пиразин
N
6
5
N
1
+
2
N
3
4
-
Cl
N-фенилфеназоний
Феназин
Хромофорная система диазиновых красителей однотипна с
хромофорной системой оксазиновых и тиазиновых красителей.
Однако введение NH-мостика в хинониминовый краситель вызывает наибольшее повышение окраски производного вследствие
наибольшего ЭД эффекта этого заместителя.
H3C
Me 2N
N
S
+
-
NMe 2Cl
Голубой краситель, макс 640 нм
H3C
N
Me 2N
NH
+
-
NMe 2 Cl
Толуиленовый красный, макс 533 нм
45.
• Диазиновая хромофорная система позволяет получатькрасители широкой гаммы цветов от фиолетово-красного до
голубого. Красители черного, коричневого цветов имеют
гибридные хромофорные системы, построенные на основе
феназиновых и тиазиновых гетероциклов.
• Простейшие феназиновые красители, соответствующие
диариламиновым, чувствительны к щелочному гидролизу и не
применяются в текстильной промышленности. Производные Nфенилфеназония – аналоги триариламиновых, более устойчивы
и на их основе получают технически важные основные,
кислотные, спирторастворимые, сернистые красители и
пигменты.
46.
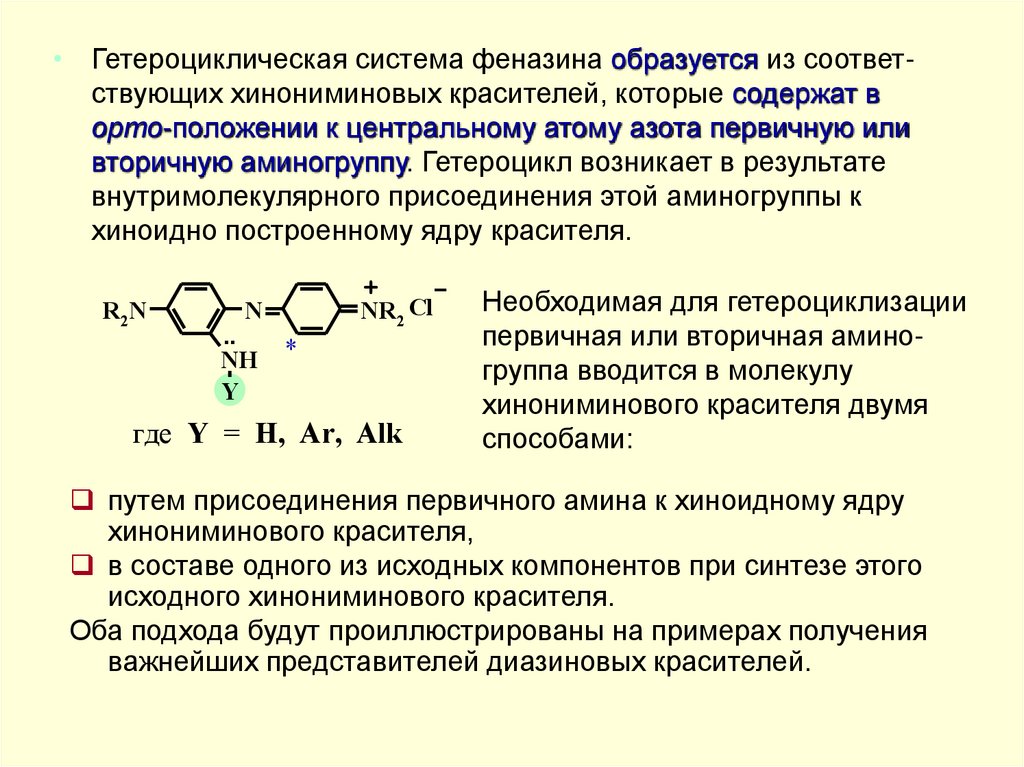
• Гетероциклическая система феназина образуется из соответствующих хинониминовых красителей, которые содержат ворто-положении к центральному атому азота первичную или
вторичную аминогруппу. Гетероцикл возникает в результате
внутримолекулярного присоединения этой аминогруппы к
хиноидно построенному ядру красителя.
R2N
..
+
N
NH
Y
-
NR2 Cl
*
где Y = H, Ar, Alk
Необходимая для гетероциклизации
первичная или вторичная аминогруппа вводится в молекулу
хинониминового красителя двумя
способами:
путем присоединения первичного амина к хиноидному ядру
хинониминового красителя,
в составе одного из исходных компонентов при синтезе этого
исходного хинониминового красителя.
Оба подхода будут проиллюстрированы на примерах получения
важнейших представителей диазиновых красителей.
47. 7.4.1. Основные диазиновые красители
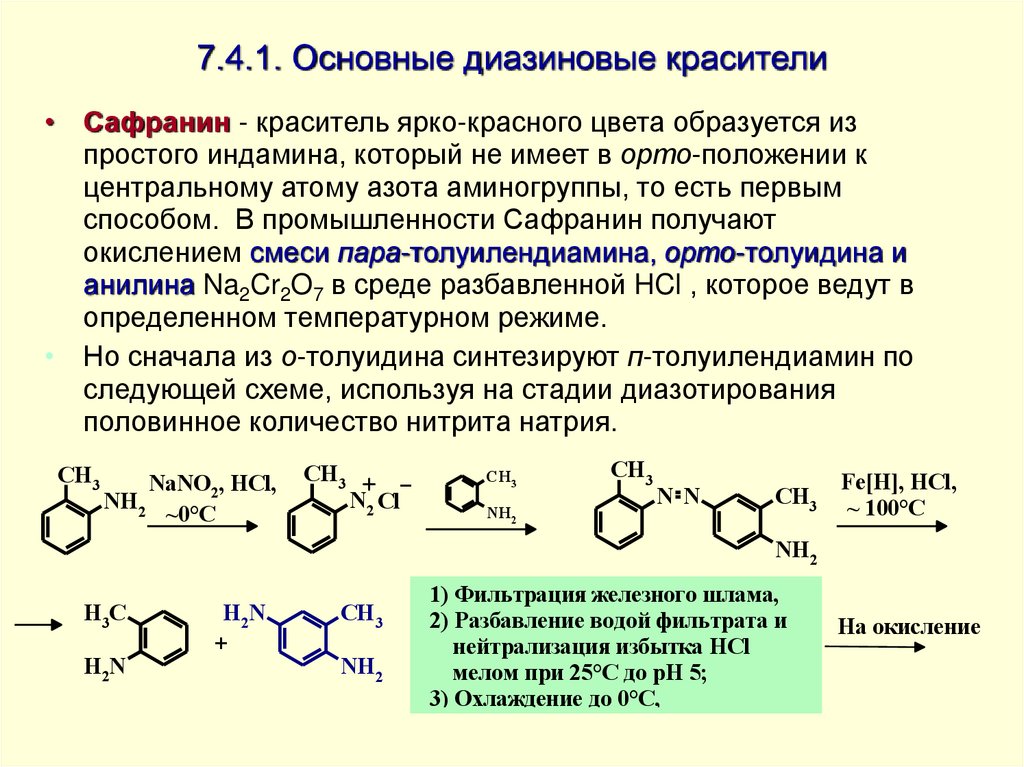
• Сафранин - краситель ярко-красного цвета образуется изпростого индамина, который не имеет в орто-положении к
центральному атому азота аминогруппы, то есть первым
способом. В промышленности Сафранин получают
окислением смеси пара-толуилендиамина, орто-толуидина и
анилина Na2Cr2O7 в среде разбавленной HCl , которое ведут в
определенном температурном режиме.
• Но сначала из о-толуидина синтезируют п-толуилендиамин по
следующей схеме, используя на стадии диазотирования
половинное количество нитрита натрия.
CH3
NaNO2, HCl,
NH2
~0°C
CH3 +
N2 Cl
CH3
NH2
CH3
N N
CH3
Fe[H], HCl,
~ 100°C
NH2
H3C
H2N
H2N
+
CH3
NH2
1) Фильтрация железного шлама,
2) Разбавление водой фильтрата и
нейтрализация избытка HCl
мелом при 25°C до рН 5;
3) Охлаждение до 0°C,
На окисление
48.
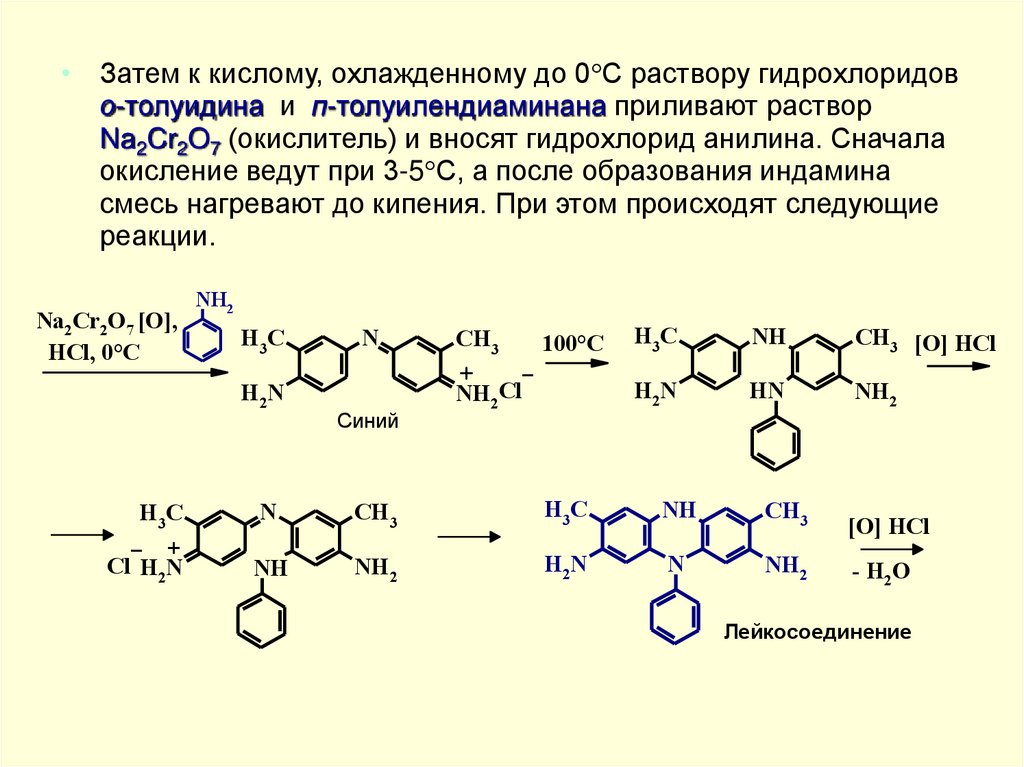
• Затем к кислому, охлажденному до 0 С раствору гидрохлоридово-толуидина и п-толуилендиаминана приливают раствор
Na2Cr2O7 (окислитель) и вносят гидрохлорид анилина. Сначала
окисление ведут при 3-5 С, а после образования индамина
смесь нагревают до кипения. При этом происходят следующие
реакции.
Na2Cr2O7 [O],
HCl, 0°C
NH2
H3C
H2N
H3C
- +
Cl H2N
N
CH3
+
Синий
100°C
-
NH2Cl
H3C
NH
CH3 [O] HCl
H2N
HN
NH2
N
CH3
H3C
NH
CH3
[O] HCl
NH
NH2
H2N
N
NH2
- H 2O
Лейкосоединение
49.
[O]H3C
H2N
N
H3C
CH3
+
N
H2N
NH2
-
Cl
N
N
CH3
+
NH2
-
Сафранин
Cl
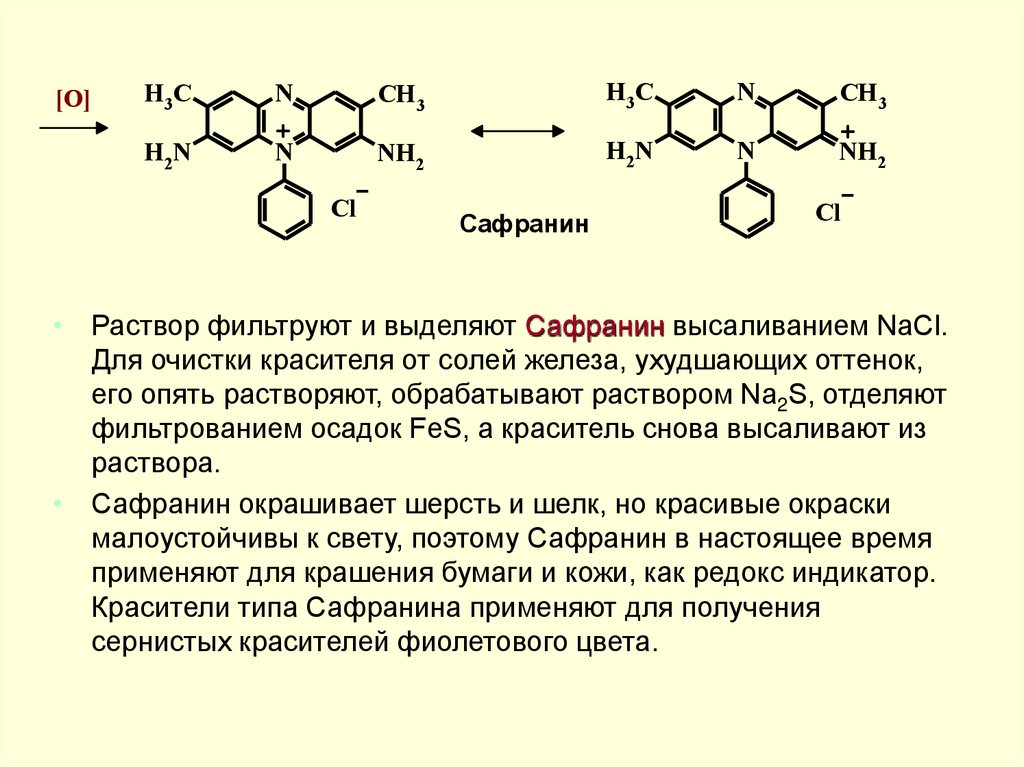
• Раствор фильтруют и выделяют Сафранин высаливанием NaCl.
Для очистки красителя от солей железа, ухудшающих оттенок,
его опять растворяют, обрабатывают раствором Na2S, отделяют
фильтрованием осадок FeS, а краситель снова высаливают из
раствора.
• Сафранин окрашивает шерсть и шелк, но красивые окраски
малоустойчивы к свету, поэтому Сафранин в настоящее время
применяют для крашения бумаги и кожи, как редокс индикатор.
Красители типа Сафранина применяют для получения
сернистых красителей фиолетового цвета.
50. 7.4.2. Кислотные диазиновые красители
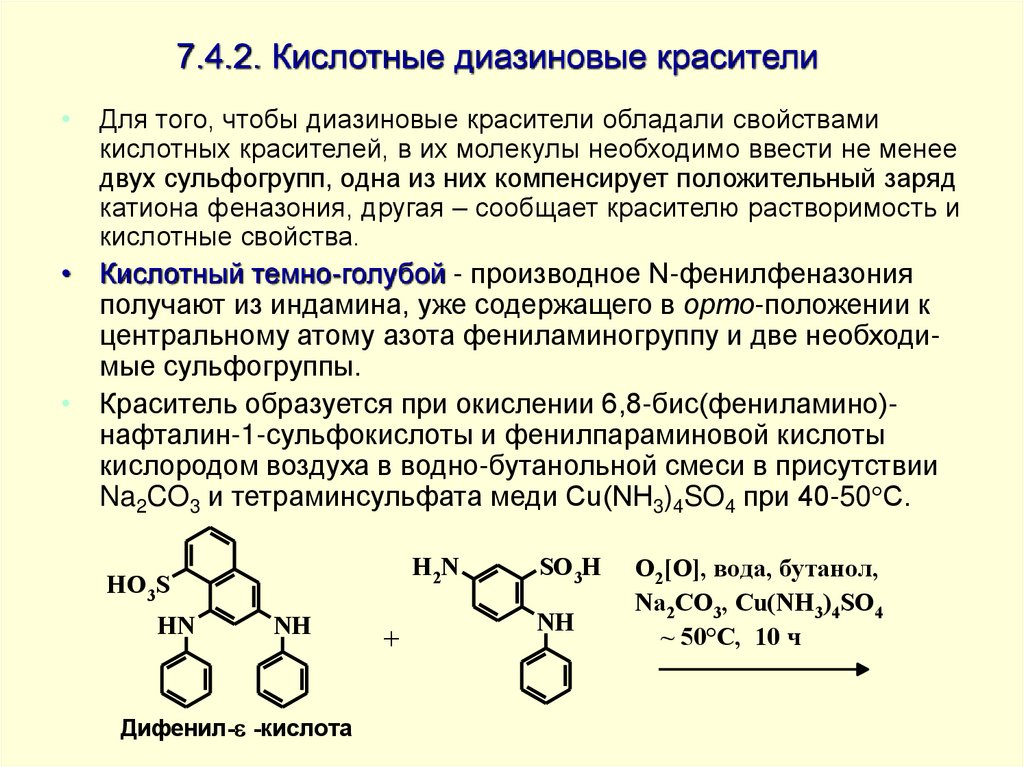
Для того, чтобы диазиновые красители обладали свойствами
кислотных красителей, в их молекулы необходимо ввести не менее
двух сульфогрупп, одна из них компенсирует положительный заряд
катиона феназония, другая – сообщает красителю растворимость и
кислотные свойства.
• Кислотный темно-голубой - производное N-фенилфеназония
получают из индамина, уже содержащего в орто-положении к
центральному атому азота фениламиногруппу и две необходимые сульфогруппы.
• Краситель образуется при окислении 6,8-бис(фениламино)нафталин-1-сульфокислоты и фенилпараминовой кислоты
кислородом воздуха в водно-бутанольной смеси в присутствии
Na2CO3 и тетраминсульфата меди Cu(NH3)4SO4 при 40-50 С.
H 2N
HO 3S
HN
NH
Дифенил- -кислота
SO 3H
NH
O2[O], вода, бутанол,
Na2CO3, Cu(NH3)4SO4
~ 50°C, 10 ч
51.
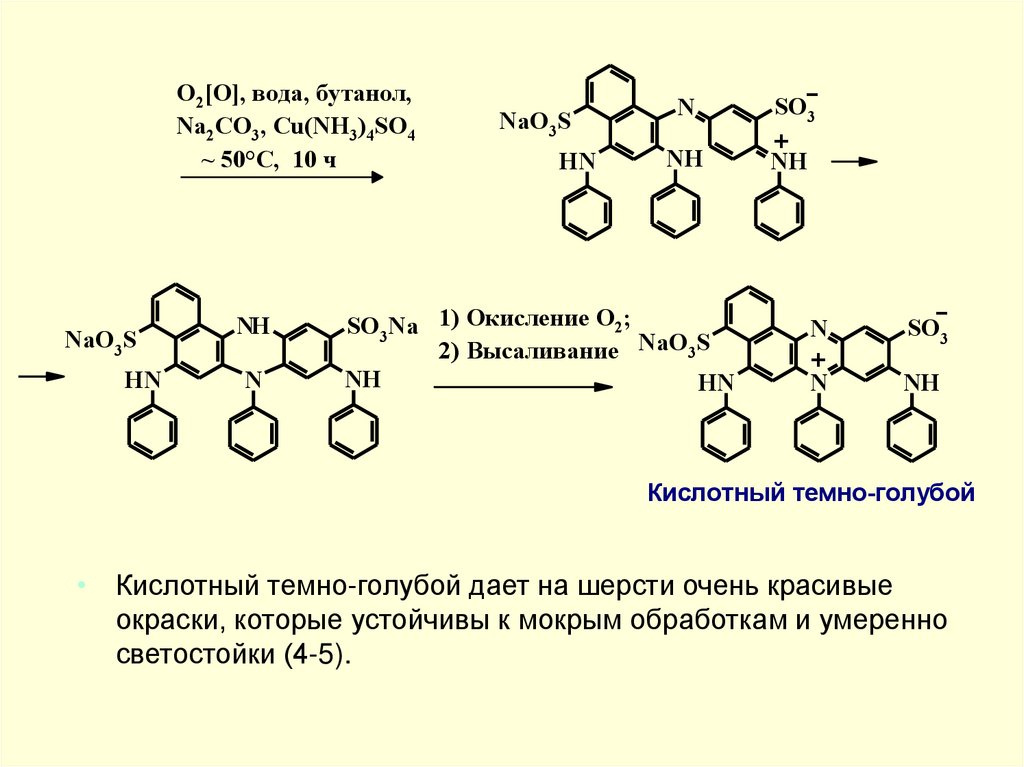
O2[O], вода, бутанол,Na2CO3, Cu(NH3)4SO4
~ 50°C, 10 ч
NaO3S
HN
NH
N
NaO3S
HN
N
SO3
NH
NH
SO3Na 1) Окисление O2;
2) Высаливание NaO3S
NH
HN
+
N
+
N
-
SO3
NH
Кислотный темно-голубой
• Кислотный темно-голубой дает на шерсти очень красивые
окраски, которые устойчивы к мокрым обработкам и умеренно
светостойки (4-5).
52. 7.4.3. Индулины и нигрозины.
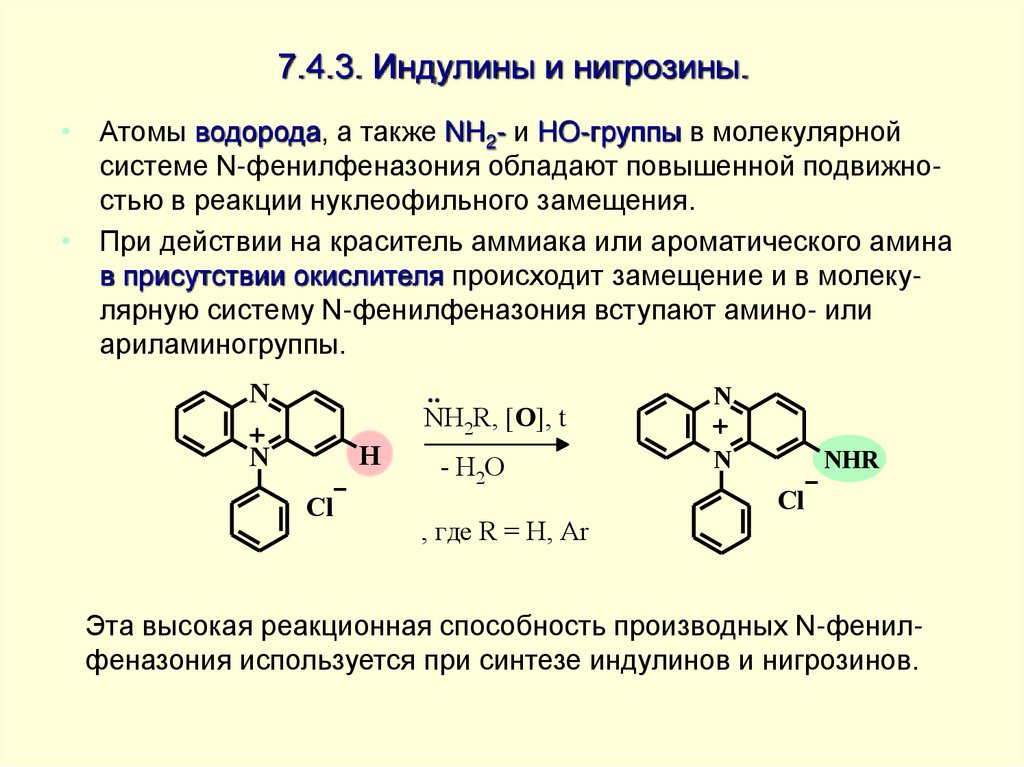
• Атомы водорода, а также NH2- и HO-группы в молекулярнойсистеме N-фенилфеназония обладают повышенной подвижностью в реакции нуклеофильного замещения.
• При действии на краситель аммиака или ароматического амина
в присутствии окислителя происходит замещение и в молекулярную систему N-фенилфеназония вступают амино- или
ариламиногруппы.
N
..
NH2R, [O], t
+
H
N
-
Cl
- H2O
N
+
N
-
NHR
Cl
, где R = H, Ar
Эта высокая реакционная способность производных N-фенилфеназония используется при синтезе индулинов и нигрозинов.
53. Индулины.
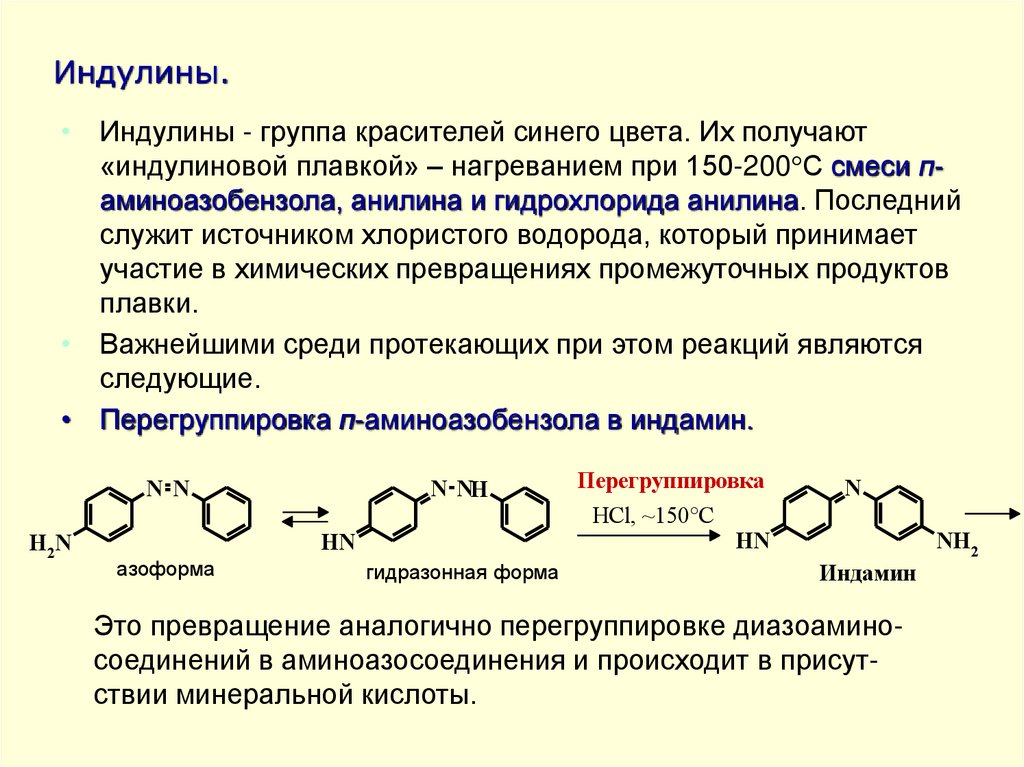
• Индулины - группа красителей синего цвета. Их получают«индулиновой плавкой» – нагреванием при 150-200 С смеси паминоазобензола, анилина и гидрохлорида анилина. Последний
служит источником хлористого водорода, который принимает
участие в химических превращениях промежуточных продуктов
плавки.
• Важнейшими среди протекающих при этом реакций являются
следующие.
• Перегруппировка п-аминоазобензола в индамин.
N N
N NH
Перегруппировка
HCl, ~150°C
H2N
HN
азоформа
гидразонная форма
N
HN
NH2
Индамин
Это превращение аналогично перегруппировке диазоаминосоединений в аминоазосоединения и происходит в присутствии минеральной кислоты.
54.
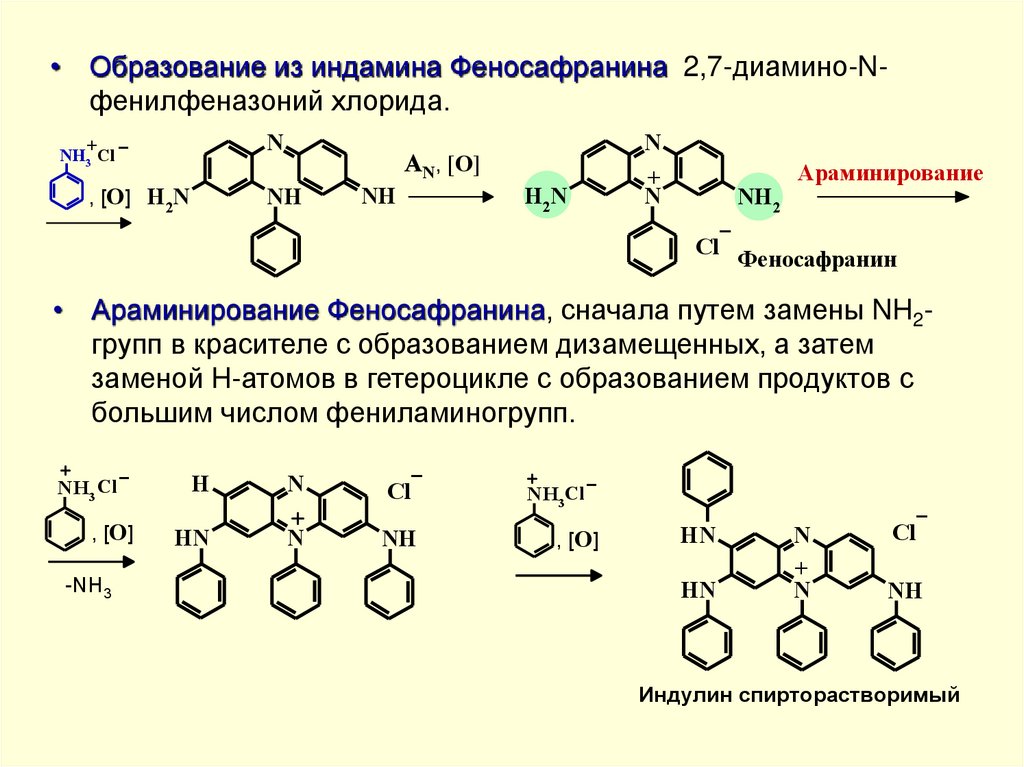
• Образование из индамина Феносафранина 2,7-диамино-Nфенилфеназоний хлорида.N
+
NH3 Cl -
, [O] H2N
AN, [O]
NH
NH
H2N
N
+
N
NH2
Араминирование
-
Cl
Феносафранин
• Араминирование Феносафранина, сначала путем замены NH2групп в красителе с образованием дизамещенных, а затем
заменой H-атомов в гетероцикле с образованием продуктов с
большим числом фениламиногрупп.
+
-
H
N
, [O ]
HN
N
NH3 Cl
-NH3
+
-
Cl
NH
+
NH3Cl -
, [O]
HN
HN
N
+
N
-
Cl
NH
Индулин спирторастворимый
55.
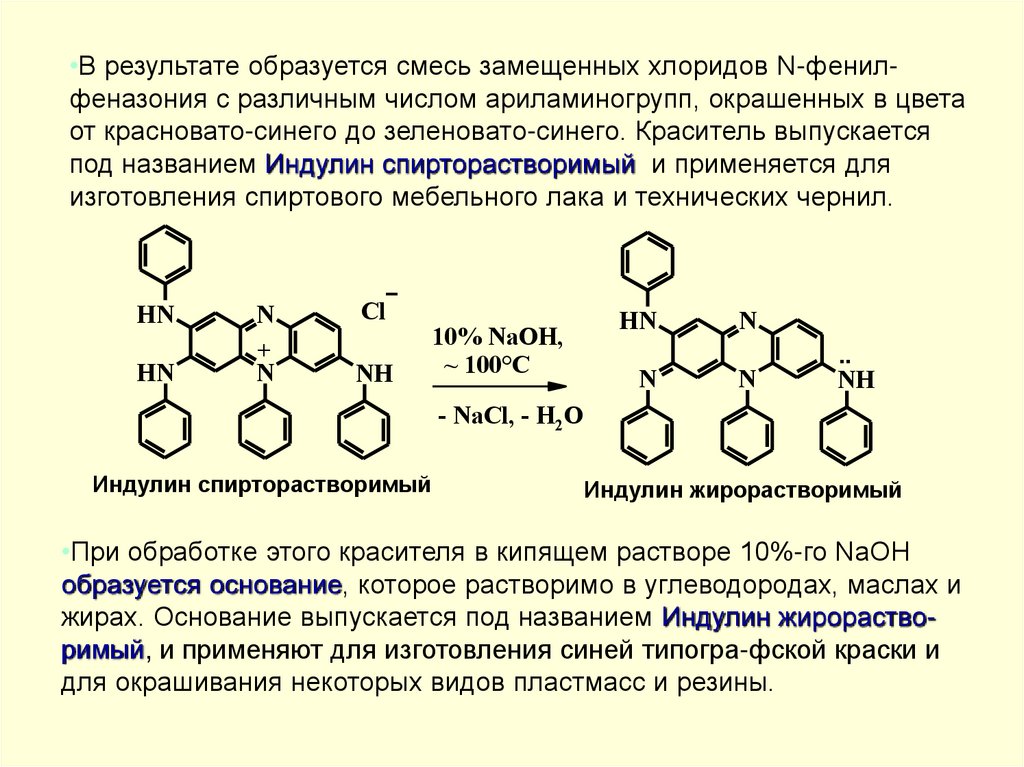
•В результате образуется смесь замещенных хлоридов N-фенилфеназония с различным числом ариламиногрупп, окрашенных в цветаот красновато-синего до зеленовато-синего. Краситель выпускается
под названием Индулин спирторастворимый и применяется для
изготовления спиртового мебельного лака и технических чернил.
HN
HN
N
+
N
-
Cl
NH
10% NaOH,
~ 100°C
HN
N
N
N
..
NH
- NaCl, - H2O
Индулин спирторастворимый
Индулин жирорастворимый
•При обработке этого красителя в кипящем растворе 10%-го NaOH
образуется основание, которое растворимо в углеводородах, маслах и
жирах. Основание выпускается под названием Индулин жирорастворимый, и применяют для изготовления синей типогра-фской краски и
для окрашивания некоторых видов пластмасс и резины.
56.
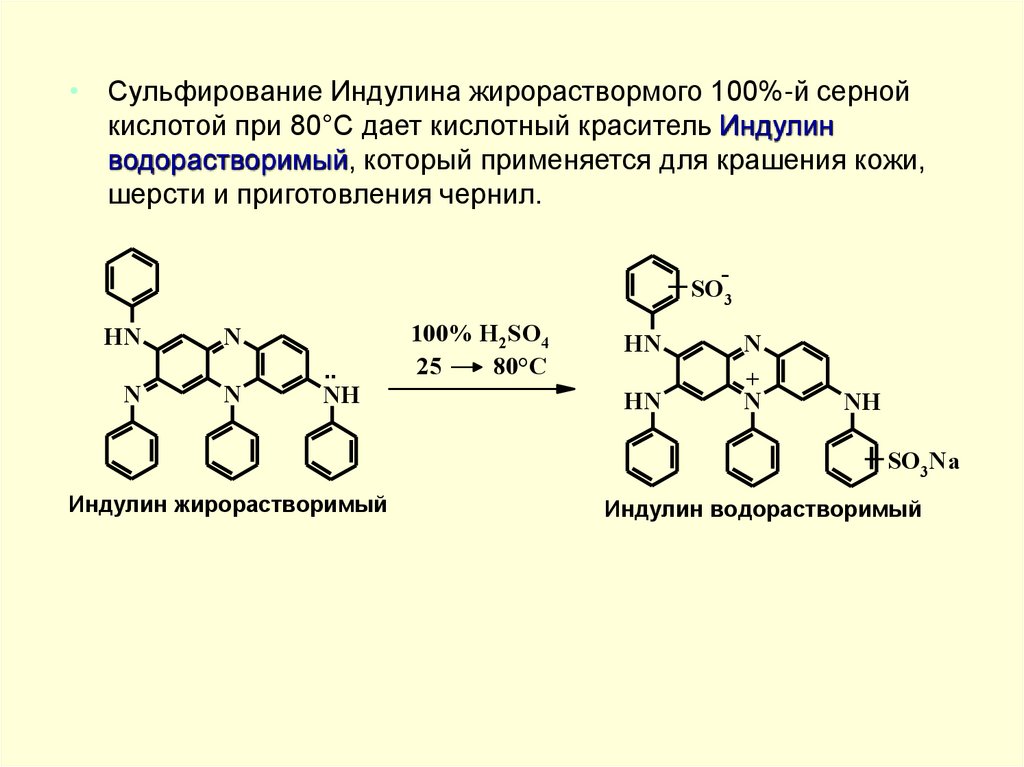
• Сульфирование Индулина жирораствормого 100%-й сернойкислотой при 80°С дает кислотный краситель Индулин
водорастворимый, который применяется для крашения кожи,
шерсти и приготовления чернил.
SO3
HN
N
N
N
..
NH
100% H2SO4
25
80°C
HN
HN
N
+
N
NH
SO3Na
Индулин жирорастворимый
Индулин водорастворимый
57. Нигрозины
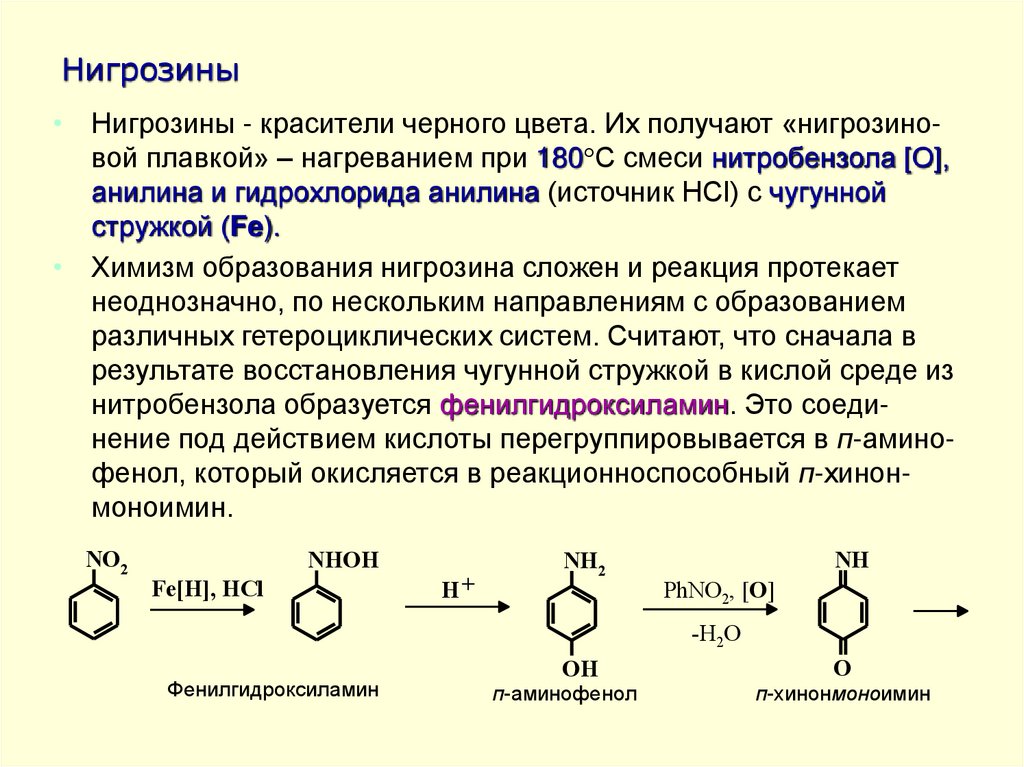
• Нигрозины - красители черного цвета. Их получают «нигрозиновой плавкой» – нагреванием при 180 С смеси нитробензола [O],анилина и гидрохлорида анилина (источник HCl) с чугунной
стружкой (Fe).
• Химизм образования нигрозина сложен и реакция протекает
неоднозначно, по нескольким направлениям с образованием
различных гетероциклических систем. Считают, что сначала в
результате восстановления чугунной стружкой в кислой среде из
нитробензола образуется фенилгидроксиламин. Это соединение под действием кислоты перегруппировывается в п-аминофенол, который окисляется в реакционноспособный п-хинонмоноимин.
NO2
NHOH
Fe[H], HCl
H+
NH2
NH
PhNO2, [O]
-H2O
Фенилгидроксиламин
OH
п-аминофенол
O
п-хинонмоноимин
58.
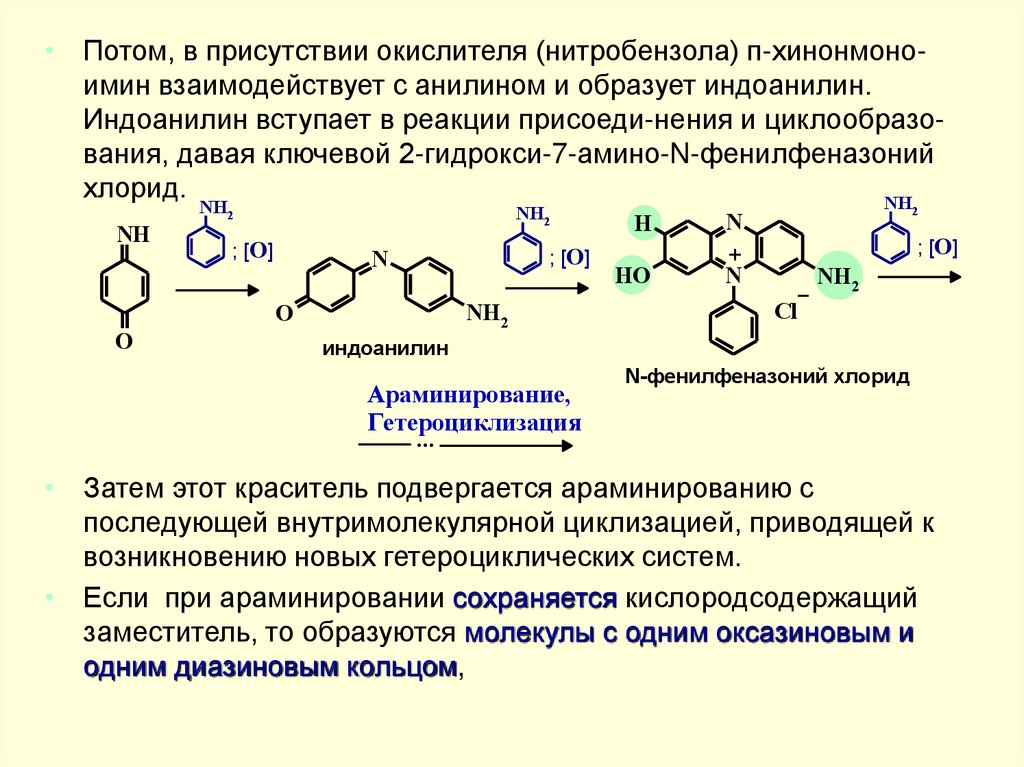
• Потом, в присутствии окислителя (нитробензола) п-хинонмоноимин взаимодействует с анилином и образует индоанилин.Индоанилин вступает в реакции присоеди-нения и циклообразования, давая ключевой 2-гидрокси-7-амино-N-фенилфеназоний
хлорид.
NH
NH
NH2
NH2
; [O]
NH2
O
O
; [O]
N
H
HO
2
N
; [O]
+
N
-
NH2
Cl
индоанилин
Араминирование,
Гетероциклизация
...
N-фенилфеназоний хлорид
• Затем этот краситель подвергается араминированию с
последующей внутримолекулярной циклизацией, приводящей к
возникновению новых гетероциклических систем.
• Если при араминировании сохраняется кислородсодержащий
заместитель, то образуются молекулы с одним оксазиновым и
одним диазиновым кольцом,
59.
NHO
N
+
N
NH
R
NH
Cl
N
N
+
N
R
NH
-
Cl
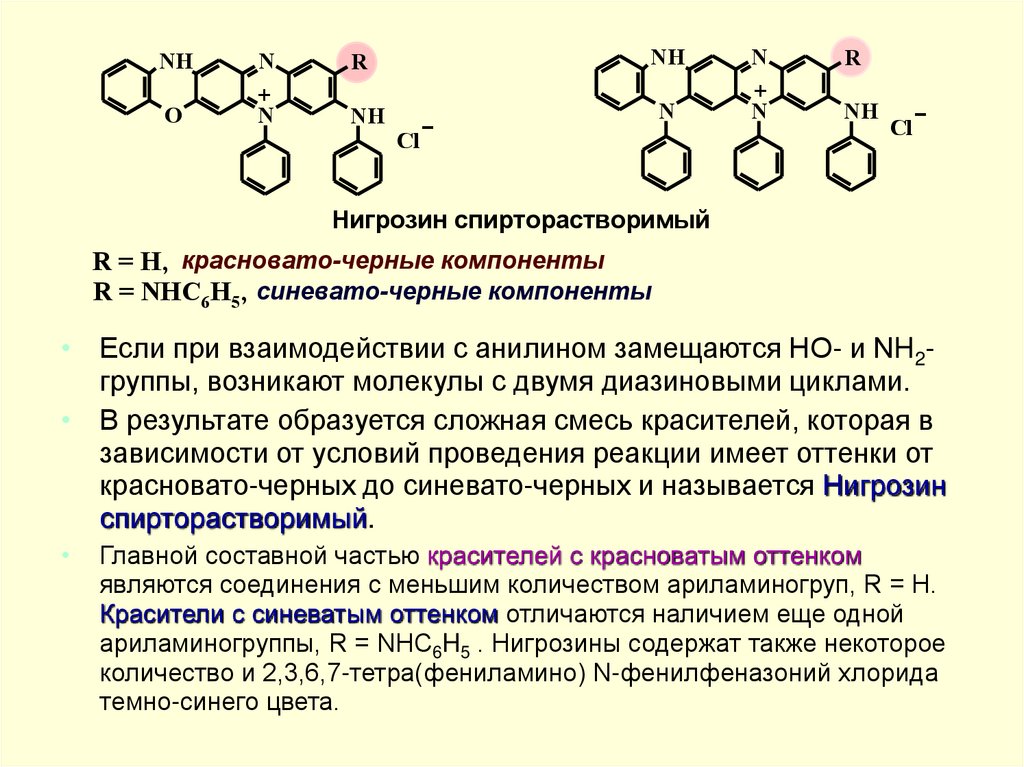
Нигрозин спирторастворимый
R = H, красновато-черные компоненты
R = NHC6H5, синевато-черные компоненты
• Если при взаимодействии с анилином замещаются HO- и NH2группы, возникают молекулы с двумя диазиновыми циклами.
• В результате образуется сложная смесь красителей, которая в
зависимости от условий проведения реакции имеет оттенки от
красновато-черных до синевато-черных и называется Нигрозин
спирторастворимый.
Главной составной частью красителей с красноватым оттенком
являются соединения с меньшим количеством ариламиногруп, R = H.
Красители с синеватым оттенком отличаются наличием еще одной
ариламиногруппы, R = NHC6H5 . Нигрозины содержат также некоторое
количество и 2,3,6,7-тетра(фениламино) N-фенилфеназоний хлорида
темно-синего цвета.
60.
• Нигрозин спирторастворимый применяется для крашенияпластмасс, дерева и изготовления спиртовых лаков. Подобно
индулинам нигрозины выпускают в виде основания и
сульфопроизводных.
• Нигрозин жирорастворимый получают из Нигрозина спирторастворимого нагреванием в 40%-ом растворе едкого натра. Его
используют для изготовления гуталина, красок для лент
пишущих машинок и типографских красок.
• Сульфированием Нигрозина спирторастворимого при 125 С в
100%-й H2SO4 (моногидрате) получают Нигрозин водорастворимый, который применяют в качестве кислотный красителя для
кожи, шерсти и шелка, а также для изготовления чернил.
61. 7.4.4. Сернистые диазиновые красители
• Осернением диазиновых красителей методом «сернистой варки»получают сернистые красители коричневого и фиолетового цвета
с красноватым оттенком, а также краситель черного цвета.
• Предполагают, что при осернении сохраняется хромофорная
система диазиновы х красителей, но возникает дисульфидные
(-S-S-) и дисульфоксидные (-SO-SO-) связи, которые соединяют
диазиновые остатки в более крупные молекулы нерастворимых в
воде красителей. Такие серосодержащие производные
приобретают способность при восстановлении Na2S переходить в
лейкосоединения растворимые в воде, благодаря присутствию в
них меркаптидных групп.
Kp S S Kp или Kp S S Kp
O O
Na2S [H]; NaOH
2 Kp SNa
O2, CO2
Лейкосоедине
Лейкосоединения выбираются из раствора целлюлозным волокном и при окислении на волокне воздухом опять превращаются в
исходные сернистые красители.
62.
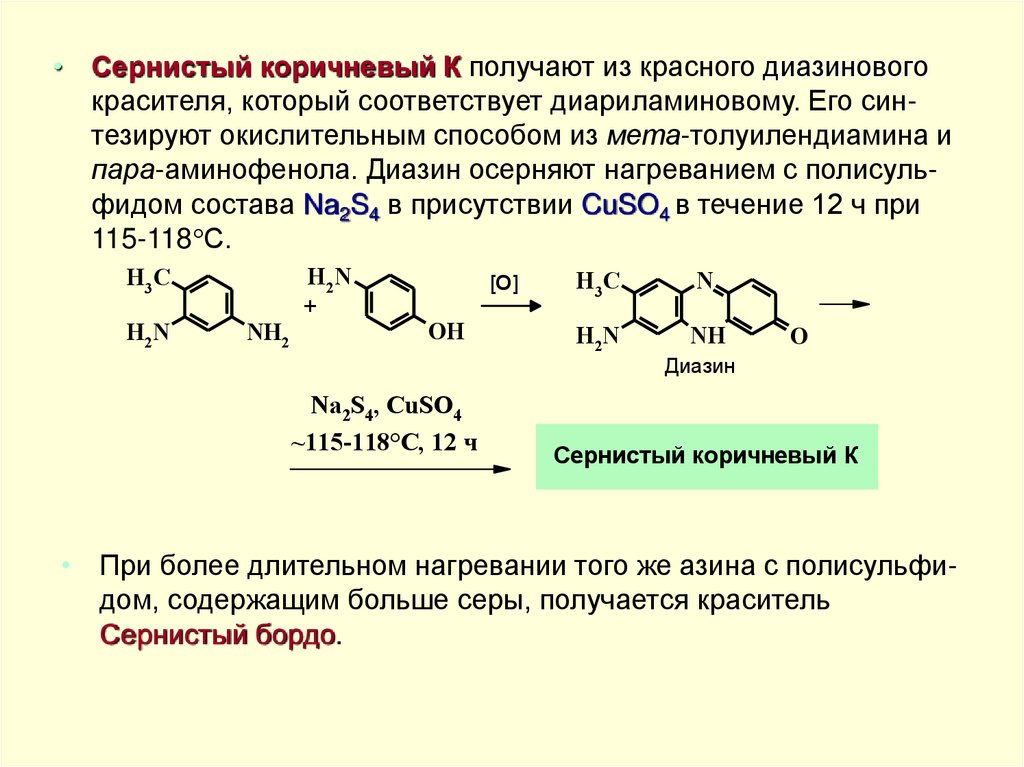
• Сернистый коричневый К получают из красного диазиновогокрасителя, который соответствует диариламиновому. Его синтезируют окислительным способом из мета-толуилендиамина и
пара-аминофенола. Диазин осерняют нагреванием с полисульфидом состава Na2S4 в присутствии CuSO4 в течение 12 ч при
115-118 С.
H3C
H2N
NH2
H 2N
+
[O]
OH
Na2S4, CuSO4
~115-118°C, 12 ч
H3C
N
H2N
NH
O
Диазин
Сернистый коричневый К
• При более длительном нагревании того же азина с полисульфидом, содержащим больше серы, получается краситель
Сернистый бордо.
63.
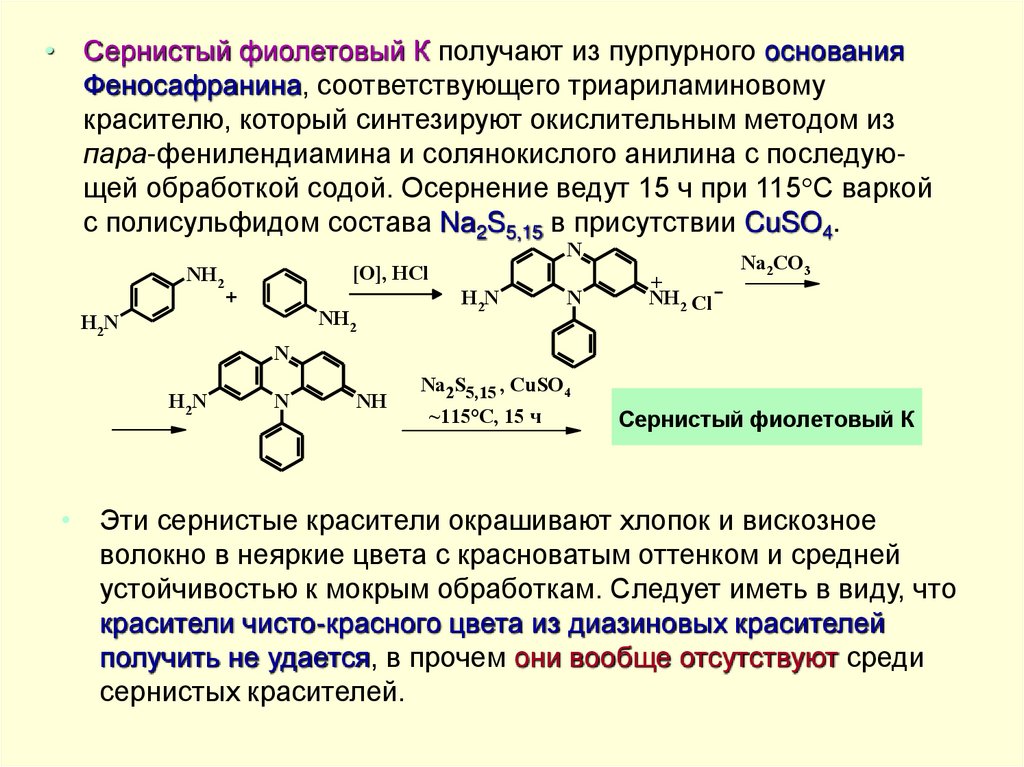
• Сернистый фиолетовый К получают из пурпурного основанияФеносафранина, соответствующего триариламиновому
красителю, который синтезируют окислительным методом из
пара-фенилендиамина и солянокислого анилина с последующей обработкой содой. Осернение ведут 15 ч при 115 С варкой
с полисульфидом состава Na2S5,15 в присутствии CuSO4.
N
NH2
[O], HCl
+
H2N
NH2
H2N
N
+
NH2 Cl
Na2CO3
N
H2N
N
NH
Na2S5,15 , CuSO4
~115°C, 15 ч
Сернистый фиолетовый К
• Эти сернистые красители окрашивают хлопок и вискозное
волокно в неяркие цвета с красноватым оттенком и средней
устойчивостью к мокрым обработкам. Следует иметь в виду, что
красители чисто-красного цвета из диазиновых красителей
получить не удается, в прочем они вообще отсутствуют среди
сернистых красителей.
64.
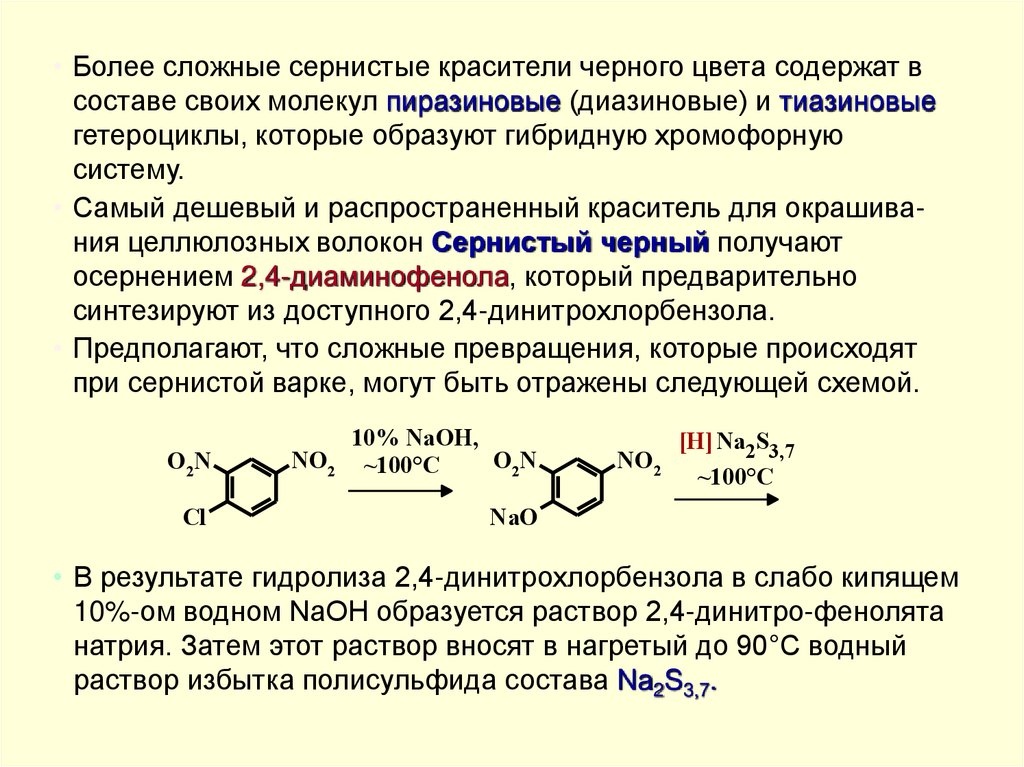
• Более сложные сернистые красители черного цвета содержат всоставе своих молекул пиразиновые (диазиновые) и тиазиновые
гетероциклы, которые образуют гибридную хромофорную
систему.
• Самый дешевый и распространенный краситель для окрашивания целлюлозных волокон Сернистый черный получают
осернением 2,4-диаминофенола, который предварительно
синтезируют из доступного 2,4-динитрохлорбензола.
• Предполагают, что сложные превращения, которые происходят
при сернистой варке, могут быть отражены следующей схемой.
O2N
10% NaOH,
NO2 ~100°C
O2N
Cl
NaO
NO2
[H] Na2S3,7
~100°C
• В результате гидролиза 2,4-динитрохлорбензола в слабо кипящем
10%-ом водном NaOH образуется раствор 2,4-динитро-фенолята
натрия. Затем этот раствор вносят в нагретый до 90°С водный
раствор избытка полисульфида состава Na2S3,7.
65.
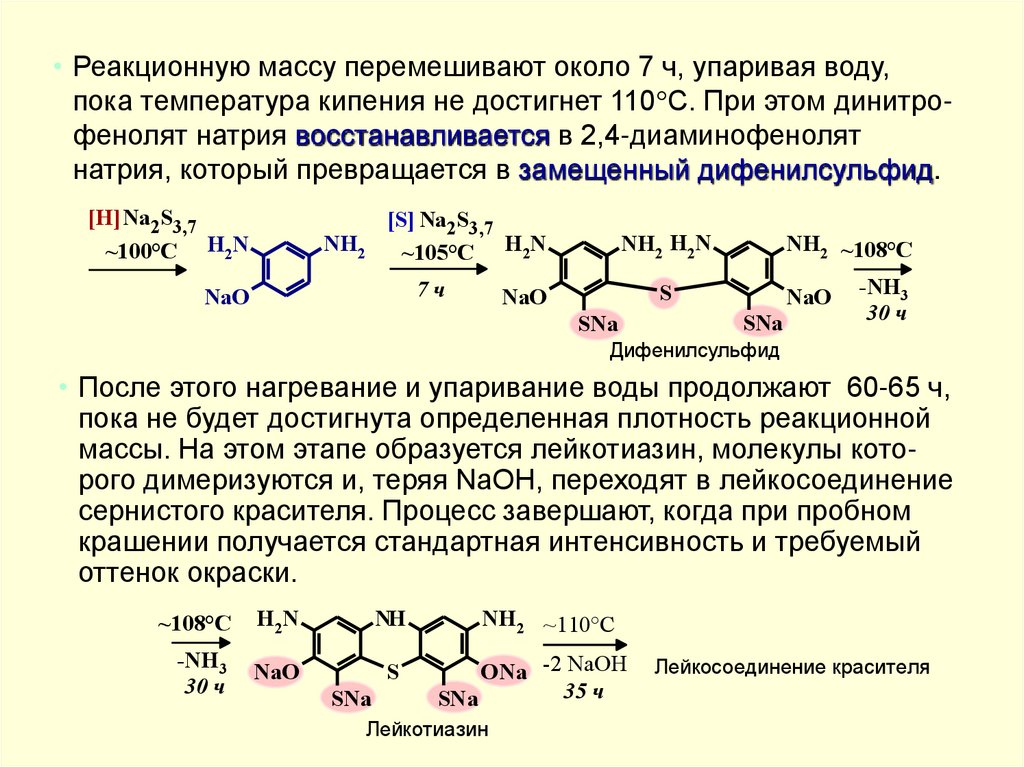
• Реакционную массу перемешивают около 7 ч, упаривая воду,пока температура кипения не достигнет 110 С. При этом динитрофенолят натрия восстанавливается в 2,4-диаминофенолят
натрия, который превращается в замещенный дифенилсульфид.
[H] Na2S3,7
~100°C H2N
[S] Na2S3,7
~105°C H2N
NH2
7ч
NaO
NH2 H2N
NH2 ~108°C
S
NaO
SNa
NaO
SNa
-NH3
30 ч
Дифенилсульфид
• После этого нагревание и упаривание воды продолжают 60-65 ч,
пока не будет достигнута определенная плотность реакционной
массы. На этом этапе образуется лейкотиазин, молекулы которого димеризуются и, теряя NaOH, переходят в лейкосоединение
сернистого красителя. Процесс завершают, когда при пробном
крашении получается стандартная интенсивность и требуемый
оттенок окраски.
~108°C
H2N
NH
NH2 ~110°C
-NH3
30 ч
NaO
S
ONa -2 NaOH
35 ч
SNa
SNa
Лейкотиазин
Лейкосоединение красителя
66.
SNaSNa
H2N
NH
NH
S
ONa
-2 NaOH
NaO
35 ч
S
NH
NH
NH2
~110°C
SNa
SNa
Na2S
Сернистый черный
в пасте
Лейкосоединение красителя
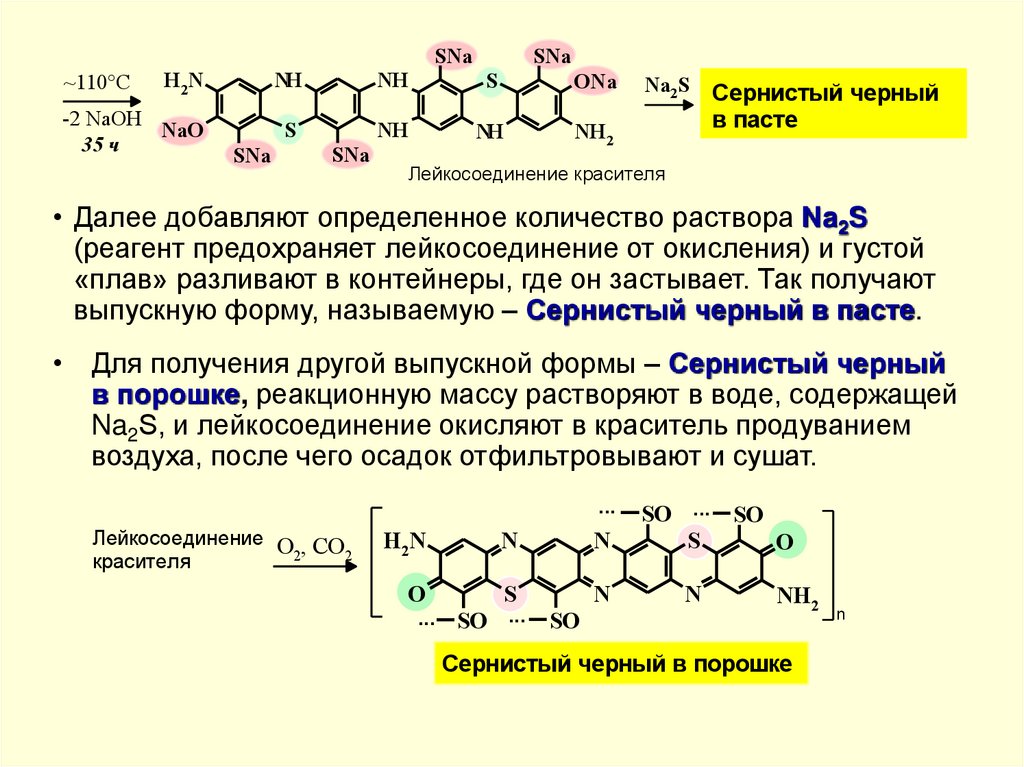
• Далее добавляют определенное количество раствора Na2S
(реагент предохраняет лейкосоединение от окисления) и густой
«плав» разливают в контейнеры, где он застывает. Так получают
выпускную форму, называемую – Сернистый черный в пасте.
• Для получения другой выпускной формы – Сернистый черный
в порошке, реакционную массу растворяют в воде, содержащей
Na2S, и лейкосоединение окисляют в краситель продуванием
воздуха, после чего осадок отфильтровывают и сушат.
...
Лейкосоединение O , CO
2
2
красителя
H2N
N
N
O
S
N
...
SO ...
SO
SO ... SO
S
O
N
NH2
Сернистый черный в порошке
n
67.
• Окраски на хлопке и вискозе устойчивы ко всем видамобработок кроме мокрого трения. Недостатком Сернистого
черного является ослабление им окрашенного волокна при
хранении. Это происходит в результате действия на волокно
серной и сернистой кислот, который образуют при окислении
серы и частично красителя сорбированных волокном.
68.
Более устойчивые к мокрым обработкам коричневые красителиполучают из соединений, образующих диазиновые красители в
процессе осернения. Однако осернение таких соединений
требует более жестких условий, чем осернение заранее
приготовленных диазиновых красителей.
• Процесс осуществляют способом так называемого сухого
сернистого плава или «запекания». Способ заключается
нагреванием смеси исходных продуктов с полисульфидом Na2Sn
или элементарной серой S8 при температуре более 200 С в
отсутствие растворителя.
69.
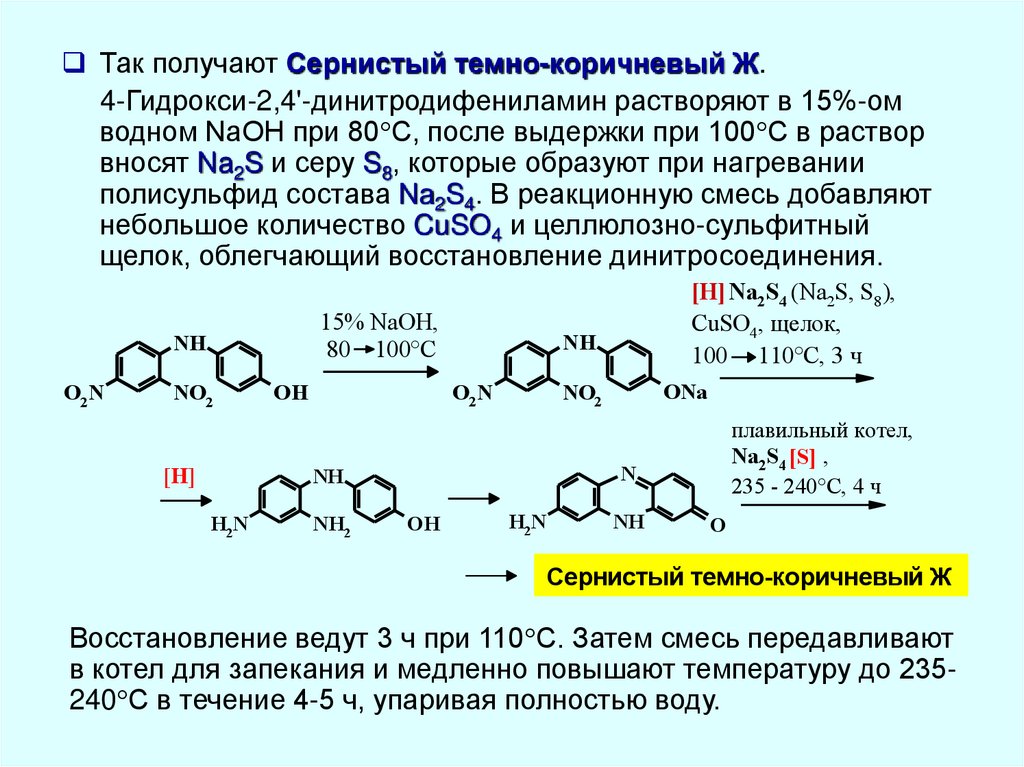
Так получают Сернистый темно-коричневый Ж.4-Гидрокси-2,4'-динитродифениламин растворяют в 15%-ом
водном NaOH при 80 С, после выдержки при 100 С в раствор
вносят Na2S и серу S8, которые образуют при нагревании
полисульфид состава Na2S4. В реакционную смесь добавляют
небольшое количество CuSO4 и целлюлозно-сульфитный
щелок, облегчающий восстановление динитросоединения.
15% NaOH,
80 100°C
NH
O2 N
NO2
[H]
NH
O2 N
OH
NH2
ONa
NO2
плавильный котел,
Na2S4 [S] ,
235 - 240°С, 4 ч
N
NH
H2 N
[H] Na2S4 (Na2S, S8),
CuSO4, щелок,
100 110°C, 3 ч
OH
H2 N
NH
O
Сернистый темно-коричневый Ж
Восстановление ведут 3 ч при 110 С. Затем смесь передавливают
в котел для запекания и медленно повышают температуру до 235240 С в течение 4-5 ч, упаривая полностью воду.
70.
• По мере загустевания массы перемешивание замедляют и вконце прекращают, поднимая мешалку. После охлаждения плав
«распахивают» мешалкой, после чего куски красителя
измельчают в мельнице.
• Сернистый темно-коричневый Ж на хлопке дает окраски
устойчивые к мокрым обработкам, но их светостойкость
невелика.
Из 4-гидрокси-2,4'-динитродифениламина осернением в иных
условиях получают красители Сернистый темно-синий ( Na2S4,5,
15 ч, 108-110°C ) и Сернистый синий (Na2S4, 3 ч, 112-116°C ).
71. 7.4.5. Тиозоли.
Для того, чтобы упростить процесс крашения хлопка и льнасернистыми красителями, а также использовать их для
окрашивания вискозного волокна в массе были разработаны
способы получения водорастворимых производных сернистых
красителей - тиозолей.Наиболее широкое применение получили
два типа производных, которые называют тиозоли и тиозоли Бс.
• Тиозоль бордо, Тиозоль синий К и другие получают S-алкилированием меркаптогрупп в лейкосоединениях сернистых красителей монохлоруксусной кислотой.
Kp-(SH)n
ClCH2COONa, NaOH
- NaCl, -H2O
Kp-(SCH2COONa)n
Для этого реакционную массу, полученную методом сернистой
«варки», нейтрализуют серной кислотой до рН 6-6,5 и удаляют
«сверхдисульфидную» серу взаимодействием с NaHSO3 (превращение в тиосульфат натрия). Затем лейкосоединение обрабатывают при 60-70 С водным раствором монохлорацетата натрия,
связывая выделяющийся HCl прибавлением едкого натра.
72.
• Тиозоль голубой Бс, Тиозоль коричневый Бс, Тиозольчерный Бс являются соединениями типа бисульфитных
производных хинонов.
Kp
CS
NaHSO3 / Na2SO3
~100°C, pH ~ 7
Kp
C
SH
SO3Na
• Их получают нагреванием сернистого красителя или его
лейкосоединения с Na2SO3 или NaHSO3 или со смесью
сульфита и гидросульфита при 95-100 С и рН 6,5-7,0.
После перехода сернистого красителя в раствор его
концентрируют упариванием воды в вакууме или высаливают.
Цвет окрасок тиозолями нередко отличается от цвета,
получаемого при обычном крашении сернистым красителем.
Это свидетельствует об изменениях в химическом строении
красителя в процессе взаимодействия с сульфитом натрия.
Так, например, из Сернистого темно-синего после обработки
NaHSO3 получают Тиозоль синий Бс.
73. 7.4.6. Кубовые диазиновые красители
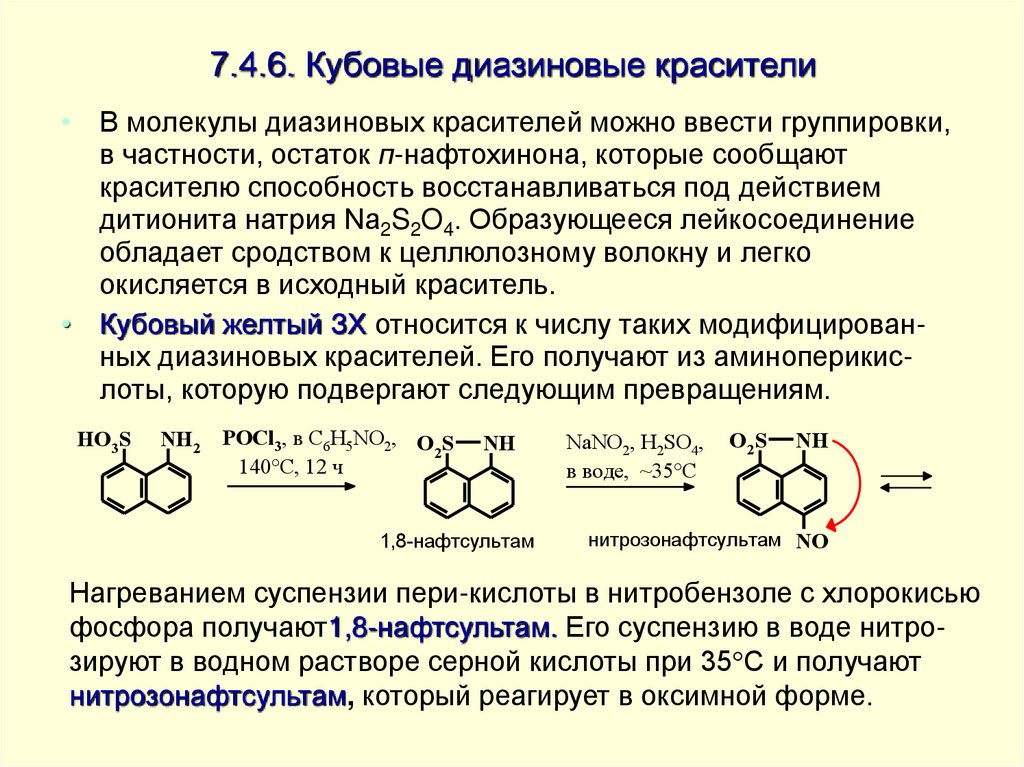
• В молекулы диазиновых красителей можно ввести группировки,в частности, остаток п-нафтохинона, которые сообщают
красителю способность восстанавливаться под действием
дитионита натрия Na2S2O4. Образующееся лейкосоединение
обладает сродством к целлюлозному волокну и легко
окисляется в исходный краситель.
• Кубовый желтый ЗХ относится к числу таких модифицированных диазиновых красителей. Его получают из аминоперикислоты, которую подвергают следующим превращениям.
HO3S
NH2
POCl3, в C6H5NO2, O S
2
140°C, 12 ч
NH
1,8-нафтсультам
NaNO2, H2SO4,
в воде, ~35°C
O 2S
NH
нитрозонафтсультам NO
Нагреванием суспензии пери-кислоты в нитробензоле с хлорокисью
фосфора получают1,8-нафтсультам. Его суспензию в воде нитрозируют в водном растворе серной кислоты при 35 С и получают
нитрозонафтсультам, который реагирует в оксимной форме.
74.
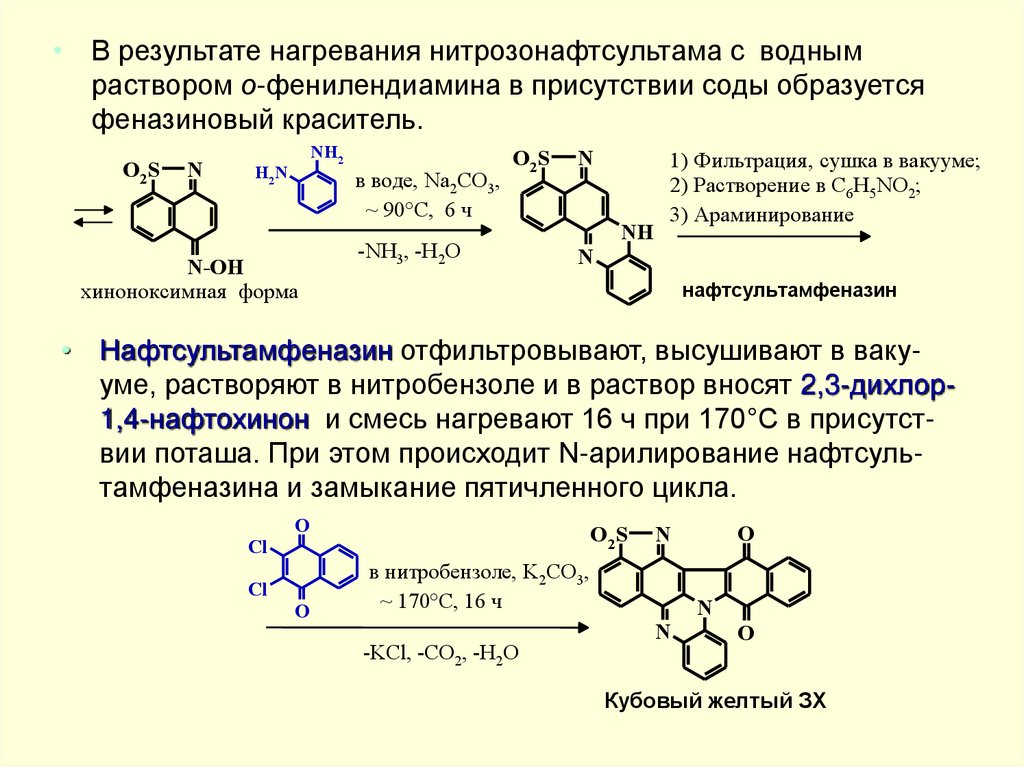
• В результате нагревания нитрозонафтсультама с воднымраствором о-фенилендиамина в присутствии соды образуется
феназиновый краситель.
O 2S
N
NH2
H2N
в воде, Na2CO3,
~ 90°C, 6 ч
N-OH
хиноноксимная форма
O 2S
-NH3, -H2O
N
NH
1) Фильтрация , сушка в вакууме;
2) Растворение в C6H5NO2;
3) Араминирование
N
нафтсультамфеназин
• Нафтсультамфеназин отфильтровывают, высушивают в вакууме, растворяют в нитробензоле и в раствор вносят 2,3-дихлор1,4-нафтохинон и смесь нагревают 16 ч при 170°С в присутствии поташа. При этом происходит N-арилирование нафтсультамфеназина и замыкание пятичленного цикла.
Cl
Cl
O
O
O 2S
в нитробензоле, K2CO3,
~ 170°C, 16 ч
-KCl, -CO2, -H2O
O
N
N
N
O
Кубовый желтый ЗХ
75.
• Затем реакционную массу медленно охлаждают до 35°С,нитробензол отгоняют с водяным паром и суспензию красителя
очищают от смолообразных примесей хлорированием в вводнощелочной среде при 85 С (окисление гипохлоритом натрия).
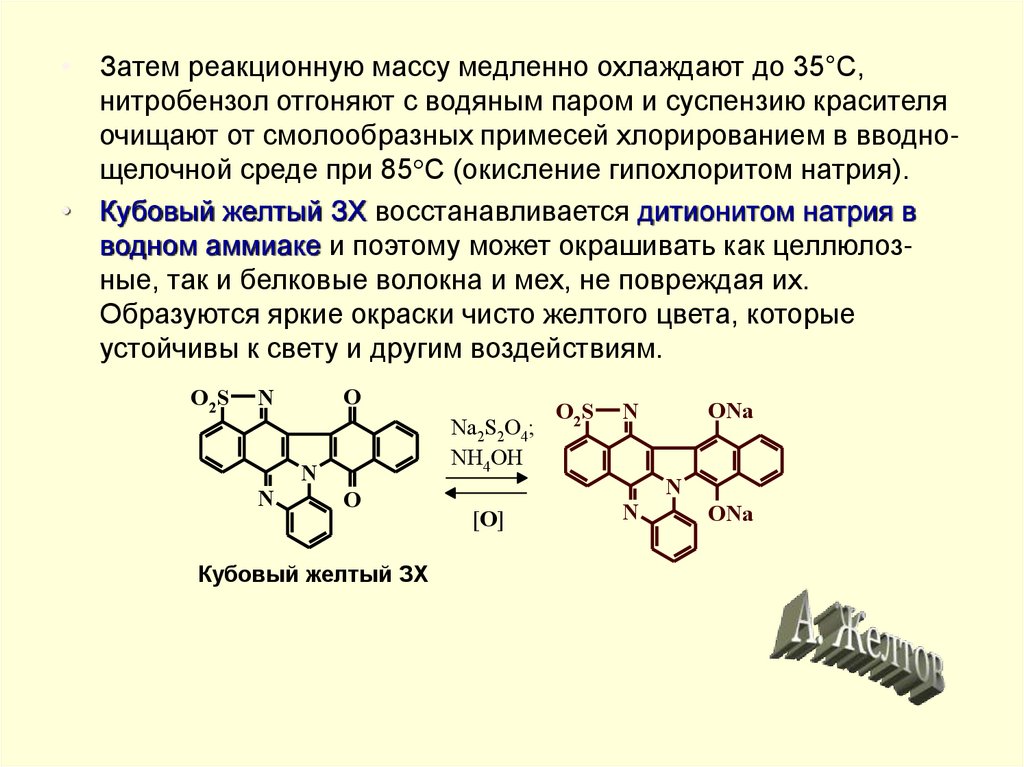
• Кубовый желтый ЗХ восстанавливается дитионитом натрия в
водном аммиаке и поэтому может окрашивать как целлюлозные, так и белковые волокна и мех, не повреждая их.
Образуются яркие окраски чисто желтого цвета, которые
устойчивы к свету и другим воздействиям.
O2S
O
N
N
Na2S2O4;
NH4OH
N
O
Кубовый желтый ЗХ
[O]
O2S
ONa
N
N
N
ONa






















 chemistry
chemistry








