Similar presentations:
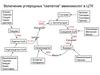
Аминокислоты. Аминоспирты
1.
Аминокислоты.Аминоспирты
H2N
H O
C C
СН3
H
N
H O H
C C N
(CH2)4
NH2
H O
C C
CH2
N
CH2 CH COOH
NH2
NH
OH
2.
ПЛАН ЛЕКЦИИ:1. Классификация аминокислот
2. Стереоизомерия аминокислот
3.Химические свойства аминокислот
4. Метаболические реакции
5.Использование аминокислот в промышленности и
медицине
6.Аминоспирты
2
3.
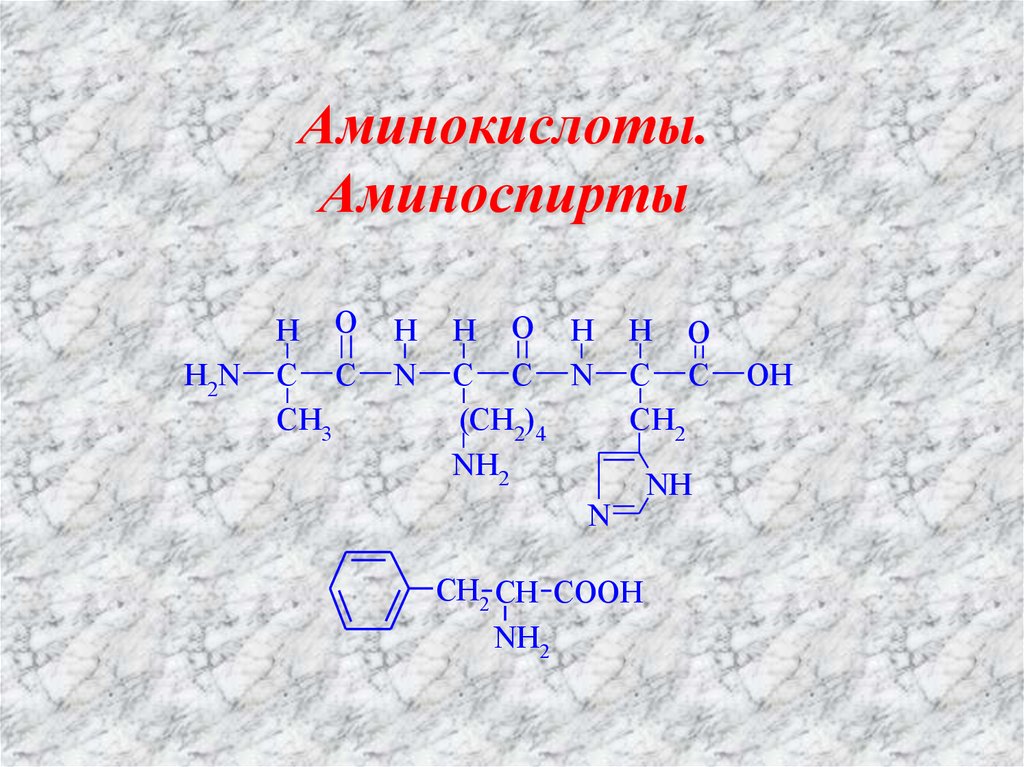
Аминокислоты – гетерофункциональные соединения,содержащие карбоксильную и аминогруппы.
R СН CООН
NH2
R СН CH2 CООН
NH2
аминокислоты
аминокислоты
R СН CH2 CH2 CООН
NH2
аминокислоты
3
4.
Классификация α-аминокислот:1.По природе радикала:
● ациклические
● ароматические
● гетероциклические
2. По полярности радикала:
● полярные
● неполярные
3. По кислотно-оснóвным свойствам:
● нейтральные
(моноаминомонокарбоновые, диаминодикарбоновые)
● оснóвные (диаминомонокарбоновые)
● кислые (моноаминодикарбоновые)
4. По возможности биосинтеза в организме человека:
● заменимые
● условно-заменимые (гистидин, аргинин, тирозин)
● незаменимые (изолейцин, метионин, фенилаланин,
триптофан, треонин, лизин, валин, лейцин)
5. По другим функциям:
● аминогидроксикислоты
● серусодержащие аминокислоты
4
5.
Классификация и структура аминокислотI. Алифатические -аминокислоты
1. Нейтральные (содержат одну СООН- и одну NH 2- группы):
H2N CH2 COOH - глицин (гли.)
гликокол
* COOH - аланин (ала.)
CH3 CH
NH2
H3C
H3C
CH
* COOH
CH
NH2
валин (вал.)
H3C
*
CH CH2 CH COOH - лейцин (лей.)
H3C
NH2
H3C CH2
CH
H3C
* COOH
CH
NH2
- изолейцин
(иле.)
2. Кислые (содержат две СООН- и одну NH 2-группы):
* COOH - аспарагиновая HOOC CH2 CH2 CH
* COOH - глутаминоHOOC CH2 CH
вая кислота
кислота (асп.)
NH2
NH2
(глу.)
3. Основные (содержат одну СООН- и две NH2-группы):
CH2 CH2 CH2 *CH COOH - орнитин
(орн.)
NH2
NH2
CH2 (CH2)3 *CH COOH - лизин (лиз.)
NH2
NH2
H2N C NH (CH2)3 *CH COOH - аргинин
(арг.)
NH2
NH
5
6.
К группе алифатических α-аминокислот относятся гидроксиаминокислоты(содержат дополнительно группу ОН-):
*
COOH
CH2 CH
OH NH2 - серин (сер.)
*
H3C CH
OH
*
COOH
CH
NH2 - треонин (тре.)
Серусодержащие аминокислоты
(содержат тиольную группу SH-, дисульфидную S-S):
* COOH - цистеин (цис.)
CH2 CH
SH NH2
* COOH
CH2 CH2 CH
NH2 - метионин (мет.)
SCH3
CH2 S S CH2
H2N CH
COOH
CH NH2
COOH
Цистин (цис.-S-S-цис.)
6
7.
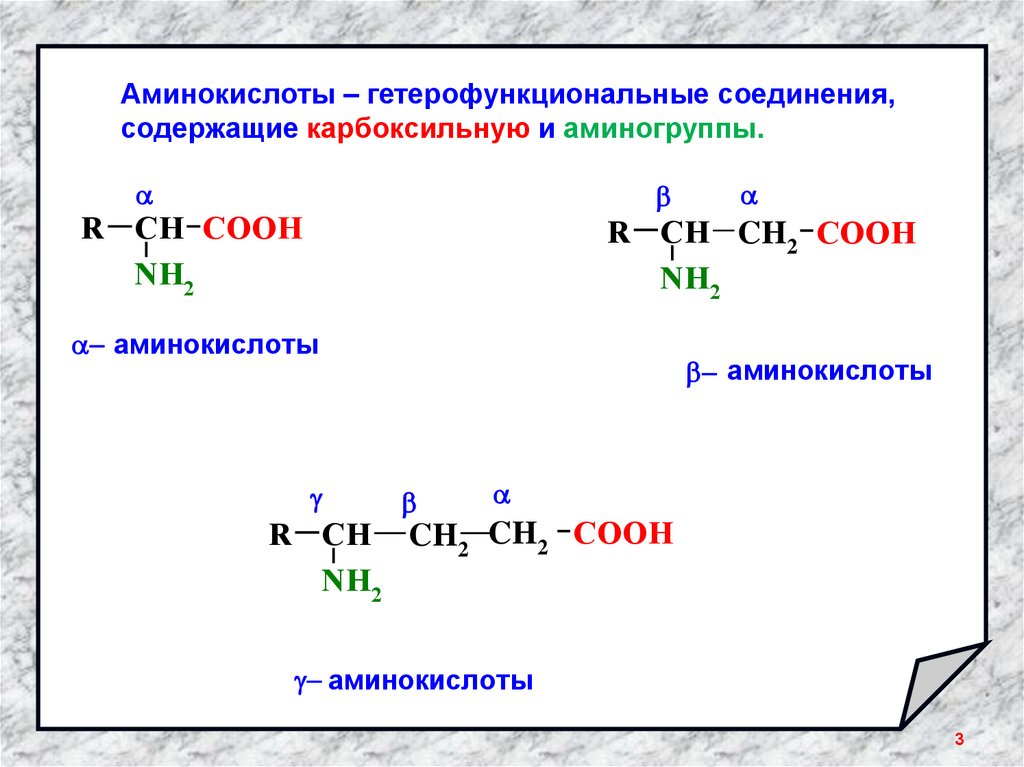
II Ароматические:* COOH - фенилаланин
CH2 CH
(фен.)
NH2
* COOH
CH2 CH
NH2 - тирозин (тир.)
HO
III Гетероциклические:
N
* COOH - гистидин
CH2 CH
N
H
NH2
IV Иминокислоты:
N
H
COOH
-пролин (про.)
(гис.)
* COOH
CH2 CH
NH2
N
H
-триптофан (три.)
HO
N
H
COOH
-гидроксипролин
(про. -ОН)
7
8.
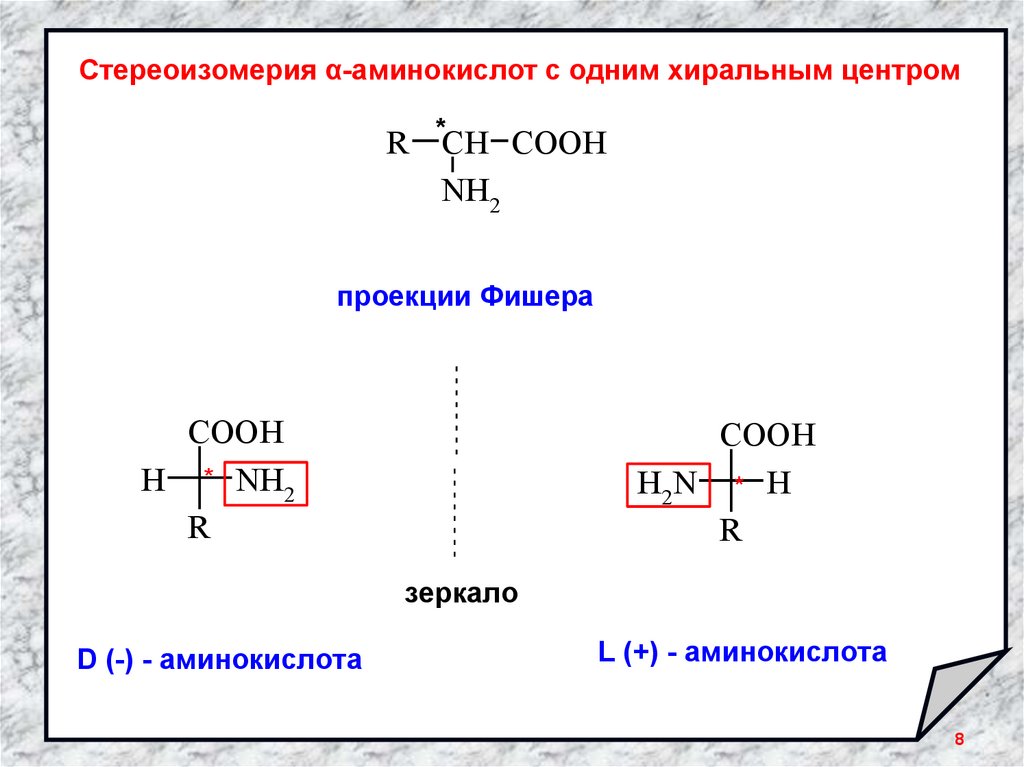
Стереоизомерия α-аминокислот с одним хиральным центромR *СН CООН
NH2
проекции Фишера
COOH
H * NH2
R
COOH
H2N * H
R
зеркало
D (-) - аминокислота
L (+) - аминокислота
8
9.
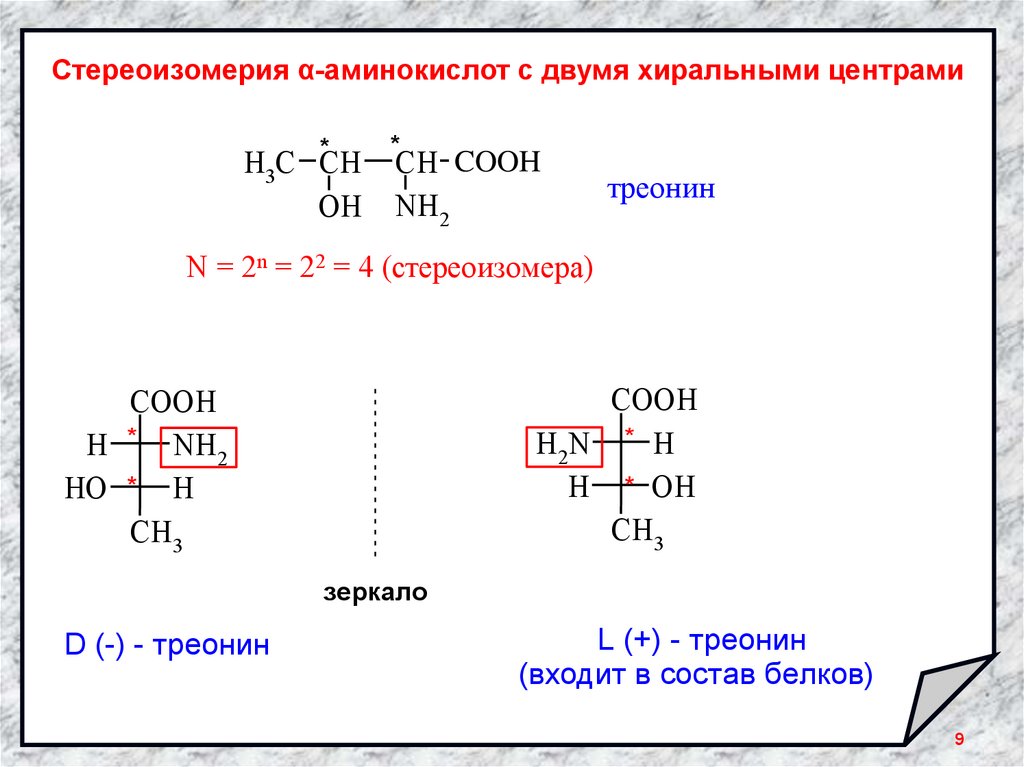
Стереоизомерия α-аминокислот с двумя хиральными центрами*
H3C CH
OH
*
CH COOH
NH2
треонин
N = 2n = 22 = 4 (стереоизомера)
COOH
H2N * H
H * OH
CH3
COOH
H * NH2
HO * H
CH3
зеркало
D (-) - треонин
L (+) - треонин
(входит в состав белков)
9
10.
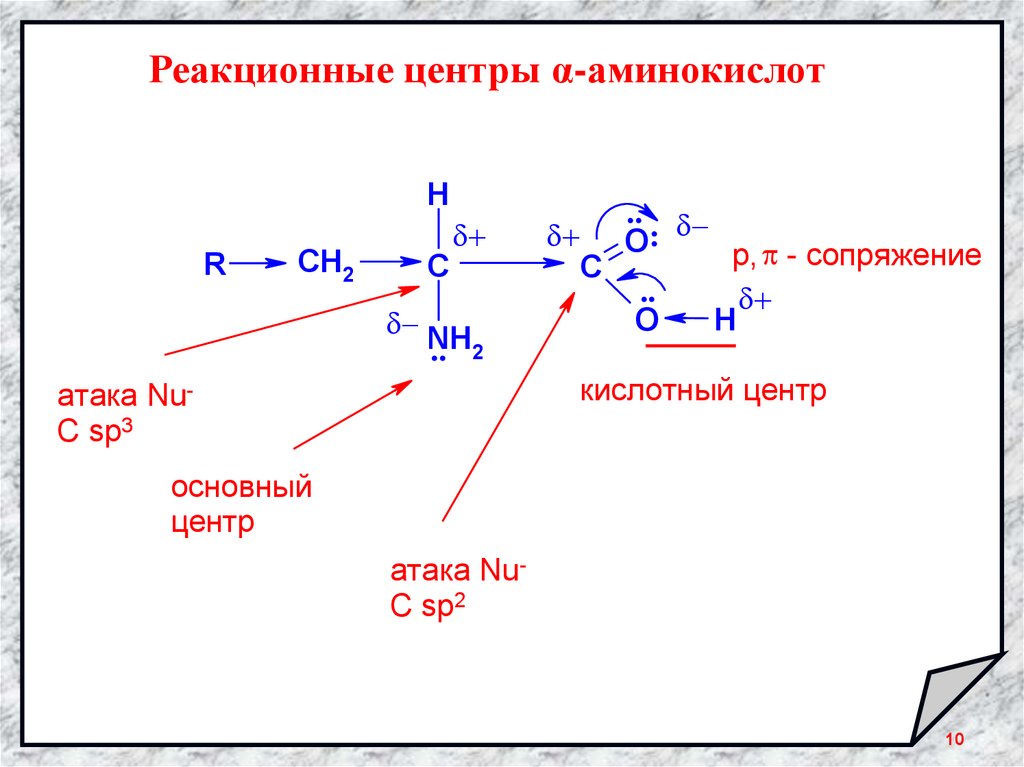
Реакционные центры α-аминокислотH
R
CH2
C
NH
.. 2
..
O:
p, - сопряжение
C
..
H
O
кислотный центр
атака NuC sp3
основный
центр
атака NuC sp2
10
11.
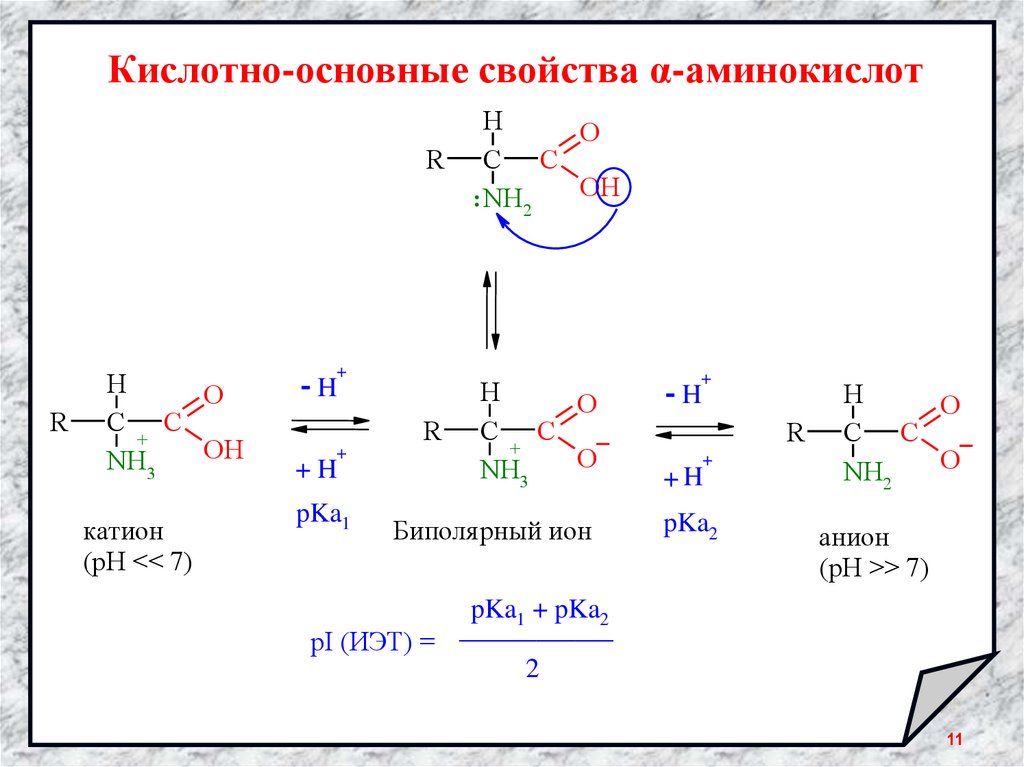
Кислотно-основные свойства α-аминокислотR
Н
O
С C
+
OH
NH3
катион
(pH << 7)
R
Н
O
С C
OH
: NH2
R
+H
Н
O
С C
+
O
NH3
+H
pKa1
Биполя рный ион
pKa2
+
-H
+
pI (ИЭТ) =
+
-H
R
+
Н
O
С C
O
NH2
анион
(рН >> 7)
pKa1 + pKa2
2
11
12.
Изоэлектрическая точка α-аминокислоты –это то значение pH раствора, при котором
большинство молекул существуют в виде
биполярных
ионов,
а
концентрации
катионной и анионной форм минимальны и
равны.
12
13.
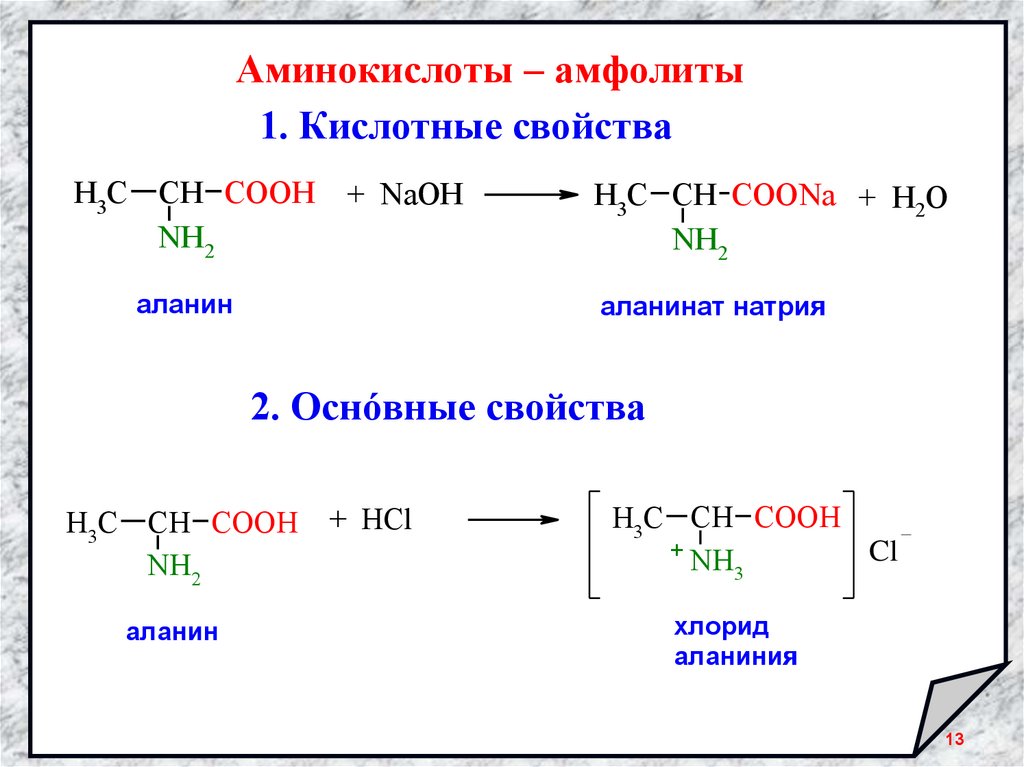
Аминокислоты – амфолиты1. Кислотные свойства
H3C СН CООН
NH2
+ NaOH
аланин
H3C СН CООNa + Н2О
NH2
аланинат натрия
я
2. Оснóвные свойства
H3C СН CООН
NH2
аланин
+ HCl
H3C СН CООН
+ NH
Cl
3
хлорид
аланиния
я
13
14.
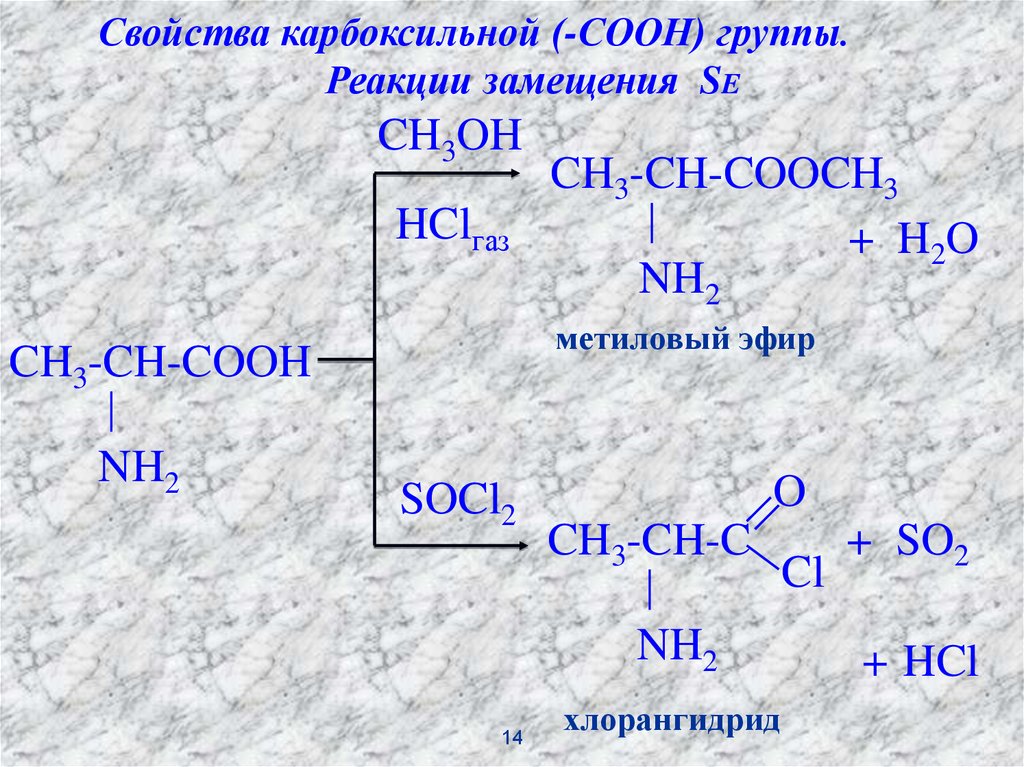
Свойства карбоксильной (-СООН) группы.Реакции замещения SE
CH3OH
HClгаз
метиловый эфир
CH3-CH-COOH
NH2
CH3-CH-COOCH3
+ H 2O
NH2
SOCl2
O
CH3-CH-C
NH2
14
хлорангидрид
Cl
+ SO2
+ HCl
15.
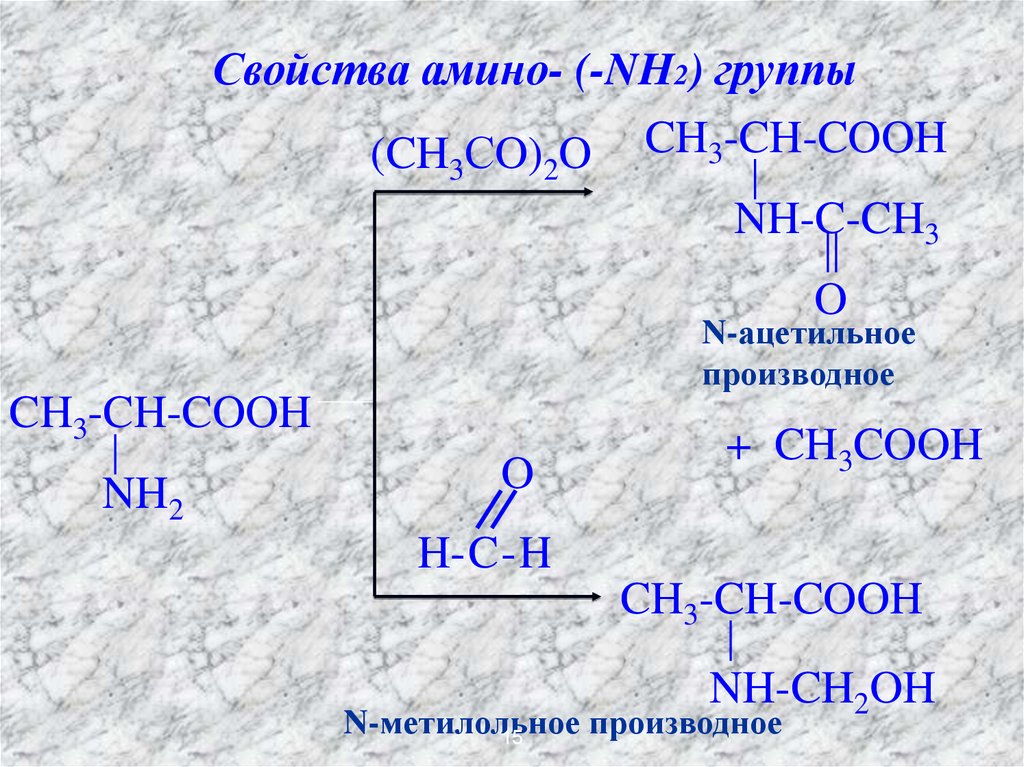
Свойства амино- (-NH2) группы(CH СO) O CH3-CH-COOH
3
2
NH-C-CH3
O
N-ацетильное
производное
CH3-CH-COOH
NH2
O
+ CH3COOH
H-C-H
CH3-CH-COOH
NH-CH2OH
N-метилольное
производное
15
16.
Дезаминирование in vitroR-CH-COOH
HNO2
R-CH-COOH + N2
OH
NH2
α-аминокислота
α-гидроксикислота
16
+ H2O
17.
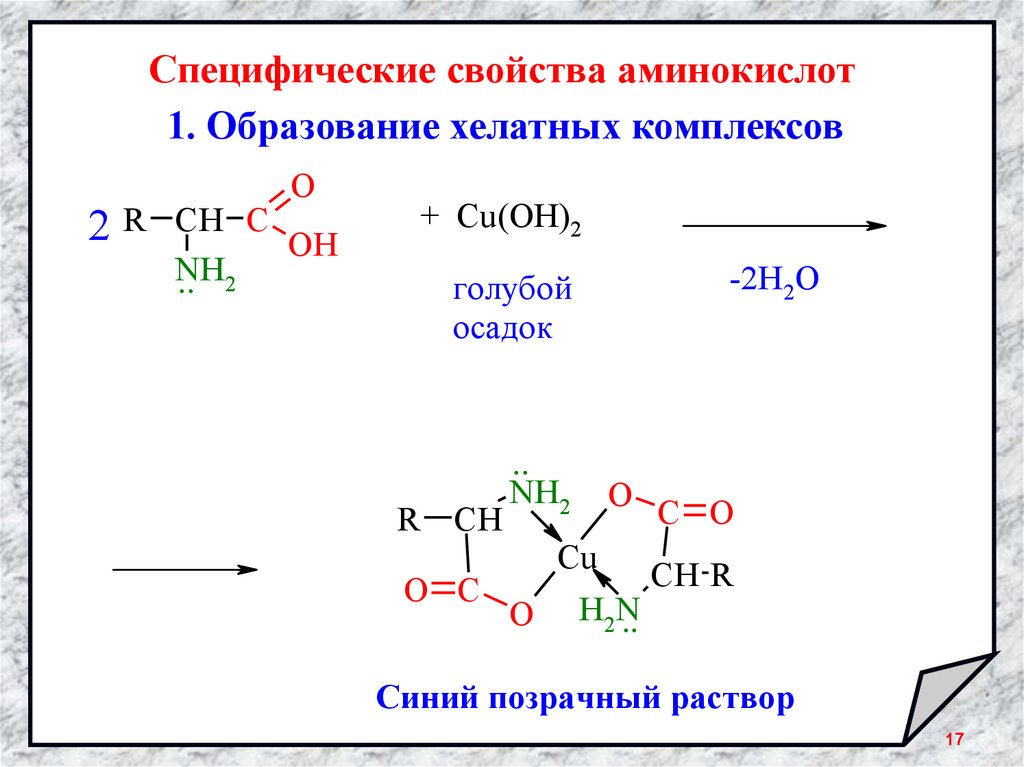
Специфические свойства аминокислот1. Образование хелатных комплексов
O
2 R СН C OH
NH
.. 2
+ Cu(OH)2
-2Н2О
голубой
осадок
R СН
O C
..
NH2
O
Cu
O
H2N
..
C O
CН R
Синий позрачный раствор
17
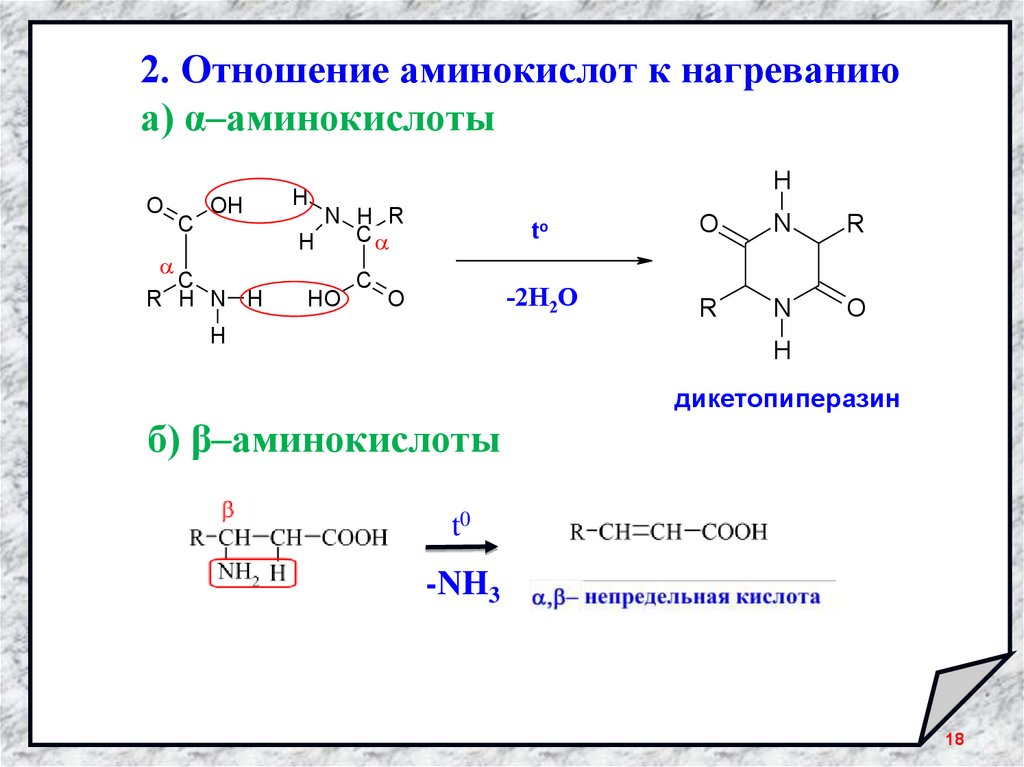
18.
2. Отношение аминокислот к нагреваниюа) α–аминокислоты
O
C
OH
C
R H N H
H
H
N H R
C
H
HO
C
O
H
to
O
N
R
-2Н2О
R
N
O
H
дикетопиперазин
б) β–аминокислоты
t0
-NH3
18
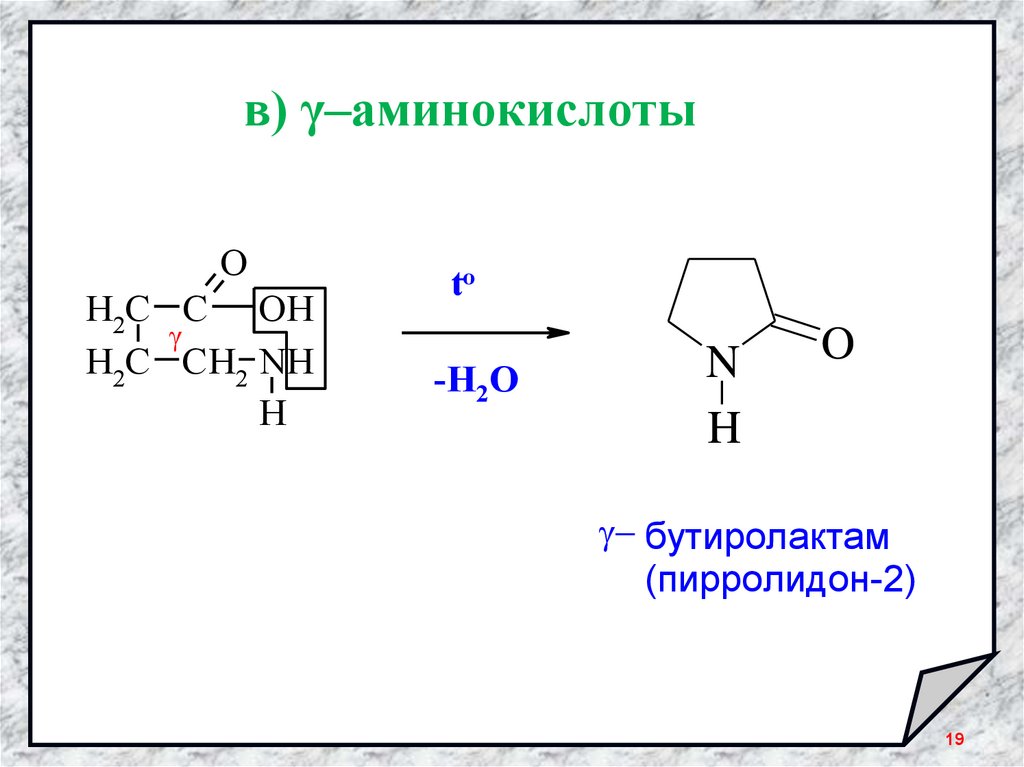
19.
в) γ–аминокислотыO
H2C C OH
H2C CH2 NH
H
to
-H2O
N
H
O
бутиролактам
(пирролидон-2)
19
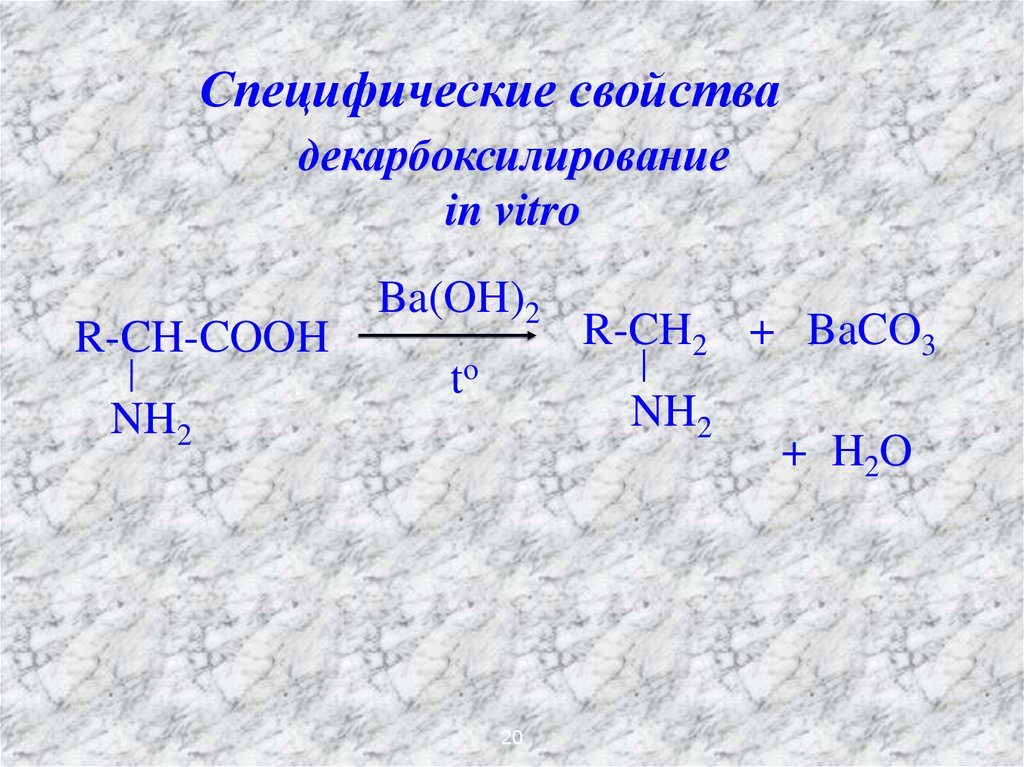
20.
Специфические свойствадекарбоксилирование
in vitro
R-CH-COOH
NH2
Ba(OH)2
to
R-CH2 + BaCO3
NH2
20
+ H2O
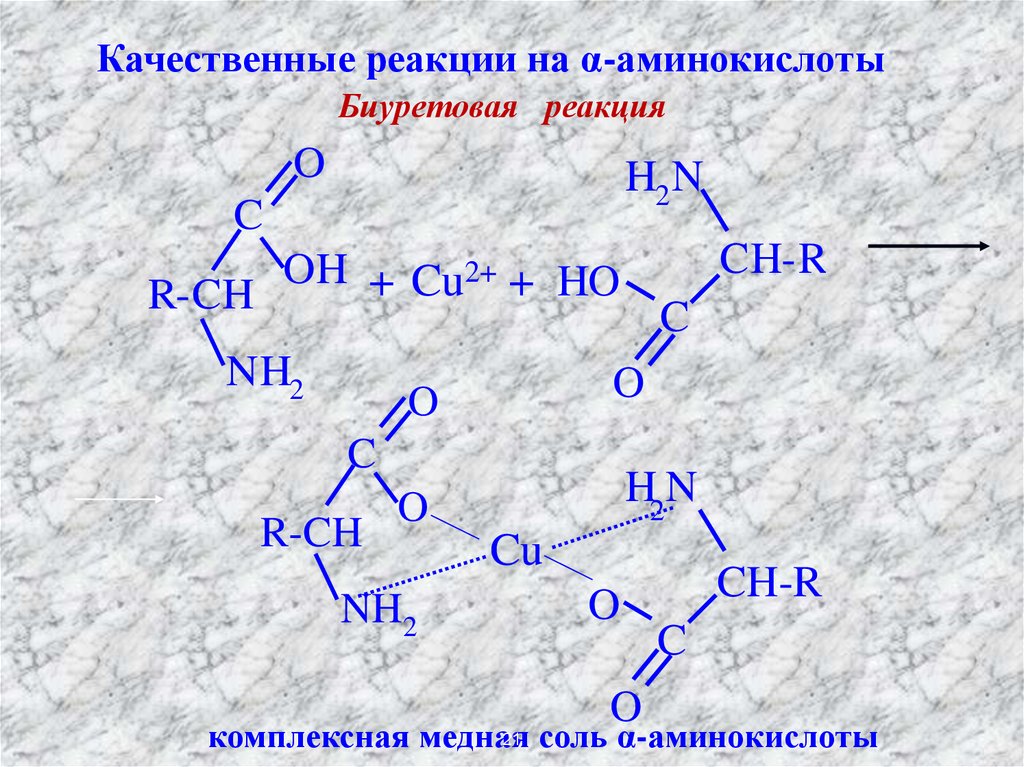
21.
Качественные реакции на α-аминокислотыБиуретовая реакция
O
H2 N
C
R-CH
CH-R
OH + Cu2+ + HO
NH2
O
O
O
H2N
C
R-CH
C
NH2
Cu
O
O
CH-R
C
21 соль α-аминокислоты
комплексная медная
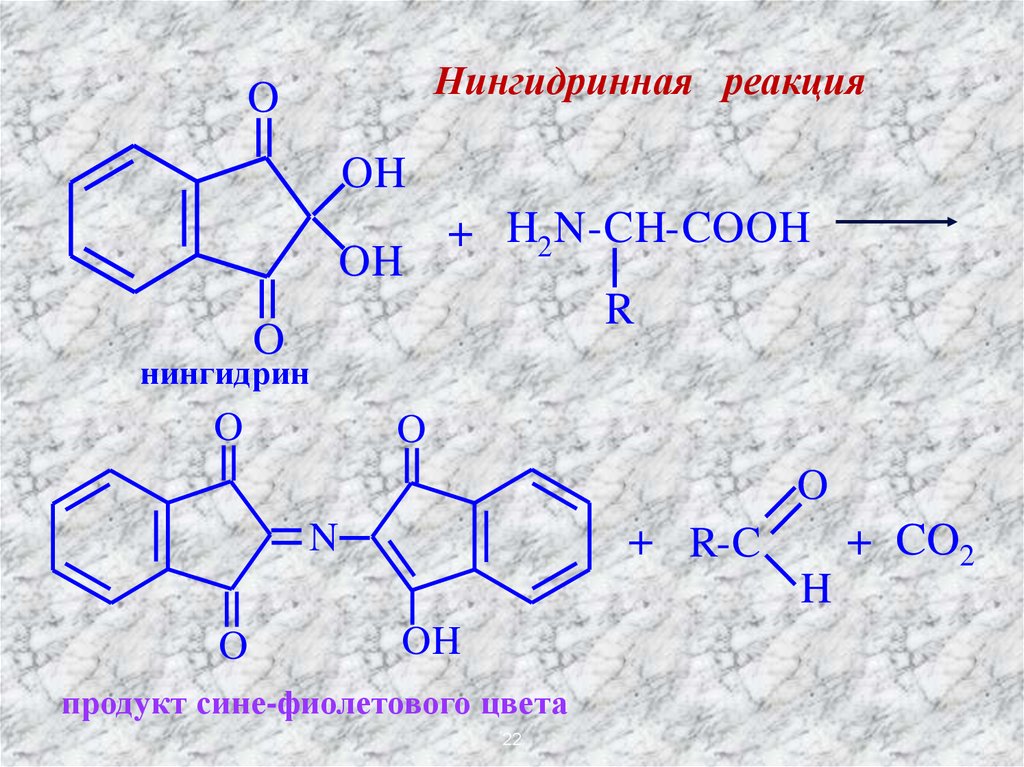
22.
Нингидринная реакцияO
OH
OH
+ H2 N-CH-COOH
R
O
нингидрин
O
O
O
N
+ R-C
+ CO2
H
O
OH
продукт сине-фиолетового цвета
22
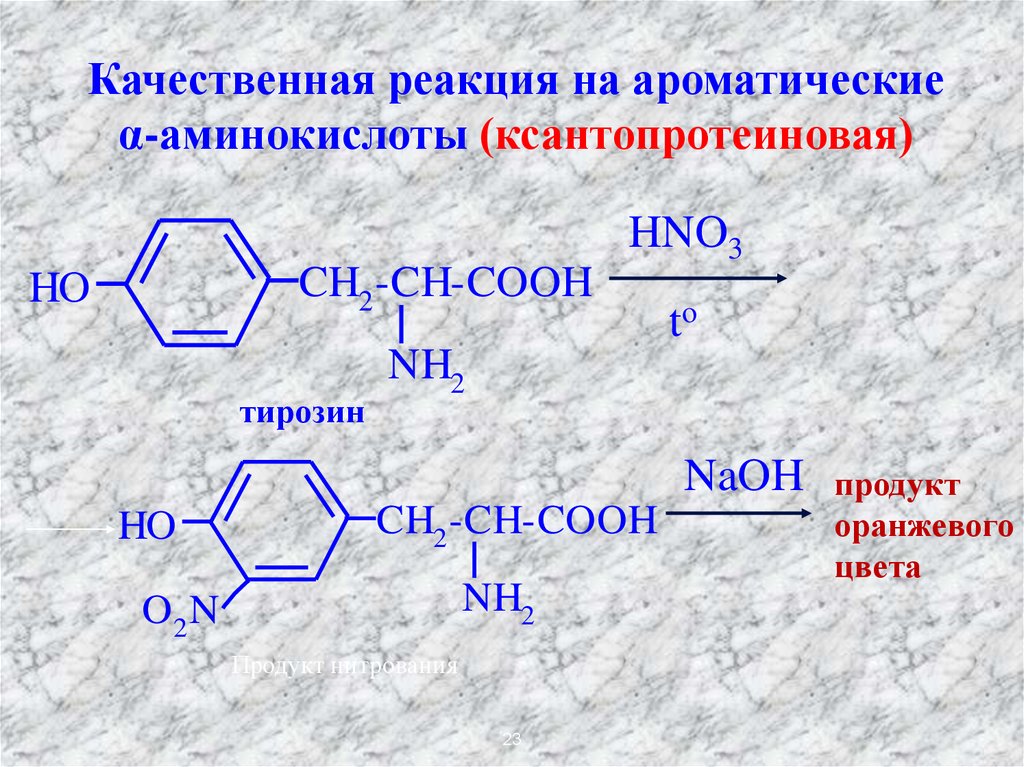
23.
Качественная реакция на ароматическиеα-аминокислоты (ксантопротеиновая)
HNO3
CH2 -CH-COOH
HO
тирозин
to
NH2
NaOH продукт
HO
CH2 -CH-COOH
NH2
O2 N
Продукт нитрования
23
оранжевого
цвета
24.
Качественная реакция на серосодержащиеα-аминокислоты
NaOH
CH2 -CH-COOH
SH NH2
to
продукты разложения
(Na2S)
(CH3COO)2Pb
цистеин
PbS
24
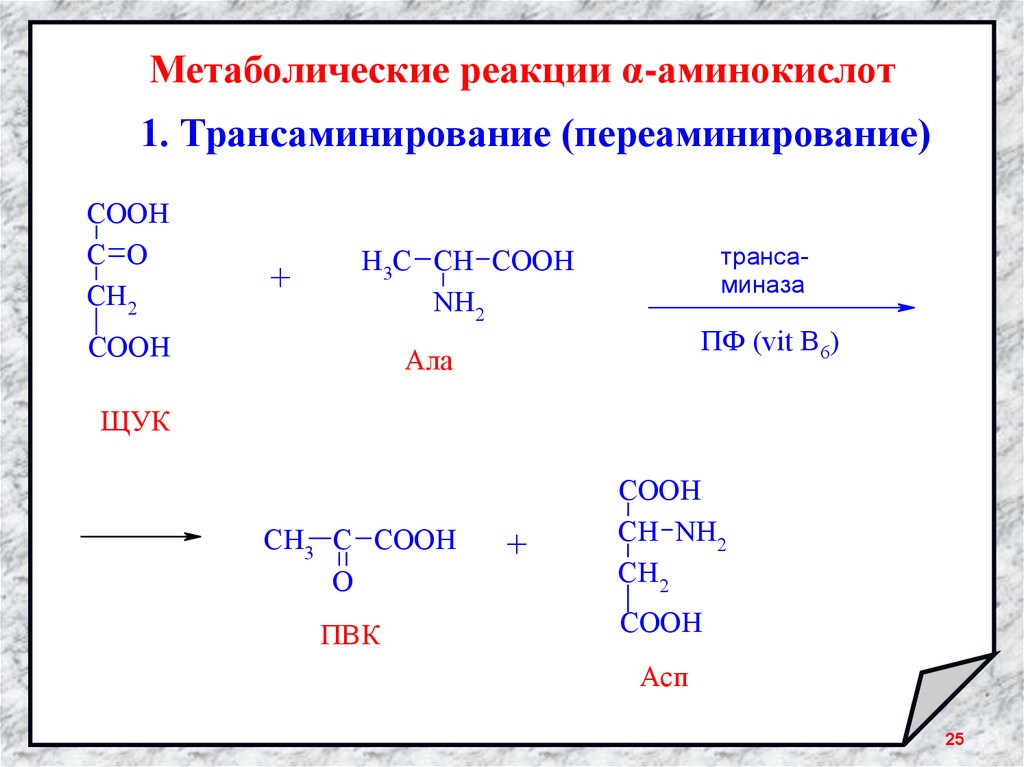
25.
Метаболические реакции α-аминокислот1. Трансаминирование (переаминирование)
COOH
C O
CH2
+
трансаминаза
H3C CH COOH
NH2
COOH
ПФ (vit B6)
Ала
ЩУК
СН3 С СООН
O
ПВК
+
COOH
CH NH2
CH2
COOH
Асп
25
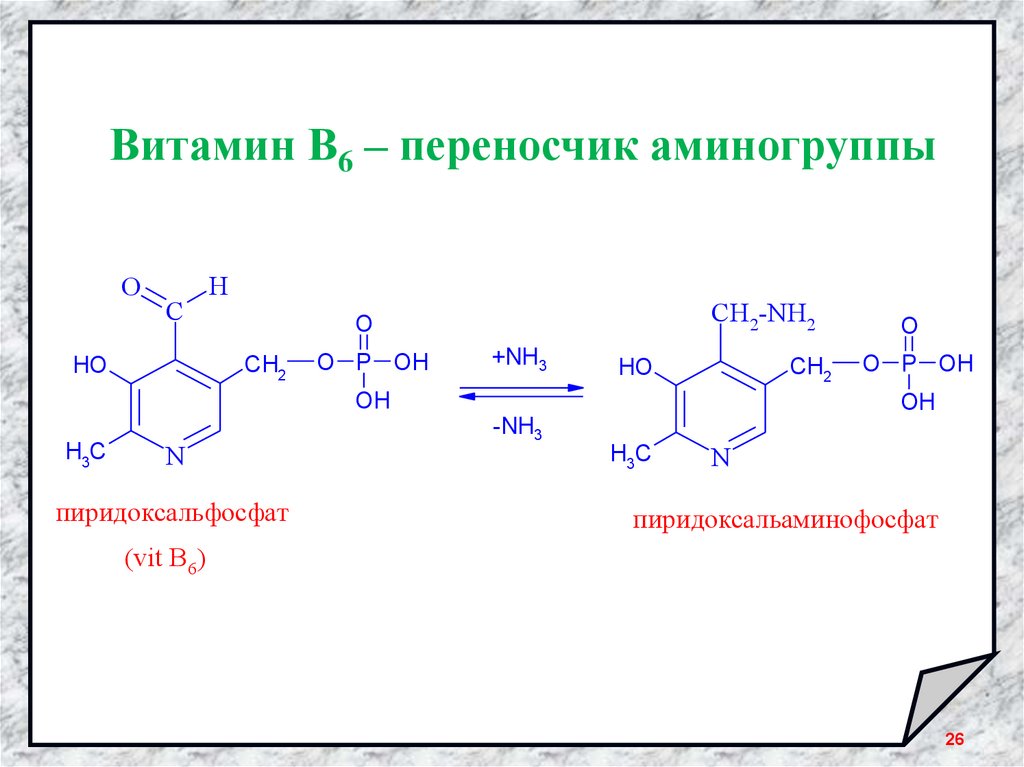
26.
Витамин В6 – переносчик аминогруппыO
C
H
CH2
HO
CH2-NH2
O
O P OH
+NH3
CH2
HO
OH
H3C
N
пиридоксальфосфат
O
O P OH
OH
-NH3
H3C
N
пиридоксальаминофосфат
(vit B6)
26
27.
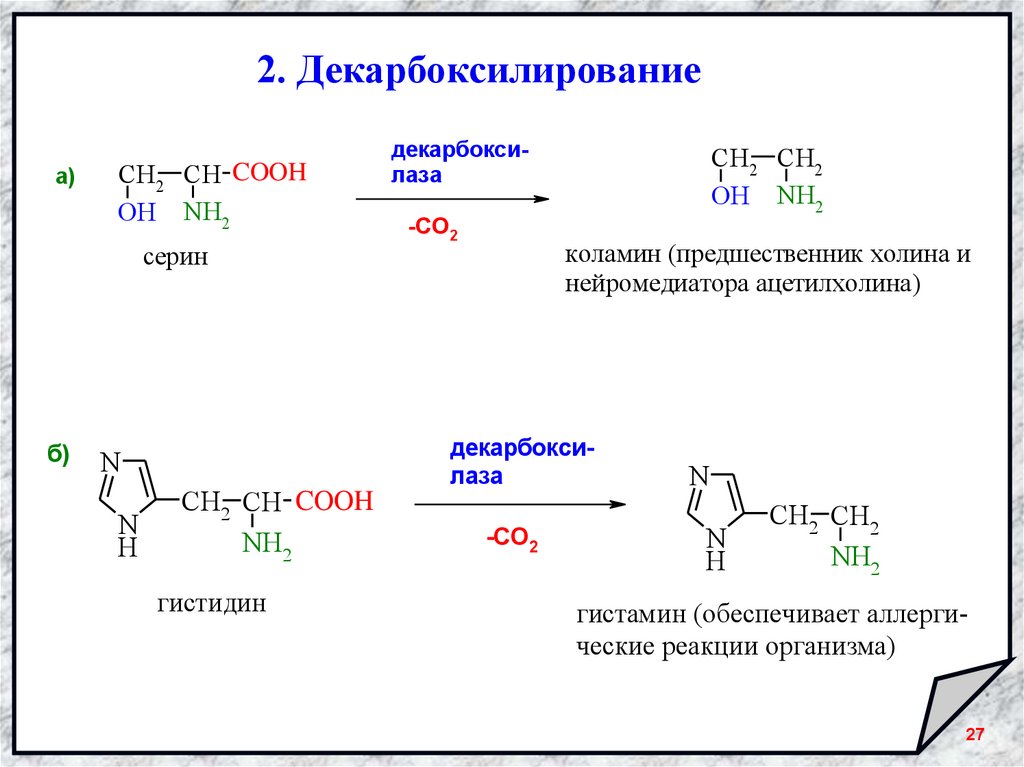
2. Декарбоксилированиеа)
CH2 CH COOH
OH NH2
серин
б)
N
N
H
CH2 CH COOH
NH2
гистидин
декарбоксилаза
-CO2
CH2 CH2
OH NH2
коламин (предшественник холина и
нейромедиатора ацетилхолина)
декарбоксилаза
-CO2
N
N
H
CH2 CH2
NH2
гистамин (обеспечивает аллергические реакции организма)
27
28.
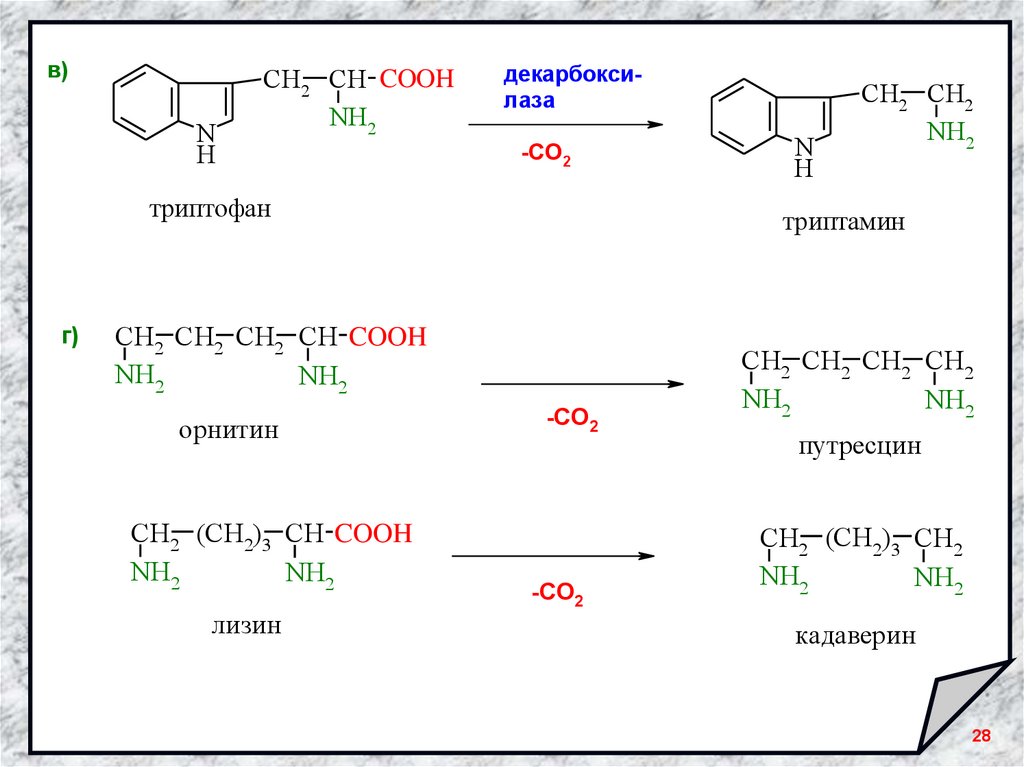
в)N
H
CH2 CH COOH
NH2
декарбоксилаза
-CO2
триптофан
г)
триптамин
CH2 CH2 CH2 CH COOH
NH2
NH2
орнитин
CH2 (CH2)3 CH COOH
NH2
NH2
лизин
N
H
CH2 CH2
NH2
-CO2
-CO2
CH2 CH2 CH2 CH2
NH2
NH2
путресцин
CH2 (CH2)3 CH2
NH2
NH2
кадаверин
28
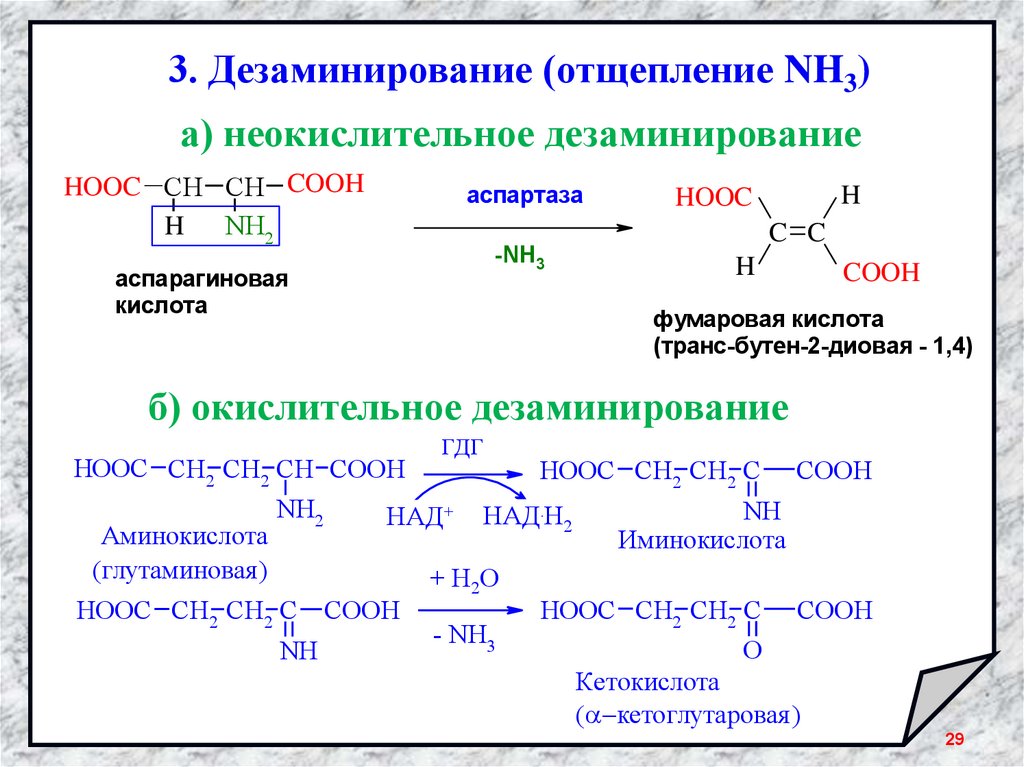
29.
3. Дезаминирование (отщепление NH3)а) неокислительное дезаминирование
HOOC CH CH COOH
H
NH2
аспартаза
-NH3
аспарагиновая
кислота
H
HOOC
C C
H
COOH
фумаровая кислота
(транс-бутен-2-диовая - 1,4)
б) окислительное дезаминирование
HOOC СН2 СН2 СН COOH
Аминокислота
(глутаминовая )
NH2
HOOC СН2 СН2 С
NH
ГДГ
НАД+
COOH
HOOC СН2 СН2 С
НАД.Н2
+ H2 O
- NH3
COOH
NH
Иминокислота
HOOC СН2 СН2 С
COOH
O
Кетокислота
( кетоглутаровая )
29
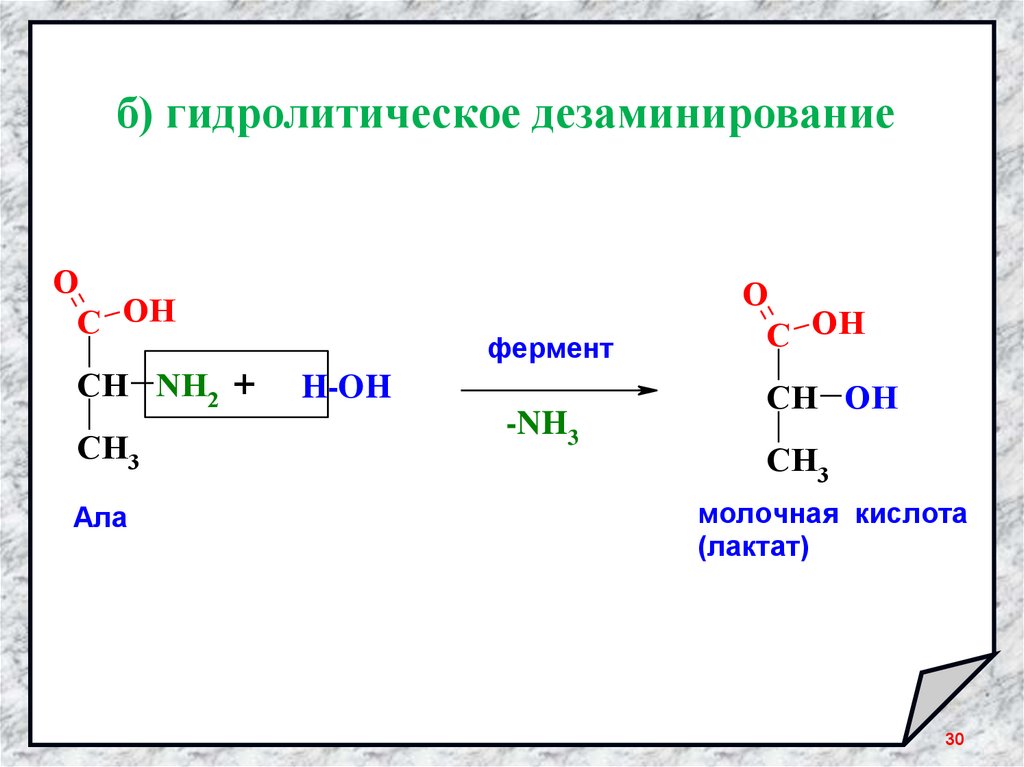
30.
б) гидролитическое дезаминированиеO
C OH
CH NH2 +
CH3
Ала
фермент
H-OH
-NH3
O
C OH
CH OH
CH3
молочная кислота
(лактат)
30
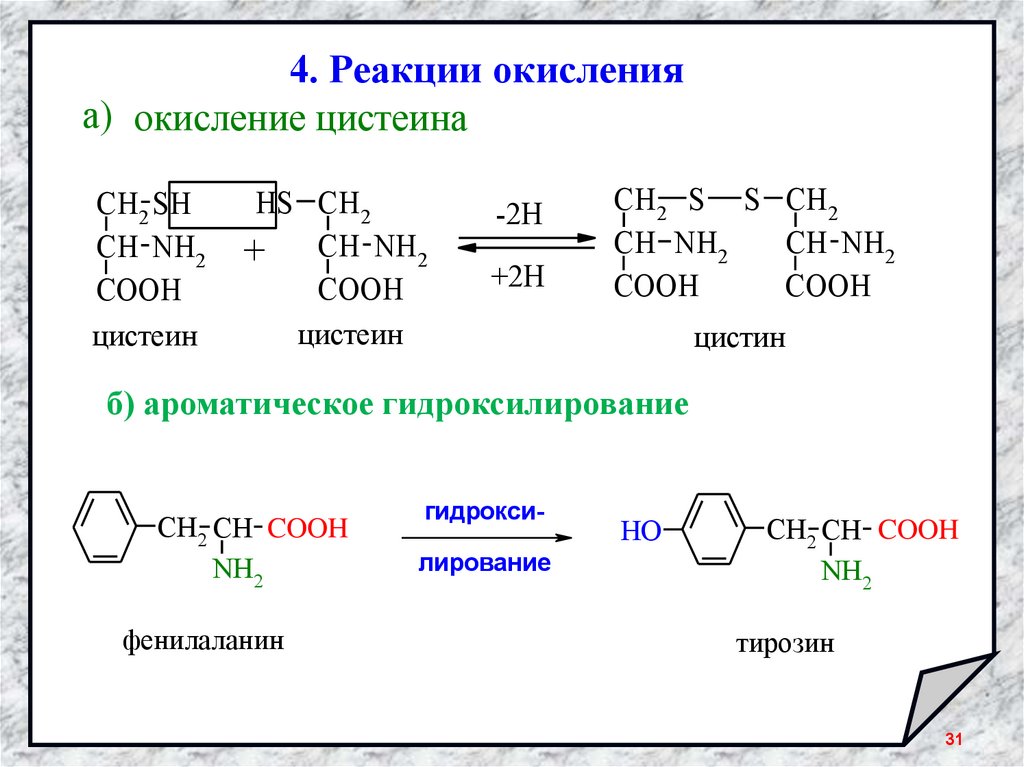
31.
4. Реакции окисленияа) окисление цистеина
CH2 SH
CH NH2
COOH
цистеин
HS CH2
+ CH NH2
COOH
цистеин
-2Н
+2Н
CH2 S S CH2
CH NH2
CH NH2
COOH
COOH
цистин
б) ароматическое гидроксилирование
CH2 CH COOH
NH2
фенилаланин
гидроксилирование
HO
CH2 CH COOH
NH2
тирозин
31
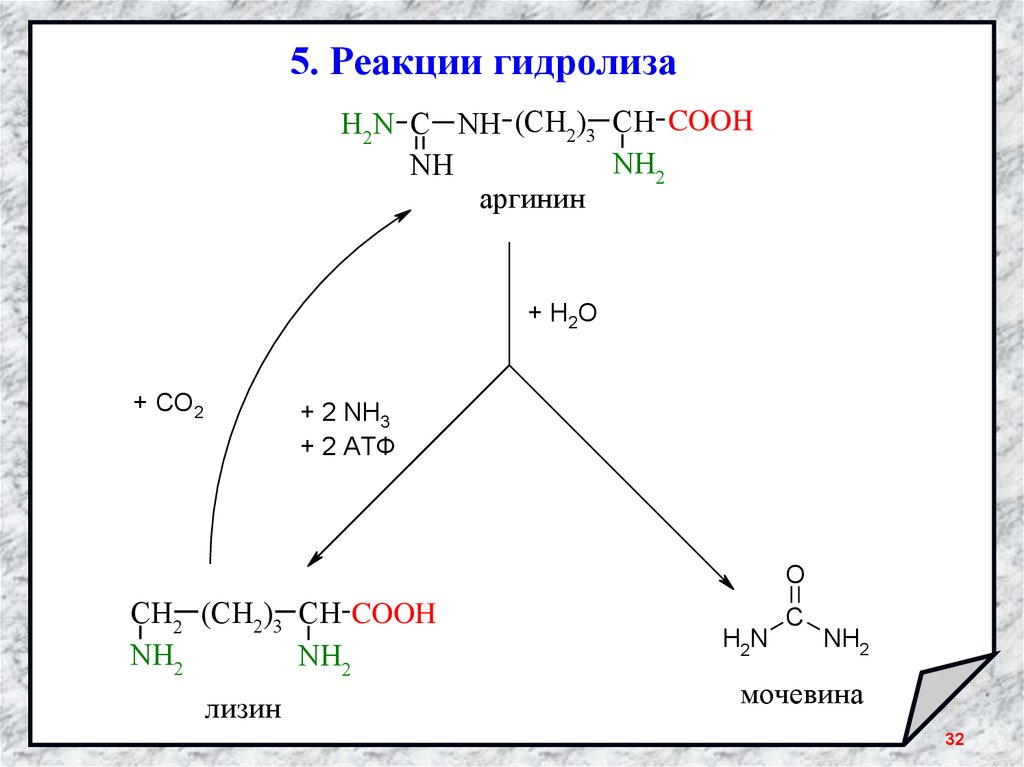
32.
5. Реакции гидролизаH2N C NH (CH2)3 CH COOH
NH2
NH
аргинин
+ H2O
+ CO2
+ 2 NH3
+ 2 АТФ
O
CH2 (CH2)3 CH COOH
NH2
NH2
лизин
H2N
C
NH2
мочевина
32
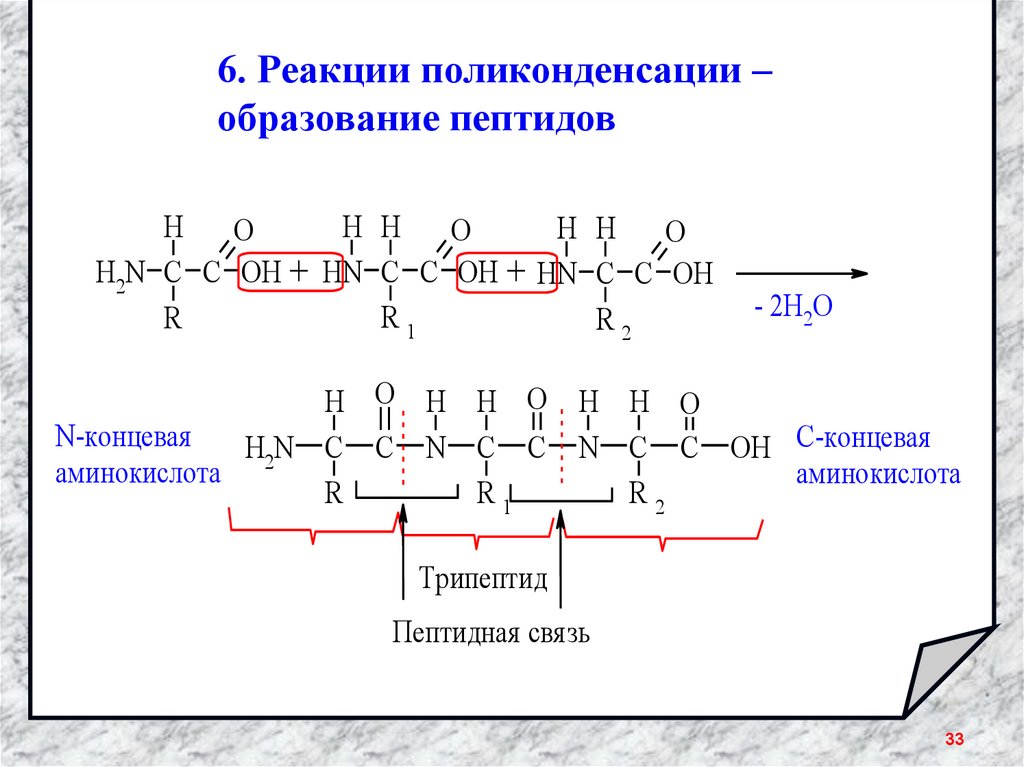
33.
6. Реакции поликонденсации –образование пептидов
H H
H
H H
O
O
O
H2N C C OH + HN C C OH + HN C C OH
R1
R
R2
- 2H2O
H O H H O H H O
N-концевая
H2N C C N C C N C C OH С-концевая
аминокислота
аминокислота
R2
R1
R
Трипептид
Пептидная свя зь
33
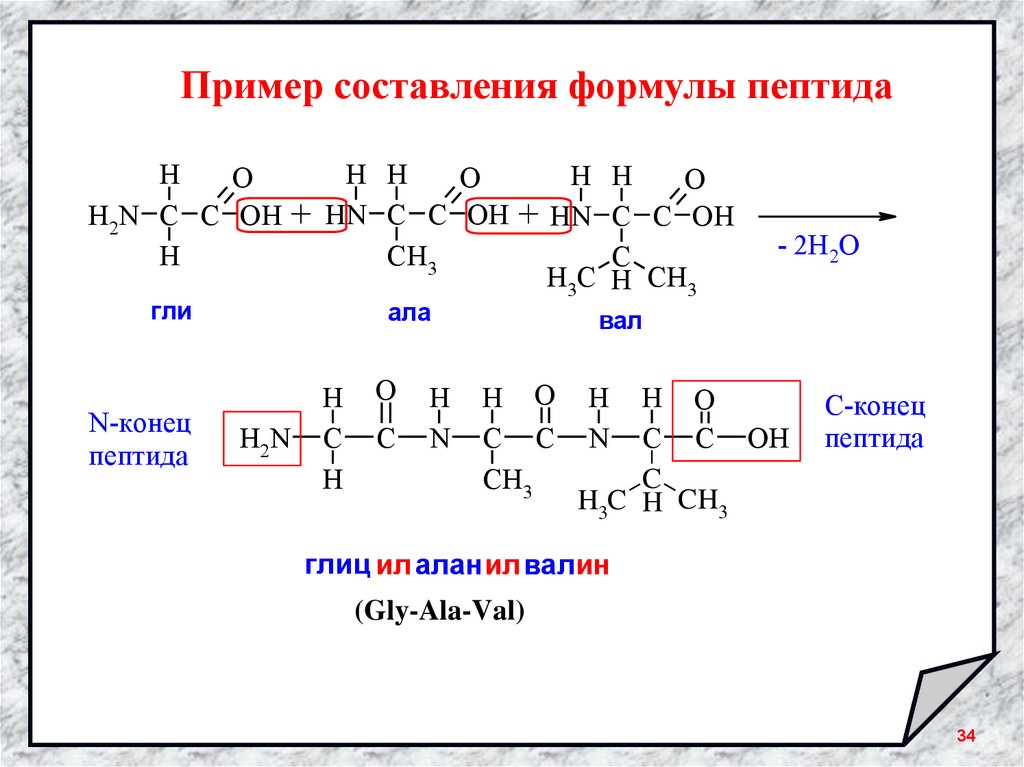
34.
Пример составления формулы пептидаH H
H
H H
O
O
O
H2N C C OH + HN C C OH + HN C C OH
CH3
H
C
H3C H CH3
гли
N-конец
пептида
ала
H2N
H
C
H
O
C
H
N
- 2H2O
вал
H O
C C
CH3
H
N
H O
C C OH
C
H3C H CH3
С-конец
пептида
глиц ил алан ил валин
(Gly-Ala-Val)
34
35.
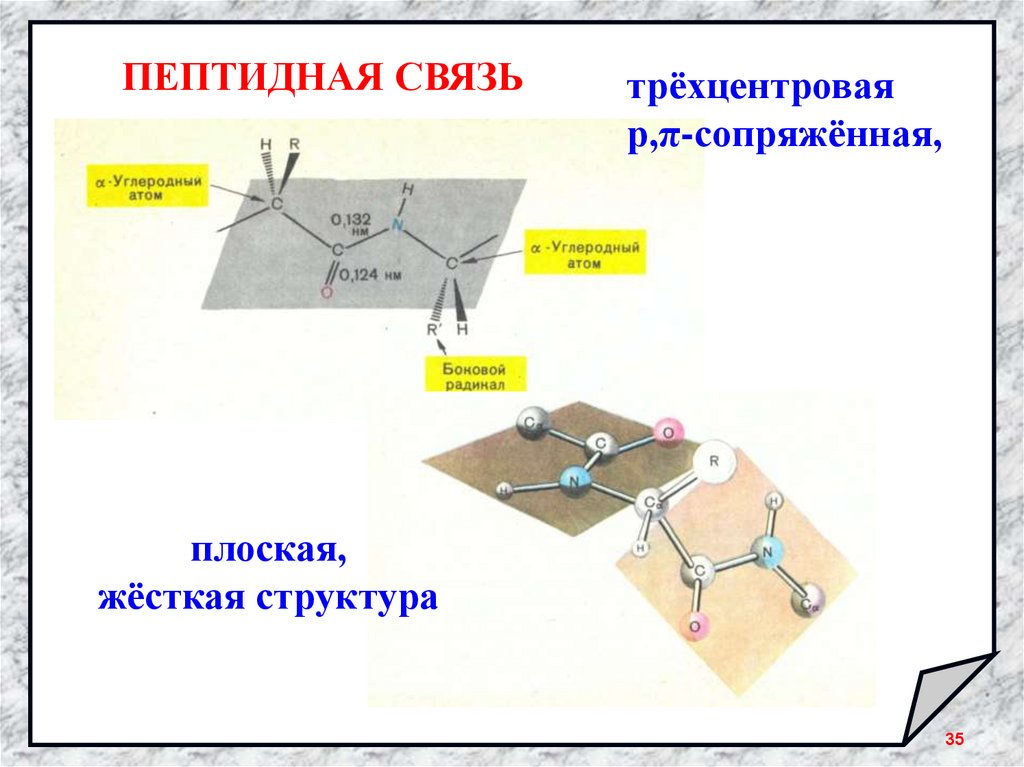
ПЕПТИДНАЯ СВЯЗЬтрёхцентровая
р,π-сопряжённая,
плоская,
жёсткая структура
35
36.
Аминокислоты нередко применяются вкачестве лекарственных средств:
Смешанные K,Mg-соли Asp (аспаркам)
или Glu (панангин) используются в кардиологии
и неврологии
36
37.
Использование аминокислот впромышленности
Аминокислоты используются для различных целей в
промышленности, в основном - в качестве добавок в корма
для животных. Такие добавки являются чрезвычайно
необходимыми, так как во многих основных компонентах
таких кормов, например, соевых бобах, очень мало или вовсе
нет некоторых незаменимых аминокислот. Лизин (L-лизин),
Метионин, Треонин, Триптофан являются наиболее важными
в производстве подобных кормов. В этой области
аминокислоты также используются в хелатных катионах
металла, чтобы улучшить поглощение минералов из пищевых
добавок, что важно для улучшения здоровья или
производительности этих животных.
37
38.
В пищевой промышленности аминокислоты также широкоиспользуются, в частности, глутаминовую кислоту используют в
качестве усилителя вкуса, а аспартам (аспартил-фенилаланин-1метиловый эфир) – в качестве низкокалорийного искусственного
подсластителя. Технологии, использующиеся в промышленности,
связанной с кормлением животных, часто используются и в пищевой
промышленности для снижения дефицита минеральных веществ
(например, при анемии), за счет улучшения усвоения минеральных
веществ из неорганических минеральных добавок.
Хелатообразующая способность аминокислот используется в
сельскохозяйственных удобрениях для облегчения доставки
минеральных веществ в растения при минеральной недостаточности
(например, дефиците железа). Эти удобрения также используются
для предотвращения возникновения болезней и улучшения общего
состояния здоровья растений.
Помимо этого, аминокислоты используются в синтезе лекарств и при
изготовлении косметики.
38
39.
Использование аминокислот вмедицине
При нарушениях азотистого обмена и наличии
аминокислотного дисбаланса в организме при ряде
патологических состояний и многих заболеваниях для
устранения дефицита, дисбаланса и увеличения доступности
аминокислот их следует вводить в виде лекарственных
препаратов или специальных пищевых добавок, диетических
блюд. Однако из-за объективных причин научного и
экономического характера лечебные свойства аминокислот в
настоящее время используются не в полной мере.
Аминокислоты широко используются в современной
медицине в качестве лекарственных средств. К таким
аминокислотам относится глутаминовая кислота, метионин,
гистидин, глицин, цистеин.
39
40.
Глутаминовая кислотаУчаствует в обмене белков и углеводов, способствует
синтезу нейромедиатора ацетилхолина, АТФ, переносу
ионов К+, стимулирует окислительные процессы.
Глутаминовая кислота относится к нейромедиаторам,
стимулирующим передачу в синапсах центральной
нервной системы возбуждения. При приёме внутрь она
хорошо проходит через клеточные мембраны, поступает
в центральную нервную систему и широко используется
для лечения заболеваний центральной нервной системы:
эпилепсии, психозов, депрессий, детского церебрального
паралича, болезни Дауна, полиомиелита.
40
41.
МетионинОтносится к числу незаменимых аминокислот, необходимых для
поддержания роста и азотистого равновесия в организме. Метионин
содержит подвижную метильную группу, которая может передаваться
другим соединениям. Таким образом, эта аминокислота может
принимать участие в таких важных процессах, как
переметилирование. Отдавая метильную группу, метионин
способствует синтезу холина, с недостатком образования которого
связывают нарушения липидного обмена, и тем самым способствует
удалению жира из печени. Метионин участвует в синтезе адреналина,
активирует действие гормонов, витаминов и ферментов. Путём
метилирования эта аминокислота обезвреживает токсичные вещества.
Метионин применяют для лечения и предупреждения
заболеваний и токсических поражений печени (цирроз, отравление
хлороформом, бензолом и другими веществами, а также при
алкоголизме и сахарном диабете). Его применяют при атеросклерозе
для снижения уровня холестерина в крови и повышения уровня
фосфолипидов.
41
42.
ГлицинЯвляется нейромедиатором тормозного типа
действия. Он улучшает метаболические процессы
в мозге и оказывает положительное влияние при
мышечной дистрофии. Эта аминокислота
применяется в медицине также как средство,
ослабляющее влечение к алкоголю и
уменьшающее депрессивные нарушения и
раздражительность у больных хроническим
алкоголизмом.
42
43.
Цистеинзаменимая аминокислота. Его характерной
особенностью является наличиесульфгидрильной
группы, которая очень реакционно способна и
может легко окисляться с образованием молекулы
цистина, которая содержит дисульфидную связь (S
– S). Лёгкое превращение цистеина в цистин и
обратимость этой реакции играют важную роль в
регуляции процессов обмена веществ. В
медицинской практике цистеин используется как
средство для задержки развития катаракты и
просветления хрусталика.
43
44.
ЛизинУчаствует в образовании антител; в процессе
метаболизма вместе с витамином С образует
карнитин, последний улучшает устойчивость к
стрессам и жировой метаболизм;
противодействует утомлению; стимулирует
умственную работоспособность.
44
45.
ТреонинУчаствует в образовании коллагена и эластина;
обладает гликогенным воздействием;
активизирует, иммунную систему, участвуя в
образовании иммуноглобулинов и антител;
стимулирует процессы роста тканей; способствует
энергообмену в мышечных клетках.
45
46.
ТриптофанВместе с биотином, витамином В, и В6
способствует релаксации и хорошему сну (в
дозировке до 250 мг), утилизации витаминов
группы В; является антидепрессантом; участвует в
образовании серотонина; повышает
сопротивляемость стрессам.
46
47.
ФенилаланинУчаствует в продукции коллагена и
соединительных тканей; является стимулятором
ЦНС; антидепрессант; участвует в синтезе
тиреоидных гормонов щитовидной железы;
улучшает функционирование кровеносной сети;
повышает работоспособность.
47
48.
АланинРегулирует уровень сахара в крови;
используется как источник энергии клетками
мозга; способствует накоплению гликогена
печенью и мышцами; участвует в процессе
создания иммуноглобулинов и антител; его можно
принимать в повышенной дозировке перед
тренировкой для создания запаса энергии;
предшественник образования оксида азота,
который расслабляет гладкие мышцы, в том числе
коронарных сосудов, улучшает память,
сперматогенез и другие функции.
48
49.
АргининСпособствует детоксикации и выведению
аммиака; снижает уровень жира в организме;
участвует в процессах образования коллагена;
стимулирует иммунную систему; предотвращает
физическую и умственную усталость; выступает в
качестве гепатопротектора; способствует синтезу
гликогена в печени и мышцах, высвобождению
глюкагона, пролактина, соматотропина,
адреналина.
49
50.
Кислота аспаргиноваяОблегчает превращение углеводов в
мышечную энергию; повышает активность
иммунной системы; увеличивает
сопротивляемость утомлению; сохраняет
способность к работе на выносливость; действует
как гепатопротектор; участвует в реакциях цикла
мочевины и переаминирования; образует
метионин, треонин и лизин.
50
51.
ГистидинНезаменимая аминокислота, при введении в организм вызывает
значительное увеличение секреции СТГ. Принимает активное участие
в синтезе карнозина — азотистого экстрактивного вещества мышц,
улучшает азотистый баланс, функцию печени, повышает желудочную
секрецию и моторную активность кишечника, иммунитет и ослабляет
воздействие на организм экстремальных факторов, нормализует
сердечный ритм. В медицине применяют при язвенной болезни,
гастритах, гепатитах, снижении иммунитета и атеросклерозе.
Гистидин в комбинации с АТФ, калием и магнием входит в
комплексный препарат АТФ-ЛОНГ (Борщаговский ХФЗ), который в
эксперименте повышает работоспособность животных, в клинике его
применяют как антиишемическое и антиаритмическое средство.
Исследованиями, проведенными в лаборатории эргогенных факторов
в спорте Государственного НИИ физической культуры и спорта
(Киев), установлен эргогенный эффект АТФ-ЛОНГ у спортсменов.
51
52.
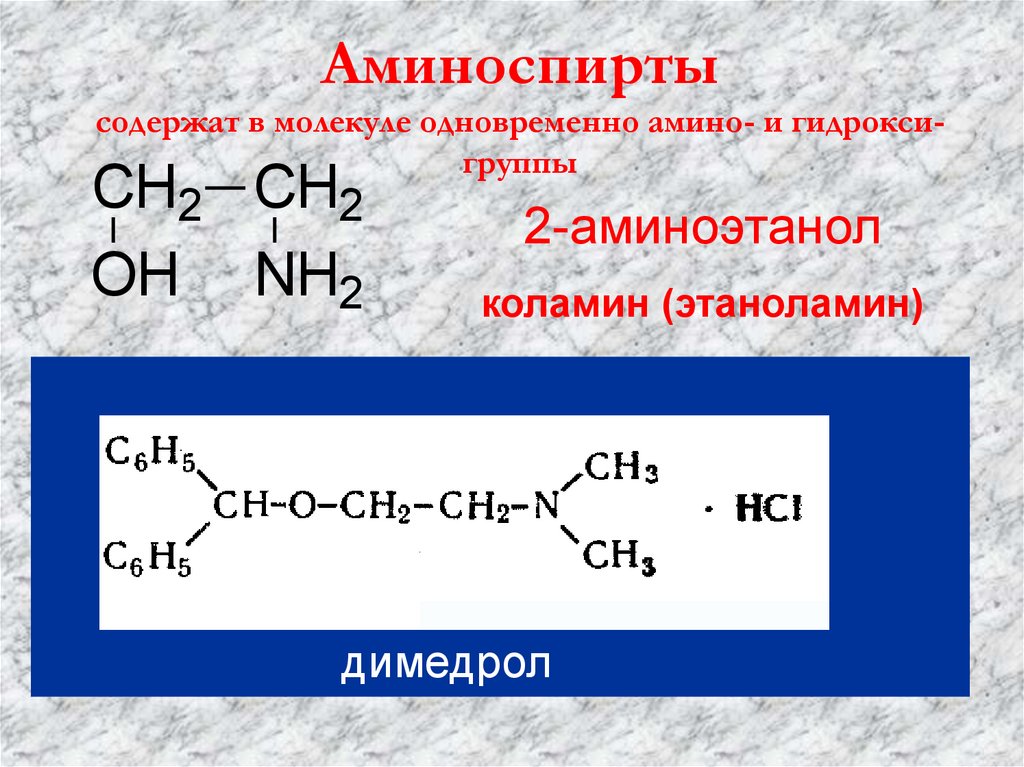
Аминоспиртысодержат в молекуле одновременно амино- и гидроксигруппы
CH2 CH2
OH NH2
2-аминоэтанол
коламин (этаноламин)
холин (триметил- -гидроксиэтилгидрат аммония):
H2C CH2
OH
CH3 +
2
N CH3 OH
CH3
димедрол
53.
При исчерпывающем метилировании этаноламинаобразуется гидроксид 2гидроксиэтилтриметиламмония.
Его катион называют холином.
54.
ХолинХолин – структурный элемент сложных
липидов. Имеет большое значение как
витаминоподобное вещество, регулирующее
жировой обмен. В организме холин может
образовываться из аминокислоты серина.
55.
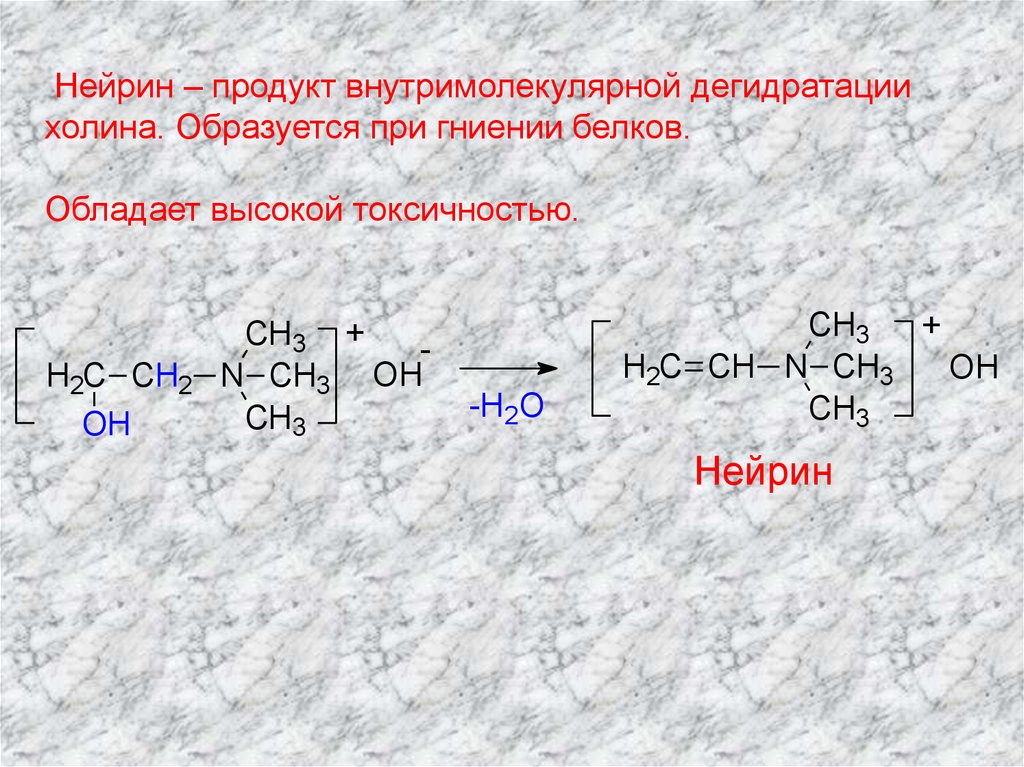
Нейрин – продукт внутримолекулярной дегидратациихолина. Образуется при гниении белков.
Обладает высокой токсичностью.
H2C CH2
OH
CH3 +
N CH3 OH
CH3
-H2O
CH3
+
H2C CH N CH3
OH
CH3
Нейрин
56.
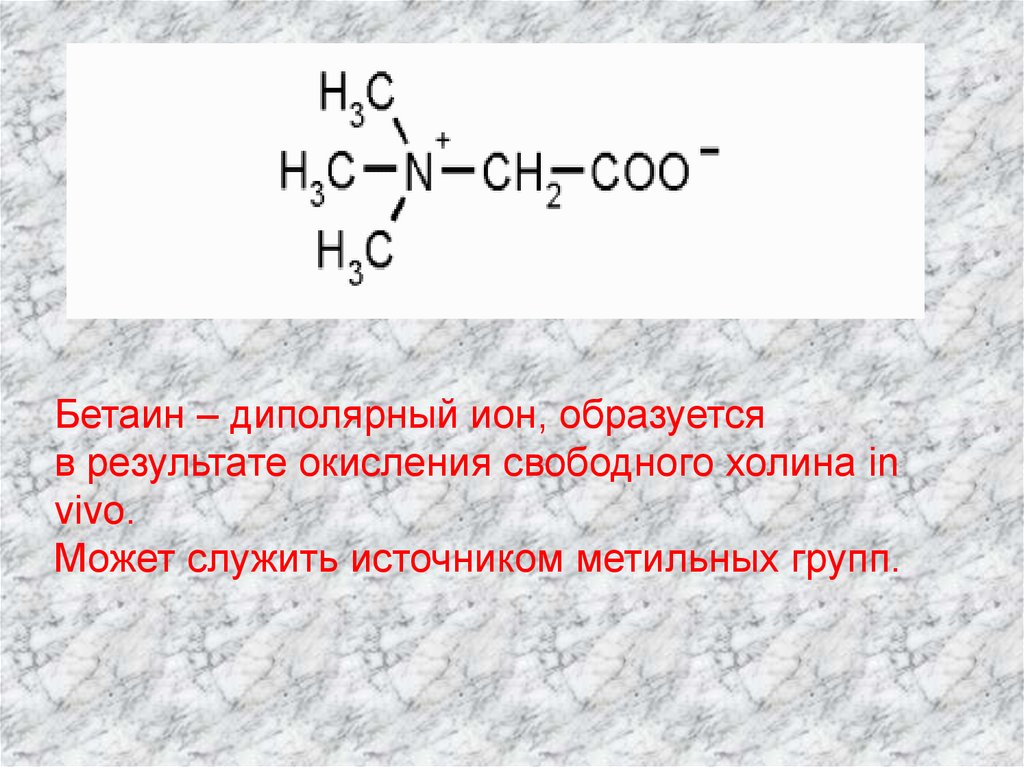
Бетаин – диполярный ион, образуетсяв результате окисления свободного холина in
vivo.
Может служить источником метильных групп.
57.
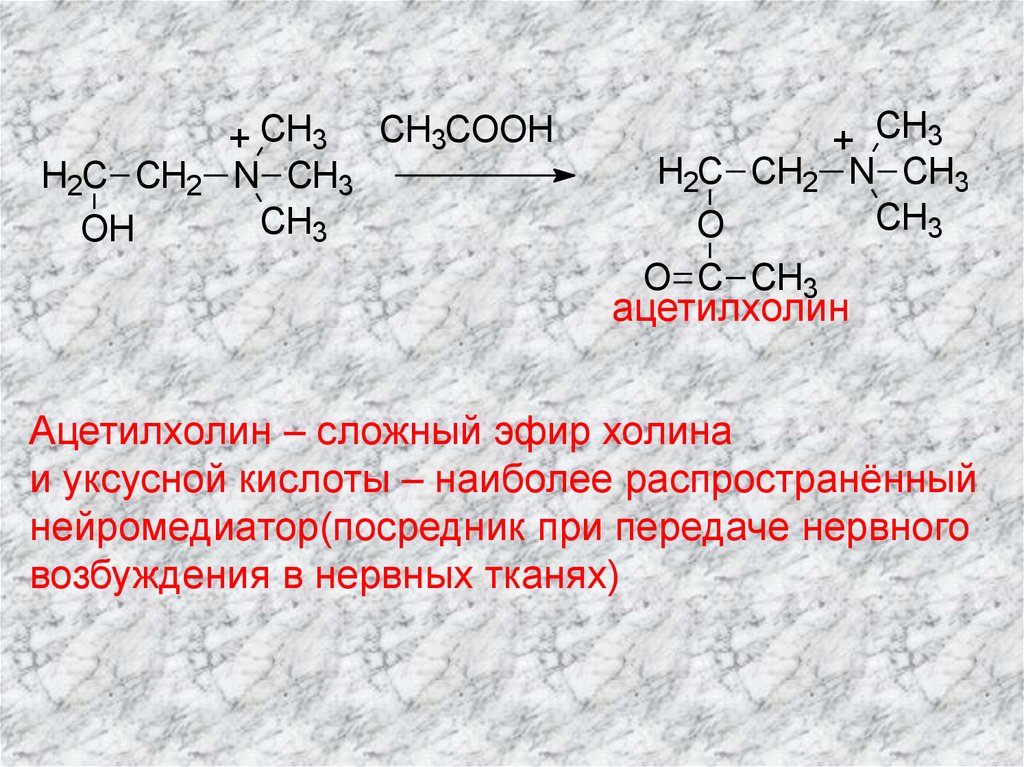
+ CH3 CH3COOHH2C CH2 N CH3
CH3
OH
+ CH3
H2C CH2 N CH3
CH3
O
O C CH3
ацетилхолин
Ацетилхолин – сложный эфир холина
и уксусной кислоты – наиболее распространённый
нейромедиатор(посредник при передаче нервного
возбуждения в нервных тканях)
























 chemistry
chemistry