Similar presentations:
(4 колл) Арилметановые
1. Арилметановые красители
2.
Этот химический класс красителей включает следующие группы:Собственно арилметановые красители. Они представляют
собой производные диарил- и триарилметана. В этих красителях центральный атом углерода может быть связан с водородом, с неароматическим остатком или ароматическим ядром.
Ar
CH
R
Ar'
M
Ar
Ar'
CH
R = H, неароматический остаток, Ar"
R
Ксантеновые красители. Эта группа является производными
гетероциклической системы ксантена и отличается от собственно арилметановых красителей наличием кислородного мостика
О, соединяющего два ароматических ядра в орто-положениях к
связям с центральным атомом углерода.
Акридиновые красители. Эта группа является производными
гетероциклической системы акридина и отличается от ксантеновых наличием NH мостика, связывающего ароматические
остатки в орто-положениях к метановому атому углерода.
3.
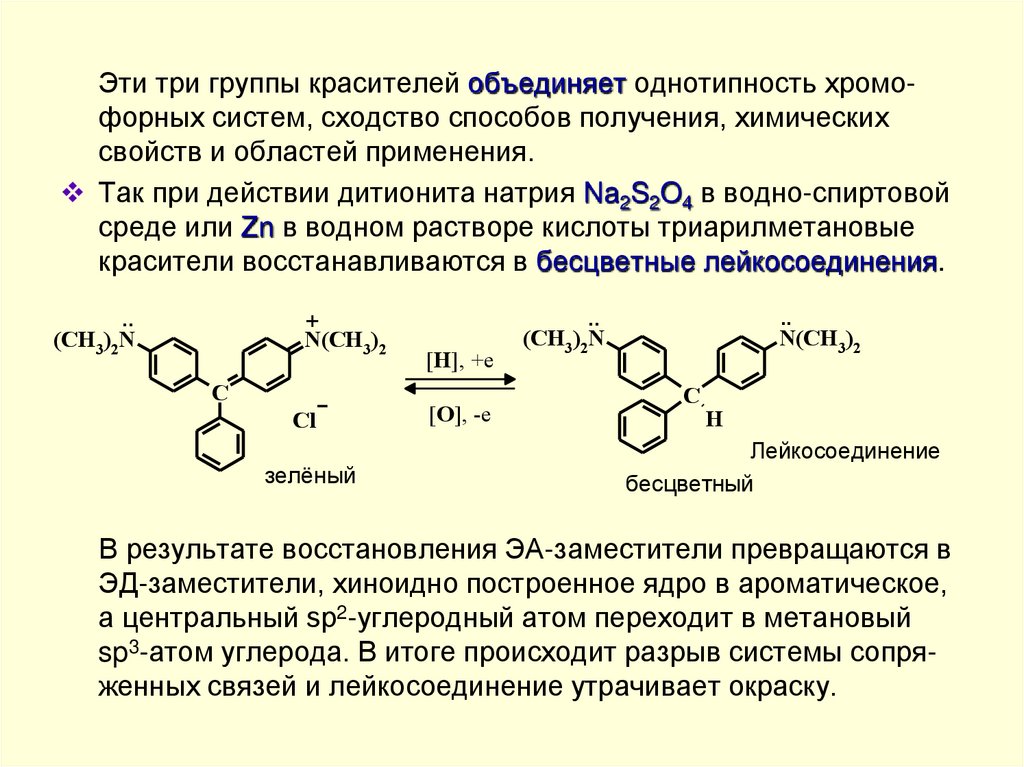
Эти три группы красителей объединяет однотипность хромофорных систем, сходство способов получения, химическихсвойств и областей применения.
Так при действии дитионита натрия Na2S2O4 в водно-спиртовой
среде или Zn в водном растворе кислоты триарилметановые
красители восстанавливаются в бесцветные лейкосоединения.
..
+
N(CH3)2
(CH3)2N
C
Cl
зелёный
..
..
[H], +e
[O], -e
(CH3)2N
N(CH3)2
C
H
Лейкосоединение
бесцветный
В результате восстановления ЭА-заместители превращаются в
ЭД-заместители, хиноидно построенное ядро в ароматическое,
а центральный sp2-углеродный атом переходит в метановый
sp3-атом углерода. В итоге происходит разрыв системы сопряженных связей и лейкосоединение утрачивает окраску.
4.
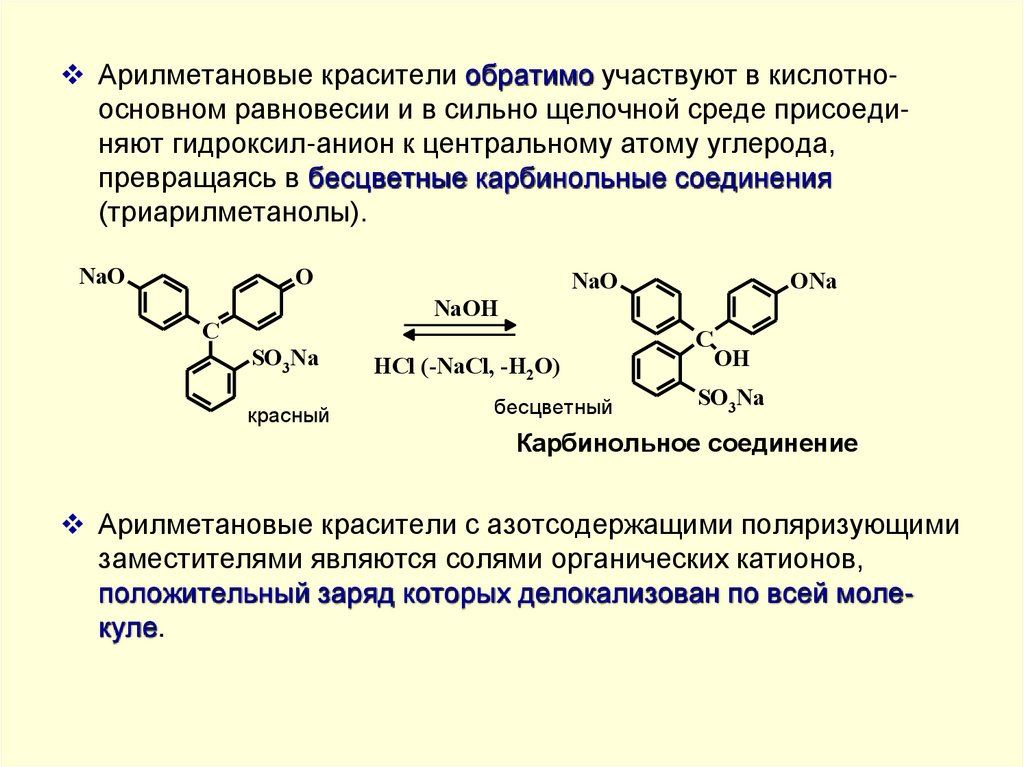
Арилметановые красители обратимо участвуют в кислотноосновном равновесии и в сильно щелочной среде присоединяют гидроксил-анион к центральному атому углерода,превращаясь в бесцветные карбинольные соединения
(триарилметанолы).
NaO
O
NaO
ONa
NaOH
C
SO3Na
красный
C
HCl (-NaCl, -H2O)
бесцветный
OH
SO3Na
Карбинольное соединение
Арилметановые красители с азотсодержащими поляризующими
заместителями являются солями органических катионов,
положительный заряд которых делокализован по всей молекуле.
5.
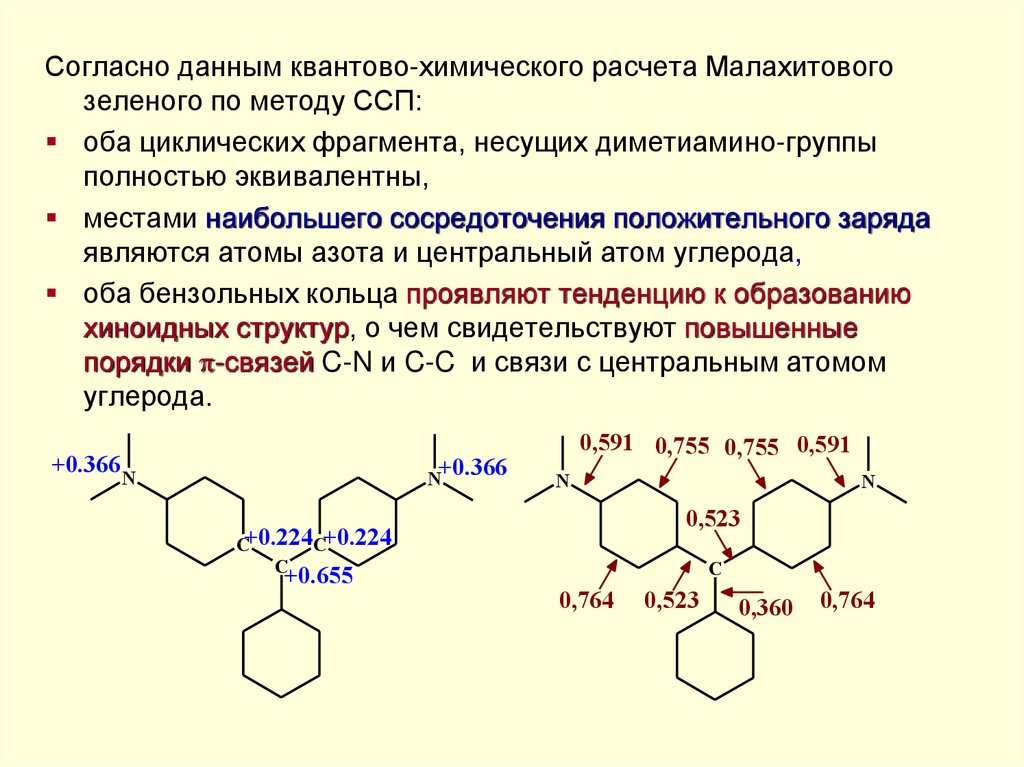
Согласно данным квантово-химического расчета Малахитовогозеленого по методу ССП:
оба циклических фрагмента, несущих диметиамино-группы
полностью эквивалентны,
местами наибольшего сосредоточения положительного заряда
являются атомы азота и центральный атом углерода,
оба бензольных кольца проявляют тенденцию к образованию
хиноидных структур, о чем свидетельствуют повышенные
порядки -связей C-N и C-C и связи с центральным атомом
углерода.
+0.366
+0.366
N
N
0,591 0,755 0,755 0,591
N
N
0,523
C+0.224C+0.224
C
+0.655
C
0,764
0,523
0,360
0,764
6.
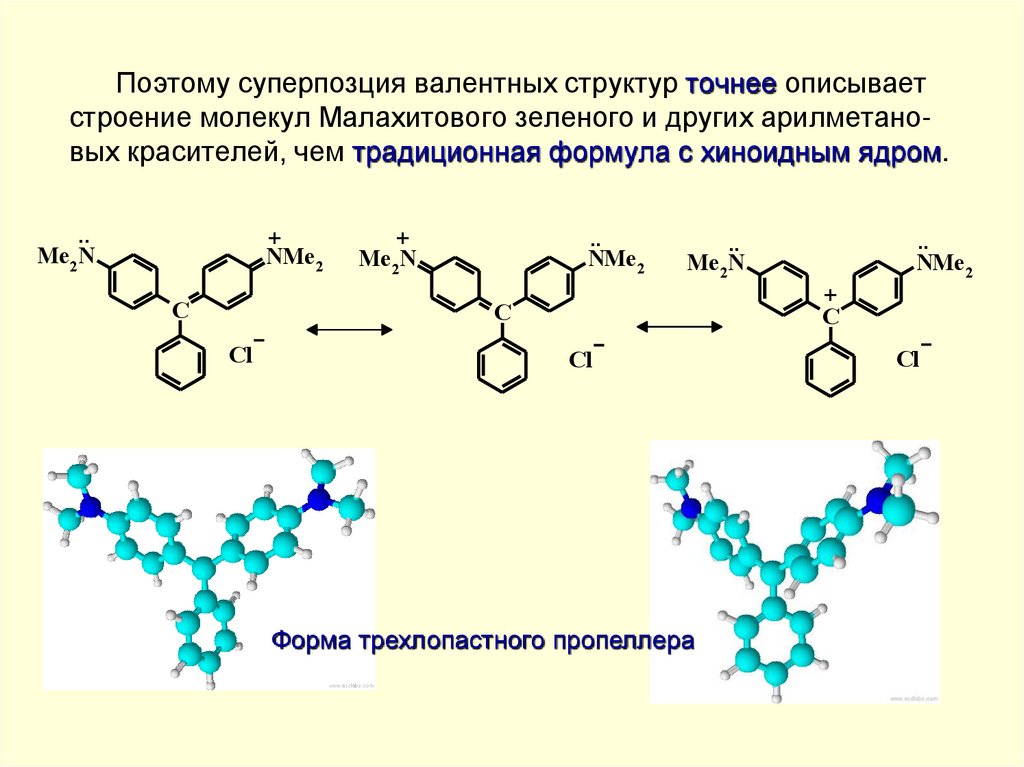
Поэтому суперпозция валентных структур точнее описываетстроение молекул Малахитового зеленого и других арилметановых красителей, чем традиционная формула с хиноидным ядром.
..
+
NMe 2
Me 2N
C
+
Me 2N
..
NMe 2
NMe 2
Me 2N
+
C
C
Cl
..
..
Cl
Форма трехлопастного пропеллера
Cl
7.
Делокализация положительного заряда по хромофорнойсистеме обусловливает высокую реакционную способность
арилметановых красителей и приводит к тому, что химические и
фотохимические реакции прежде всего нарушают хромофорную систему красителя. Поэтому в большинстве случаев
устойчивость окрасок на природных гидрофильных волокнах
низка и арилметановые красители в настоящее время находят
ограниченное применение в текстильной промышленности.
Вместе с тем следует подчеркнуть, что красители этого
класса дают интенсивные, яркие и чистые окраски.
Хромофорная система арилметановых красителей
характеризуется наличием цепочки сопряженных двойных
связей, которая состоит из двух ароматических остатков,
способных существовать в хиноидной форме и несущих
электронодонорный и электроноакцепторный заместители, а также соединяющего их центрального атома
углерода.
8. 5.1. Способы получения арилметановых красителей
В основе всех способов построения арилметановой системыкрасителей лежит конденсация карбонилсодержащего соединения с амино- или гидроксипроизводными ароматического ряда.
Реакция обычно происходит по свободному пара-положению
ароматического ядра, активированному ЭД-заместителем, через
стадию электрофильной атаки электронодефицитным С-атомом
карбонильной группы.
..
(CH3)2N
R
+
C
R
O
..
(CH3)2N
H R
+ C R
O
(CH3)2N
R
C R
OH
Эту реакцию катализируют сильные кислоты (H2SO4, HCl, щавелевая кислота), которые протонируют кислород карбонильной
группы, увеличивая положительный заряд на её атоме углерода.
+
R CH O
.. : + H
+
R CH OH
..
+
R CH OH
9.
При этом образуется высокоактивный карбкатион, которыйвзаимодействует по вышеприведенной схеме электрофильного
замещения.
Способствуют протеканию конденсации также и кислоты
Льюиса, так называемые «водоотнимающие средства». Например, безводный ZnCl2 координируется по О-атому карбонильной
группы и активирует атом углерода в ней, усиливая эффективный положительный заряд.
C O
ZnCl2
В зависимости от применяемых в реакции конденсации
карбонильных соединений различают четыре способа
получения арилметановых красителей.
10. Бензальдегидный метод
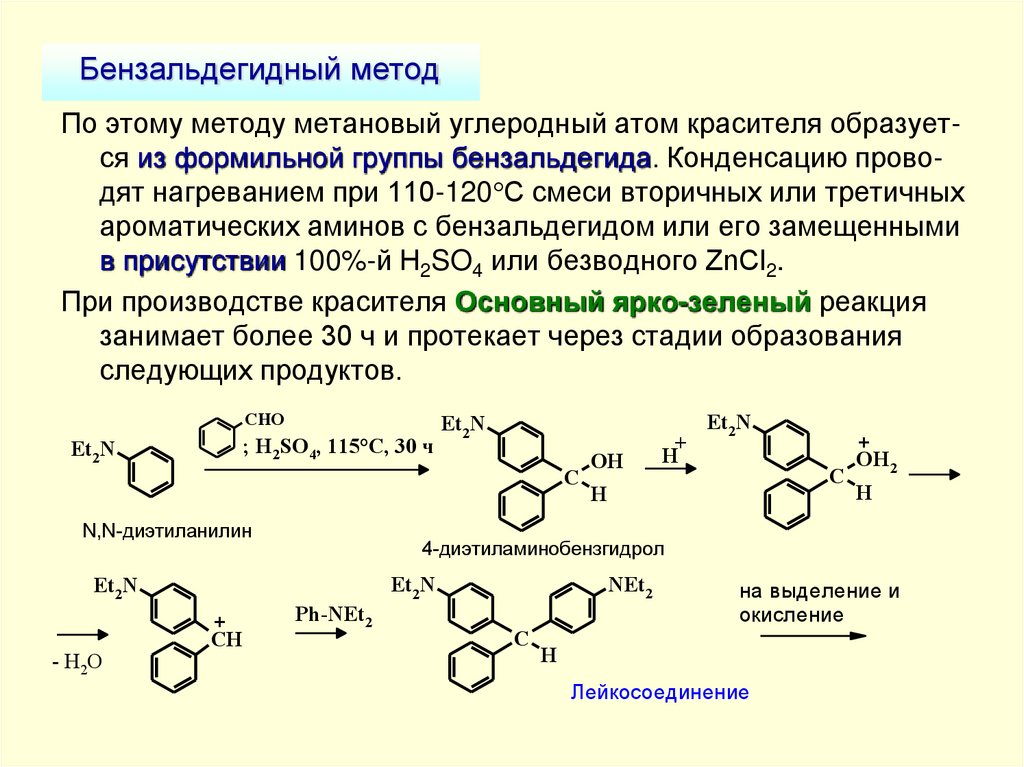
По этому методу метановый углеродный атом красителя образуется из формильной группы бензальдегида. Конденсацию проводят нагреванием при 110-120 С смеси вторичных или третичныхароматических аминов с бензальдегидом или его замещенными
в присутствии 100%-й H2SO4 или безводного ZnCl2.
При производстве красителя Основный ярко-зеленый реакция
занимает более 30 ч и протекает через стадии образования
следующих продуктов.
CHO
Et2N
; H2SO4, 115°C, 30 ч
C
N,N-диэтиланилин
Et2N
- H2O
Et2N
+
CH
OH
+
H
Et2N
C
H
+
OH2
H
4-диэтиламинобензгидрол
Ph-NEt2
NEt2
Et2N
C
на выделение и
окисление
H
Лейкосоединение
11.
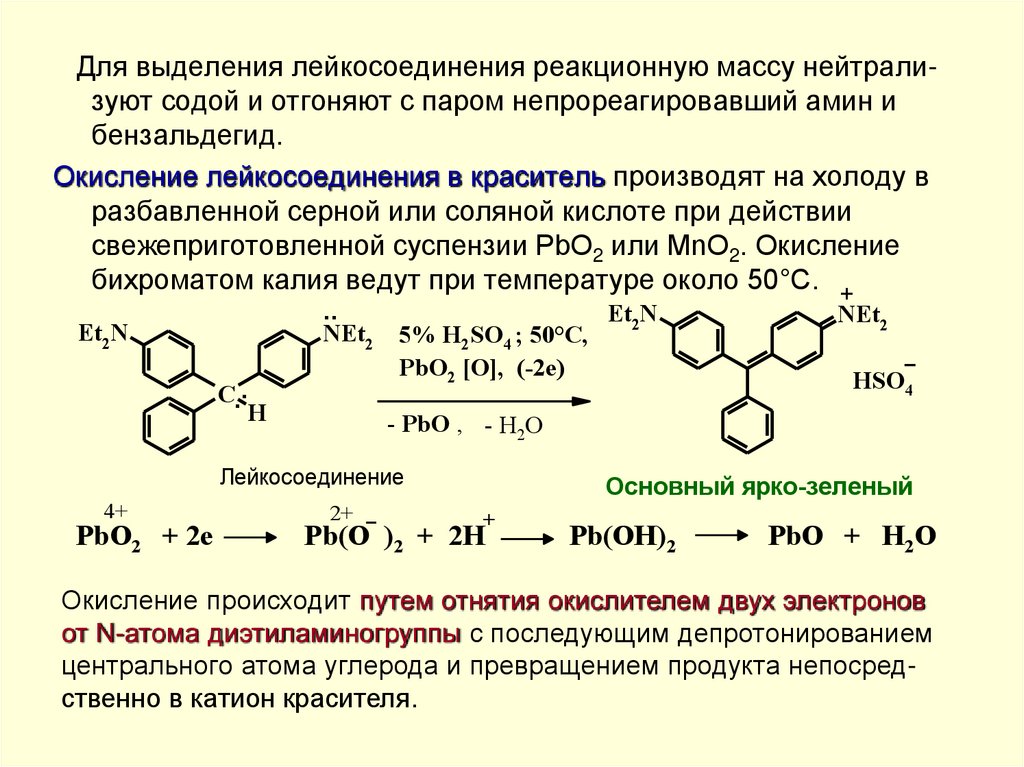
Для выделения лейкосоединения реакционную массу нейтрализуют содой и отгоняют с паром непрореагировавший амин ибензальдегид.
Окисление лейкосоединения в краситель производят на холоду в
разбавленной серной или соляной кислоте при действии
свежеприготовленной суспензии PbO2 или MnO2. Окисление
бихроматом калия ведут при температуре около 50°С. +
..
NEt2
Et2N
C..
H
5% H2SO4 ; 50°C,
PbO2 [O], (-2e)
PbO2 + 2e
NEt2
HSO4
- PbO , - H2O
Лейкосоединение
4+
Et2N
2+
Основный ярко-зеленый
+
Pb(O )2 + 2H
Pb(OH)2
PbO + H2O
Окисление происходит путем отнятия окислителем двух электронов
от N-атома диэтиламиногруппы с последующим депротонированием
центрального атома углерода и превращением продукта непосредственно в катион красителя.
12.
Приведенный в учебнике другой механизм окисления –прямой отрыв от центрального С-атома гидрид-аниона :H с
помощью акцептора, например, диоксида свинца термодинамически не обоснован и представляется маловероятным.
Соли свинца осаждают в виде PbSO4, после фильтрации,
фильтрат подщелачивают, осадок свободного основания
промывают водой путем декантации. Если краситель выпускают
в виде хлорида, то основание растворяют в водной соляной
кислоте и высаливают NaCl при 70 С. Аналогично получают
сульфат красителя, но тогда высаливают из раствора в серной
кислоте с помощью сульфата натрия.
13.
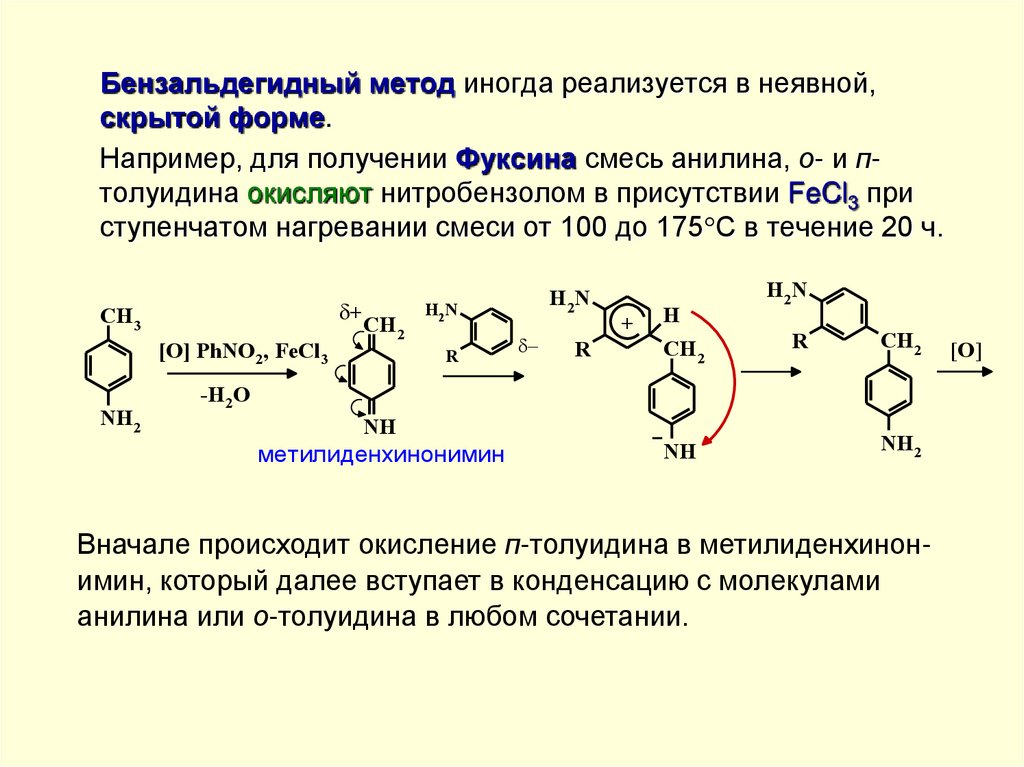
Бензальдегидный метод иногда реализуется в неявной,скрытой форме.
Например, для получении Фуксина смесь анилина, о- и птолуидина окисляют нитробензолом в присутствии FeCl3 при
ступенчатом нагревании смеси от 100 до 175 С в течение 20 ч.
+
CH3
[O] PhNO2, FeCl3
NH2
CH2
H2N
H2N
R
R
+
H
CH2
H2N
R
CH2
-H2O
NH
метилиденхинонимин
NH
NH2
Вначале происходит окисление п-толуидина в метилиденхинонимин, который далее вступает в конденсацию с молекулами
анилина или о-толуидина в любом сочетании.
[O]
14.
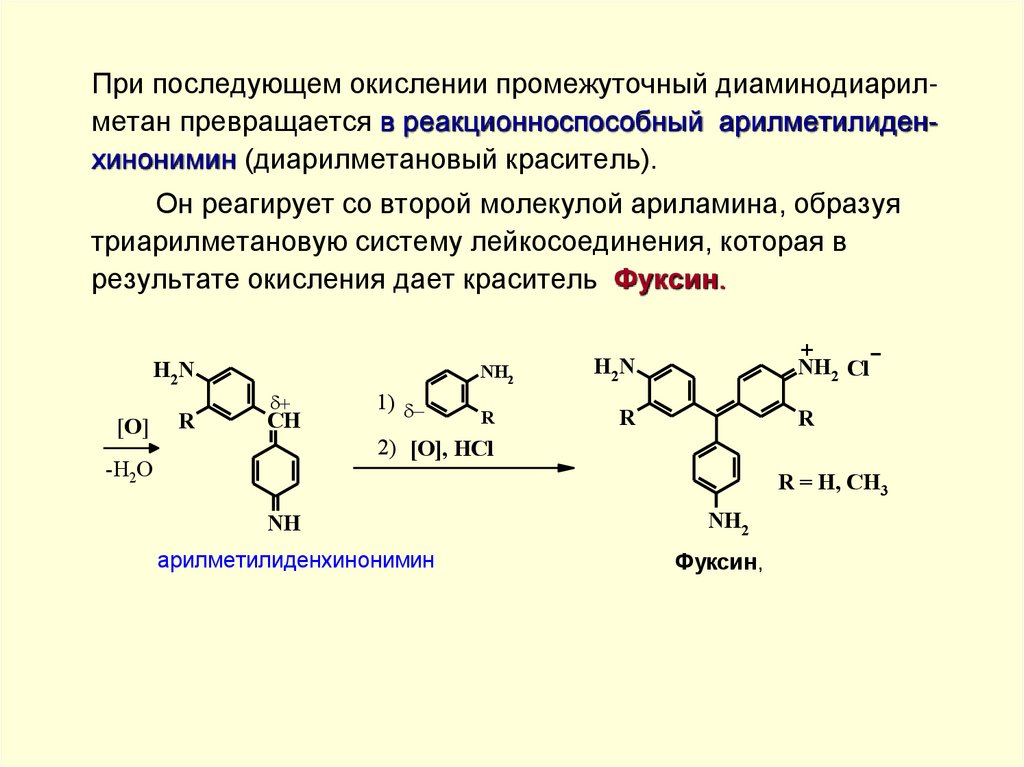
При последующем окислении промежуточный диаминодиарилметан превращается в реакционноспособный арилметилиденхинонимин (диарилметановый краситель).Он реагирует со второй молекулой ариламина, образуя
триарилметановую систему лейкосоединения, которая в
результате окисления дает краситель Фуксин.
H2N
[O]
R
NH2
CH
1)
R
+
H2N
NH2 Cl
R
R
2) [O], HCl
-H2O
R = H, CH3
NH
NH2
арилметилиденхинонимин
Фуксин,
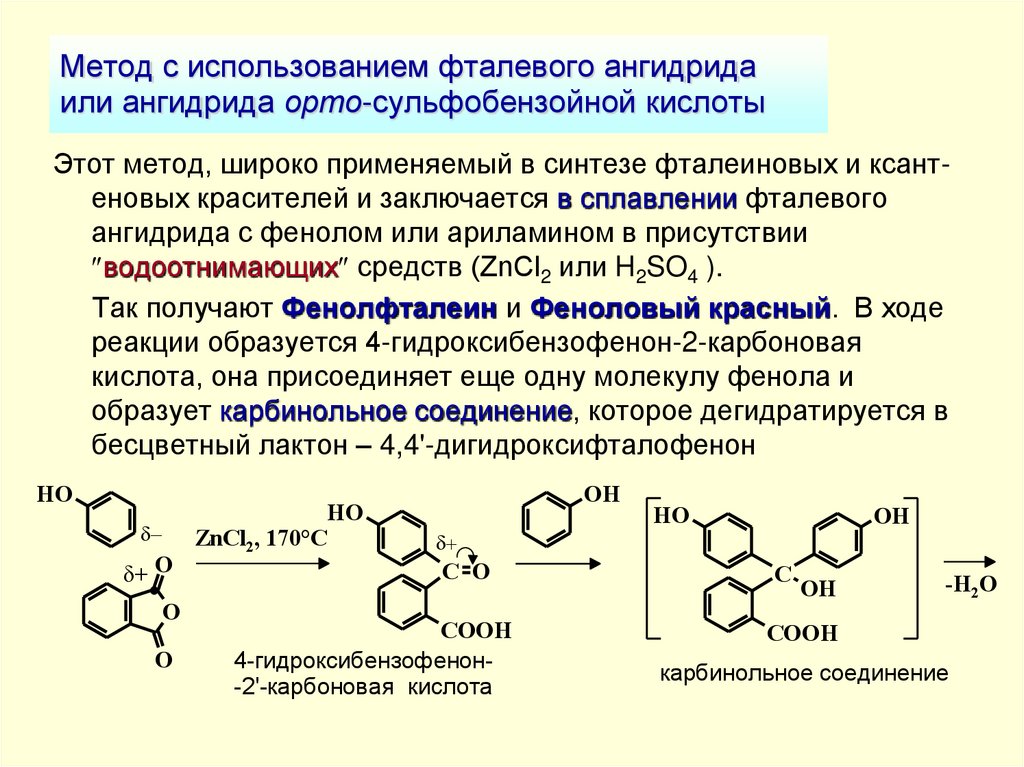
15. Метод с использованием фталевого ангидрида или ангидрида орто-сульфобензойной кислоты
Этот метод, широко применяемый в синтезе фталеиновых и ксантеновых красителей и заключается в сплавлении фталевогоангидрида с фенолом или ариламином в присутствии
водоотнимающих средств (ZnCl2 или H2SO4 ).
Так получают Фенолфталеин и Феноловый красный. В ходе
реакции образуется 4-гидроксибензофенон-2-карбоновая
кислота, она присоединяет еще одну молекулу фенола и
образует карбинольное соединение, которое дегидратируется в
бесцветный лактон – 4,4'-дигидроксифталофенон
HO
+ O
O
O
HO
ZnCl2, 170°C
OH
HO
OH
C O
COOH
4-гидроксибензофенон-2'-карбоновая кислота
C
OH
-H2O
COOH
карбинольное соединение
16.
HOOH
5%- NaOH, 30°C
C
-H2O
O
C
O
HO
O
COONa
OH
C
NaO
NaOH
-H2O
OH
COONa
Лактон
4,4'-дигидроксифталофенон
C
желтая соль
HO
O
C
CH3COOH
COONa
красная соль
Фенолфталеин
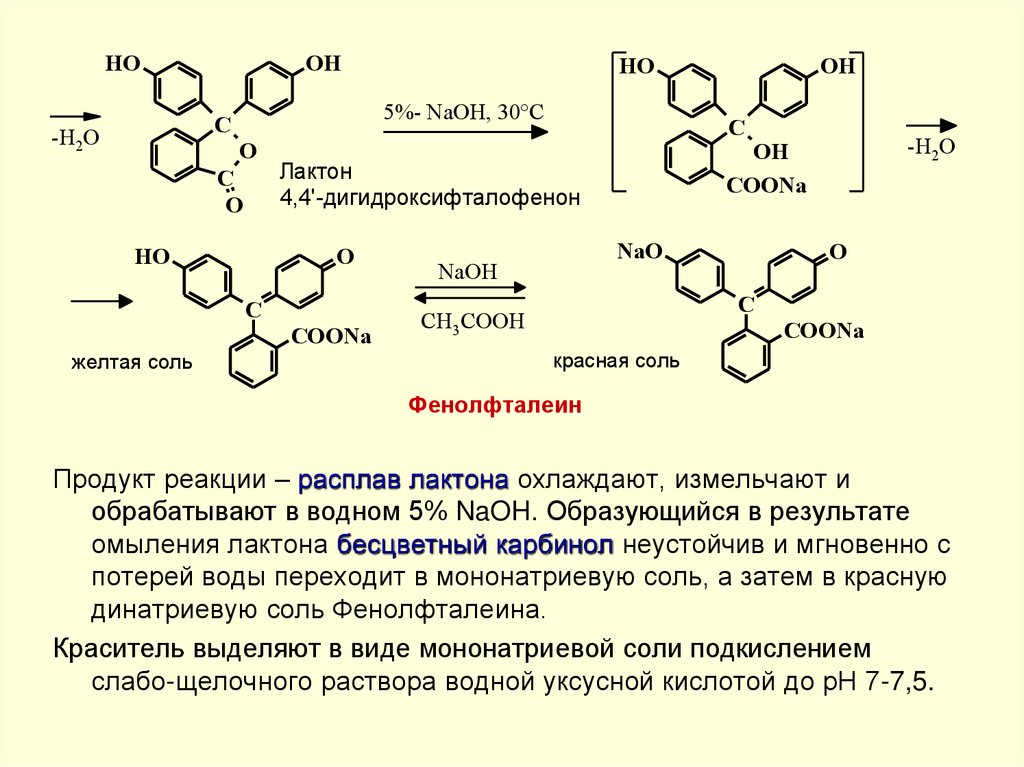
Продукт реакции – расплав лактона охлаждают, измельчают и
обрабатывают в водном 5% NaOH. Образующийся в результате
омыления лактона бесцветный карбинол неустойчив и мгновенно с
потерей воды переходит в мононатриевую соль, а затем в красную
динатриевую соль Фенолфталеина.
Краситель выделяют в виде мононатриевой соли подкислением
слабо-щелочного раствора водной уксусной кислотой до рН 7-7,5.
17. Формальдегидный или бензгидрольный метод
По этому методу центральный углеродный атом красителяобразуется из формальдегида путем его конденсации с
ариламинами со свободным пара-положением.
Синтез обычно ведут в две стадии с выделением промежуточно
образующегося производного дифенилметана - бензгидрола.
Затем его вводят в реакцию с ароматическим соединением c
подвижным атомом водорода.
Стадии различаются условиями проведения
конденсации и применяемым конденсирующим агентом.
18.
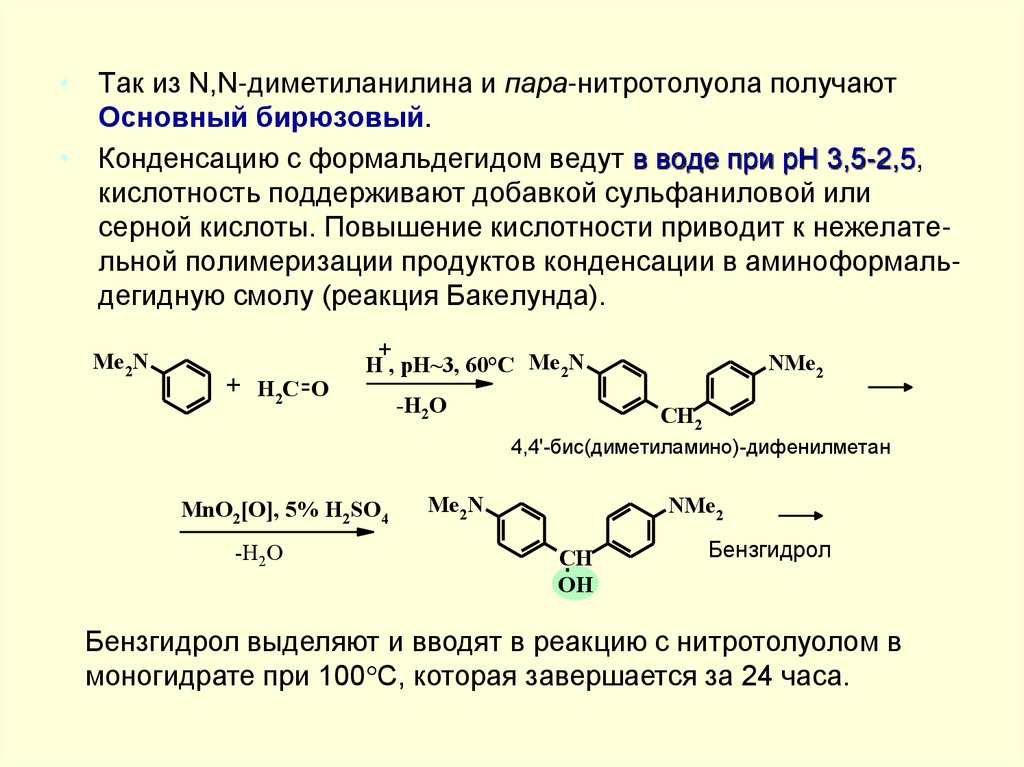
• Так из N,N-диметиланилина и пара-нитротолуола получаютОсновный бирюзовый.
• Конденсацию с формальдегидом ведут в воде при рН 3,5-2,5,
кислотность поддерживают добавкой сульфаниловой или
серной кислоты. Повышение кислотности приводит к нежелательной полимеризации продуктов конденсации в аминоформальдегидную смолу (реакция Бакелунда).
Me 2N
+
+ H2C O
H , pH~3, 60°C Me 2N
-H2O
NMe 2
CH 2
4,4'-бис(диметиламино)-дифенилметан
MnO2[O], 5% H2SO4
-H2O
Me 2N
NMe 2
CH
OH
Бензгидрол
Бензгидрол выделяют и вводят в реакцию с нитротолуолом в
моногидрате при 100 С, которая завершается за 24 часа.
19.
Me 2N100% H2SO4,
100°C, 24 ч
NMe 2
+
CH
CH3
Me 2N
O2N
O2N
Карбкатион
-H2O
Me 2N
-H+
*
O2N
+
NMe 2
MnO2[O], HCl
H
CH3
Лейкосоединение
+
C
HH
CH3
Me 2N
NMe 2
C
NMe 2
C
Cl
CH3
-H2O
O2N
Основный бирюзовый
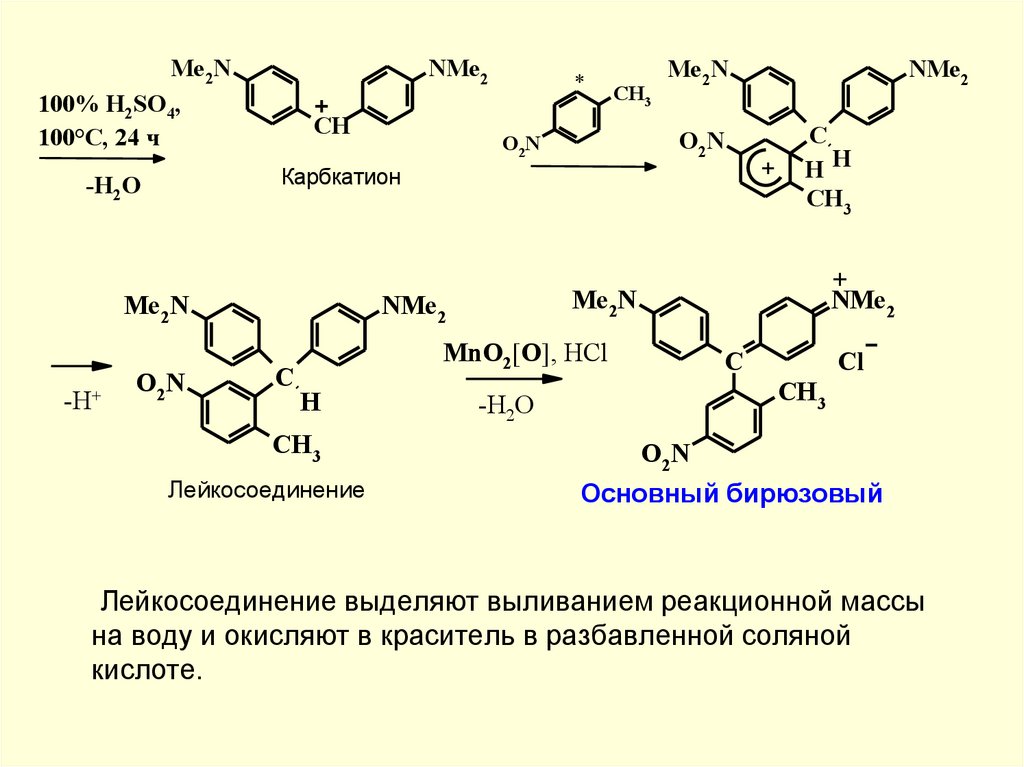
Лейкосоединение выделяют выливанием реакционной массы
на воду и окисляют в краситель в разбавленной соляной
кислоте.
20.
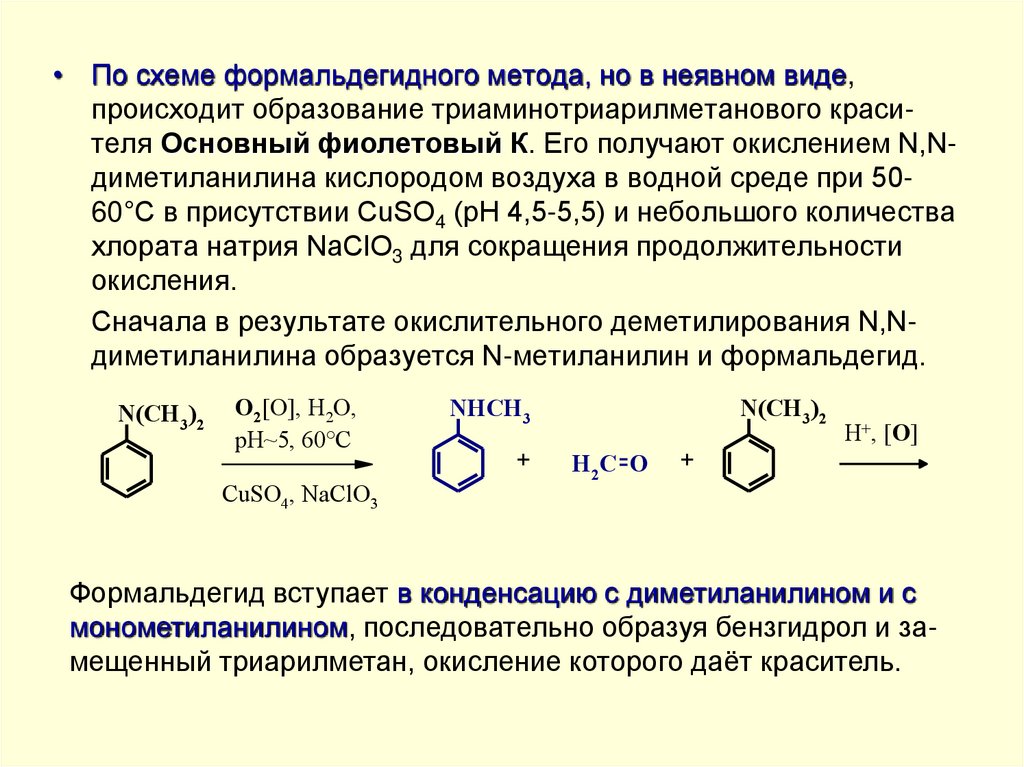
• По схеме формальдегидного метода, но в неявном виде,происходит образование триаминотриарилметанового красителя Основный фиолетовый К. Его получают окислением N,Nдиметиланилина кислородом воздуха в водной среде при 5060°С в присутствии CuSO4 (рН 4,5-5,5) и небольшого количества
хлората натрия NaClO3 для сокращения продолжительности
окисления.
Сначала в результате окислительного деметилирования N,Nдиметиланилина образуется N-метиланилин и формальдегид.
N(CH3)2
O2[O], H2O,
pH~5, 60°C
CuSO4, NaClO3
NHCH3
+
N(CH3)2
H2C O
+
H+, [O]
Формальдегид вступает в конденсацию с диметиланилином и с
монометиланилином, последовательно образуя бензгидрол и замещенный триарилметан, окисление которого даёт краситель.
21.
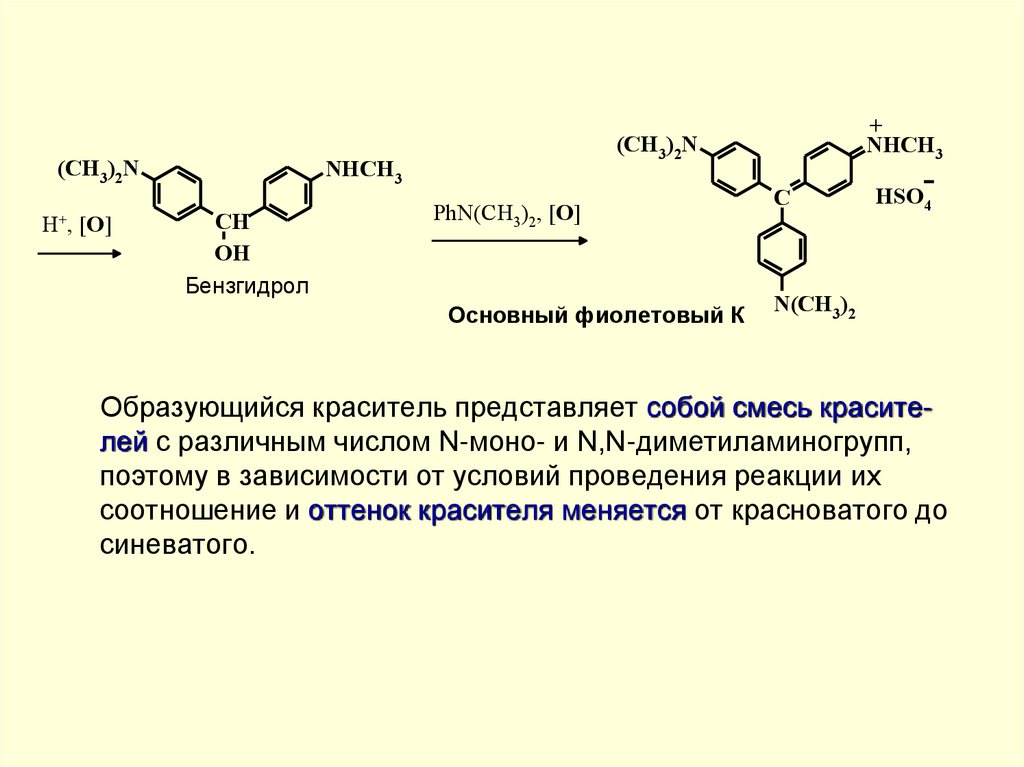
(CH3)2NH+, [O]
NHCH3
CH
OH
Бензгидрол
+
NHCH 3
(CH3)2N
PhN(CH3)2, [O]
Основный фиолетовый К
C
HSO4
N(CH3)2
Образующийся краситель представляет собой смесь красителей с различным числом N-моно- и N,N-диметиламиногрупп,
поэтому в зависимости от условий проведения реакции их
соотношение и оттенок красителя меняется от красноватого до
синеватого.
22.
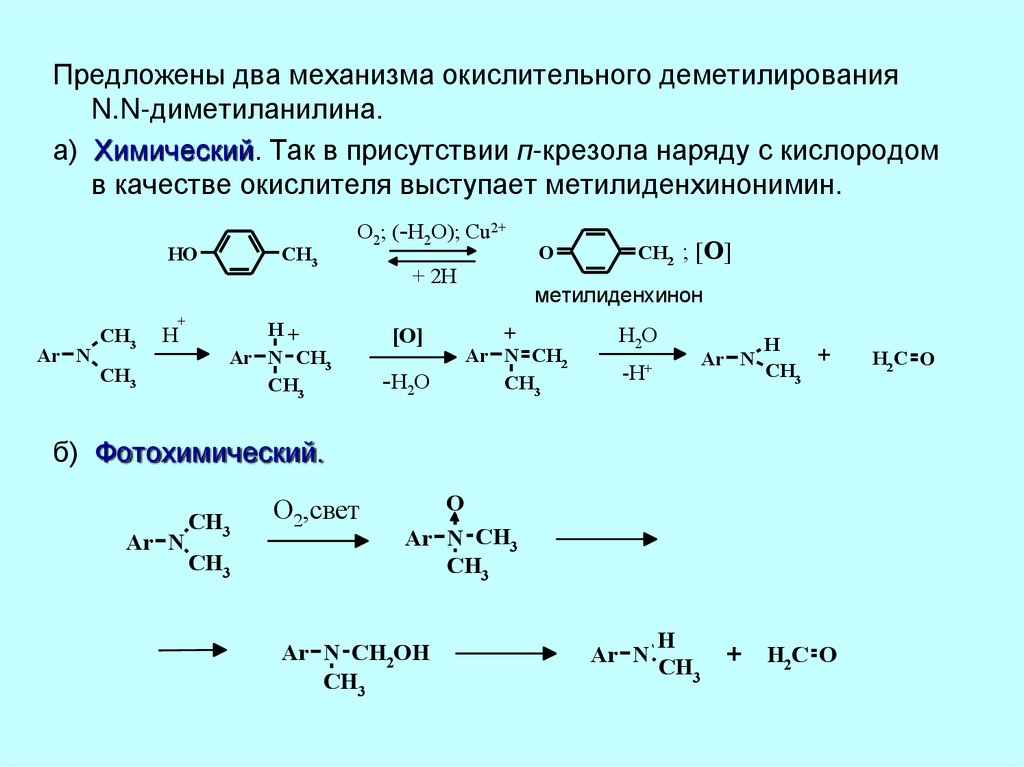
Предложены два механизма окислительного деметилированияN.N-диметиланилина.
а) Химический. Так в присутствии п-крезола наряду с кислородом
в качестве окислителя выступает метилиденхинонимин.
HO
Ar N
CH3
+
H
CH3
CH3
O2; (-H2O); Cu2+
H+
Ar N CH3
CH3
+ 2H
O
метилиденхинон
+
Ar N CH2
CH3
[O]
-H2O
CH2 ; [O]
H2O
-H+
Ar N
H
CH3
+
б) Фотохимический.
Ar N
CH3
CH3
O2,свет
O
Ar N CH3
CH3
Ar N CH2OH
CH3
Ar N
H
CH3
+
H2C O
H2C O
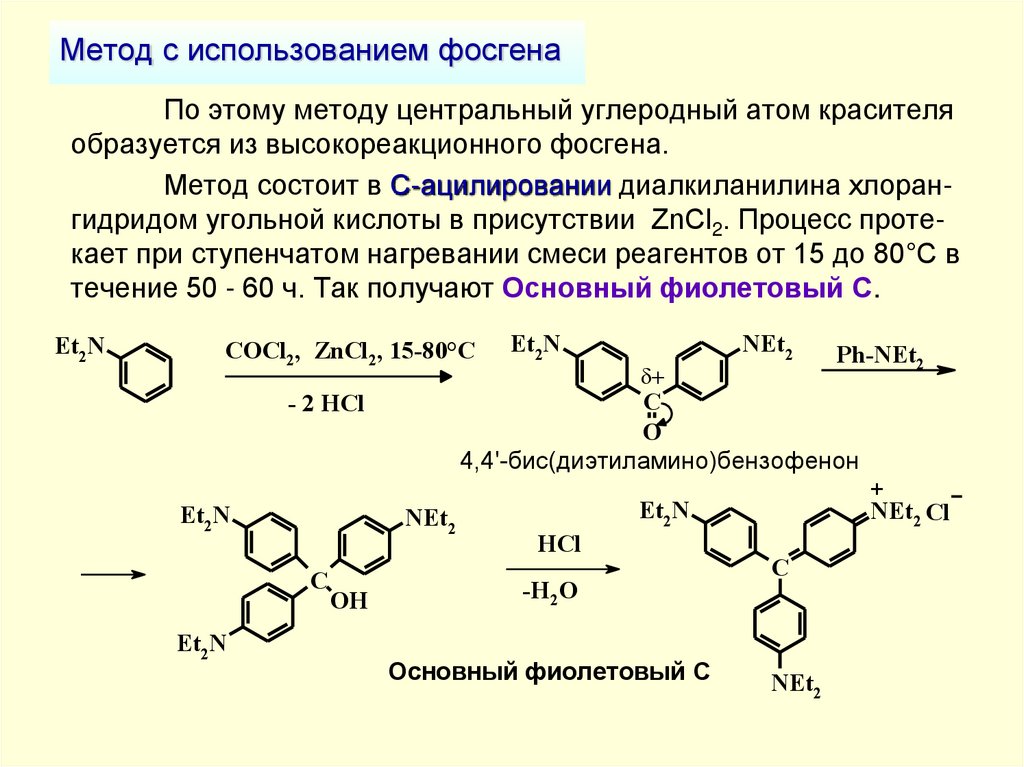
23. Метод с использованием фосгена
По этому методу центральный углеродный атом красителяобразуется из высокореакционного фосгена.
Метод состоит в С-ацилировании диалкиланилина хлорангидридом угольной кислоты в присутствии ZnCl2. Процесс протекает при ступенчатом нагревании смеси реагентов от 15 до 80°С в
течение 50 - 60 ч. Так получают Основный фиолетовый С.
Et2N
COCl2, ZnCl2, 15-80°C
NEt2
C
Et2N
OH
NEt2
Ph-NEt2
C
O
4,4'-бис(диэтиламино)бензофенон
- 2 HCl
Et2N
Et2N
HCl
+
Et2N
-H2O
Основный фиолетовый C
NEt2 Cl
C
NEt2
24.
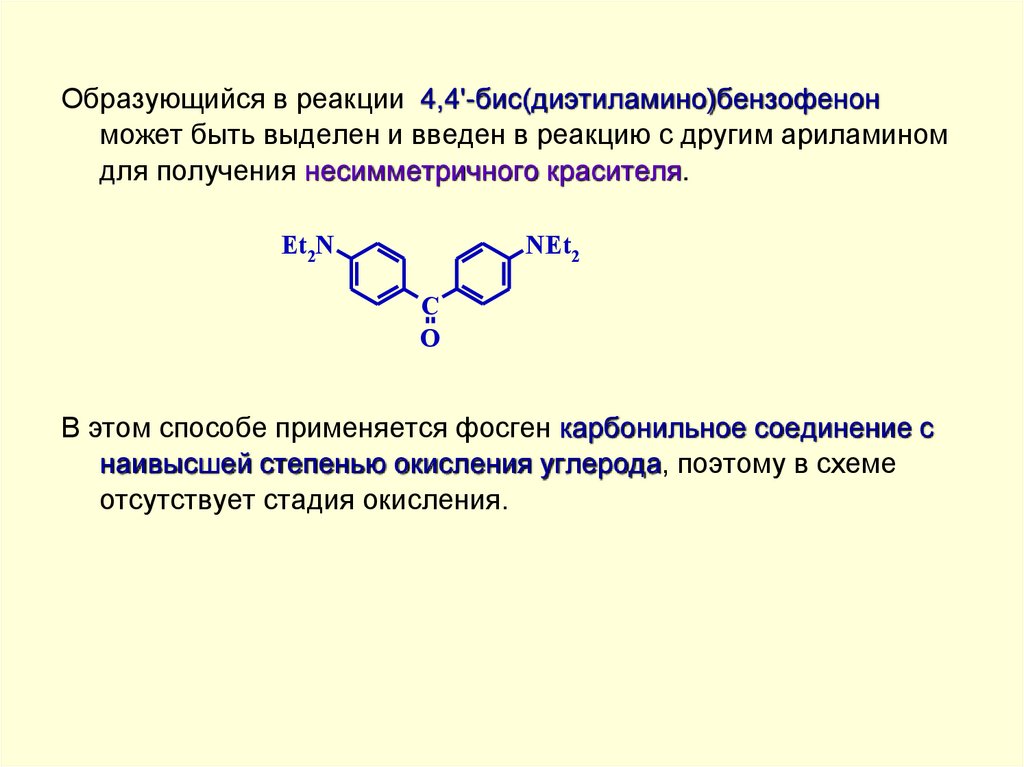
Образующийся в реакции 4,4'-бис(диэтиламино)бензофенонможет быть выделен и введен в реакцию с другим ариламином
для получения несимметричного красителя.
Et2N
NEt2
C
O
В этом способе применяется фосген карбонильное соединение с
наивысшей степенью окисления углерода, поэтому в схеме
отсутствует стадия окисления.
25.
Не огорчайся, я потомтебе всё объясню!
26. 5.2. Собственно арилметановые красители
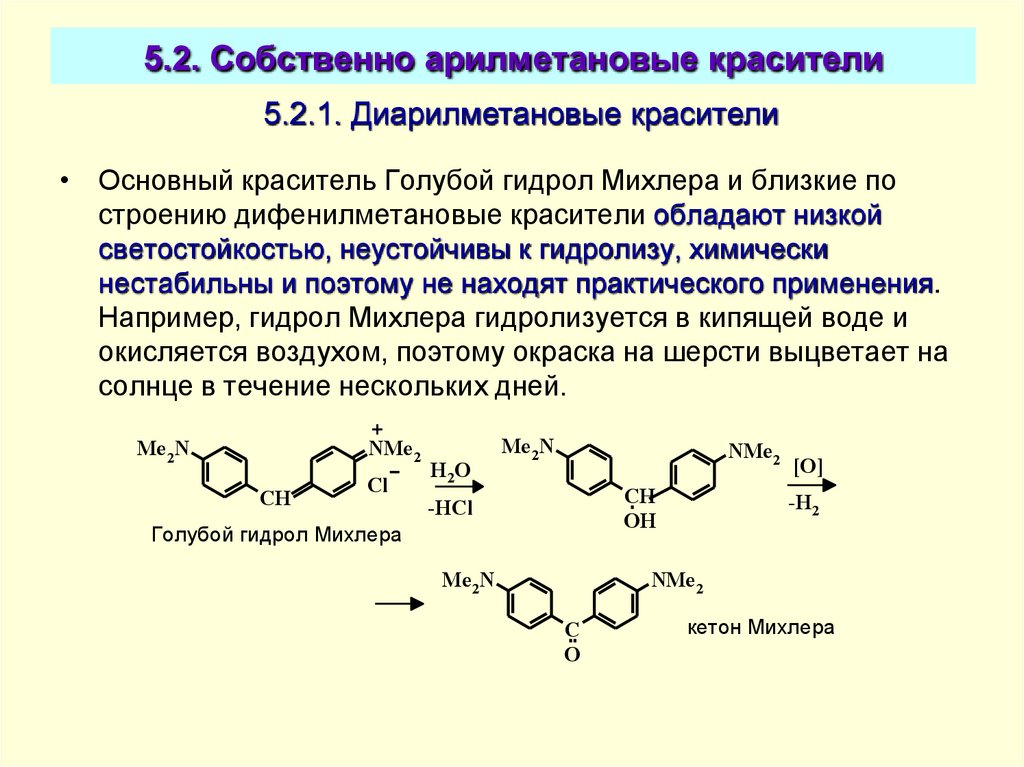
5.2.1. Диарилметановые красители• Основный краситель Голубой гидрол Михлера и близкие по
строению дифенилметановые красители обладают низкой
светостойкостью, неустойчивы к гидролизу, химически
нестабильны и поэтому не находят практического применения.
Например, гидрол Михлера гидролизуется в кипящей воде и
окисляется воздухом, поэтому окраска на шерсти выцветает на
солнце в течение нескольких дней.
+
NMe 2
Me 2N
CH
Cl
H2 O
Me 2N
NMe 2
CH
OH
-HCl
Голубой гидрол Михлера
Me 2N
[O]
-H2
O
NMe 2
C
O
кетон Михлера
27.
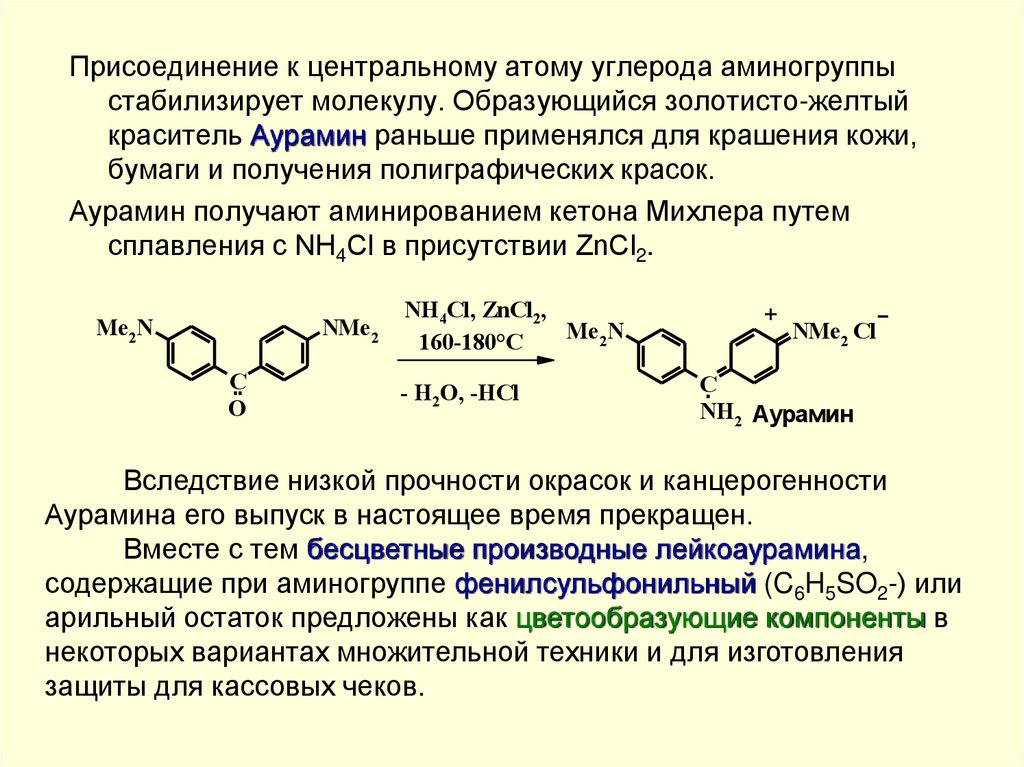
Присоединение к центральному атому углерода аминогруппыстабилизирует молекулу. Образующийся золотисто-желтый
краситель Аурамин раньше применялся для крашения кожи,
бумаги и получения полиграфических красок.
Аурамин получают аминированием кетона Михлера путем
сплавления с NH4Cl в присутствии ZnCl2.
Me 2N
NMe 2
C
O
NH4Cl, ZnCl2,
Me 2N
160-180°C
- H2O, -HCl
+
NMe 2 Cl
C
NH2 Аурамин
Вследствие низкой прочности окрасок и канцерогенности
Аурамина его выпуск в настоящее время прекращен.
Вместе с тем бесцветные производные лейкоаурамина,
содержащие при аминогруппе фенилсульфонильный (C6H5SO2-) или
арильный остаток предложены как цветообразующие компоненты в
некоторых вариантах множительной техники и для изготовления
защиты для кассовых чеков.
28.
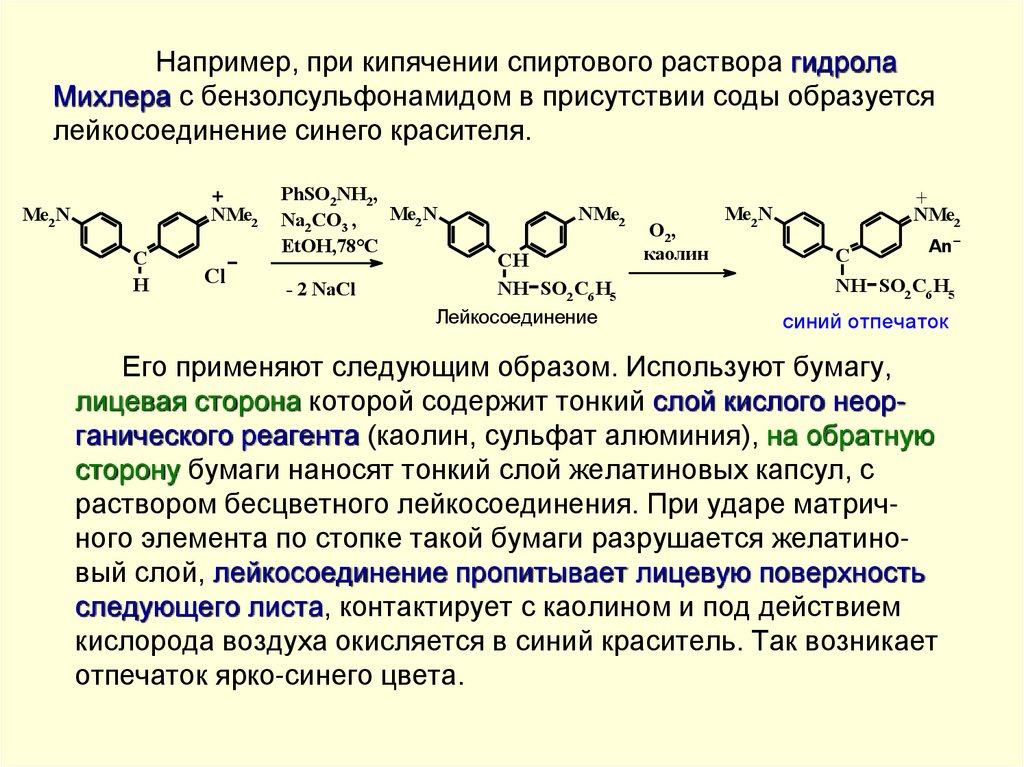
Например, при кипячении спиртового раствора гидролаМихлера с бензолсульфонамидом в присутствии соды образуется
лейкосоединение синего красителя.
+
Me2 N
NMe2
C
H
Cl
PhSO2NH2,
Me2 N
Na2CO3 ,
EtOH,78°C
- 2 NaCl
NMe2
CH
NH SO2 C6 H5
Лейкосоединение
O2,
каолин
+
Me2 N
NMe2
C
An-
NH SO2 C6 H5
синий отпечаток
Его применяют следующим образом. Используют бумагу,
лицевая сторона которой содержит тонкий слой кислого неорганического реагента (каолин, сульфат алюминия), на обратную
сторону бумаги наносят тонкий слой желатиновых капсул, с
раствором бесцветного лейкосоединения. При ударе матричного элемента по стопке такой бумаги разрушается желатиновый слой, лейкосоединение пропитывает лицевую поверхность
следующего листа, контактирует с каолином и под действием
кислорода воздуха окисляется в синий краситель. Так возникает
отпечаток ярко-синего цвета.
29. 5.2.2. Триарилметановые красители
Усложнение молекулярной и хромофорной системы, которое происходит при переходе от диарилметановых к триарилметановымкрасителям,
сопровождается общим повышением химической и фотохимической стабильности молекул и соответственно улучшением
прочностных показателей получаемых окрасок;
создает больше возможностей для синтеза красителей с полноразмерной гаммой цветов от желтого до зеленого, что достигается путем изменения размеров -системы третьего арильного
остатка и регулированием величины электронных эффектов и
числа поляризующих заместителей в молекуле;
позволяет изменять технические свойства красителей за счет
введения в триарилметановые красители различных функциональных групп и получать основные, кислотные, хромовые,
спирторастворимые красители, пигменты и лаки, обладающие
исключительной яркостью и чистотой цвета.
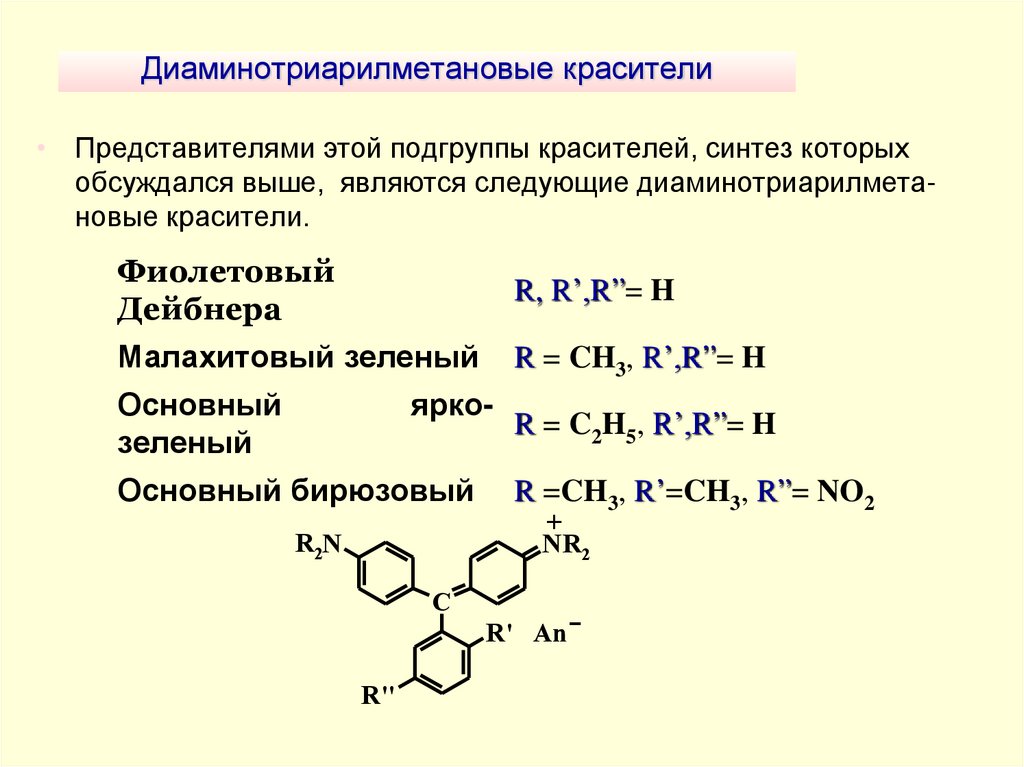
30. Диаминотриарилметановые красители
• Представителями этой подгруппы красителей, синтез которыхобсуждался выше, являются следующие диаминотриарилметановые красители.
Фиолетовый
Дейбнера
R, R’,R”= H
Малахитовый зеленый
R = CH3, R’,R”= H
Основный
зеленый
R = C2H5, R’,R”= H
ярко-
Основный бирюзовый
R2N
C
R"
R =CH3, R’=CH3, R”= NO2
+
N R2
R' An-
31.
• Красители не содержат кислотные группы, поэтому при растворении в воде они диссоциируют с образованием окрашенныхкатионов и относятся к числу основных красителей. Их выпускают в виде солей: гидрохлоридов, сульфатов, оксалатов или
двойных солей хлоридов с ZnCl2.
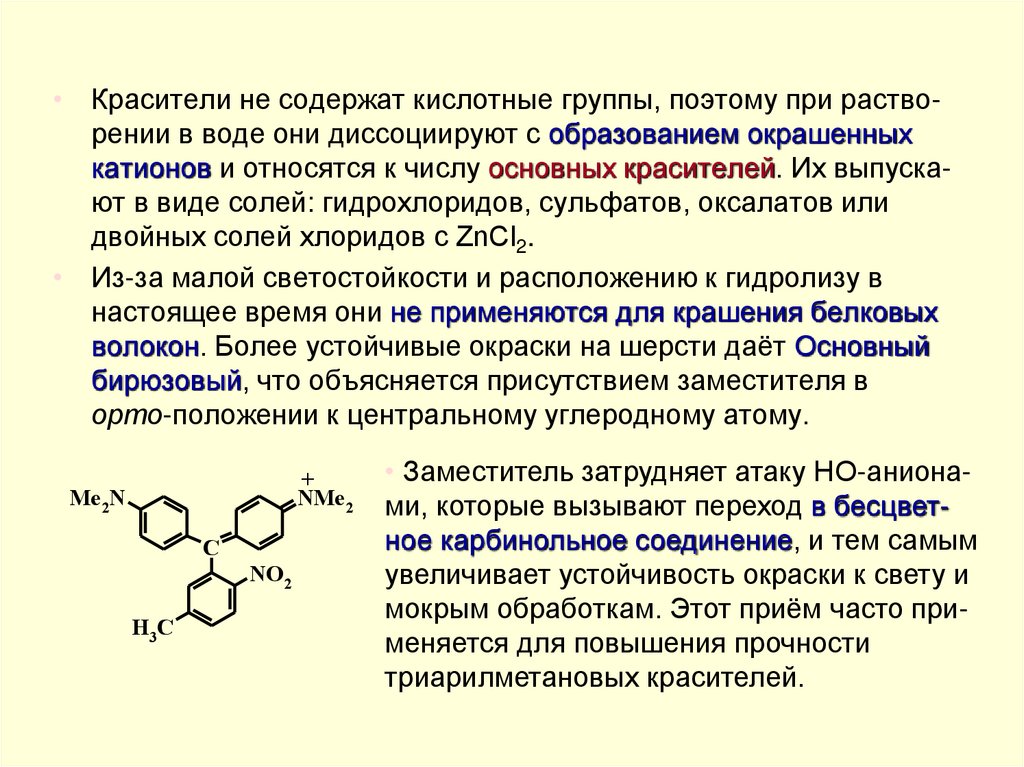
• Из-за малой светостойкости и расположению к гидролизу в
настоящее время они не применяются для крашения белковых
волокон. Более устойчивые окраски на шерсти даёт Основный
бирюзовый, что объясняется присутствием заместителя в
орто-положении к центральному углеродному атому.
+
NMe 2
Me 2N
C
NO2
H3C
• Заместитель затрудняет атаку НО-анионами, которые вызывают переход в бесцветное карбинольное соединение, и тем самым
увеличивает устойчивость окраски к свету и
мокрым обработкам. Этот приём часто применяется для повышения прочности
триарилметановых красителей.
32.
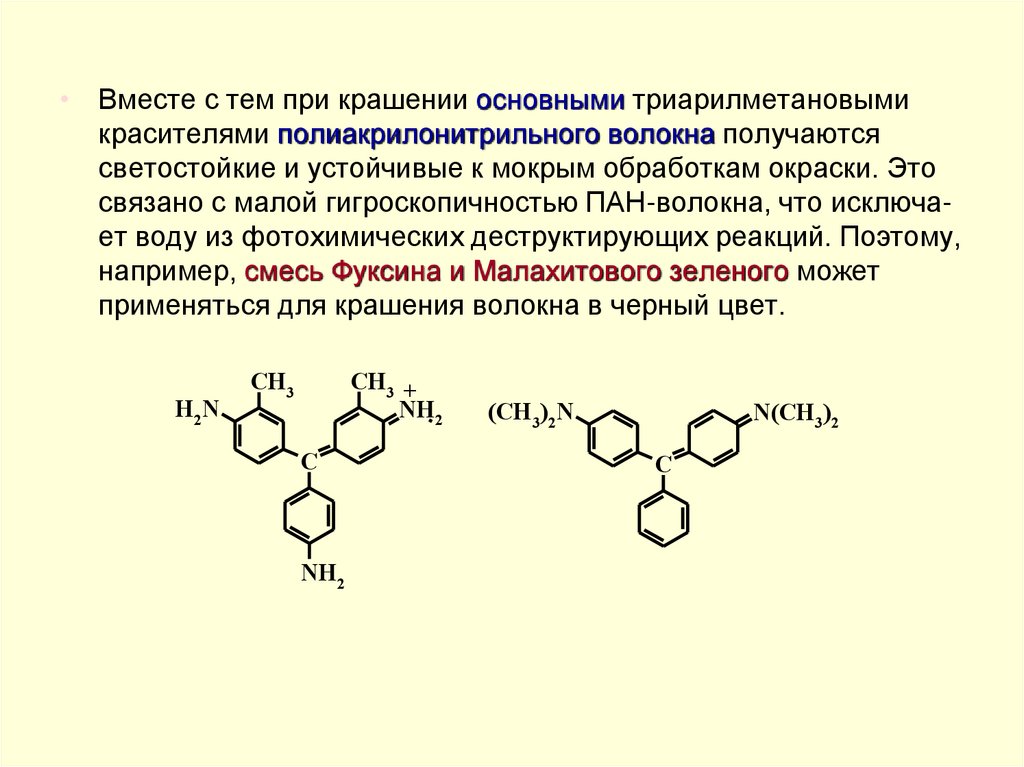
• Вместе с тем при крашении основными триарилметановымикрасителями полиакрилонитрильного волокна получаются
светостойкие и устойчивые к мокрым обработкам окраски. Это
связано с малой гигроскопичностью ПАН-волокна, что исключает воду из фотохимических деструктирующих реакций. Поэтому,
например, смесь Фуксина и Малахитового зеленого может
применяться для крашения волокна в черный цвет.
H2N
CH3 +
NH2
CH3
C
NH2
(CH3)2N
N(CH3)2
C
33.
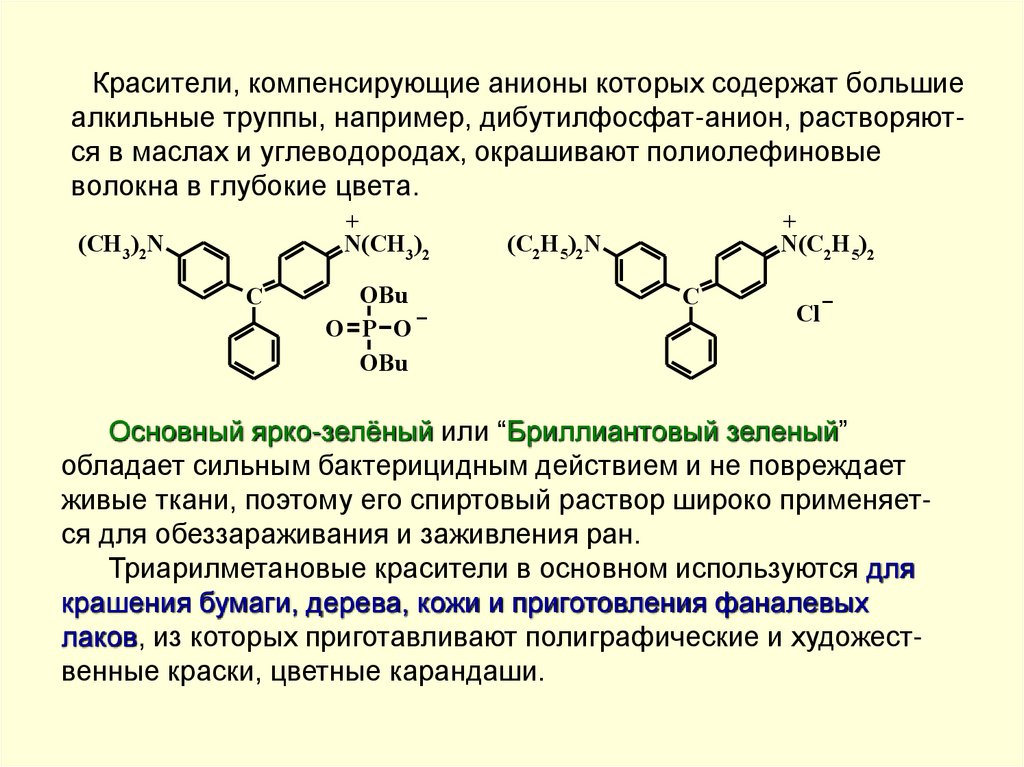
Красители, компенсирующие анионы которых содержат большиеалкильные труппы, например, дибутилфосфат-анион, растворяются в маслах и углеводородах, окрашивают полиолефиновые
волокна в глубокие цвета.
+
N(CH 3)2
(CH 3)2N
C
OBu
O P OOBu
+
N(C2H5)2
(C2H5)2N
C
Cl
-
Основный ярко-зелёный или “Бриллиантовый зеленый”
обладает сильным бактерицидным действием и не повреждает
живые ткани, поэтому его спиртовый раствор широко применяется для обеззараживания и заживления ран.
Триарилметановые красители в основном используются для
крашения бумаги, дерева, кожи и приготовления фаналевых
лаков, из которых приготавливают полиграфические и художественные краски, цветные карандаши.
34.
Фаналевые лаки - нерастворимые в воде кислые соли основных триарилметановых красителей с гетерополикислотами фофсофорномолибденовой, H7P(Mo2O7)6,фосфорновольфрамовой, H7P(W2O7)6 ,
кремнемолибденовой, H8Si(Mo2O7)6 или их смесей.
Такие лаки образуются при внесении раствора рассчитанного
количества гетерополикислоты в почти кипящий водный
раствор красителя.
вода, 100°C
+
4 Kp=NR2 Cl
+
H7P(Mo2O7)6
+
4
(Kp=NR2)4 H3 P(Mo2O7)6 + 4 HCl
фаналевый лак
Фаналевые лаки отличаются высокой светостойкостью и
сохраняют чистоту и яркость оттенка присущие трифенилметанвым красителям.
35.
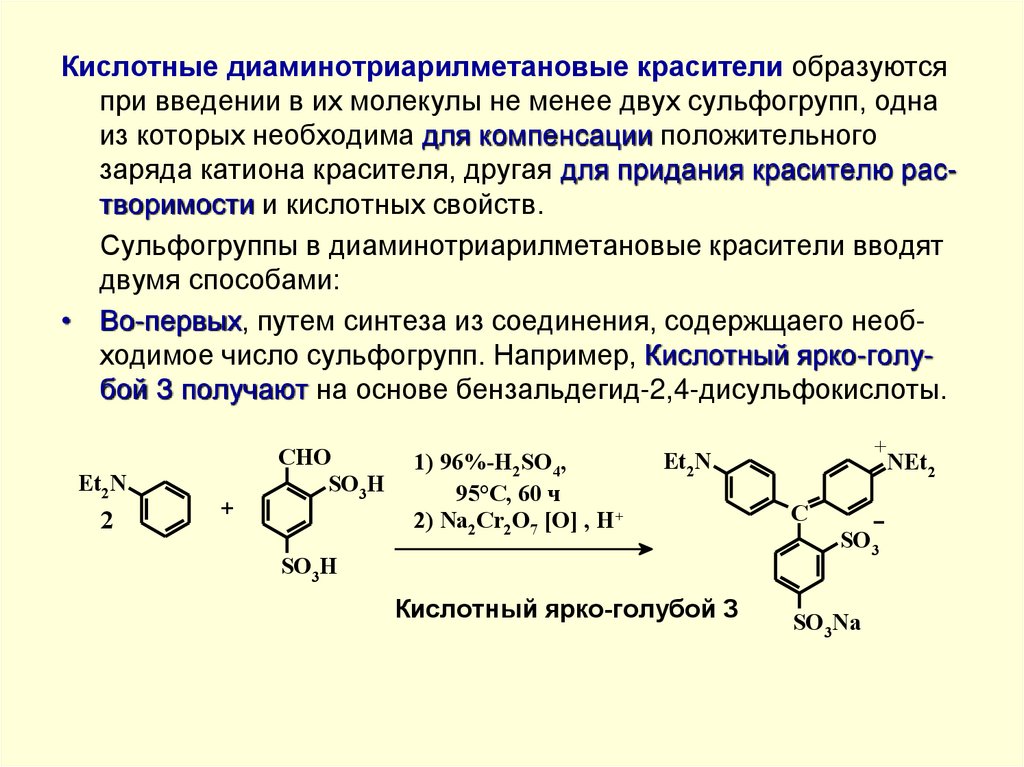
Кислотные диаминотриарилметановые красители образуютсяпри введении в их молекулы не менее двух сульфогрупп, одна
из которых необходима для компенсации положительного
заряда катиона красителя, другая для придания красителю растворимости и кислотных свойств.
Сульфогруппы в диаминотриарилметановые красители вводят
двумя способами:
• Во-первых, путем синтеза из соединения, содержщаего необходимое число сульфогрупп. Например, Кислотный ярко-голубой З получают на основе бензальдегид-2,4-дисульфокислоты.
Et2N
2
+
CHO
SO3H
1) 96%-H2SO4,
95°C, 60 ч
2) Na2Cr2O7 [O] , H+
+
Et2N
SO3H
Кислотный ярко-голубой З
NEt2
C
SO3
SO3Na
36.
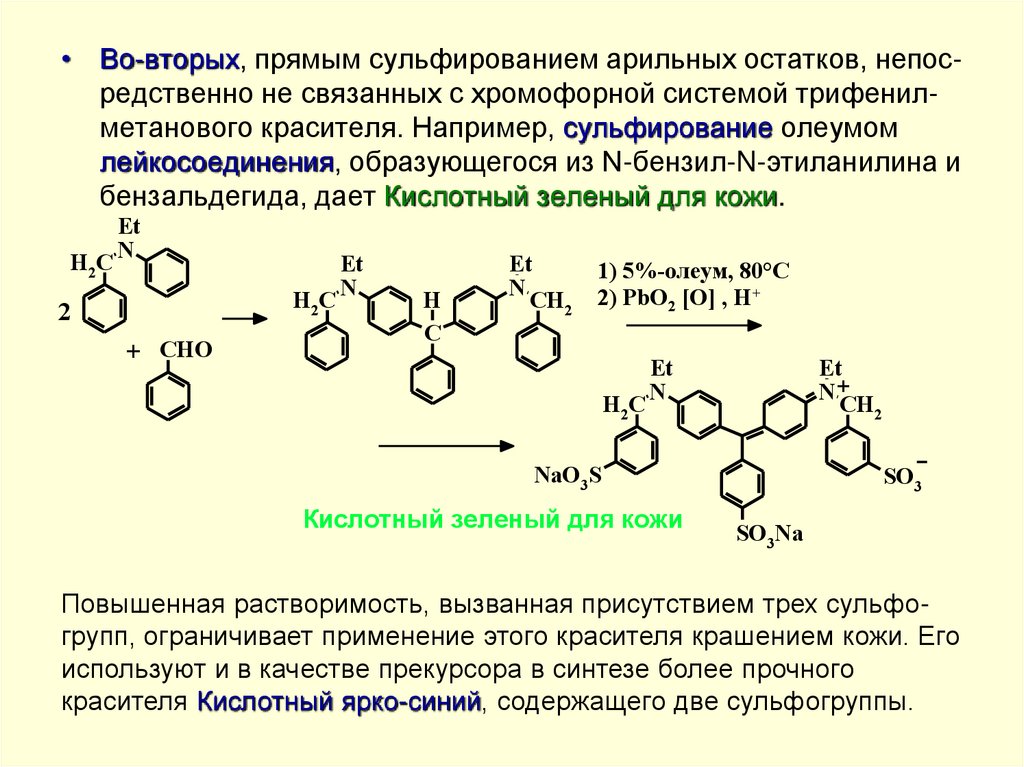
• Во-вторых, прямым сульфированием арильных остатков, непосредственно не связанных с хромофорной системой трифенилметанового красителя. Например, сульфирование олеумомлейкосоединения, образующегося из N-бензил-N-этиланилина и
бензальдегида, дает Кислотный зеленый для кожи.
H2C
Et
N
H2C
2
+ CHO
Et
N
H
C
Et
N
CH2
1) 5%-олеум, 80°C
2) PbO2 [O] , H+
H2C
Et
N+
CH2
Et
N
NaO3S
Кислотный зеленый для кожи
SO3
SO3Na
Повышенная растворимость, вызванная присутствием трех сульфогрупп, ограничивает применение этого красителя крашением кожи. Его
используют и в качестве прекурсора в синтезе более прочного
красителя Кислотный ярко-синий, содержащего две сульфогруппы.
37.
Внутрикошачье смешение цветов38. Триаминотриарилметановые красители
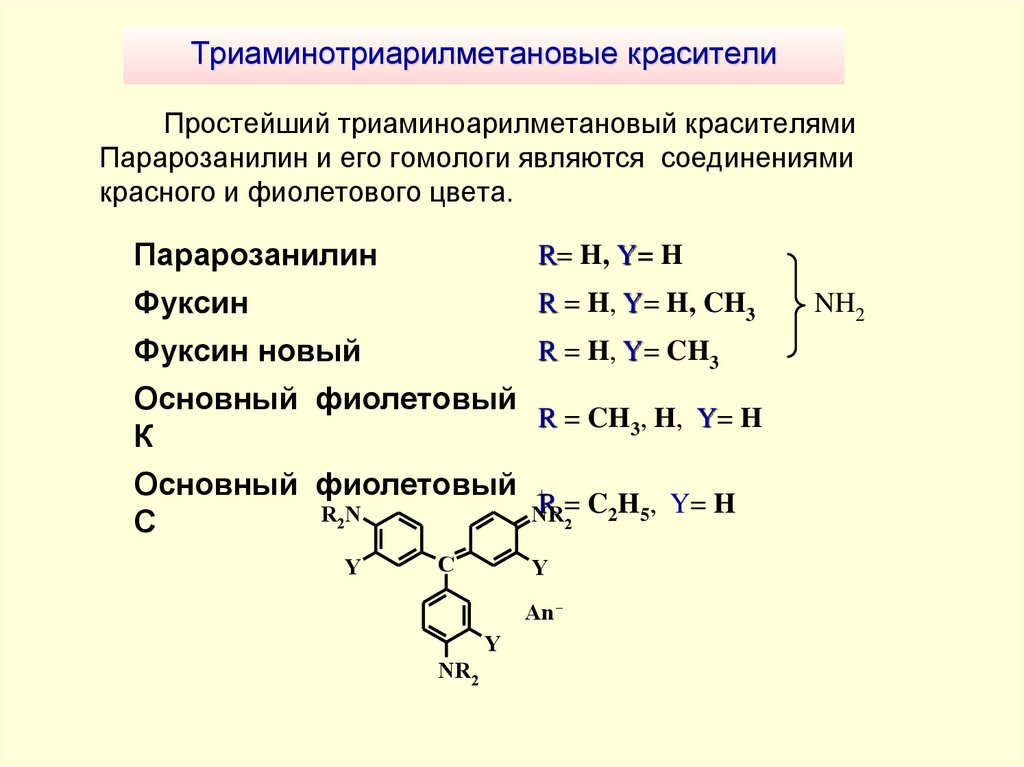
Простейший триаминоарилметановый красителямиПарарозанилин и его гомологи являются соединениями
красного и фиолетового цвета.
Парарозанилин
R= H, Y= H
Фуксин
R = H, Y= H, CH3
Фуксин новый
R = H, Y= CH3
Основный фиолетовый
R = CH3, H, Y= H
К
Основный фиолетовый +
R = C2H5, Y= H
R2N
NR
2
С
Y
C
Y
AnY
NR2
NH2
39.
• Эти основные красители получают по схемам бензальдегидногои формальдегидного метода, а также с использованием фосгена.
• Все эти красители близки по свойствам, окрашивают шерсть и
шелк в яркие и красивые цвета, но окраски отличаются низкой
светостойкостью и устойчивостью к внешним воздействиям.
• Поэтому они используются в основном для крашения бумаги,
кожи, приготовления чернил, спиртовых лаков, копировальной
бумаги и фаналевых лаков для полиграфии.
• Благодаря отчетливым цветовым переходам при изменении рН
среды некоторые триаминотриарилметановые красители
применяются в качестве индикаторов в ацидометрии.
• Для получения красителей более глубокого цвета и повышения
прочностных показателей к мокрым обработкам в аминогруппы
вводят вместо алкильных арильные остатки.
40.
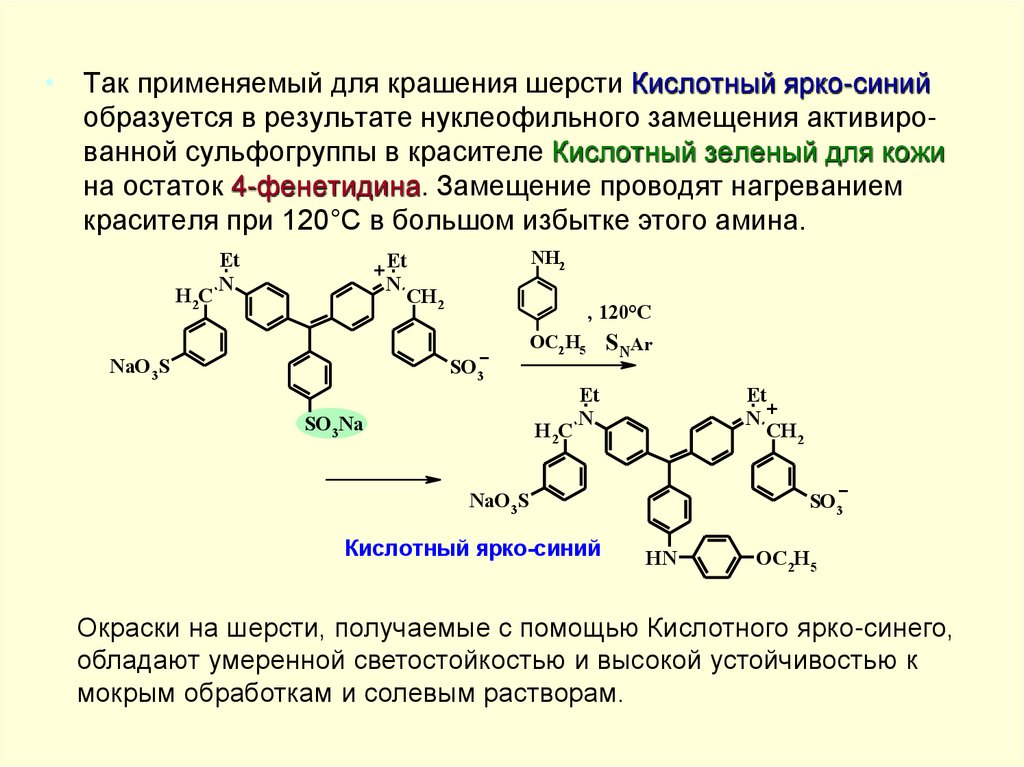
• Так применяемый для крашения шерсти Кислотный ярко-синийобразуется в результате нуклеофильного замещения активированной сульфогруппы в красителе Кислотный зеленый для кожи
на остаток 4-фенетидина. Замещение проводят нагреванием
красителя при 120°С в большом избытке этого амина.
H2C
Et
N
+
NH2
Et
N
CH2
, 120°C
SO -
NaO3S
OC2 H5
3
SO3Na
H2C
SNAr
Et
N
Et
N+
CH2
SO 3
NaO3S
Кислотный ярко-синий
HN
OC2H5
Окраски на шерсти, получаемые с помощью Кислотного ярко-синего,
обладают умеренной светостойкостью и высокой устойчивостью к
мокрым обработкам и солевым растворам.
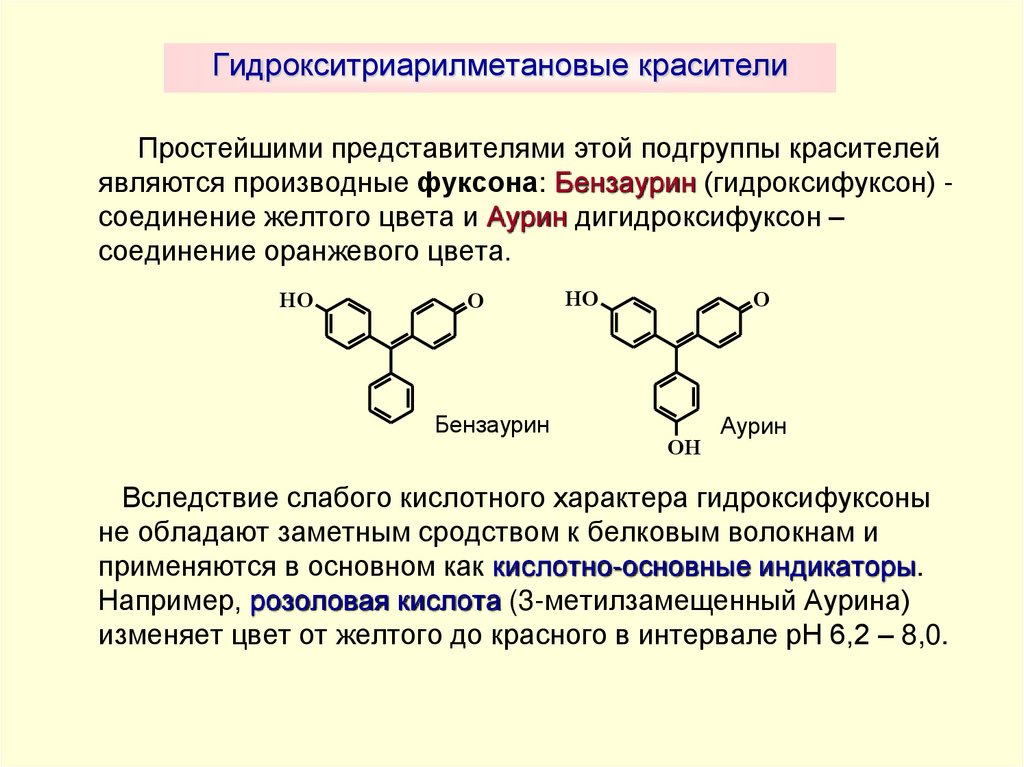
41. Гидрокситриарилметановые красители
Простейшими представителями этой подгруппы красителейявляются производные фуксона: Бензаурин (гидроксифуксон) соединение желтого цвета и Аурин дигидроксифуксон –
соединение оранжевого цвета.
HO
O
Бензаурин
HO
O
OH
Аурин
Вследствие слабого кислотного характера гидроксифуксоны
не обладают заметным сродством к белковым волокнам и
применяются в основном как кислотно-основные индикаторы.
Например, розоловая кислота (3-метилзамещенный Аурина)
изменяет цвет от желтого до красного в интервале рН 6,2 – 8,0.
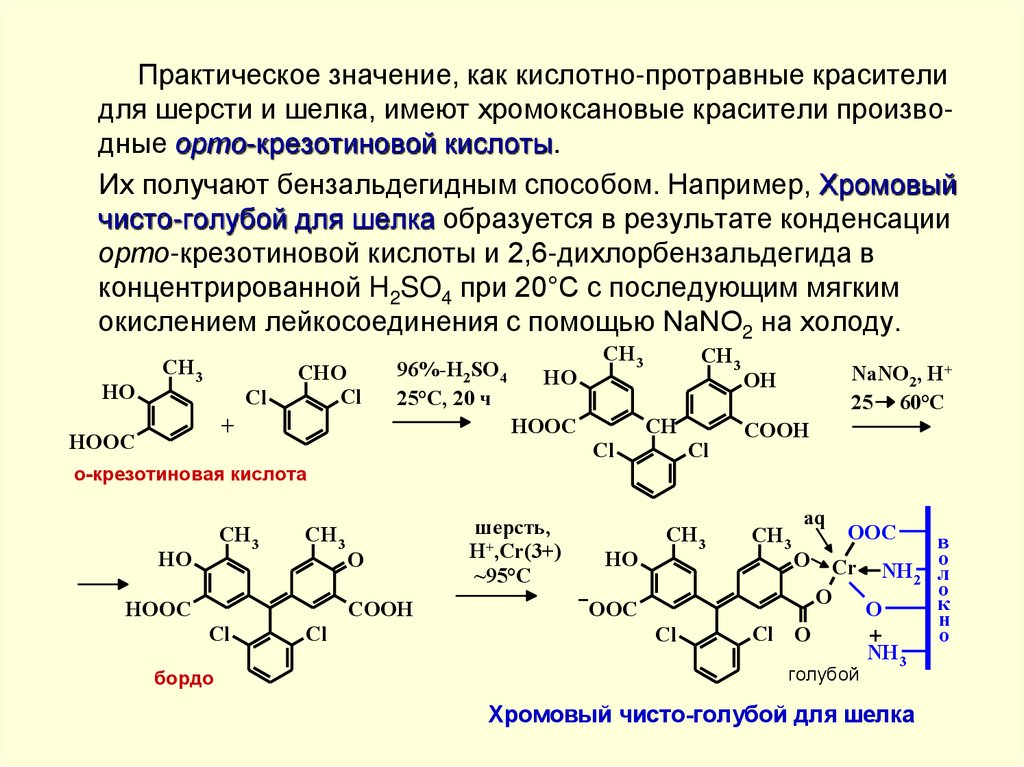
42.
Практическое значение, как кислотно-протравные красителидля шерсти и шелка, имеют хромоксановые красители производные орто-крезотиновой кислоты.
Их получают бензальдегидным способом. Например, Хромовый
чисто-голубой для шелка образуется в результате конденсации
орто-крезотиновой кислоты и 2,6-дихлорбензальдегида в
концентрированной H2SO4 при 20°С с последующим мягким
окислением лейкосоединения с помощью NaNO2 на холоду.
HO
CH3
Cl
CHO
Cl
96%-H2SO4
25°C, 20 ч
+
HOOC
HO
CH3
HOOC
CH3
CH
Cl
Cl
NaNO2, H+
25 60°C
OH
COOH
о-крезотиновая кислота
CH3
HO
CH3
HOOC
O
COOH
Cl
бордо
Cl
шерсть,
H+,Cr(3+)
~95°C
HO
CH3
CH3
aq
O
OOC
Cr
O
-OOC
Cl
Cl O
голубой
NH2
O
+
NH3
Хромовый чисто-голубой для шелка
в
о
л
о
к
н
о
43.
При комплексообразовании краситель прочно сорбируетсяволокном из-за утраты растворимости (лак) и связывания с
функциональными группами волокна через атом Cr, который
координируется как с красителем, так и белковой макромолекулой. Поэтому получаемые окраски и отличаются высокой
прочностью к мокрым обработкам и светопогоде.
Хромирование хромоксановых красителей из группы ортокрезотиновой кислоты сопровождается значительным углублением окраски.
Красители более высокого цвета образуются при введении
в пара-положение третьего кольца NC2H5- (синий) или NHPhгруппы (фиолетовый).
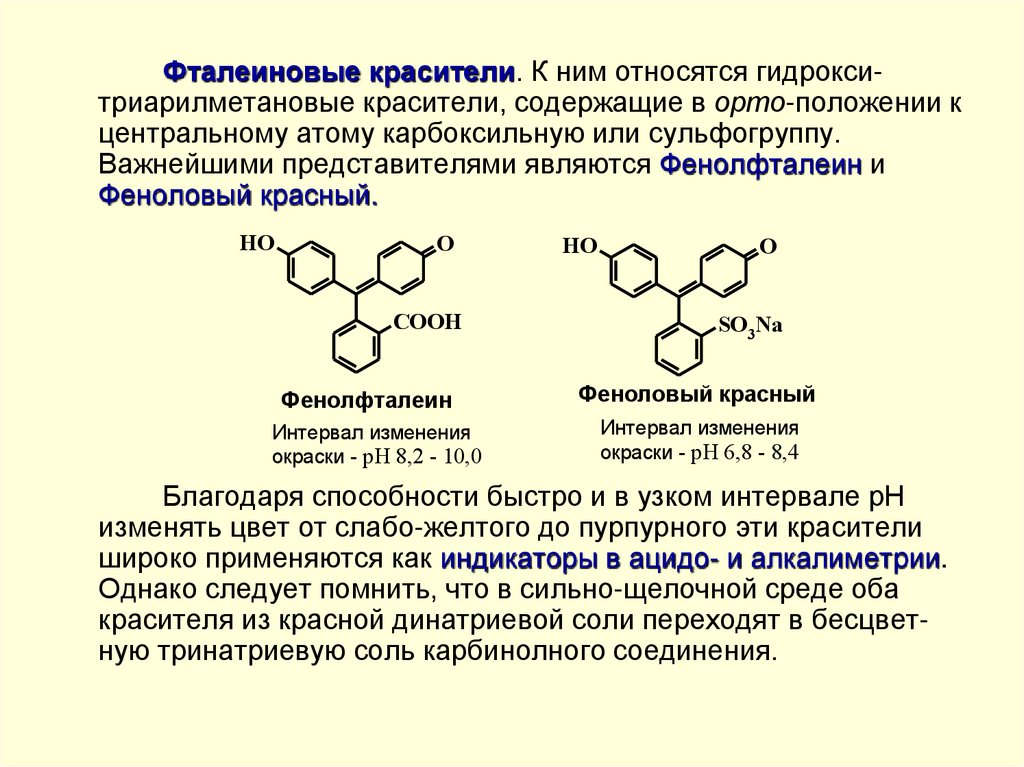
44.
Фталеиновые красители. К ним относятся гидрокситриарилметановые красители, содержащие в орто-положении кцентральному атому карбоксильную или сульфогруппу.
Важнейшими представителями являются Фенолфталеин и
Феноловый красный.
HO
O
COOH
HO
O
SO3Na
Фенолфталеин
Феноловый красный
Интервал изменения
окраски - pH 8,2 - 10,0
Интервал изменения
окраски - pH 6,8 - 8,4
Благодаря способности быстро и в узком интервале рН
изменять цвет от слабо-желтого до пурпурного эти красители
широко применяются как индикаторы в ацидо- и алкалиметрии.
Однако следует помнить, что в сильно-щелочной среде оба
красителя из красной динатриевой соли переходят в бесцветную тринатриевую соль карбинолного соединения.
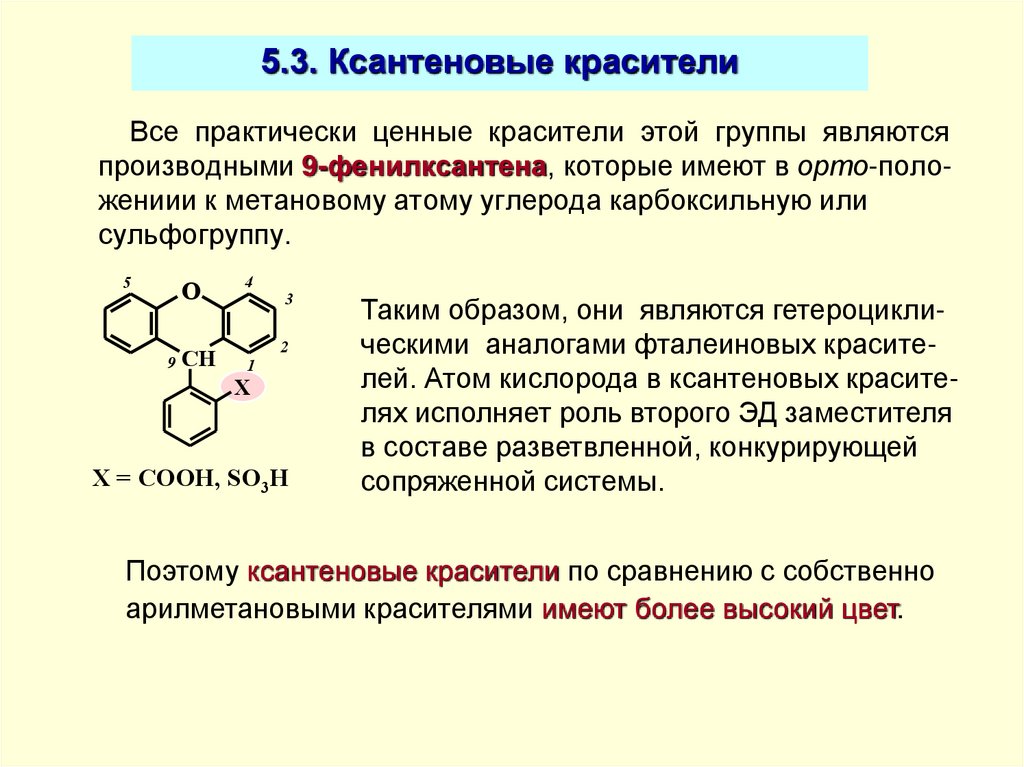
45. 5.3. Ксантеновые красители
Все практически ценные красители этой группы являютсяпроизводными 9-фенилксантена, которые имеют в орто-положениии к метановому атому углерода карбоксильную или
сульфогруппу.
5
O
9 CH
4
1
3
2
X
X = COOH, SO3H
Таким образом, они являются гетероциклическими аналогами фталеиновых красителей. Атом кислорода в ксантеновых красителях исполняет роль второго ЭД заместителя
в составе разветвленной, конкурирующей
сопряженной системы.
Поэтому ксантеновые красители по сравнению с собственно
арилметановыми красителями имеют более высокий цвет.
46. Дигидроксиксантеновые красители
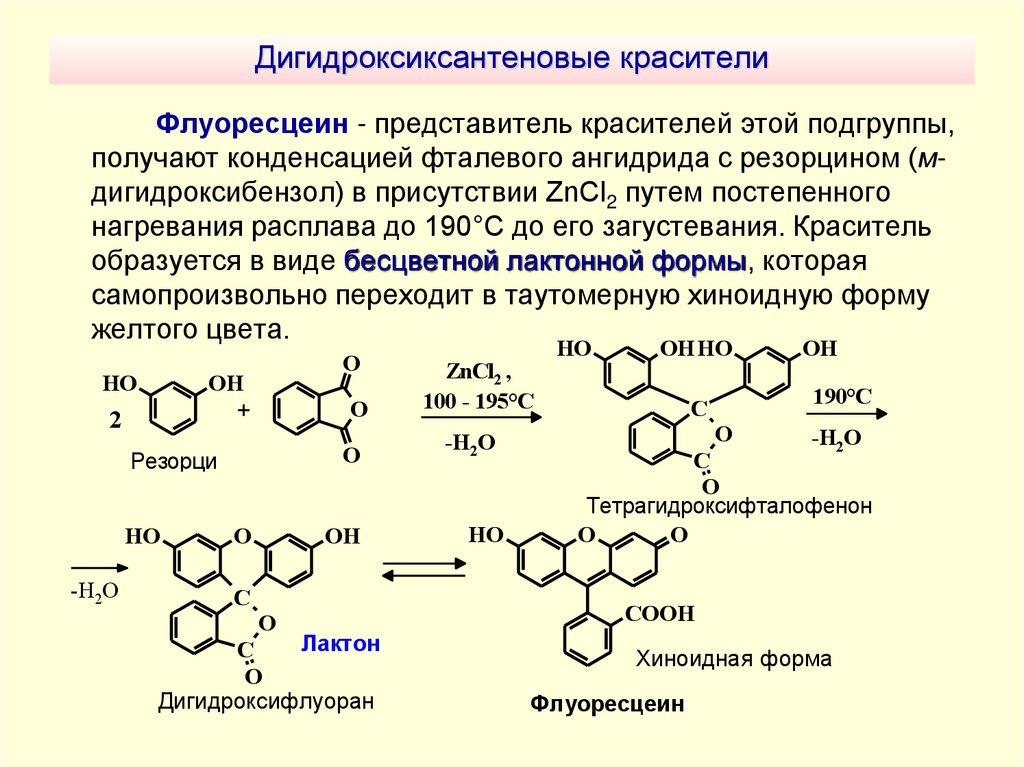
Флуоресцеин - представитель красителей этой подгруппы,получают конденсацией фталевого ангидрида с резорцином (мдигидроксибензол) в присутствии ZnCl2 путем постепенного
нагревания расплава до 190°С до его загустевания. Краситель
образуется в виде бесцветной лактонной формы, которая
самопроизвольно переходит в таутомерную хиноидную форму
желтого цвета.
HO
OH
2
+
O
Резорци
HO
-H2O
O
O
ZnCl2 ,
100 - 195°C
O
-H2O
OH
HO
C
O
Лактон
C
O
Дигидроксифлуоран
HO
OH HO
OH
190°C
C
O
-H2O
C
O
Тетрагидроксифталофенон
O
O
COOH
Хиноидная форма
Флуоресцеин
47.
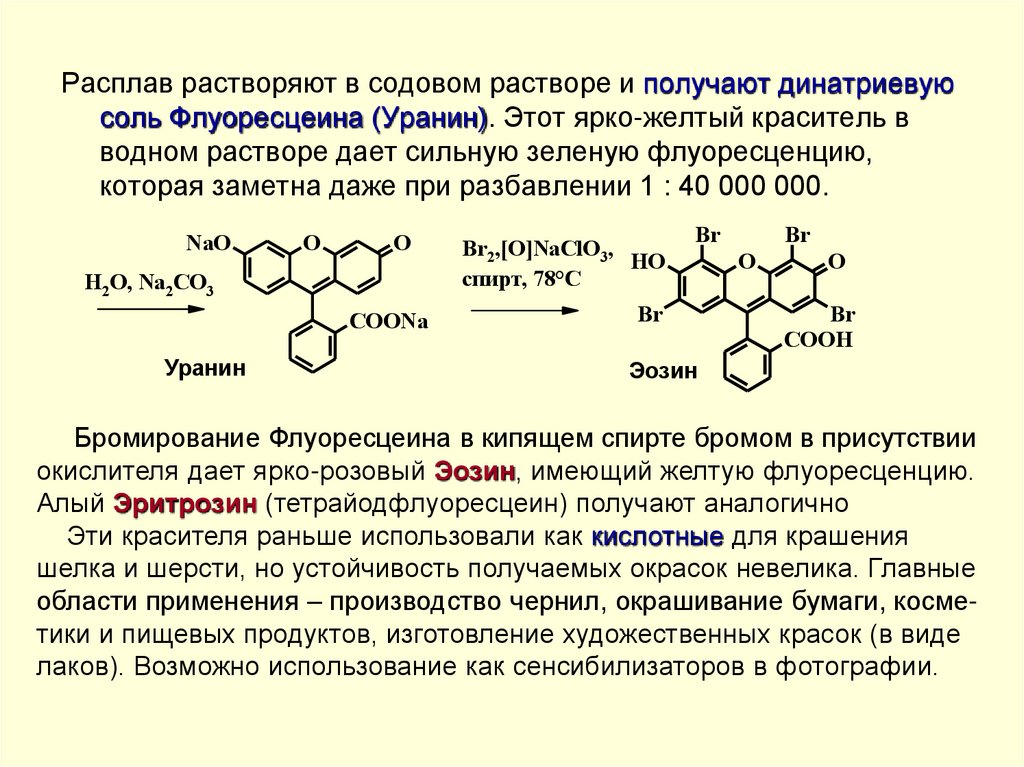
Расплав растворяют в содовом растворе и получают динатриевуюсоль Флуоресцеина (Уранин). Этот ярко-желтый краситель в
водном растворе дает сильную зеленую флуоресценцию,
которая заметна даже при разбавлении 1 : 40 000 000.
NaO
O
O
H2O, Na2CO3
COONa
Уранин
Br2,[O]NaClO3,
HO
спирт, 78°С
Br
Br
Br
O
O
Br
COOH
Эозин
Бромирование Флуоресцеина в кипящем спирте бромом в присутствии
окислителя дает ярко-розовый Эозин, имеющий желтую флуоресценцию.
Алый Эритрозин (тетрайодфлуоресцеин) получают аналогично
Эти красителя раньше использовали как кислотные для крашения
шелка и шерсти, но устойчивость получаемых окрасок невелика. Главные
области применения – производство чернил, окрашивание бумаги, косметики и пищевых продуктов, изготовление художественных красок (в виде
лаков). Возможно использование как сенсибилизаторов в фотографии.
48. Диаминоксантеновые красители
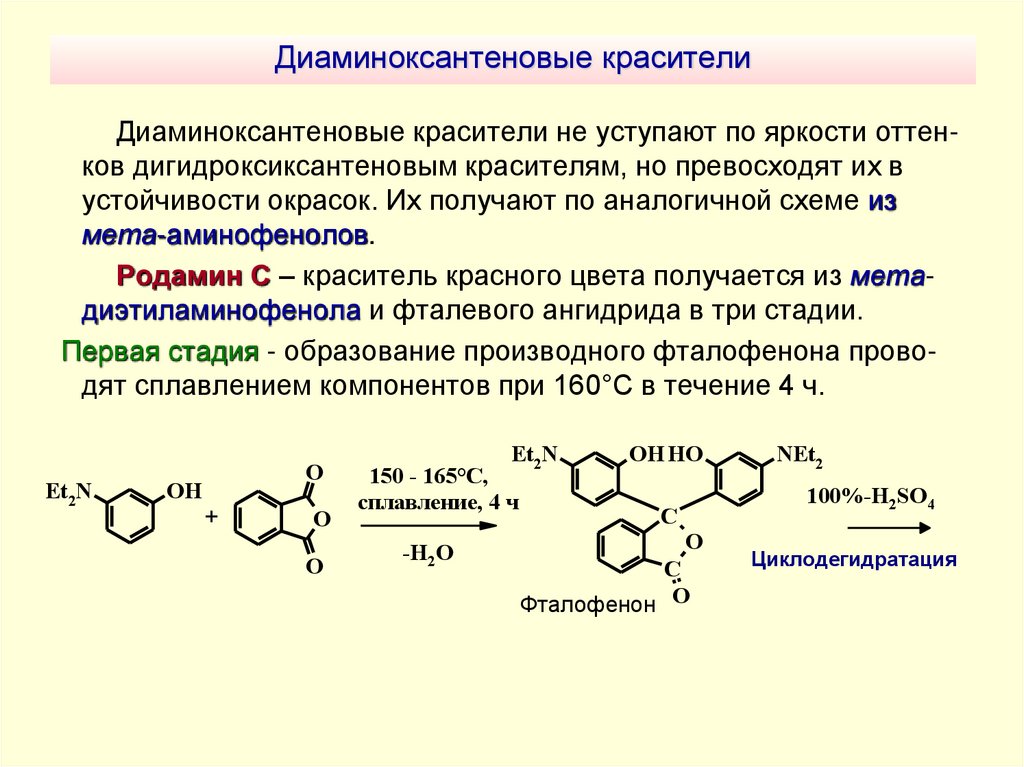
Диаминоксантеновые красители не уступают по яркости оттенков дигидроксиксантеновым красителям, но превосходят их вустойчивости окрасок. Их получают по аналогичной схеме из
мета-аминофенолов.
Родамин С – краситель красного цвета получается из метадиэтиламинофенола и фталевого ангидрида в три стадии.
Первая стадия - образование производного фталофенона проводят сплавлением компонентов при 160°С в течение 4 ч.
Et2N
OH
O
+
O
O
Et2N
150 - 165°C,
сплавление, 4 ч
-H2O
OH HO
NEt2
100%-H2SO4
C
O
C
Фталофенон O
Циклодегидратация
49.
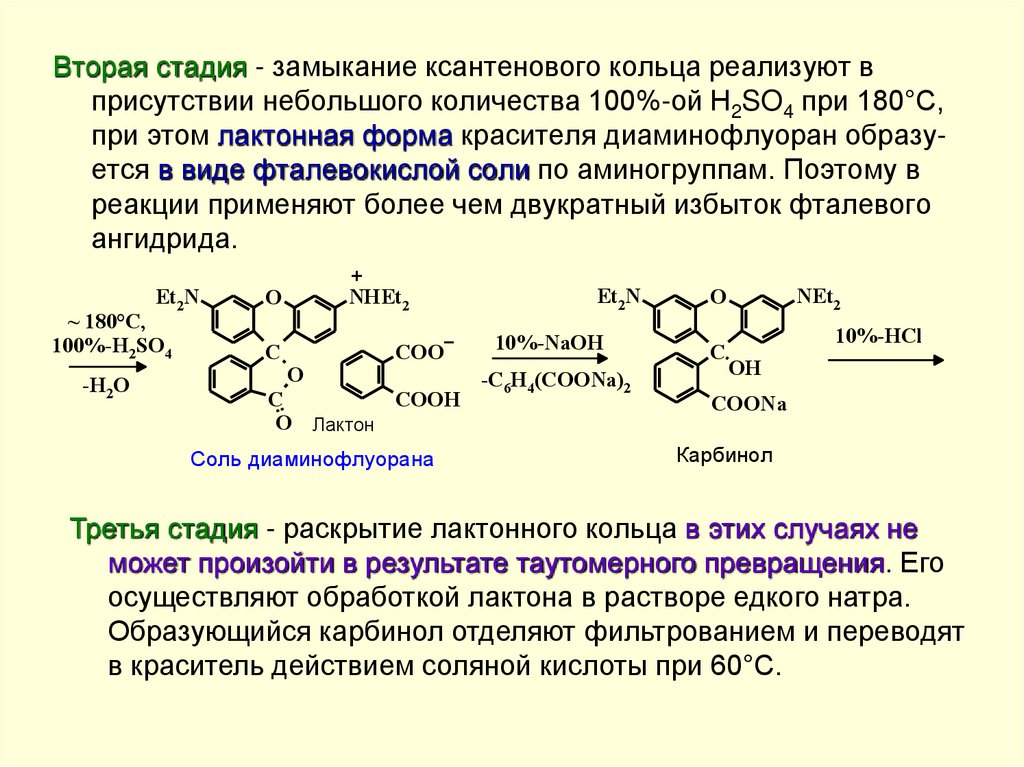
Вторая стадия - замыкание ксантенового кольца реализуют вприсутствии небольшого количества 100%-ой H2SO4 при 180°С,
при этом лактонная форма красителя диаминофлуоран образуется в виде фталевокислой соли по аминогруппам. Поэтому в
реакции применяют более чем двукратный избыток фталевого
ангидрида.
Et2N
~ 180°C,
100%-H2SO4
,
-H2O
+
NHEt2
O
C
O
COO
C
COOH
O Лактон
Соль диаминофлуорана
Et2N
10%-NaOH
-С6H4(COONa)2
NEt2
O
C
10%-HCl
OH
COONa
Карбинол
Третья стадия - раскрытие лактонного кольца в этих случаях не
может произойти в результате таутомерного превращения. Его
осуществляют обработкой лактона в растворе едкого натра.
Образующийся карбинол отделяют фильтрованием и переводят
в краситель действием соляной кислоты при 60°С.
50.
Et2NO
+
NEt2 Cl
10%-HCl
-H2O
COOH
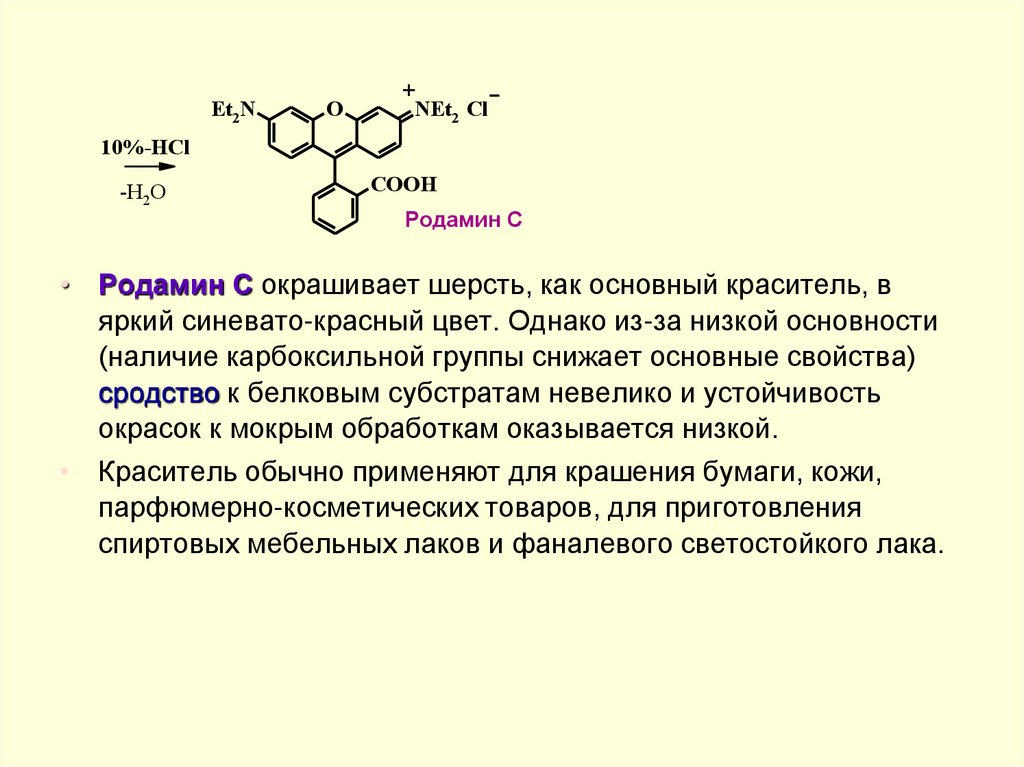
Родамин С
• Родамин С окрашивает шерсть, как основный краситель, в
яркий синевато-красный цвет. Однако из-за низкой основности
(наличие карбоксильной группы снижает основные свойства)
сродство к белковым субстратам невелико и устойчивость
окрасок к мокрым обработкам оказывается низкой.
• Краситель обычно применяют для крашения бумаги, кожи,
парфюмерно-косметических товаров, для приготовления
спиртовых мебельных лаков и фаналевого светостойкого лака.
51.
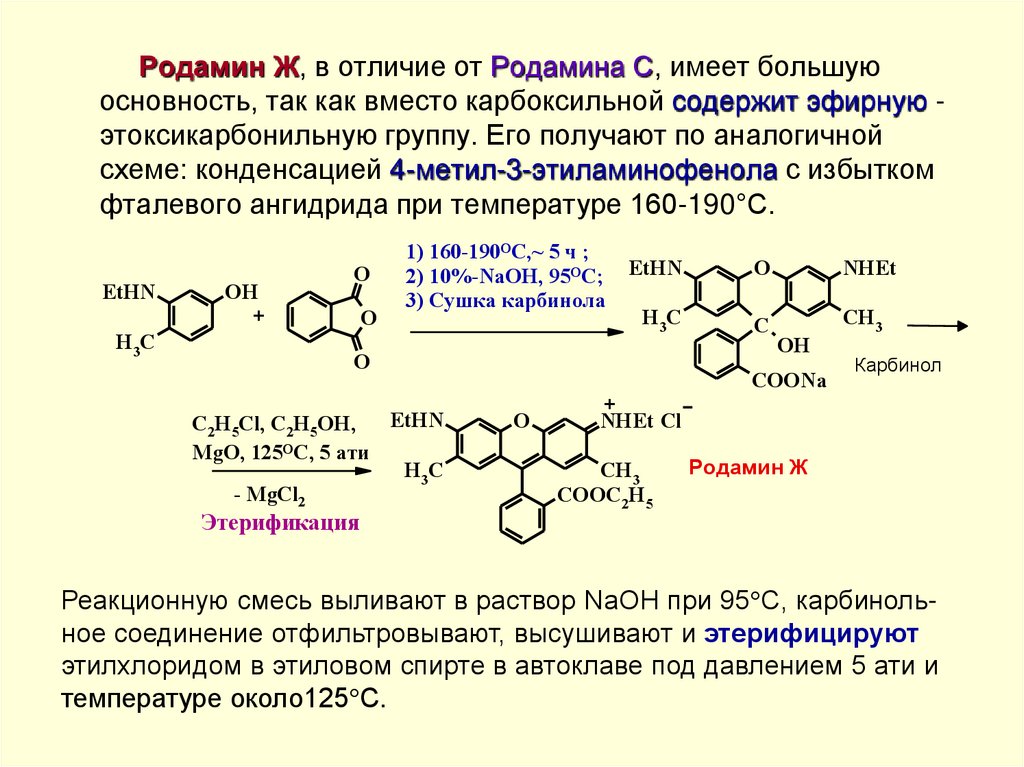
Родамин Ж, в отличие от Родамина С, имеет большуюосновность, так как вместо карбоксильной содержит эфирную этоксикарбонильную группу. Его получают по аналогичной
схеме: конденсацией 4-метил-3-этиламинофенола с избытком
фталевого ангидрида при температуре 160-190°С.
EtHN
H3C
OH
O
+
O
1) 160-190OC,~ 5 ч ;
2) 10%-NaOH, 95OC;
3) Сушка карбинола
EtHN
O
NHEt
H3C
C
CH3
O
EtHN
C2H5Cl, C2H5OH,
MgO, 125OC, 5 ати
H3C
- MgCl2
Этерификация
OH
COONa
O
Карбинол
+
NHEt Cl
CH3
COOC2H5
Родамин Ж
Реакционную смесь выливают в раствор NaOH при 95 С, карбинольное соединение отфильтровывают, высушивают и этерифицируют
этилхлоридом в этиловом спирте в автоклаве под давлением 5 ати и
температуре около125 С.
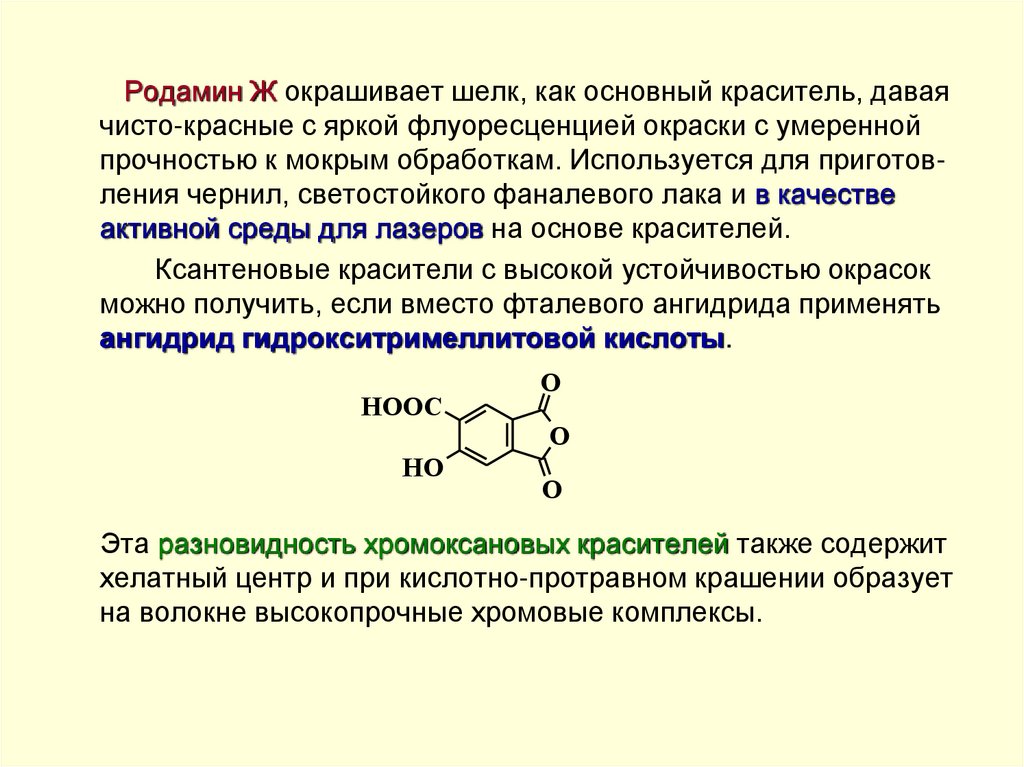
52.
Родамин Ж окрашивает шелк, как основный краситель, даваячисто-красные с яркой флуоресценцией окраски с умеренной
прочностью к мокрым обработкам. Используется для приготовления чернил, светостойкого фаналевого лака и в качестве
активной среды для лазеров на основе красителей.
Ксантеновые красители с высокой устойчивостью окрасок
можно получить, если вместо фталевого ангидрида применять
ангидрид гидрокситримеллитовой кислоты.
HOOC
O
O
HO
O
Эта разновидность хромоксановых красителей также содержит
хелатный центр и при кислотно-протравном крашении образует
на волокне высокопрочные хромовые комплексы.
53.
Лабутен! Это лучлазера на красителе.
54.
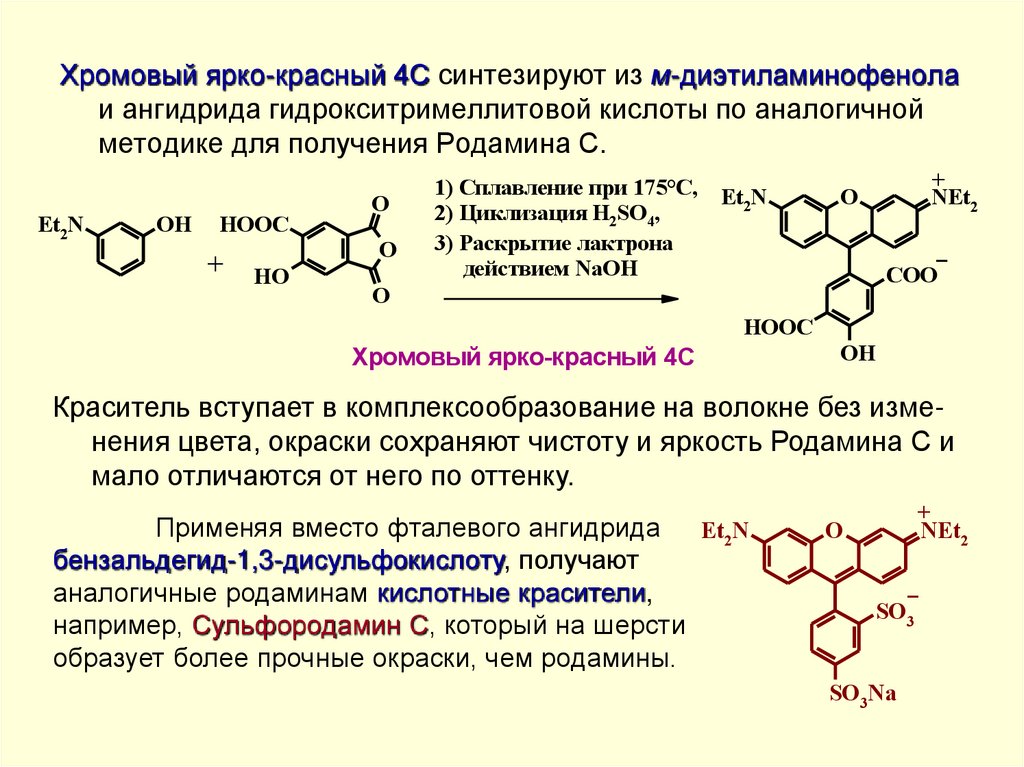
Хромовый ярко-красный 4С синтезируют из м-диэтиламинофенолаи ангидрида гидрокситримеллитовой кислоты по аналогичной
методике для получения Родамина С.
Et2N
OH
HOOC
+
O
O
HO
1) Сплавление при 175°C,
2) Циклизация H2SO4,
3) Раскрытие лактрона
действием NaOH
Et2N
+
NEt2
O
-
COO
O
HOOC
Хромовый ярко-красный 4С
OH
Краситель вступает в комплексообразование на волокне без изменения цвета, окраски сохраняют чистоту и яркость Родамина С и
мало отличаются от него по оттенку.
Применяя вместо фталевого ангидрида
Et2N
бензальдегид-1,3-дисульфокислоту, получают
аналогичные родаминам кислотные красители,
например, Сульфородамин С, который на шерсти
образует более прочные окраски, чем родамины.
+
NEt2
O
-
SO3
SO3Na
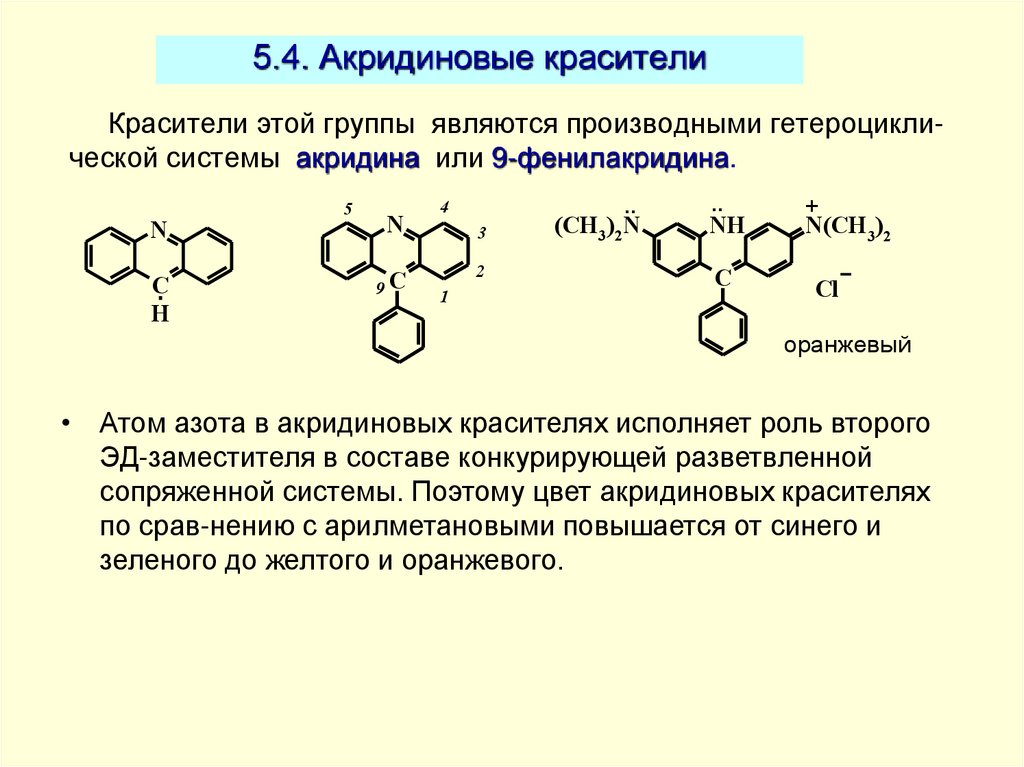
55. 5.4. Акридиновые красители
Красители этой группы являются производными гетероциклической системы акридина или 9-фенилакридина.N
C
H
5
N
9C
..
4
3
2
1
(CH3)2N
..
NH
C
+
N(CH3)2
Cl
оранжевый
• Атом азота в акридиновых красителях исполняет роль второго
ЭД-заместителя в составе конкурирующей разветвленной
сопряженной системы. Поэтому цвет акридиновых красителях
по срав-нению с арилметановыми повышается от синего и
зеленого до желтого и оранжевого.
56.
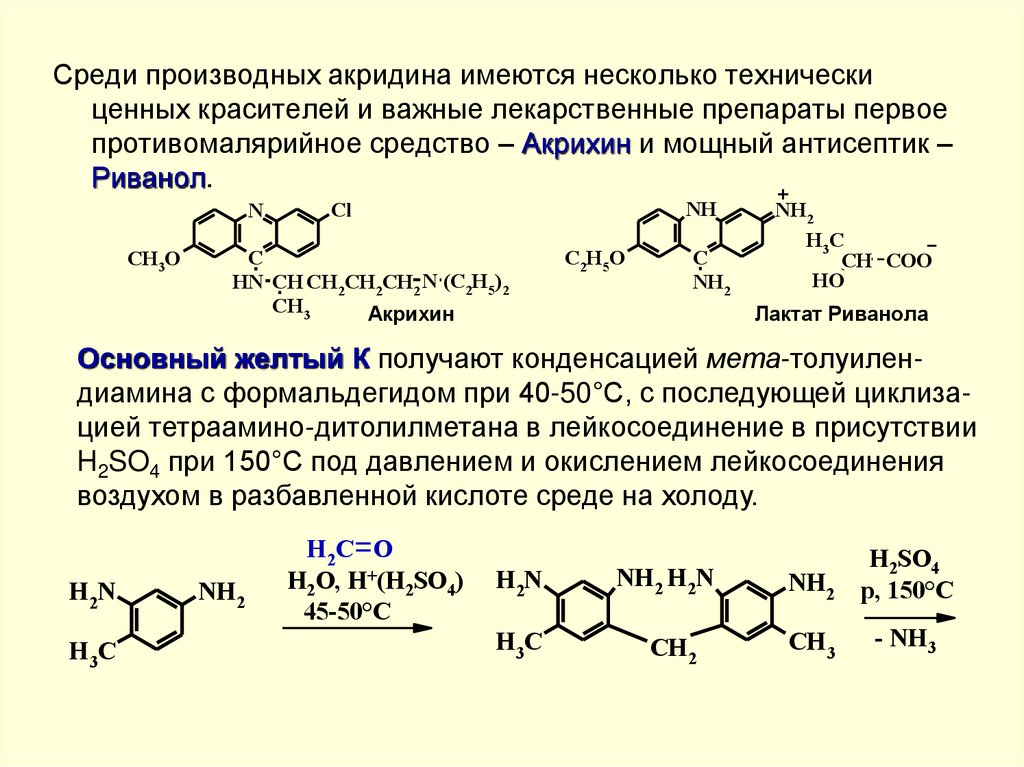
Среди производных акридина имеются несколько техническиценных красителей и важные лекарственные препараты первое
противомалярийное средство – Акрихин и мощный антисептик –
Риванол.
+
N
CH3O
NH
Cl
C
HN CH CH2CH2CH2 N (C2H5)2
CH3
Акрихин
C2H5O
C
NH2
NH2
H3C
CH COO
HO
Лактат Риванола
Основный желтый К получают конденсацией мета-толуилендиамина с формальдегидом при 40-50°С, с последующей циклизацией тетраамино-дитолилметана в лейкосоединение в присутствии
H2SO4 при 150°С под давлением и окислением лейкосоединения
воздухом в разбавленной кислоте среде на холоду.
H2N
H3C
NH2
H2C O
H2O, H+(H2SO4)
45-50°C
H2N
NH2 H2N
NH2
H2SO4
p, 150°C
H3C
CH2
CH3
- NH3
57.
H2SO4p, 150°C
H2N
NH
NH2
- NH3
H3C
CH2
CH3
Лейкосоединение
O2, 2%-HCl
+
H2N
NH
NH2 Cl
H3C
CH
CH3
Основный желтый К
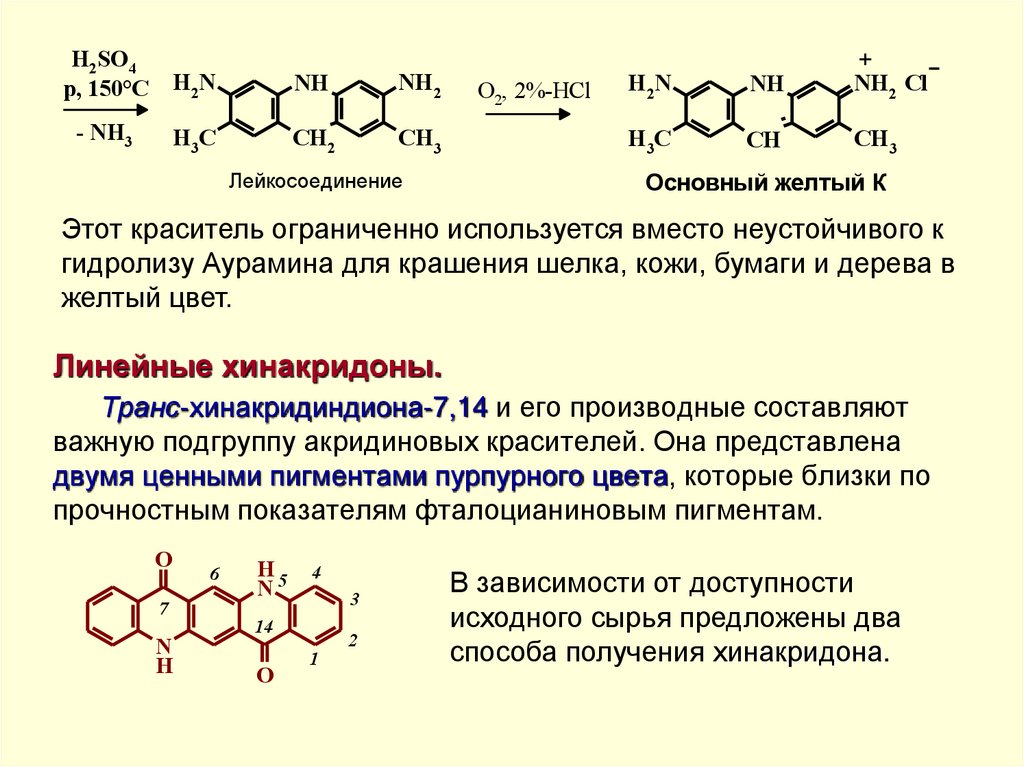
Этот краситель ограниченно используется вместо неустойчивого к
гидролизу Аурамина для крашения шелка, кожи, бумаги и дерева в
желтый цвет.
Линейные хинакридоны.
Транс-хинакридиндиона-7,14 и его производные составляют
важную подгруппу акридиновых красителей. Она представлена
двумя ценными пигментами пурпурного цвета, которые близки по
прочностным показателям фталоцианиновым пигментам.
O
7
N
H
6
H5
N
4
3
14
O
1
2
В зависимости от доступности
исходного сырья предложены два
способа получения хинакридона.
58.
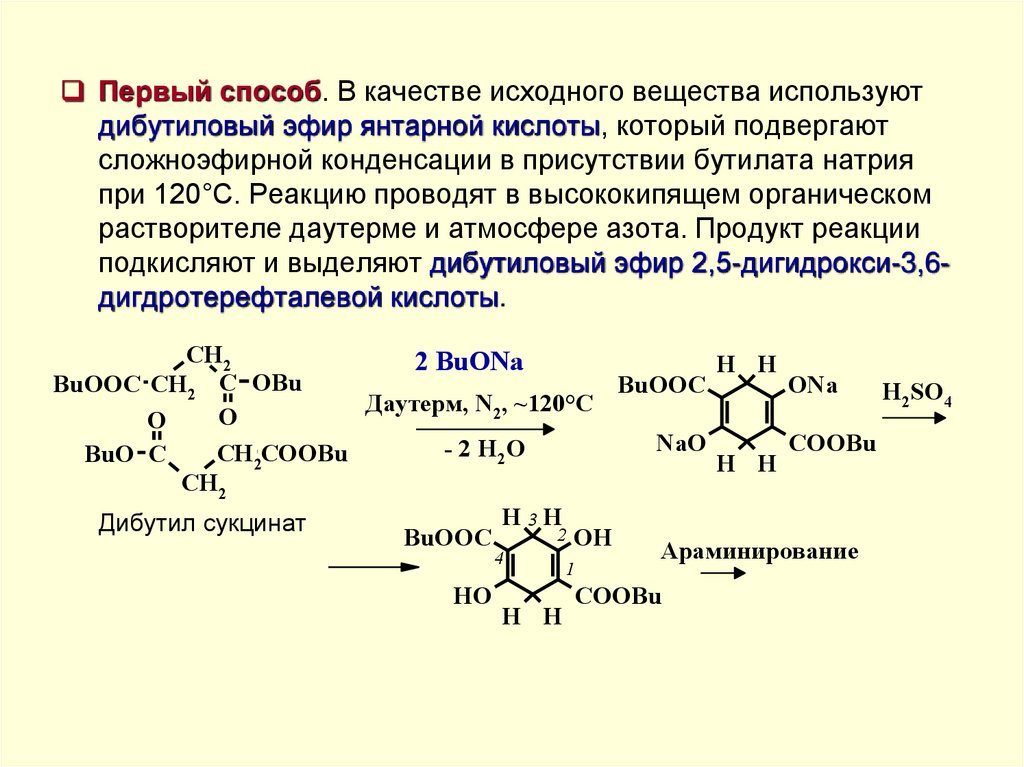
Первый способ. В качестве исходного вещества используютдибутиловый эфир янтарной кислоты, который подвергают
сложноэфирной конденсации в присутствии бутилата натрия
при 120°С. Реакцию проводят в высококипящем органическом
растворителе даутерме и атмосфере азота. Продукт реакции
подкисляют и выделяют дибутиловый эфир 2,5-дигидрокси-3,6дигдротерефталевой кислоты.
CH2
2 BuONa
H H
BuOOC CH2 C OBu
BuOOC
ONa
H2SO4
Даутерм, N2, ~120°C
O
O
NaO
COOBu
- 2 H2 O
CH2COOBu
BuO C
H H
CH2
H3H
Дибутил сукцинат
2 OH
BuOOC
Араминирование
4
1
HO
H H
COOBu
59.
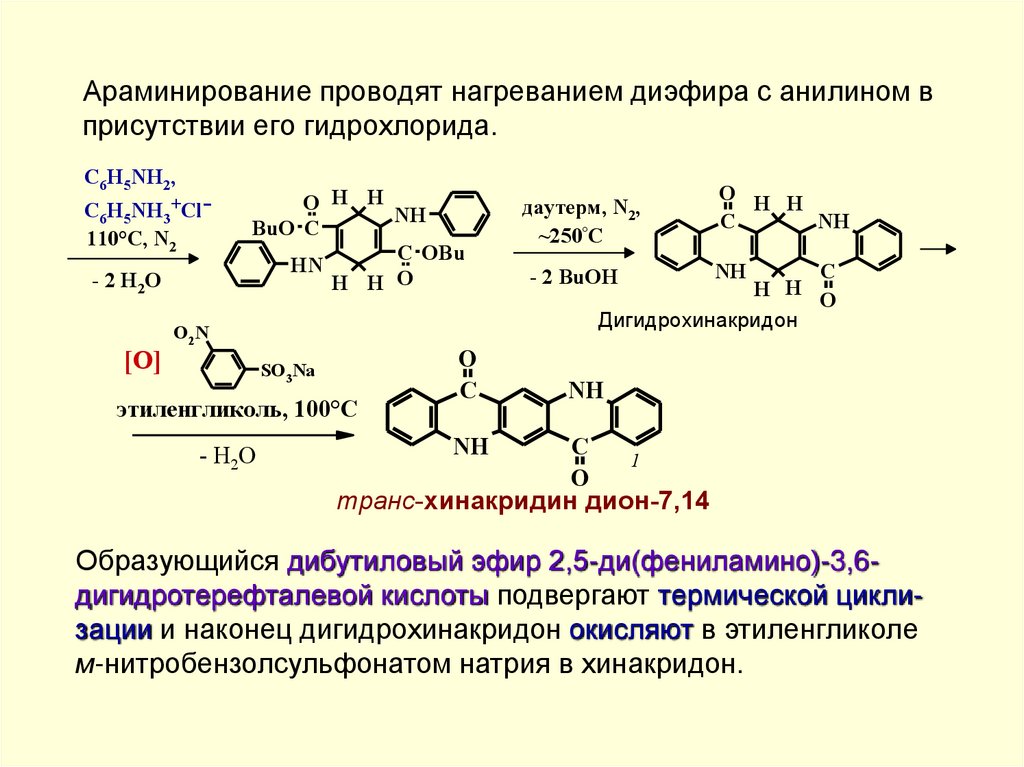
Араминирование проводят нагреванием диэфира с анилином вприсутствии его гидрохлорида.
C6H5NH2,
C6H5NH3+Cl110°C, N2
- 2 H 2O
[O]
O H H
NH
BuO C
C OBu
HN
H H O
O 2N
SO 3Na
этиленгликоль, 100°C
- H2O
O
C
NH
даутерм, N2,
~250°C
O H H
C
NH
NH
C
H H O
Дигидрохинакридон
- 2 BuOH
NH
C
O
1
транс-хинакридин дион-7,14
Образующийся дибутиловый эфир 2,5-ди(фениламино)-3,6дигидротерефталевой кислоты подвергают термической циклизации и наконец дигидрохинакридон окисляют в этиленгликоле
м-нитробензолсульфонатом натрия в хинакридон.
60.
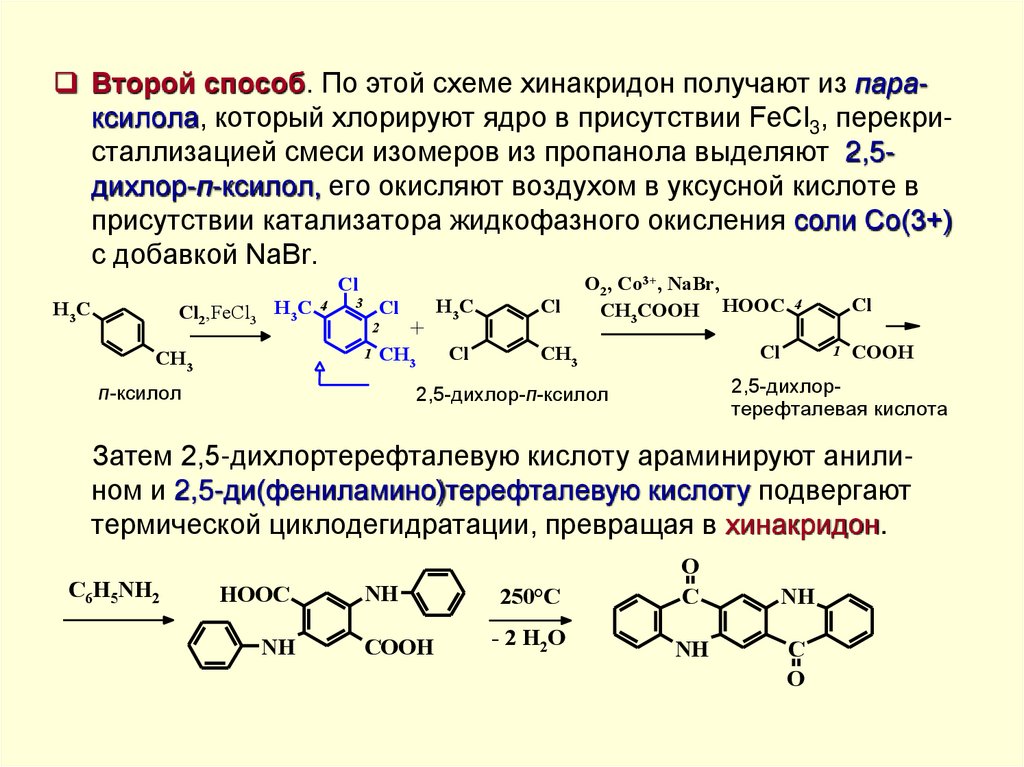
Второй способ. По этой схеме хинакридон получают из параксилола, который хлорируют ядро в присутствии FeCl3, перекристаллизацией смеси изомеров из пропанола выделяют 2,5дихлор-п-ксилол, его окисляют воздухом в уксусной кислоте вприсутствии катализатора жидкофазного окисления соли Со(3+)
с добавкой NaBr.
Cl
Cl2,FeCl3 H3C 4
H3C
CH3
3
Cl
2
+
1 CH
3
п-ксилол
H3C
Cl
Cl
CH3
O2, Co3+, NaBr,
CH3COOH HOOC 4
Cl
Cl
1
COOH
2,5-дихлортерефталевая кислота
2,5-дихлор-п-ксилол
Затем 2,5-дихлортерефталевую кислоту араминируют анилином и 2,5-ди(фениламино)терефталевую кислоту подвергают
термической циклодегидратации, превращая в хинакридон.
C6H5NH2
HOOC
NH
NH
250°C
O
C
COOH
- 2 H2O
NH
NH
C
O
61.
Хинакридон образуется в реакции в красной кристаллической-модификации, для которой характерен тусклый оттенок,
повышенная растворимость в органических растворителях и
плохая красящая способность. Чтобы получить пигмент с
необходимыми колористическими свойствами, необходимо
изменить кристаллическую структуру его частиц.
Для этого -форму подвергают специальной механохимической обработке в вибромельнице и осуществляют полиморфное
превращение красителя.
Пигмент розовый хинакридоновый С ( -модификация) образуется при диспергировании препарата в диметилформамиде
(ДМФА) в присутствии NaCl.
Пигмент фиолетовый хинакридоновый ( -модификация)
образуется при диспергировании в ксилоле или о-дихлорбензоле в присутствии NaCl.
Оба пигмента применяются для изготовления автомобильных
эмалей, печати по тканям, окрашивания поливинилхлорида,
изготовления типографских красок.
















 chemistry
chemistry








