Similar presentations:
Галогенопроизводные алифатические углеводороды
1.
Галогенопроизводныеалифатические
углеводороды
2.
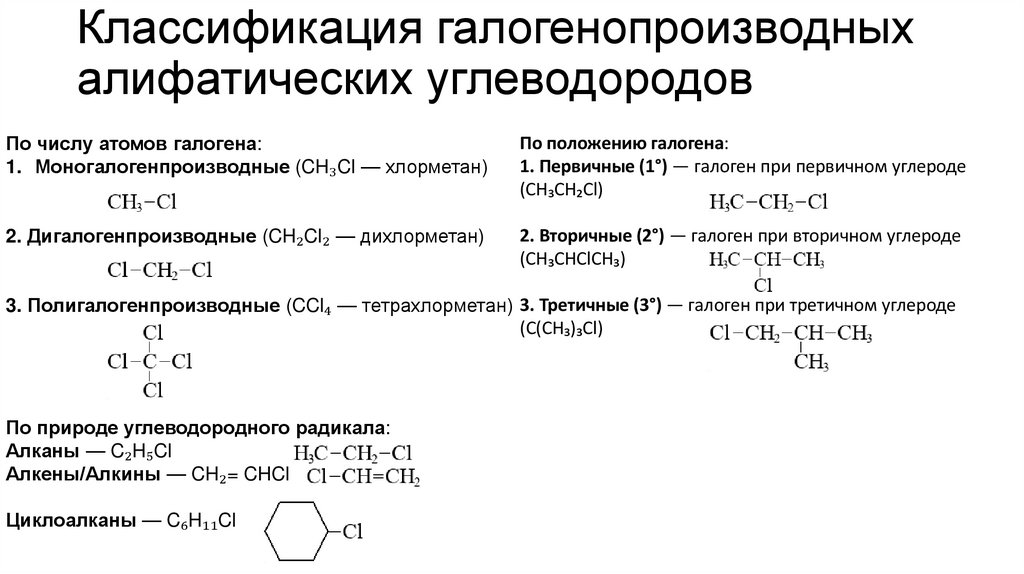
Классификация галогенопроизводныхалифатических углеводородов
По числу атомов галогена:
1. Моногалогенпроизводные (CH₃Cl — хлорметан)
По положению галогена:
1. Первичные (1°) — галоген при первичном углероде
(CH₃CH₂Cl)
2. Дигалогенпроизводные (CH₂Cl₂ — дихлорметан)
2. Вторичные (2°) — галоген при вторичном углероде
(CH₃CHClCH₃)
3. Полигалогенпроизводные (CCl₄ — тетрахлорметан) 3. Третичные (3°) — галоген при третичном углероде
(C(CH₃)₃Cl)
По природе углеводородного радикала:
Алканы — C₂H₅Cl
Алкены/Алкины — CH₂= CHCl
Циклоалканы — C₆H₁₁Cl
3.
Химические и физические свойстваФизические свойства
1. Летучие галогеналканы — жидкости или газы с
характерным запахом.
2. Малорастворимы в воде, хорошо растворяются в
органических растворителях.
3. Плотность увеличивается с ростом массы и числом
галогенов.
Химические свойства
Нуклеофильное замещение (SN1 и SN2):
RCl + NaOH → ROH + NaCl
CH₃CH₂Br + KCN → CH₃CH₂CN + KBr
Элиминирование (дегалогенирование, дегидрогалогенирование):
C₂H₅Br + KOH(спиртовой) → C₂H₄ + KBr + H₂O
Реакции восстановления:
CCl₄ + 2H₂ → CH₄ + 4HCl
Реакции с металлами (реакция Вюрца):
2CH₃Br + 2Na → C₂H₆ + 2NaBr


 chemistry
chemistry








