Similar presentations:
Стереоизомерия
1.
СТЕРЕОИЗОМЕРИЯ2.
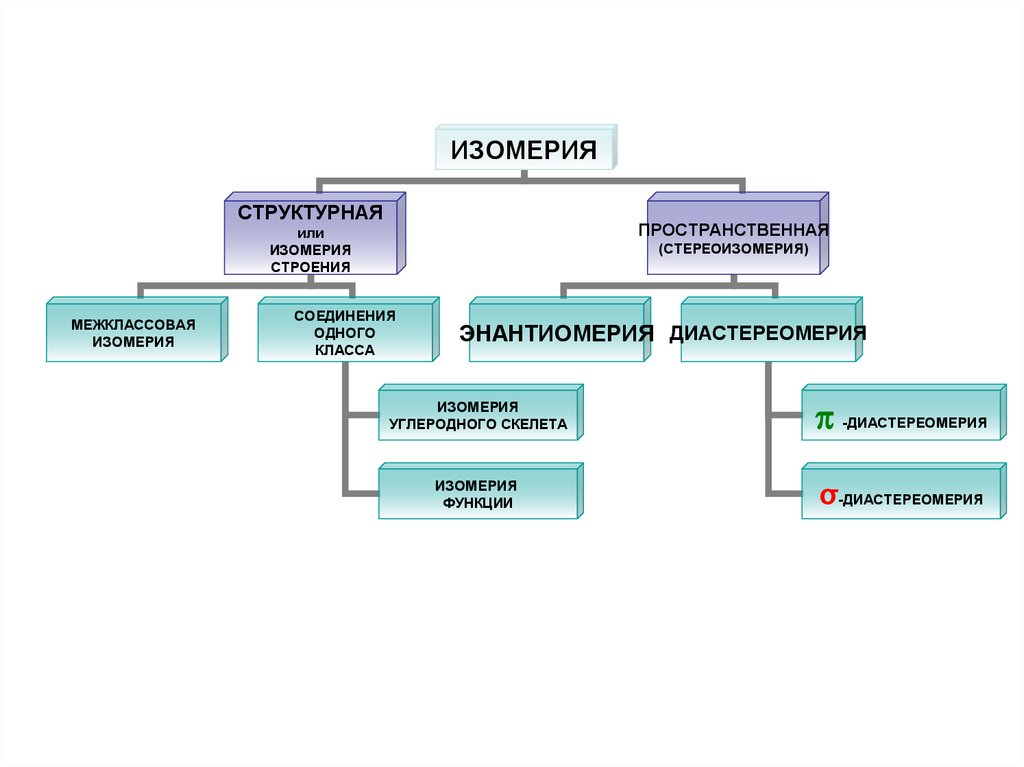
ИЗОМЕРИЯСТРУКТУРНАЯ
ПРОСТРАНСТВЕННАЯ
или
ИЗОМЕРИЯ
СТРОЕНИЯ
МЕЖКЛАССОВАЯ
ИЗОМЕРИЯ
(СТЕРЕОИЗОМЕРИЯ)
СОЕДИНЕНИЯ
ОДНОГО
КЛАССА
ЭНАНТИОМЕРИЯ ДИАСТЕРЕОМЕРИЯ
ИЗОМЕРИЯ
УГЛЕРОДНОГО СКЕЛЕТА
-ДИАСТЕРЕОМЕРИЯ
ИЗОМЕРИЯ
ФУНКЦИИ
σ-ДИАСТЕРЕОМЕРИЯ
3.
Стереоизомерия - изомерия,обусловленная различным
расположением в пространстве атомов в
молекулах.
Стереоизомеры – вещества, имеющие
один и тот же состав (молекулярную
формулу) и одинаковое строение
(структурную ф-лу), но различающиеся
расположением атомов в пространстве.
Расположение атомов в
пространстве, характеризующее
определённый стереоизомер называется
конфигурацией.
4.
С позиций относительной устойчивостистереоизомеры разделяют на
конфигурационные и конформационные
Конфигурационные изомеры могут
существовать в виде индивидуальных
форм , т.е. обладают конфигурационной
устойчивостью. Переход одного изомера в
другой требует разрыва связей.
Конформационные изомеры структуры молекул, различающиеся
степенью поворота ее фрагментов
относительно простых связей. Переход
одного изомера в другой не требует
разрыва связей.
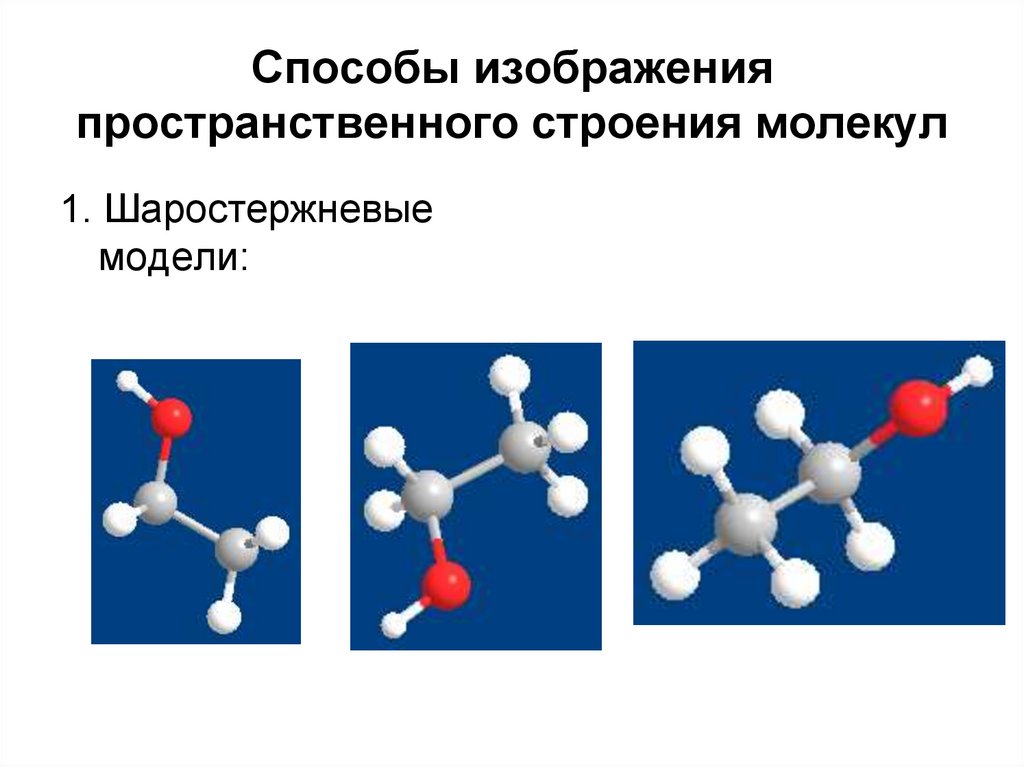
5. Способы изображения пространственного строения молекул
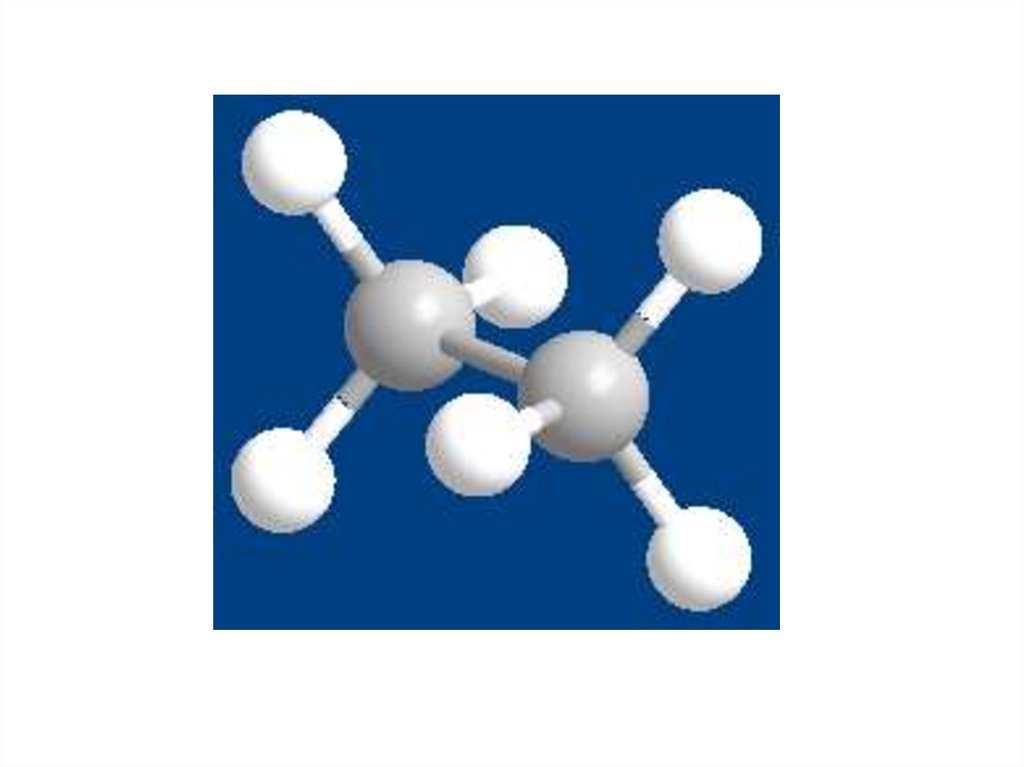
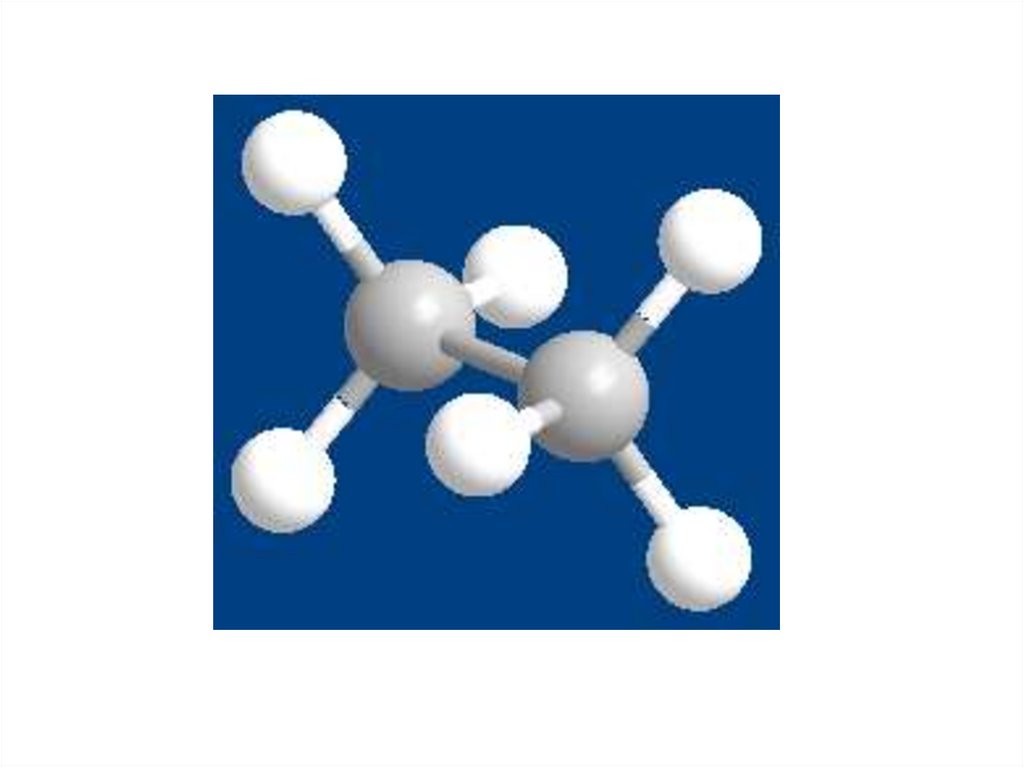
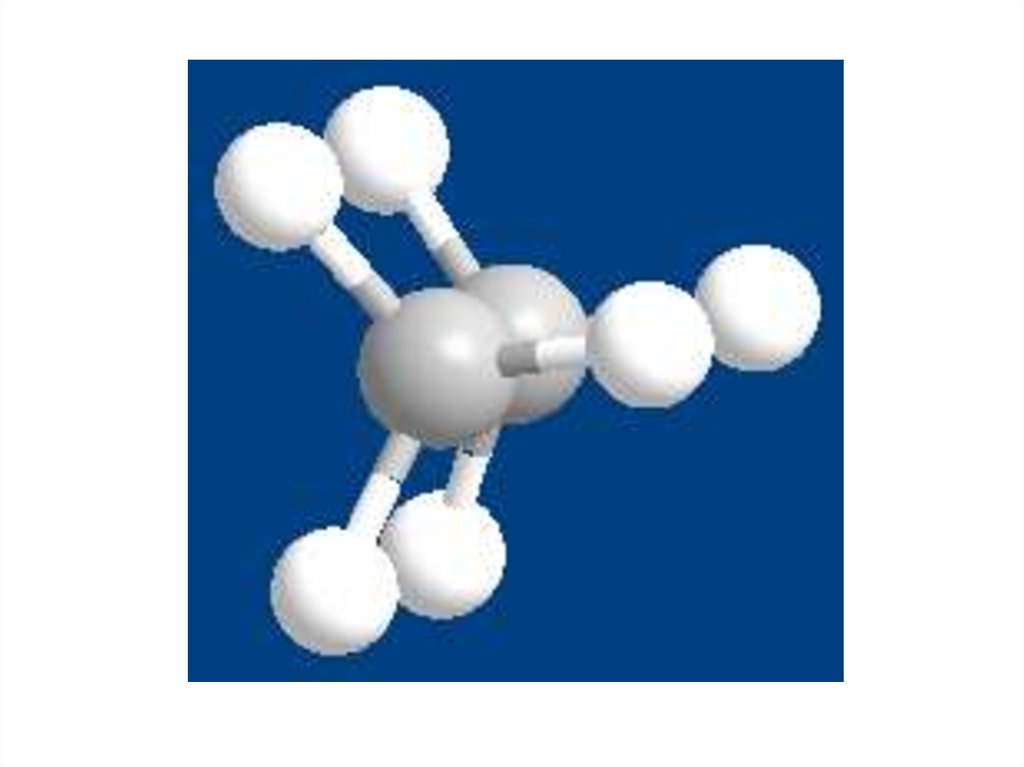
1. Шаростержневыемодели:
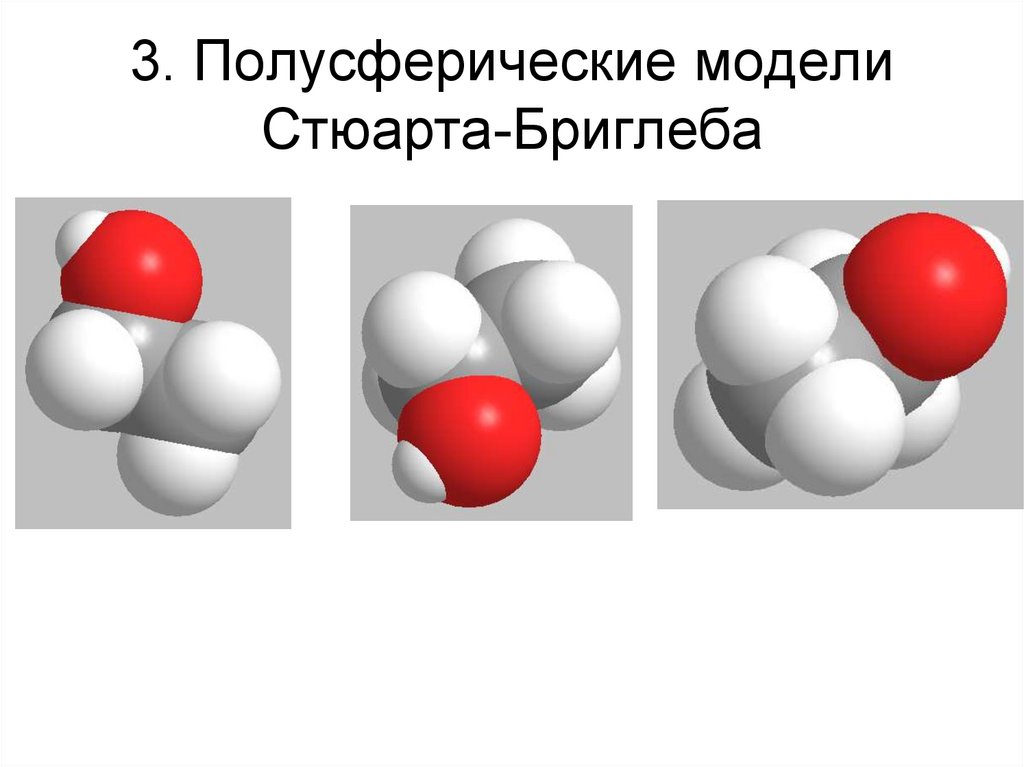
6. 3. Полусферические модели Стюарта-Бриглеба
7. КОНФОРМАЦИОННАЯ ИЗОМЕРИЯ
• характерна для соединений с цепями ициклами, содержащими атомы углерода
в sp3-гибридном состоянии. Возможно
свободное вращение метильных (СН3-)
и метиленовых (-CH2-) групп вокруг С-С
связей. Для этого не требуется
больших затрат энергии. Однако
молекулы предпочитают существовать
в наиболее устойчивой конформации.
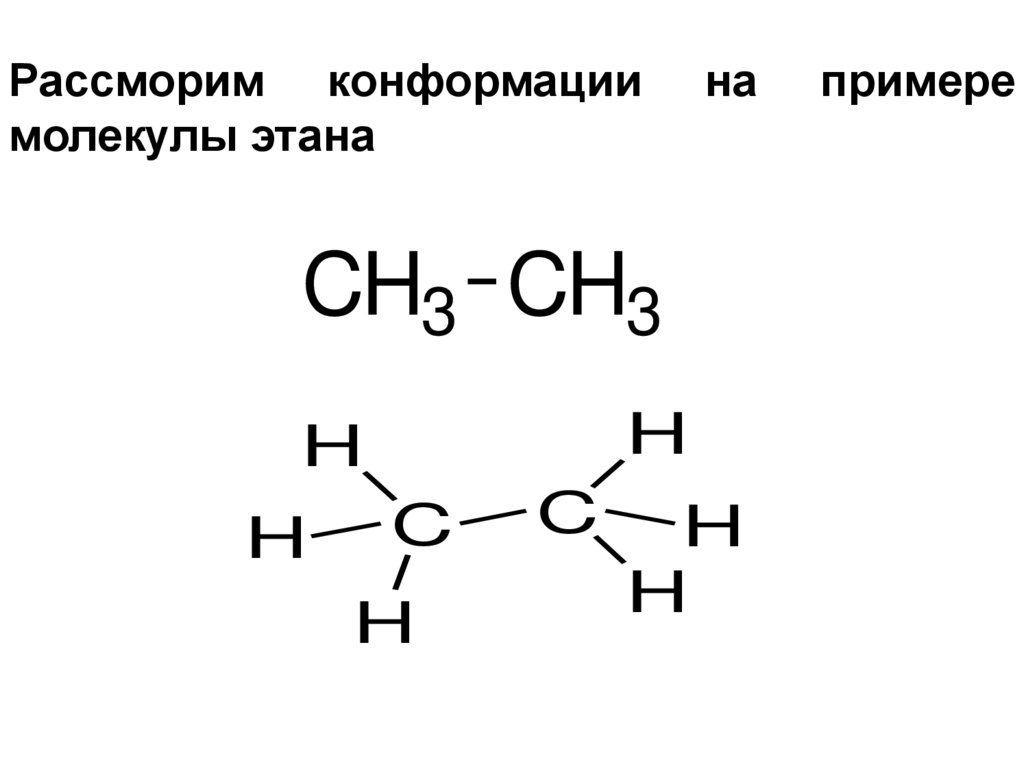
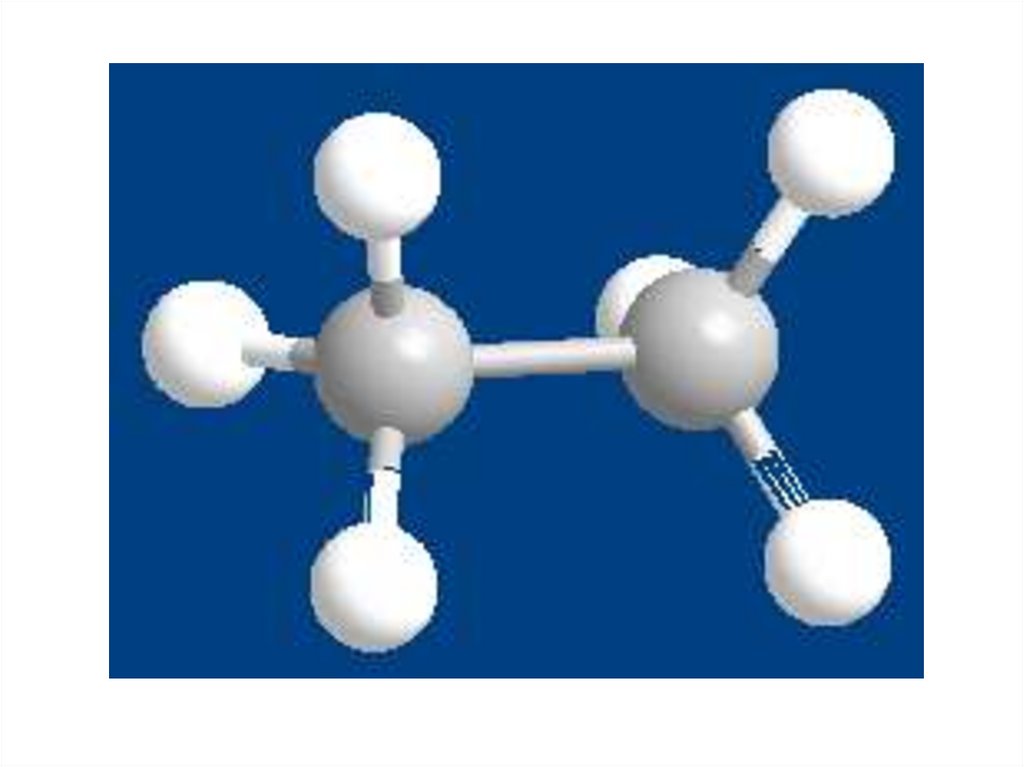
8.
Рассморим конформациимолекулы этана
на
CH3 CH3
H
H
H
C
H
C
H
H
примере
9.
HH
H
H
H
a)
H
H
H
H
C
H
H
H
H
H
C
H
H
H
H
б)
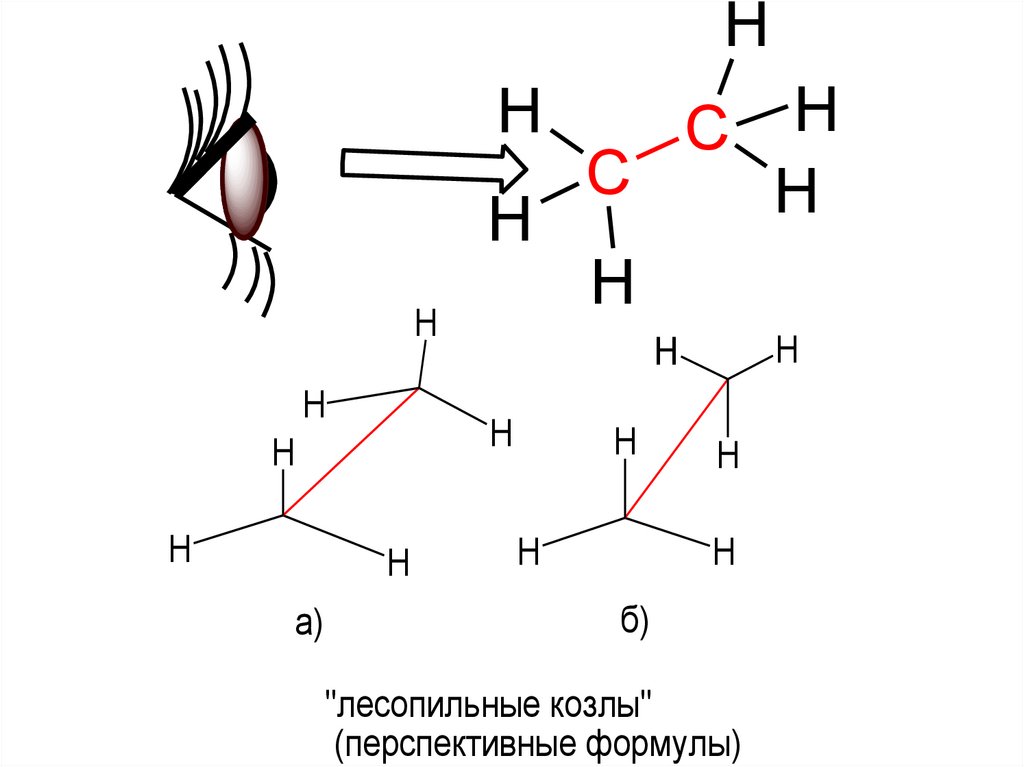
"лесопильные козлы"
(перспективные формулы)
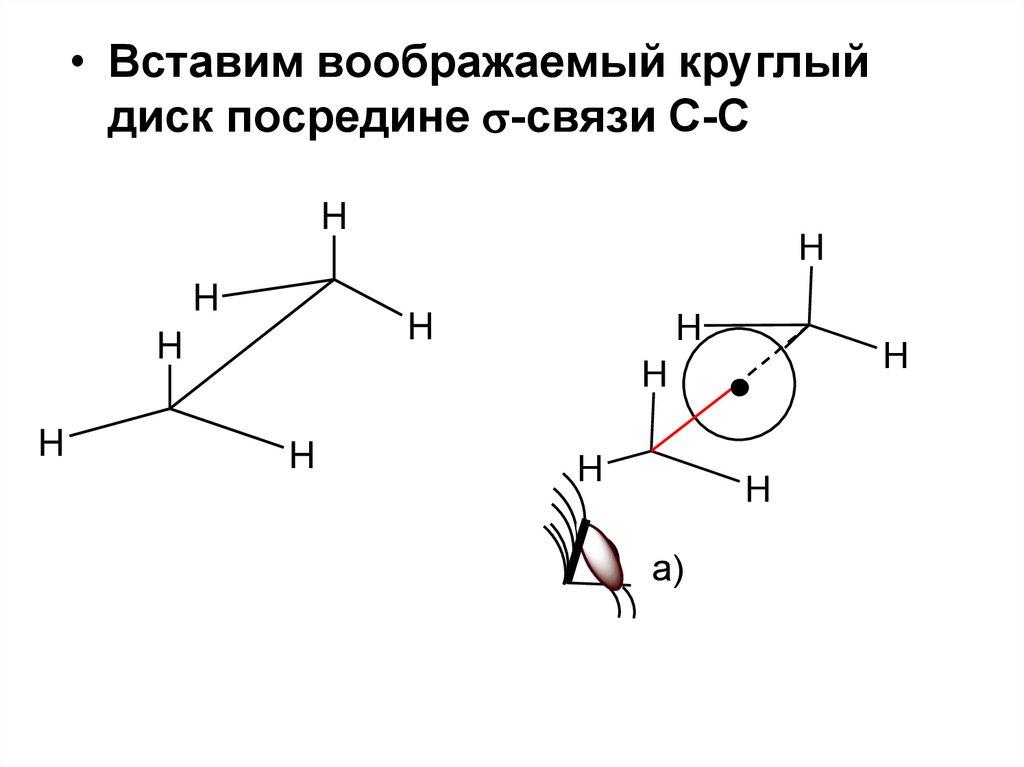
10.
• Вставим воображаемый круглыйдиск посредине -связи С-С
H
H
H
H
H
H
H
H
H
H
H
H
a)
11.
HH
H
H
H
H
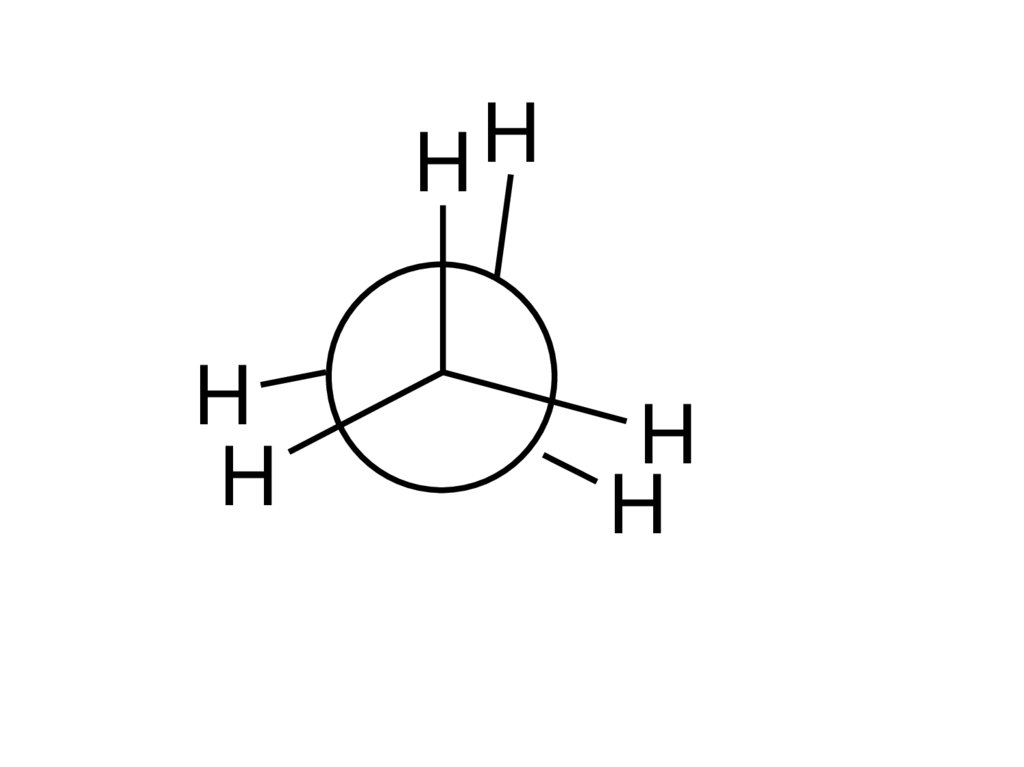
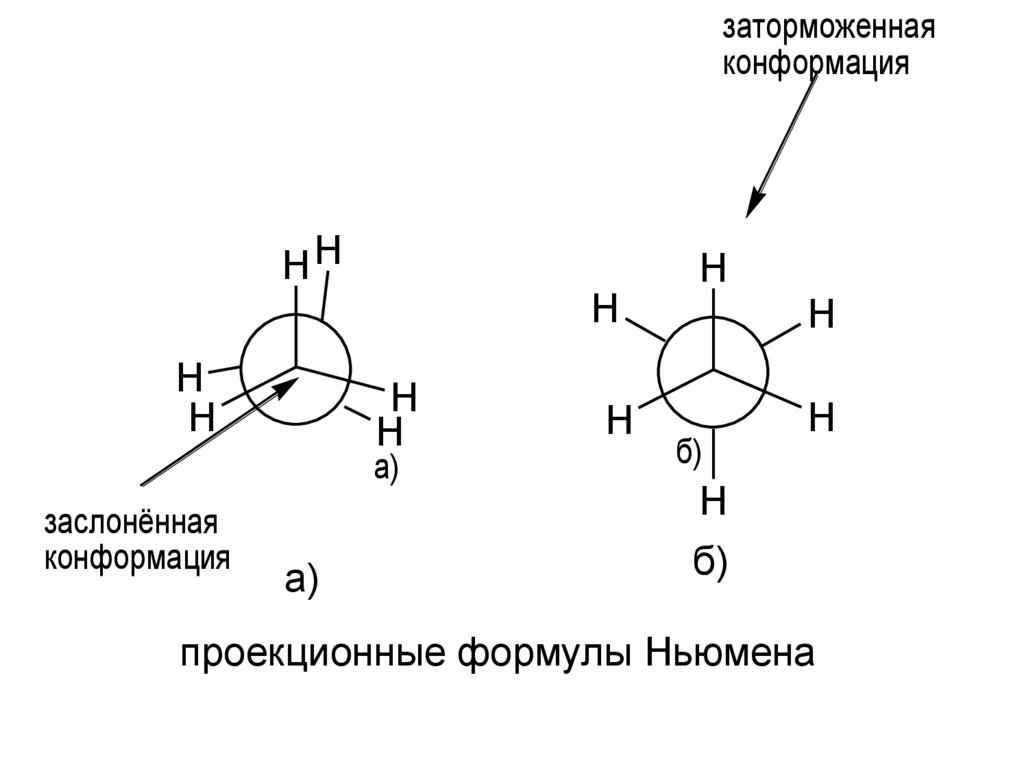
12.
заторможеннаяконформация
HH
H
H
H
H
H
a)
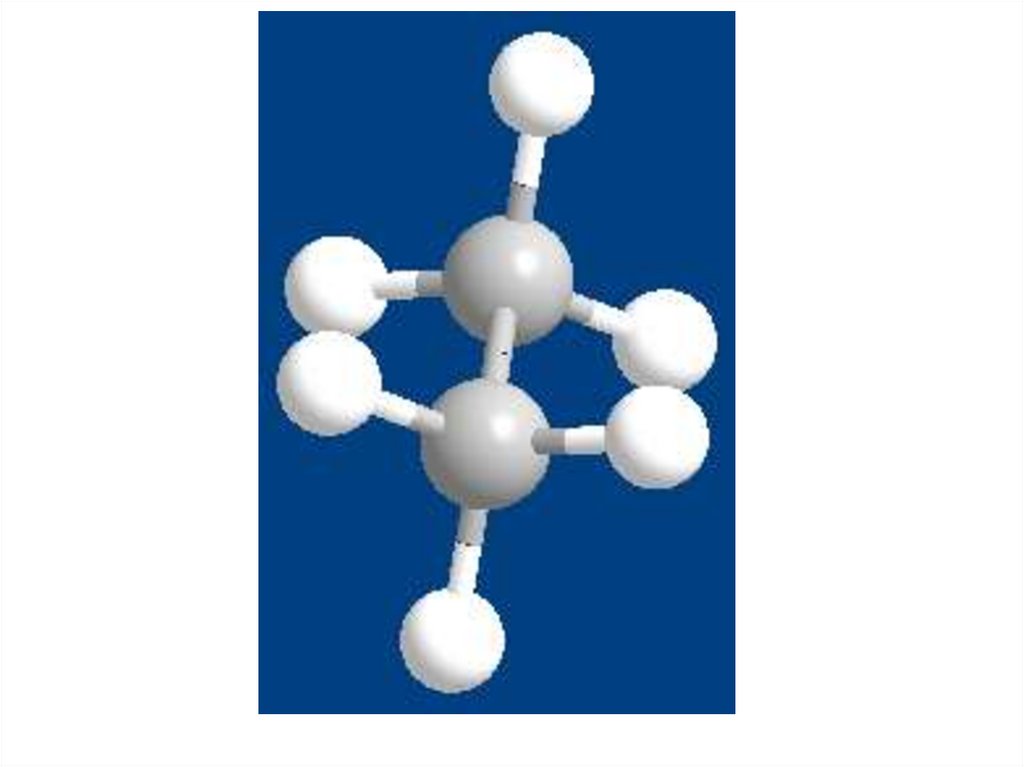
заслонённая
конформация
H
H
H
H
б)
H
a)
б)
проекционные формулы Ньюмена
13.
• Однако вращение вокруг -связи не совсемсвободное, для этого требуется некоторое
количество энергии – барьер вращения.
• Стабильность заторможенной
конформации больше, чем
стабильность заслоненной (на 12
кДж/моль)
• Почему? – Атомы водорода
максимально удалены друг от друга,
что существенно снижает энергию их
взаимного отталкивания.
14.
15.
16.
17.
18.
19.
20. ЭНАНТИОМЕРИЯ
Энантиомерия обусловленаасимметрией органических молекул.
Такие молекулы, как правило содержат
хиральный центр - асимметрический атом
С, т. е. такой атом, который связан с 4
различными атомами или группами.
Такие молекулы обладают хиральностью.
Хиральностью называют свойство
объекта не совпадать со своим
зеркальным отображением.
21. В общем случае молекула хиральна, когда не имеет никаких элементов симметрии – ни центра, ни плоскости симметрии; в противном
случаемолекула ахиральна.
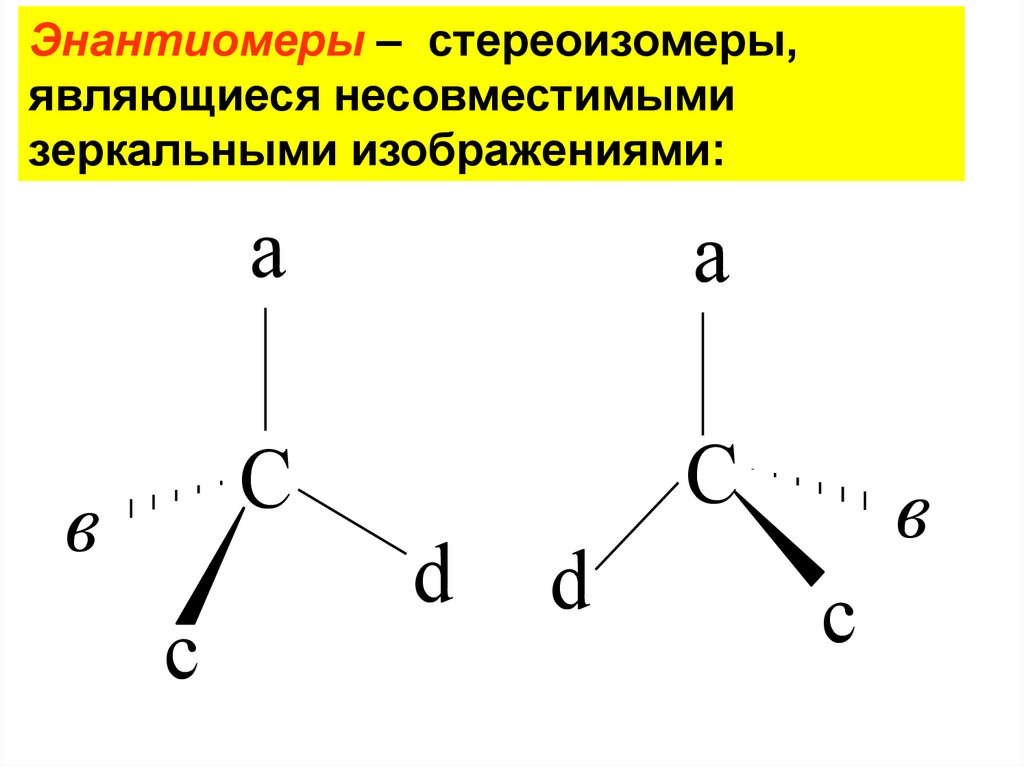
22.
Энантиомеры – стереоизомеры,являющиеся несовместимыми
зеркальными изображениями:
в
c
a
a
C
C
d
d
в
c
23.
Энантиомерия как явление проявляется воптической активности хиральных
соединений.
Оптическая активность хиральных
соединений проявлятся в их способности
вращать плоскость поляризации
плоскополяризованного света
(оптическом вращении).
Оптическую активность измеряют с
помощью прибора поляриметра
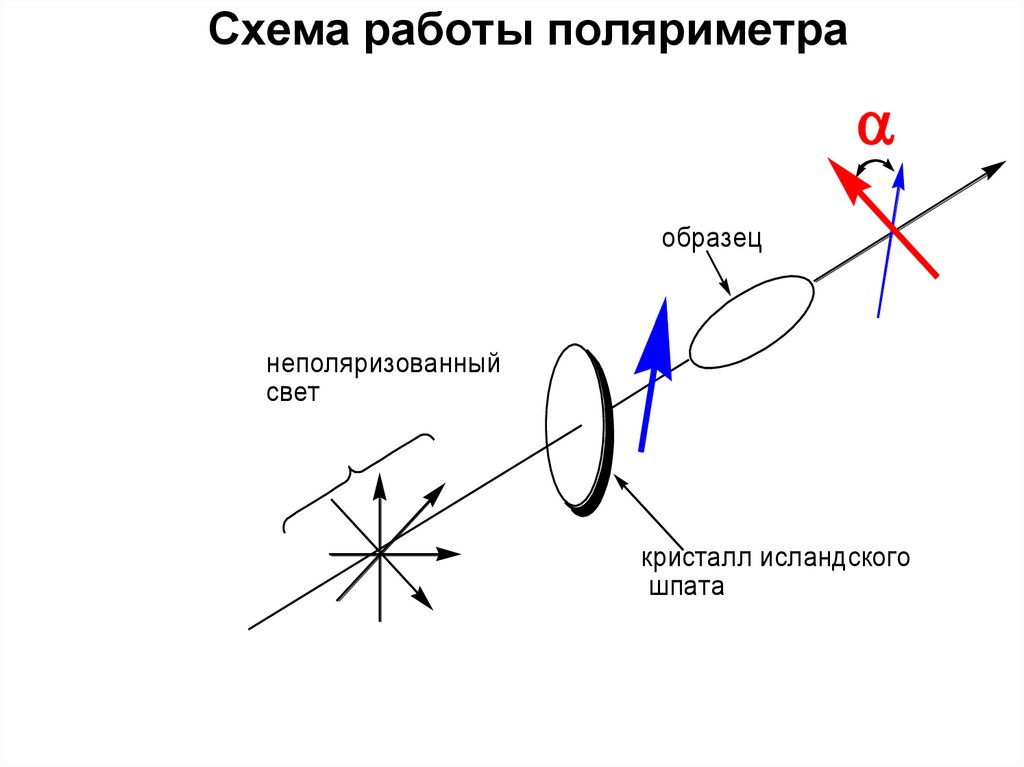
24. Схема работы поляриметра
образецнеполяризованный
свет
кристалл исландского
шпата
25.
• Если образец отклоняет плоскостьполяризации света вправо – вещество
правовращающее (обозначается знаком
«+») если влево – левовращающее («-»)
• Оптическая активность соединения
характеризуется величиной удельного
вращения [ ], которая измеряется в градусах
[ ] = lc
• где - наблюдаемое вращение;
l- длина трубки с образцом;
с- концентрация
26.
Энантиомеры обладают идентичнымифизическими свойствами и отличаются
друг от друга лишь направлением
вращения плоскости поляризации
света.
Если энантиомеры содержатся в
равномолекулярном количестве (так
называемые рацемические формы или
модификации), то оптической
активностью они не обладают
вследствие компенсации вращения _
обозначаются +
27.
Рацемическая смесь – механическаяэквимолярная смесь энантиомеров.
Рацемат – молекулярное соединение
двух энантиомеров.
28.
Способы изображения энантиомеровТрехмерные клиновидные проекции
(см.выше, только хиральный атом не
изображается). Валентные связи
хирального атома, лежащие в плоскости
бумаги, обозначают сплошными линиями;
связи, выступающие вперед –
клиновидными; связи, уходящие за
плоскость - штрих-пунктирными.
Рассмотрим на примере молочной
кислоты.
H*
CH
C COOH
3
OH
29.
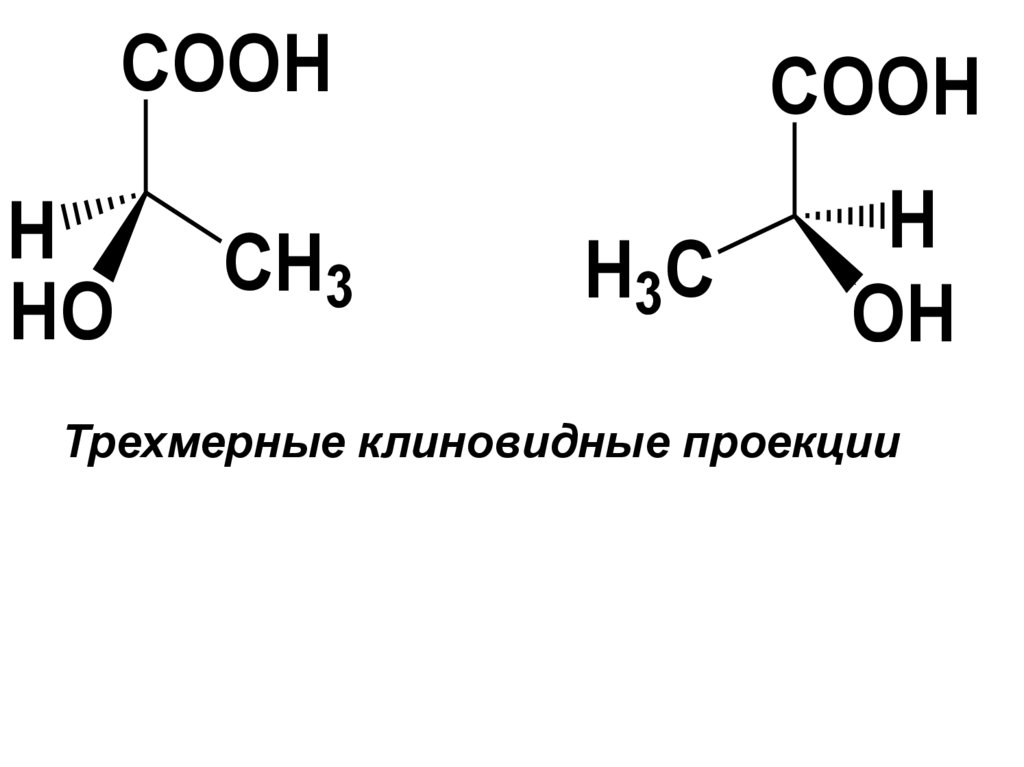
HHO
COOH
COOH
CH3
H
OH
H3C
Трехмерные клиновидные проекции
30.
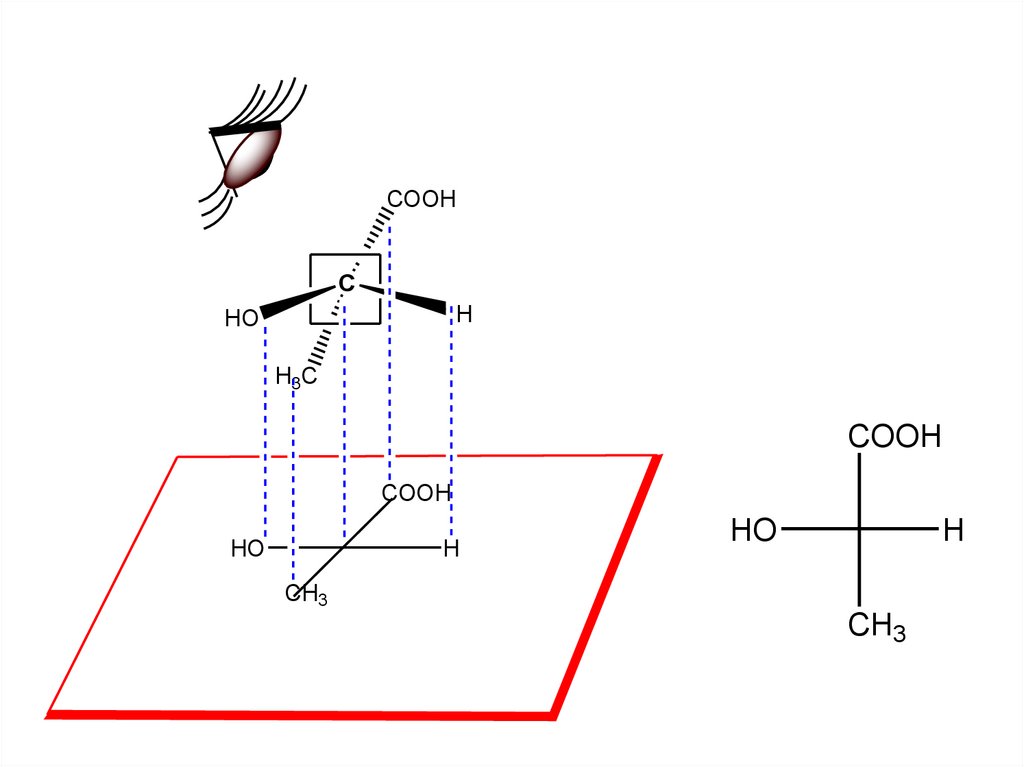
Проекционные формулы ФишераНа плоскость бумаги проецируется тетраэдр,
для чего:
1) С-цепь располагают вертикально так, чтобы
старшая гр. по ИЮПАК оказалась вверху;
2) Заместители, связанные с хиральным
центром вертикальными линиями, находятся
за плоскостью чертежа (направлены «от
наблюдателя»), а заместители, связанные с
хиральным центром горизонтальными
линиями – находятся перед плоскостью
(направлены «к наблюдателю»);
3) Асимметрический С-атом обозначают точкой
пересечения горизонтальной и вертикальной
линий.
31.
COOHC
H
HO
H3C
COOH
COOH
HO
H
HO
H
CH3
CH3
32.
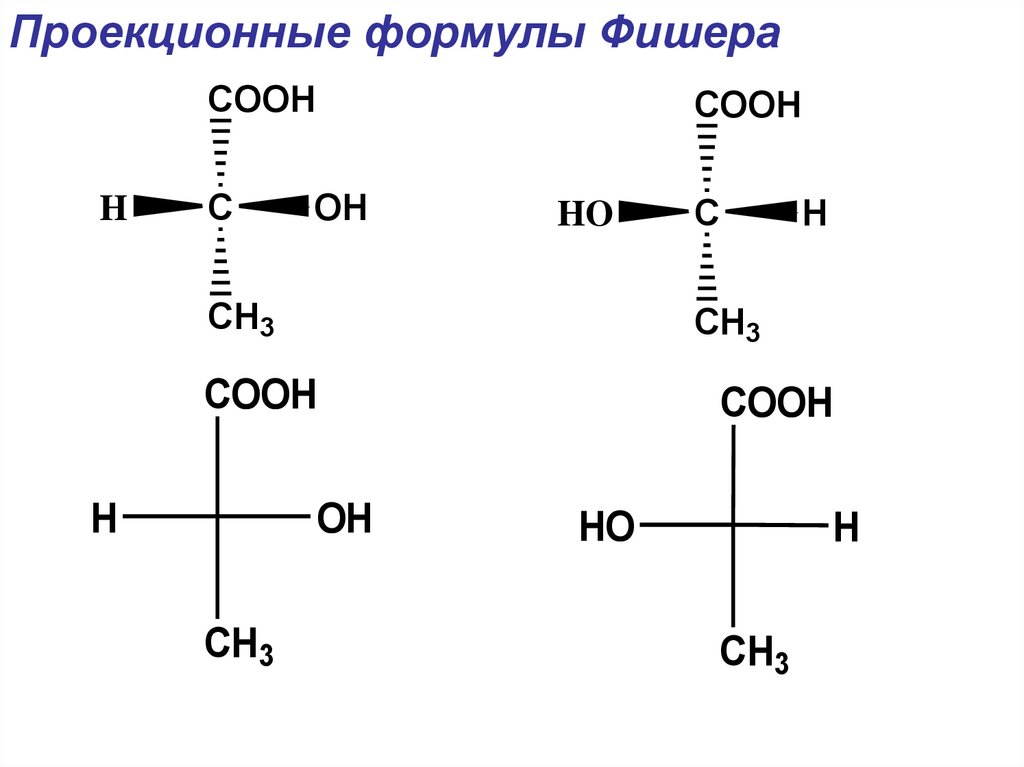
Проекционные формулы ФишераCOOH
H
C
COOH
OH
HO
CH3
OH
CH3
H
CH3
COOH
H
C
COOH
HO
H
CH3
33.
Когда приходится изменять положениепроекционной формулы Фишера на
плоскости, во избежание искажения
стереохимического смысла
преобразования проводят с соблюдением
определенных правил
34.
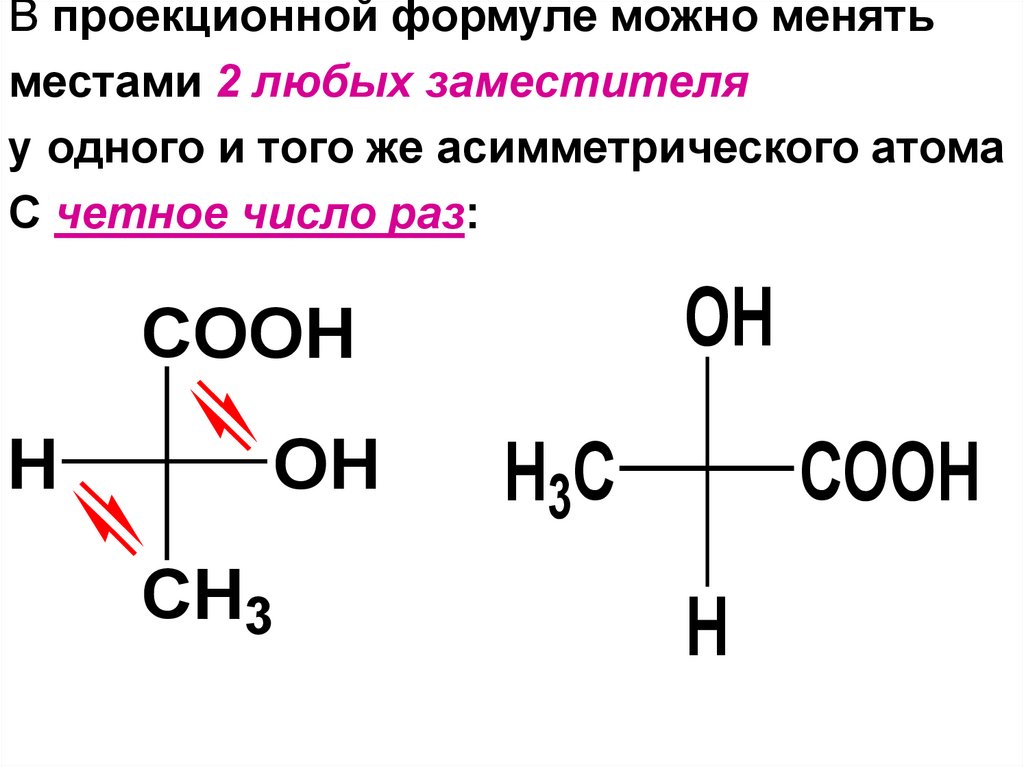
В проекционной формуле можно менятьместами 2 любых заместителя
у одного и того же асимметрического атома
С четное число раз:
OH
COOH
H
OH
CH3
H3C
COOH
H
35.
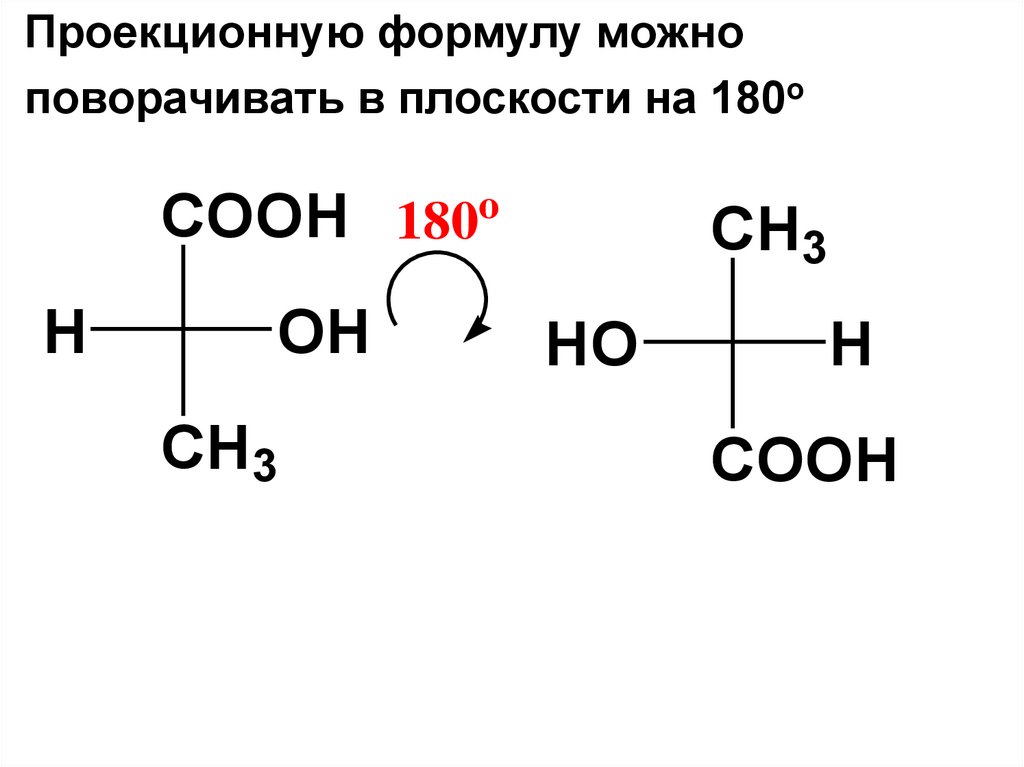
Проекционную формулу можноповорачивать в плоскости на 180о
COOH 180o
H
OH
CH3
CH3
HO
H
COOH
36.
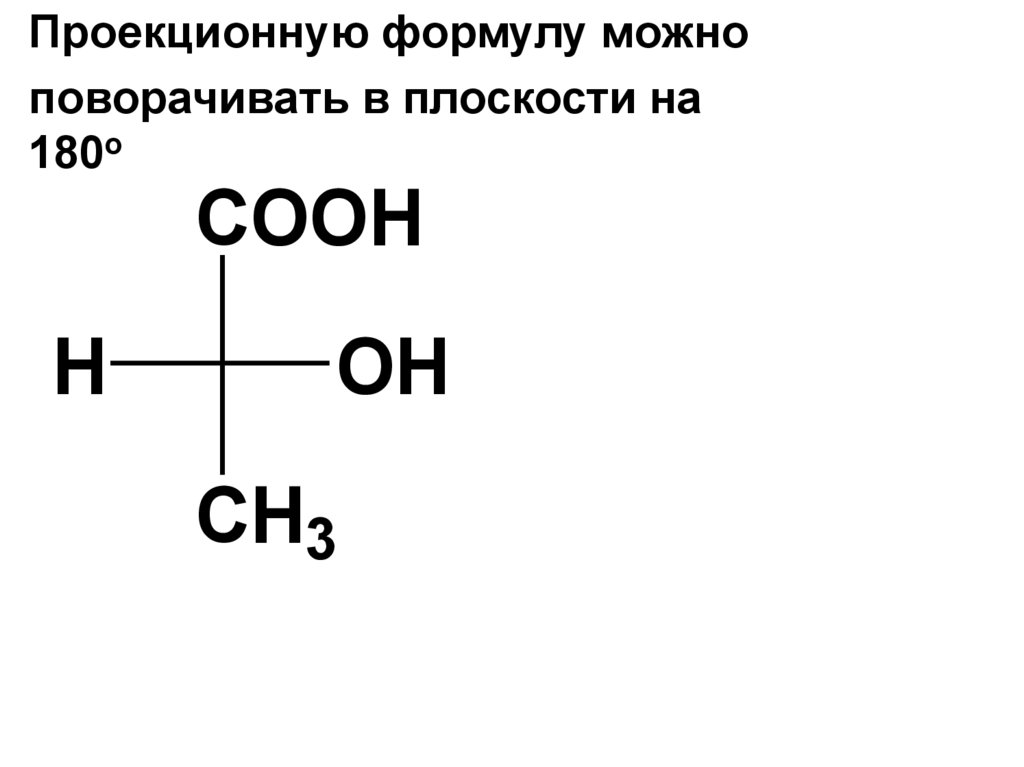
Проекционную формулу можноповорачивать в плоскости на
180о
COOH
H
OH
CH3
37. Для определения относительной конфигурации некоторых рядов оптически активных соединений определяют расположение заместителей
поотношению к стандартным соединениям
D(+)- и L(-)-глицериновому альдегиду.
38.
CHOH
OH
CHO
HO
H
CH2OH
CH2OH
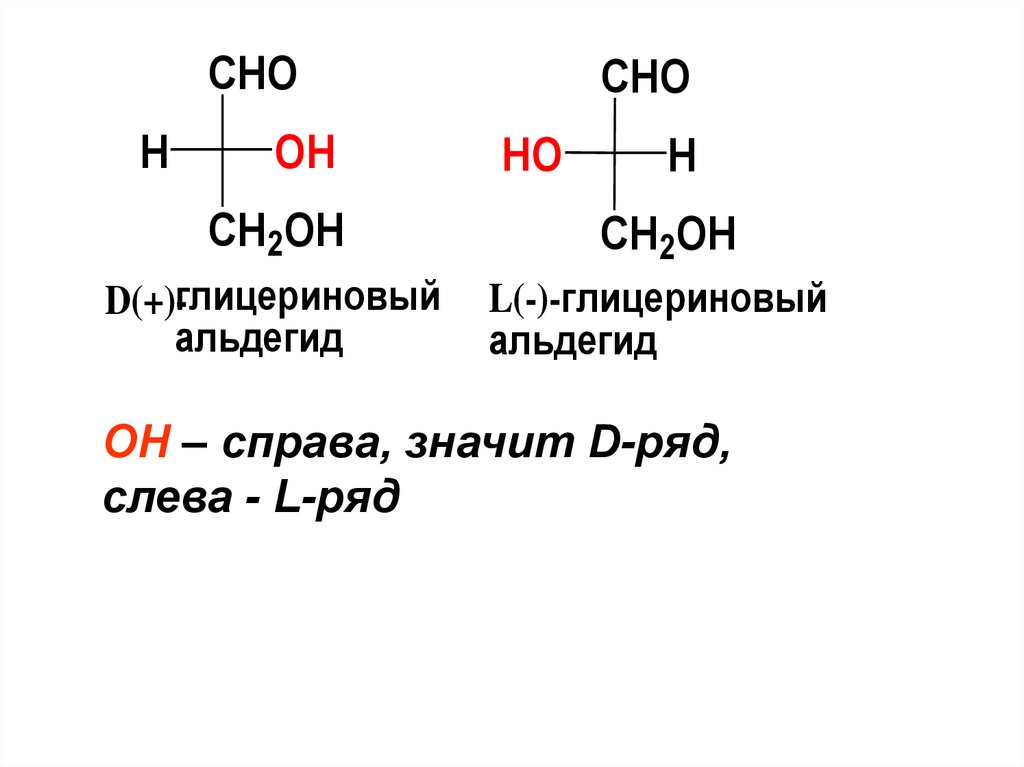
D(+)-глицериновый
альдегид
L(-)-глицериновый
альдегид
ОН – справа, значит D-ряд,
слева - L-ряд
39.
R,S-номенклатура – устанавливаетабсолютную конфигурацию
стереоизомеров и является
универсальной.
Для определения абс. конфигурации
необходимо:
1) Установить старшинство
заместителей. Старшинство
определяется по порядковому номеру
атома, непосредственно связанного с
хиральным центром. Если атомы
одинаковые, то сравнивают следующий
ряд атомов в заместителе и т.д. При этом,
если атом связан двойной связью, его
считают за 2 атома, тройной – за 3.
40.
2) Модель молекулы располагают так,чтобы младший заместитель был
наиболее удален от наблюдателя.
Если старшинство заместителей в
повернутом к наблюдателю основанию
тетраэдра, убывает по часовой стрелке,
то R (правый – rectus), против – S (левый
– sinister).
Так, для молочной кислоты
О
8
H
O
> C H > H
H > C
O H
H
6
1
6
8, 8, 8
1, 1, 1
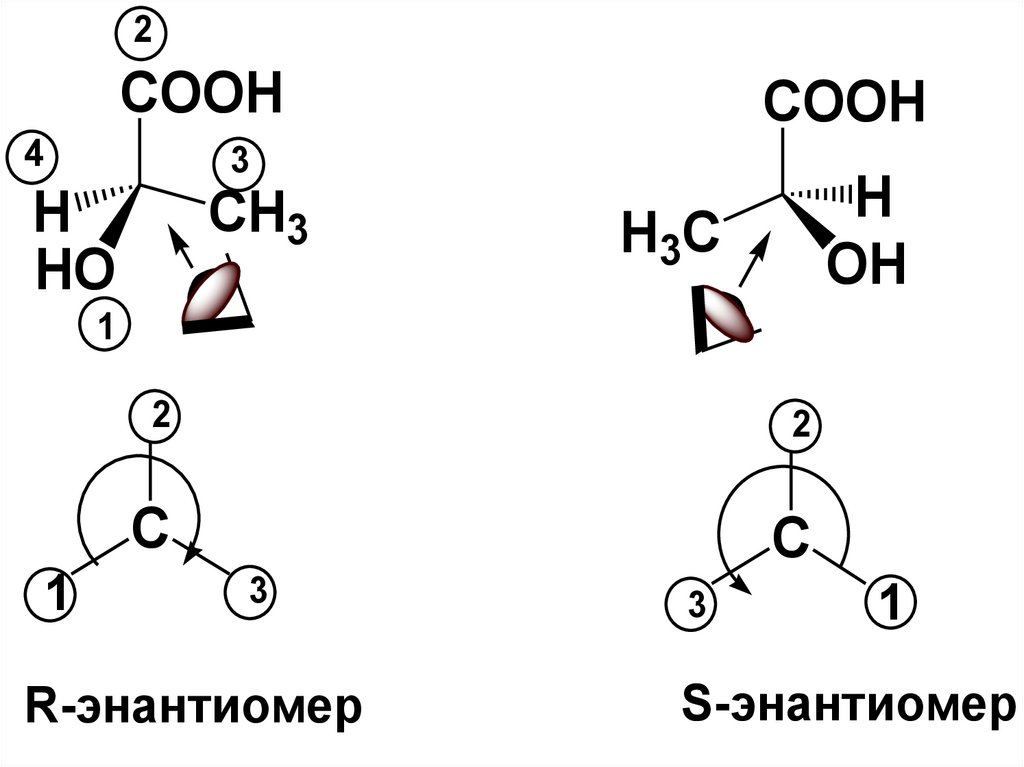
41.
2COOH
4
3
H
HO
CH3
COOH
H
OH
H3C
1
1
2
2
C
C
3
R-энантиомер
3
1
S-энантиомер
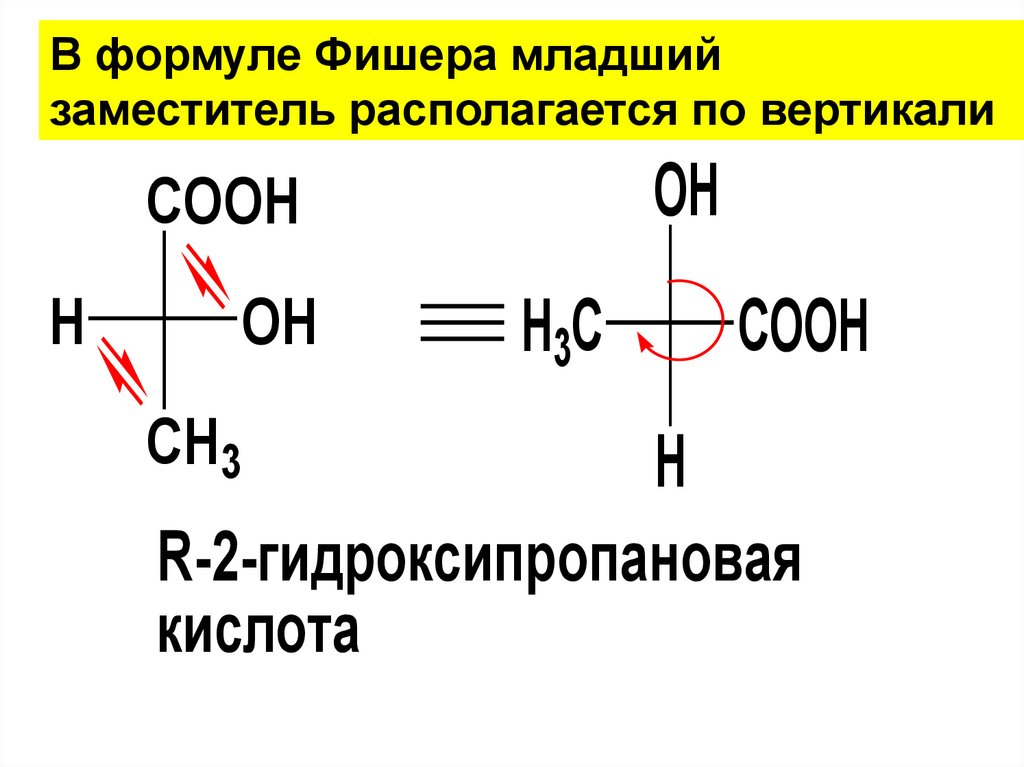
42.
В формуле Фишера младшийзаместитель располагается по вертикали
OH
COOH
H
OH
CH3
H3C
COOH
H
R-2-гидроксипропановая
кислота
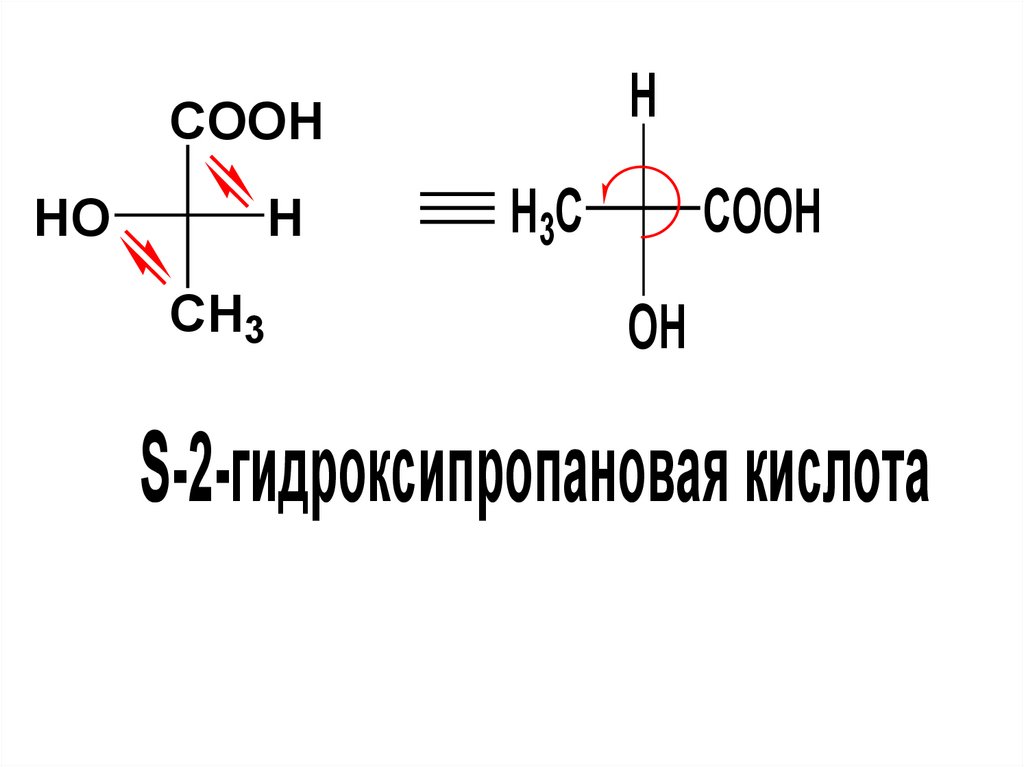
43.
HCOOH
НО
H
CH3
H3C
COOH
ОН
S-2-гидроксипропановая кислота
44. Диастереомерия
σ-Диастереомеры – это вещества,содержащие 2 и более центров
хиральности.
Число стереоизомеров определяют по
формуле:
n
N= 2
N-число стереоизомеров
n- число асимметрических центров
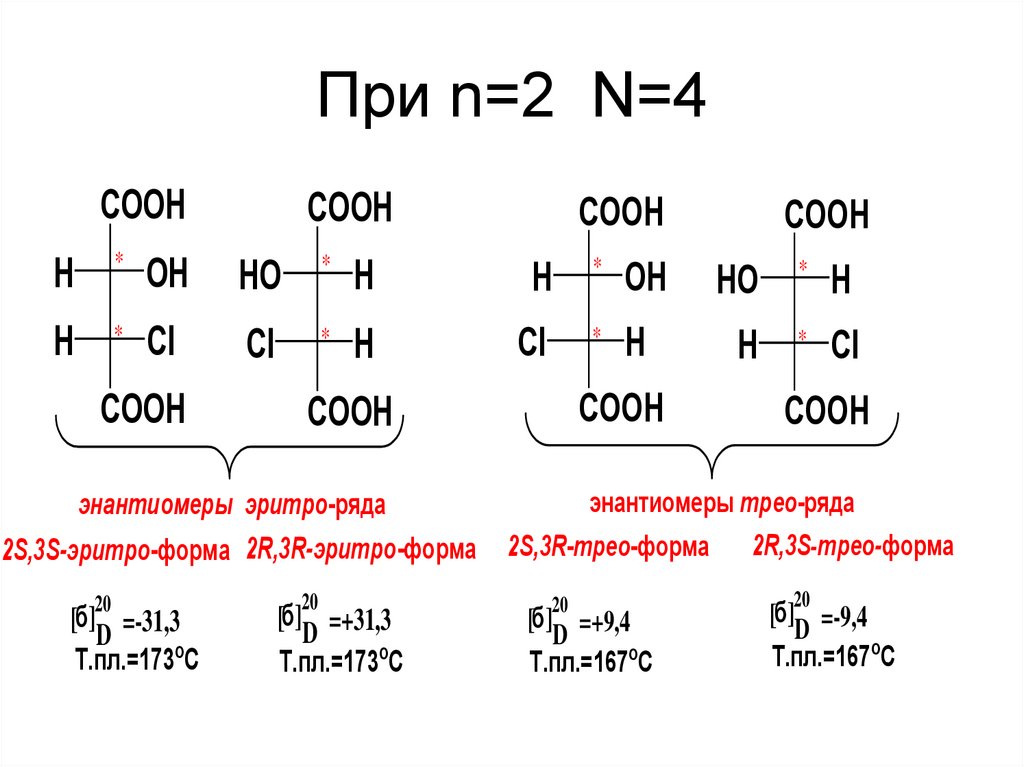
45. При n=2 N=4
COOHCOOH
COOH
COOH
H
*
OH
HO
*
H
H
*
OH
HO
*
H
H
*
Cl
Cl
*
H
Cl
*
H
H
*
Cl
COOH
COOH
COOH
COOH
энантиомеры трео-ряда
энантиомеры эритро-ряда
2S,3S-эритро-форма 2R,3R-эритро-форма 2S,3R-трео-форма 2R,3S-трео-форма
20
[б] =-31,3
D
Т.пл.=173оС
20
[б] =+31,3
D
Т.пл.=173оС
20
[б] =+9,4
D
Т.пл.=167оС
20
[б] =-9,4
D
Т.пл.=167оС
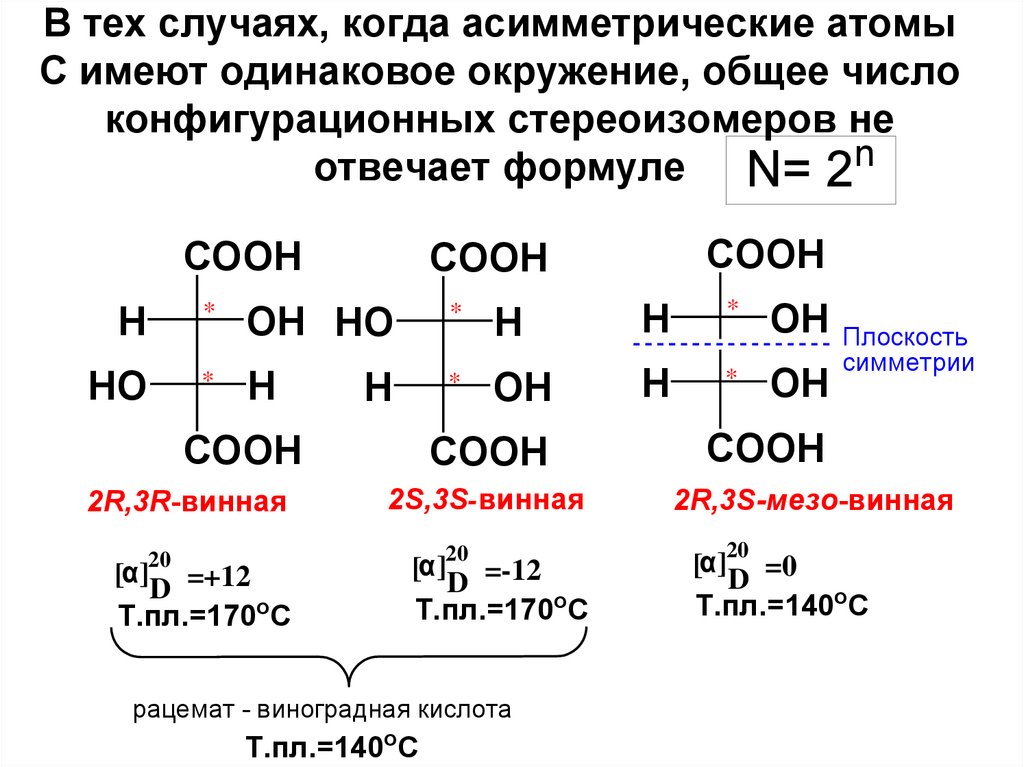
46. В тех случаях, когда асимметрические атомы С имеют одинаковое окружение, общее число конфигурационных стереоизомеров не
отвечает формуле N= 2nCOOH
H
*
OH HO
*
HO
*
H
*
H
COOH
2R,3R-винная
20
[α] =+12
D
Т.пл.=170оС
COOH
COOH
H
OH
COOH
2S,3S-винная
20
[α] =-12
D
Т.пл.=170оС
рацемат - виноградная кислота
Т.пл.=140оС
H
*
H
*
OH Плоскость
OH
симметрии
COOH
2R,3S-мезо-винная
20
[α] =0
D
Т.пл.=140оС
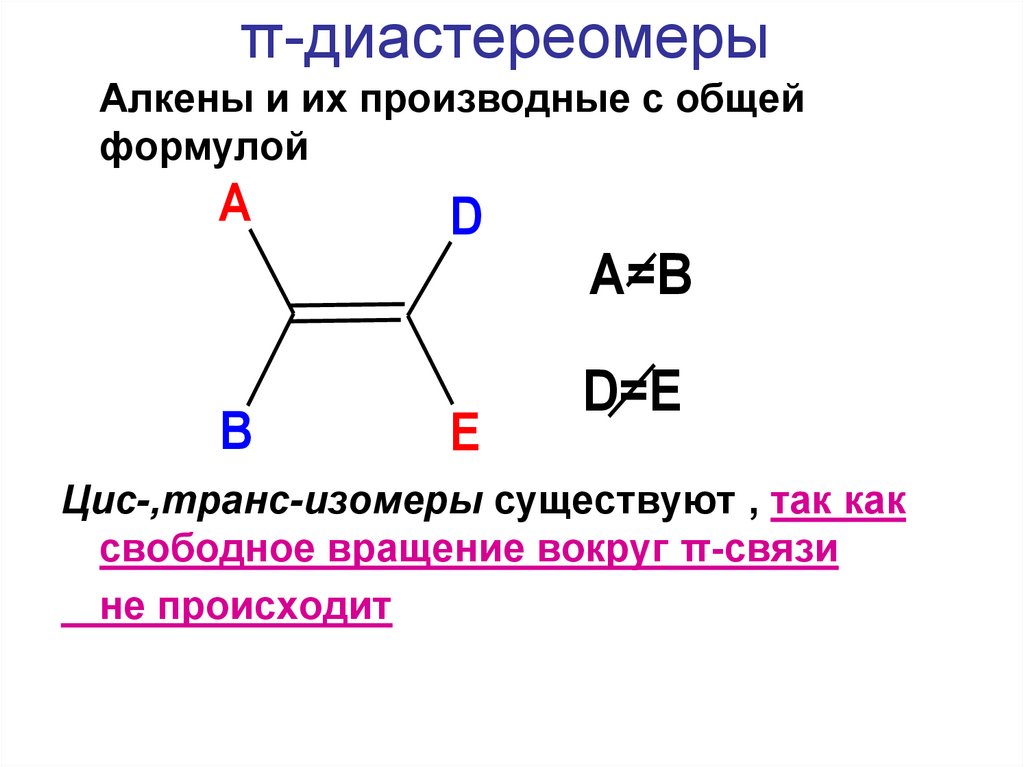
47. π-диастереомеры
Алкены и их производные с общейформулой
A
B
D
E
A=B
D=E
Цис-,транс-изомеры существуют , так как
свободное вращение вокруг π-связи
не происходит
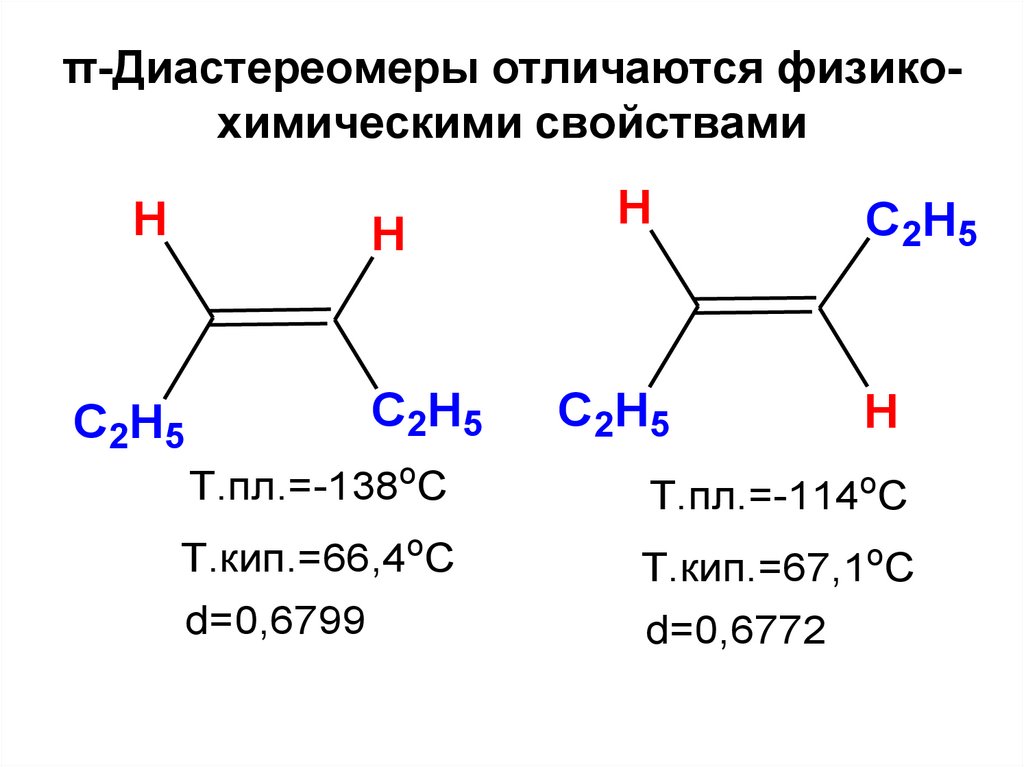
48. π-Диастереомеры отличаются физико-химическими свойствами
π-Диастереомеры отличаются физикохимическими свойствамиH
H
C2H5
C2H5
H
C2H5
C2H5
H
Т.пл.=-138оС
Т.пл.=-114оС
Т.кип.=66,4оС
Т.кип.=67,1оС
d=0,6799
d=0,6772
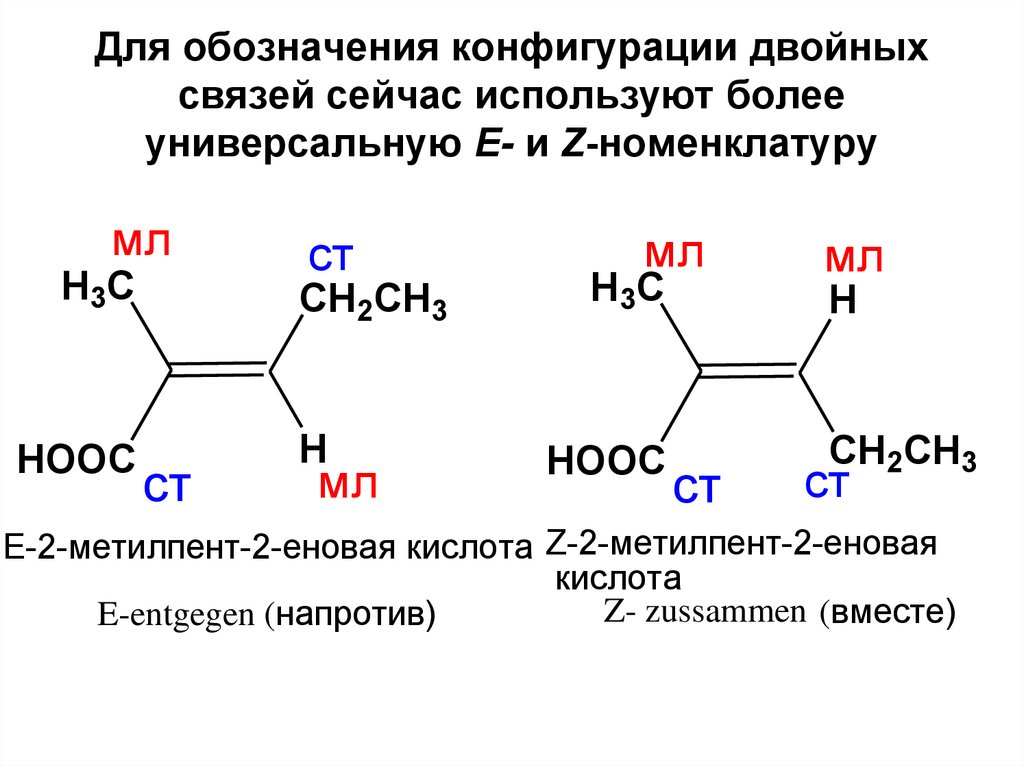
49. Для обозначения конфигурации двойных связей сейчас используют более универсальную Е- и Z-номенклатуру
млH3C
HOOC
ст
CH2CH3
ст
H
мл
мл
H3C
HOOC
мл
H
ст
CH2CH3
ст
E-2-метилпент-2-еновая кислота Z-2-метилпент-2-еновая
кислота
Z- zussammen (вместе)
E-entgegen (напротив)


















 chemistry
chemistry