Similar presentations:
Кислоты в животном мире
1.
„Поддельный перстень или золотой?Не станет ювелир гадать напрасно,
К металлу прикоснется кислотой И станет все через мгновенье ясно.“
Яков Абрамович Козловский,
перевод с лакского (Юсуп Хаппалаев)
2.
Кислоты в животном миреЕсть в муравьях и крапиве невинная,
С пользой для нас – кислота муравьиная.
Жжет она кожу, но есть в ней и прок –
Ваш ревматизм она вылечит в срок.
Голожаберные моллюски в
порядке самообороны
выстреливают парами
серной кислоты
Тропический паук педипальпида
стреляет во врагов струйкой жидкости,
содержащей 84% уксусной кислоты.
3.
Кислоты в растительном миреЛишайники выделяют кислоты,
которые разрушают
горные породы
Мухоморы в качестве ядовитых токсинов
«используют» иботеновую кислоту. Это
вещество так ядовито, что мухомору
незачем прятаться.
4.
Кислоты в жизни человекаВ организме
В кулинарии и продуктах питания
В медицине
В народном хозяйстве
Молочная
кислота
образуется в
мышцах при
нагрузке
Соляная кислота в желудке
способствует перевариванию пищи
5.
Кислотные дожди – одна изэкологических проблем
Н2О
Н2О
Н2О
SО2
NО2
Н2S
НNО2
Н2SО3
НNО3
6.
Тема урока: Химическиесвойства кислот.
Цель урока: Изучить
химические свойства,
характерные для класса
кислоты.
7.
«Химии никоем образомнаучиться невозможно, не видав
самой практики и не принимаясь
за химические операции»
М.В Ломоносов
8.
Техника безопасности при работе скислотами
1. Выполнять все указания учителя;
2. Не пробовать вещества на вкус;
3. Не приступать к выполнению опыта, не зная, что
и как нужно делать;
4. Обращаться с лабораторной посудой бережно;
5. Закончив работу, привести рабочее место в
порядок;
6. При попадании кислоты на кожу надо смыть её
струёй воды и обработать 2 % раствором
гидрокарбоната натрия.
9.
Химические свойства кислотИнструктивная карта
Действие кислот на
индикаторы
Взаимодействие кислот
с металлами и
оксидами металлов
Взаимодействие кислот
с основаниями
Взаимодействие кислот
с солями
Уравнение реакций
Выводы
10.
Химические свойства кислотИнструктивная
карта
Уравнение реакций
Действие кислот на
индикаторы
Лакмусовая бумага+ H 2SO4
красный
Фенолфталеин+ H 2SO4
бесцветный
Метилоранж+ H 2SO4
розовый
Независимо от вида
кислоты индикаторы
изменяют свой цвет
одинаково, а это означает,
что все кислоты обладают
сходными свойствами.
Zn+ H 2SO4 = ZnSO4 + H2↑
Cu+ H 2SO4 = реакция не идет
СuO + H 2SO4 = СuSO4 + H 2O
Если металл находится в
ряду напряжений до
водорода, то выделяется
водород и образуется соль.
При взаимодействии с
основными оксидами
образуется соль и вода.
Взаимодействие
кислот с металлами
и оксидами
металлов
Выводы
11.
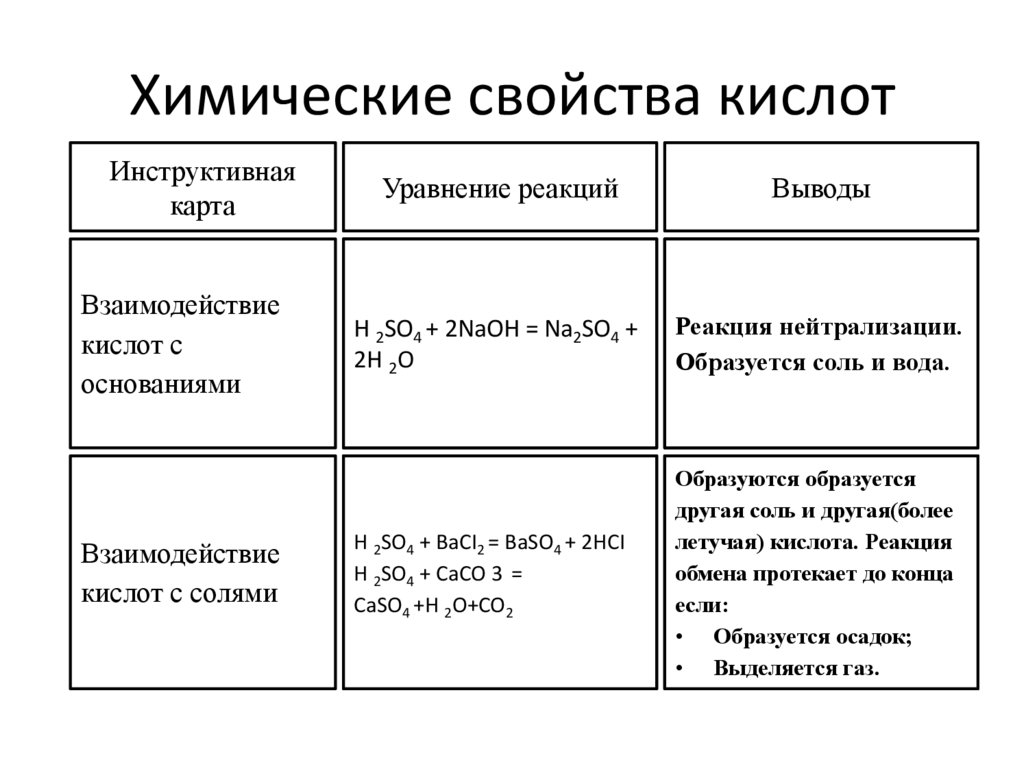
Химические свойства кислотИнструктивная
карта
Взаимодействие
кислот с
основаниями
Взаимодействие
кислот с солями
Уравнение реакций
Выводы
H 2SO4 + 2NaOH = Na2SO4 +
2H 2O
Реакция нейтрализации.
Образуется соль и вода.
H 2SO4 + BaCI2 = BaSO4 + 2HCI
H 2SO4 + CaCO 3 =
CaSO4 +H 2O+CO2
Образуются образуется
другая соль и другая(более
летучая) кислота. Реакция
обмена протекает до конца
если:
• Образуется осадок;
• Выделяется газ.
12.
Вопрос 1Выберите те металлы, которые вступают в реакцию с соляной кислотой:
• золото
• кальций
• медь
• магний
Вопрос 2
Лакмус в растворе серной кислоты приобретает окраску:
• синюю
• красную
• не меняет цвет
Вопрос 3
В реакцию с раствором соляной кислоты вступает следующий оксид:
• SO3
• CO
• MgO
• P2O5
Вопрос 4
В реакцию с раствором серной кислоты вступают следующие вещества:
• Na2CO3
• Н2CO3
• Ca(OH)2
• Au
13.
Продолжите фразы:СЕГОДНЯ НА УРОКЕ МНЕ БЫЛО ИНТЕРЕСНО …
У МЕНЯ БЫЛИ ЗАТРУДНЕНИЯ…
МНЕ ПОНРАВИЛОСЬ…
УЧАСТНИКИ МОЕЙ ГРУППЫ…
МНЕ НЕПОНЯТНО…
14.
Домашнее заданиеПараграф 45,
№ 2-4 стр.155 (письменно)













 chemistry
chemistry








