Similar presentations:
Гетероциклические соединения. Классификация гетероциклических соединений. Фуран. Производные фурана
1.
«Гетероциклические соединения.Классификация гетероциклических
соединений. Фуран. Производные
фурана»
2.
Гетероциклические соединения являются одной из групп,объединяющих лекарственные средства природного и синтетического
происхождения.
Важнейшие направления исследований лекарственных средств на
основе гетероциклических соединений.
Гетероциклические системы природных веществ как один из путей
создания новых лекарств. Исследования в области синтеза природных
гетероциклических соединений для изучения взаимосвязи между
биологической активностью и химической структурой. Синтетические
аналоги природных биологически активных веществ
гетероциклического ряда.
Классификация гетероциклических препаратов.
Применение общих химических и физических законов в порядке
требований к качеству лекарственных средств и методов анализа на
основе строения гетероциклических систем.
Кислородосодержащие гетероциклы. Фурановые, бензофурановые
производные.
5-нитрофурановые препараты: нитрофурол (фурацилин),
нитрофурантоин (фура-золидон), фуразидин (фурадонин), фурагин.
Производные бензофурана-амиодарон (кордарон).
3.
Гетероциклические соединения – этоциклические соединения, циклы которых
построены не только из атомов углерода, но
содержат также атомы других элементов
(гетероатомы).
Обычно гетероатомами являются азот,
кислород, сера. Гетероциклические соединения –
наиболее многочисленный класс органических
соединений. Они играют большую роль в
жизнедеятельности растительных и животных
организмов.
К ним относятся алкалоиды, витамины,
антибиотики, природные пигменты; они входят в
виде структурных фрагментов в молекулы
нуклеиновых кислот и белков.
4.
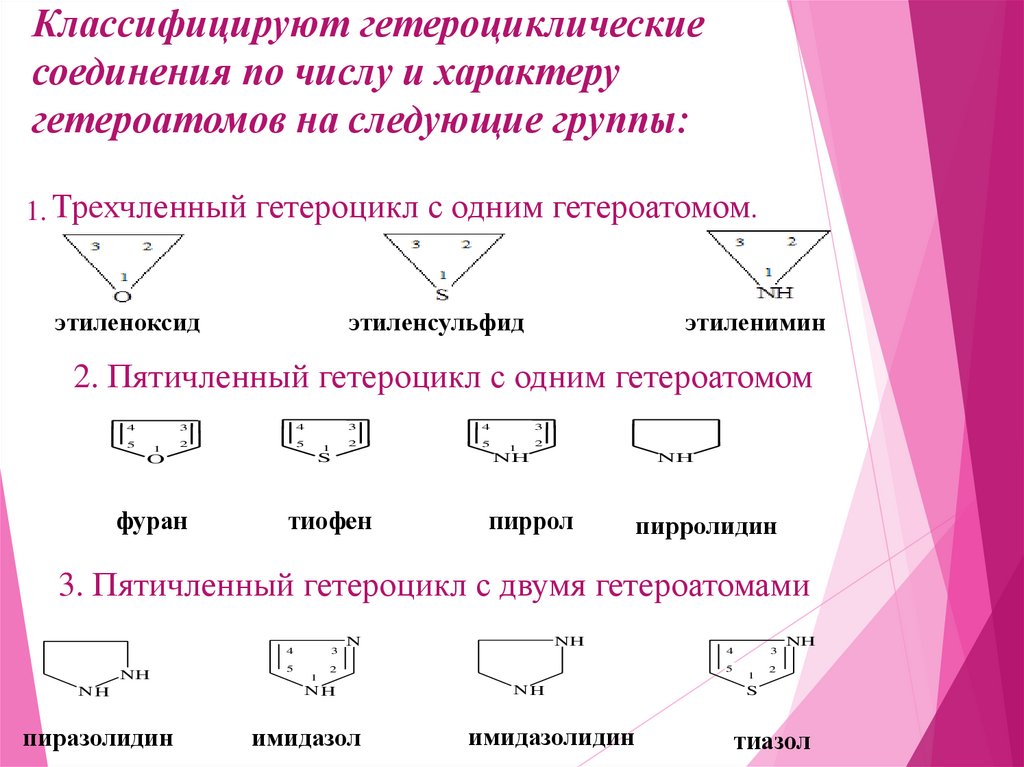
Классифицируют гетероциклическиесоединения по числу и характеру
гетероатомов на следующие группы:
1. Трeхчленный гетероцикл с одним гетероатомом.
этиленоксид
этиленсульфид
этиленимин
2. Пятичленный гетероцикл с одним гетероатомом
4
3
4
3
4
5
2
5
2
5
1
1
O
S
фуран
тиофен
3
1
2
NH
NH
пиррол
пирролидин
3. Пятичленный гетероцикл с двумя гетероатомами
4
NH
NH
пиразолидин
3
5
1
NH
N
5
2
NH
имидазол
4
NH
имидазолидин
3
1
NH
2
S
тиазол
5.
5. Шестичленный гетероцикл с несколькими гетероатомами4
5
6
1
4
3
5
2
6
N
N
N
5
2
6
1
N
пиридазин
NH
4
N
3
4
3
5
2
6
1
N
пиримидин
3
N5
2
6
1
NH
пиразин
пиперазин
4
N
3
2
1
N
1,3,5 - триазин
6. Семичленный гетероцикл с одним или двумя гетероатомами
N
5
5
4
6
7
3
6
2
7
S
2
1
4
3
7
2
6
3
4
1
1
5
NH
NH
NH
азепин
1,4-диазепин
1,5-тиазепин
6.
Лекарственные средства, имеющие гетероциклическую структуру,можно получить из природного сырья или синтетическим путем.
Некоторые гетероциклические соединения выделяют из продуктов
переработки каменноугольной смолы, содержащей пиридин и его
гомологи, хинолин, изохинолин, акридин, индол и др. Древесная смола
содержит метилфуран, фурфурол. Более сложные по химической
структуре гетероциклические соединения представляют собой многие
алкалоиды, витамины, ферменты, содержащиеся в растениях.
Способы синтеза гетероциклических соединений разнообразны. Их
синтезируют из ряда алифатических производных путем замыкания
цикла, превращения гетероциклов друг в друга (рециклизация),
гидрирования ненасыщенных гетероциклических соединений до
насыщенных, введения различных радикалов в простые по структуре
гстероциклы или получения из них конденсированных систем.
7.
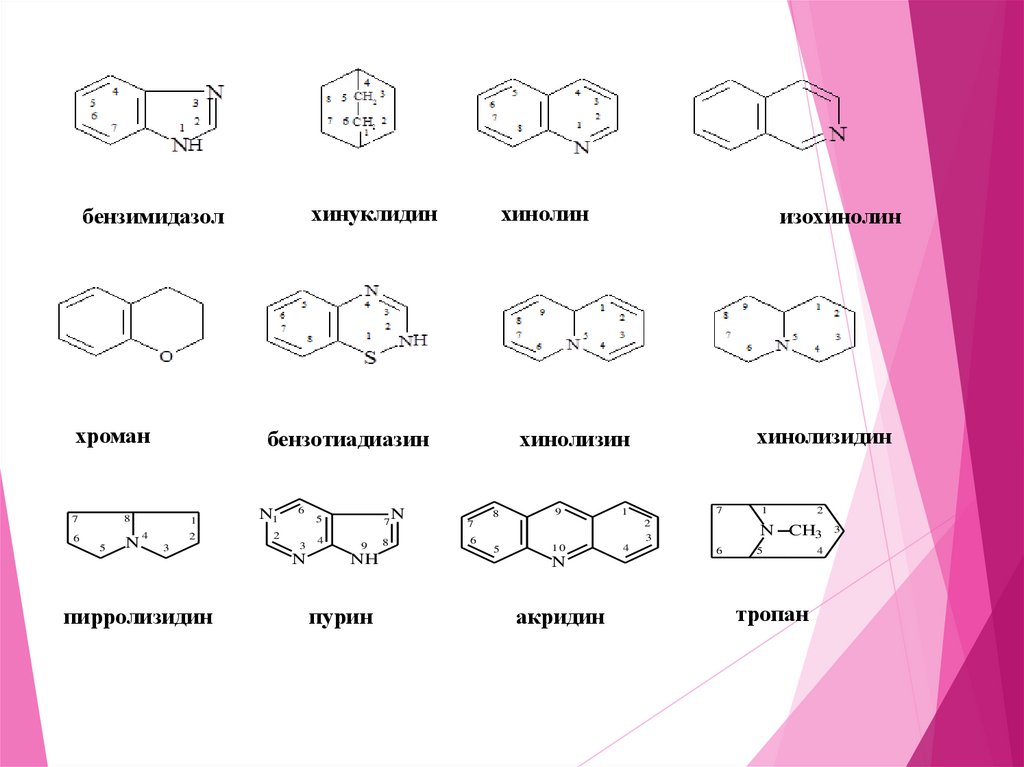
хинуклидинбензимидазол
хроман
бензотиадиазин
8
7
6
5
N
хинолин
4
1
N1
2
2
3
пирролизидин
6
3
N
5
4
7
9
NH
пурин
8
N
изохинолин
хинолизидин
хинолизин
8
9
6
7
1
2
3
7
5
10
N
акридин
4
1
2
N CH3
6
5
тропан
4
3
8.
22
1
3
4
8
10
A
11
4
12
11
12
10
13
9
14
5
15
7
морфинан
7
13
B
2
1
5
C
3
4
N
NH
21
D
14
15
NH
16
8
6
6
9
1
3
N
5
C H3
20
19
6
16
7
E 18
17
апорфин
аллойохимбан
CH
NH
9
2
1
8
3
7
5
6
CH
CH
4
N
1,4-бензодиазепин
9.
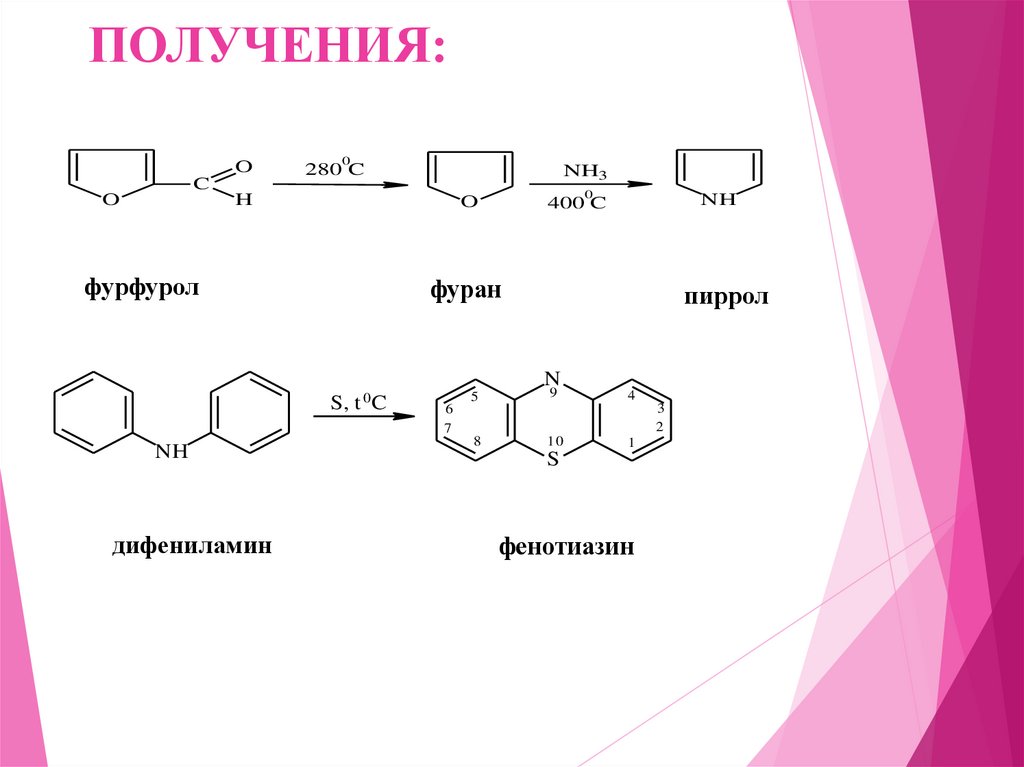
ПОЛУЧЕНИЯ:O
C
O
0
280 C
N H3
H
0
O
фурфурол
NH
400 C
фуран
пиррол
N
0
S, t C
NH
дифениламин
5
9
8
10
4
3
2
6
7
1
S
фенотиазин
10.
+ 2O
C
CH3CO
O
CH3CO
5
4
6
H
- 3 CH COOH
3
OH
7
2
1
O
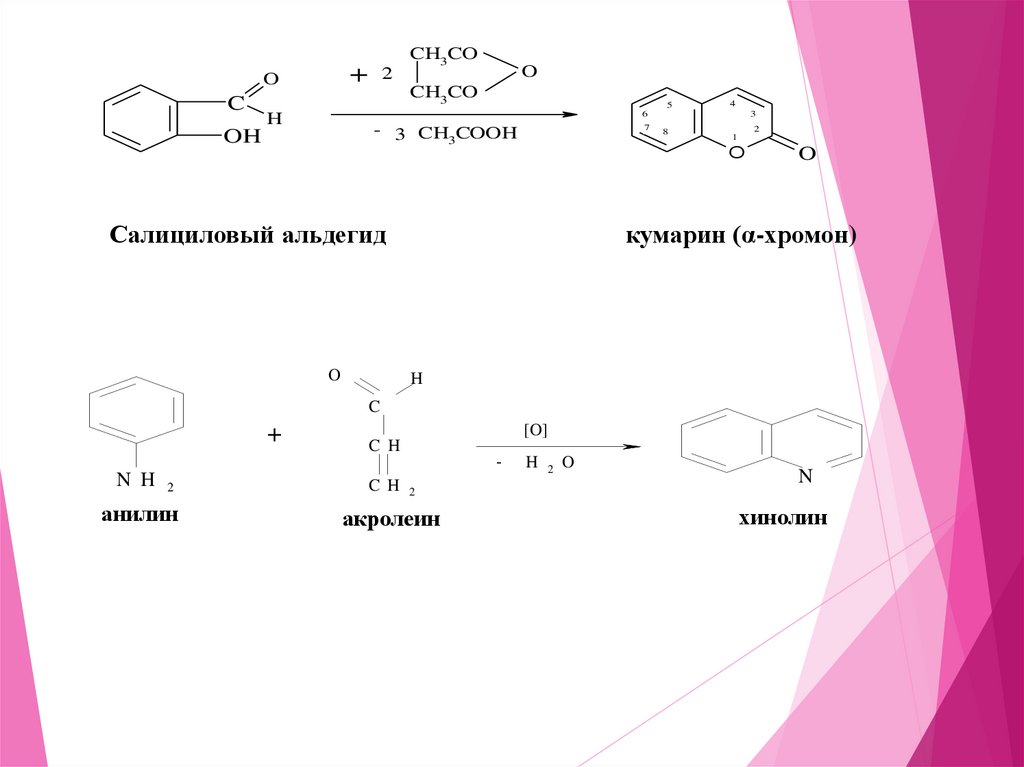
Салициловый альдегид
O
3
8
O
кумарин (α-хромон)
H
C
+
[O]
C H
-
N H 2
C H 2
анилин
акролеин
H 2 O
N
хинолин
11.
Фуран — органическое соединение с формулой C4H4O.Пятичленный гетероцикл с одним атомом кислорода.
Представляет собой бесцветную жидкость с характерным
запахом. Родоначальник большой группы органических соединений,
многие из которых имеют практическое значение, например
фурфурол, тетрагидрофуран, α-метилфуран (сильван). Фуран –
пятичленный гетероцикл с гетероатомом кислорода; ему, как и бензолу,
присущ ароматический характер Сам фуран не обладает
физиологической активностью, но его нитропроизводные,
особенно 2-нитрофуран используют как антибактериальные
средства. Они подавляют рост грамположительных,
грамотрицательных микробов в довольно высоких разведениях 1 :
10000, 1 : 20000.
12.
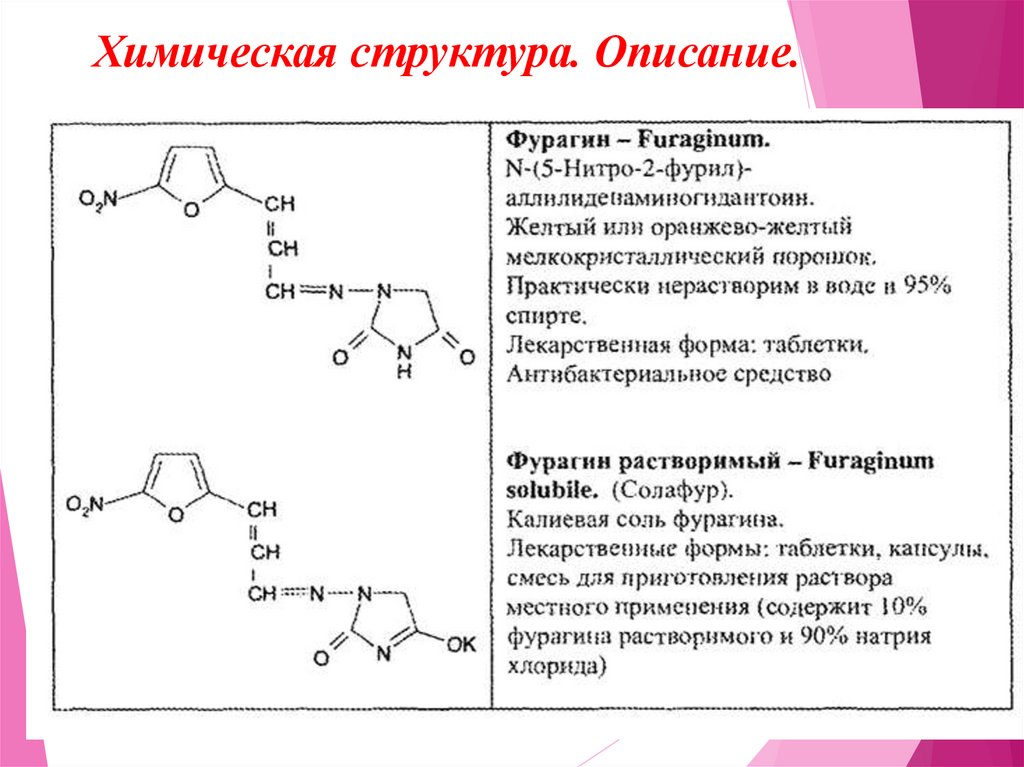
Химическая структура. Описание.13.
14.
Связь между структурой и фармацевтическимдействием
1. Наличия ароматической нитрогруппы в 5 положении
придаёт антибактериальное действие; проявляется в
отношении вирусов, простейших, грамположительных,
грамотрицательных бактерий – т. е. по действию близки к
антибиотикам. Но обладают меньшей токсичностью и
устойчивы при хранении.
2. Если перенести нитрогруппу в другое положение то
активность снизится; введение 2 нитрогруппы также
понизит активность.
3. Перенесение боковой цепи из положения 2 в любое другое
положение приводит к потере физиологической активности
4. Удлинение боковой цепи приводит к повышению
активности и снижению токсичности препарата.
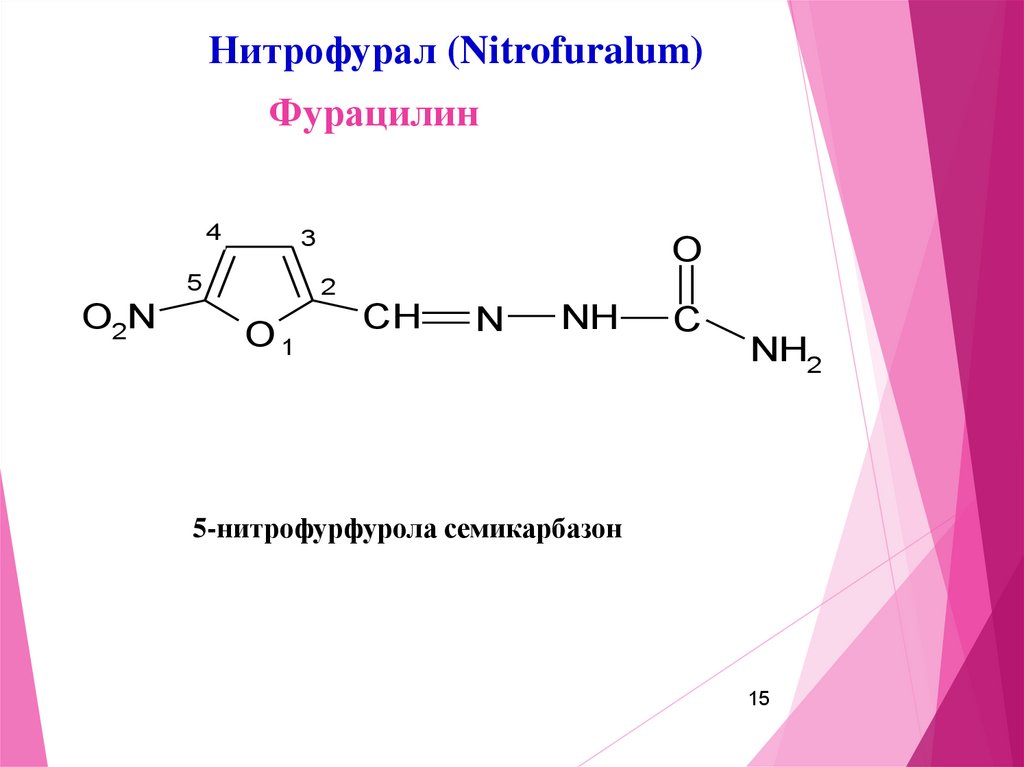
15.
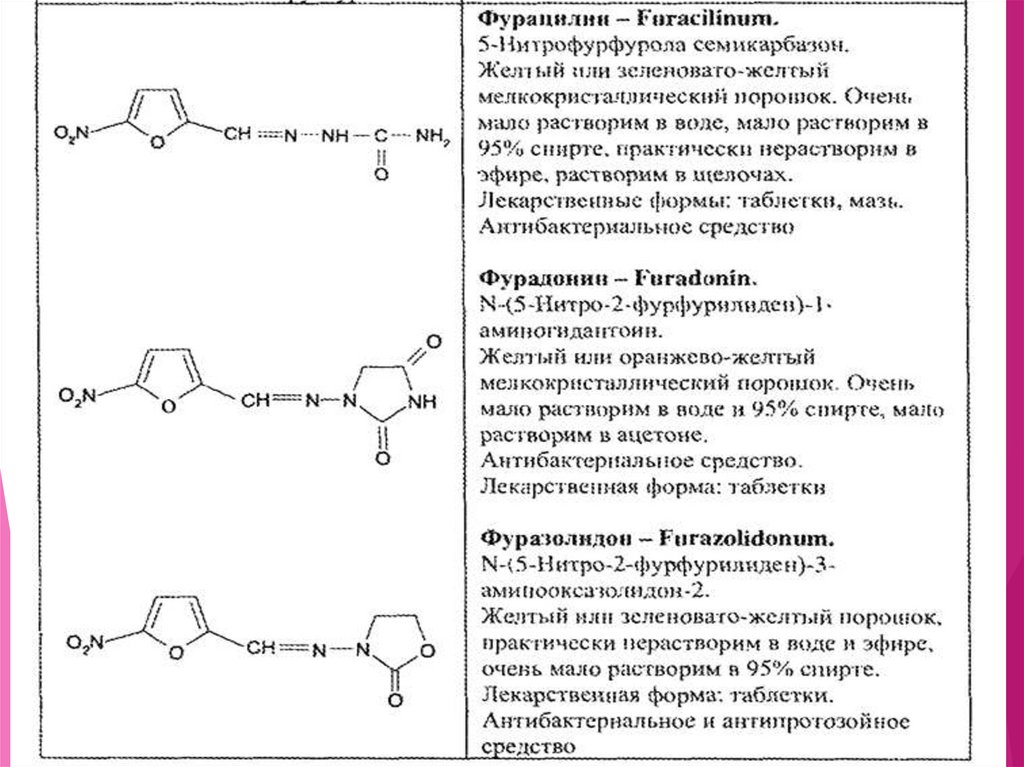
Нитрофурал (Nitrofuralum)Фурацилин
4
3
5
O2N
O
2
O1
CH
N
NH
C
NH2
5-нитрофурфурола семикарбазон
15
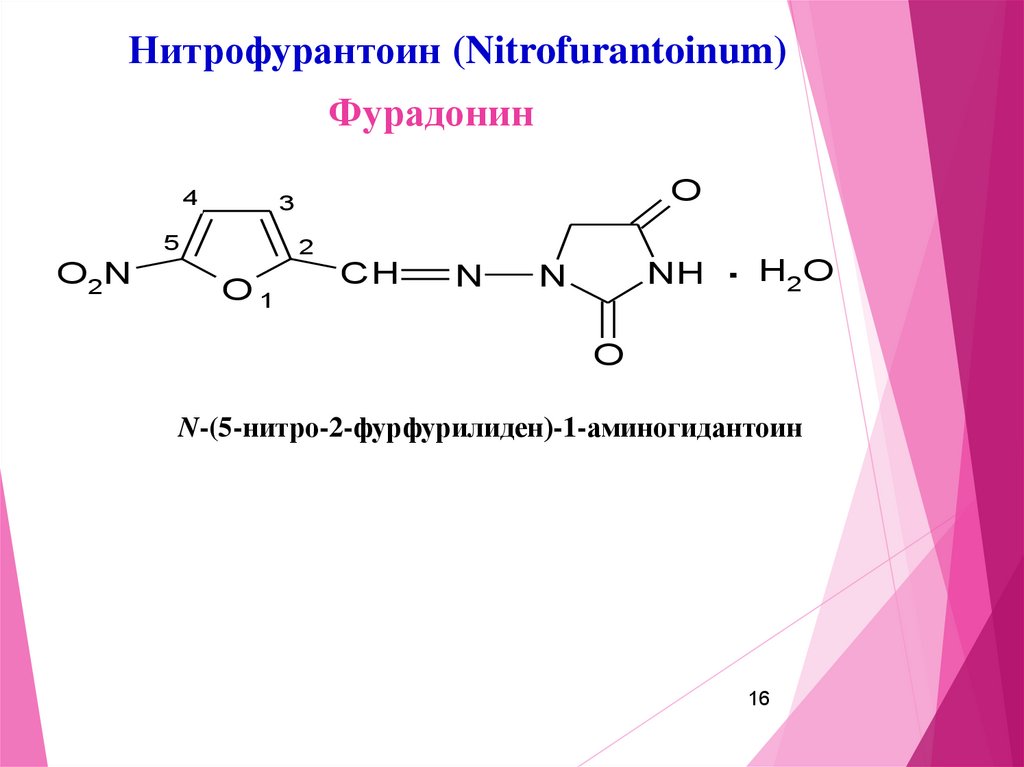
16.
Нитрофурантоин (Nitrofurantoinum)Фурадонин
4
5
O2N
O
3
2
O1
CH
N
NH
N
.HO
2
O
N-(5-нитро-2-фурфурилиден)-1-аминогидантоин
16
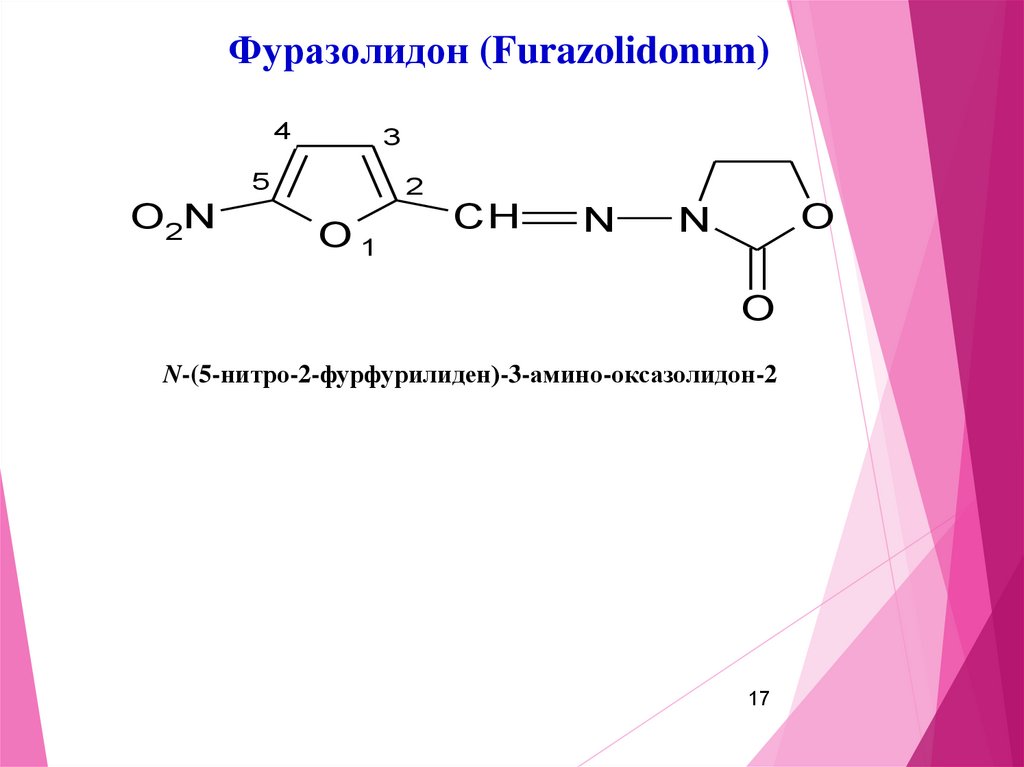
17.
Фуразолидон (Furazolidonum)4
3
5
O2N
2
O1
CH
N
O
N
O
N-(5-нитро-2-фурфурилиден)-3-амино-оксазолидон-2
17
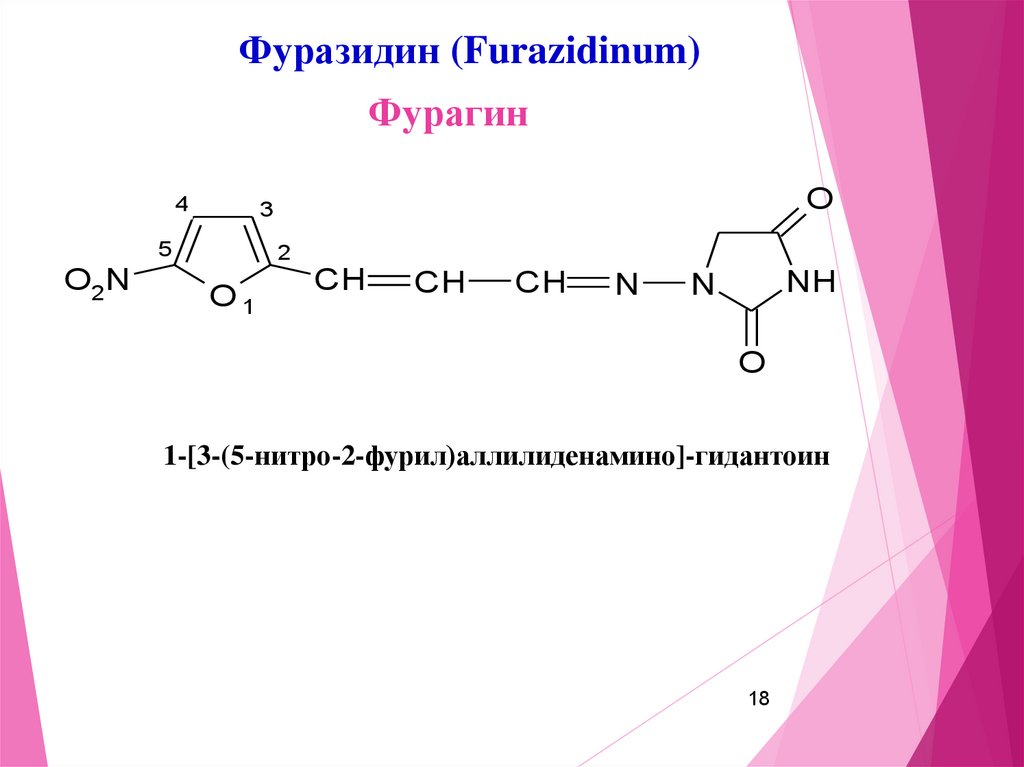
18.
Фуразидин (Furazidinum)Фурагин
4
5
O2N
O
3
2
O1
CH
CH
CH
N
NH
N
O
1-[3-(5-нитро-2-фурил)аллилиденамино]-гидантоин
18
19.
Это желтые с зеленоватым (нитрофурал,нитрофрантоин, фуразолидон) или оранжевым
оттенком (фуразидин) кристаллические вещества, без
запаха, горького вкуса, о.м.р. воде и спирте. Ввиду
наличия нитро и амидной групп нитрофурал имеет в
растворах кислую реакцию и лучше других
растворяется в щелочах
Фуразидин растворимый содержит 10% калиевой
соли фуразидина и 90% NaCl
19
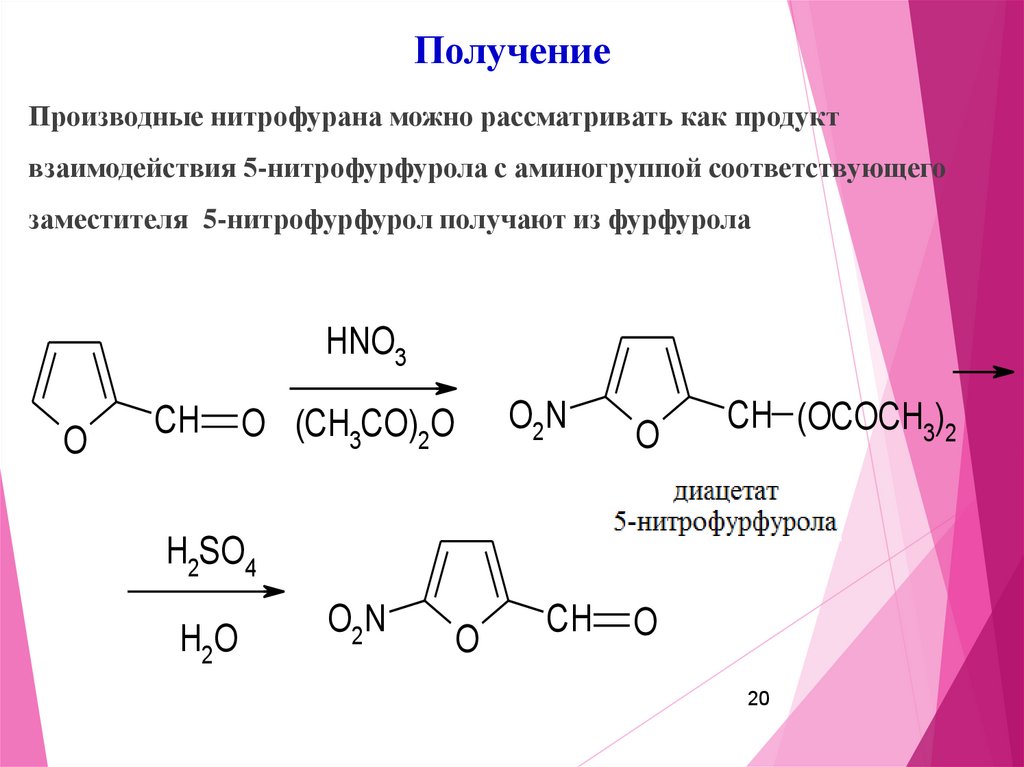
20.
ПолучениеПроизводные нитрофурана можно рассматривать как продукт
взаимодействия 5-нитрофурфурола с аминогруппой соответствующего
заместителя 5-нитрофурфурол получают из фурфурола
HNO3
O
CH
O (CH3CO)2O
O2N
O
CH
O
CH (OCOCH3)2
H2SO4
H2O
O2N
O
20
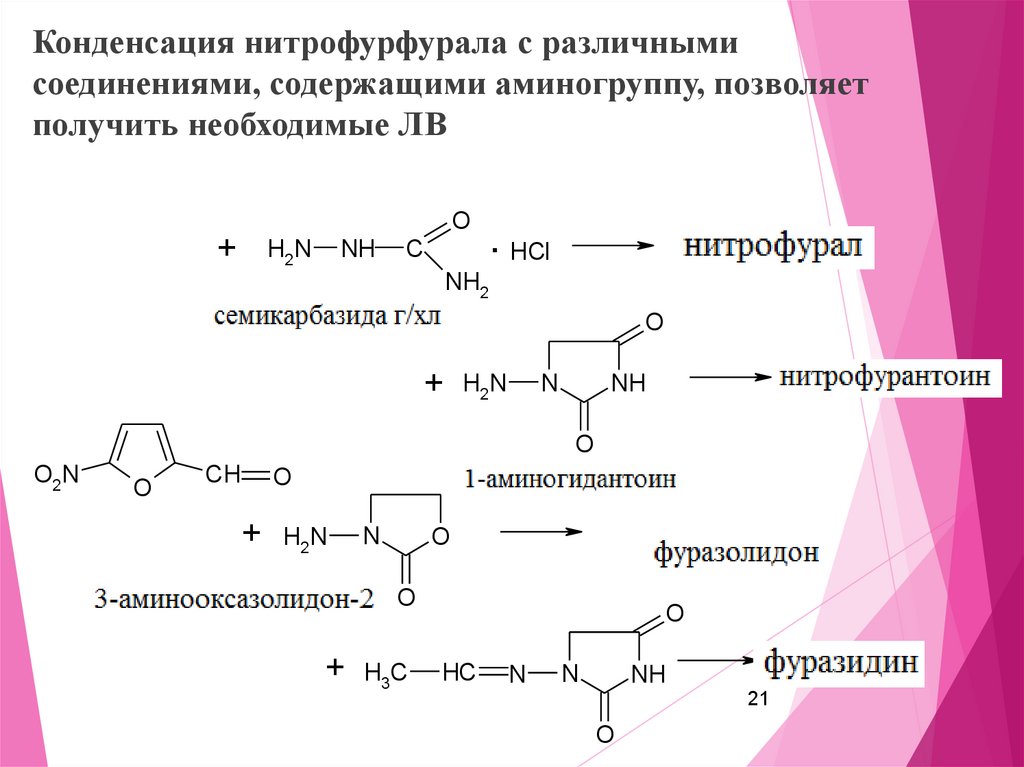
21.
Конденсация нитрофурфурала с различнымисоединениями, содержащими аминогруппу, позволяет
получить необходимые ЛВ
O
+
H2N
NH
C
. HCl
NH2
O
+ H2N
N
NH
O
O2N
O
CH
O
+ H2N
N
O
O
+ H3C
O
HC
N
N
NH
21
O
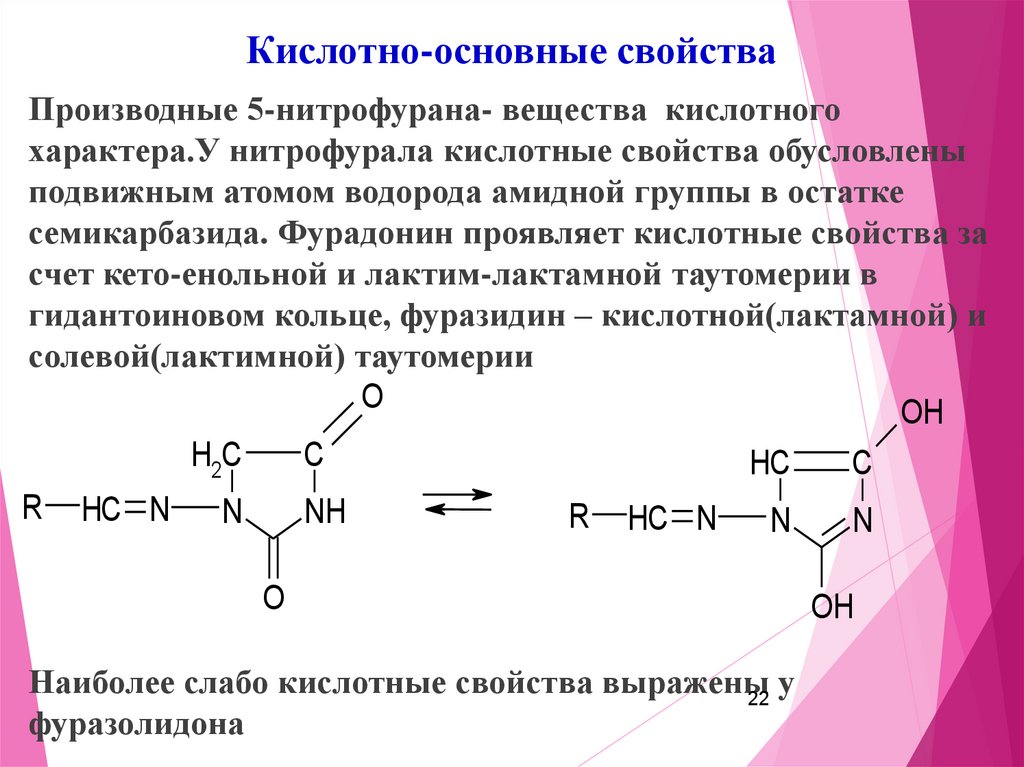
22.
Кислотно-основные свойстваПроизводные 5-нитрофурана- вещества кислотного
характера.У нитрофурала кислотные свойства обусловлены
подвижным атомом водорода амидной группы в остатке
семикарбазида. Фурадонин проявляет кислотные свойства за
счет кето-енольной и лактим-лактамной таутомерии в
гидантоиновом кольце, фуразидин – кислотной(лактамной) и
солевой(лактимной) таутомерии
O
OH
R
HC N
H2C
C
N
NH
R
HC N
HC
C
N
N
O
Наиболее слабо кислотные свойства выражены
у
22
фуразолидона
OH
23.
Реакции подлинности:Характерные цветные реакции, позволяющие отличать друг
от друга производные 5-нитрофурана, дает спиртовый
раствор гидроксида калия в сочетании с ацетоном:
нитрофурал приобретает темно-красное окрашивание,
нитрофурантоин — зеленовато-желтое, переходящее в
бурое с выпадением бурого осадка, фуразолидон —
постепенно появляющееся красное окрашивание,
переходящее в бурое, фуразидин приобретает красное
окрашивание с выпадением объемного красного осадка.
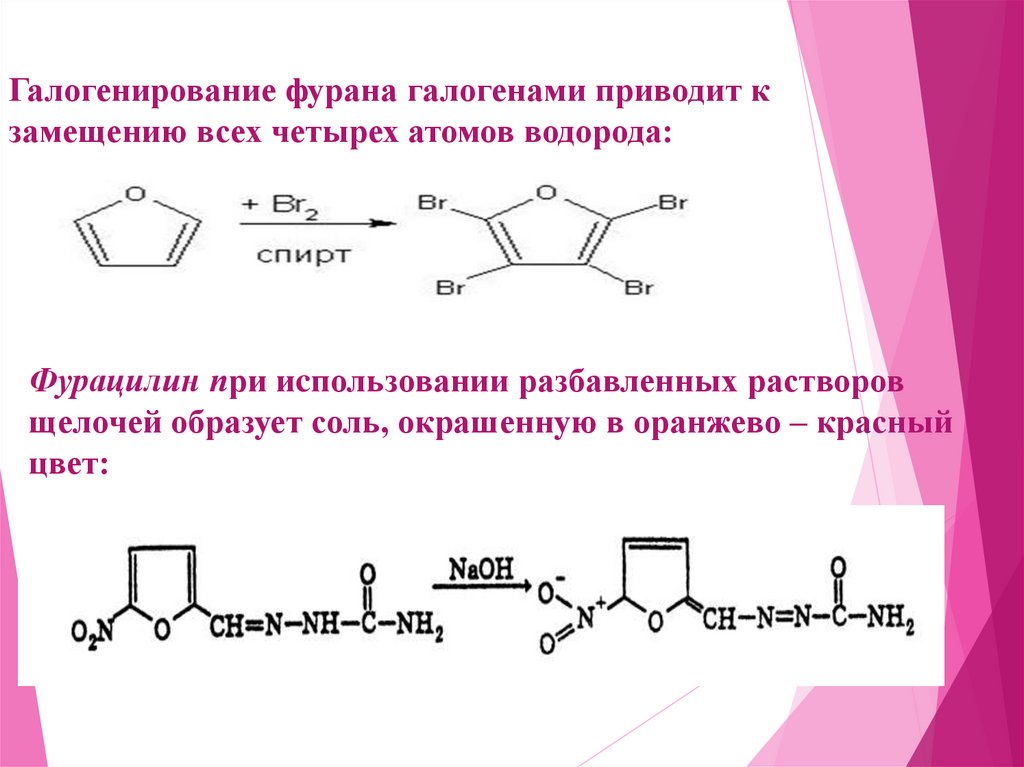
24.
Галогенирование фурана галогенами приводит кзамещению всех четырех атомов водорода:
Фурацилин при иcпользовании разбавленных растворов
щелочей образует соль, окрашенную в оранжево – красный
цвет:
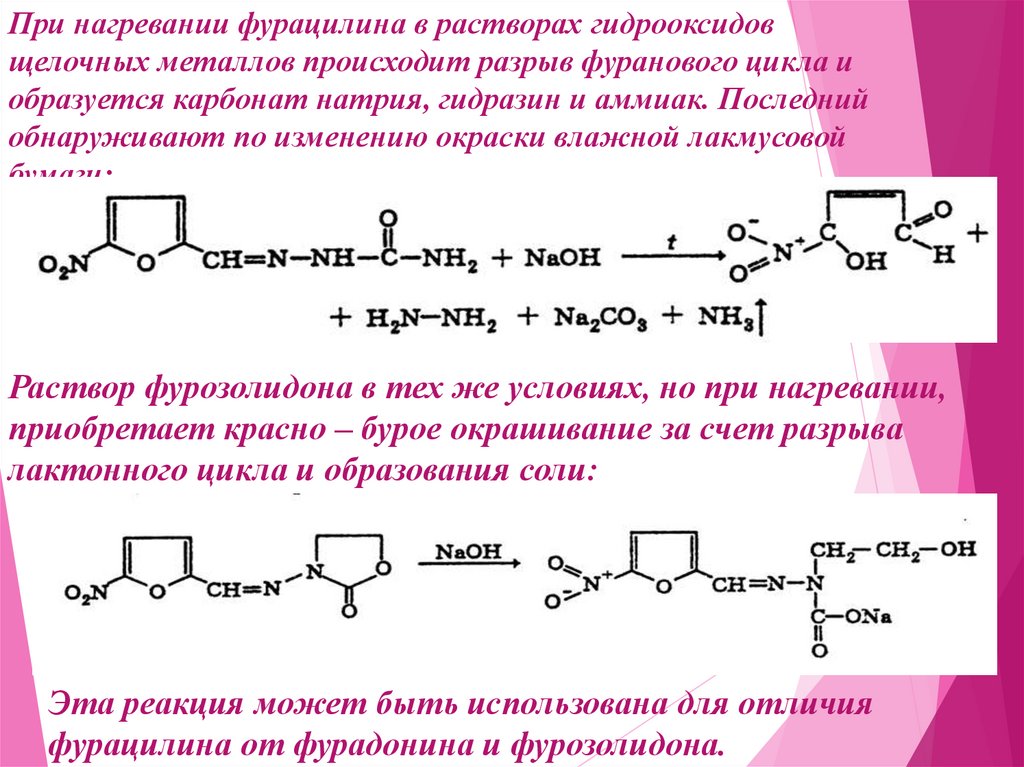
25.
При нагревании фурацилина в растворах гидрооксидовщелочных металлов происходит разрыв фуранового цикла и
образуется карбонат натрия, гидразин и аммиак. Последний
обнаруживают по изменению окраски влажной лакмусовой
бумаги:
Раствор фурозолидона в тех же условиях, но при нагревании,
приобретает красно – бурое окрашивание за счет разрыва
лактонного цикла и образования соли:
Эта реакция может быть использована для отличия
фурацилина от фурадонина и фурозолидона.
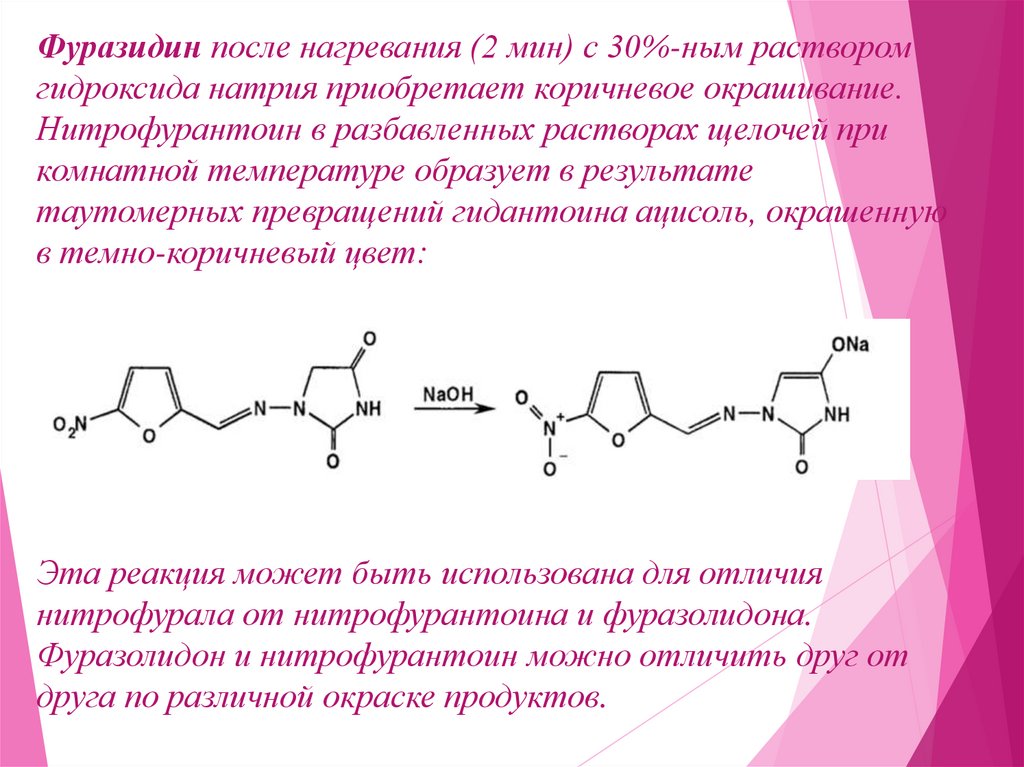
26.
Фуразидин после нагревания (2 мин) с 30%-ным растворомгидроксида натрия приобретает коричневое окрашивание.
Нитрофурантоин в разбавленных растворах щелочей при
комнатной температуре образует в результате
таутомерных превращений гидантоина ацисоль, окрашенную
в темно-коричневый цвет:
Эта реакция может быть использована для отличия
нитрофурала от нитрофурантоина и фуразолидона.
Фуразолидон и нитрофурантоин можно отличить друг от
друга по различной окраске продуктов.
27.
Кислотный характер производных 5-нитрофурана дает возможностьпроводить реакции комплексообразования с ионами тяжелых металлов
(Cu2+, Co2+, Ag+ )- образуются окрашенные комплексные соединения
(через Na соль). Эти реакции неспецифичны.
O
ONa
NH
R N
O
+ CuSO4
2+
Cu
NH
R N
O
+ Na2SO4
2
27
28.
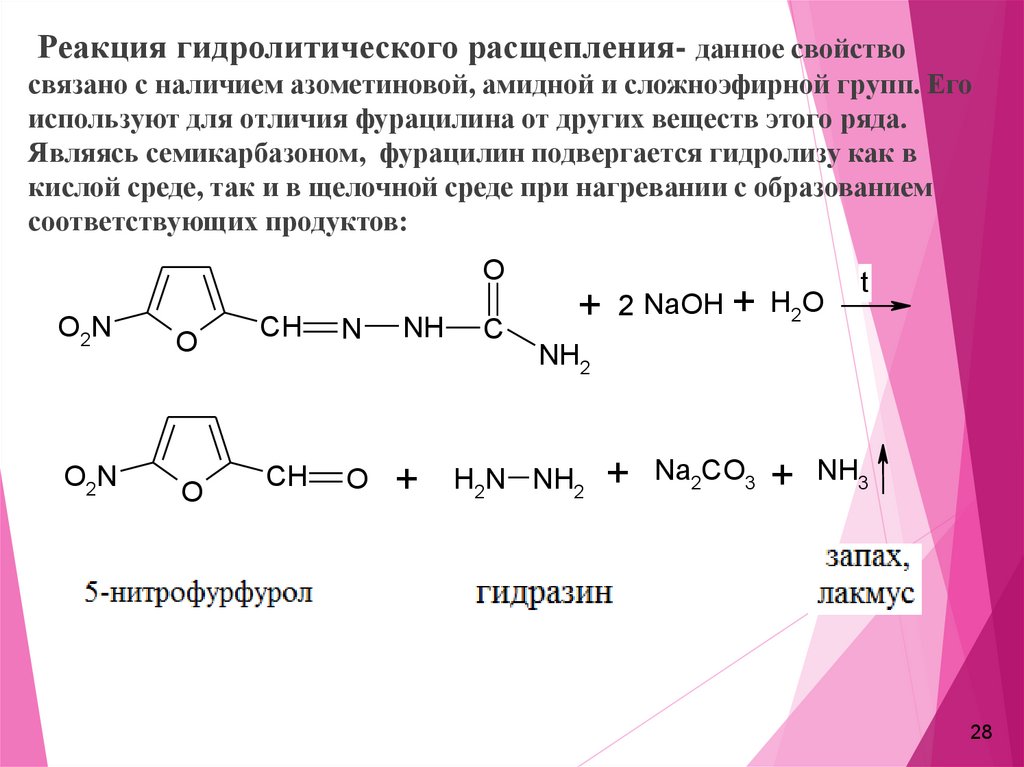
Реакция гидролитического расщепления- данное свойствосвязано с наличием азометиновой, амидной и сложноэфирной групп. Его
используют для отличия фурацилина от других веществ этого ряда.
Являясь семикарбазоном, фурацилин подвергается гидролизу как в
кислой среде, так и в щелочной среде при нагревании с образованием
соответствующих продуктов:
O
O2N
O2N
O
O
CH
CH
N
NH
O
+
C
+ 2 NaOH + H2O
t
NH2
H2N NH2
+ Na2CO3 + NH3
28
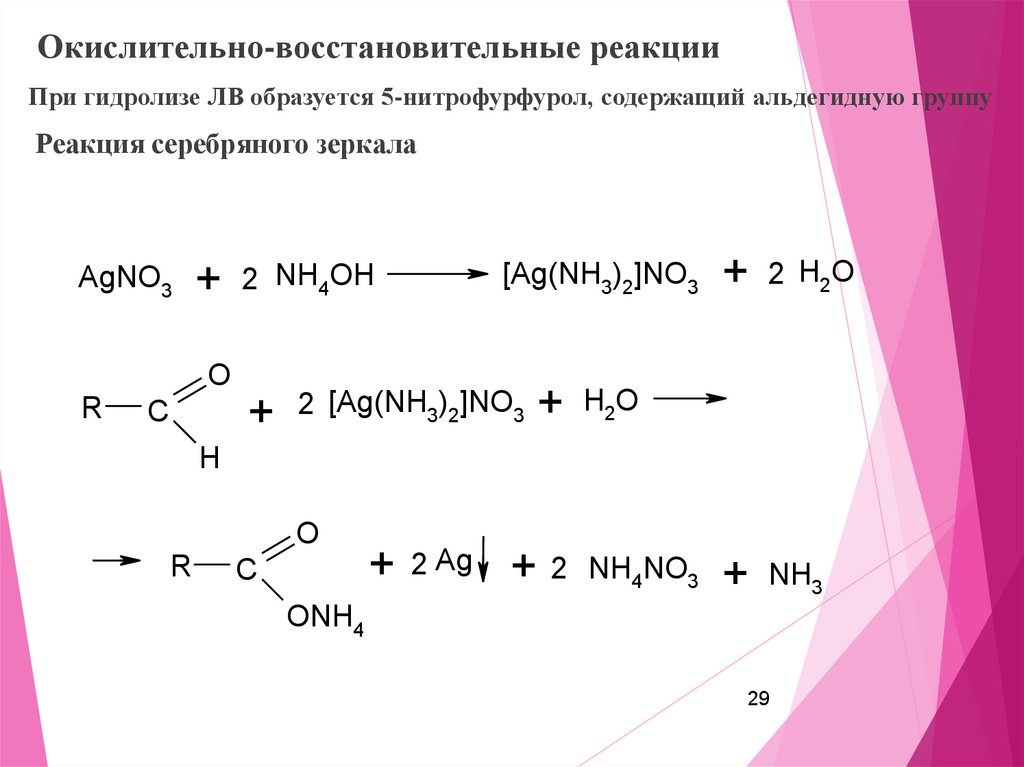
29.
Окислительно-восстановительные реакцииПри гидролизе ЛВ образуется 5-нитрофурфурол, содержащий альдегидную группу
Реакция серебряного зеркала
AgNO3
+ 2 NH4OH
O
R
C
[Ag(NH3)2]NO3
+ 2 H2O
+ 2 [Ag(NH3)2]NO3 + H2O
H
O
R
C
+ 2 Ag + 2 NH4NO3 + NH3
ONH4
29
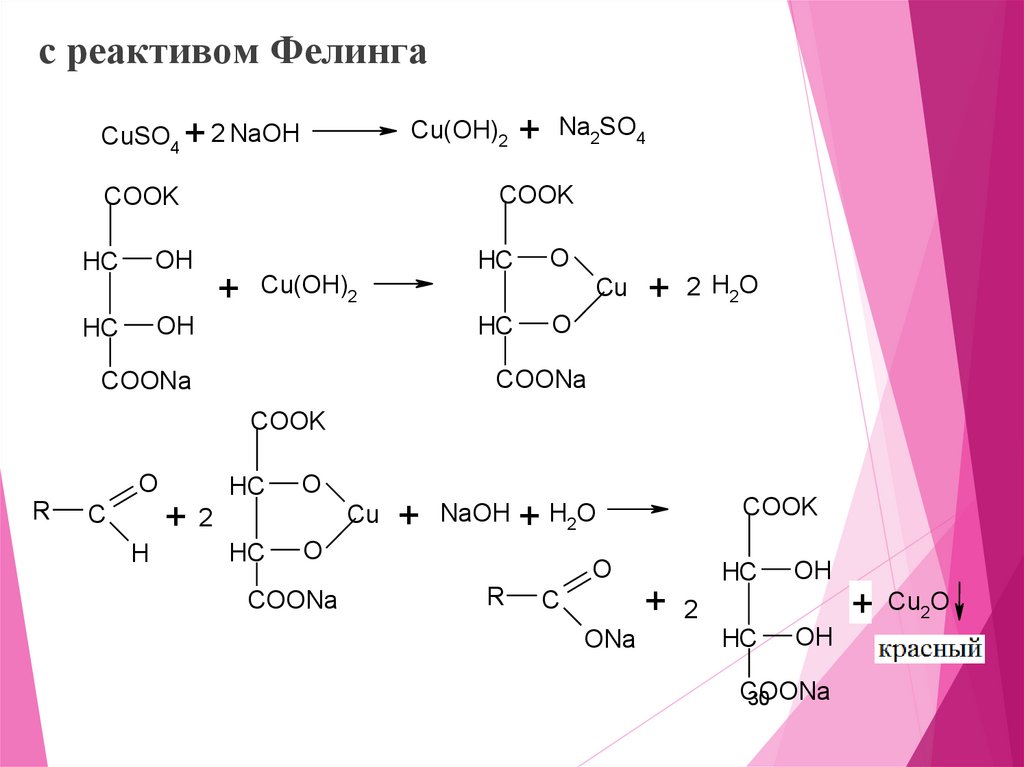
30.
с реактивом ФелингаCu(OH)2 + Na2SO4
CuSO4 + 2 NaOH
COOK
COOK
OH
HC
HC
O
+ Cu(OH)2
OH
HC
Cu
HC
+ 2 H2O
O
COONa
COONa
COOK
O
R
HC
O
+2
C
H
Cu
HC
O
COONa
COOK
+ NaOH + H2O
O
R
HC
OH
+ 2
C
ONa
+ Cu2O
HC
OH
COONa
30
31.
С реактивом НесслераO
R
+ K2HgI4 + 3 KOH
C
H
O
R
C
+ 4 KI + Hg + 2 H2O
OK
Если нагревать нитрофурфурол с Zn в HCl, то образуется
аминогруппа, но соединения неустойчивы, фурановый цикл
разрывается и азокраситель получить не удается
31
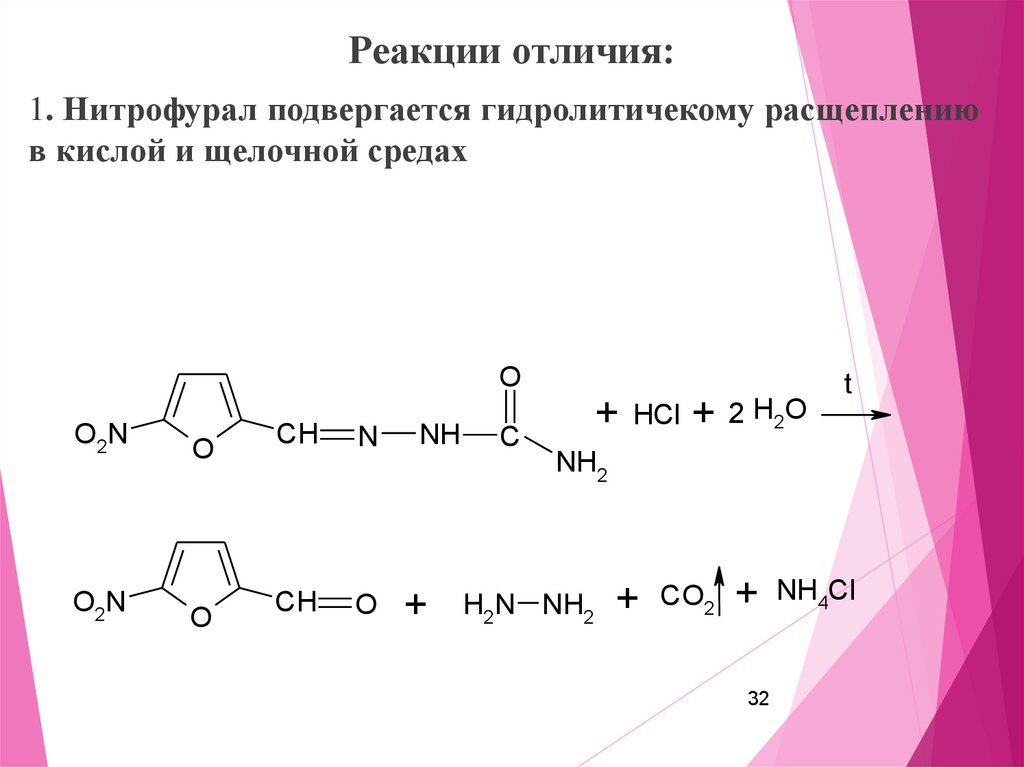
32.
Реакции отличия:1. Нитрофурал подвергается гидролитичекому расщеплению
в кислой и щелочной средах
O
O2N
O2N
O
O
CH
CH
N
NH
O
+
C
+ HCl + 2 H2O
t
NH2
H2N NH2
+ CO2 + NH4Cl
32
33.
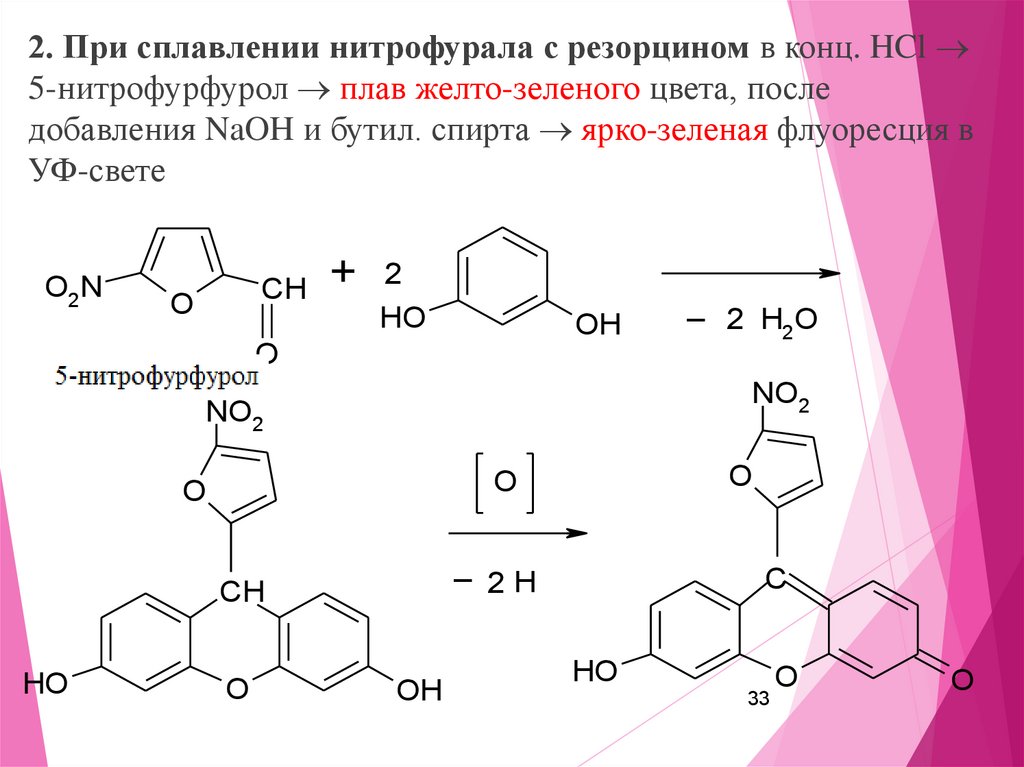
2. При сплавлении нитрофурала с резорцином в конц. HCl5-нитрофурфурол плав желто-зеленого цвета, после
добавления NaOH и бутил. спирта ярко-зеленая флуоресция в
УФ-свете
O2N
CH
O
+ 2
HO
OH
O
NO2
NO2
O
O
O
_
CH
HO
O
_ 2 HO
2
OH
C
2H
HO
33
O
O
34.
ПримесиВ ЛВ устанавливают содержание посторонних примесей –
ТСХ
В фуразидине определяют отсутствие легко обугливающихся
(при 250 оС) примесей
34
35.
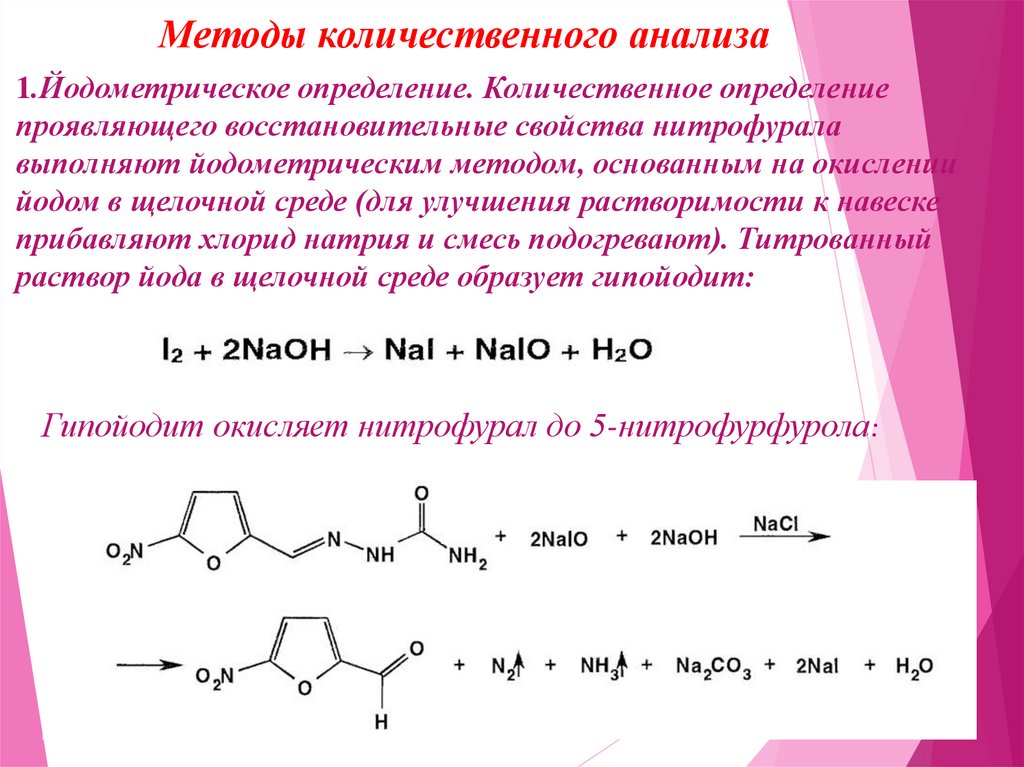
Методы количественного анализа1.Йодометрическое определение. Количественное определение
проявляющего восстановительные свойства нитрофурала
выполняют йодометрическим методом, основанным на окислении
йодом в щелочной среде (для улучшения растворимости к навеске
прибавляют хлорид натрия и смесь подогревают). Титрованный
раствор йода в щелочной среде образует гипойодит:
Гипойодит окисляет нитрофурал до 5-нитрофурфурола:
36.
После окончания процесса окисления нитрофурала растворподкисляют и титруют выделившийся избыток йода тиосульфатом
натрия:
2. Известен способ определения нитрофурала броматометрическим
методом, основанным на окислении гидразиновой группы в
присутствии концентрированных кислот при температуре 80-90°С:
3.Фуразидин-калий количественно определяют ацидиметрически,
титруя 0,01 М раствором хлороводородной кислоты (индикатор
бромтимоловый синий).
4.Количественное определение нитрофурала, нитрофурантоина и
фуразолидона можно проводить фотоколориметрическим
методом, основанным на использовании цветных реакций с едкой
щелочью в различных растворителях.
37.
За последние годы химия фурана развивалась весьма успешно ифурановые соединения стали играть заметную практическую
роль и сами по себе, и как полупродукты в органическом
синтезе.
Нитрофураны имеют значение, главным образом, при лечении
острых неосложненных форм инфекции, кишечных и
протозойных инфекций
Оказывают бактериостатический или бактерицидный
эффект. К нитрофуранам редко развивается лекарственная
резистентность микроорганизмов.
Нитрофураны характеризуются достаточно широким
спектром действия.
Быстро выводятся из организма.
38.
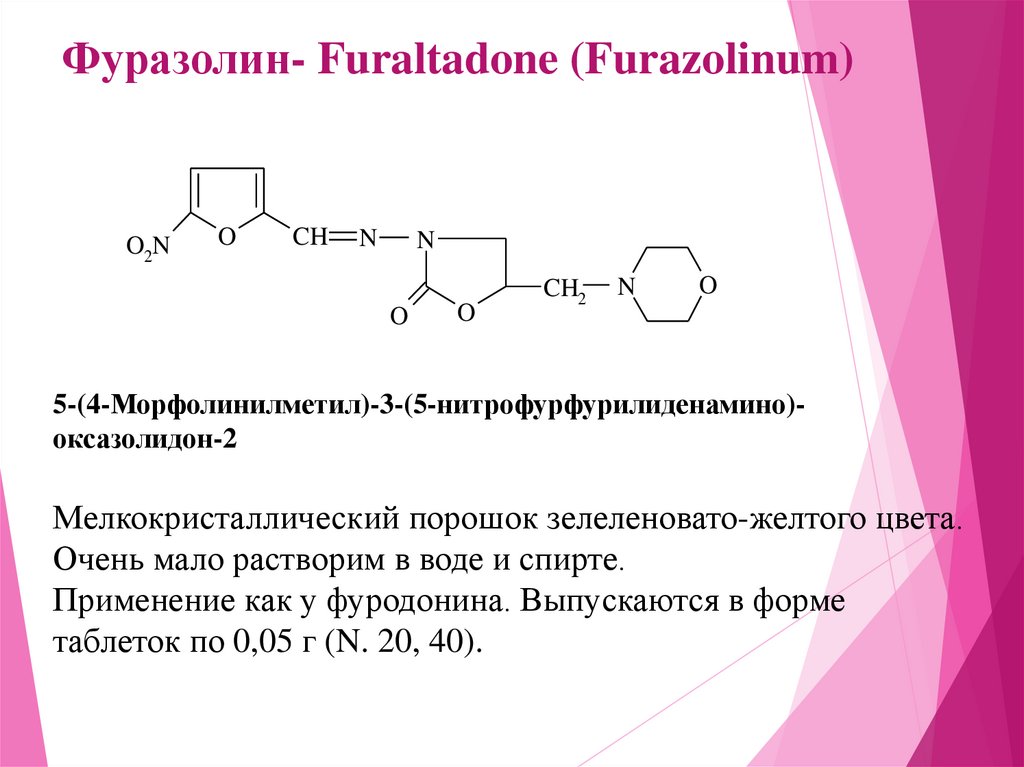
Фуразолин- Furaltadone (Furazolinum)O2N
O
CH
N
N
O
O
CH2
N
O
5-(4-Морфолинилметил)-3-(5-нитрофурфурилиденамино)оксазолидон-2
Мелкокристаллический порошок зелеленовато-желтого цвета.
Очень мало растворим в воде и спирте.
Применение как у фуродонина. Выпускаются в форме
таблеток по 0,05 г (N. 20, 40).
39.
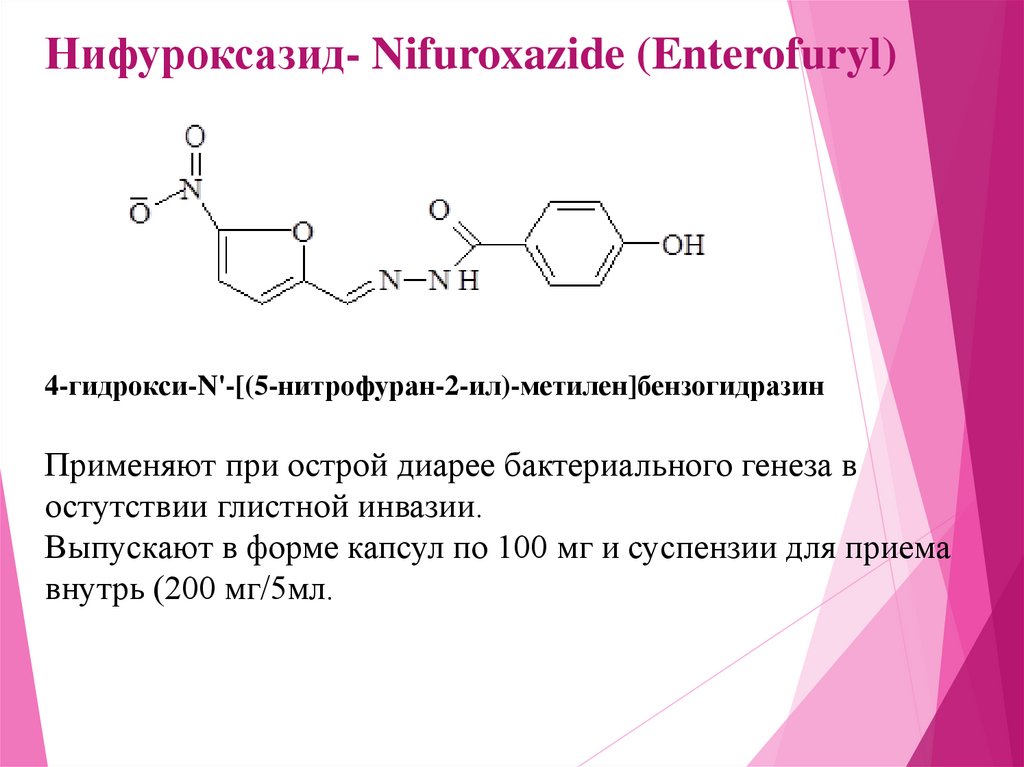
Нифуроксазид- Nifuroxazide (Enterofuryl)4-гидрокси-N'-[(5-нитрофуран-2-ил)-метилен]бензогидразин
Применяют при острой диарее бактериального генеза в
остутствии глистной инвазии.
Выпускают в форме капсул по 100 мг и суспензии для приема
внутрь (200 мг/5мл.
40.
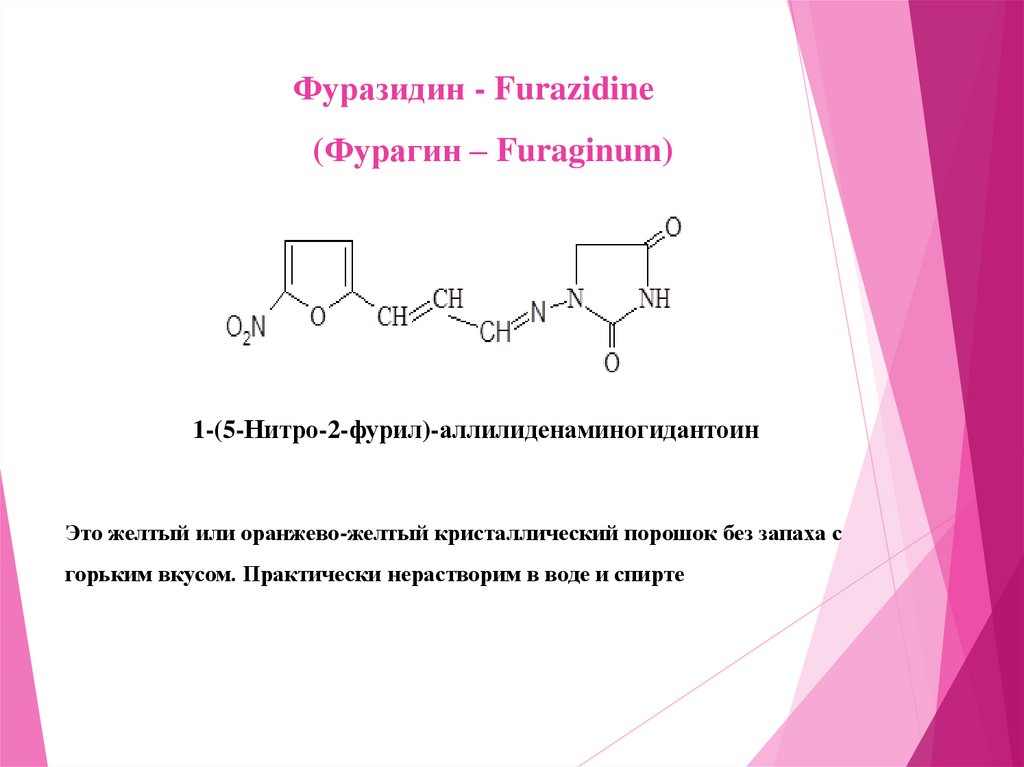
Фуразидин - Furazidine(Фурагин – Furaginum)
1-(5-Нитро-2-фурил)-аллилиденаминогидантоин
Это желтый или оранжево-желтый кристаллический порошок без запаха с
горьким вкусом. Практически нерастворим в воде и спирте
41.
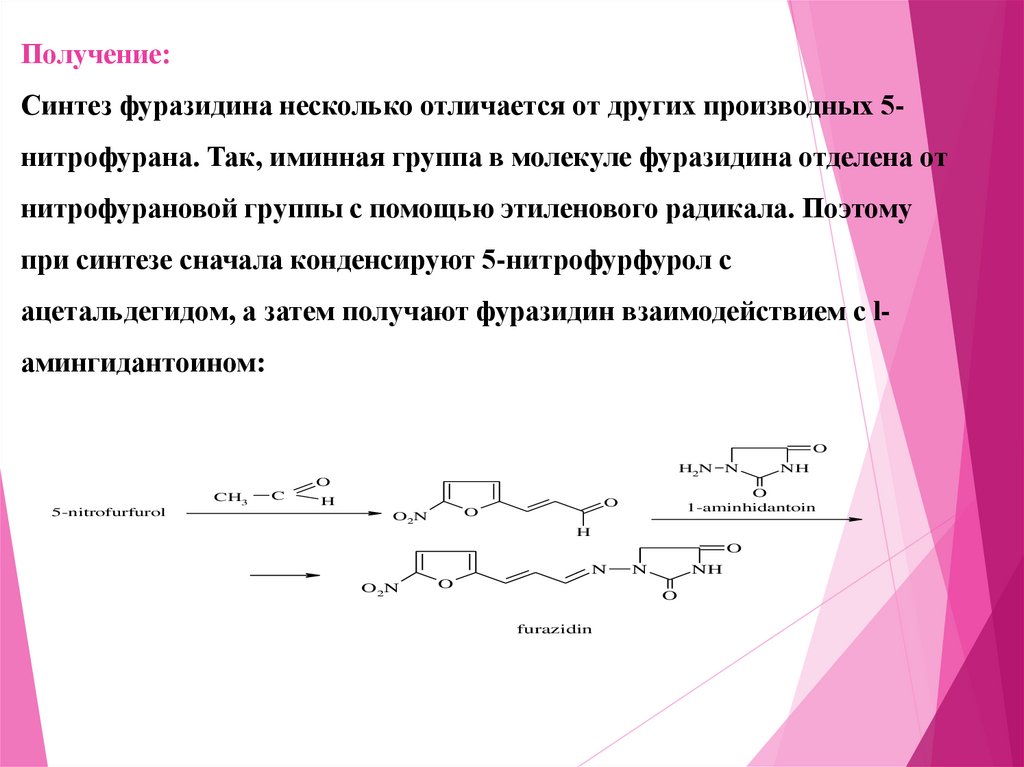
Получение:Синтез фуразидина несколько отличается от других производных 5нитрофурана. Так, иминная группа в молекуле фуразидина отделена от
нитрофурановой группы с помощью этиленового радикала. Поэтому
при синтезе сначала конденсируют 5-нитрофурфурол с
ацетальдегидом, а затем получают фуразидин взаимодействием с l-
амингидантоином:
O
H2N N
O
CH3
5-nitrofurfurol
C
H
O2N
O
1-aminhidantoin
O
O
H
O
N
O2N
N
NH
O
O
furazidin
NH
42.
Количественное определение фурагина проводят с помощью УФспектрофотометрии (0,6% раствор диметилформамида врастворитель-ацетатном буферном растворе).
Назначают внутрь и наружно. Внутрь при инфекционных
заболеваниях почек и мочевыводящих путей, местно изотонические растворы 1:13000 применяют для промывания ран,
а также для клизм, в акушерско-гинекологической практике, а
также для лечения гнойных ран и ожогов. Выпускаются таблетки
по 0,05 г.
43.
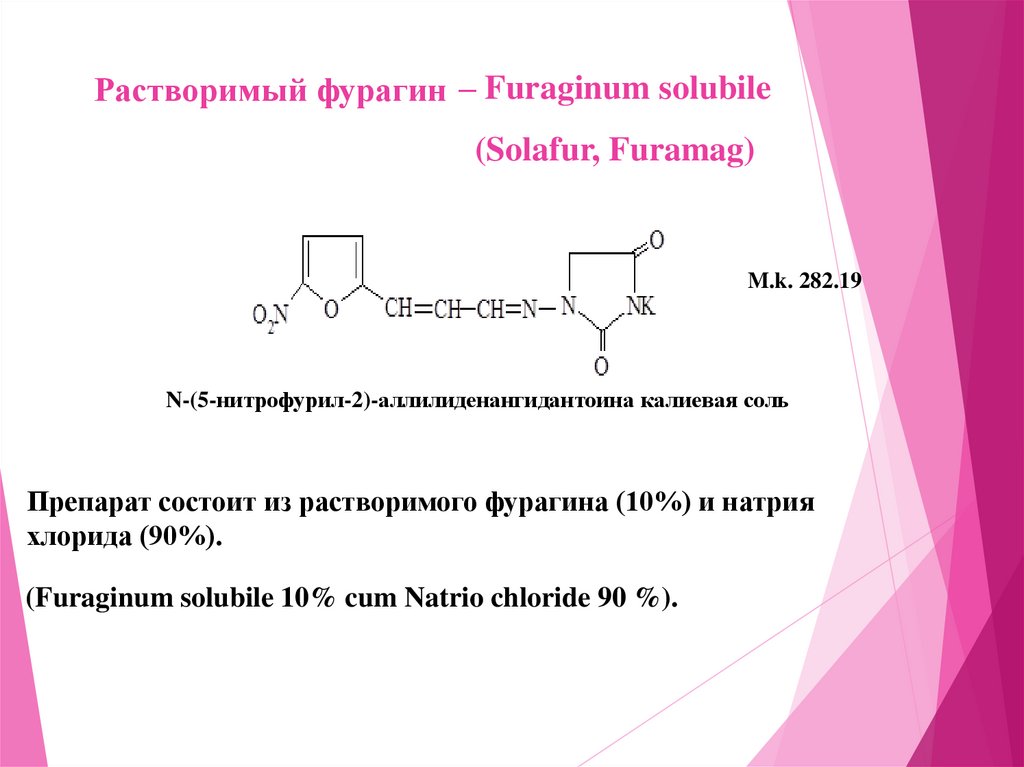
Растворимый фурагин – Furaginum solubile(Solafur, Furamag)
M.k. 282.19
N-(5-нитрофурил-2)-аллилиденангидантоина калиевая соль
Препарат состоит из растворимого фурагина (10%) и натрия
хлорида (90%).
(Furaginum solubile 10% cum Natrio chloride 90 %).
44.
ПОДЛИННОСТЬ1) Дает оранжево-красную, а затем коричневую окраску с раствором
NaOH в воде;
2) С 1 М раствором диметилформамида и гидроксида калия в 50%
спирте дает оранжевую окраску;
3) При добавлении к 1М раствору ацетона и гидроксида калия в 50%
спирте образуется красный осадок.
45.
Количественное определение1) Проводится методом нейтрализации (ацидиметрии). 0,1% раствор
препарата титруют от красного до желтого цвета 0,01 М соляной
кислотой (индикатор - бромфеноловый синий; Т=0,0030229 г/мл).
2) Спектрофотометрический метод: растворитель - 1% раствор
диметилформамида в воде; Он дает максимальное поглощение при длине
волны 290 нм (E_1cm^(1%)=800,67); Показатель удельного поглощения
раствора препарата в 0,01 М NaOH при 301 нм д.е. составляет
Е_1см^(1%)=799,69.
Растворимый фурагин выпускается в виде порошка по 100 г и капсул по
0,05 г. 1% раствор применяют при ожогах.
46.
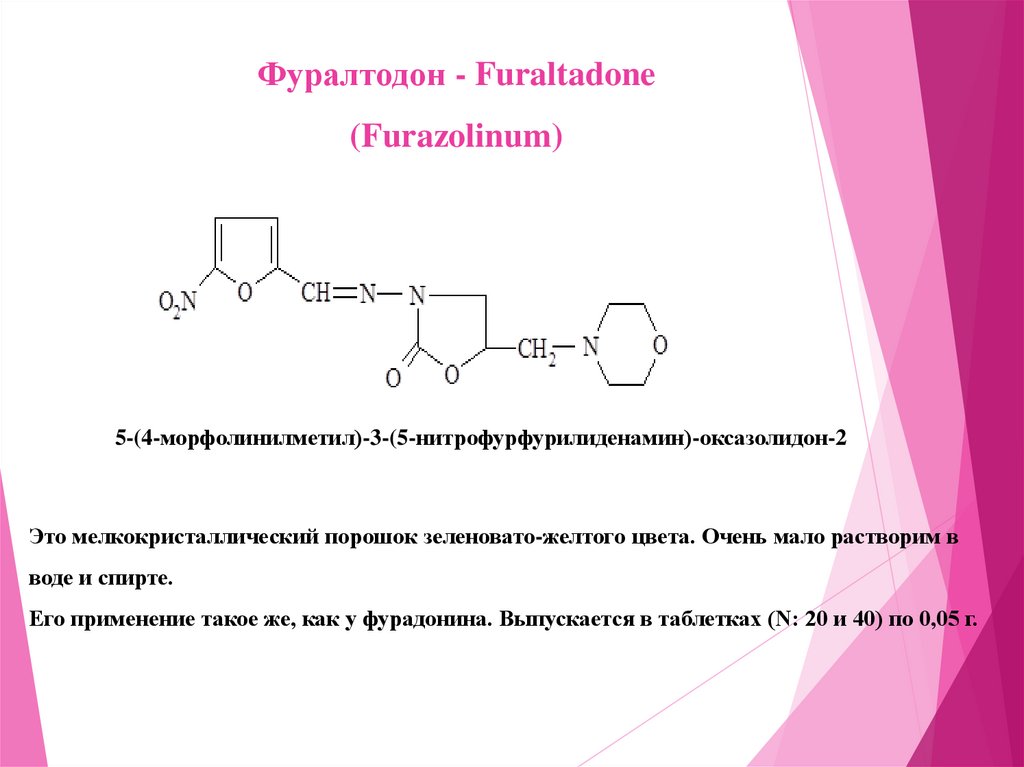
Фуралтодон - Furaltadone(Furazolinum)
5-(4-морфолинилметил)-3-(5-нитрофурфурилиденамин)-оксазолидон-2
Это мелкокристаллический порошок зеленовато-желтого цвета. Очень мало растворим в
воде и спирте.
Его применение такое же, как у фурадонина. Выпускается в таблетках (N: 20 и 40) по 0,05 г.
47.
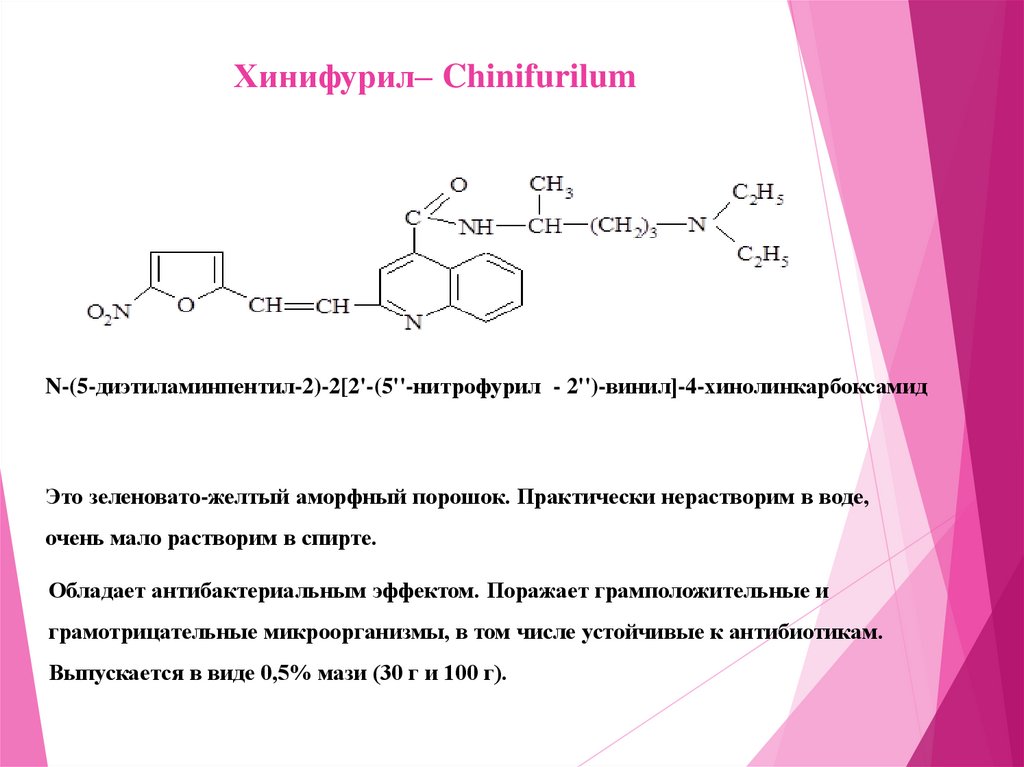
Хинифурил– ChinifurilumN-(5-диэтиламинпентил-2)-2[2'-(5''-нитрофурил - 2'')-винил]-4-хинолинкарбоксамид
Это зеленовато-желтый аморфный порошок. Практически нерастворим в воде,
очень мало растворим в спирте.
Обладает антибактериальным эффектом. Поражает грамположительные и
грамотрицательные микроорганизмы, в том числе устойчивые к антибиотикам.
Выпускается в виде 0,5% мази (30 г и 100 г).
48.
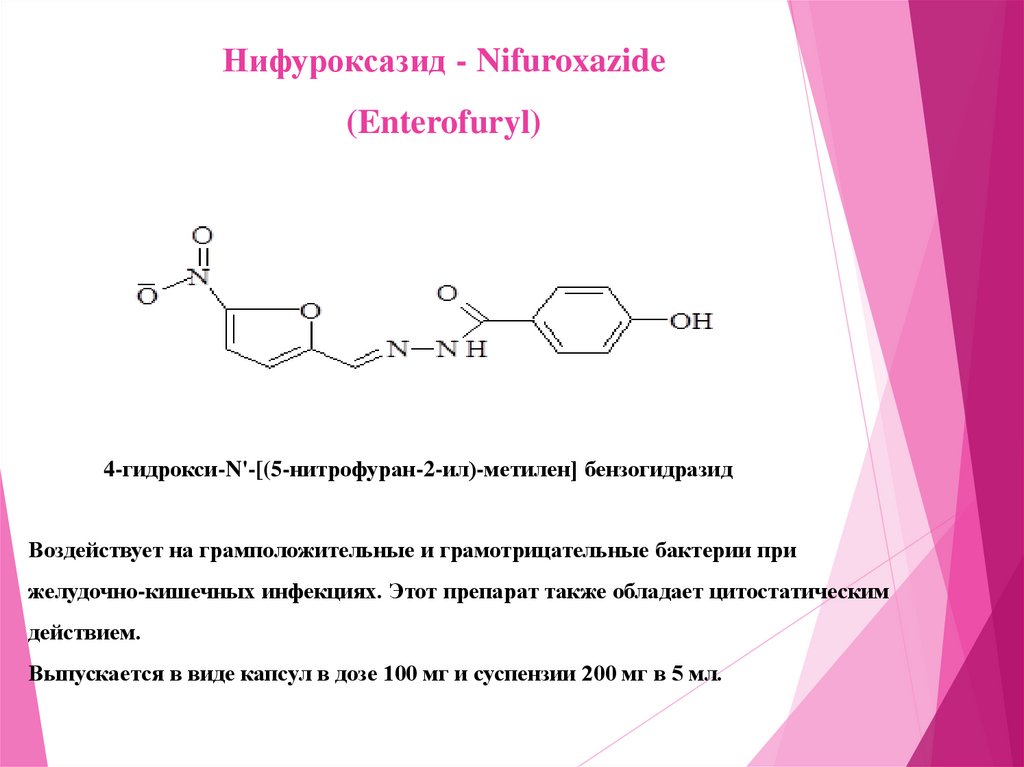
Нифуроксазид - Nifuroxazide(Enterofuryl)
4-гидрокси-N'-[(5-нитрофуран-2-ил)-метилен] бензогидразид
Воздействует на грамположительные и грамотрицательные бактерии при
желудочно-кишечных инфекциях. Этот препарат также обладает цитостатическим
действием.
Выпускается в виде капсул в дозе 100 мг и суспензии 200 мг в 5 мл.
49.
Нифурател – Nifuratel(Macmiror)
5-[(метилтио)метил]-3-[(1E)-(5-нитро-2-фурил) метиленамин]-1,3-оксазолидин-2-ОН
Обладает антибактериальной, противогрибковой и противопротозойной активностью.
Эффект такой же, как у ксинифурила. Выпускается в виде таблеток в дозе 200 мг.
Макмирор комплекс выпускают в форме вагинальных суппозиториев (содержащих 500 мг
нифурател и 200 000 МЕ нистатина) и вагинального крема (1 г содержит 100 мг нифурател
и 40 000 МЕ нистатина).
50.
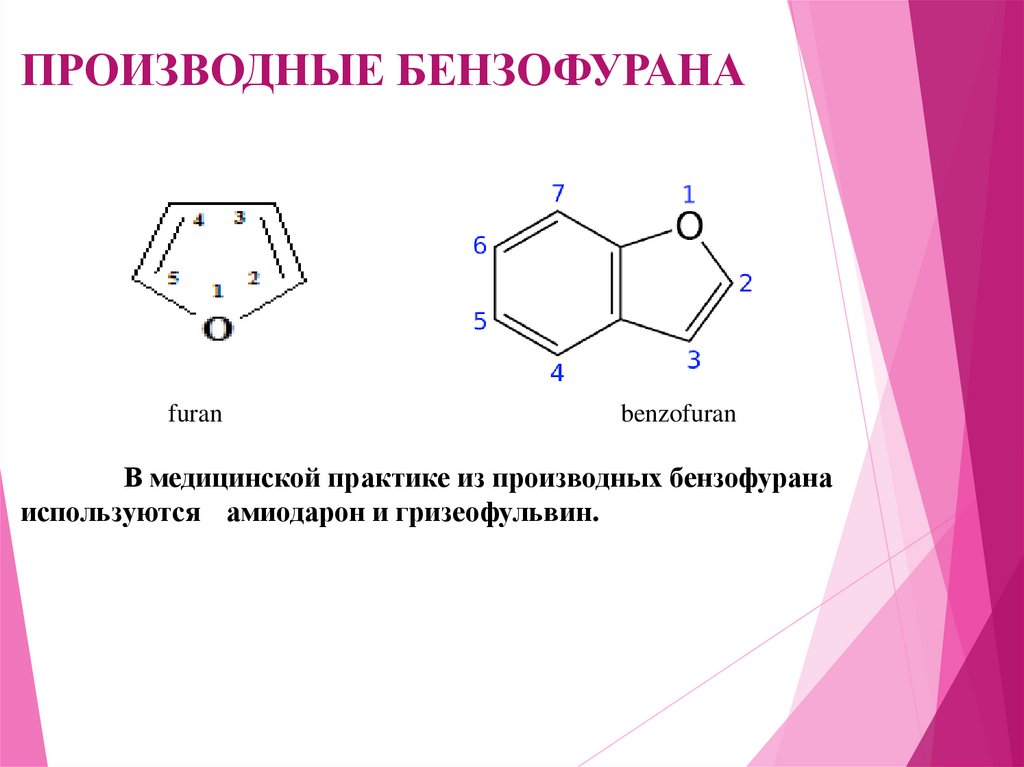
ПРОИЗВОДНЫЕ БЕНЗОФУРАНАfuran
benzofuran
В медицинской практике из производных бензофурана
используются амиодарон и гризеофульвин.
51.
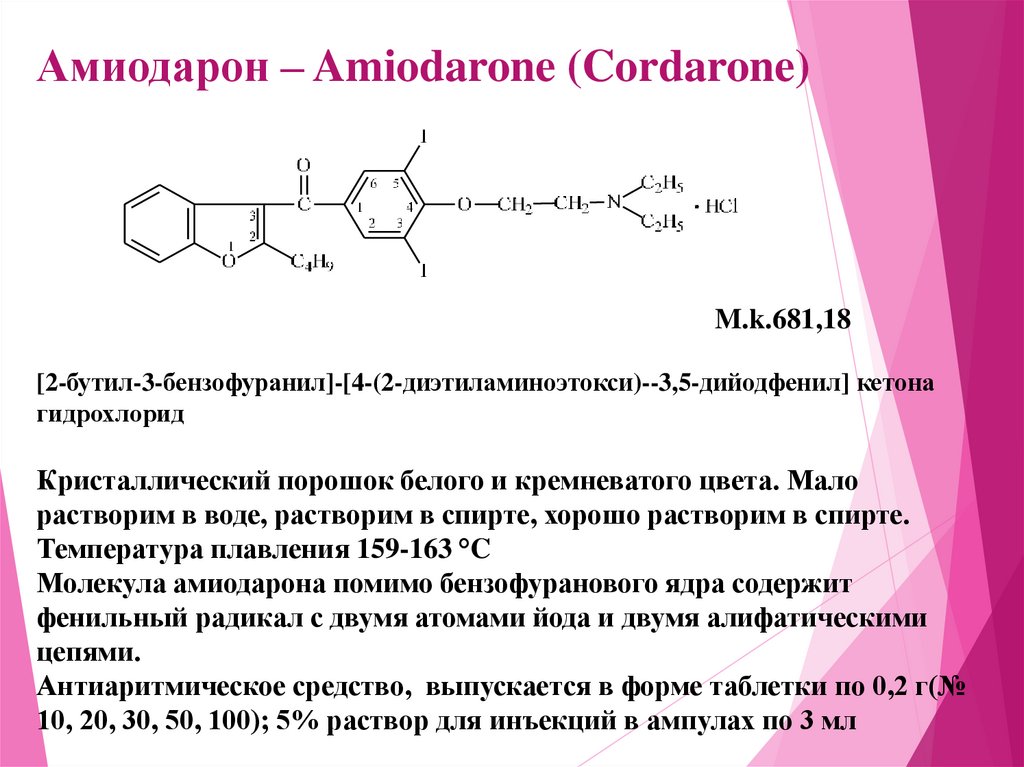
Амиодарон – Amiodarone (Cordarone)M.k.681,18
[2-бутил-3-бензофуранил]-[4-(2-диэтиламиноэтокси)--3,5-дийодфенил] кетона
гидрохлорид
Кристаллический порошок белого и кремневатого цвета. Мало
растворим в воде, растворим в спирте, хорошо растворим в спирте.
Температура плавления 159-163 °C
Молекула амиодарона помимо бензофуранового ядра содержит
фенильный радикал с двумя атомами йода и двумя алифатическими
цепями.
Антиаритмическое средство, выпускается в форме таблетки по 0,2 г(№
10, 20, 30, 50, 100); 5% раствор для инъекций в ампулах по 3 мл
52.
Определение подлинности1) Навеску препарата помещают в пробирку, добавляют к ней бихромат
калия и конц. серную кислоту; пробирку накрывают фильтровальной
бумагой, смоченной раствором дифенилкарбазида в уксусной кислоте.
Фильтровальная бумага окрашена в пурпурно-красный цвет;
дифенилкарбазон образуется в результате реакции:
53.
2) Проводят реакцию на наличие хлорид-иона3) УФ-спектрофотометрия: оптическую плотность 0,002% раствора
препарата в метаноле определяют на спектрофотометре при 242 и 270 нм
д.е.: отношение (D при 242 нм к D при 270 нм) должно быть между 0,92 и
3,22.
4) Сравнивают IQ-спектры испытуемых веществ и стандартных
образцов, снятых дисках с бромидом калия в области 4000-400 см ˉ ˡ
5) Методом ТСХ: хроматограммы исследуемого и стандартного
амиодарона должно совпадать по цвету и интенсивности с основным
пятном.
6) Методом ВЭЖХ: ИК-спектры испытуемых веществ и стандартных
образцов.
54.
Определение чистотыНаличие примеси
йодидов определяют фотоколориметрическим
методом при длине волны 420 нм , после действия раствором йодата
калия
в
кислой
среде.
Примеси
родственных
соединедений определяют методом ТСХ.
по
структуре
Остаточные растворители
определяют методом ГЖХ с плазмезменно-ионизационным детектором.
55.
Количественное определение1) Проводится методом нейтрализации (алкалиметрии). 0,01 М раствора
препарата в смеси соляной кислоты и этанола титруют 0,1 М раствором
NaOH. Эквивалентная точка определяется потенциометром. Параллельно
проводят контрольный опыт (Т=0,06818 г/мл).
Основание амиодарона ∙ HCl + NaOH → основание амиодарона
+ NaCl + H2O
2) Методом ВЭЖХ.
56.
Это антиангинальное и антиаритмическое вещество.Применяется при стенокардии и инфаркте миокарда.
Таблетки в дозе 0,2 г и 5% раствор для инъекций в
количестве 3 мл.
выпущен для
Препарат хранят в плотно закрытой таре при температуре не
выше +25℃, в защищенном от света месте.
57.
Гризеофульвин−Griseofulvin(Fulcin, Lamoryl, Sporostatin)
7 хлор-2',4,6-триметокси-6'-метилгризен-2'-дион3,4'
Белый или белый с желтоватым оттенком наимельчайший порошок со слабым
специфическим (грибным) запахом. Практически нерастворим в воде, мало
растворим в спирте. Температура плавления 218-224°C.
Является противогрибковым антибиотиком. Выпускается в форме порошка
(Гризеофульфин форте); таблеток по 0,125 г; 10% суспензии для приема внутрь в
банках по 100 мл; 2,5% линимент в банках по 10, 15, 20 и 30 г
58.
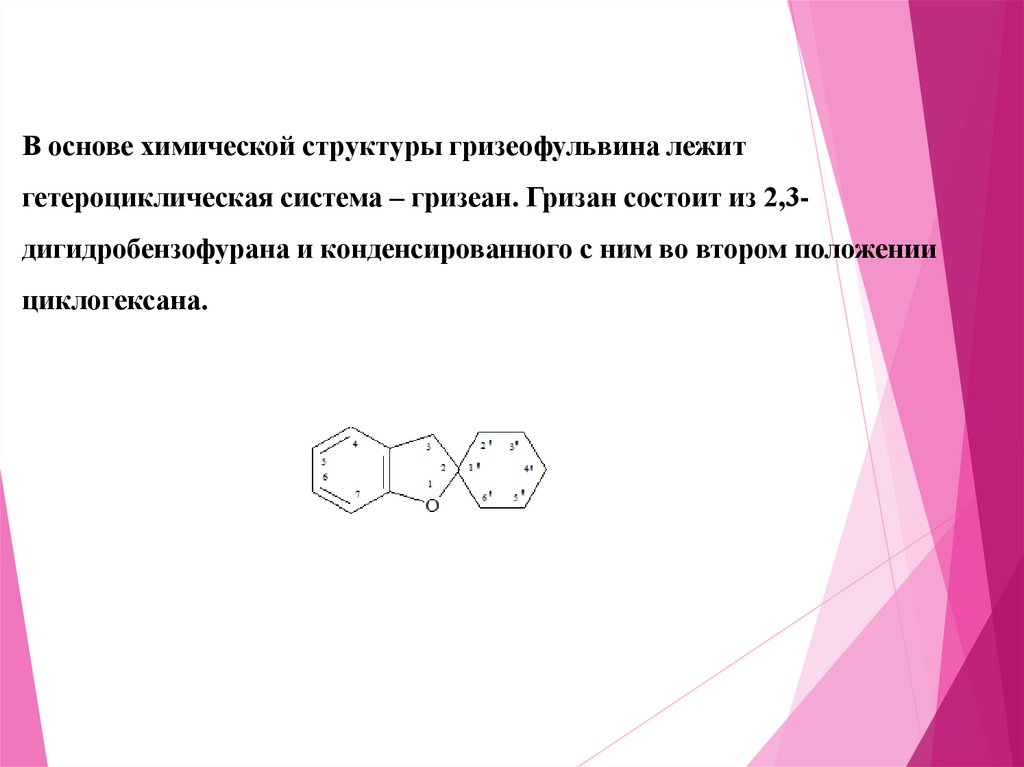
В основе химической структуры гризеофульвина лежитгетероциклическая система – гризеан. Гризан состоит из 2,3дигидробензофурана и конденсированного с ним во втором положении
циклогексана.
59.
Гризефульвин — антибиотик, синтезируемый грибкомPenicillium nigricans griseofulvum.
Гризеофульвин практически нерастворим в воде и эфире,
мало растворим в этаноле, ацетоне и бутилацетате, легко
растворим в диметилформамиде. Представляет собой белый
или желтовато-белый мелкодисперсный кристаллический
порошок. Температура плавления 218-224°С, показатель
удельного вращения [α] = +355 – +3660 (для 1% раствора с
диметилформамидом).
60.
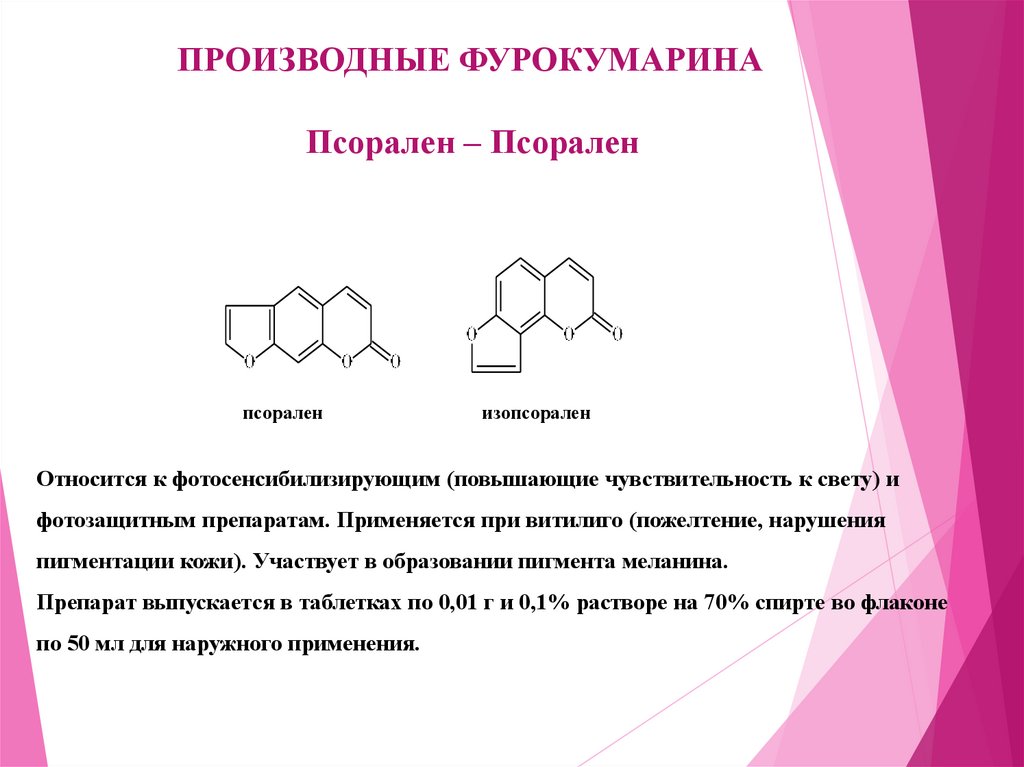
ПРОИЗВОДНЫЕ ФУРОКУМАРИНАПсорален – Псорален
псорален
изопсорален
Относится к фотосенсибилизирующим (повышающие чувствительность к свету) и
фотозащитным препаратам. Применяется при витилиго (пожелтение, нарушения
пигментации кожи). Участвует в образовании пигмента меланина.
Препарат выпускается в таблетках по 0,01 г и 0,1% растворе на 70% спирте во флаконе
по 50 мл для наружного применения.
61.
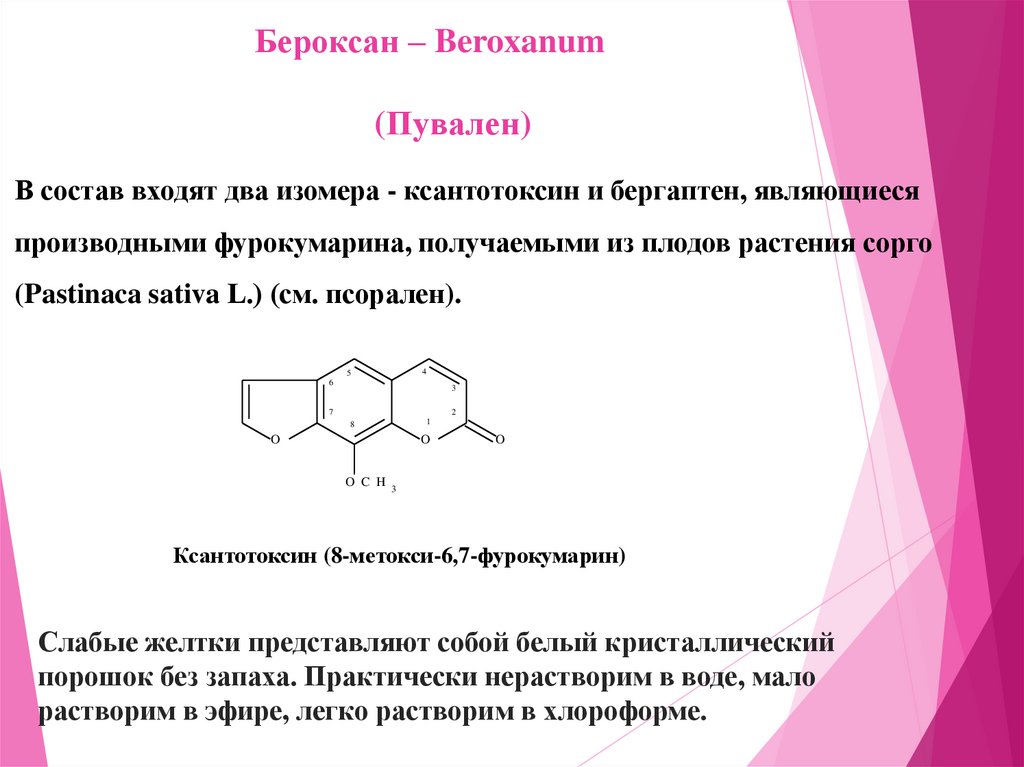
Бероксан – Beroxanum(Пувален)
В состав входят два изомера - ксантотоксин и бергаптен, являющиеся
производными фурокумарина, получаемыми из плодов растения сорго
(Pastinaca sativa L.) (см. псорален).
5
4
6
3
7
2
8
O
1
O
O
O C H 3
Ксантотоксин (8-метокси-6,7-фурокумарин)
Слабые желтки представляют собой белый кристаллический
порошок без запаха. Практически нерастворим в воде, мало
растворим в эфире, легко растворим в хлороформе.
62.
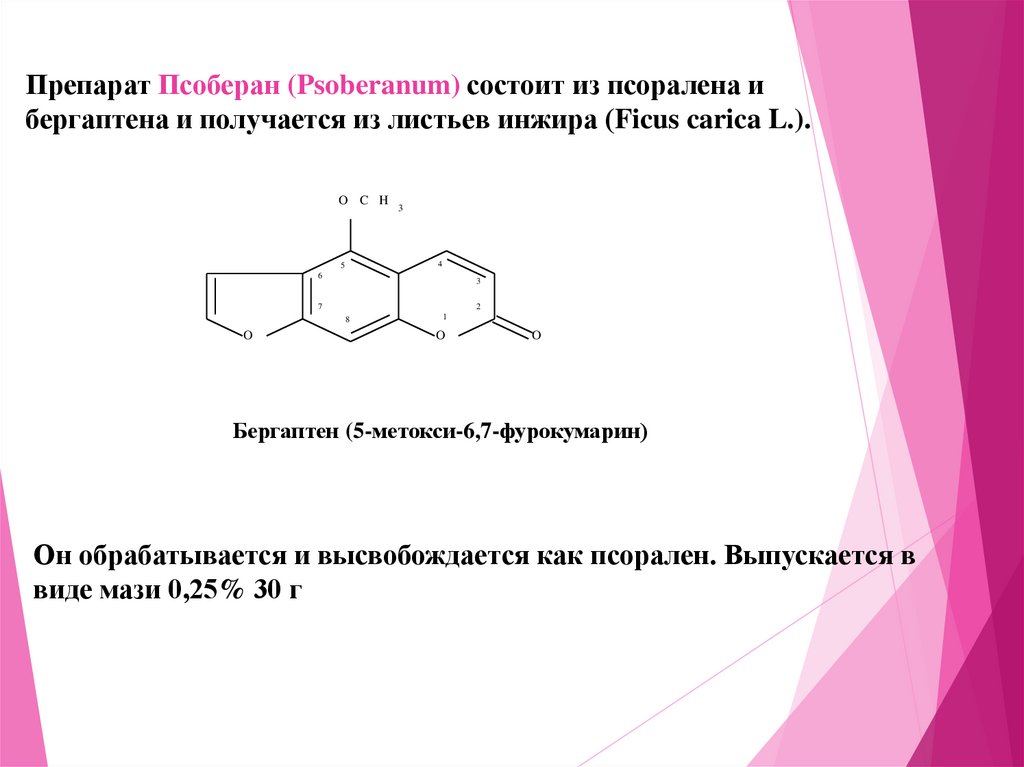
Препарат Псоберан (Psoberanum) состоит из псоралена ибергаптена и получается из листьев инжира (Ficus carica L.).
O C H
3
4
5
6
3
7
2
8
O
1
O
O
Бергаптен (5-метокси-6,7-фурокумарин)
Он обрабатывается и высвобождается как псорален. Выпускается в
виде мази 0,25% 30 г
63.
Определение подлинности1) К раствору препарата в спирте прибавляют щелочной раствор и
нагревают его, после чего реагируют с диазореагентом; получается
темно-красная окраска (см. фепромарон).
2) При нагревании с нингидрином и твердой серной кислотой
получается коричневый цвет (кумарин).
3) Температура плавления должна быть 124-1270С.
Количественное определение
Проводится методом полярографии.
Обработка препарата такая же, как у псоралена. Бероксан выпускают в
таблетках по 0,02 г, 0,25 и 0,5% растворы во флаконах по 50 мл, Пувален
в таблетках по 0,015 г.



























 chemistry
chemistry








