Similar presentations:
Основы промышленной экологии. Занятие 2
1.
ОСНОВЫ ПРОМЫЩЛЕННОЙ ЭКОЛОГИИзанятие 2
Основные характеристики химикотехнологического процесса
2.
Что предстоит ?1. Лекции (8 лекций)
2. Семинары (8 семинаров)
3. Контрольные работы:
1 и 2 контрольные - до 10 баллов,
зачетная контрольная работа – до 40 баллов.
Самостоятельная работа:
ответы на вопросы к лекциям – до 8 баллов,
на семинарах – до 8 баллов.
Контрольные по фильмам – до 14 баллов.
Презентации с докладами10 баллов
Итого в семестре максимальное количество баллов -100
Минимальное количество балов для зачета - 55
3.
Контрольные вопросы к лекции 11. Проведите сравнение малого биогеохимического и техногенного круговоротов веществ. Что у
них общего, чем они различаются?
2. В чём сходство и различие понятий побочный продукт, вторичное сырьё и вторичные
материальные ресурсы?
3. В чем разница в подводе реагентов в зону реакции при молекулярной диффузии и конвекции?
4.
Биологический (малый) круговорот• Извлечение и поглощение растениями углерода и
кислорода из атмосферы и азота, водорода, кислорода,
кальция, фосфора и др. элементов.
• Построение растительных организмов.
• Разложение отмерших растительных организмов и
освобождение заключенных в них элементов.
• Вовлечение элементов в новый круговорот.
5.
В чём сходство и различие понятий побочный продукт, вторичное сырьё ивторичные материальные ресурсы?
Вторичные минеральные ресурсы (ВМР) – минеральное сырье, содержащееся в отходах производства
или потребления , переработка которого технологически возможна и экономически целесообразна для
получения конечной продукции, эквивалентной по своим свойствам продукции из первичного
минерального сырья.
Вторичное сырьё – отходы производства или потребления, заменяющие первичное сырье и
применяемые для производства основной или дополнительной продукции.
Побочные продукты - все остальные продукты образующиеся в данном ХТП .
Побочные продукты могут получаться как в целевой, так и в побочных реакциях.
Если побочный продукт используется, то его называют вторичным сырьем
Если побочный продукт не находит применения, его называют отходом.
6.
В чем разница в подводе реагентов в зону реакции примолекулярной диффузии и конвекции?
При молекулярной диффузии в зону реакции поставляется
реагенты.
При конвекции в зону реакции подводится раствор, содержащий
реагенты.
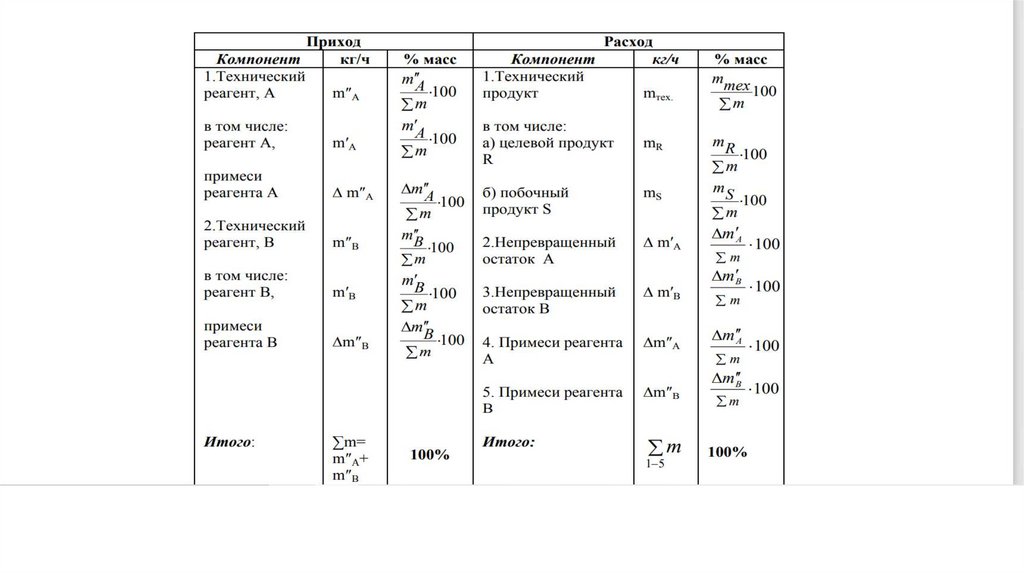
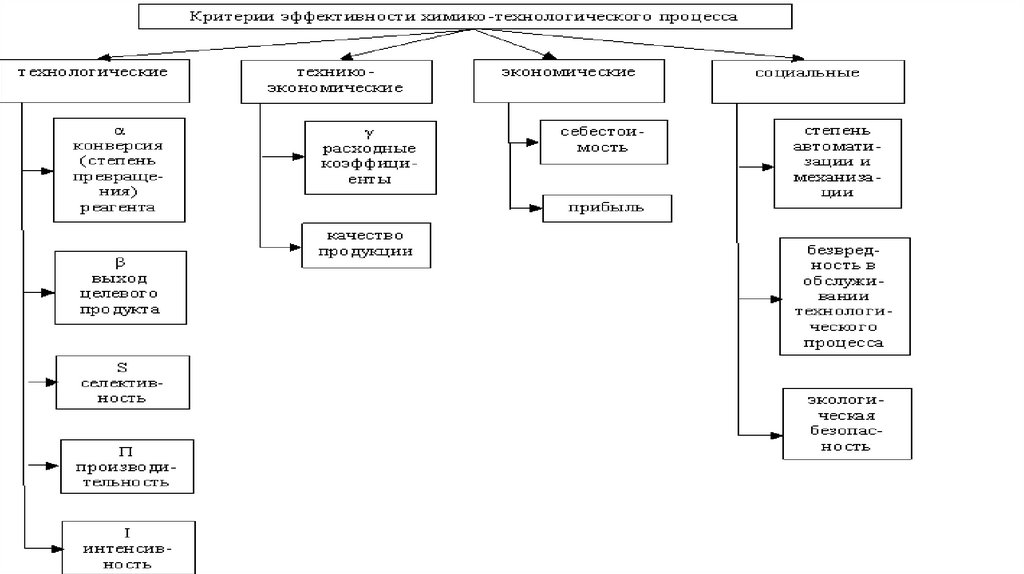
7.
8.
9.
Конверсия (степень превращения)где Nпод., Nпрев., Nнепревр. – соответственно количество поданного,
превращенного и непревращенного реагента. Эти величины
можно задавать в единицах количества вещества (моль, кмоль)
или в единицах массы (г, кг и др.). Степень превращения
выражают в долях или в процентах; в последнем случае
выражение (1) для расчета α умножают на 100.
10.
Часто, особенно в непрерывных процессах, конверсиюрассчитывают через концентрацию реагента в исходной и
реакционной
смеси:
где С0 –концентрация реагента в исходной смеси, С –
концентрация
реагента
в
реакционной
смеси.
Выражение
справедливо лишь в том случае, когда реакция протекает без
изменения объема реакционной смеси.
11.
Селективность (избирательность, избирательная конверсия)Nпрев. В целев. прод- количество реагента, пошедшее на
образование целевого продукта;
N общ. прев. – общее количество превращенного
реагента.
12.
Селективность (избирательность, избирательнаяконверсия)
Эти величины можно задавать в единицах количества вещества
(моль, кмоль) или в единицах массы (г, кг и др.).
Полную селективность выражают в долях или процентах; в
последнем случае выражение для S умножают на 100.
13.
ПроизводительностьПроизводительность - это показатель, который отражает результат производственной
деятельности или всего рабочего коллектива, или одного работника, измеренный
количеством выпущенной продукции, выполненных работ, или оказанных услуг, за
определенный промежуток времени, будь то год, полугодие, квартал, месяц, день или
даже час.
Производительность в химической промышленности
Производительностью называется количество целевого продукта или переработанного
для его получения сырья в единицу времени. Производительность может быть отнесена к
отдельному аппарату, технологической линии, цеху, предприятию в целом. Максимально
возможная в данных условиях производительность называется мощностью.
Производительность и мощность выражаются в кг/ч, м 3 /сут, т/год и так далее в
зависимости от масштабов производства.
14.
ИнтенсивностьИнтенсивностью аппарата называется его производительность,
отнесенная к единице величины, характеризующей размеры
рабочей части аппарата — его реакционного объема V или
площади
сечения
S.
Интенсивность
—
это
критерий
эффективности работы аппарата. Она позволяет сравнивать по
эффективности
аппараты
различной
мощности.
интенсивность соответственно в кг/м3 и кг/м2.
Выражается
15.
Выход продуктаЭто отношение практически полученной массы или
объема продукта к теоретически возможной массе или объему
(в %):
Максимальная масса (объем) продукта, которая может быть
получена из данного сырья, рассчитывается по уравнению
реакции, при этом учитывается содержание в сырье реагента,
подлежащего превращению.
16.
17.
18.
19.
20.
Задача 2Через известковую воду, содержащую 4,0 г гидроксида
кальция, пропустили углекислый газ. Выпавший осадок
отфильтровали,
высушили,
взвесили.
Его
масса
оказалась равной 4,5 г. Вычислить выход продукта
реакции (в процентах) от теоретически возможного.
21.
Решение (1 способ)Определим количество веществ, участвующих в превращении в молях
М.М. (Ca(OH)2 = 40 + 34 = 74 у.е.
М (Ca(OH)2 ) = 4 / 74 = 0,054 моль.
М.М. (CaCO3) = 100 у.е.
М. (CaCO3) = 4,5 /100 = 0,045 моль.
Процесс протекает по уравнению:
Ca(OH)2 + СО2 = CaCO3 + Н2О
Таким образом из 1 моль Ca(OH)2 образуется 1 моль CaCO3 , а значит, из 0,054 моль
Ca(OH)2 теоретически должно получиться столько же, то есть 0,054 моль CaCO3.
Было получено 0,045 моль CaCO3, отсюда, выход реакции составит:
wвых.(CaCO3) = 0,045 / 0,054 * 100 % = 83,3%
Ответ: Выход продукта составит 83,3%
22.
Решение (2 способ)по уравнению:
Ca(OH)2 + СО2 = CaCO3 + Н2О
Из 74 г Ca(OH)2 должно образоваться 100 г CaCO3, составим пропорцию:
74 - 100
4 -х
Х = 4* 100/74 = 5,4 г.
Но получено лишь 4,5 г CaCO3, отсюда выход продукта составит:
wвых.(CaCO3) = 4,5 *100%/ 5,4 = 83,3%
Ответ: Выход продукта составит 83,3%
23.
Самостоятельная работаЗадача 1
При взаимодействии магния массой 36 г с избытком хлора получено
128,25 г хлорида магния. Определить выход продукта реакции в
процентах от теоретически возможного.
Задача 2
В реакции 50 г С6Н6 с бромом образовалось 30 г С6Н5Вr,
оцените выход реакции.
https://chistenkoeschool.ru/portrety/kak-naiti-vyhod-reakcii-reshenie-tipovyh-zadach-po-himii-raschet-massy-veshchestva/




















 chemistry
chemistry ecology
ecology








