Similar presentations:
Синтез реакционноспособных олигомеров и полимеров на их основе
1. СИНТЕЗ РЕАКЦИОННОСПОСОБНЫХ ОЛИГОМЕРОВ И ПОЛИМЕРОВ НА ИХ ОСНОВЕ
ЛЕКЦИЯ № 42. План лекции
1.2.
3.
ОБЩИЕ ПРЕДСТАВЛЕНИЯ О СИНТЕЗЕ ПОЛИМЕРОВ МЕТОДОМ
ПОЛИКОНДЕНСАЦИИ
ФУНКЦИОНАЛЬНОСТЬ МОНОМЕРОВ
ЛИНЕЙНАЯ ПОЛИКОНДЕНСАЦИЯ
Принципиальные отличия поликонденсации от полимеризации
Причины возникновения неэквивалентности функциональных групп
Кинетика поликонденсации, обратимые и необратимые реакции
поликонденсации, катализ поликонденсации
Поликонденсационное равновесие и средняя степень поликонденсации
Молекулярная масса и молекулярно-массовое распределение в
процессах поликонденсации
Получение олигомеров и ВМ полимеров методом поликонденсации
4. СПОСОБЫ ПРОВЕДЕНИЯ ПОЛИКОНДЕНСАЦИИ
5. ТРЕХМЕРНАЯ ПОЛИКОНДЕНСАЦИЯ
Точка гелеобразования
Глубина поликонденсации при гелеобразовании
6. СРАВНЕНИЕ ПРОЦЕССОВ ЛИНЕЙНОЙ И ТРЕХМЕРНОЙ
ПОЛИКОНДЕНСАЦИИ
3. Процесс поликонденсации
Процесс синтеза полимеров из би- или полифункциональных соединений, вкотором рост макромолекул происходит путем химического взаимодействия
молекул мономеров друг с другом и с n-мерами (олигомерами),
накапливающимися в ходе реакции, а также молекул n-меров между собой
называют поликонденсацией.
XRX +YR'Y
XRZR'Y
-a
nXRY
X
RZ
nXRX
X
RZ
n
n
XRX
YR'Y
XRZR'Y
XRZR'Z
R'Y
RY
RX
Процессами
поликонденсации
называются
реакции
образования
макромолекул из би- или полифункциональных соединений, протекающие
ступенчато (т.е. последовательными, независимыми актами присоединения)
путем взаимодействия функциональных групп, принадлежащих различным
молекулам.
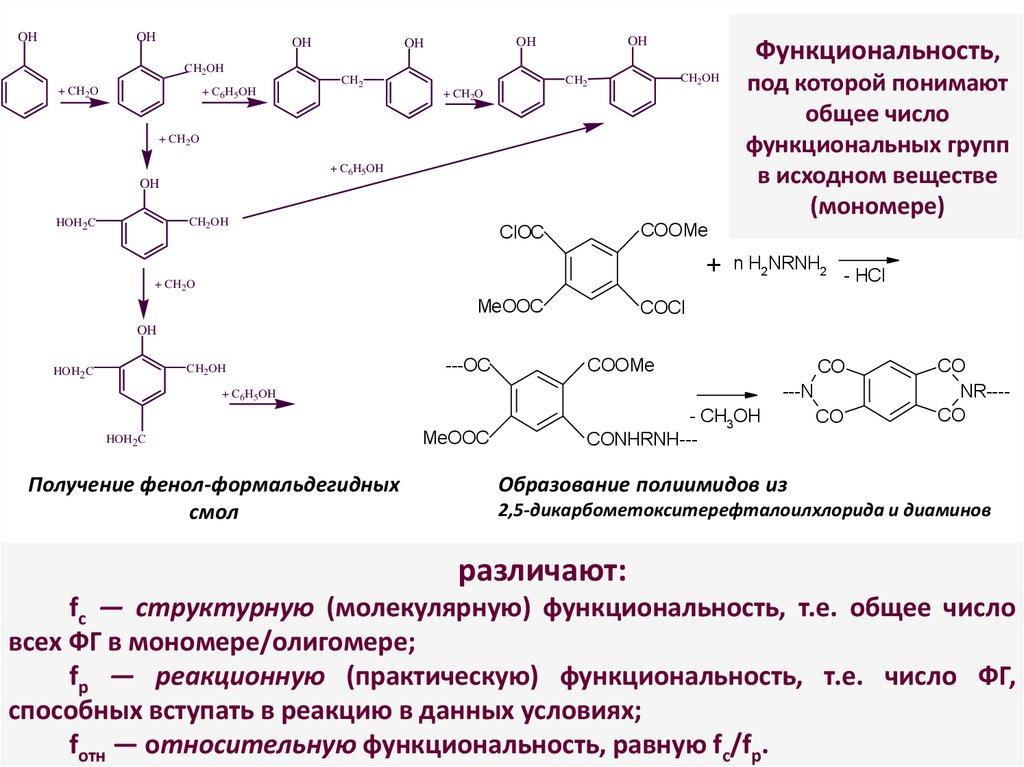
4. Функциональность, под которой понимают общее число функциональных групп в исходном веществе (мономере)
OHOH
OH
CH2OH
+ CH2O
+ C6H5OH
OH
OH
OH
CH2OH
CH2
CH2
Функциональность,
+ CH2O
+ CH2O
+ C6H5OH
OH
CH2OH
HOH2C
под которой понимают
общее число
функциональных групп
в исходном веществе
(мономере)
COOMe
ClOC
+
+ CH2O
MeOOC
n H2NRNH2
- HCl
COCl
OH
CH2OH
HOH2C
---OC
COOMe
---N
+ C6H5OH
HOH2C
Получение фенол-формальдегидных
смол
CO
MeOOC
- CH3OH
CONHRNH---
CO
CO
NR---CO
Образование полиимидов из
2,5-дикарбометокситерефталоилхлорида и диаминов
различают:
fс — структурную (молекулярную) функциональность, т.е. общее число
всех ФГ в мономере/олигомере;
fр — реакционную (практическую) функциональность, т.е. число ФГ,
способных вступать в реакцию в данных условиях;
fотн — относительную функциональность, равную fс/fр.
5.
причины возникновения неэквивалентности ФГ:• в реакцию вводят неэквивалентные количества исходных
реагентов;
• ФГ реагентов претерпевают химические изменения по ходу
реакции ПК, превращаясь в нереакционноспособные в условиях
реакции (влияние температуры реакции или химические взаимодействия с
молекулами растворителя или примесями);
в реакционной смеси присутствуют монофункциональные
вещества, которые взаимодействуют с ФГ молекул мономера (чем
больше монофункционального вещества в системе, тем на более ранней
стадии ПК прекратится рост ММ полимера),
выпадение молекул образующегося полимера из раствора;
• в реагирующих системах могут образовываться циклические
молекулы, что удаляет часть ФГ из реакций ПК.
термодинамическая устойчивость цикла
вероятностью встречи двух концевых ФГ одной молекулы
K ПК M
2
VПК
K ' M
VЦ
KЦ M
6. допущения, выдвинутые Полом Джоном Флори в 30х годах XX века
• реакционная способность обеих ФГбифункционального мономера одинакова
• реакционная способность одной ФГ
бифункционального мономера не зависит от того,
прореагировала или нет другая ФГ, т.е. реакционная
способность ФГ не меняется
• реакционная способность ФГ не зависит от
размера молекулы (длины цепи)
Исходя из принципа равной реакционной способности
ФГ у мономеров и полимеров (олигомеров)
поликонденсацию можно рассматривать как одну
бимолекулярную химическую реакцию.
7.
Кинетика ПК:Начальная стадия ПК
1.
Гомополиконденсация мономеров типа
случай линейной поликонденсации
n HO
CH2
m
XRX
CH2
OH
m
– это наиболее простой
O
n
+ (n-1) H2O
2. Скорость
расходования функциональных групп в начальной стадии процесса,
когда обратимостью реакции можно пренебречь, будет описываться уравнением
кинетики реакции второго порядка:
d X
dt
= k X
2
3. Выражение для скорости поликонденсации мономеров типа XRY
4.
d X
dt
=
d Y
dt
= k X Y = k X = k Y
2
2
Аналогичное уравнение справедливо и для кинетики гетерополиконденсации
мономеров
(XRX + YR Y) при исходном [X]=[Y].
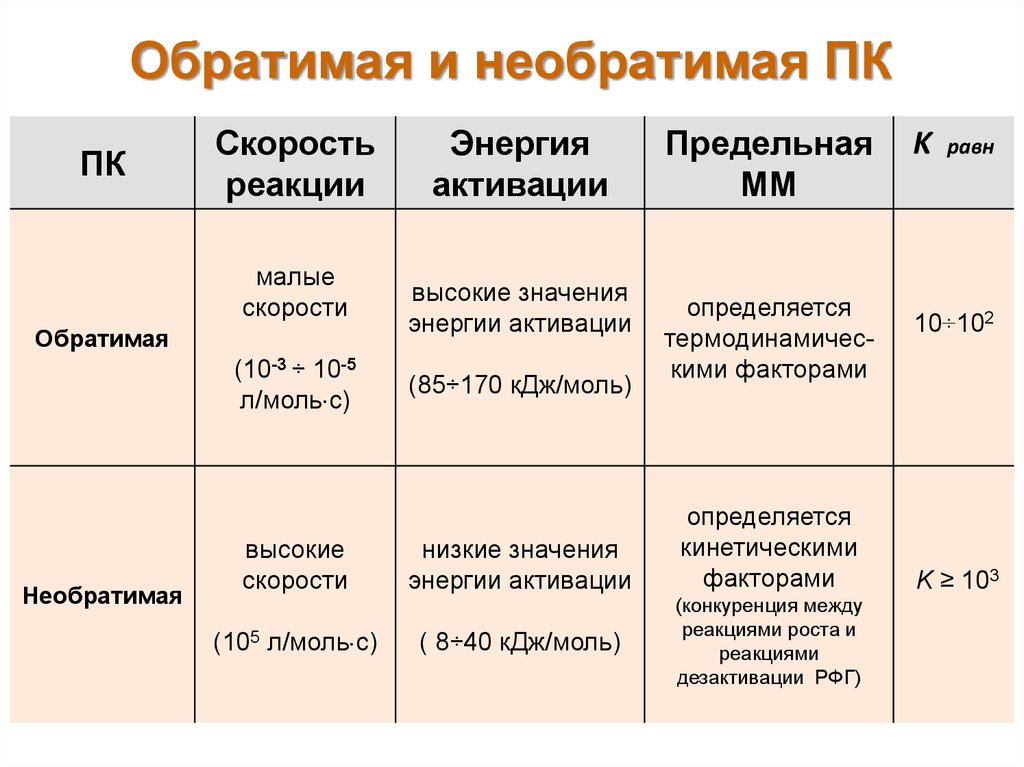
8. Обратимая и необратимая ПК
ПКСкорость
реакции
малые
скорости
Обратимая
(10-3 ÷ 10-5
л/моль с)
Необратимая
Энергия
активации
высокие значения
энергии активации
(85÷170 кДж/моль)
высокие
скорости
низкие значения
энергии активации
(105 л/моль с)
( 8÷40 кДж/моль)
Предельная
ММ
определяется
термодинамическими факторами
определяется
кинетическими
факторами
(конкуренция между
реакциями роста и
реакциями
дезактивации РФГ)
K
равн
10÷102
K ≥ 103
9.
Константы равновесияполиконденсационных процессов,
протекающих без выделения и с выделением побочных продуктов, соответственно:
[X] и [Y] – равновесные концентрации функциональных групп, не вступивших в реакцию,
[Z] – равновесная концентрация связей, образовавшихся в результате реакции ПК,
[A] – концентрация побочного продукта в реакционной смеси.
Основной характеристикой обратимых процессов поликонденсации
является конденсационное равновесие,
т.е. наличие в заданных условиях предельно допустимой степени
превращения,
а соответственно и средней степени поликонденсации.
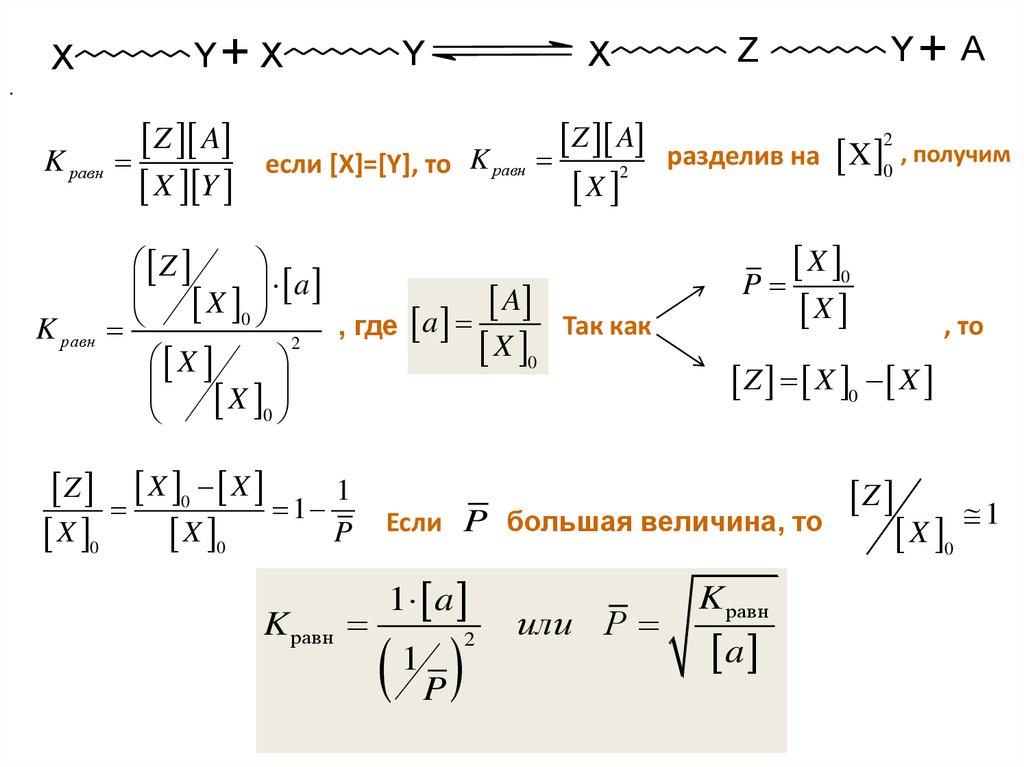
10.
X.
Y+ X
Z A
K равн
X Y
K равн
Y
X
Z A
K равн
2
X
если [X]=[Y], то
Z
a
A
X 0
Так как
, где a
2
X 0
X
X
0
Z X 0 X 1 1
P
X 0
X 0
K равн
разделив на X 0 , получим
2
X 0
P
X
P
1
2
или P
, то
Z X 0 X
Если P большая величина, то
1 a
Y+ A
Z
K равн
a
Z
X 0 1
11.
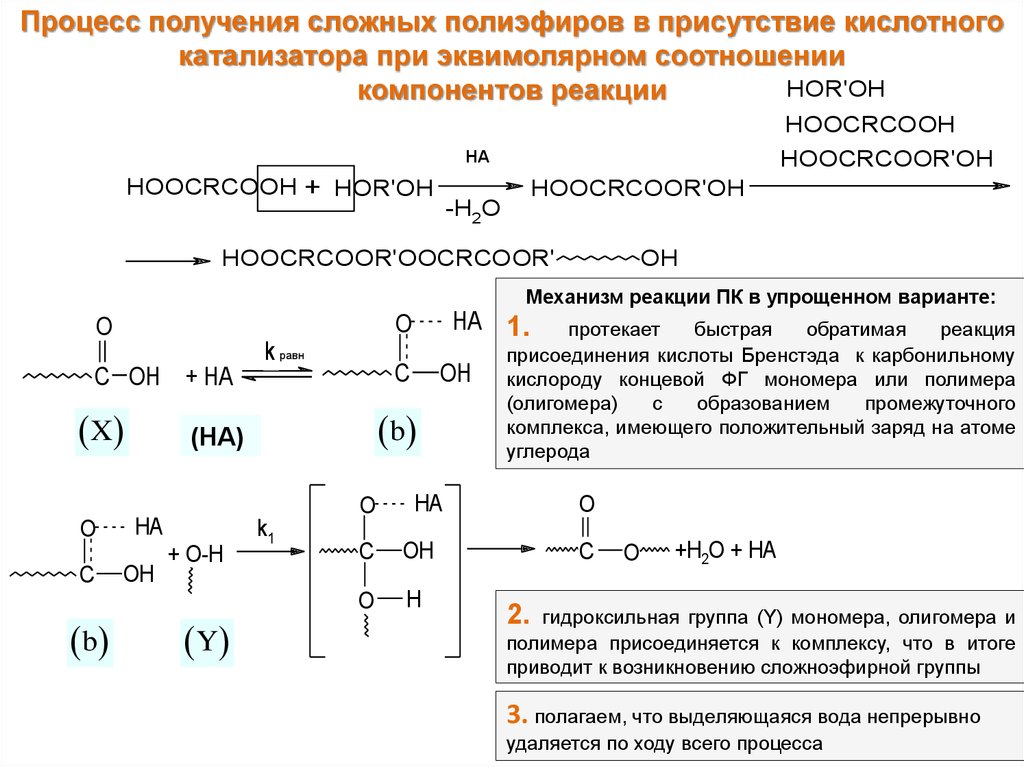
Процесс получения сложных полиэфиров в присутствие кислотногокатализатора при эквимолярном соотношении
HOR'OH
компонентов реакции
HOOCRCOOH
HOOCRCOOR'OH
HA
HOOCRCOOH + HOR'OH
HOOCRCOOR'OH
-H2O
HOOCRCOOR'OOCRCOOR'
OH
Механизм реакции ПК в упрощенном варианте:
k равн
X
C
b
b
(HA)
O
HA
OH
+ O-H
Y
OH
C
C OH + HA
O
HA 1.
O
O
k1
протекает
быстрая
обратимая
реакция
присоединения кислоты Бренстэда к карбонильному
кислороду концевой ФГ мономера или полимера
(олигомера)
с
образованием
промежуточного
комплекса, имеющего положительный заряд на атоме
углерода
HA
C
OH
O
H
O
C
O
+H2O + HA
2.
гидроксильная группа (Y) мономера, олигомера и
полимера присоединяется к комплексу, что в итоге
приводит к возникновению сложноэфирной группы
3. полагаем, что выделяющаяся вода непрерывно
удаляется по ходу всего процесса
12.
Уравнение для скорости ПК будет иметь следующий вид:VПК = -
-
d X
dt
d X
dt
b
= k1 b Y ; k равн
X HA
= k1 Y k равн X HA
(A)
Так как [HA] остается постоянной по ходу всего процесса, то
-
-
d X
dt
d X
dt
= k Y X , где k = k1k равн HA Если [X]=[Y] (эквимолярное
соотношение компонентов реакции), то
= k X
2
Интегрируя данное выражение, получаем:
1
1
= k t
X t X 0
X 0
X t
Умножив обе части этого уравнения на [X]о, будем иметь:
- 1 = k t X 0
или
P = k t X 0 +1
(B)
13.
Процесс получения сложных полиэфировв отсутствие кислотного катализатора
В этом случае сам мономер, содержащий карбоксильную группу, может
выполнять роль катализатора.
d X
= k1 Y k равн X HA
[HA]-const или нет ?
dt
В данных системах [HA] не является постоянной, из-за непрерывного
снижения концентрации карбоксильных групп по ходу процесса .
Если [HA]=[X] и [X]=[Y] , то
-
d X
dt
2
3
= k1k равн Y X = k X , где k k1k равн
2k t =
При интегрировании уравнения (С) получаем:
Умножив обе части этого
уравнения на
получим:
X 0
2
(С)
1
X t
2
X 0
=
- 1 = P 2 -1 или
X
t
-
1
X 0
2
2
2k t X 0
2
P = 1+2k t X 0 ;
2
2
P = 1+2k t X 0
2
(D)
14.
Молекулярная массаи молекулярно-массовое распределение
в процессах поликонденсации
P
Рассмотрим систему, состоящую из двух мономеров:
XRX и YR Y, причем, YR Y взят в избытке
X
P=
N0 =
Nt =
Y
No
Nt
N X0 +N Y0
2
NXt +NYt
2
N X0
N X0 1+ 1
=
2
; α=α X =
q
= N
X0
2q
N X0 - N X t
N X0
N Y0 = q( 1) или N Y0 =
N Х0
q
q+1
; αN X0 = NX0 - NXt = NY0 - NYt
NXt = NX0 1- α ; NYt = NY0 - αNX0 =
N X0
q
- αNX0 =
N X0
q
1- αq
15.
N0P=
Nt
=
N X0
2q
q+1
N X0
q+1
1-α q+ 1-αq
=
2q
q+1-2qα
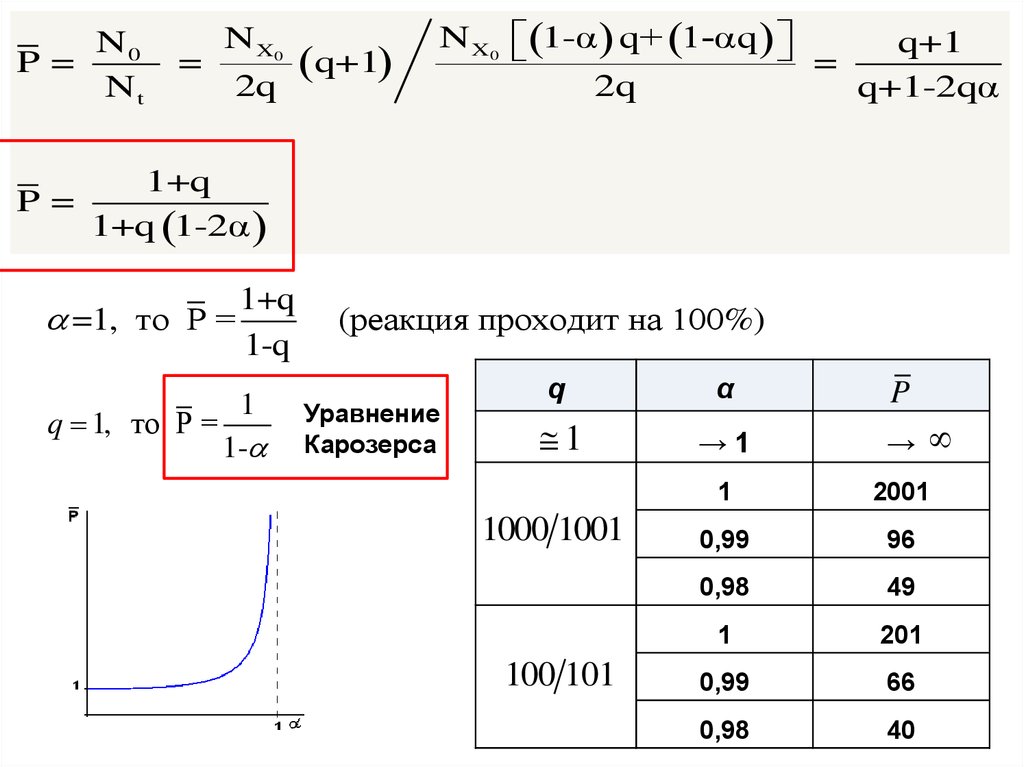
1+q
P=
1+q 1-2α
1+q
=1, то P =
1-q
1
q 1, то P =
1-
(реакция проходит на 100%)
Уравнение
Карозерса
q
α
P
1
→1
→
1
2001
0,99
96
0,98
49
1
201
0,99
66
0,98
40
1000 1001
100 101
16.
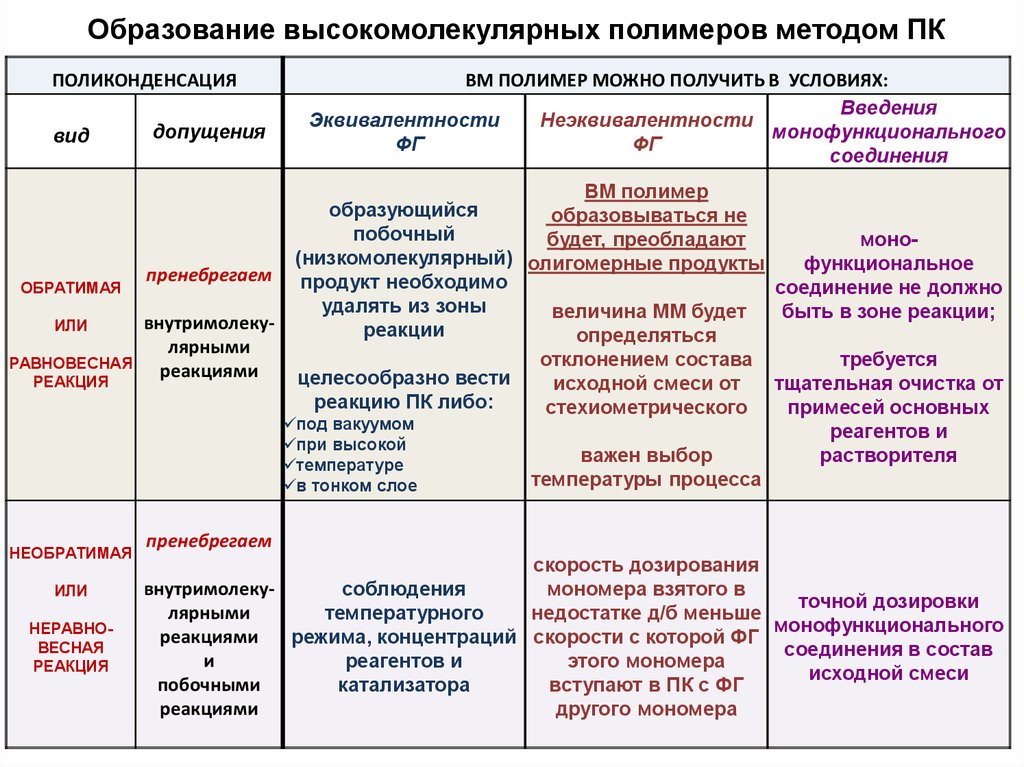
Образование высокомолекулярных полимеров методом ПКПОЛИКОНДЕНСАЦИЯ
вид
ОБРАТИМАЯ
ИЛИ
РАВНОВЕСНАЯ
РЕАКЦИЯ
НЕОБРАТИМАЯ
ИЛИ
НЕРАВНОВЕСНАЯ
РЕАКЦИЯ
допущения
ВМ ПОЛИМЕР МОЖНО ПОЛУЧИТЬ В УСЛОВИЯХ:
Введения
Эквивалентности
Неэквивалентности
монофункционального
ФГ
ФГ
соединения
ВМ полимер
образующийся
образовываться не
побочный
будет, преобладают
моно(низкомолекулярный) олигомерные продукты
функциональное
пренебрегаем продукт необходимо
соединение не должно
удалять из зоны
величина ММ будет
быть в зоне реакции;
внутримолекуреакции
определяться
лярными
отклонением состава
требуется
реакциями
целесообразно вести
исходной смеси от
тщательная очистка от
реакцию ПК либо:
стехиометрического
примесей основных
под вакуумом
реагентов и
при высокой
важен выбор
растворителя
температуре
температуры процесса
в тонком слое
пренебрегаем
скорость дозирования
внутримолекусоблюдения
мономера взятого в
точной дозировки
лярными
температурного
недостатке д/б меньше
монофункционального
реакциями
режима, концентраций скорости с которой ФГ
соединения в состав
и
реагентов и
этого мономера
исходной смеси
побочными
катализатора
вступают в ПК с ФГ
реакциями
другого мономера
17. Технологические особенности проведения реакций ПК
Обратимая1. Отгонка НМ продукта из сферы реакции
2. Используют растворители с Ткип выше, чем у НМ
продукта
3. Используют растворитель образующий азеотроп с НМ
продуктом, причем его Ткип ниже, чем у растворителя
4. Используют растворитель в котором хорошо
растворяются полимеры, а НМ продукты плохо
5. Процесс ПК ведут при 100÷200 oC и постоянном притоке
свежего растворителя
1.
Необратимая
2.
Низкотемпературная (ниже 100 oC )
Эмульсионная ПК
Межфазная ПК
Высокотемпературная (выше 100oC), в условиях
медленного нагрева реакционной смеси
18. Способы проведения реакций ПК и их преимущества
В расплаве притемпературе 200÷400 oС
(в токе инертного газа)
1. Применение мономеров с низкой реакционной
способностью
2. Высокий выход полимера
3. Получение полимера высокой чистоты
4. Непосредственное использование расплава для
получения волокон и пленок
5. Простота технологической схемы
В растворе при
температуре
не выше 200 oС
(как в индивидуальном
растворителе, так и
смеси растворителей)
1.
2.
3.
4.
5.
6.
На границе раздела фаз
1. Подача компонентов в зону реакции регулируется
скоростью их диффузии к границе раздела фаз
2. Образуются полимеры высокого молекулярного
веса, недостижимого при других методах ПК
3. Высокая скорость реакции
4. Не так важна чистота реагентов.
5. Возможно получать высокоплавкие полимеры
"межфазная поликонденсация"
Относительно мягкие условия проведения ПК
Растворитель может выполнять роль катализатора
Возможность удаления НМ продукта
Хорошая теплоотдача
Быстрое смешение мономеров
Непосредственное использование раствора для
получения волокон и пленок
19.
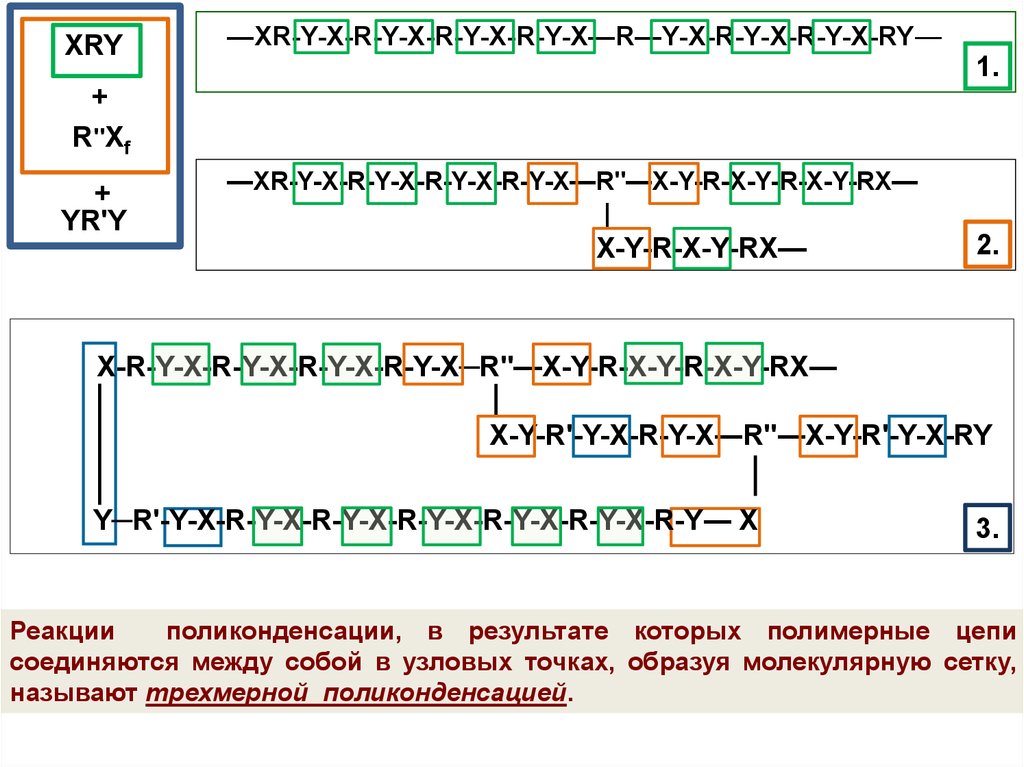
XRY—XR-Y-X-R-Y-X-R-Y-X-R-Y-X—R—Y-X-R-Y-X-R-Y-X-RY—
1.
+
R"Xf
+
YR'Y
—XR-Y-X-R-Y-X-R-Y-X-R-Y-X—R"—X-Y-R-X-Y-R-X-Y-RX—
|
X-Y-R-X-Y-RX—
2.
X-R-Y-X-R-Y-X-R-Y-X-R-Y-X─R"—X-Y-R-X-Y-R-X-Y-RX―
X-Y-R'-Y-X-R-Y-X―R''―X-Y-R'-Y-X-RY
Y─R'-Y-X-R-Y-X-R-Y-X-R-Y-X-R-Y-X-R-Y-X-R-Y― X
3.
Реакции
поликонденсации, в результате которых полимерные цепи
соединяются между собой в узловых точках, образуя молекулярную сетку,
называют трехмерной поликонденсацией.
20.
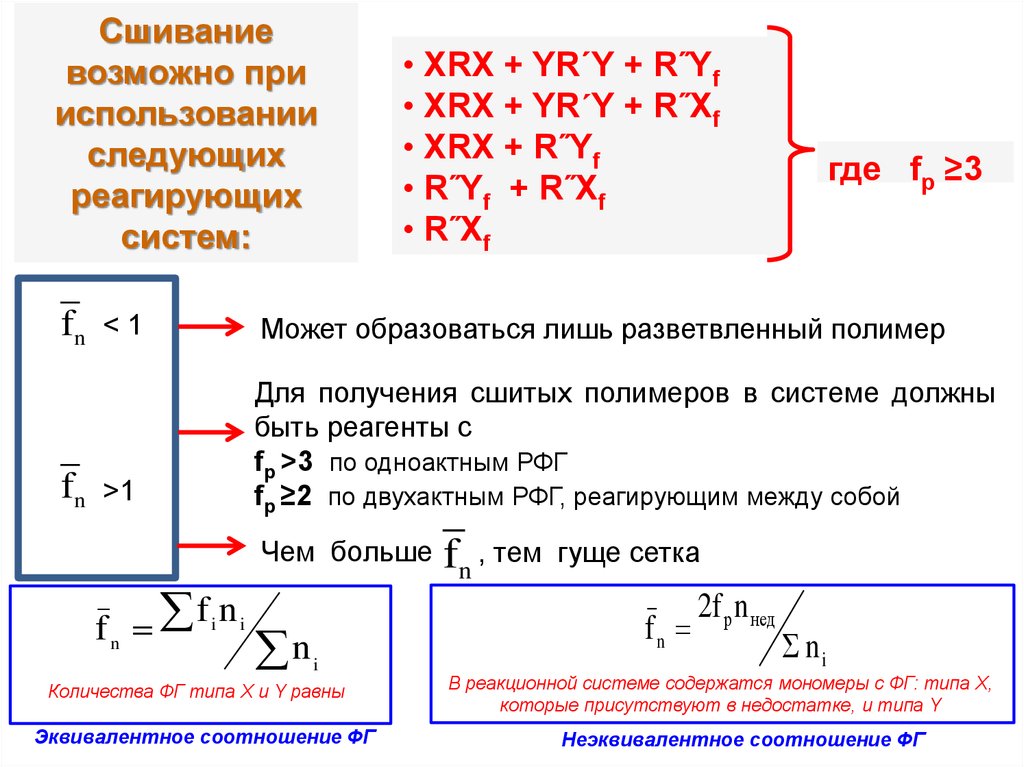
Сшиваниевозможно при
использовании
следующих
реагирующих
систем:
fn
fn
• XRX + YR´Y + R˝Yf
• XRX + YR´Y + R˝Xf
• XRX + R˝Yf
• R˝Yf + R˝Xf
• R˝Xf
где fр ≥3
<1
Может образоваться лишь разветвленный полимер
>1
Для получения сшитых полимеров в системе должны
быть реагенты с
fр >3 по одноактным РФГ
fр ≥2 по двухактным РФГ, реагирующим между собой
Чем больше
fn
fn
i
i
ni
Количества ФГ типа X и Y равны
Эквивалентное соотношение ФГ
fn , тем
гуще сетка
fn
2f р n нед
Σ ni
В реакционной системе содержатся мономеры с ФГ: типа X,
которые присутствуют в недостатке, и типа Y
Неэквивалентное соотношение ФГ
21.
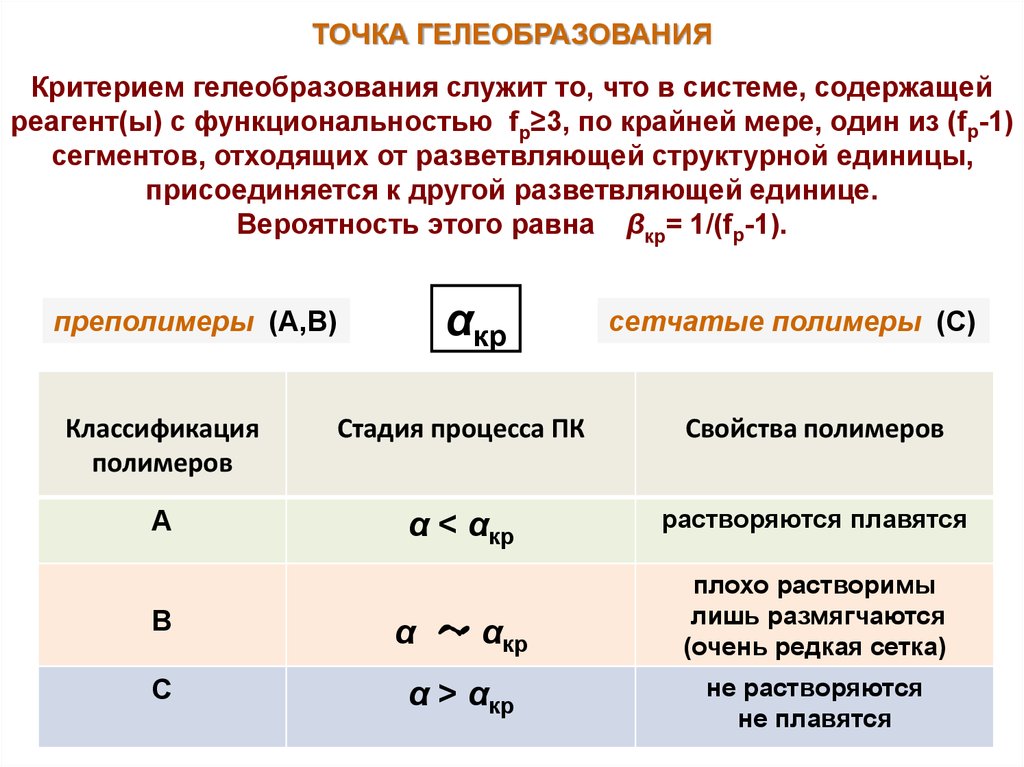
ТОЧКА ГЕЛЕОБРАЗОВАНИЯКритерием гелеобразования служит то, что в системе, содержащей
реагент(ы) с функциональностью fр≥3, по крайней мере, один из (fр-1)
сегментов, отходящих от разветвляющей структурной единицы,
присоединяется к другой разветвляющей единице.
Вероятность этого равна βкр= 1/(fр-1).
αкр
преполимеры (А,В)
сетчатые полимеры (С)
Классификация
полимеров
Стадия процесса ПК
Свойства полимеров
А
α < αкр
растворяются плавятся
В
С
α
αкр
α > αкр
плохо растворимы
лишь размягчаются
(очень редкая сетка)
не растворяются
не плавятся
22.
ОЦЕНКА ЗАВЕРШЕННОСТИ РЕАКЦИИ В ТОЧКЕ ГЕЛЕОБРАЗОВАНИЯС помощью уравнения Карозерса
эквивалентное
соотношение ФГ
исходных реагентов
неэквивалентное
соотношение ФГ
исходных реагентов
исходное число ФГ в реакционной системе
fin i
N0
n
i
2f р n нед
N0
n
i
число ФГ, вступивших в ПК 2(N 0 - N)
кр
исходное число ФГ
N 0 fn
кр 2/fn (1 1/P)
если Р→∞
кр
No
1
(1 )
f p n нед
Рn
Статистический метод
• ПК протекает только между
различными молекулами,
• все ФГ одинакового типа имеют
равную реакционную способность
1. R˝Xf +XRX + YR´Y
(ФГ типа Y взяты в избытке)
кр =
1
q+qρ f p - 2
2. XRX+R"Yf
1
α кр
q (f p 1)
1
(fр 1)
3. R´Xf
1
2
αкр (fр 1)
α кр 1
(f р 1)
fр – реакционная функциональность (разветвляющей единицы) ; q – стехиометрический разбаланс ;
ρ - доля ФГ типа X, принадлежащих мономерным молекулам R˝Xf , от суммы одноименных ФГ.
23.
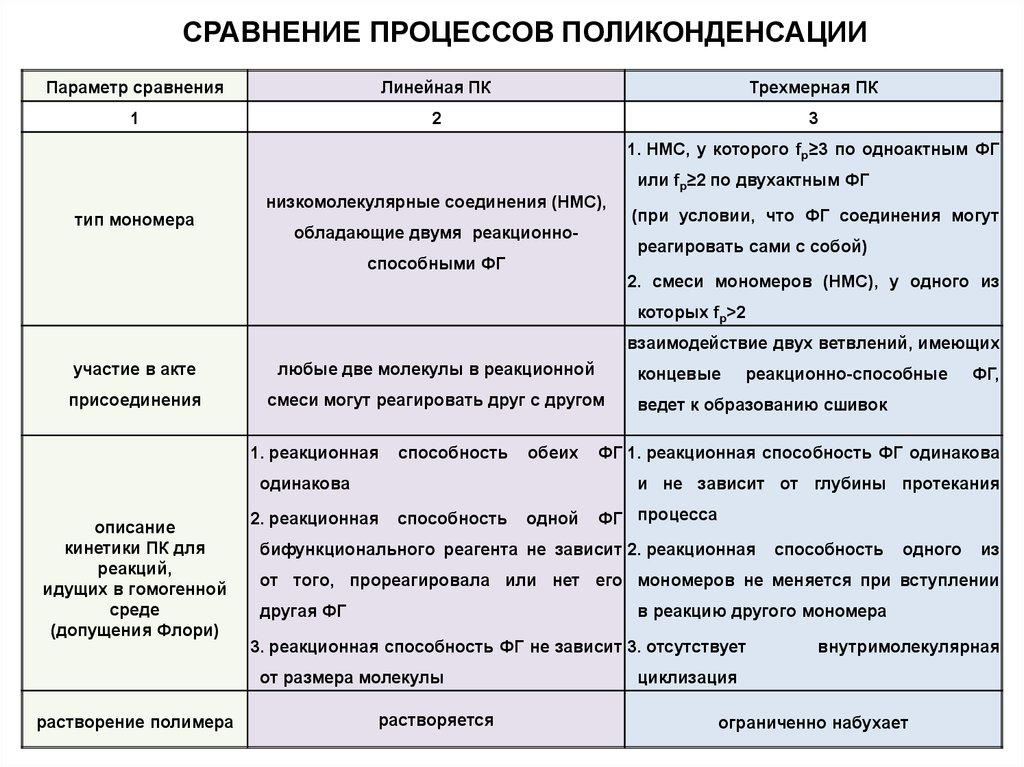
СРАВНЕНИЕ ПРОЦЕССОВ ПОЛИКОНДЕНСАЦИИПараметр сравнения
Линейная ПК
Трехмерная ПК
1
2
3
1. НМС, у которого fр≥3 по одноактным ФГ
тип мономера
низкомолекулярные соединения (НМС),
обладающие двумя реакционно-
или fр≥2 по двухактным ФГ
(при условии, что ФГ соединения могут
реагировать сами с собой)
способными ФГ
2. смеси мономеров (НМС), у одного из
которых fр>2
взаимодействие двух ветвлений, имеющих
участие в акте
любые две молекулы в реакционной
присоединения
смеси могут реагировать друг с другом
1. реакционная
способность
обеих
одинакова
описание
кинетики ПК для
реакций,
идущих в гомогенной
среде
(допущения Флори)
реакционно-способные
ФГ,
ведет к образованию сшивок
ФГ 1. реакционная способность ФГ одинакова
и не зависит от глубины протекания
2. реакционная
способность
одной
ФГ процесса
бифункционального реагента не зависит 2. реакционная
способность
одного
из
от того, прореагировала или нет его мономеров не меняется при вступлении
другая ФГ
в реакцию другого мономера
3. реакционная способность ФГ не зависит 3. отсутствует
от размера молекулы
растворение полимера
концевые
растворяется
внутримолекулярная
циклизация
ограниченно набухает
24.
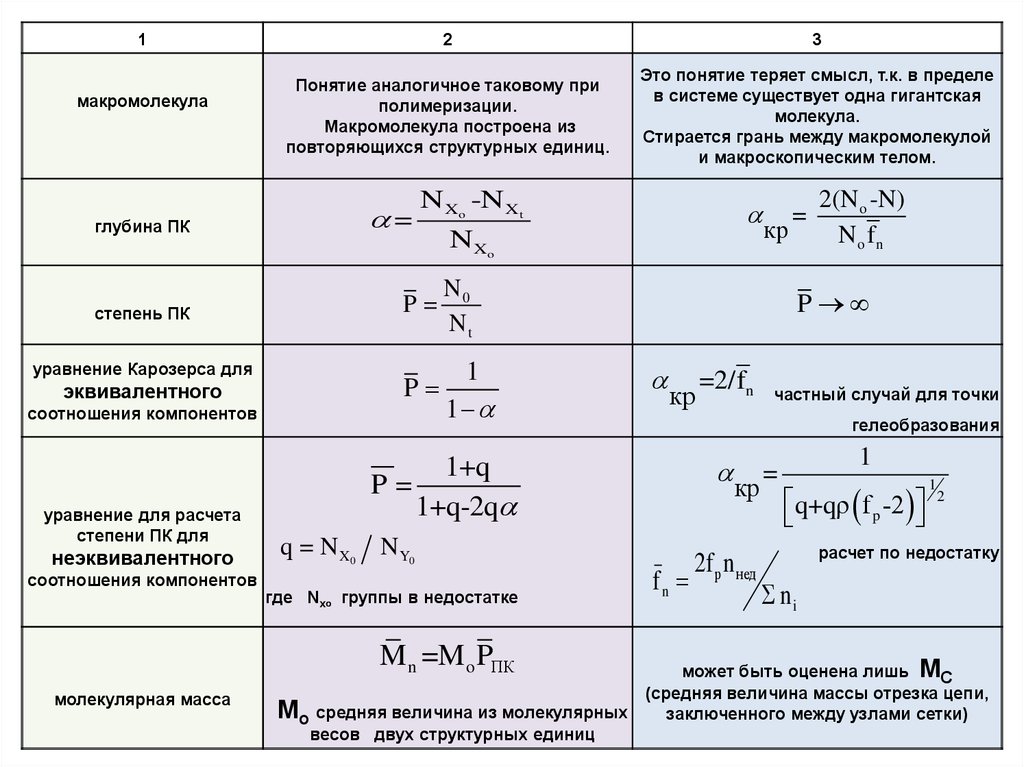
1макромолекула
глубина ПК
степень ПК
уравнение Карозерса для
эквивалентного
2
3
Понятие аналогичное таковому при
полимеризации.
Макромолекула построена из
повторяющихся структурных единиц.
Это понятие теряет смысл, т.к. в пределе
в системе существует одна гигантская
молекула.
Стирается грань между макромолекулой
и макроскопическим телом.
=
неэквивалентного
соотношения компонентов
N0
Nt
P
1
1
q = N X0 N Y0
где Nxo группы в недостатке
Мo средняя величина из молекулярных
весов двух структурных единиц
кр
=
2(N o -N)
N o fn
P
кр
=2/fn
частный случай для точки
гелеобразования
1+q
P=
1+q-2q
M n =M o PПК
молекулярная масса
N Xo
P=
соотношения компонентов
уравнение для расчета
степени ПК для
N Xo -N Xt
fn
кр
2f р n нед
=
1
q+qρ f p -2
1
2
расчет по недостатку
Σ ni
может быть оценена лишь МС
(средняя величина массы отрезка цепи,
заключенного между узлами сетки)













 chemistry
chemistry