Similar presentations:
Общая характеристика неметаллов. 9 класс
1.
2.
ГрафитКрасный
фосфор
Фтор
Сера
Бром
Иод
Кремний
3.
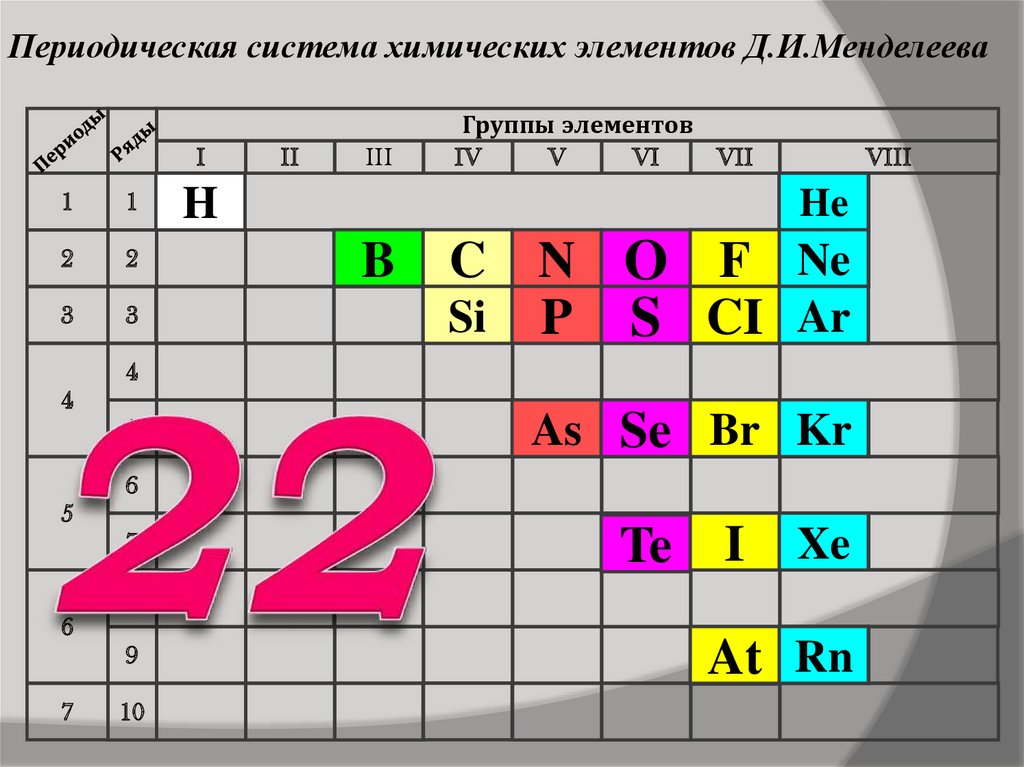
Периодическая система химических элементов Д.И.МенделееваI
1
1
2
2
3
3
II
III
Группы элементов
IV
V
VI
VII
H
VIII
He
B
C
Si
N O F Ne
P S CI Ar
4
4
5
As Se Br Kr
6
5
7
Te
I
Xe
8
6
9
7
10
At Rn
4.
Особенности атомного строения элементов-неметаллов.Небольшой атомный радиус (в сравнении
с радиусами атомов-металлов одного с ними
периода)
S +16 2ē8ē6ē
Большее число электронов на внешнем уровне
(4-8 е).
CI +17 2ē8ē7ē
Элементы-неметаллы расположены только
в главных подгруппах
C +6 2ē4ē
Ne +10 2ē8ē
Для атомов-неметаллов характерны
высокие значения ЭО
5.
Заполняетсявнешний электронный
слой
В основном это р - элементы
Способны
принимать электроны
(8- Nгруппы) и отдавать (Nгруппы)
Неме + nē →Неме-nē
Неме - nē →Неме+nē
Являются
окислителями
Имеют несколько степеней окисления.
Например: N-3 N+1 N+2 N+3 N+4 N+5
6.
СвязьКовалентная неполярная
Между большим
числом атомов
Между двумя и
несколькими атомами
Строение
немолекулярное
Вещества
молекулярное
C, Si, P, B
H2, O2, CI2, I2, F2, S2, N2
Кристаллические решетки
Атомная
Молекулярная
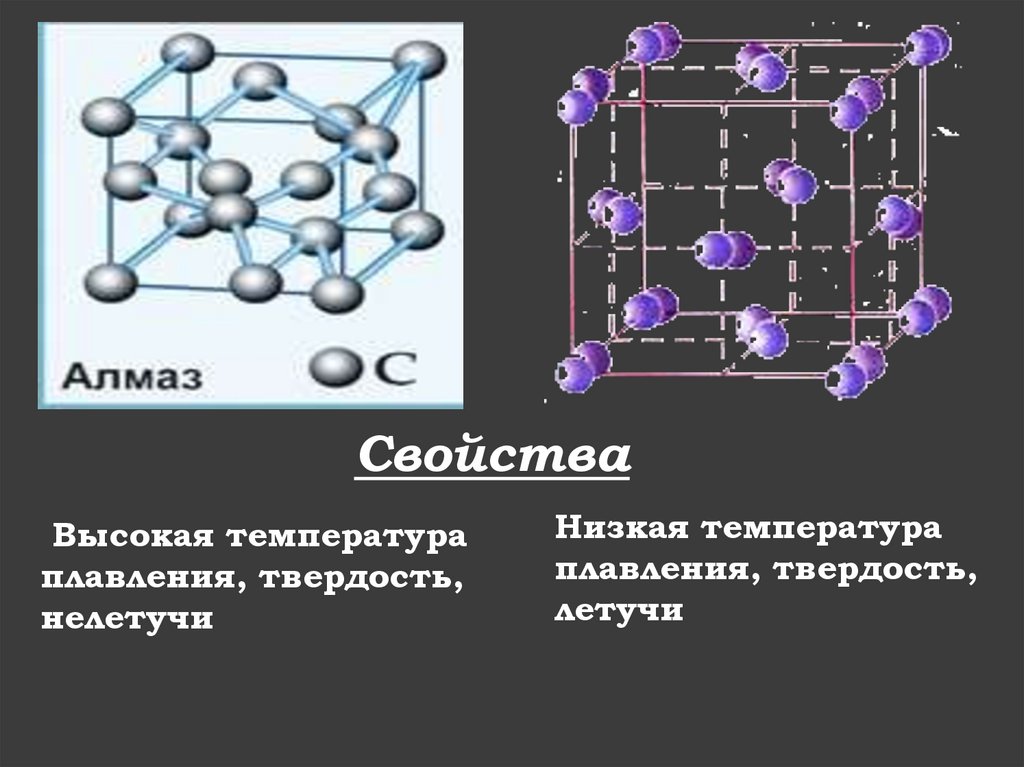
7.
СвойстваВысокая температура
плавления, твердость,
нелетучи
Низкая температура
плавления, твердость,
летучи
8.
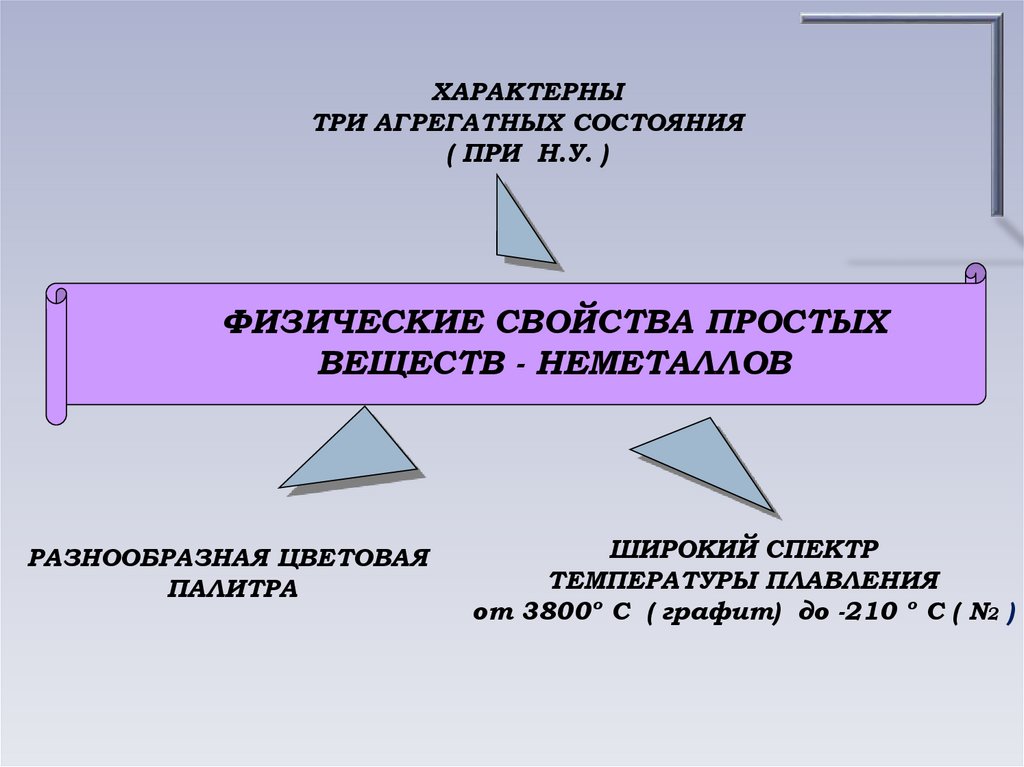
ХАРАКТЕРНЫТРИ АГРЕГАТНЫХ СОСТОЯНИЯ
( ПРИ Н.У. )
ФИЗИЧЕСКИЕ СВОЙСТВА ПРОСТЫХ
ВЕЩЕСТВ - НЕМЕТАЛЛОВ
РАЗНООБРАЗНАЯ ЦВЕТОВАЯ
ПАЛИТРА
ШИРОКИЙ СПЕКТР
ТЕМПЕРАТУРЫ ПЛАВЛЕНИЯ
от 3800º С ( графит) до -210 º С ( N2 )
9.
Твердые: C, P, I2P
фосфор
C
углерод
I2
йод
10.
Твердые: Si, S11.
Жидкие: Br211
12.
Газообразные: O2, N2, Cl2, F2F2
фтор
Cl2
хлор
13.
Газообразные: H2, O2, N214. Дополнение
Не обладают блескомНе проводят ток и тепло
Не пластичны
15. Аллотропия
Явление существованиянескольких простых
веществ, образованных
одним химическим
элементом
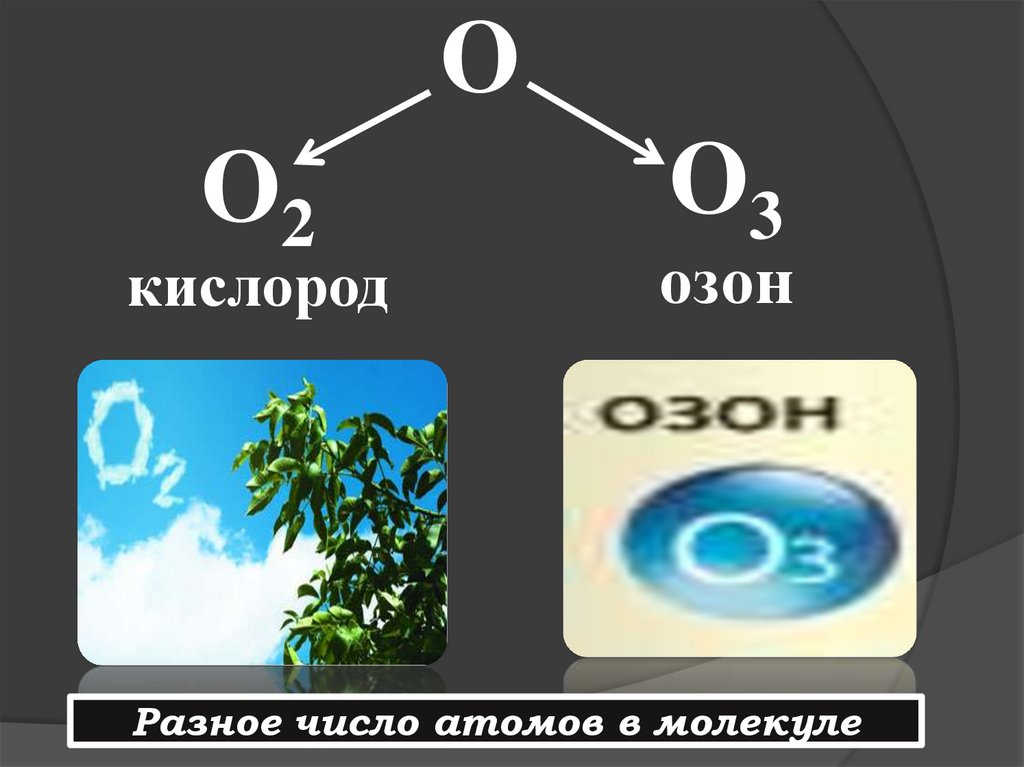
16.
OO2
кислород
O3
озон
Разное число атомов в молекуле
17.
Разная кристаллическая решеткаАлмаз
атомная
Красный
Графит
молекулярная
Белый
18.
Разное расположение атомов вкристаллической решетке
19.
20.
1. Для атомов неметалловхарактерно:
а) большое число электронов
на последнем уровне
б) относительно большой
радиус атома
в) малое число электронов на
последнем уровне
г) относительно малый
радиус атома
21.
2.Для простых веществ
неметаллов характерны
кристаллические
решетки:
а) атомные и ионные
б) ионные и молекулярные
в) атомные и молекулярные
г) металлические и ионные
22.
3. К простым веществамнеметаллам не относится:
а) кислород
б) озон
в) воздух
г) бром
23.
4. Аллотропноймодификацией кислорода
является:
а) азот
б) озон
в) воздух
г) йод
24.
5. явление аллотропии несвойственно элементу:
а) фосфор
б) азот
в) кремний
г) бор
25.
6. атомную кристаллическуюрешетку имеет:
а) йод
б) белый фосфор
в) кремний
г) кислород
26.
7. Количество неметалловравно:
а)
б)
в)
г)
80
400
22
50
27.
28.
Способныпринимать
электроны (8- Nгруппы)
Неме + nē →Неме-nē
Являются
окислителями
Могут отдавать электроны к
более ЭО атому-неметаллу
(N группы)
Неме - nē →Неме+nē
Являются восстановителями
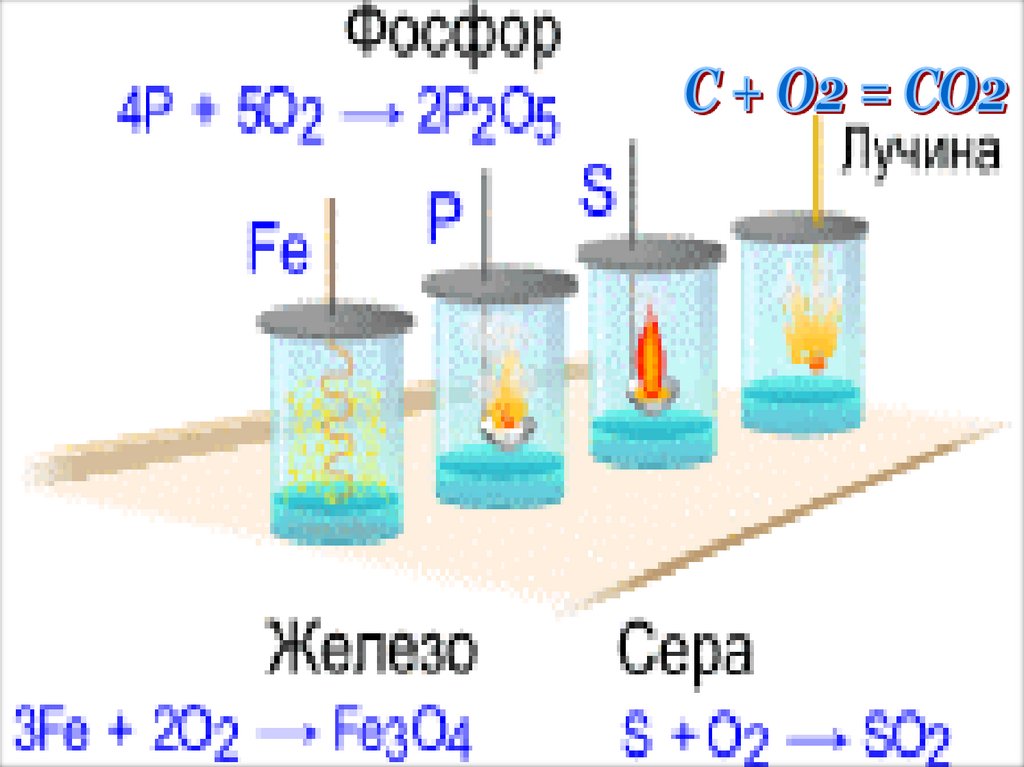
29. Химические свойства
Окислительные(с менее ЭО)
Восстановительные
(с более ЭО)






























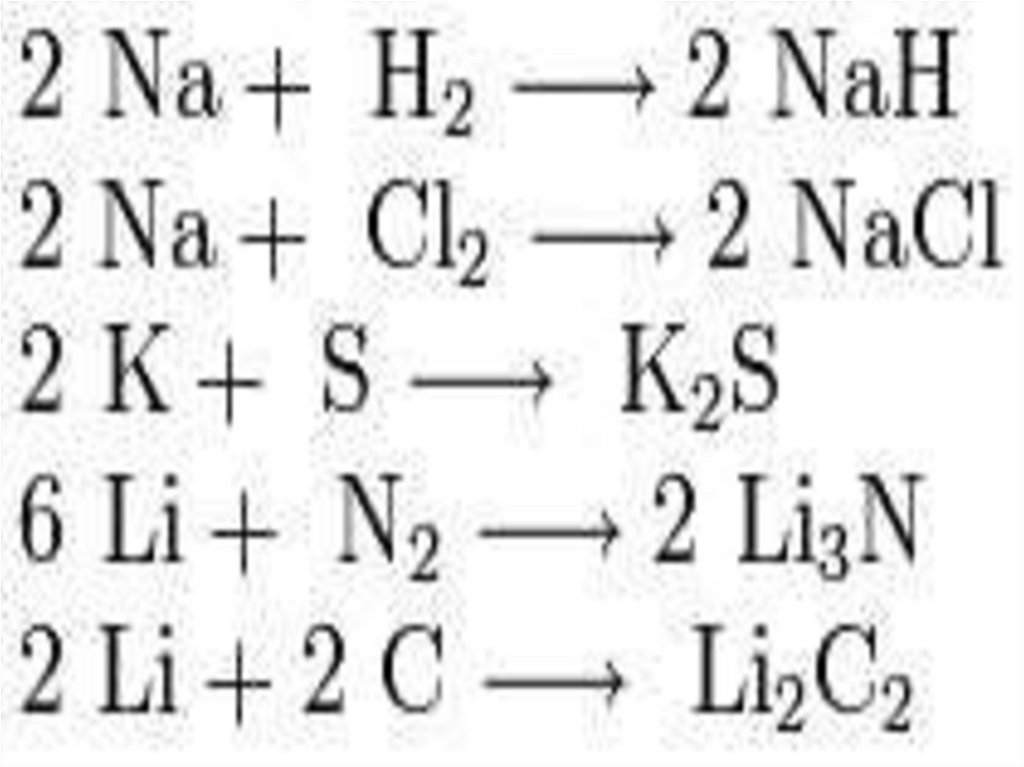

 chemistry
chemistry








