Similar presentations:
Гетерофункциональные соединения
1.
Гетерофункциональныесоединения
2. Органические соединения, содержащие разные функциональные группы, называются гетерофункциональными
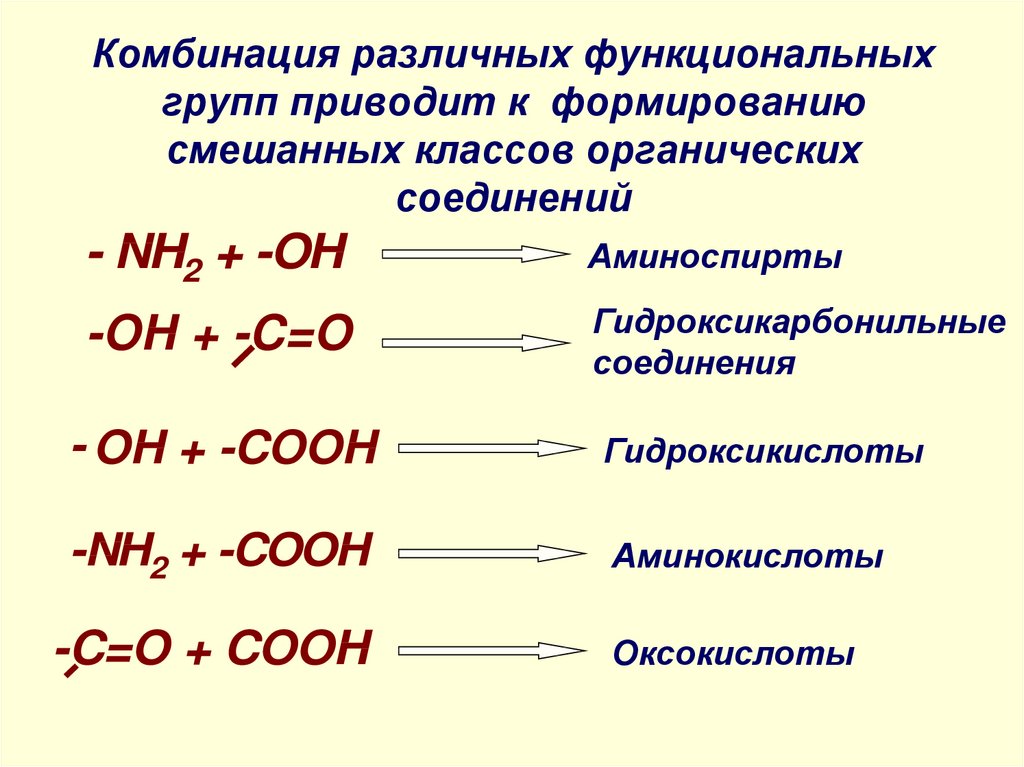
3. Комбинация различных функциональных групп приводит к формированию смешанных классов органических соединений
- NH2 + -OHАминоспирты
-OH + -C=O
Гидроксикарбонильные
соединения
- OH + -COOH
Гидроксикислоты
-NH2 + -COOH
Аминокислоты
-C=O + COOH
Оксокислоты
4.
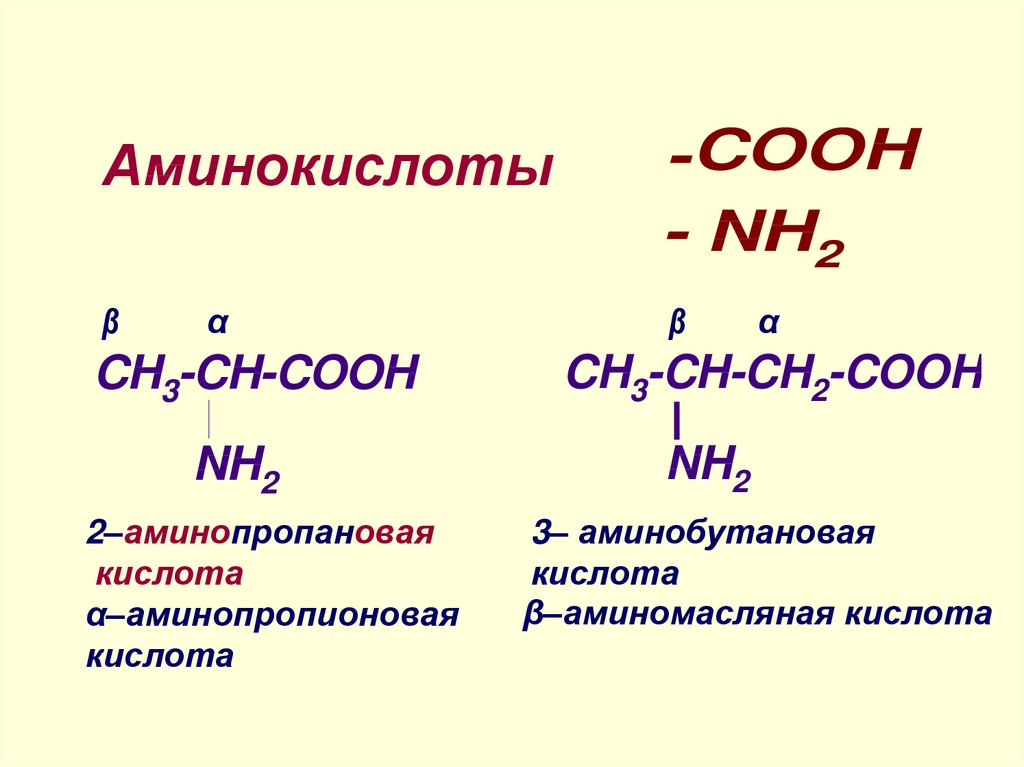
Аминокислоты-COOH
- NH2
β
β
α
CH3-CH-COOH
NH2
2–аминопропановая
кислота
α–аминопропионовая
кислота
α
CH3-CH-CH2-COOH
NH2
3– аминобутановая
кислота
β–аминомасляная кислота
5.
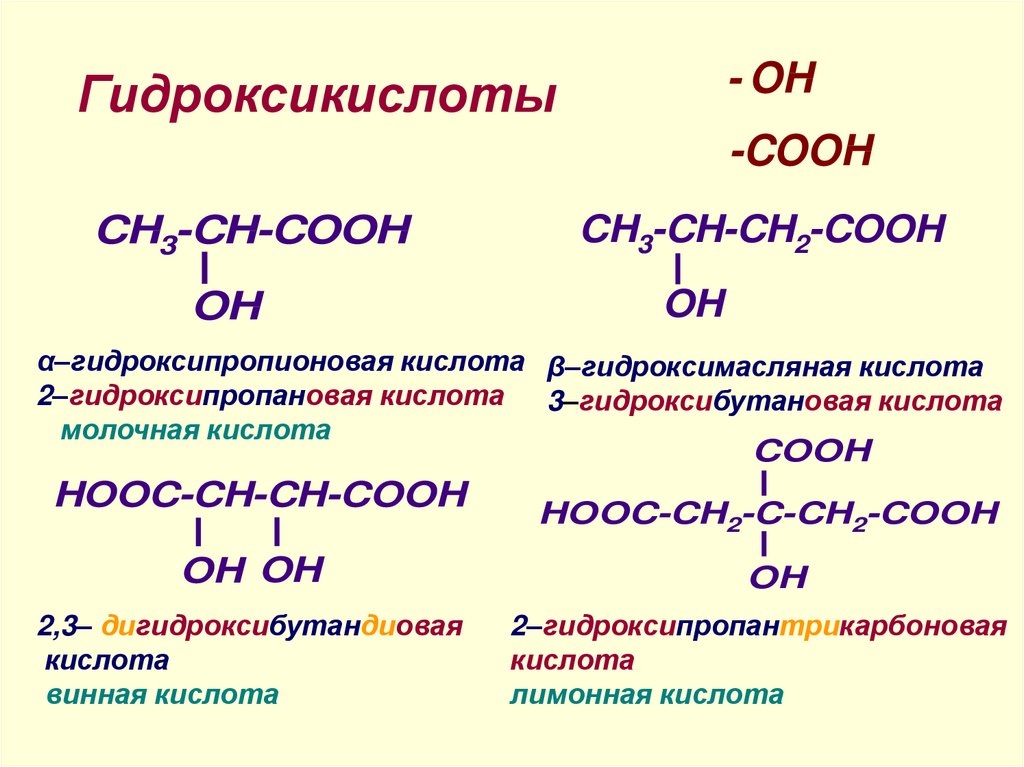
- OHГидроксикислоты
-COOH
CH3-CH-COOH
OH
CH3-CH-CH2-COOH
OH
α–гидроксипропионовая кислота β–гидроксимасляная кислота
2–гидроксипропановая кислота 3–гидроксибутановая кислота
молочная кислота
COOH
HOOC-CH-CH-COOH
OH OH
2,3– дигидроксибутандиовая
кислота
винная кислота
HOOC-CH2-C-CH2-COOH
OH
2–гидроксипропантрикарбоновая
кислота
лимонная кислота
6.
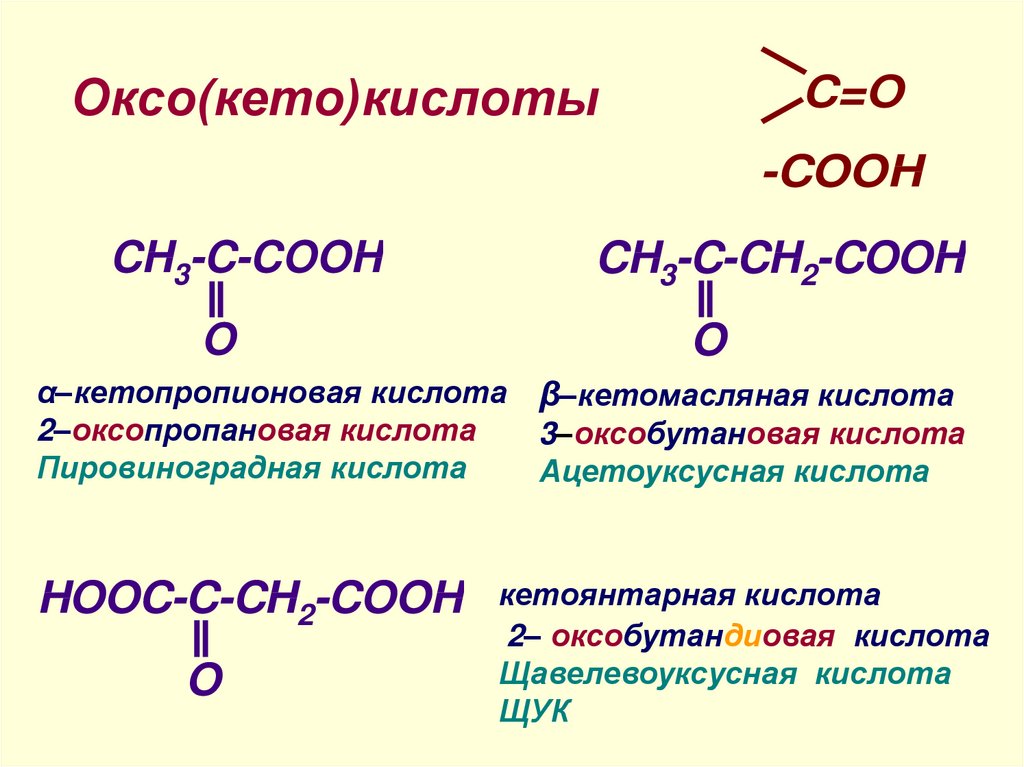
Оксо(кето)кислотыC=O
-COOH
CH3-C-COOH
CH3-C-CH2-COOH
O
O
α–кетопропионовая кислота
2–оксопропановая кислота
Пировиноградная кислота
HOOC-C-CH2-COOH
O
β–кетомасляная кислота
3–оксобутановая кислота
Ацетоуксусная кислота
кетоянтарная кислота
2– оксобутандиовая кислота
Щавелевоуксусная кислота
ЩУК
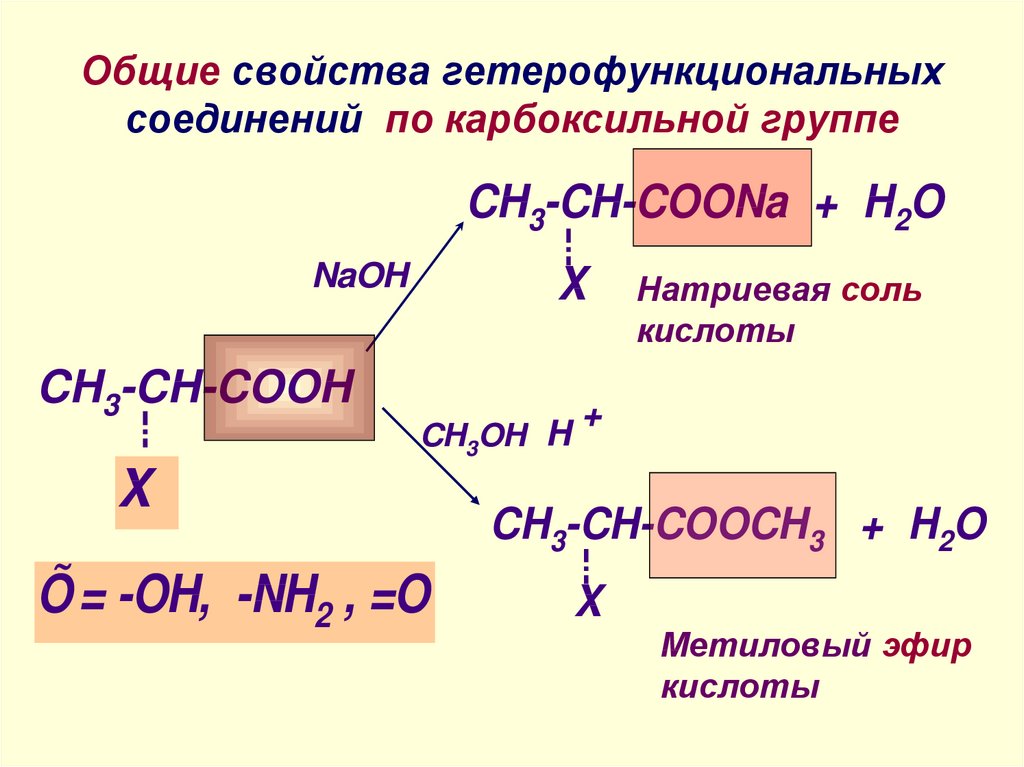
7. Общие свойства гетерофункциональных соединений по карбоксильной группе
CH3-CH-COONa + H2ONaOH
CH3-CH-COOH
X
CH3OH H
X
Õ = -OH, -NH2 , =O
Натриевая соль
кислоты
+
CH3-CH-COOCH3 + H2O
X
Метиловый эфир
кислоты
8.
+CH3-CH2
C
+
CH3-CH
O
-I эффект гидроксильной
группы
+
O
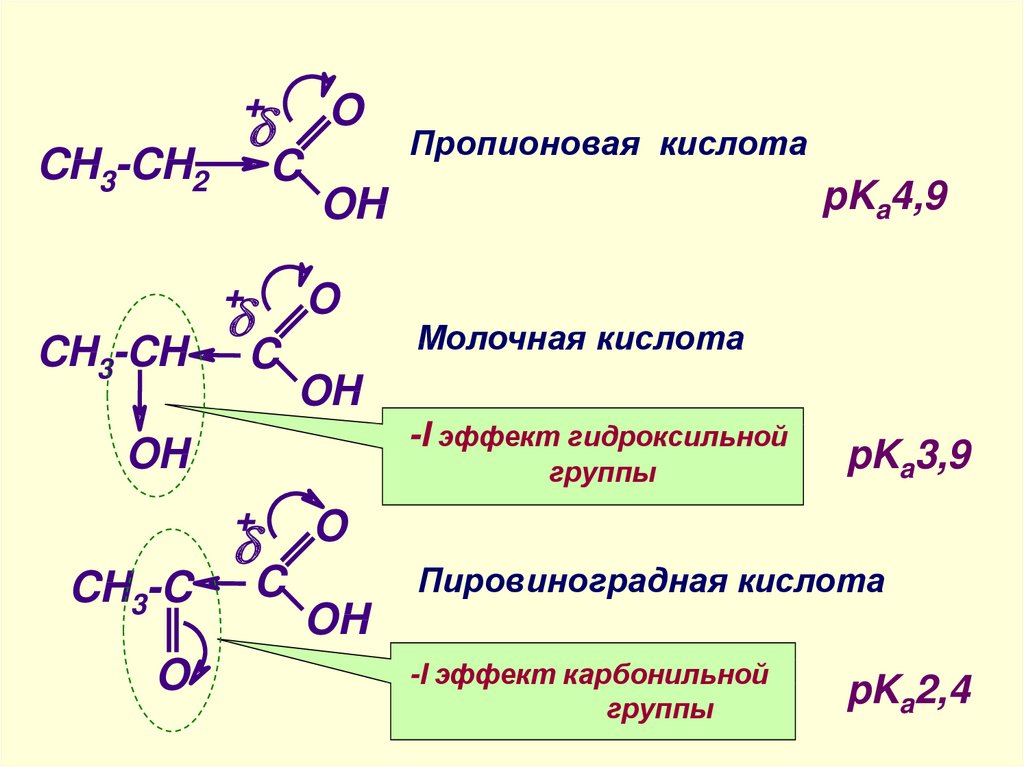
Молочная кислота
OH
OH
CH3-C
pKa4,9
OH
O
C
Пропионовая кислота
C
pKa3,9
O
Пировиноградная кислота
OH
-I эффект карбонильной
группы
pKa2,4
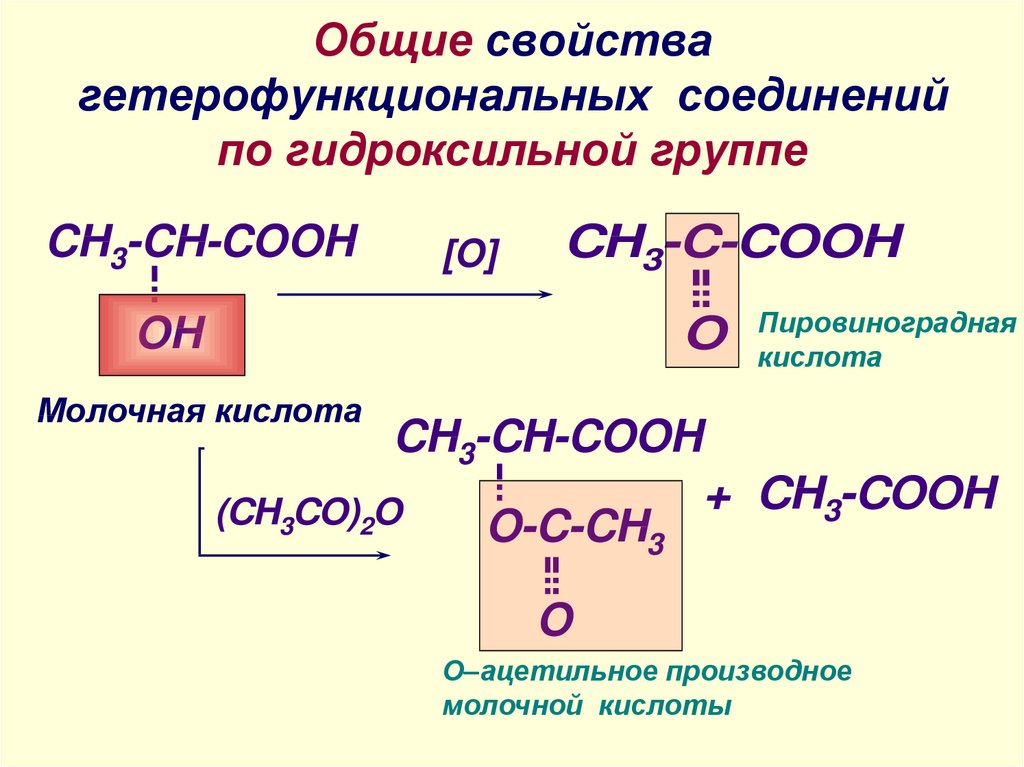
9. Общие свойства гетерофункциональных соединений по гидроксильной группе
CH3-CH-COOH[O]
CH3-C-COOH
O
OH
Пировиноградная
кислота
Молочная кислота
CH3-CH-COOH
+ CH3-COOH
(CH3CO)2O
O-C-CH3
O
О–ацетильное производное
молочной кислоты
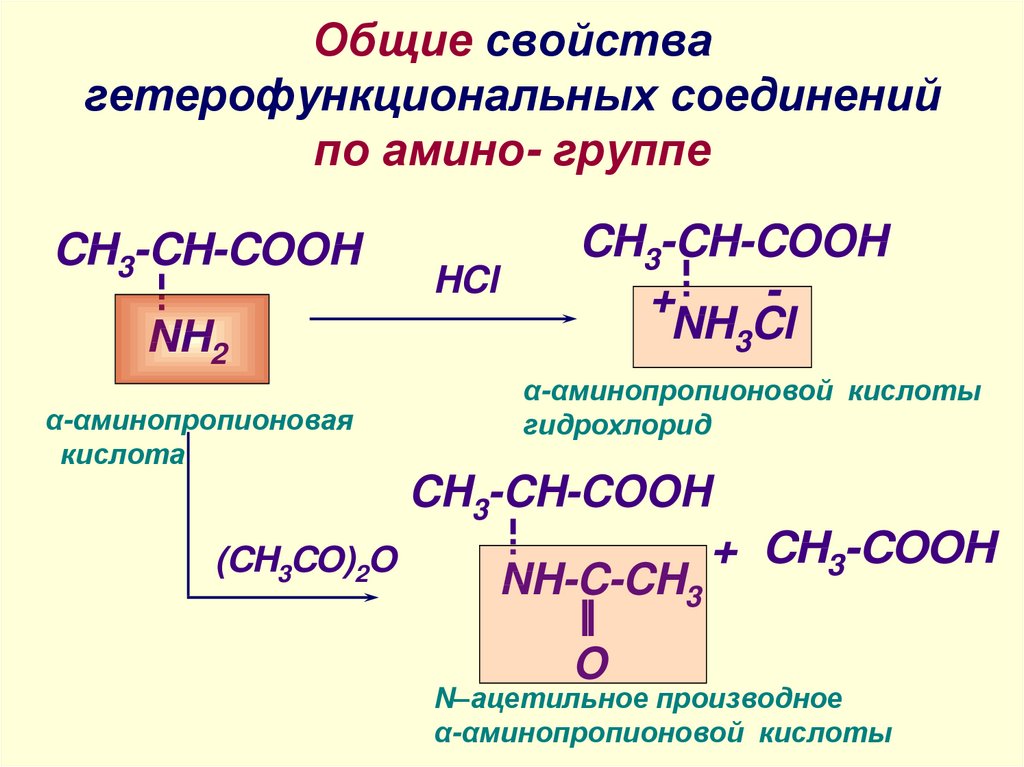
10. Общие свойства гетерофункциональных соединений по амино- группе
CH3-CH-COOHNH2
α-αминопропионовая
кислота
HCl
CH3-CH-COOH
+
NH3Cl
α-αминопропионовой кислоты
гидрохлорид
CH3-CH-COOH
+ CH3-COOH
(CH3CO)2O
NH-C-CH3
O
N–ацетильное производное
α-αминопропионовой кислоты
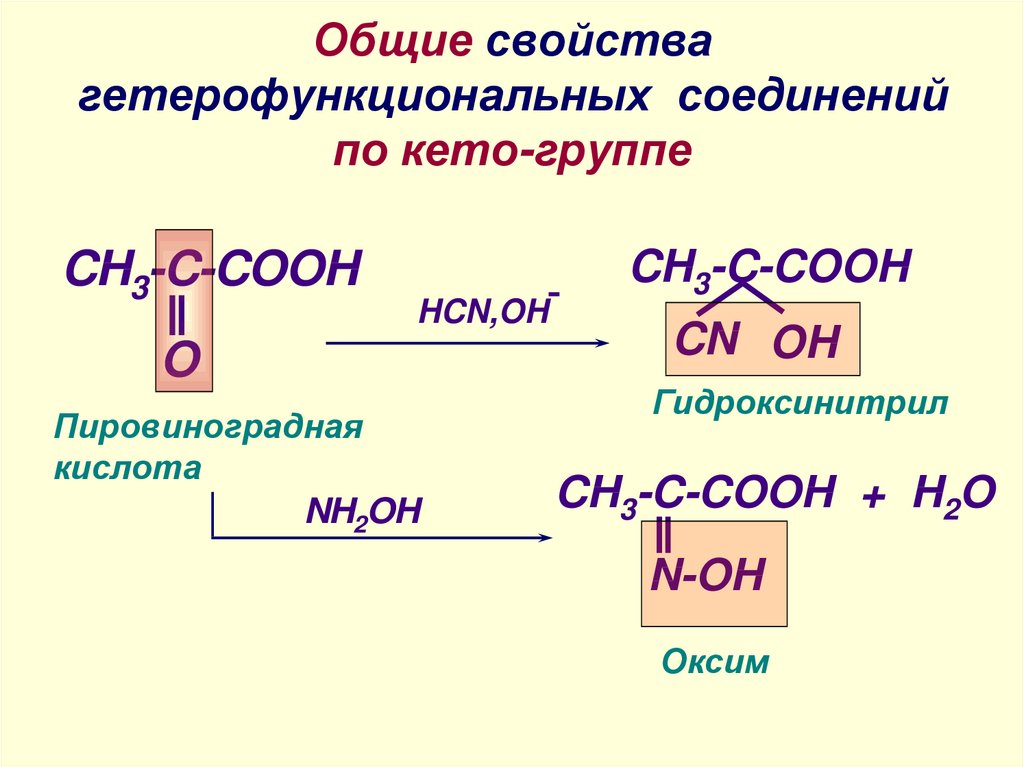
11. Общие свойства гетерофункциональных соединений по кето-группе
CH3-C-COOHHCN,OH
O
Пировиноградная
кислота
NH2OH
CH3-C-COOH
CN OH
Гидроксинитрил
CH3-C-COOH + H2O
N-OH
Оксим
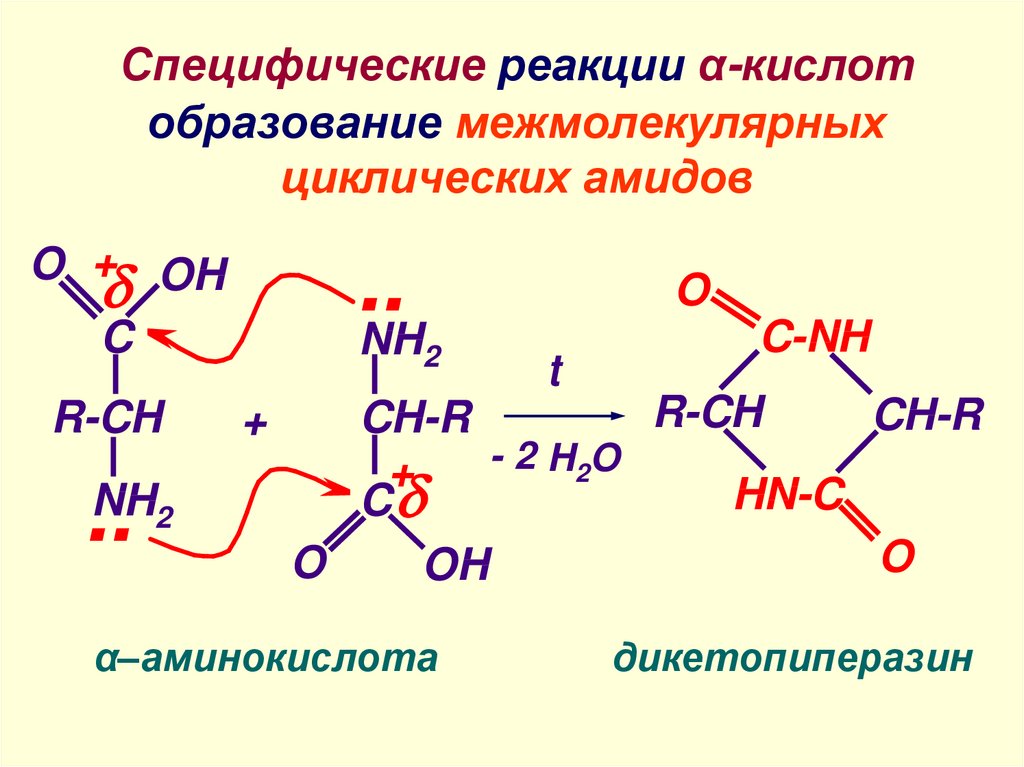
12. Специфические реакции α-кислот образование межмолекулярных циклических амидов
O + OHC
R-CH
..
NH2
..
NH2
+
O
t
C-NH
R-CH
CH-R
CH-R
- 2 H 2O
+
HN-C
C
O
O
OH
α–аминокислота
дикетопиперазин
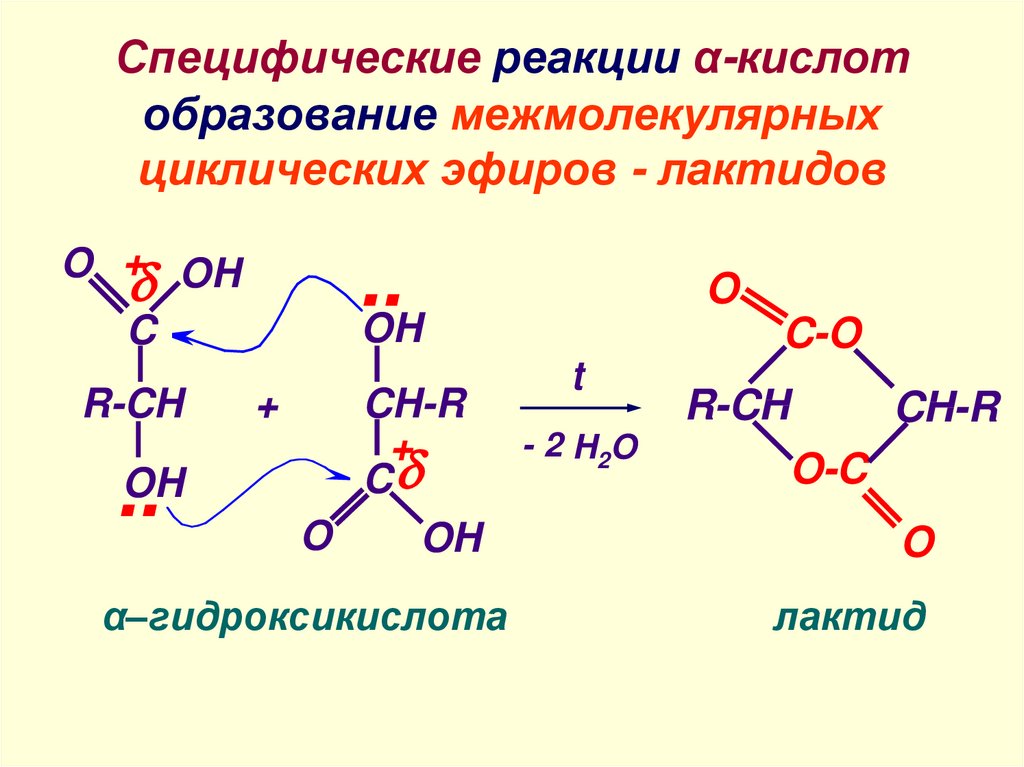
13. Специфические реакции α-кислот образование межмолекулярных циклических эфиров - лактидов
O + OHC
R-CH
..
OH
..
OH
+
O
C-O
t
CH-R
- 2 H 2O
+
C
O
OH
α–гидроксикислота
R-CH
CH-R
O-C
O
лактид
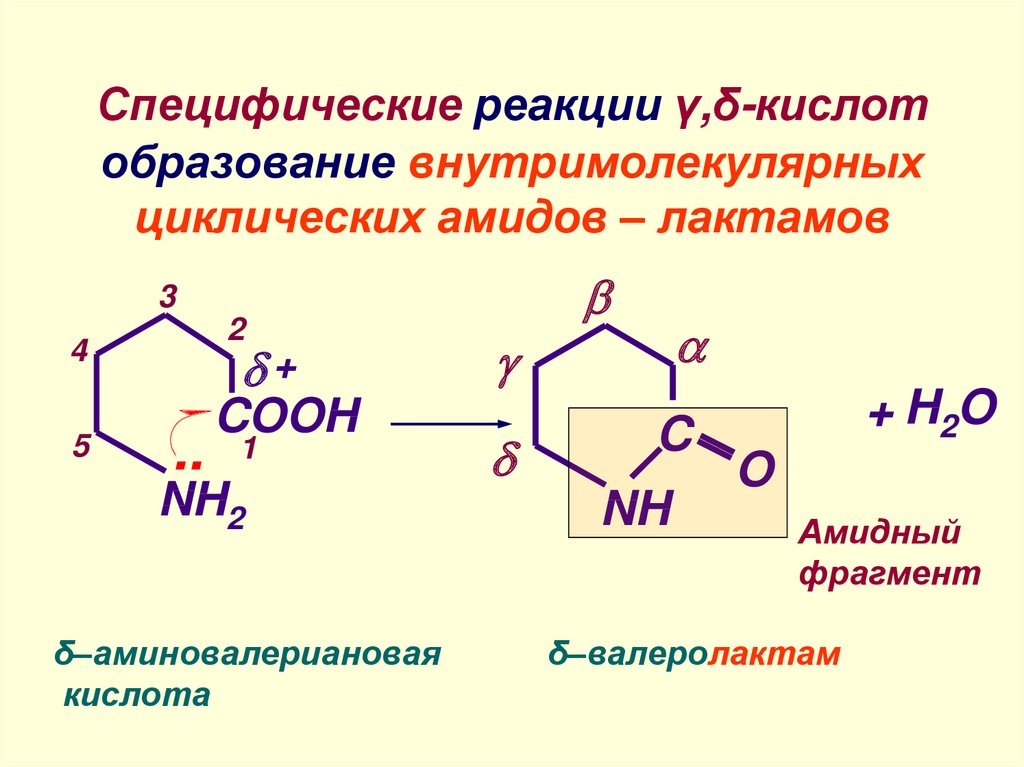
14. Специфические реакции γ,δ-кислот образование внутримолекулярных циклических амидов – лактамов
32
+
4
5
..
COOH
1
NH2
δ–аминовалериановая
кислота
C
NH
+ H2O
O
Амидный
фрагмент
δ–валеролактам
15. Специфические реакции γ,δ -кислот образование внутримолекулярных циклических эфиров – лактонов
32
4
..
+
COOH
C
1
OH
γ–гидроксимасляная
кислота
+ H2O
O
O
Сложноэфирный
фрагмент
γ–бутиролактон
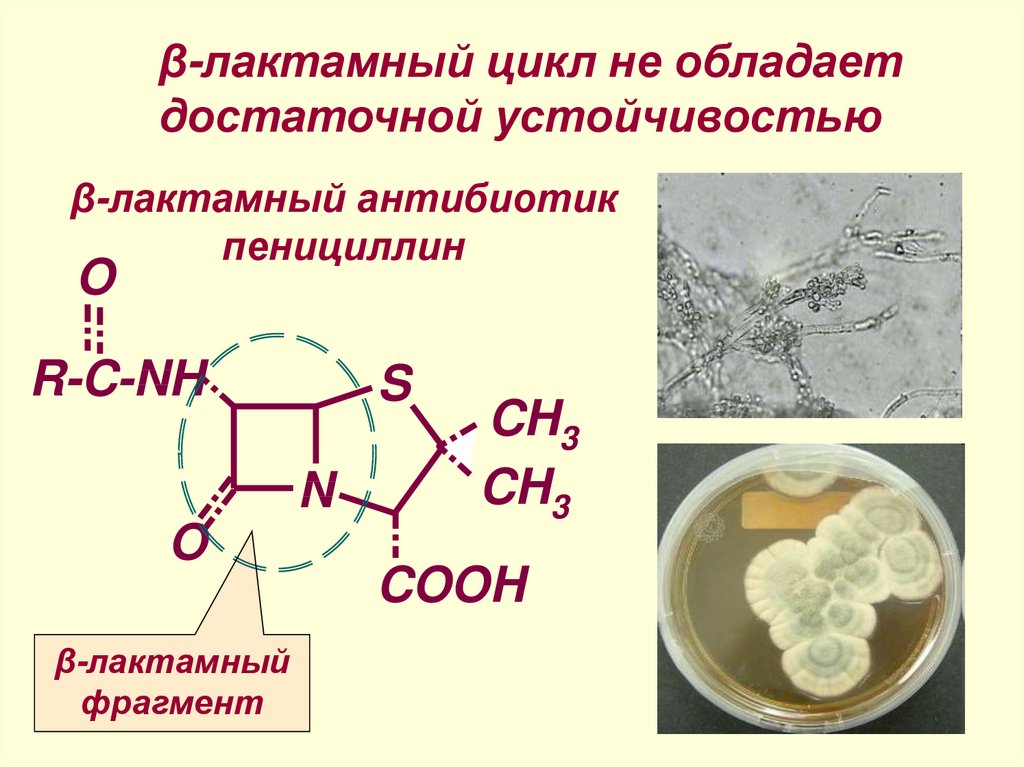
16. β-лактамный антибиотик пенициллин
β-лактамный цикл не обладаетдостаточной устойчивостью
β-лактамный антибиотик
пенициллин
O
R-C-NH
S
N
O
β-лактамный
фрагмент
CH3
CH3
COOH
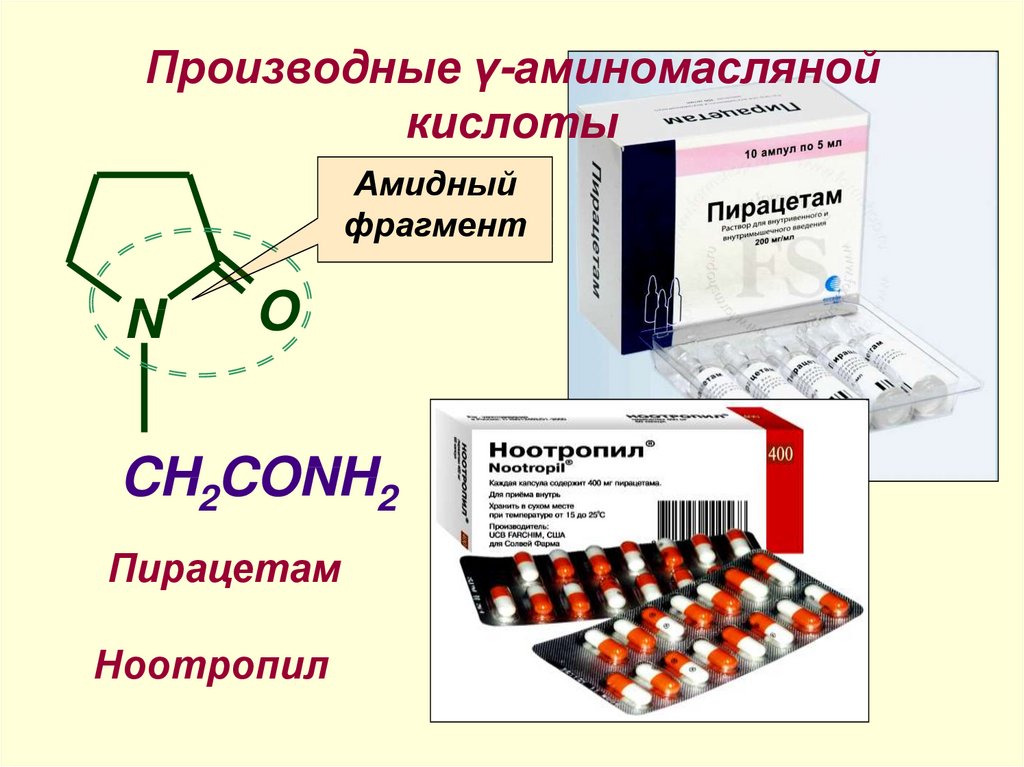
17. Производные γ-аминомасляной кислоты
Амидныйфрагмент
N
O
CH2CONH2
Пирацетам
Ноотропил
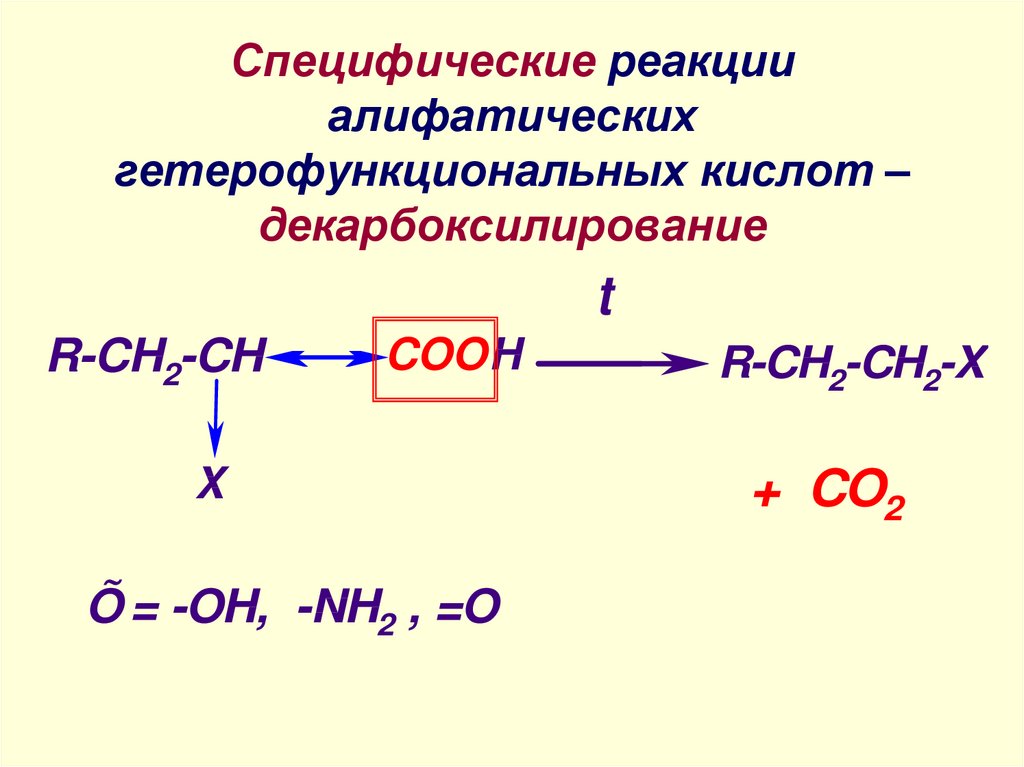
18. Специфические реакции алифатических гетерофункциональных кислот – декарбоксилирование
tR-CH2-CH
COO H
X
Õ = -OH, -NH2 , =O
R-CH2-CH2-X
+ CO2
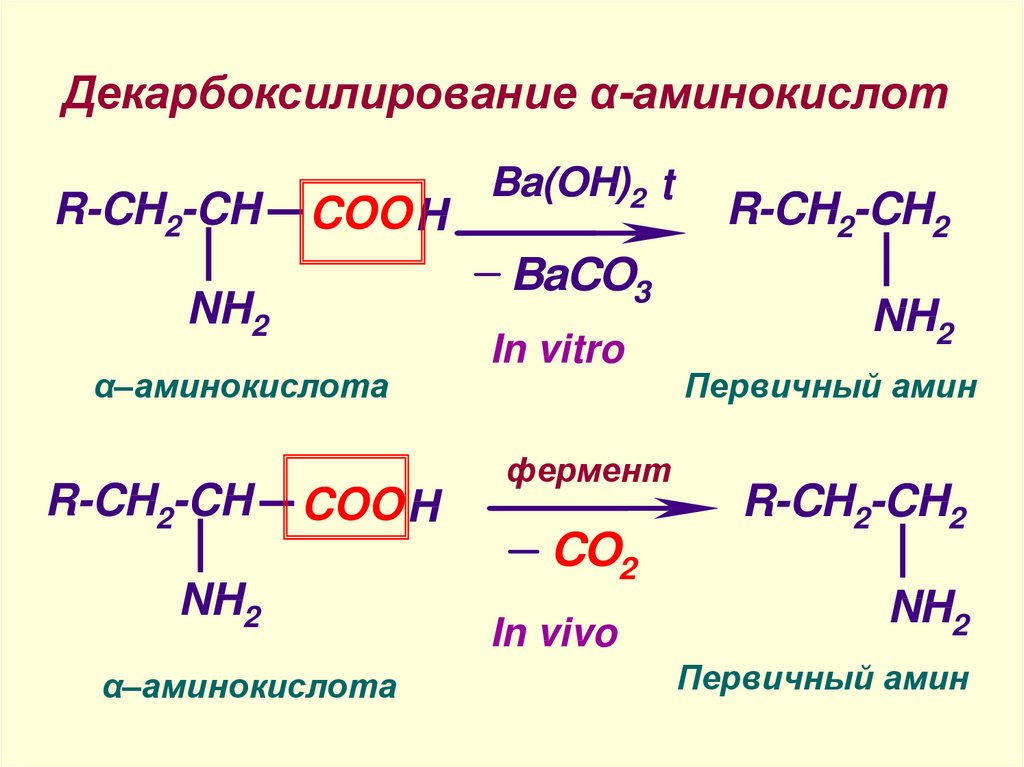
19. Декарбоксилирование α-аминокислот
R-CH2-CHCOO H
+ BaCO3
NH2
α–аминокислота
R-CH2-CH
Ba(OH)2 t
COO H
NH2
α–аминокислота
In vitro
фермент
+ CO2
In vivo
R-CH2-CH2
NH2
Первичный амин
R-CH2-CH2
NH2
Первичный амин
20. Декарбоксилирование α-гидроксикислот
R-CH2-CHCOOH c. H2SO4 t
OH
α-гидроксикислота
O
R-CH2-C
Альдегид
+
H
H-COOH
Муравьиная
кислота
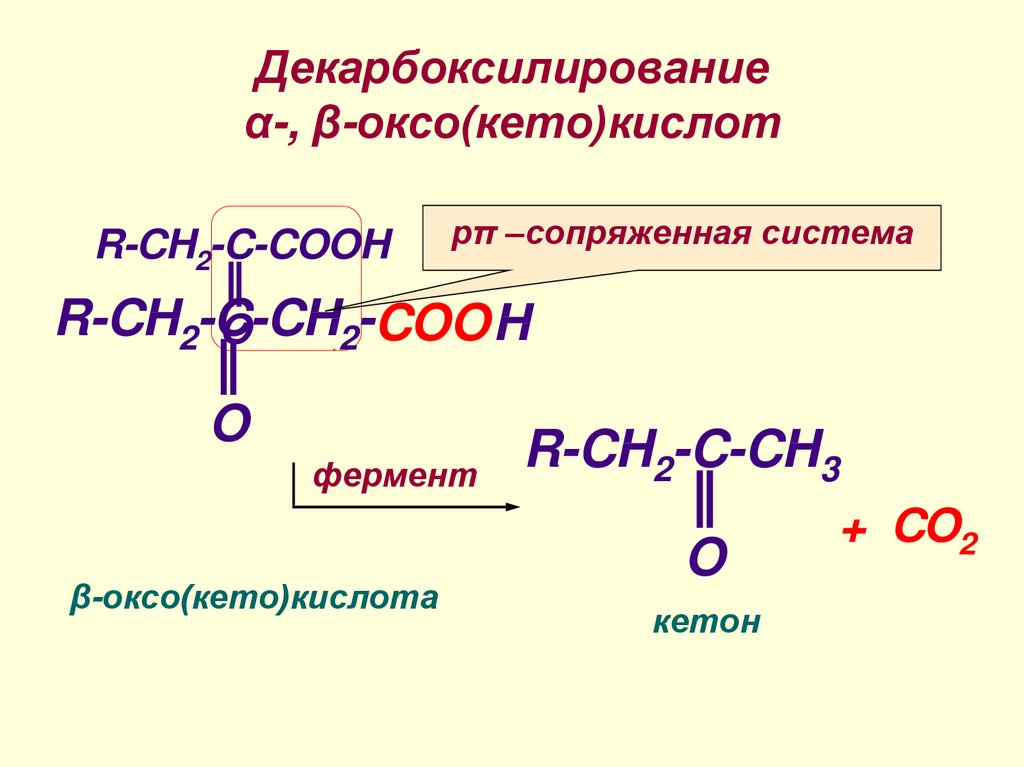
21. Декарбоксилирование α-, β-оксо(кето)кислот
R-CH2-C-COOHpπ –сопряженная система
R-CH2-C-CH
O
2-COO H
O
фермент
β-оксо(кето)кислота
R-CH2-C-CH3
O
кетон
+ CO2
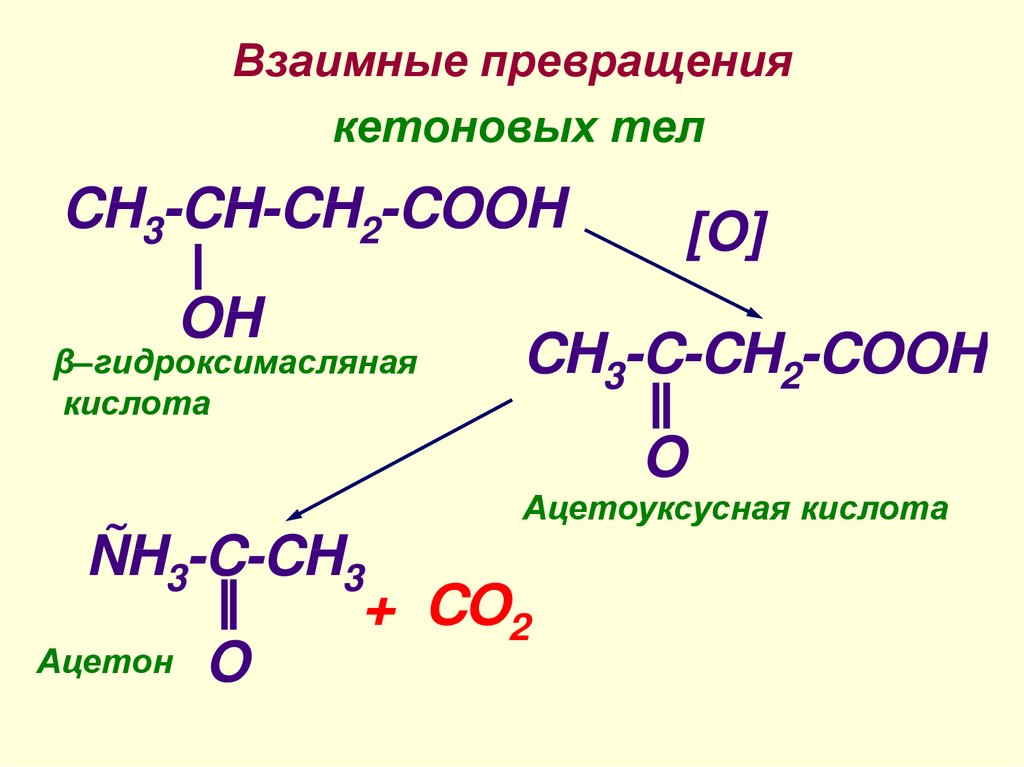
22. Взаимные превращения кетоновых тел
CH3-CH-CH2-COOHOH
β–гидроксимасляная
кислота
[O]
CH3-C-CH2-COOH
O
Ацетоуксусная кислота
ÑH3-C-CH3
+ CO2
Ацетон O
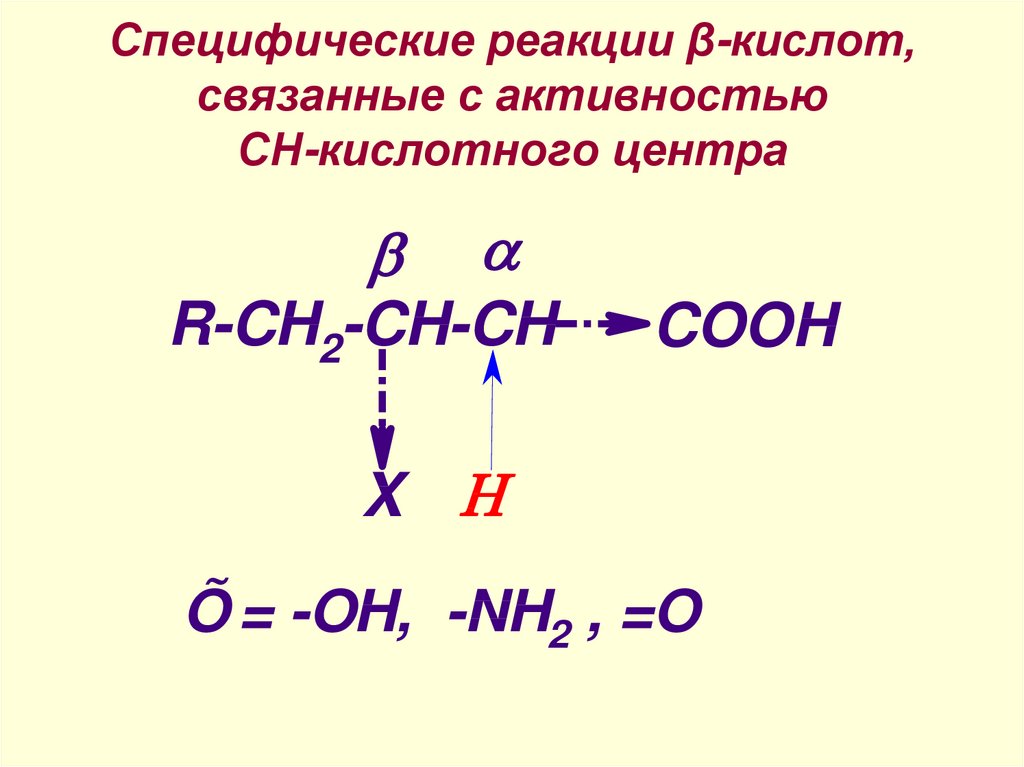
23. Специфические реакции β-кислот, связанные с активностью СН-кислотного центра
R-CH2-CH-CH2X
COOH
Õ = -OH, -NH2 , =O
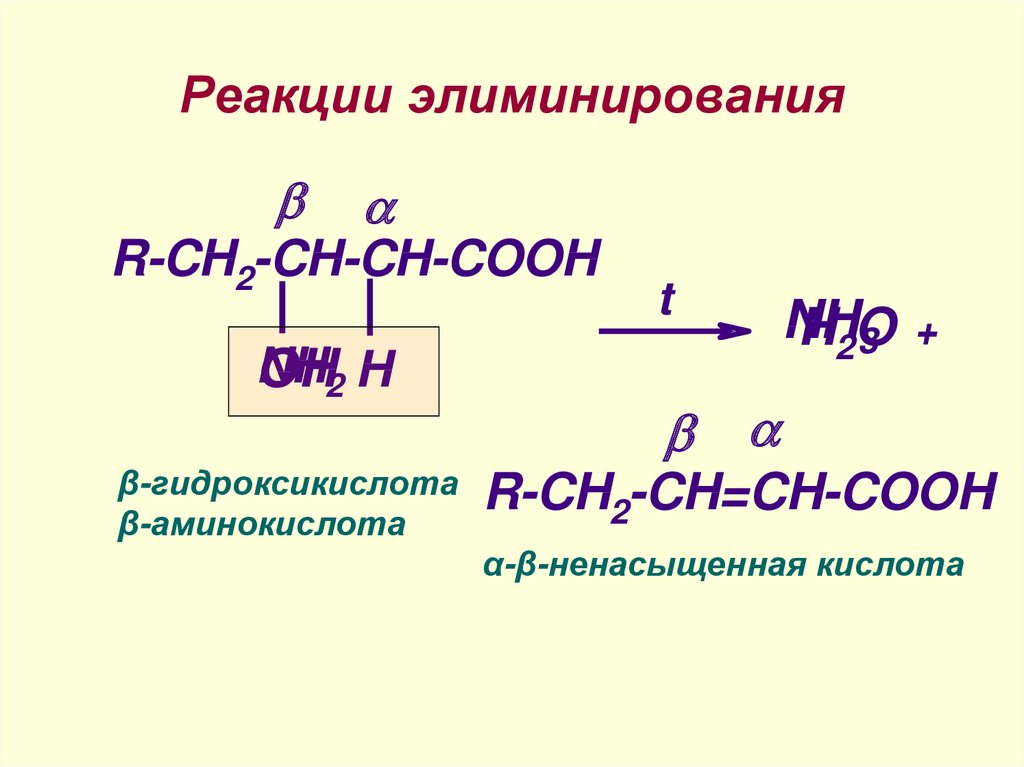
24. Реакции элиминирования
R-CH2-CH-CH-COOHNH
OH2 H
β-гидроксикислота
β-аминокислота
t
NH
H2O
3 +
R-CH2-CH=CH-COOH
α-β-ненасыщенная кислота
25. Специфические реакции β-оксо(кето)кислот, связанные с активностью СН-кислотного центра – это их способность к существованию в
двух таутомерных формах.Таутомерия – равновесная
динамическая изомерия.
Таутомеры самопроизвольно
превращаются друг в друга и
существуют в подвижном
равновесии за счет переноса какойлибо подвижной группы.
26.
Таутомерия ацетоуксусного эфираСН–кислотный центр
CH3-C
:O
H
C
H
O
C
92,5%
OC2H5
Кето–форма
Основный центр
O
7,5%
CH3-C=CH-C
OH
OC2H5
Енольная форма
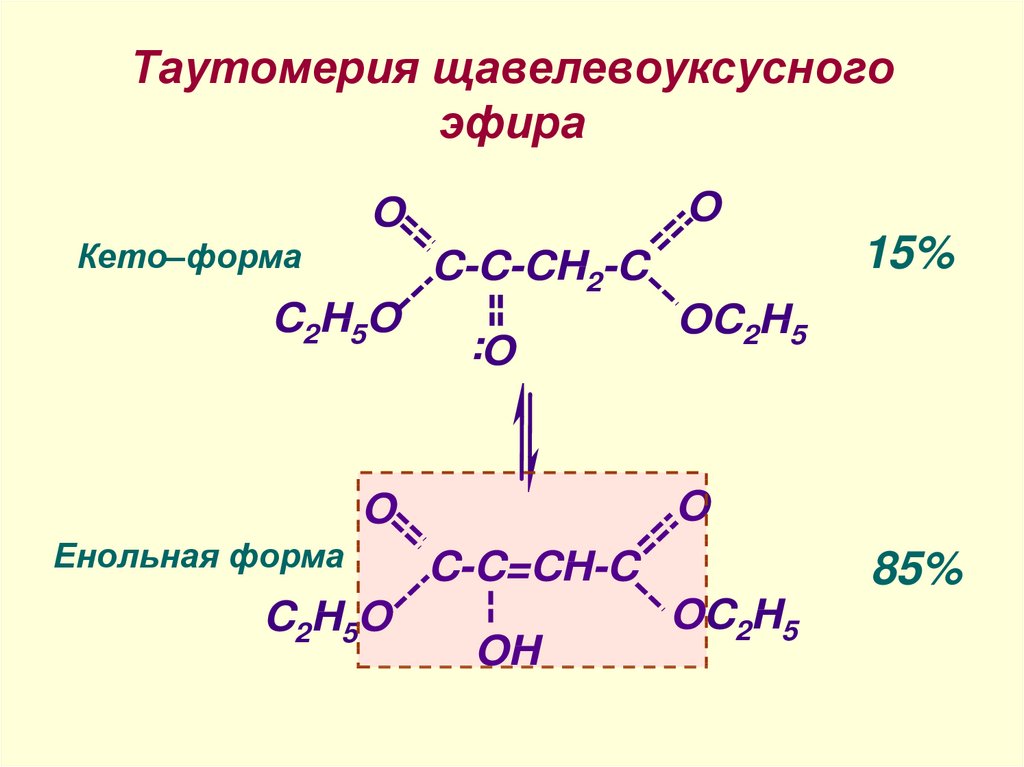
27. Таутомерия щавелевоуксусного эфира
OO
Кето–форма
15%
C-C-CH2-C
C2H5O
:O
O
O
Енольная форма
C2H5O
OC2H5
85%
C-C=CH-C
OH
OC2H5
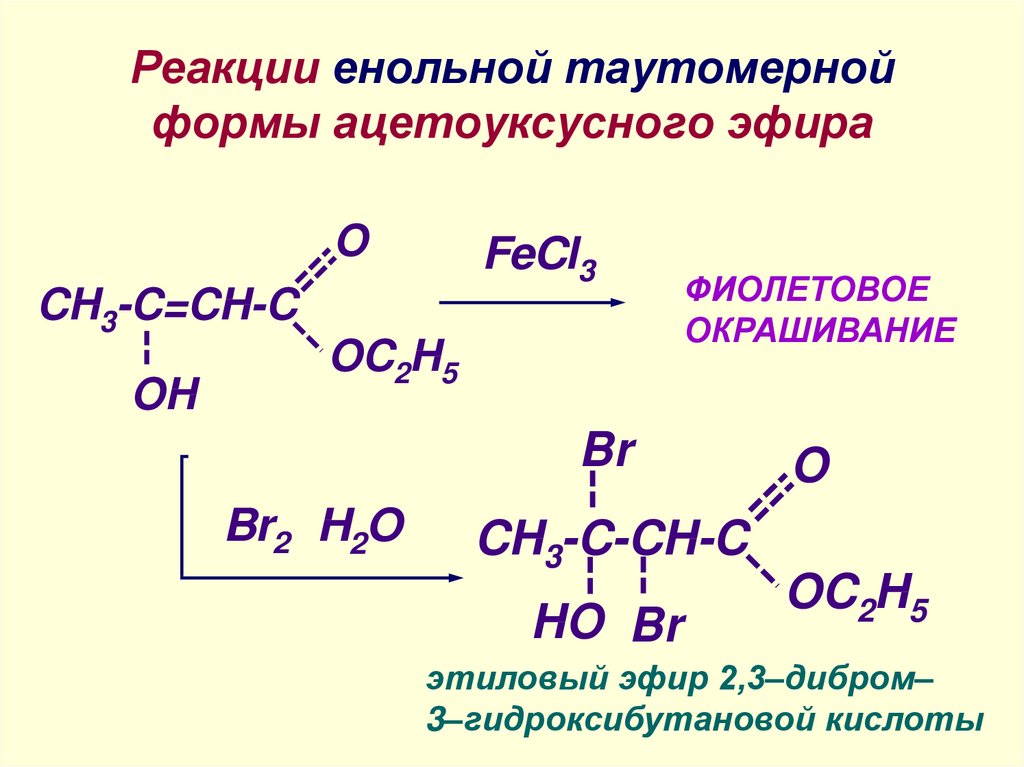
28. Реакции енольной таутомерной формы ацетоуксусного эфира
OFeCl3
CH3-C=CH-C
OH
OC2H5
ФИОЛЕТОВОЕ
ОКРАШИВАНИЕ
Br
Br2 H2O
CH3-C-CH-C
HO Br
O
OC2H5
этиловый эфир 2,3–дибром–
3–гидроксибутановой кислоты
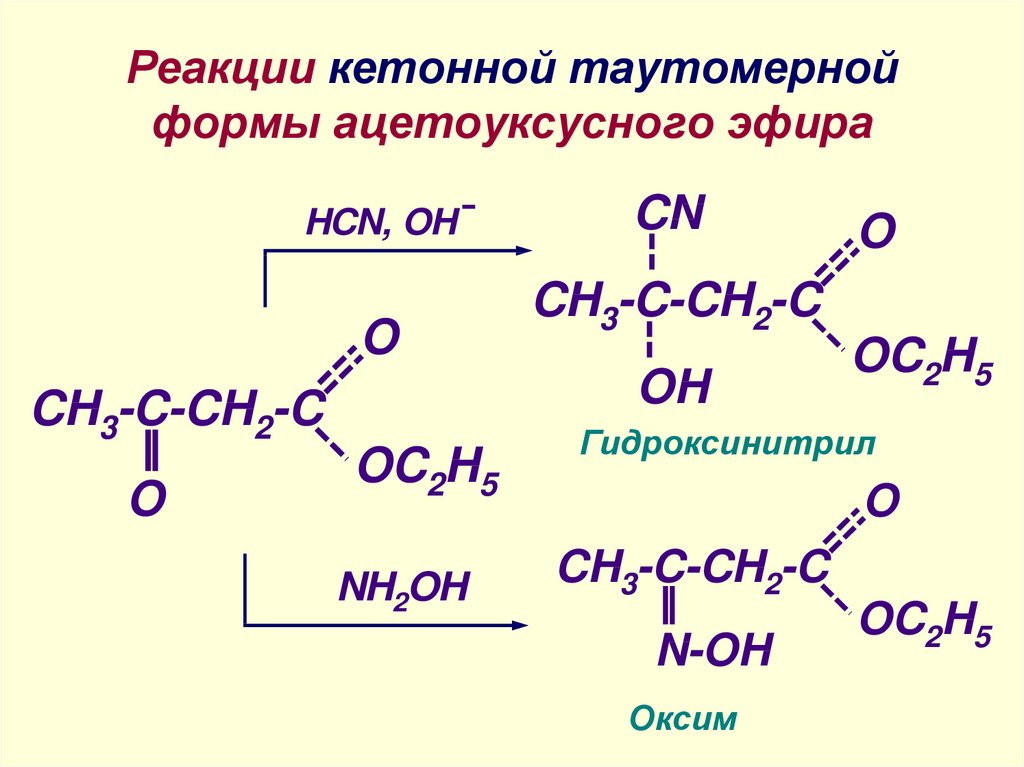
29. Реакции кетонной таутомерной формы ацетоуксусного эфира
HCN, OHO
OC2H5
NH2OH
O
CH3-C-CH2-C
OH
CH3-C-CH2-C
O
CN
OC2H5
Гидроксинитрил
O
CH3-C-CH2-C
N-OH
Оксим
OC2H5
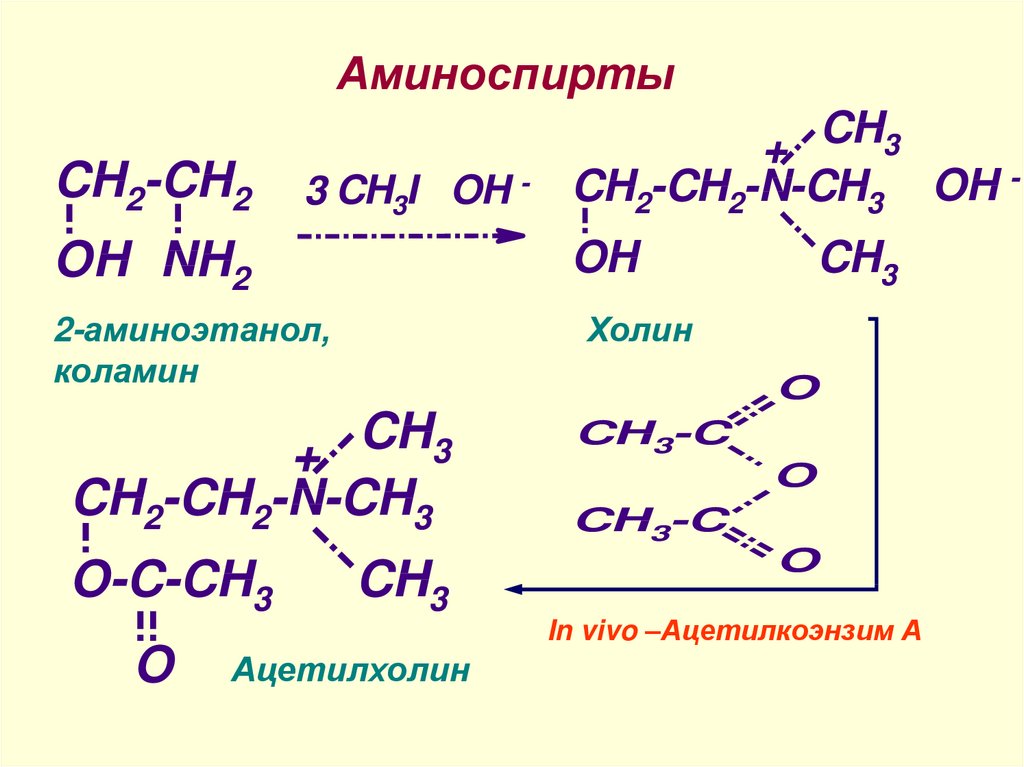
30. Аминоспирты
CH2-CH23 CH3I OH -
OH
OH NH2
O
CH
3
+
CH2-CH2-N-CH3
O
CH3
Холин
2-аминоэтанол,
коламин
O-C-CH3
+ CH3
CH2-CH2-N-CH3 OH -
CH3
Ацетилхолин
CH3-C
O
CH3-C
O
In vivo –Ацетилкоэнзим А
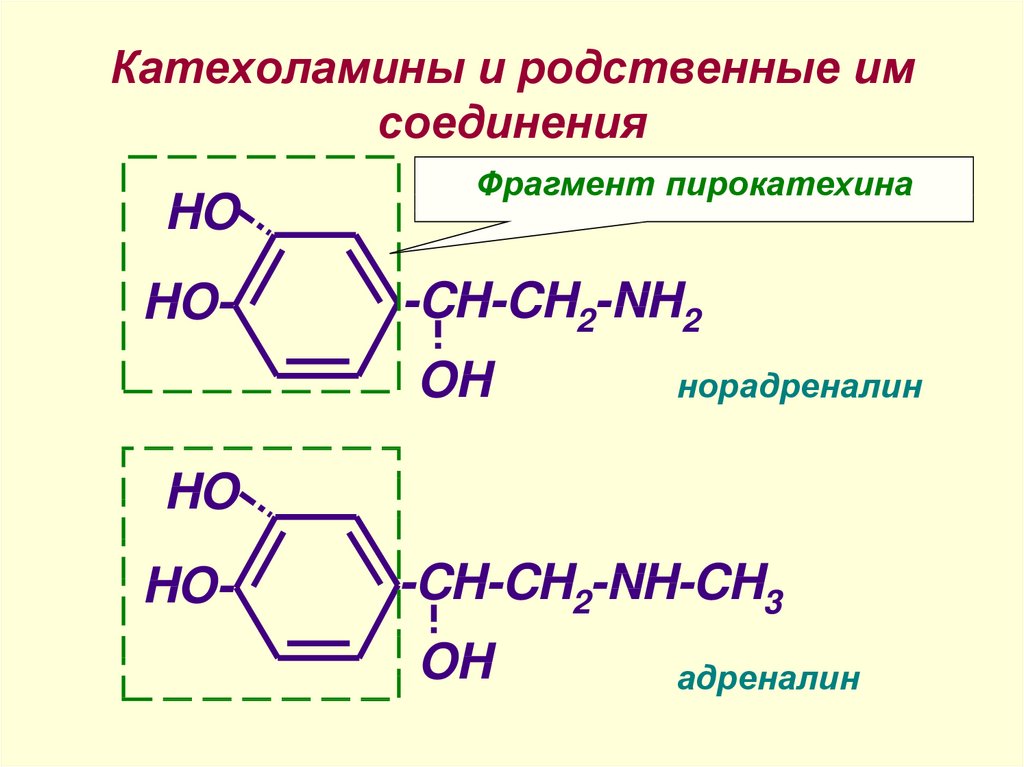
31. Катехоламины и родственные им соединения
HOHO-
Фрагмент пирокатехина
-CH-CH2-NH2
OH
норадреналин
HO
HO-
-CH-CH2-NH-CH3
OH
адреналин
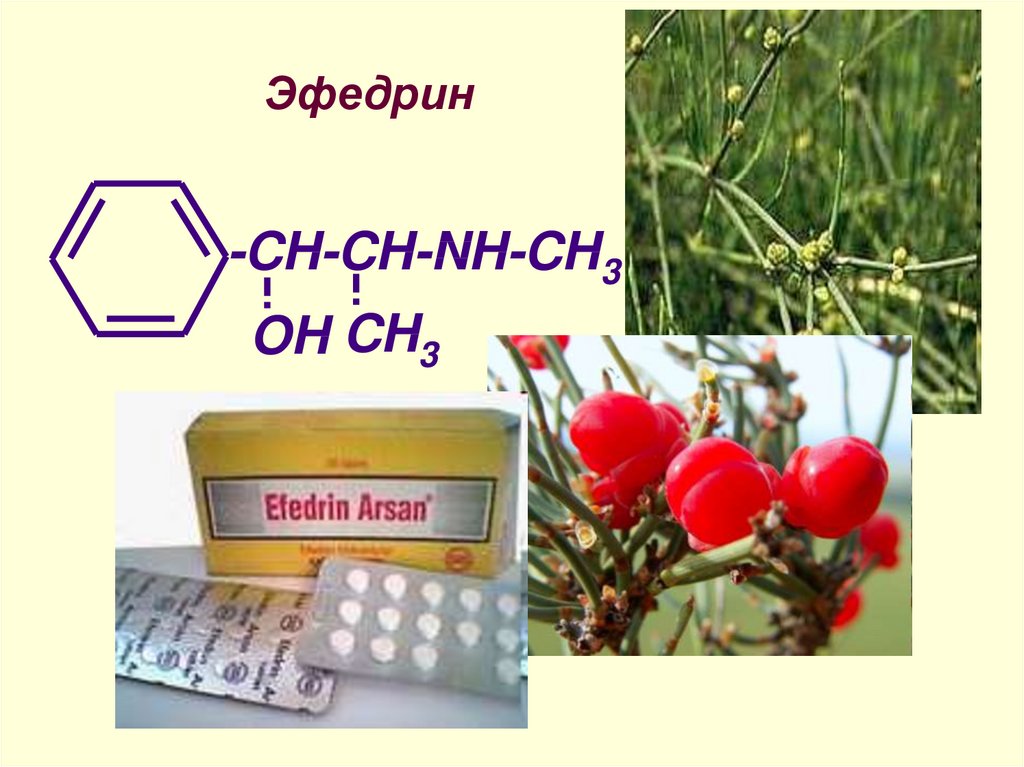
32.
Эфедрин-CH-CH-NH-CH3
OH CH3
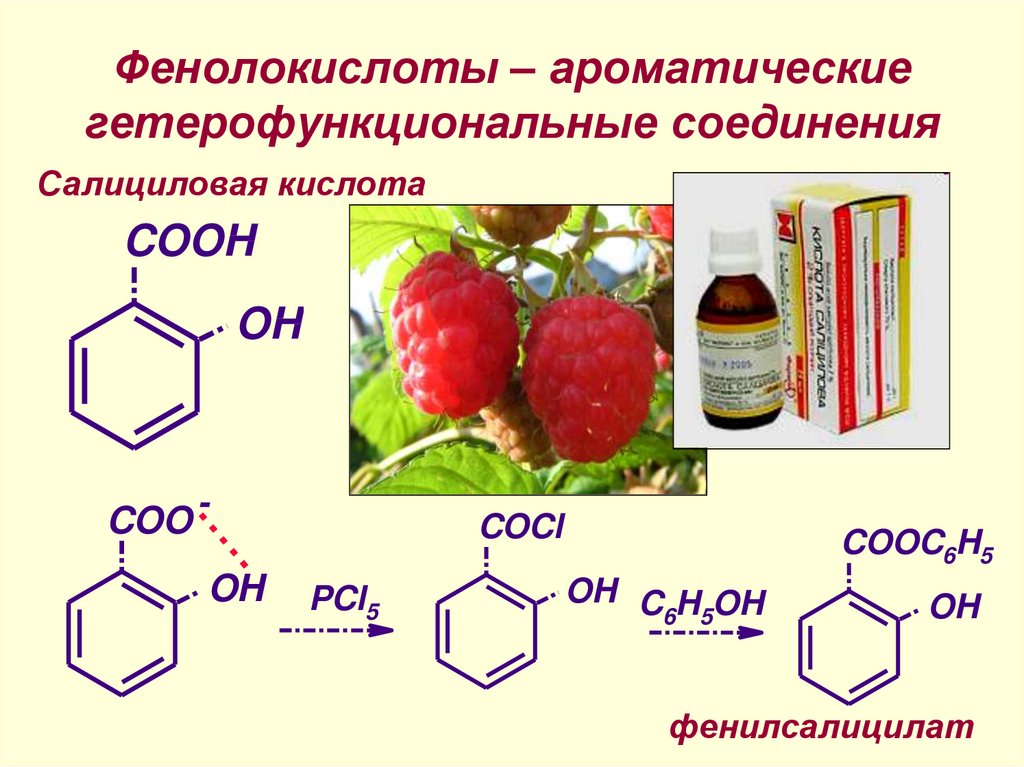
33. Фенолокислоты – ароматические гетерофункциональные соединения
Салициловая кислотаCOOH
OH
COO OH
COCl
PCl5
COOC6H5
OH C H OH
6 5
OH
фенилсалицилат
34.
COOHOH
+ (CH3CO)2O
COOH
O-C-CH3
+ CH3COOH
O
Ацетилсалициловая кислота
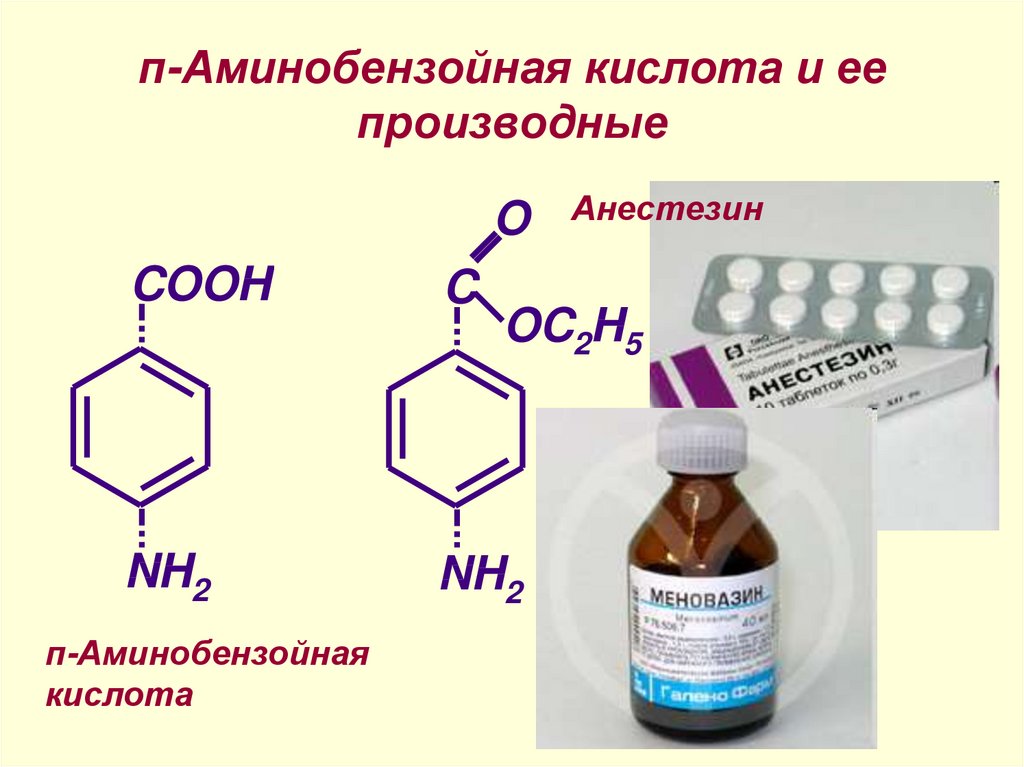
35. п-Аминобензойная кислота и ее производные
OCOOH
C
NH2
NH2
п-Аминобензойная
кислота
Анестезин
OC2H5
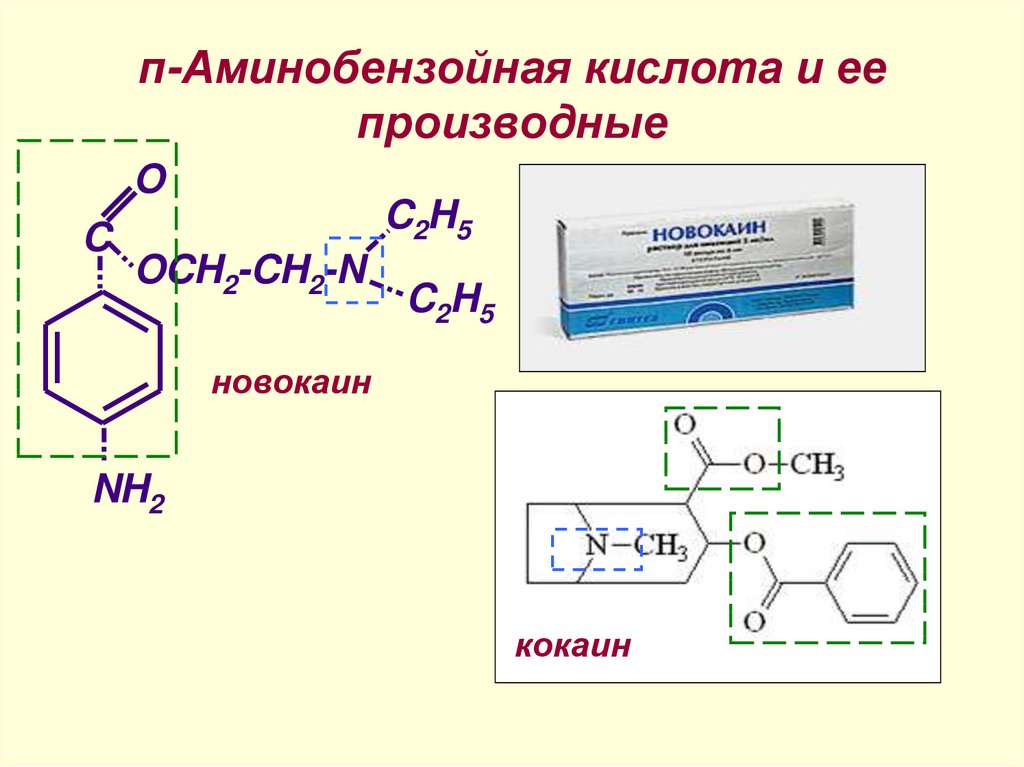
36. п-Аминобензойная кислота и ее производные
OC
C2H5
OCH2-CH2-N
C2H5
новокаин
NH2
кокаин







 chemistry
chemistry








