Similar presentations:
Иондық және ковалентті байланысы бар қосылыстардың электролиттік диссоциациясы
1. Қайталау сұрақтары 1. Ерітінді дегеніміз не? Ерітіндінің қандай түрлері бар? 2. Ерігіштік дегеніміз не? Еру? 3. Диссоциация
деген не?4.Электролиттер деген не?
5.Бейэлектролиттер деген не?
6.Катион және анион деген не?
2. 8. Концентрация дегеніміз не? 9. Масалық үлесті қалай анықтаймыз? 10. Неге су мен бензин араласпайды?
3.
Диссоциация деген не?Электролиттер деген не?
Бейэлектролиттер деген не?
Катион және анион деген не?
Диссоциациялану теориясын негізін
қалаушы кім?
4. Мына теңдеулерді аяқтаңдар:
Na2CO3 + HCIK3PO4 + H2SO4
Au+H2SO4
NaOH + HCI
Fe(OH)3 + HNO3
Mg + H2SO4
Жүретін химиялық реакция теңдеулерін жазыңдар
5. Сабақтың тақырыбы:
Лабораториялық жұмыс №2«Иондық және ковалентті
байланысы бар қосылыстардың
электролиттік диссоциациясы».
6. Сабақтың мақсаты
9.3.4.7 H+(сулы)және OH-(сулы) иондарынтүзуге бейім заттардың иондалуын білу;
9.3.4.8 сулы ерітіндіде H+(сулы) ионының
болуын қышқылдық деп түсіну;
9.3.4.9 сулы ерітіндіде ОH-(сулы) ионының
болуы сілтілік деп түсіну;
9.3.4.13 ерітінді ортасын анықтау және
тұздар гидролизінің реакция теңдеуін
құрастыру;
7. Бағалау критерийлері:
-өз әрекеті мен нәтижелер кестесіндегі бақылаулардыайқындайды;
-қышқылдық және негіздік ортаны сипаттайтын иондарды
анықтайды;
-күшті және әлсіз негіздер мен қышқылдарды анықтайды;
- молярлық концентрация мен еріген заттың массалық
үлесін есептей алу;
- ерітіндідегі жүретін реакция теңдеуін иондық түрде
өрнектей алады.
8.
НегіздерҚышқылдар
9.
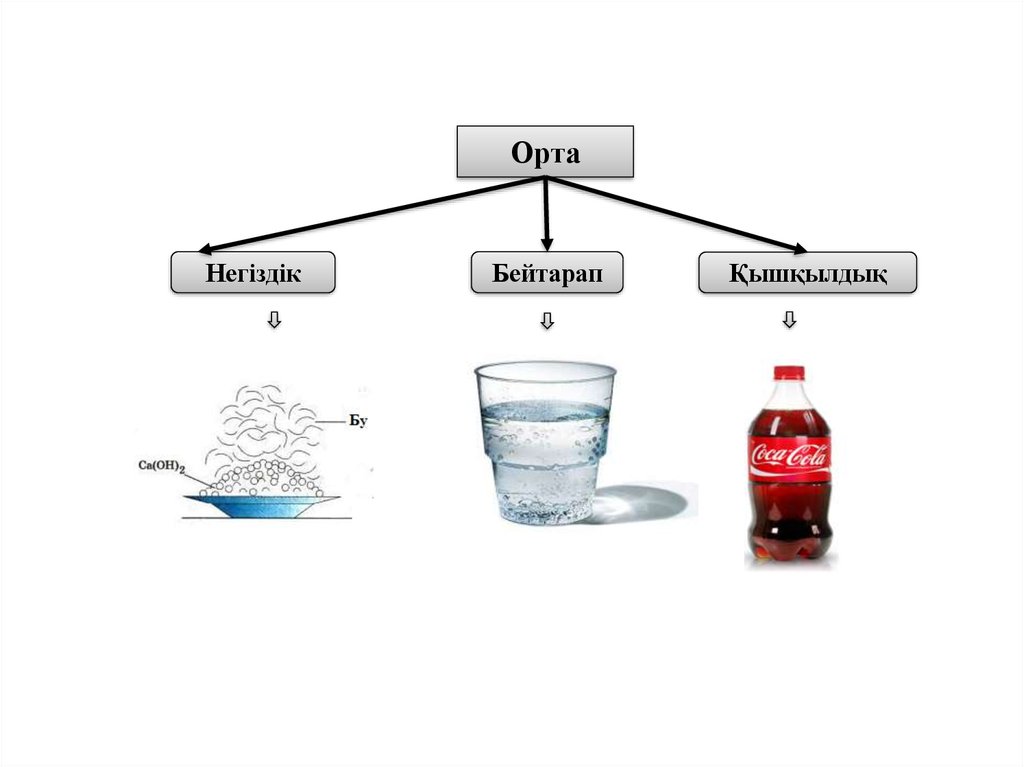
ОртаНегіздік
Бейтарап
Қышқылдық
10.
Индикатор11.
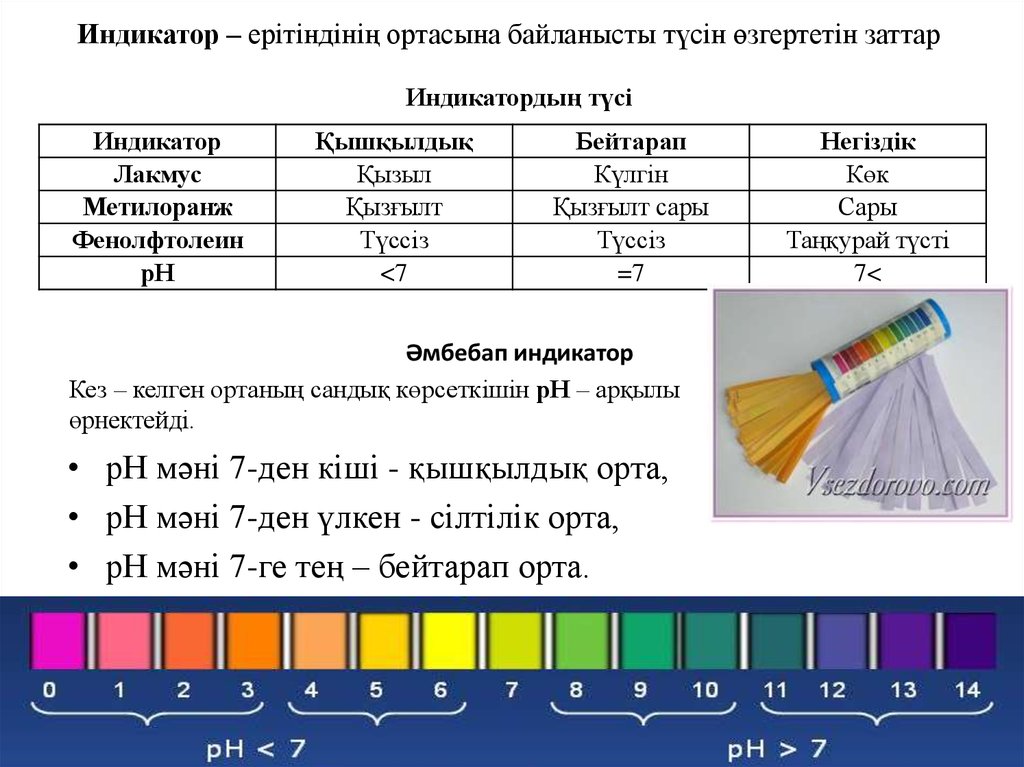
Индикатор – ерітіндінің ортасына байланысты түсін өзгертетін заттарИндикатордың түсі
Индикатор
Лакмус
Метилоранж
Фенолфтолеин
рН
Қышқылдық
Қызыл
Қызғылт
Түссіз
<7
Бейтарап
Күлгін
Қызғылт сары
Түссіз
=7
Әмбебап индикатор
Кез – келген ортаның сандық көрсеткішін рН – арқылы
өрнектейді.
• рН мәні 7-ден кіші - қышқылдық орта,
• рН мәні 7-ден үлкен - сілтілік орта,
• рН мәні 7-ге тең – бейтарап орта.
Негіздік
Көк
Сары
Таңқурай түсті
7<
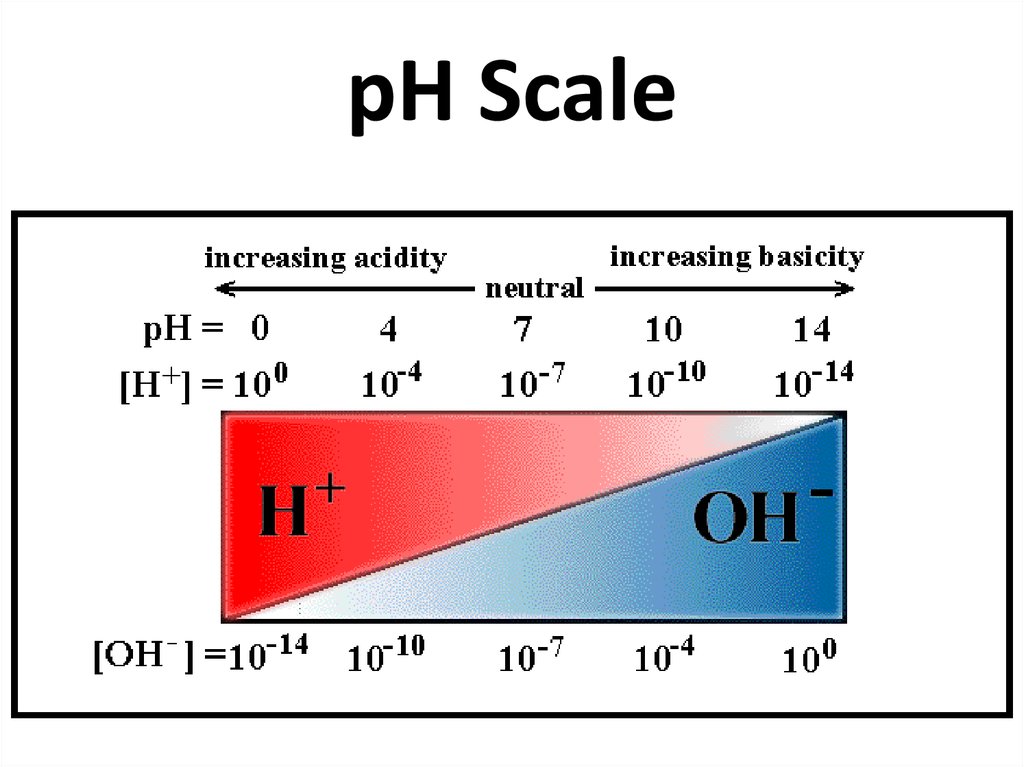
12. pH Scale
13.
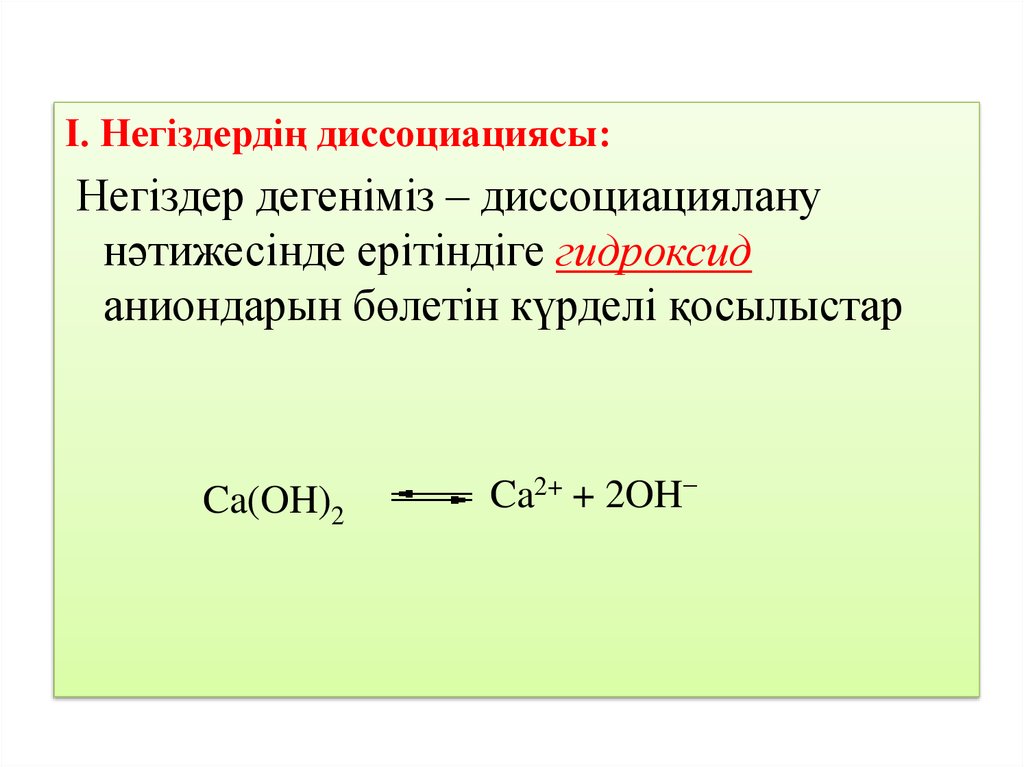
І. Негіздердің диссоциациясы:Негіздер дегеніміз – диссоциациялану
нәтижесінде ерітіндіге гидроксид
аниондарын бөлетін күрделі қосылыстар
Ca(OH)2
Ca2+ + 2OH−
14.
• ІІ. Қышқылдардың диссоциациялануыҚышқылдар дегеніміз – диссоциациялану
нәтижесінде ерітіндіге сутек катиондарын
бөлетін күрделі заттар
H2SO4
2H+ + SO42−
15.
• ІІІ. Тұздардың диссоциациялануТұздар дегеніміз – диссоциациялану
нәтижесінде ерітіндіге металл катиондары
мен қышқыл қалдығының аниондарын
бөлетін күрделі заттар
CuSO4 = Cu2+ + SO42−
BaCl2 = Ba2+ + 2Cl−
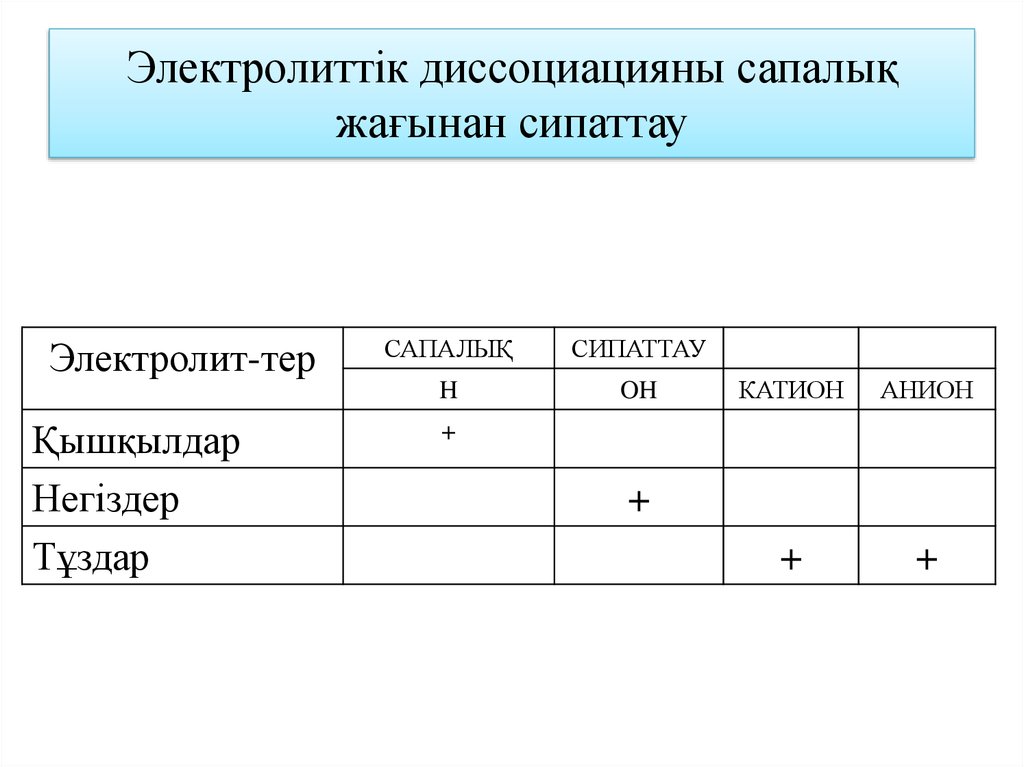
16. Электролиттік диссоциацияны сапалық жағынан сипаттау
Электролит-терҚышқылдар
Негіздер
Тұздар
САПАЛЫҚ
СИПАТТАУ
H
OH
КАТИОН
АНИОН
+
+
+
+
17. ТАПСЫРМА
• МЫНА ҚОСЫЛЫСТАРДЫҢДИССОЦИАЦИЯЛАНУЫ ТЕҢДЕУЛЕРІН
ЖАЗЫҢДАР:
• Na2CO3,
HCL
• Fe( OH)2
HNO3
• AlCl3,
H2CO3
• Na3PO4,
H2SO4
• AlCL3,
H3PO4
• FeSO4
H3PO3
18. (f) (I) Қалыптастырушы бағалауға арналған тапсырмалар
Оқу мақсаты:• ерітіндідегі жүретін реакция теңдеуін
иондық түрде жаза білу.













 chemistry
chemistry








