Similar presentations:
Конденсированные гетероциклические соединения
1. КОНДЕНСИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
Мы учим и лечимс 1888 года
КОНДЕНСИРОВАННЫЕ
ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
Чешкова Т.В.
Доцент кафедры химии,
к.х.н
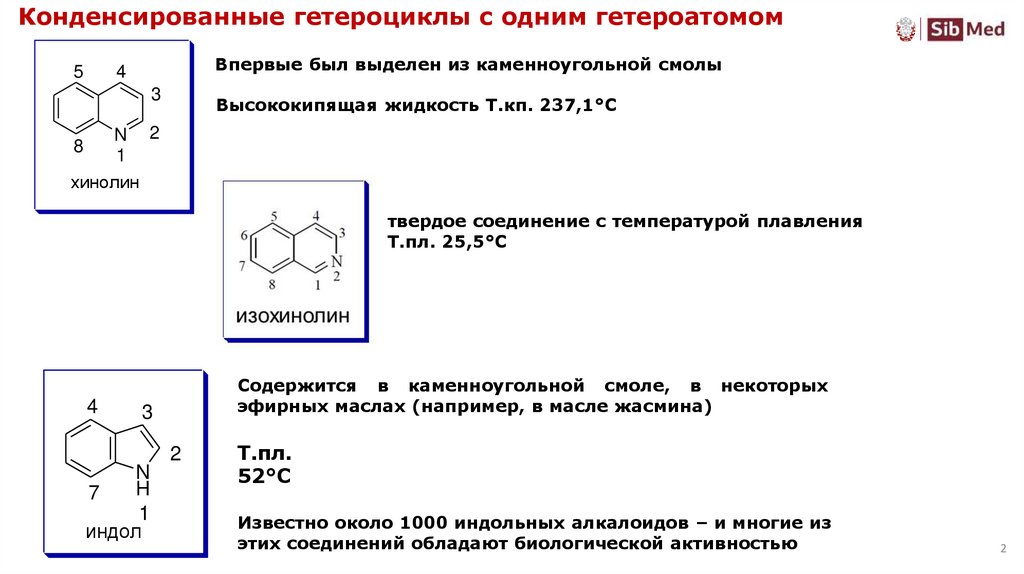
2. Конденсированные гетероциклы c одним гетероатомом
5Впервые был выделен из каменноугольной смолы
4
3
Высококипящая жидкость Т.кп. 237,1°С
N 2
8
1
хинолин
твердое соединение с температурой плавления
Т.пл. 25,5°С
4
Содержится в каменноугольной смоле, в некоторых
эфирных маслах (например, в масле жасмина)
3
N
H
7
1
индол
2
Т.пл.
52°С
Известно около 1000 индольных алкалоидов – и многие из
этих соединений обладают биологической активностью
2
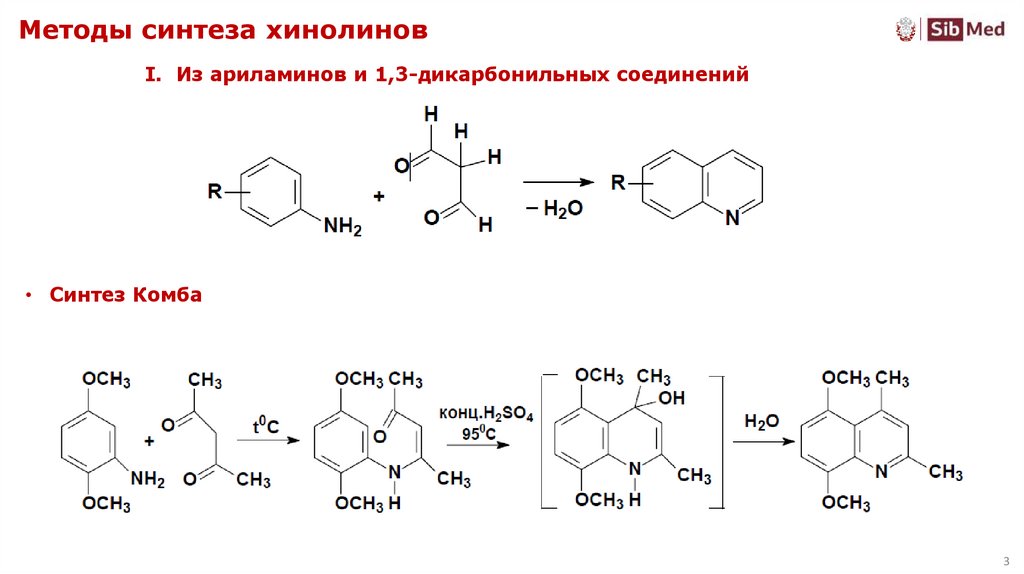
3. Методы синтеза хинолинов
I. Из ариламинов и 1,3-дикарбонильных соединений• Синтез Комба
3
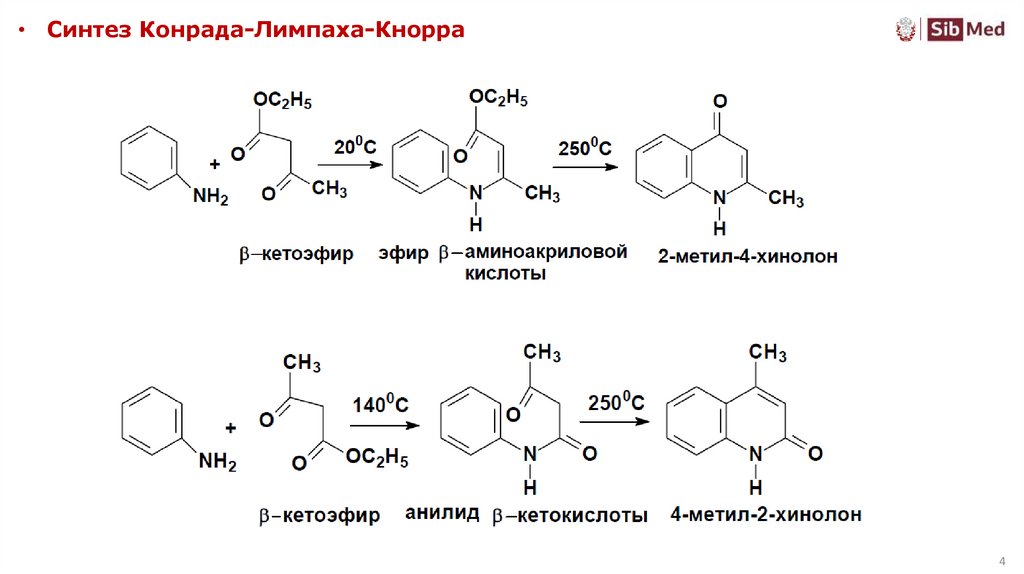
4. Синтез Конрада-Лимпаха-Кнорра
• Синтез Конрада-Лимпаха-Кнорра4
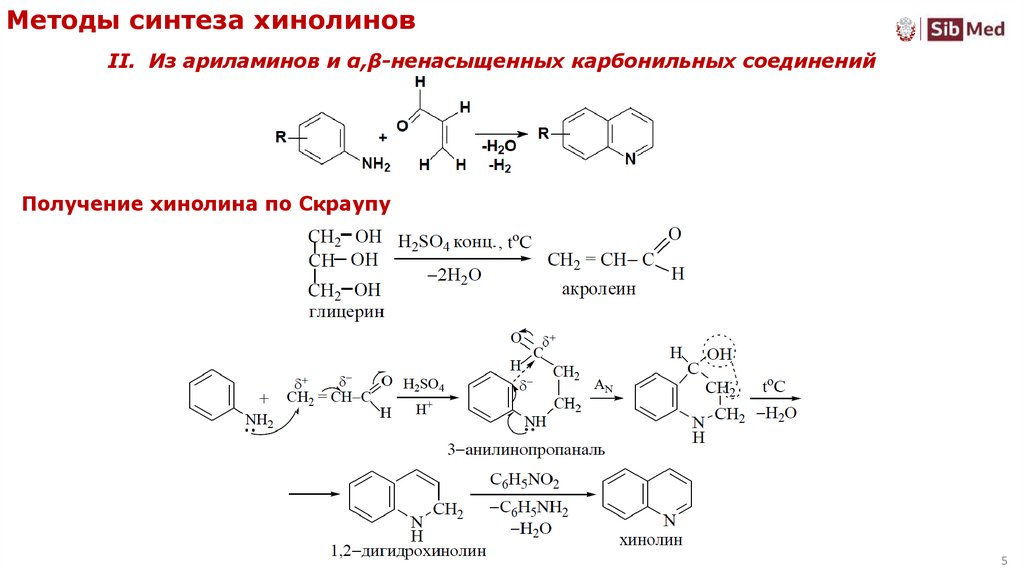
5. Получение хинолина по Скраупу
Методы синтеза хинолиновII. Из ариламинов и α,β-ненасыщенных карбонильных соединений
Получение хинолина по Скраупу
5
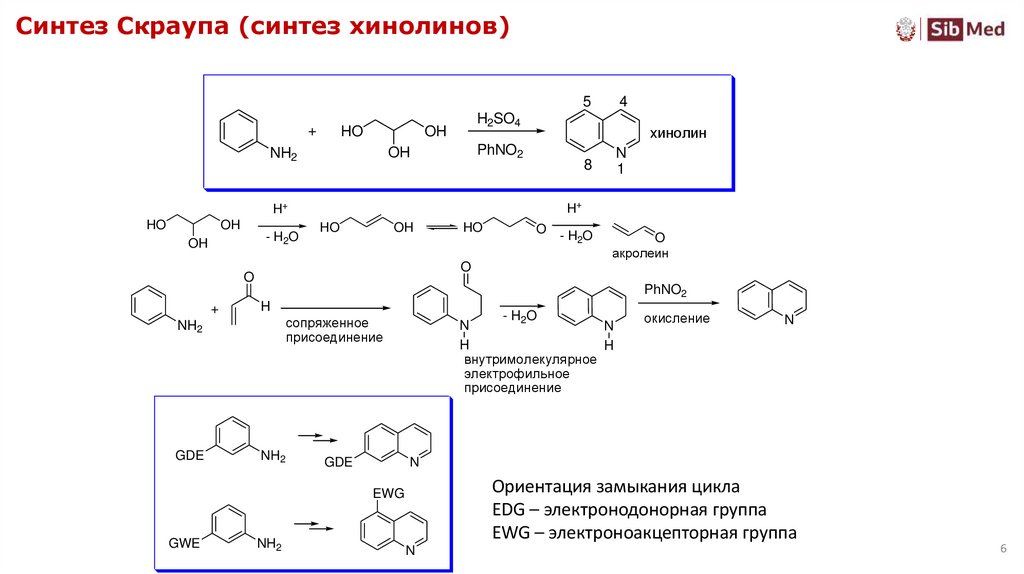
6. Синтез Скраупа (синтез хинолинов)
5+
HO
H2SO4
OH
хинолин
PhNO2
OH
NH2
OH
- H2O
OH
H+
HO
OH
H
- H2O
O
акролеин
- H2O
N
N
H
H
внутримолекулярное
электрофильное
присоединение
сопряженное
присоединение
NH2
GDE
NH2
окисление
N
N
Ориентация замыкания цикла
EDG – электронодонорная группа
EWG – электроноакцепторная группа
EWG
GWE
O
PhNO2
NH2
GDE
HO
O
O
+
N
1
8
H+
HO
4
N
6
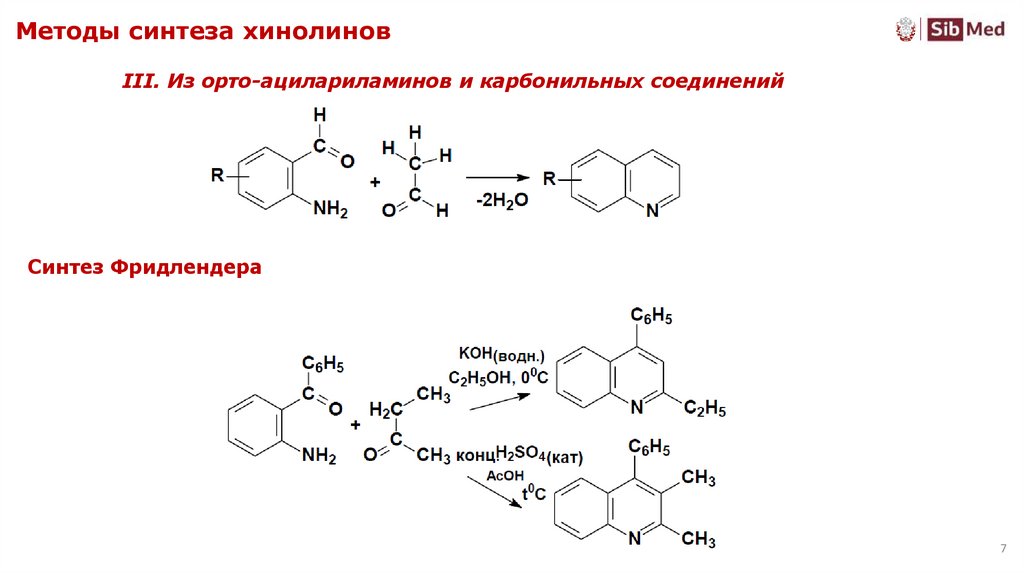
7. Методы синтеза хинолинов
III. Из орто-ацилариламинов и карбонильных соединенийСинтез Фридлендера
7
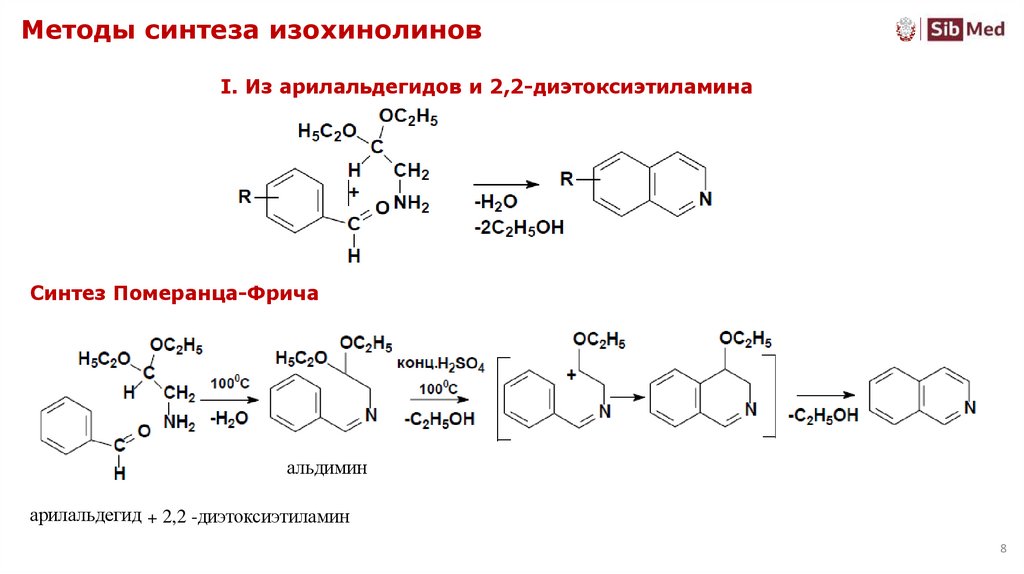
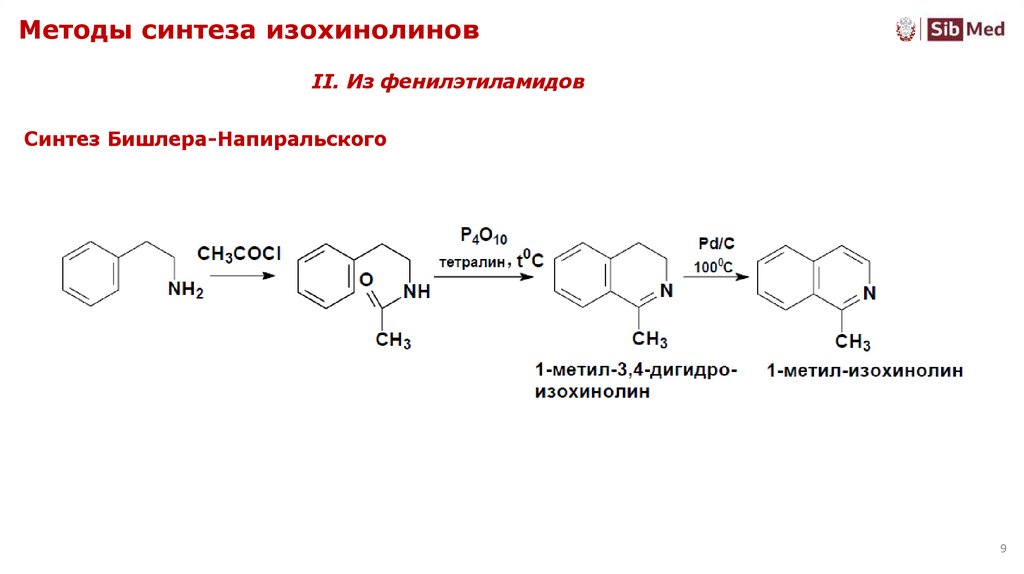
8. Методы синтеза изохинолинов
I. Из арилальдегидов и 2,2-диэтоксиэтиламинаСинтез Померанца-Фрича
альдимин
арилальдегид + 2,2 -диэтоксиэтиламин
8
9. Методы синтеза изохинолинов
II. Из фенилэтиламидовСинтез Бишлера-Напиральского
9
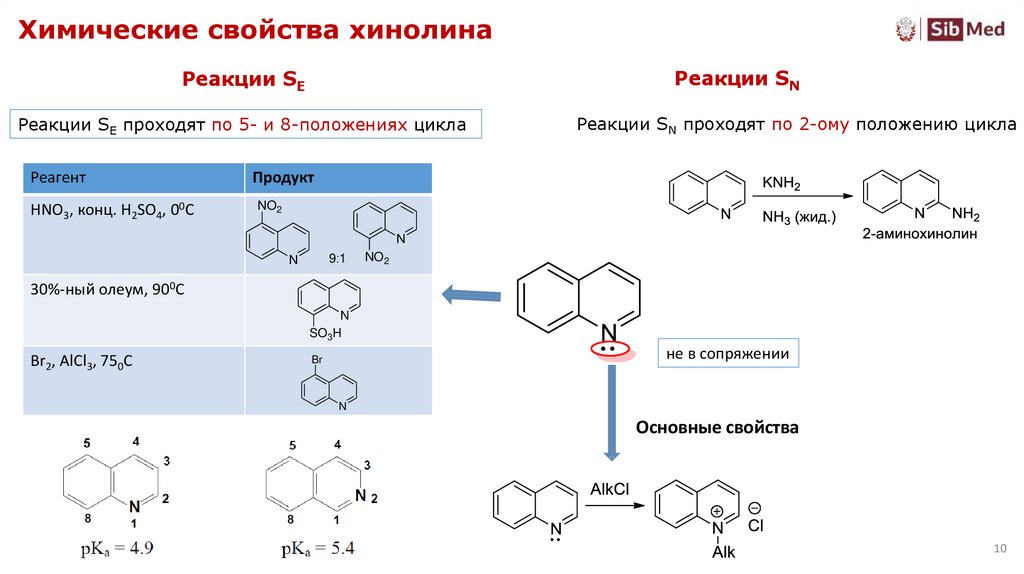
10. Химические свойства хинолина
Реакции SNРеакции SE
Реакции SE проходят по 5- и 8-положениях цикла
Реагент
Продукт
HNO3, конц. H2SO4, 00С
NO2
Реакции SN проходят по 2-ому положению цикла
N
9:1
N
NO2
30%-ный олеум, 900С
N
SO3H
Br2, AlCl3, 750C
не в сопряжении
Br
N
Основные свойства
10
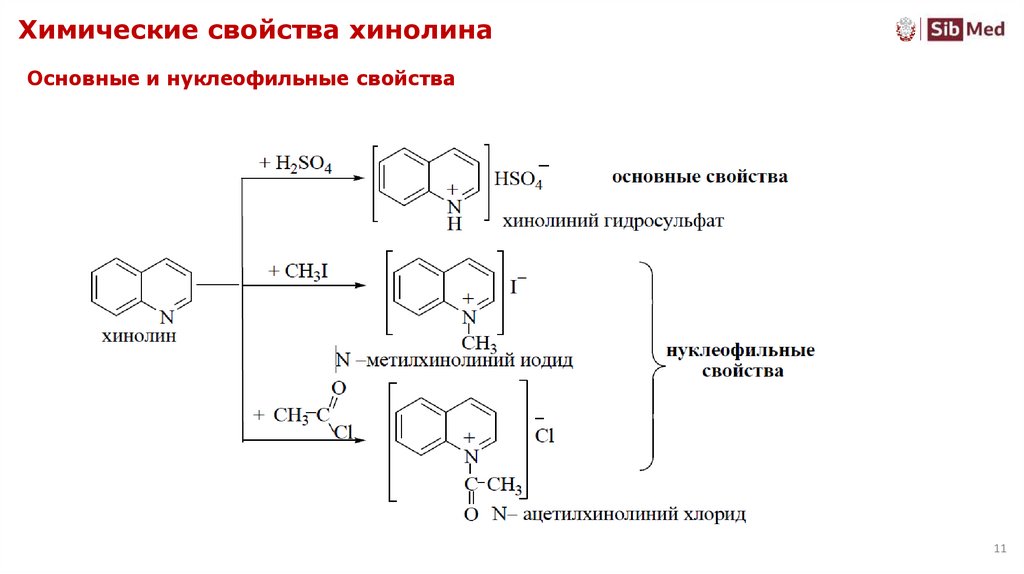
11. Химические свойства хинолина
Основные и нуклеофильные свойства11
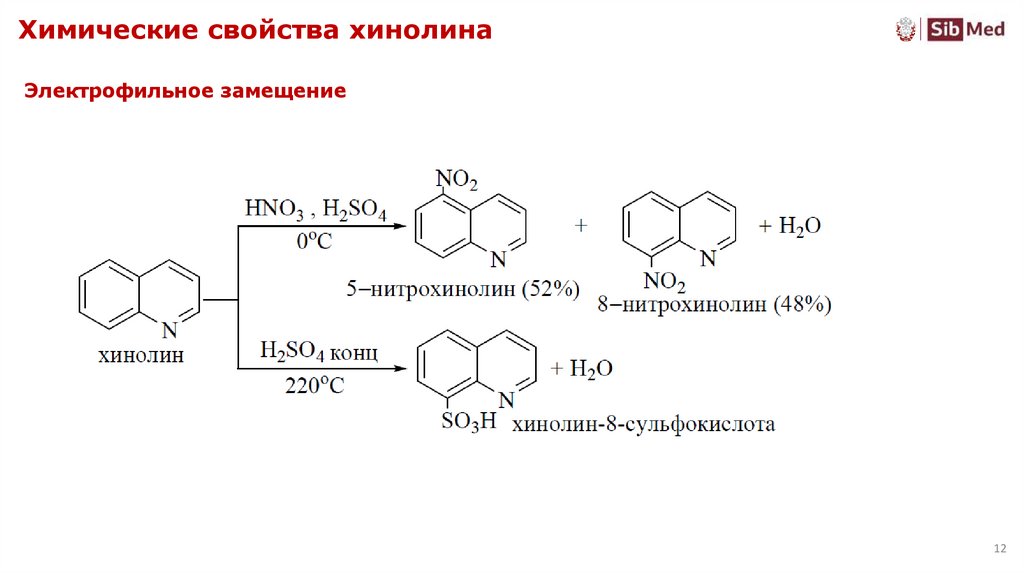
12. Химические свойства хинолина
Электрофильное замещение12
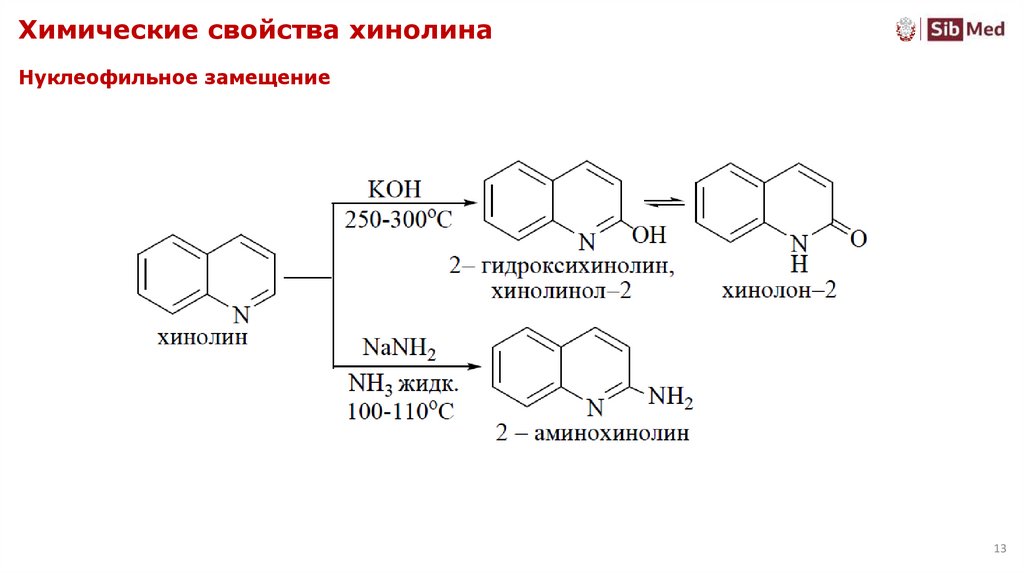
13. Химические свойства хинолина
Нуклеофильное замещение13
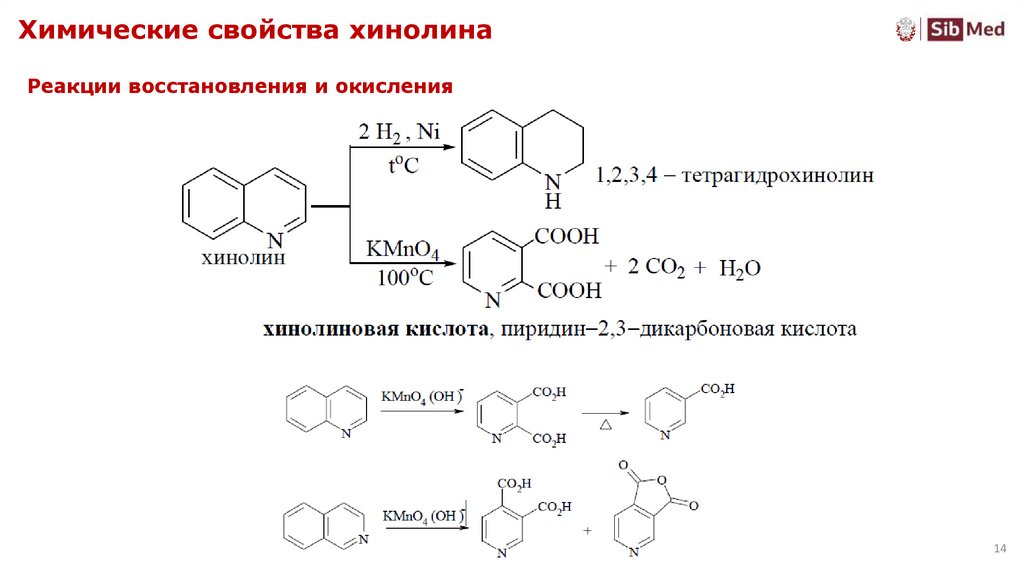
14. Химические свойства хинолина
Реакции восстановления и окисления14
15. Производные хинолина
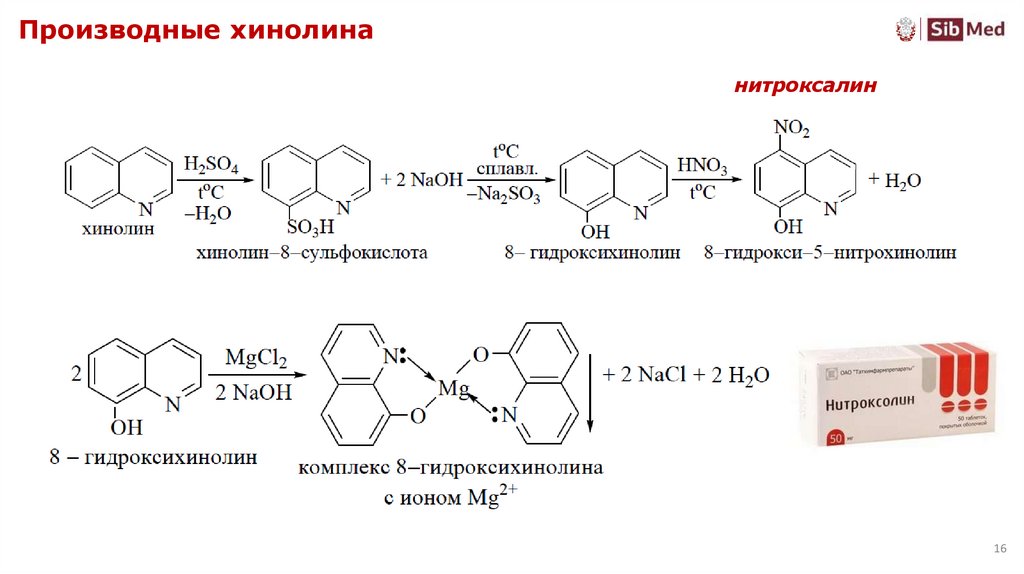
1516. Производные хинолина
нитроксалин16
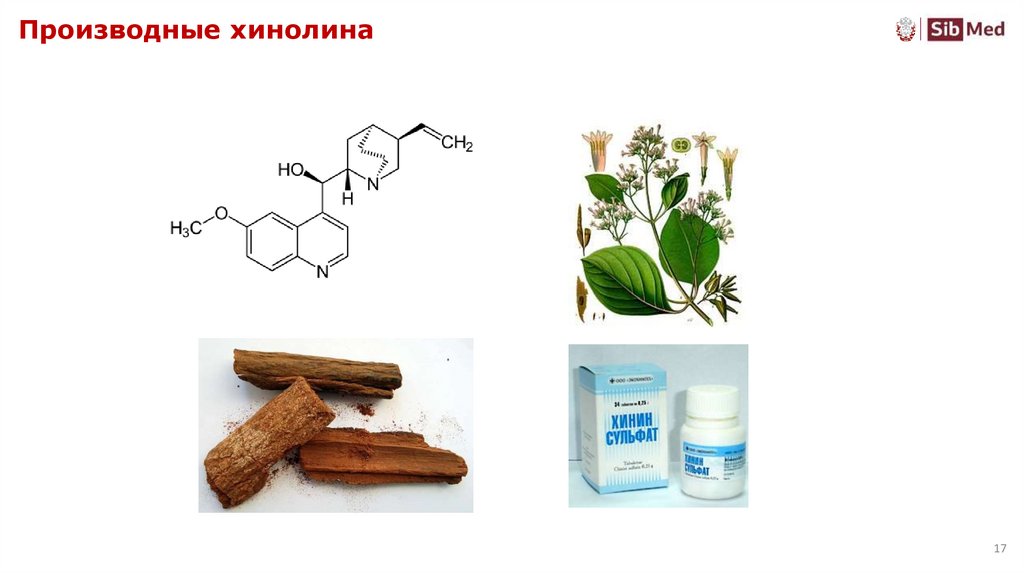
17. Производные хинолина
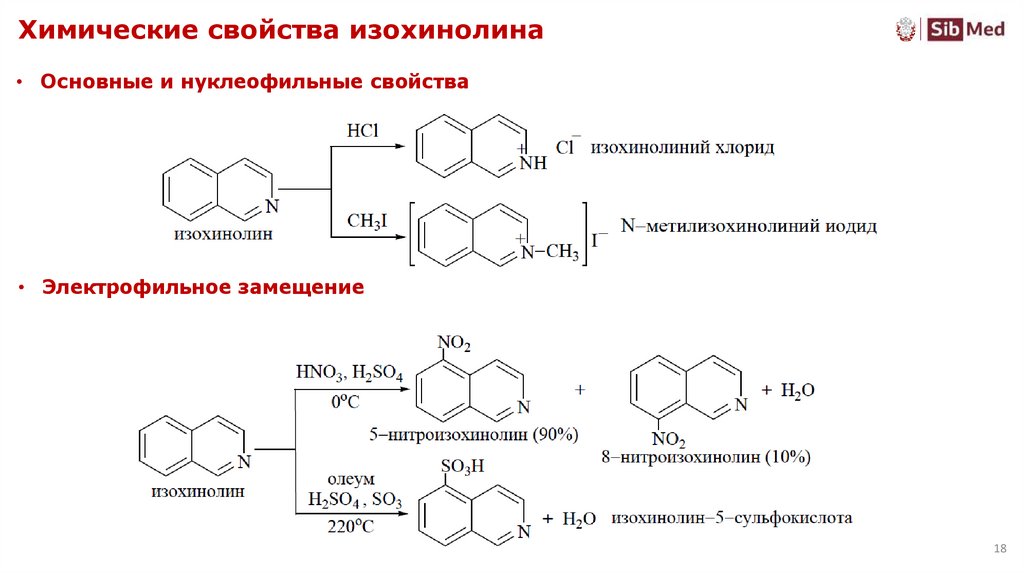
1718. Химические свойства изохинолина
• Основные и нуклеофильные свойства• Электрофильное замещение
18
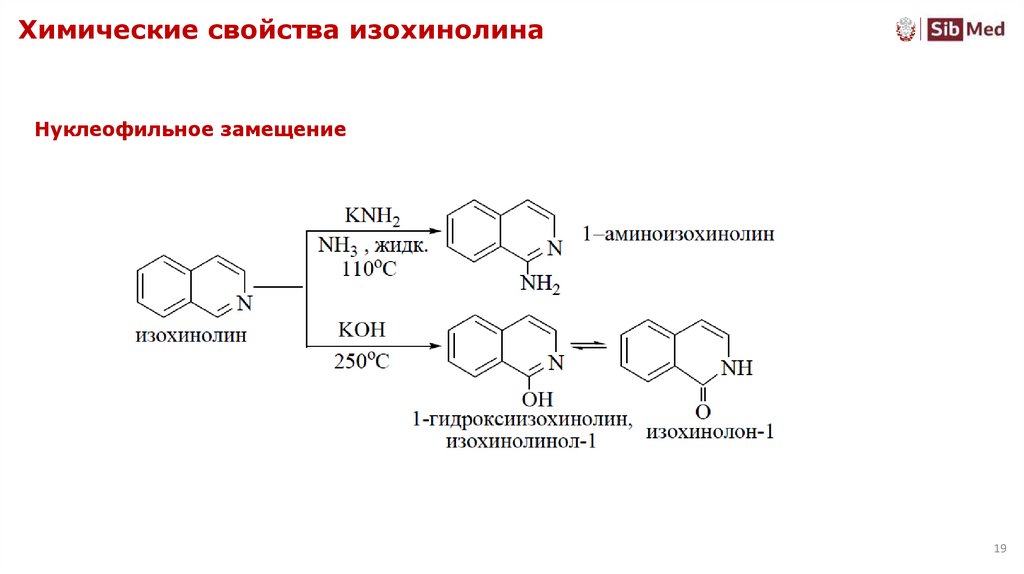
19. Химические свойства изохинолина
Нуклеофильное замещение19
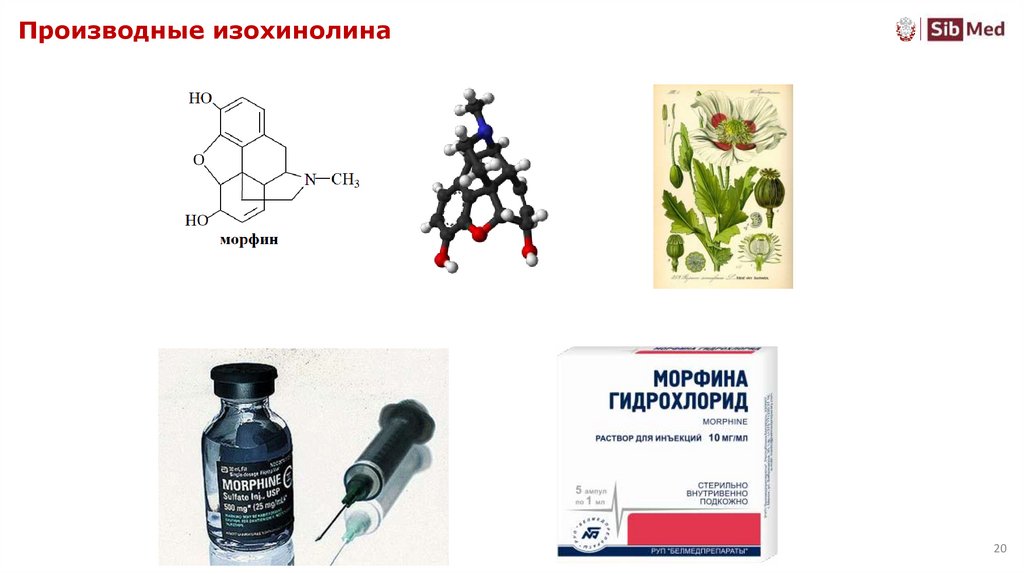
20. Производные изохинолина
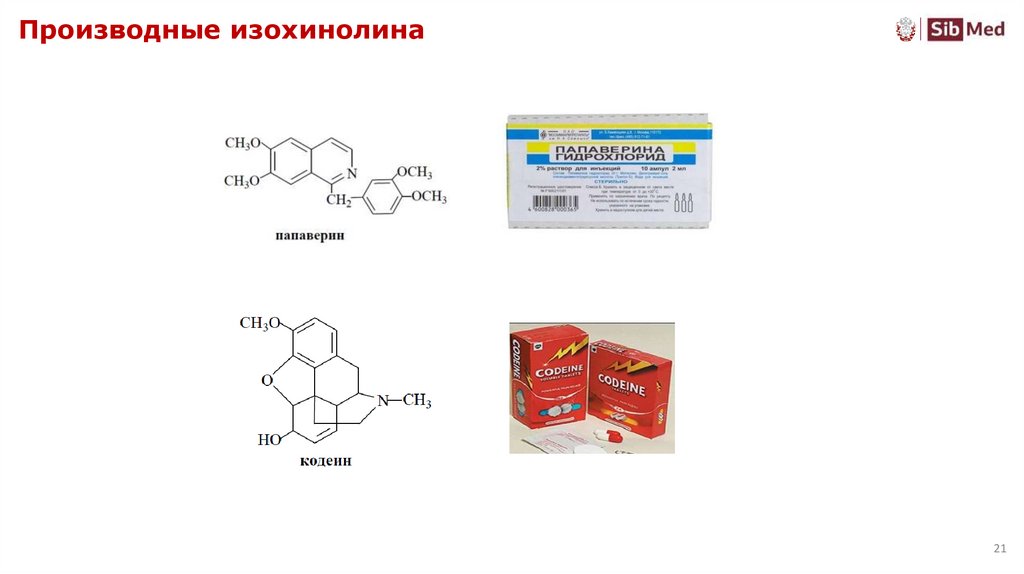
2021. Производные изохинолина
2122. Индол
43
N
H
7
1
индол
2
22
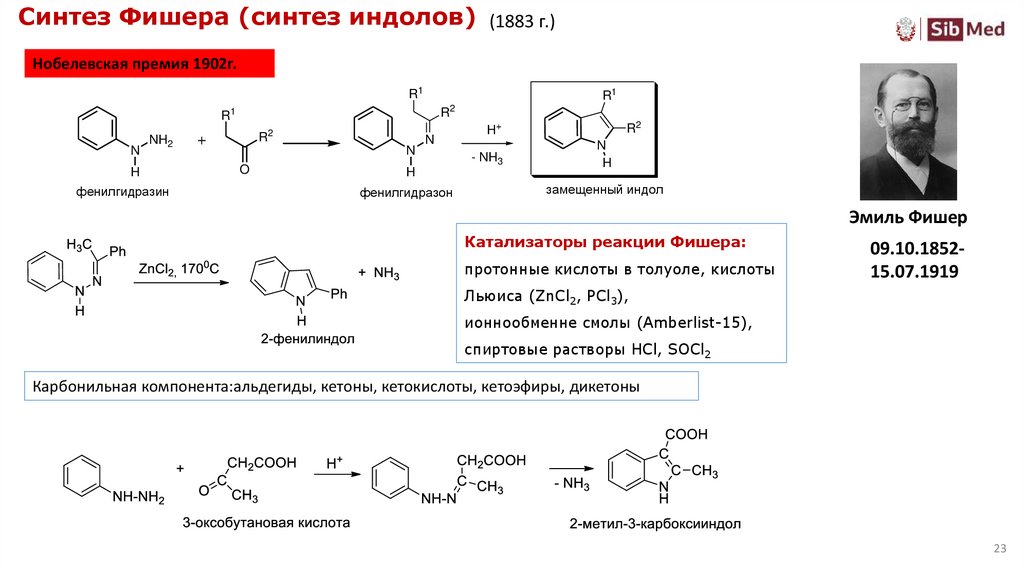
23. Синтез Фишера (синтез индолов)
(1883 г.)Нобелевская премия 1902г.
R1
R1
R2
R1
N
NH2
H
фенилгидразин
R2
+
N
O
N
H
фенилгидразон
R2
H+
- NH3
N
H
замещенный индол
Эмиль Фишер
Катализаторы реакции Фишера:
протонные кислоты в толуоле, кислоты
09.10.185215.07.1919
Льюиса (ZnCl2, PCl3),
ионнообменне смолы (Amberlist-15),
спиртовые растворы HCl, SOCl2
Карбонильная компонента:альдегиды, кетоны, кетокислоты, кетоэфиры, дикетоны
23
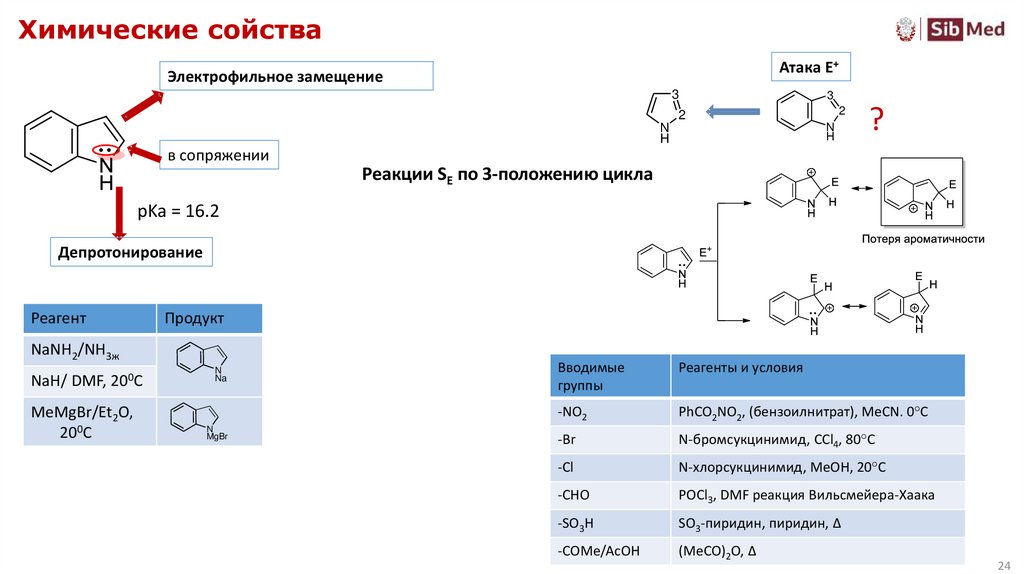
24. Химические сойства
Атака Е+Электрофильное замещение
3
3
2
2
N
H
N
H
?
в сопряжении
Реакции SE по 3-положению цикла
pKа = 16.2
Депротонирование
Реагент
Продукт
NaNH2/NH3ж
NaH/ DMF, 200C
MeMgBr/Et2O,
200C
N
Na
N
MgBr
Вводимые
группы
Реагенты и условия
-NO2
PhCO2NO2, (бензоилнитрат), MeCN. 0°C
-Br
N-бромсукцинимид, CCl4, 80°C
-Cl
N-хлорсукцинимид, MeOH, 20°C
-CHO
POCl3, DMF реакция Вильсмейера-Хаака
-SO3H
SO3-пиридин, пиридин, ∆
-СOMe/AcOH
(MeCO)2O, ∆
24
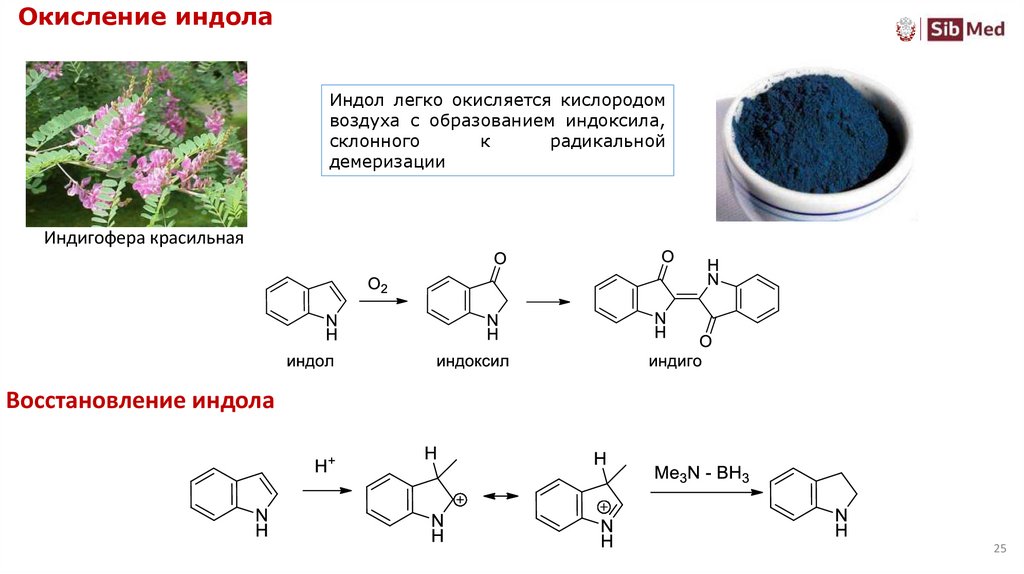
25. Окисление индола
Индол легко окисляется кислородомвоздуха с образованием индоксила,
склонного
к
радикальной
демеризации
Индигофера красильная
Восстановление индола
25
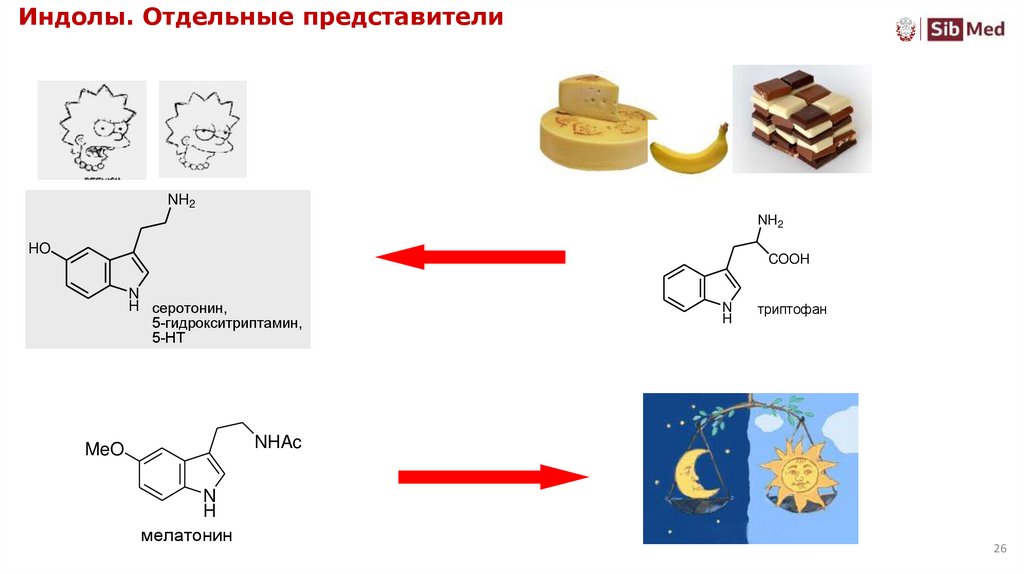
26. Индолы. Отдельные представители
NH2NH2
HO
COOH
N
H серотонин,
5-гидрокситриптамин,
5-НТ
N
H
триптофан
NHAc
MeO
N
H
мелатонин
26
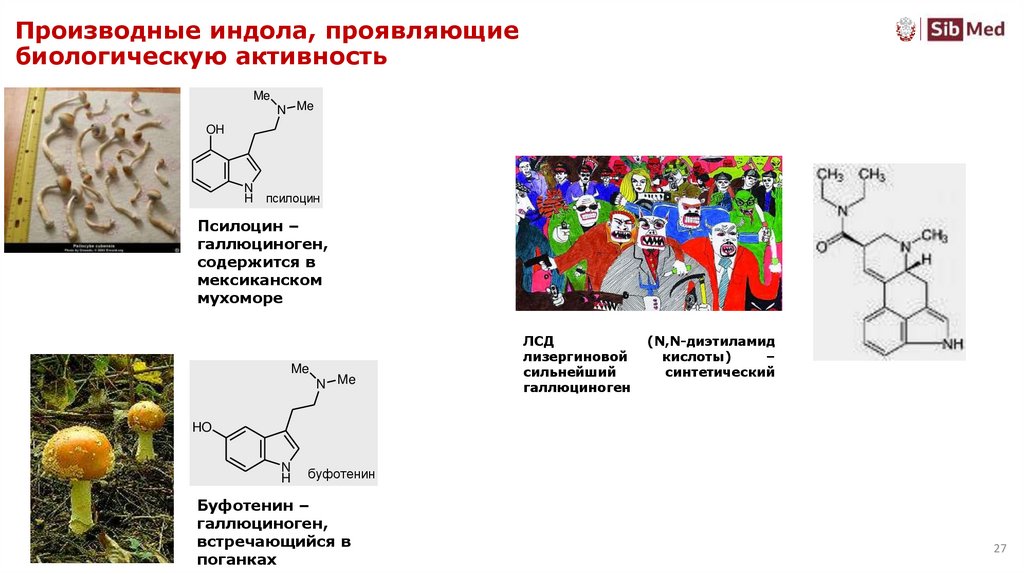
27. Производные индола, проявляющие биологическую активность
MeN Me
OH
N
H
псилоцин
Псилоцин –
галлюциноген,
содержится в
мексиканском
мухоморе
Me
N Me
ЛСД
лизергиновой
сильнейший
галлюциноген
(N,N-диэтиламид
кислоты)
–
синтетический
HO
N
H
буфотенин
Буфотенин –
галлюциноген,
встречающийся в
поганках
27
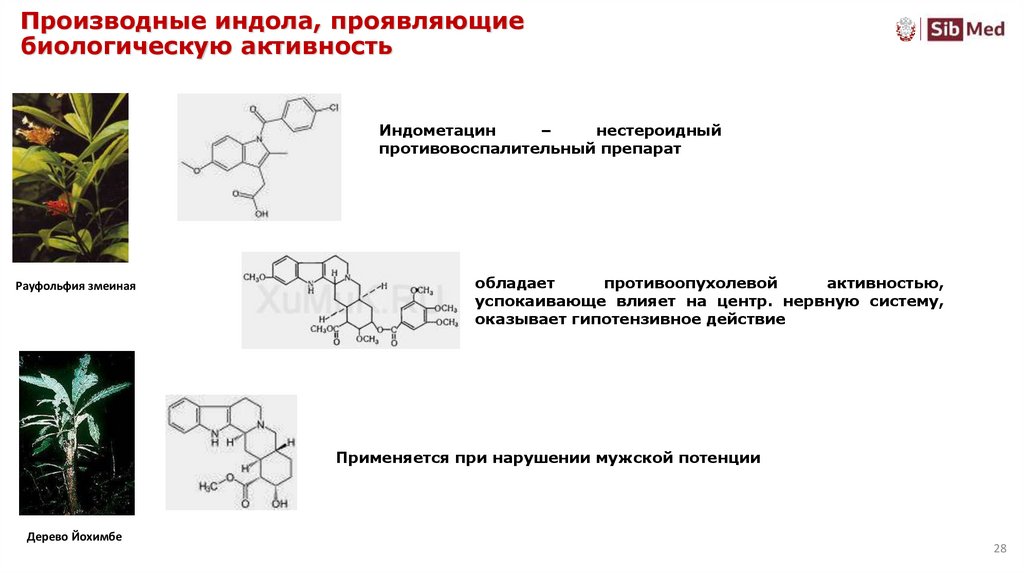
28. Производные индола, проявляющие биологическую активность
Индометацин–
нестероидный
противовоспалительный препарат
Рауфольфия змеиная
обладает
противоопухолевой
активностью,
успокаивающе влияет на центр. нервную систему,
оказывает гипотензивное действие
Применяется при нарушении мужской потенции
Дерево Йохимбе
28
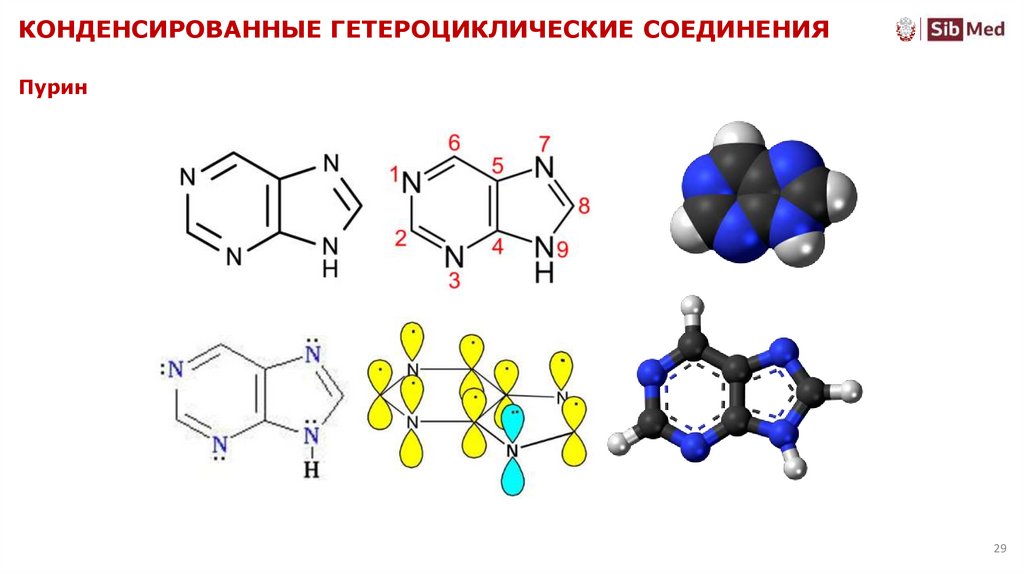
29. КОНДЕНСИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
Пурин29
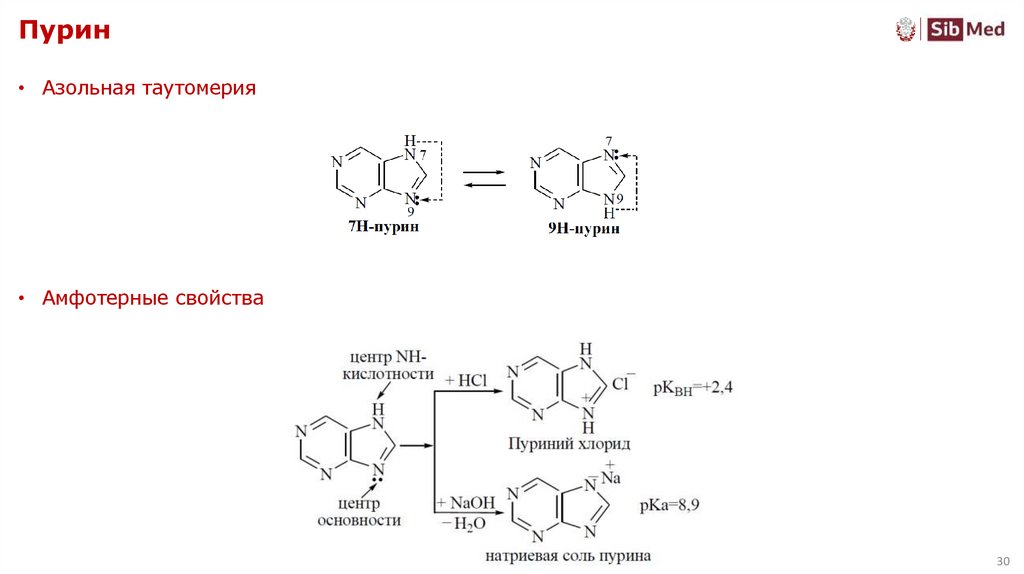
30. Пурин
• Азольная таутомерия• Амфотерные свойства
30
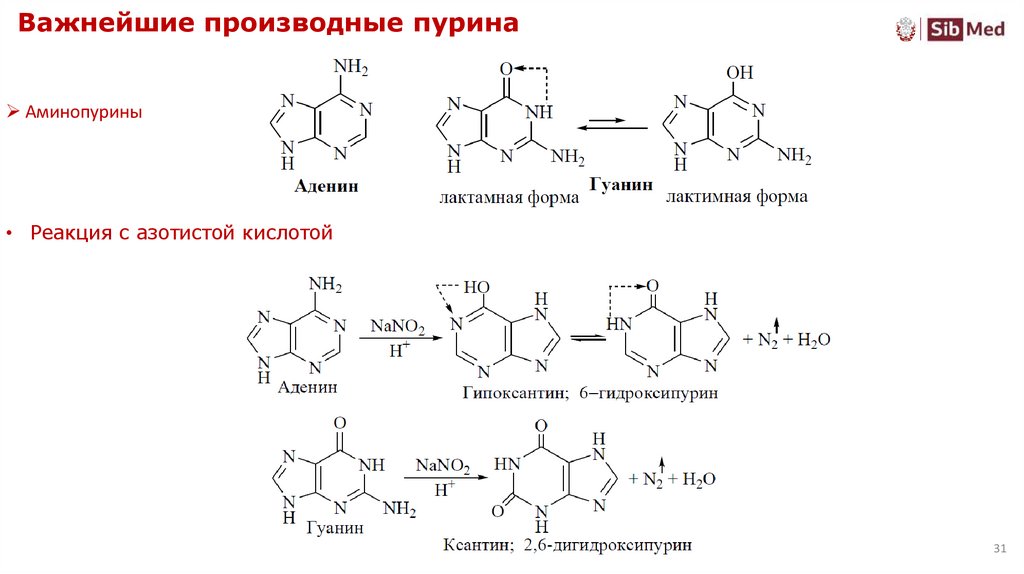
31. Важнейшие производные пурина
Аминопурины• Реакция с азотистой кислотой
31
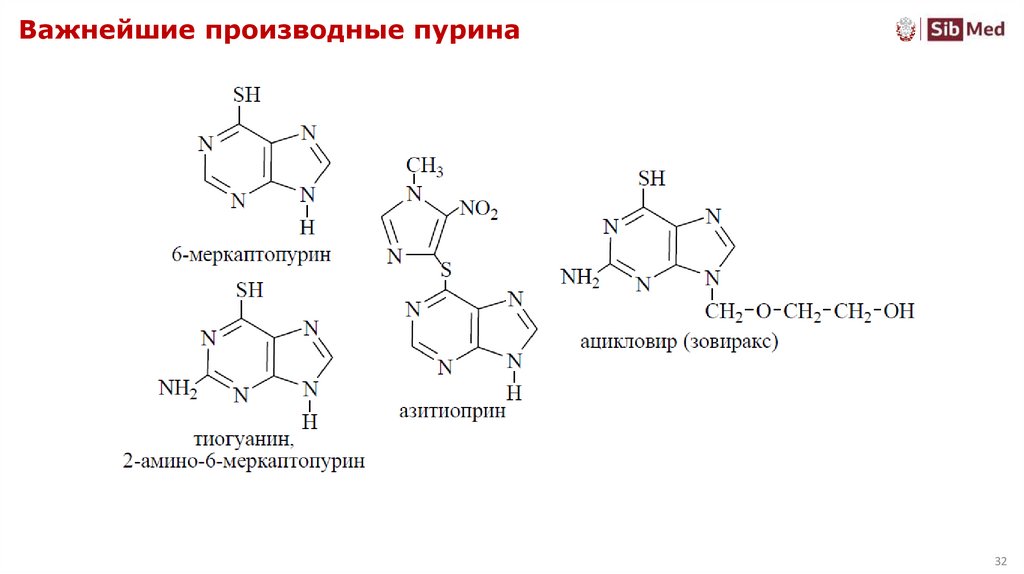
32. Важнейшие производные пурина
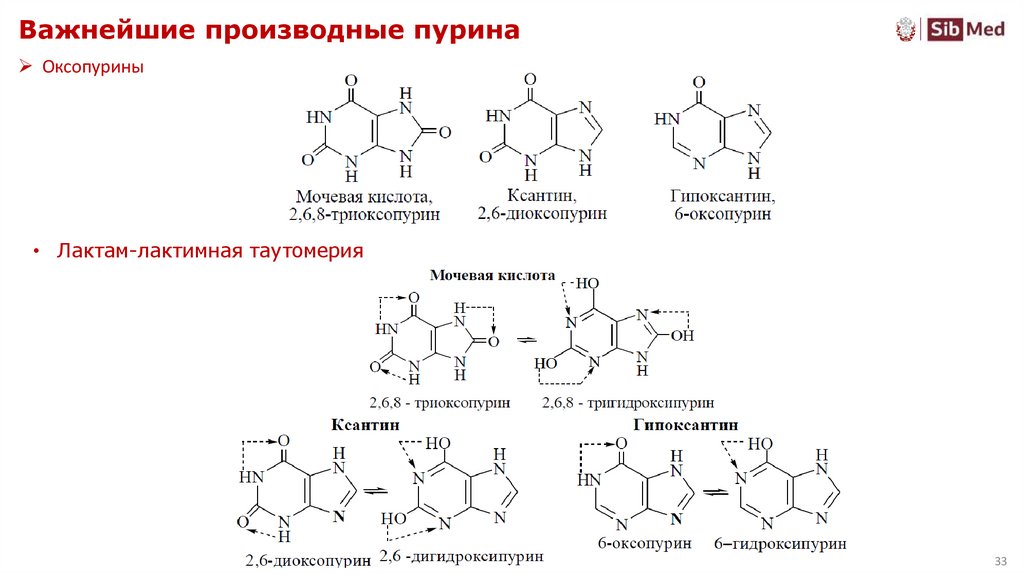
3233. Важнейшие производные пурина
Оксопурины• Лактам-лактимная таутомерия
33
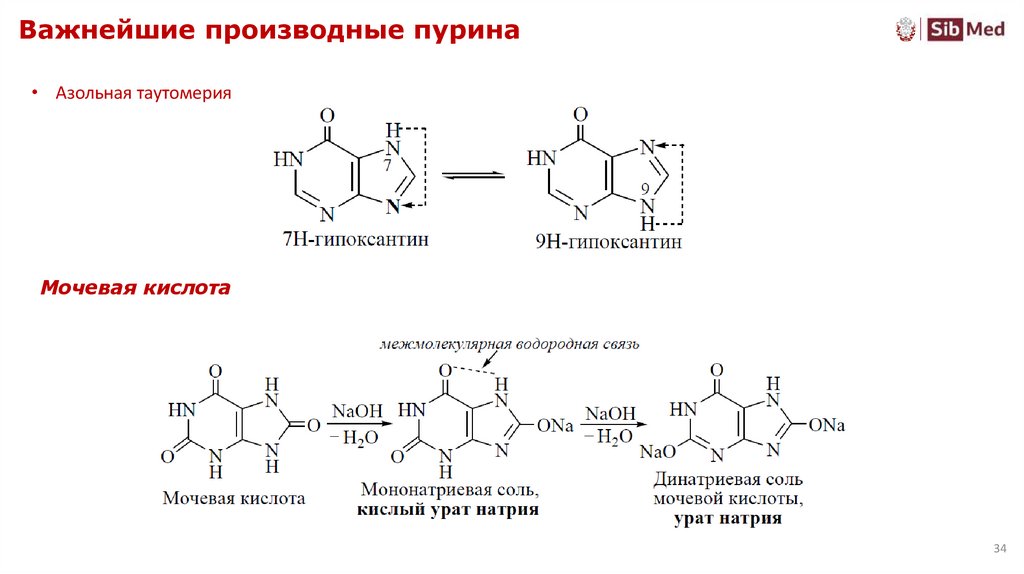
34. Важнейшие производные пурина
• Азольная таутомерияМочевая кислота
34
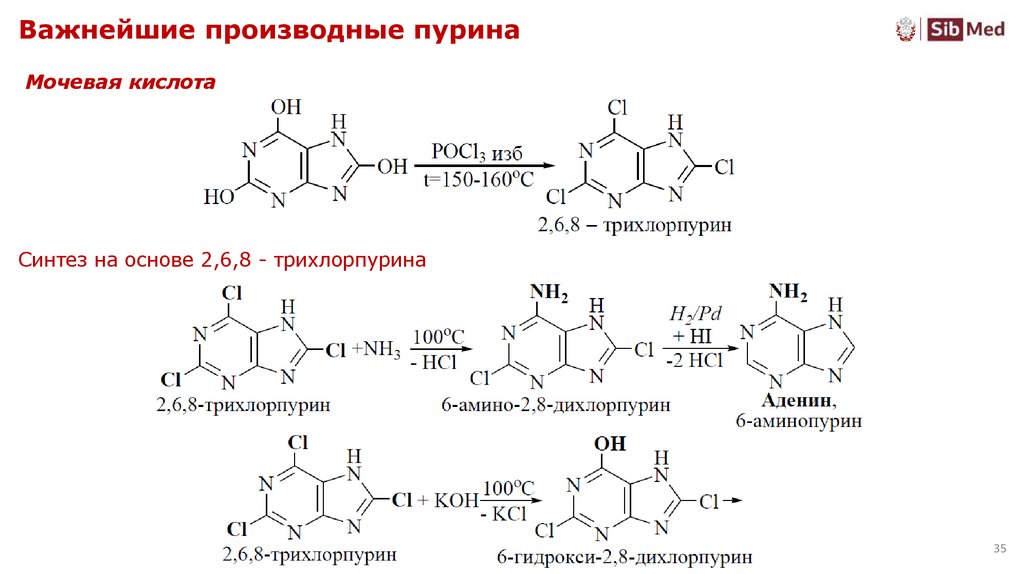
35. Важнейшие производные пурина
Мочевая кислотаСинтез на основе 2,6,8 - трихлорпурина
35
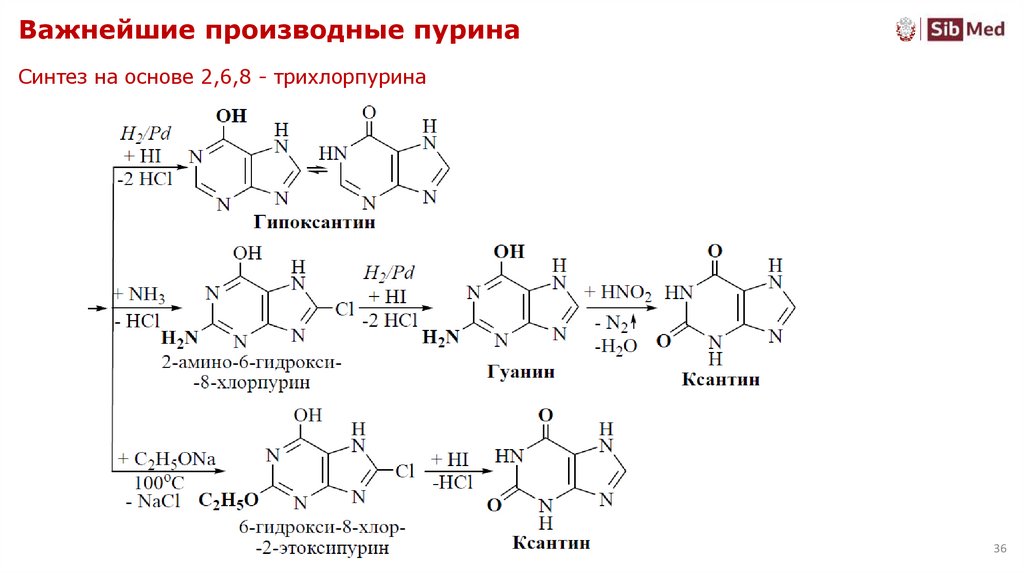
36. Важнейшие производные пурина
Синтез на основе 2,6,8 - трихлорпурина36
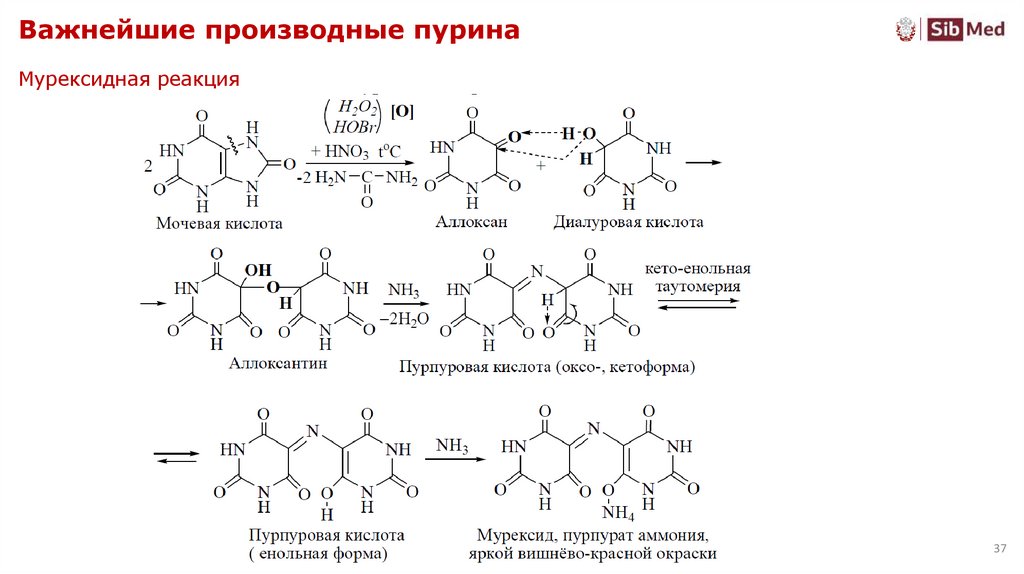
37. Важнейшие производные пурина
Мурексидная реакция37
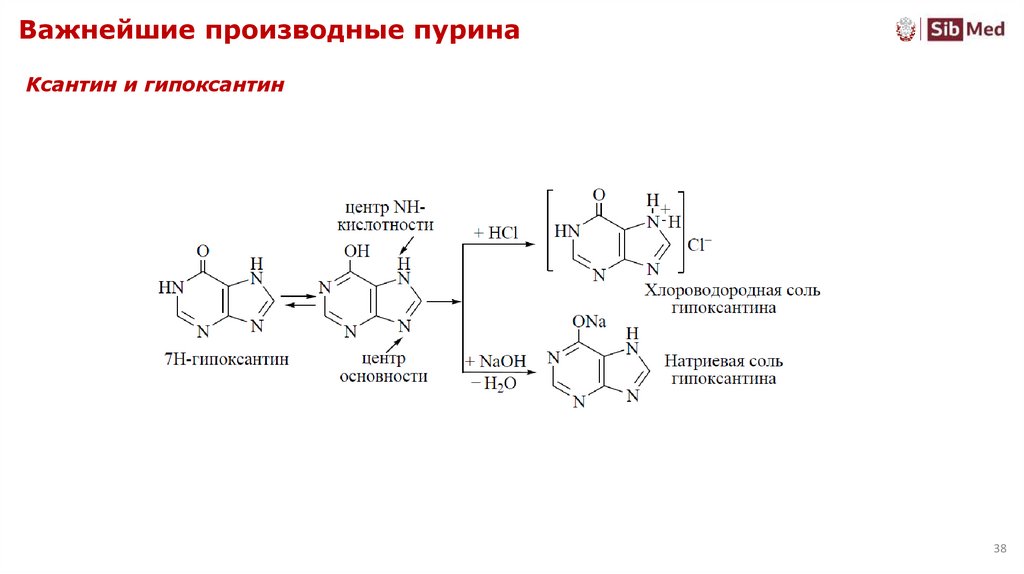
38. Важнейшие производные пурина
Ксантин и гипоксантин38
39. Важнейшие производные пурина
Пуриновые алкалоиды39
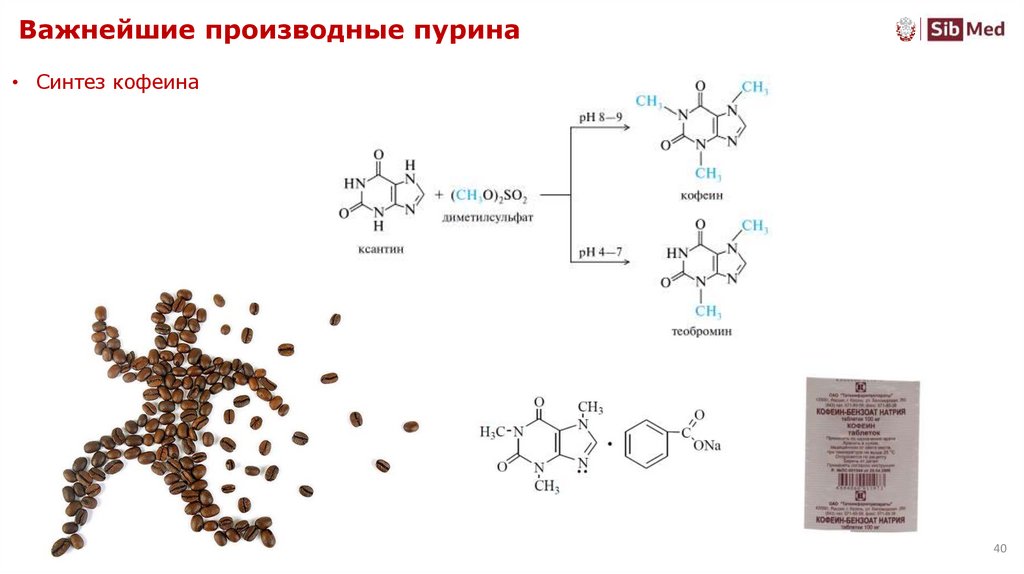
40. Важнейшие производные пурина
• Синтез кофеина40
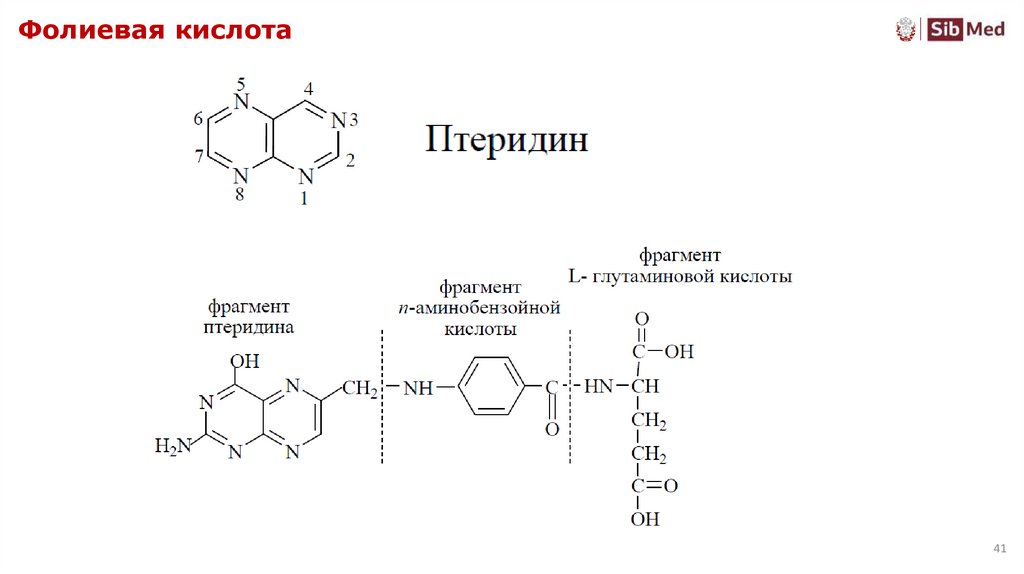
41. Фолиевая кислота
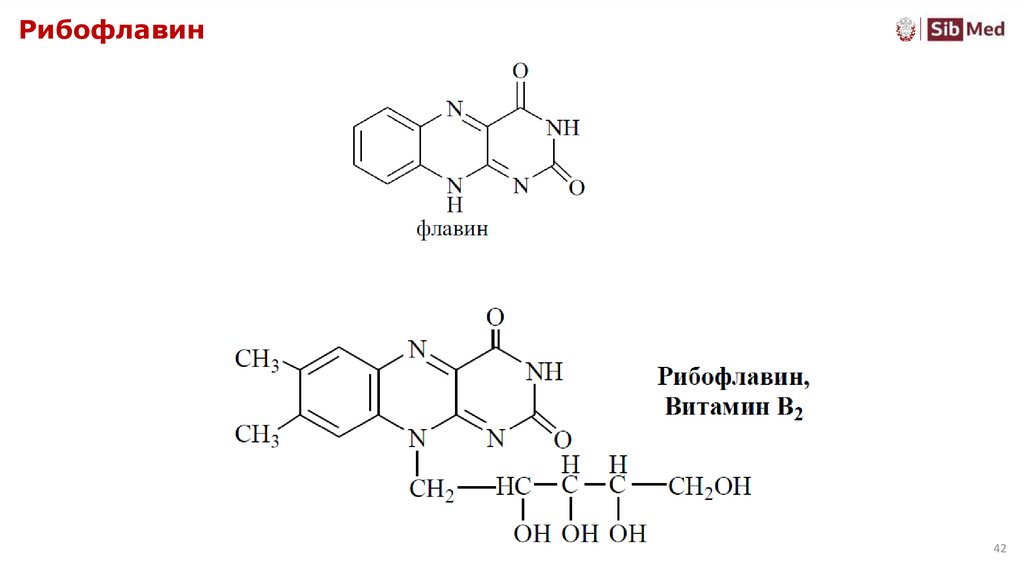
4142. Рибофлавин
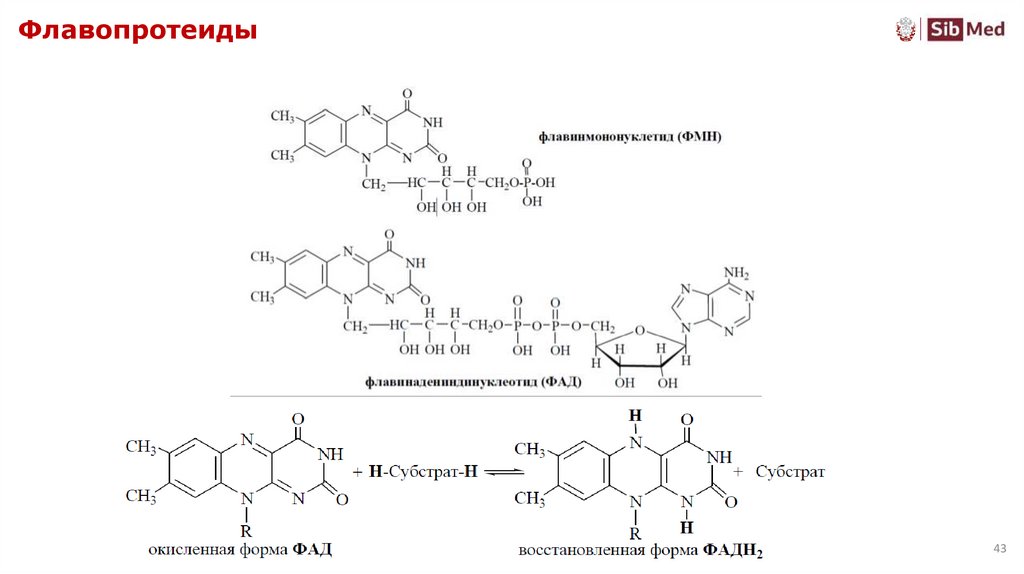
4243. Флавопротеиды
4344.
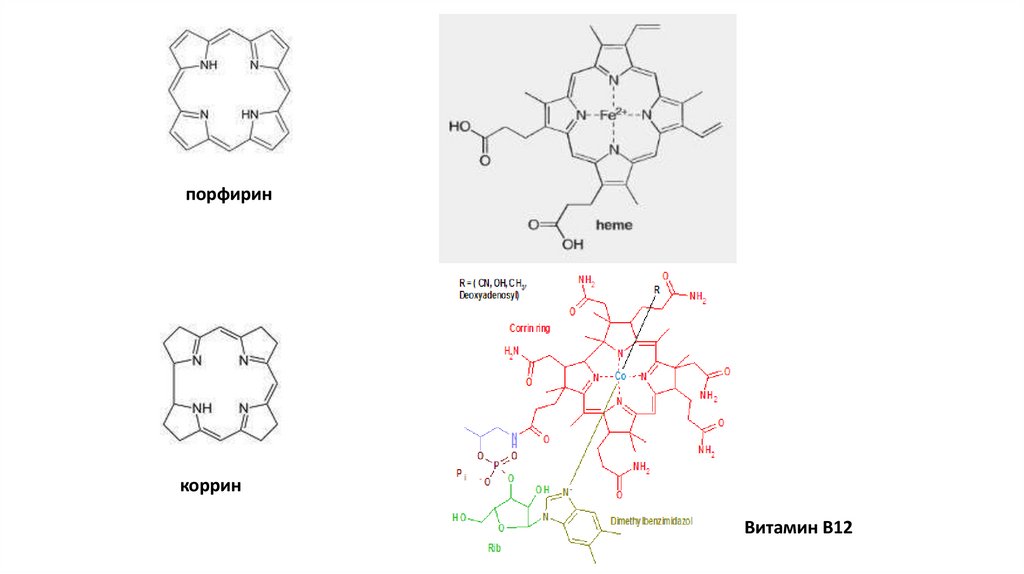
порфиринкоррин
Витамин В12



 chemistry
chemistry