Similar presentations:
Частные пути обмена отдельных аминокислот
1. ФГБОУ ВО УГМУ МИНЗДРАВА кафедра биохимии
Частные пути обмена отдельныхаминокислот.
Патология обмена.
Доцент Каминская Л.А.
2025
2. План:
Заменимые аминокислотыСерин, Глицин, Цистеин
Глутаминовая кислота,
Аспарагиновая кислота
Незаменимые аминокислоты
Метионин Фенилаланин
Тирозин Триптофан
3. Заменимые аминокислоты
Взаимно превращаются друг в друга.Синтезируются в организме
Синтез заменимых аминокислот
связан с обменом глюкозы,
субстратами гликолиза и цикла
Кребса.
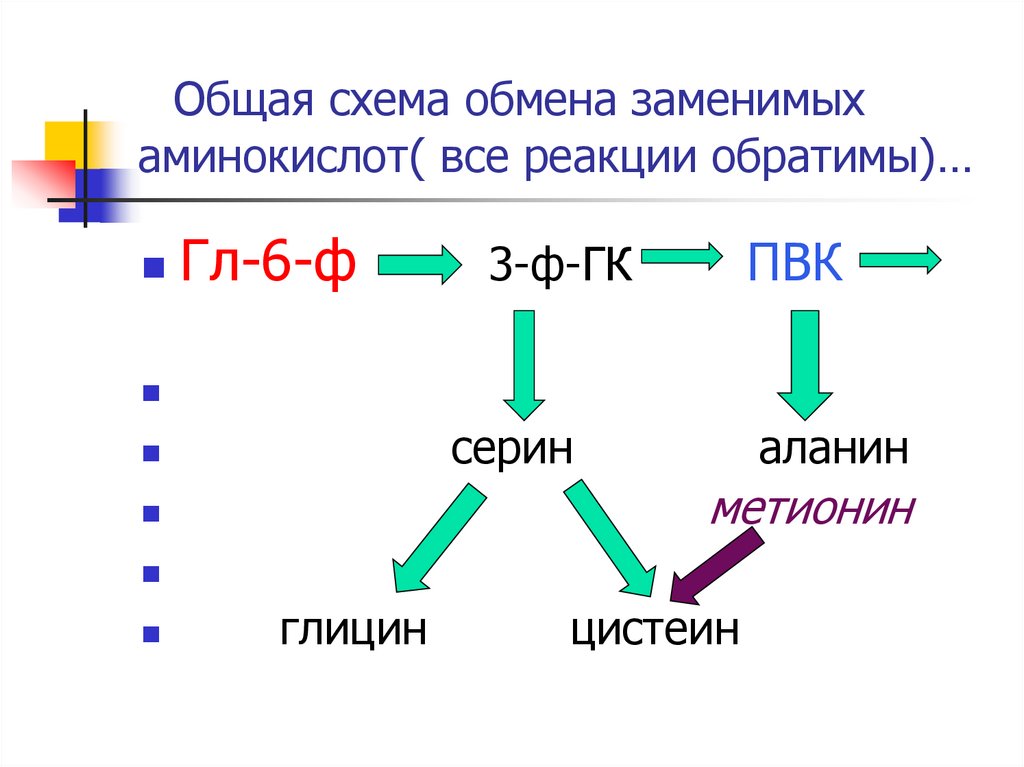
4. Общая схема обмена заменимых аминокислот( все реакции обратимы)…
Гл-6-фПВК
3-ф-ГК
серин
аланин
метионин
глицин
цистеин
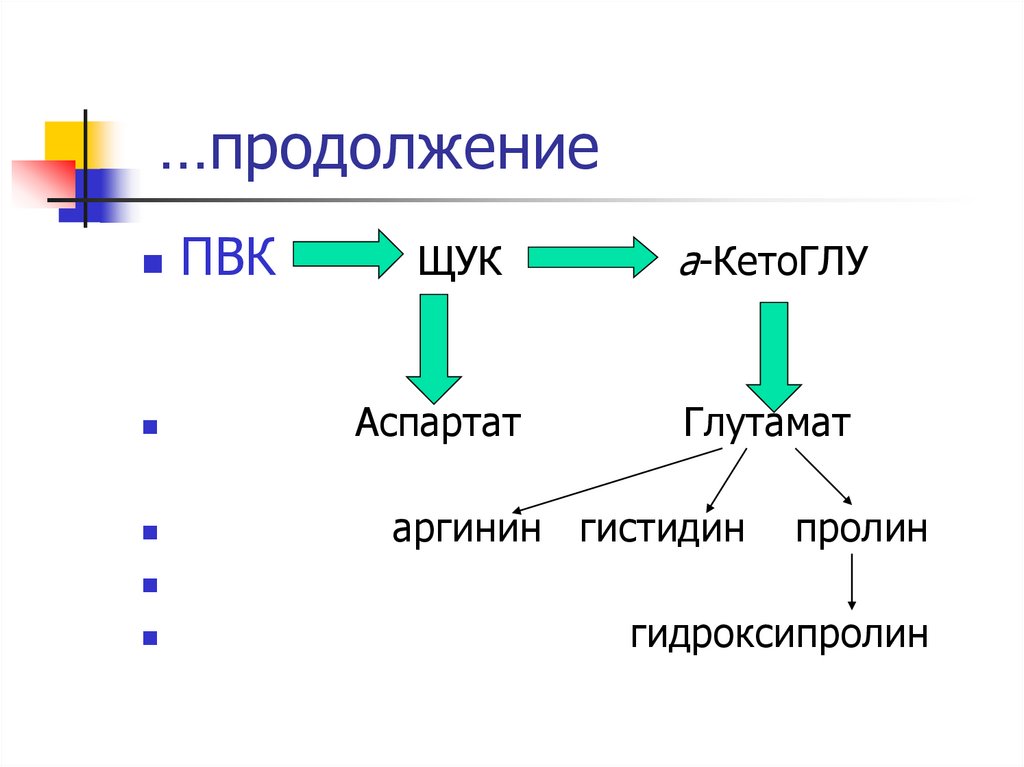
5. …продолжение
ПВКЩУК
а-КетоГЛУ
Аспартат
Глутамат
аргинин гистидин
пролин
гидроксипролин
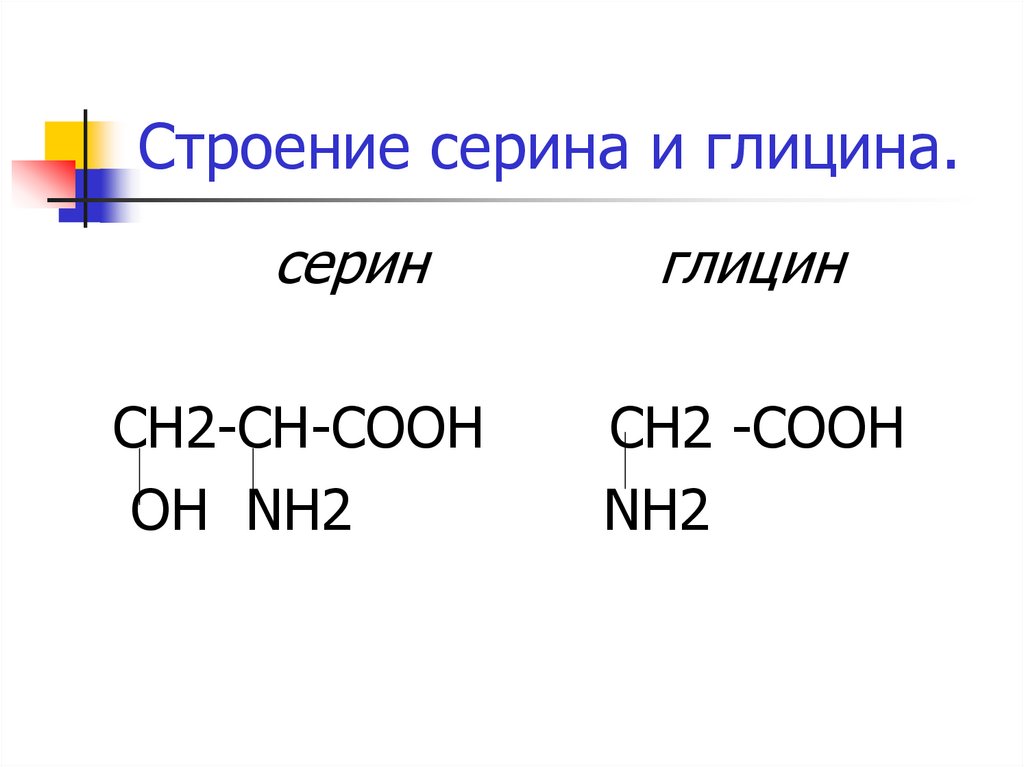
6. Строение серина и глицина.
серинСН2-СН-СООН
OH NH2
глицин
СН2 -СООН
NH2
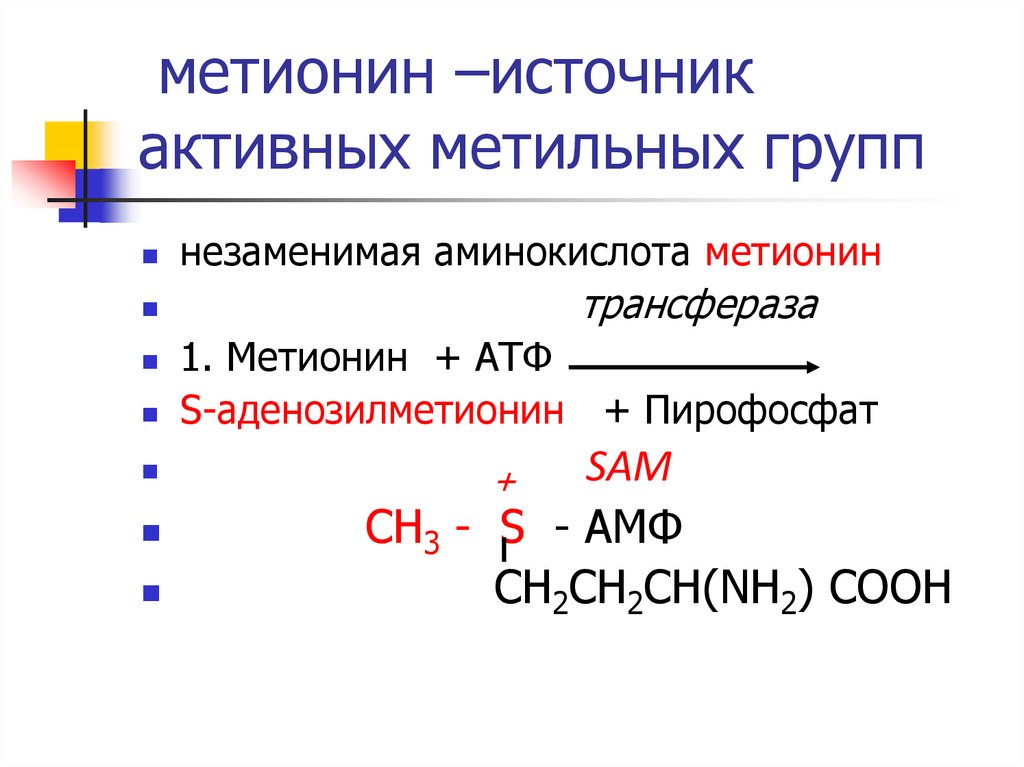
7. метионин –источник активных метильных групп
незаменимая аминокислота метионинтрансфераза
1. Метионин + АТФ
S-аденозилметионин
+ Пирофосфат
SAM
СН3 - S - АМФ
СН2СН2СН(NН2) СООН
+
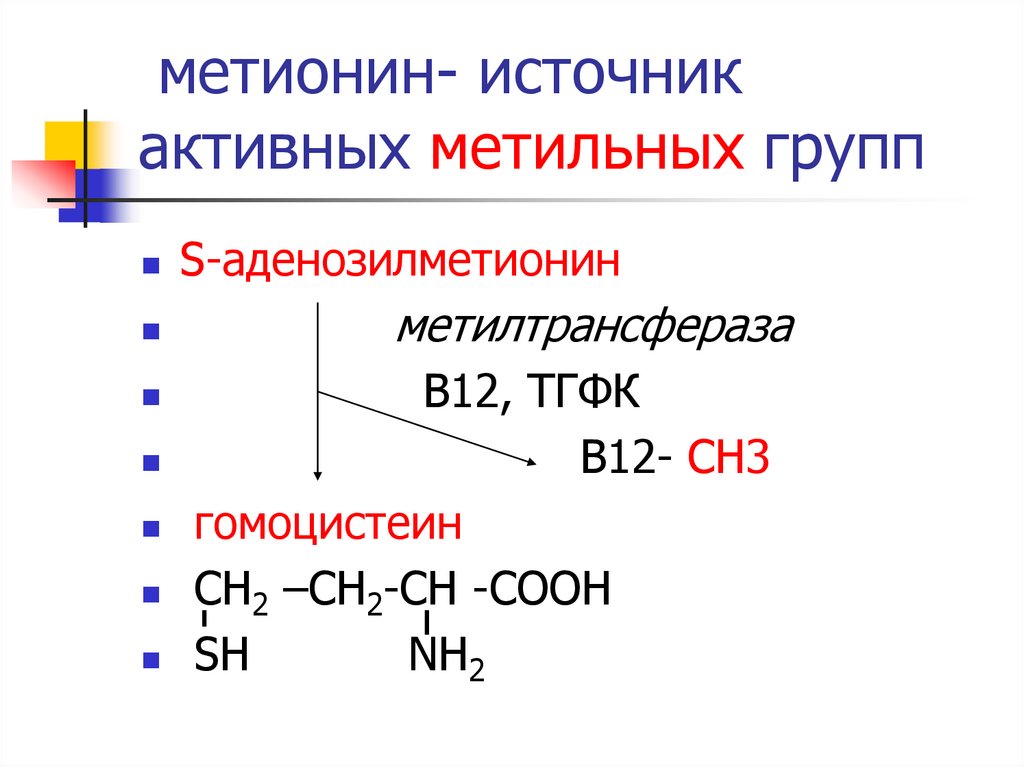
8. метионин- источник активных метильных групп
S-аденозилметионинметилтрансфераза
В12, ТГФК
В12- СН3
гомоцистеин
СН2 –СН2-СН -СООН
SH
NН2
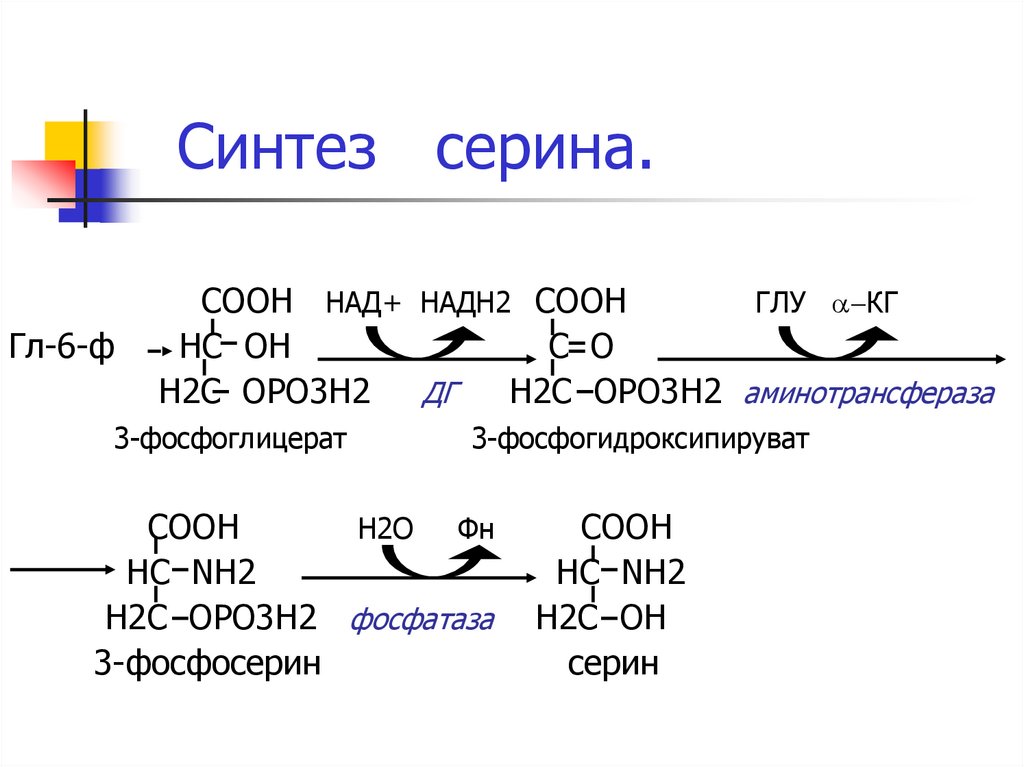
9. Cинтез серина.
Гл-6-фСООН НАД+ НАДН2 СООН
ГЛУ a-КГ
НС ОН
С О
Н2С ОРО3Н2
ДГ
Н2С ОРО3Н2 аминотрансфераза
3-фосфоглицерат
3-фосфогидроксипируват
СООН
H2O
Фн
НС NH2
H2C OPO3H2 фосфатаза
3-фосфосерин
COOH
HC NH2
H2C OH
серин
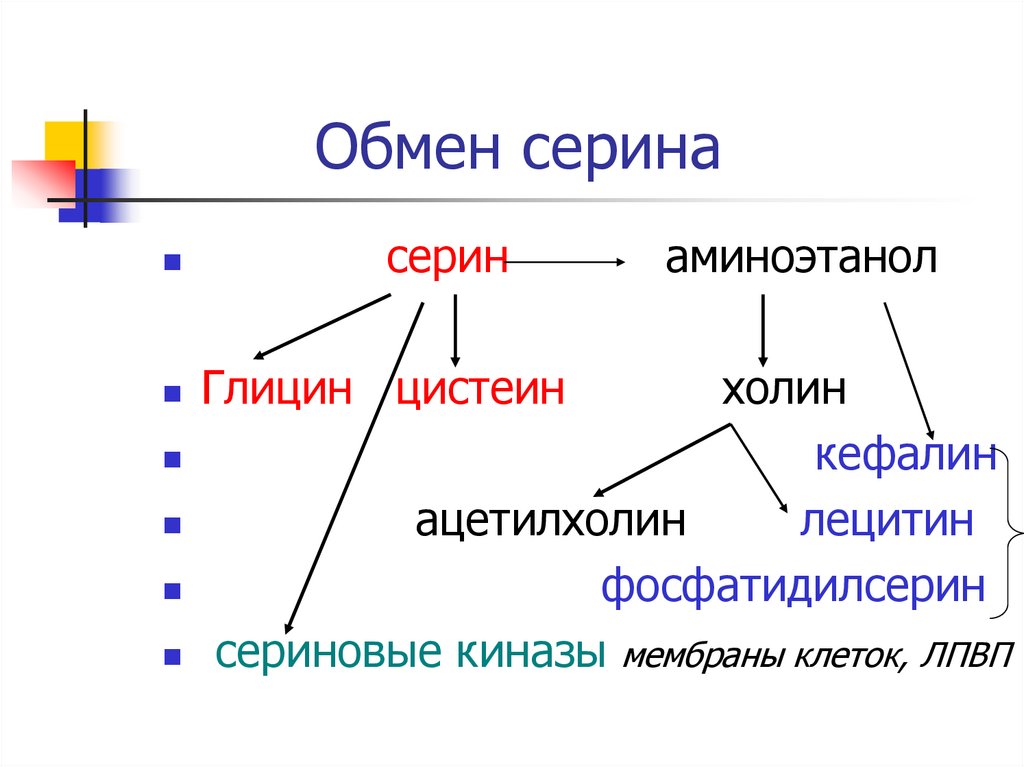
10. Обмен серина
серинГлицин цистеин
аминоэтанол
холин
кефалин
ацетилхолин
лецитин
фосфатидилсерин
сериновые киназы мембраны клеток, ЛПВП
11. синтез коламина и холина
Серин( сериндекарбоксилаза, В6)
+ s-аденозилметионин
(метилтрансфераза, В12 )
НO-СН2-СН2-NH2
аминоэтанол( коламин)
НO-СН2-СН2-N+(СН3)3 холин
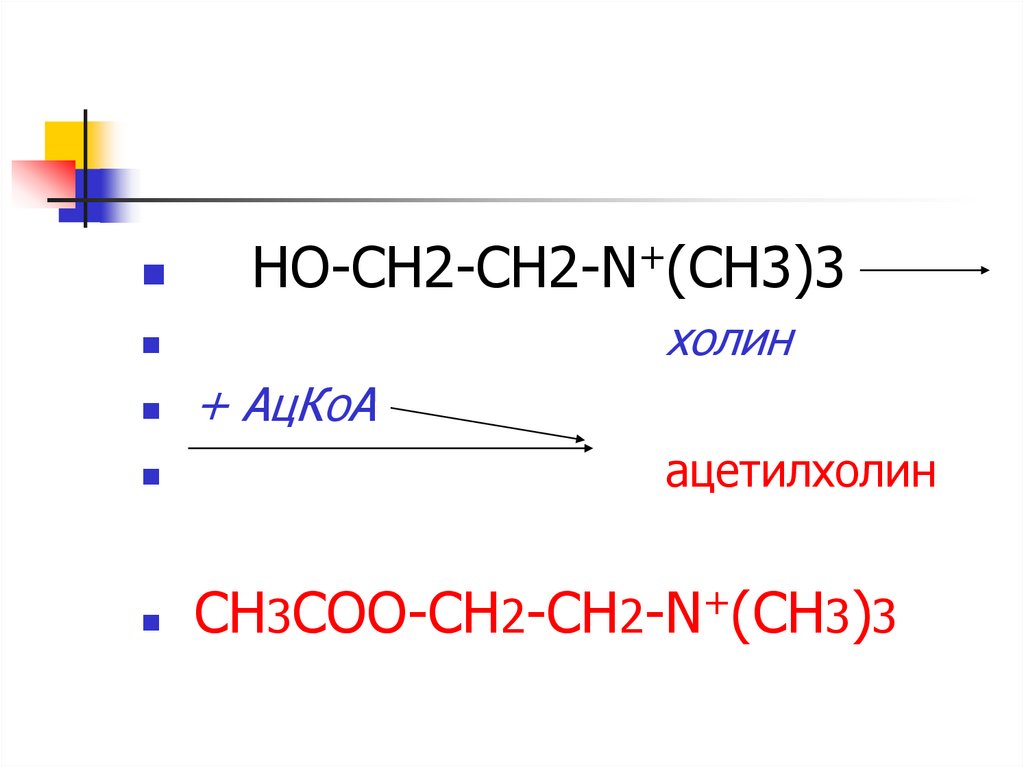
12.
НO-СН2-СН2-N+(СН3)3холин
+ АцКоА
ацетилхолин
СН3СОO-СН2-СН2-N+(СН3)3
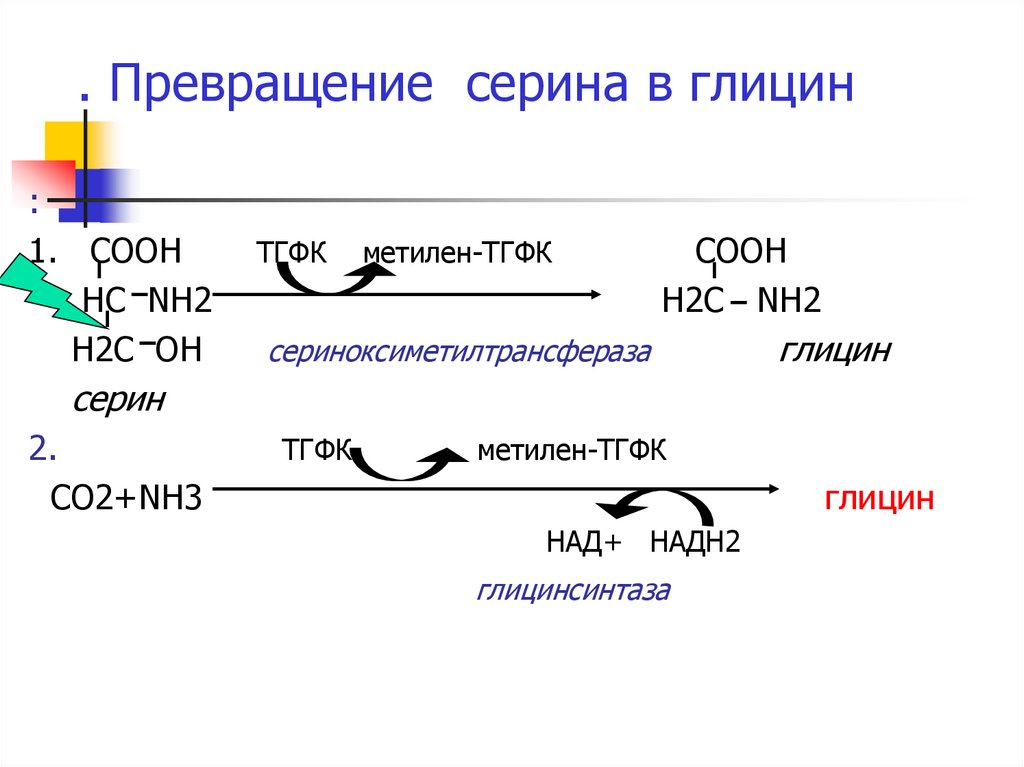
13. . Превращение серина в глицин
:1. COOH
HC NH2
H2C OH
ТГФК
метилен-ТГФК
COOH
H2C NH2
сериноксиметилтрансфераза
глицин
серин
2.
СО2+NH3
ТГФК
метилен-ТГФК
глицин
НАД+ НАДН2
глицинсинтаза
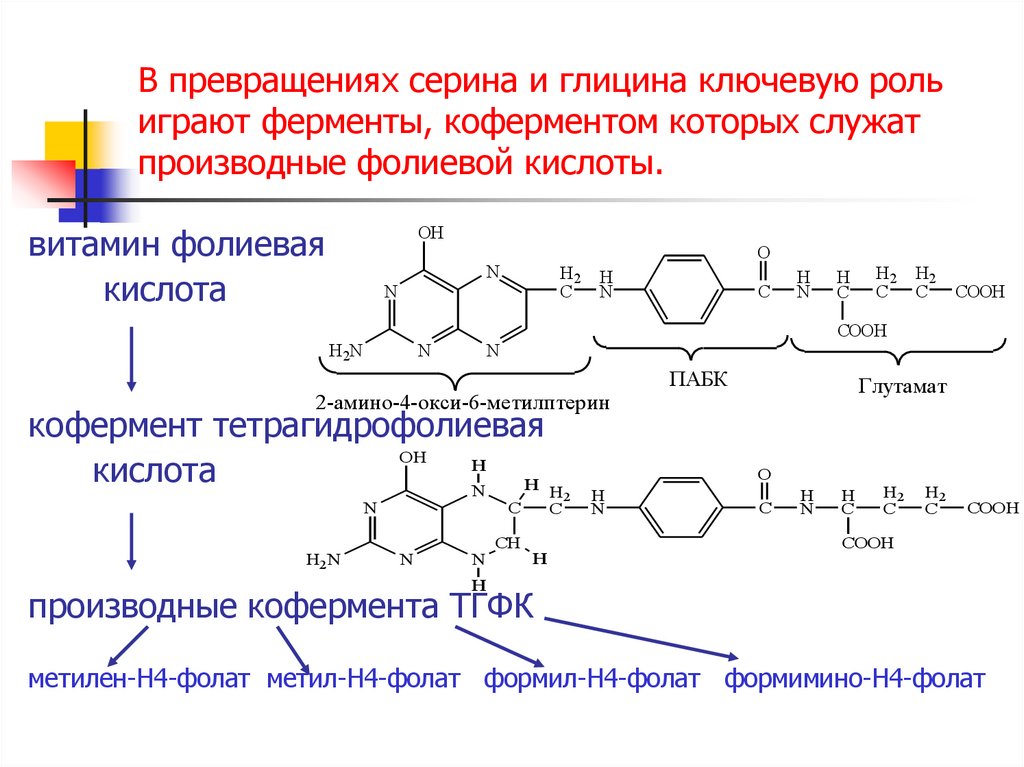
14. В превращениях серина и глицина ключевую роль играют ферменты, коферментом которых служат производные фолиевой кислоты.
витамин фолиеваякислота
OH
O
N
N
H2N
N
H2
C
H
N
N
C
N
H
C
H2
C
H2
C
COOH
COOH
кофермент тетрагидрофолиевая
OH
H
кислота
H H
N
N
H
N
N
2-амино-4-окси-6-метилптерин
H2N
C
CH
C
H
2
ПАБК
Глутамат
O
H
N
C
H
N
H
C
H2
C
H2
C
COOH
COOH
H
производные кофермента ТГФК
метилен-Н4-фолат метил-Н4-фолат формил-Н4-фолат формимино-Н4-фолат
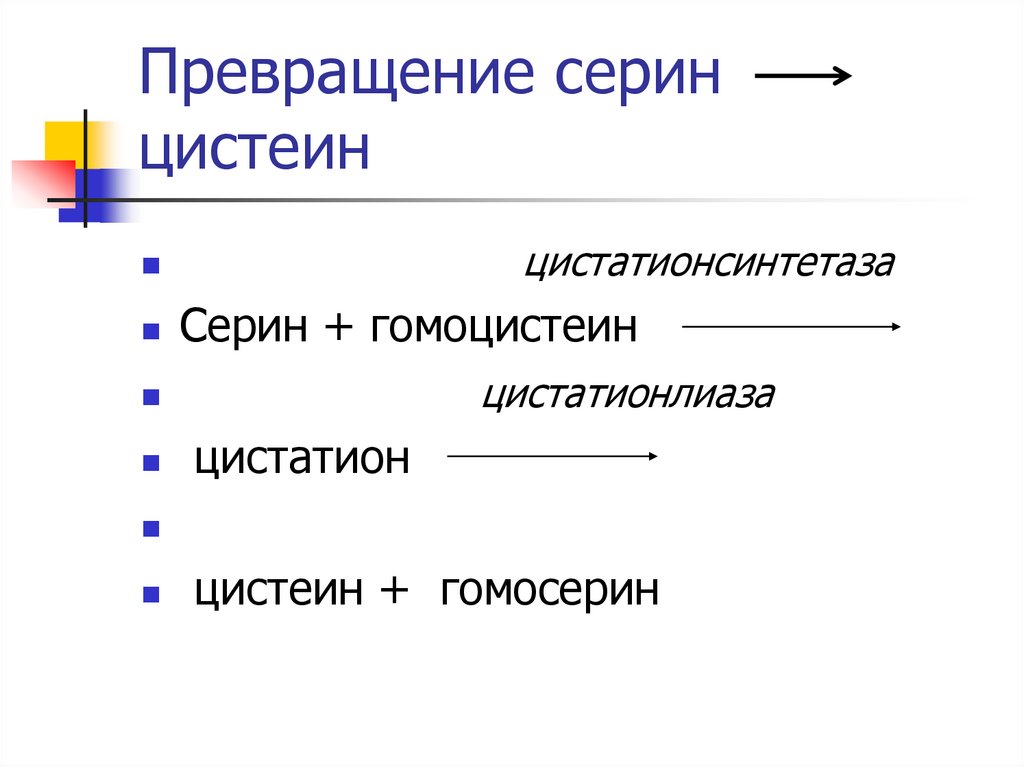
15. Превращение серин цистеин
цистатионсинтетазаСерин + гомоцистеин
цистатионлиаза
цистатион
цистеин + гомосерин
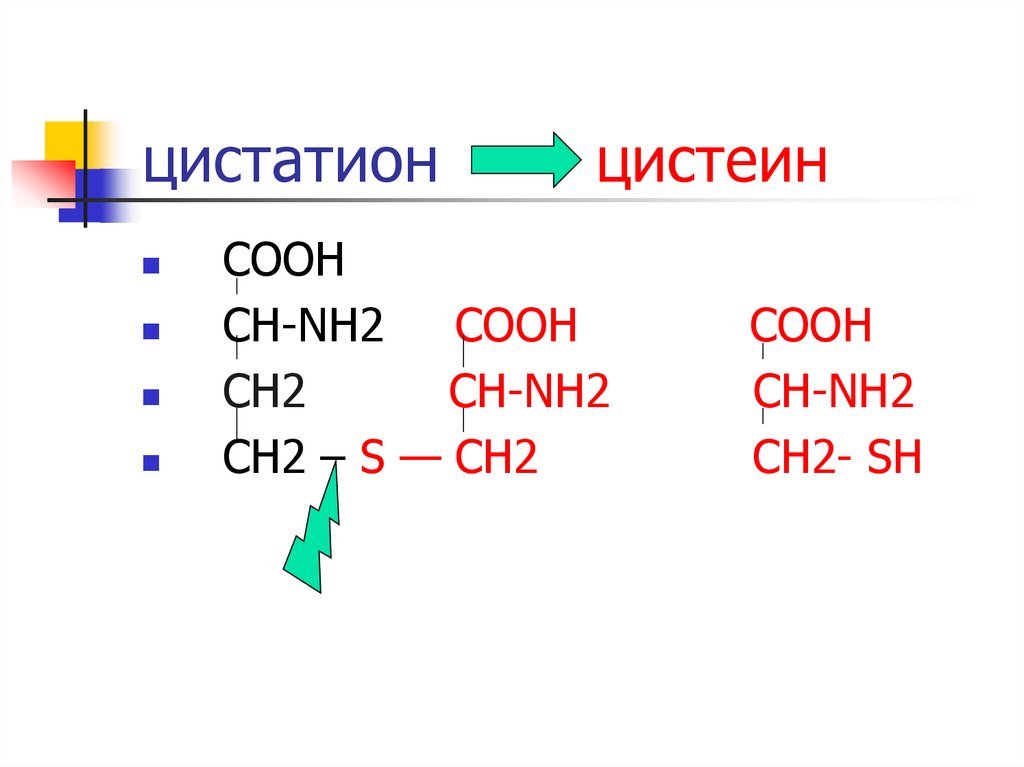
16. цистатион цистеин
COOHCH-NH2
COOH
CH2
CH-NH2
CH2 – S — CH2
СООН
CH-NH2
СН2- SН
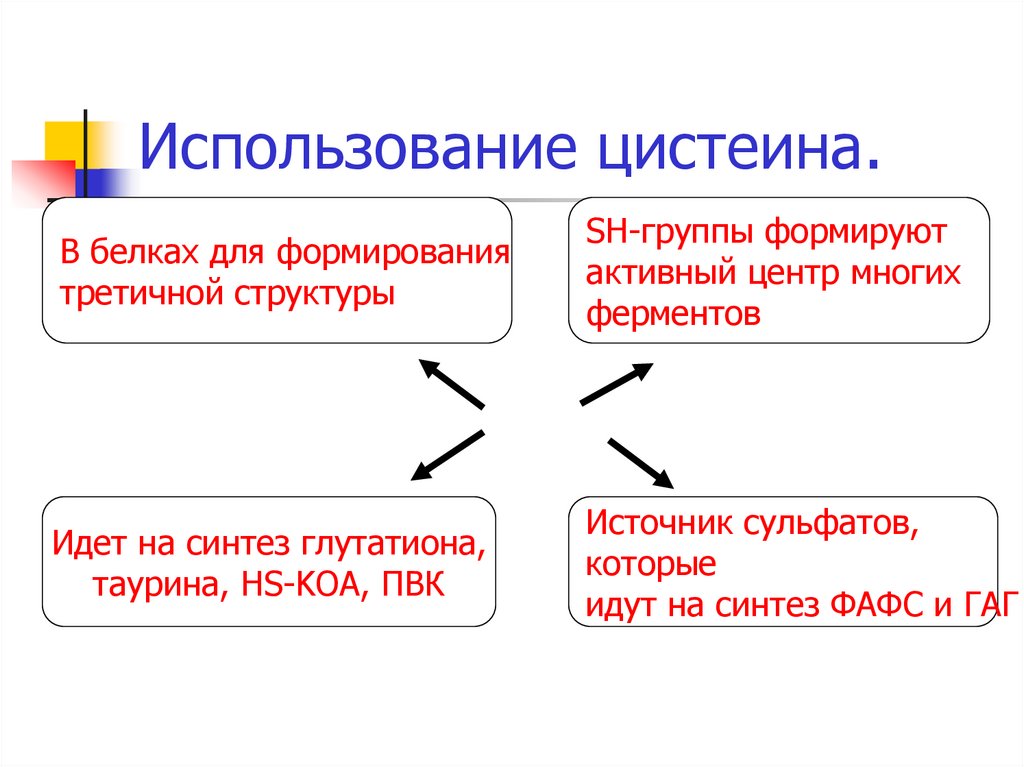
17. Использование цистеина.
В белках для формированиятретичной структуры
SH-группы формируют
активный центр многих
ферментов
Идет на синтез глутатиона,
таурина, HS-KOA, ПВК
Источник сульфатов,
которые
идут на синтез ФАФС и ГАГ
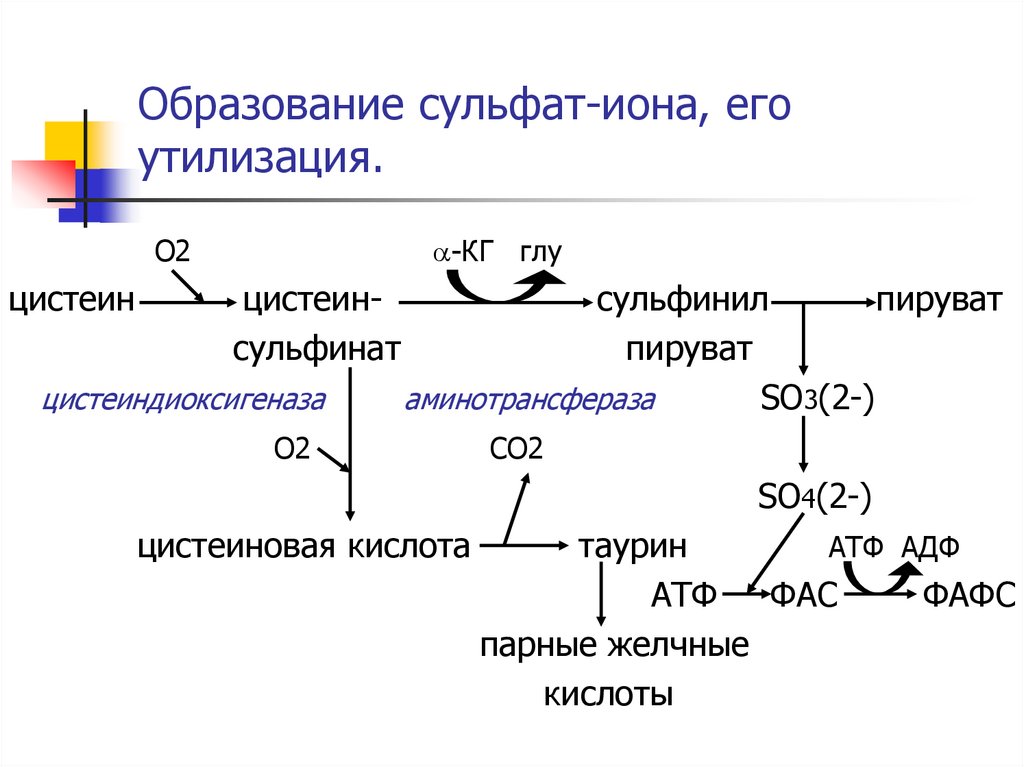
18. Образование сульфат-иона, его утилизация.
a-КГ глуО2
цистеин
цистеинсульфинат
цистеиндиоксигеназа
сульфинил
пируват
пируват
аминотрансфераза
SО3(2-)
O2
CO2
SO4(2-)
цистеиновая кислота
таурин
АТФ АДФ
АТФ
ФАС
ФАФС
парные желчные
кислоты
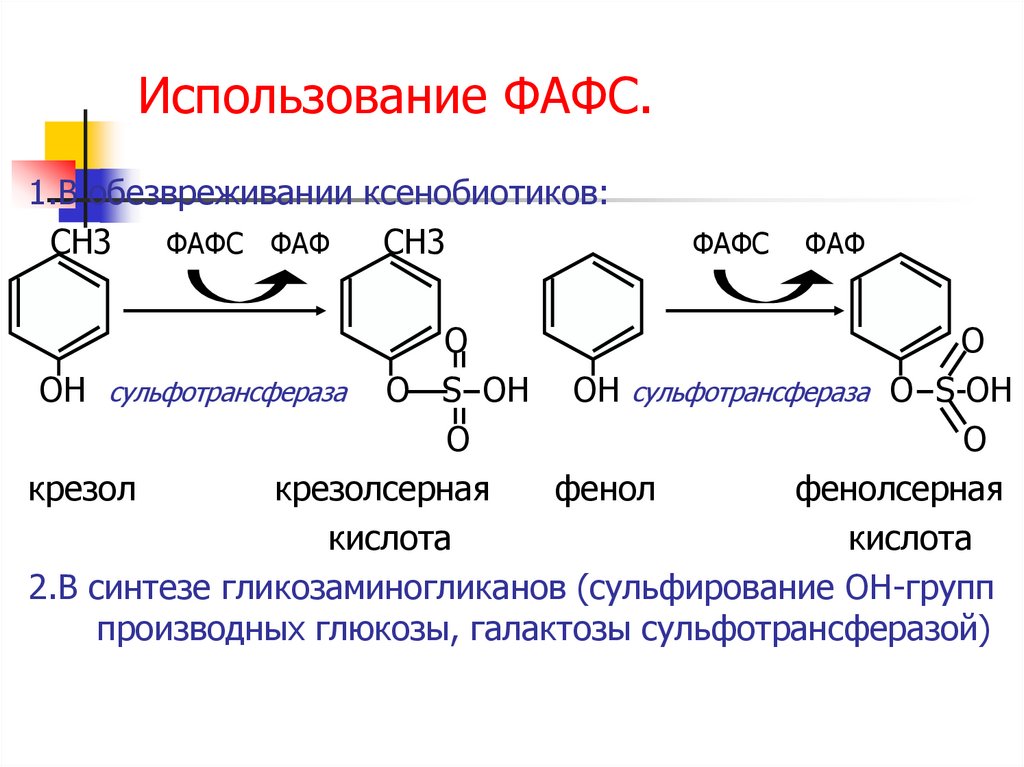
19. Использование ФАФС.
1.В обезвреживании ксенобиотиков:СН3
ФАФС ФАФ
СН3
ФАФС
ФАФ
O
O
OH сульфотрансфераза О S OH OH сульфотрансфераза О S OH
O
O
крезол
крезолсерная
фенол
фенолсерная
кислота
кислота
2.В синтезе гликозаминогликанов (сульфирование ОН-групп
производных глюкозы, галактозы сульфотрансферазой)
20. Пути использования глицина
содержание в коллагене -33%синтез гема(совместно с сукцКоА)
Синтез пуринового цикла( А, Гнуклеотиды, НК )
синтез глутатиона
синтез креатинина
желчные кислоты –гликохолевая
обезвреживание
эндогенных и
экзогенных токсических соединений
21. катаболизм глицина
1. глицин (МХ печени, ТГФК )СО2 + NH3 + H2O
2. глицин (трансаминирование, В6)
НООС-СНО (окисление)
НООС-СООН щавелевая кислота
источник оксалатов ! силитиаз
22. Патология обмена глицина
1.2.
Глицинурия – характеризуется
повышенным выделением глицина с
мочой (до 1 г/сут). Причина – нарушение
реабсорбции глицина в почках.
Первичная гипероксалатурия –
характеризуется постоянным выделением
оксалата с мочой. Дефект
глицинаминотрансферазы блокирует
превращение глиоксилата в глицин
(глицин – глиоксилат – оксалат).
23.
1.Гиперглицинемия – характеризуется повышенной
концентрацией глицина в крови в следствии
дефекта глицинрасщепляющей ферментной
системы.
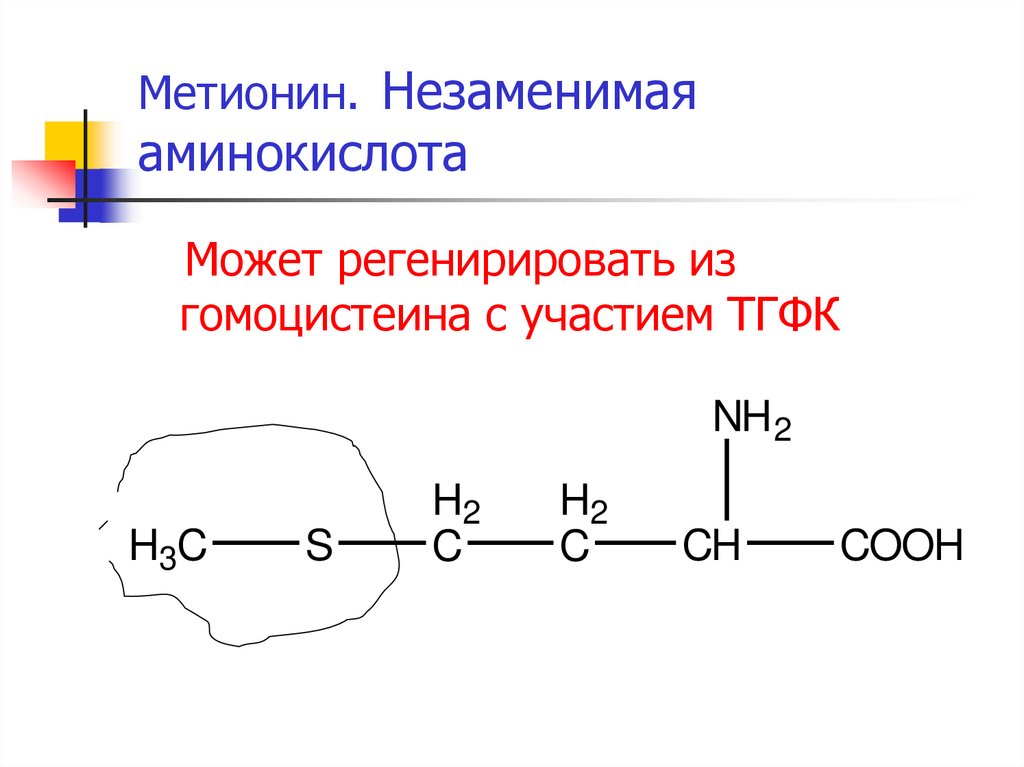
24. Метионин. Незаменимая аминокислота
Может регенирировать изгомоцистеина с участием ТГФК
NH2
H3C
S
H2
C
H2
C
CH
COOH
25. Обмен обеспечивается витаминами В12, Фолиевой кислотой
участвует в синтезе белков организма;является источником метильной группы,
используемой в реакциях
трансметилирования;
является источником атома серы,
необходимого для синтеза цистеина;
Метионил-тРНК участвует в инициации
процесса трансляции.
26. Пути использования метильной группы метионина
Синтез веществ в реакцияхтрансметилирования
креатина
тимина из урацила
холина из коламина
адреналина из норадреналина
ансерина из карнозина
27. гиповитаминоз В12 и фолиевой кислоты
Нарушение обмена одноуглеродныхфрагментов и трансметилирования –
патология синтеза ДНК и РНК
возникает мегалобластная
(макроцитарная) анемия :
снижается количество эритроцитов,
содержание
Hb, увеличение
размеров эритроцитов.
28.
2.Увеличивается содержаниегомоцистеина в крови.
Особенно опасно в первые недели
беременности!- одна из причин
патологии развития плода.
Обязательный прием В12 и
фолиевой кислоты ! при плановой
беременности заранее 2-3 недели.
29. Нарушения обмена метионина:
Гомоцитинурия – характеризуетсянаследственной недостаточностью
цистатионин-b-синтетазы,
гиповитаминозом фолиевой кислоты,
витаминов В6 и В12;
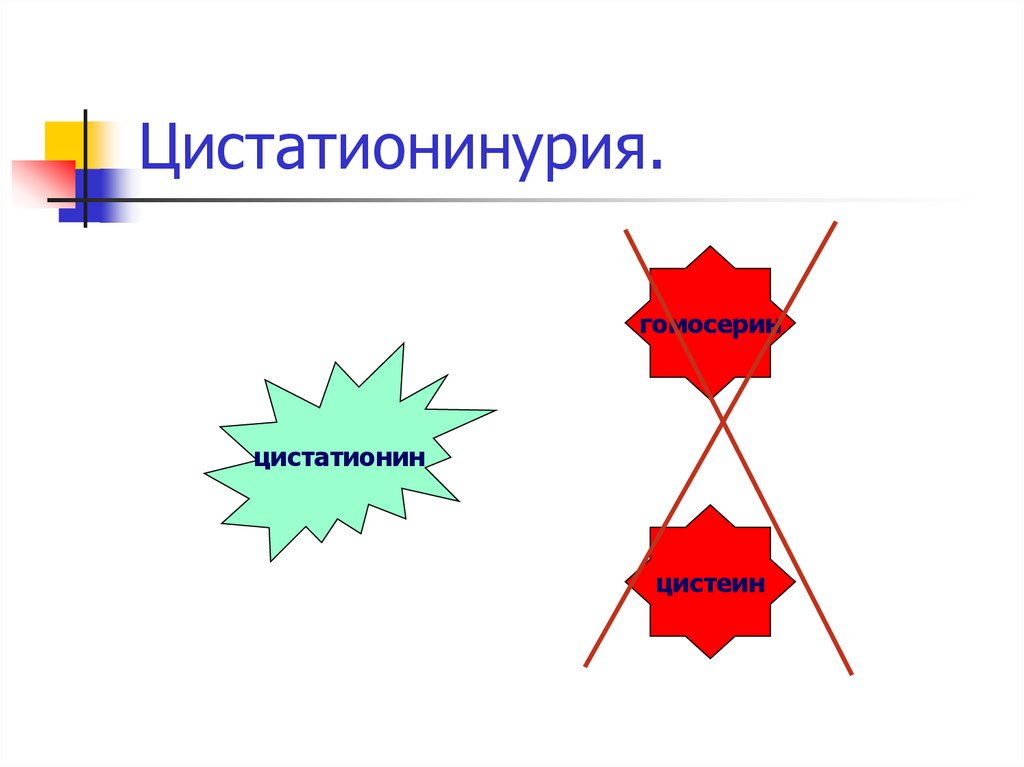
Цистатионинурия – характеризуется
выделением цистатионина с мочой. Этот
процесс вызывается блокированием
реакции распада цистатионина на
гомосерин и цистеин.
30. Цистатионинурия.
гомосеринцистатионин
цистеин
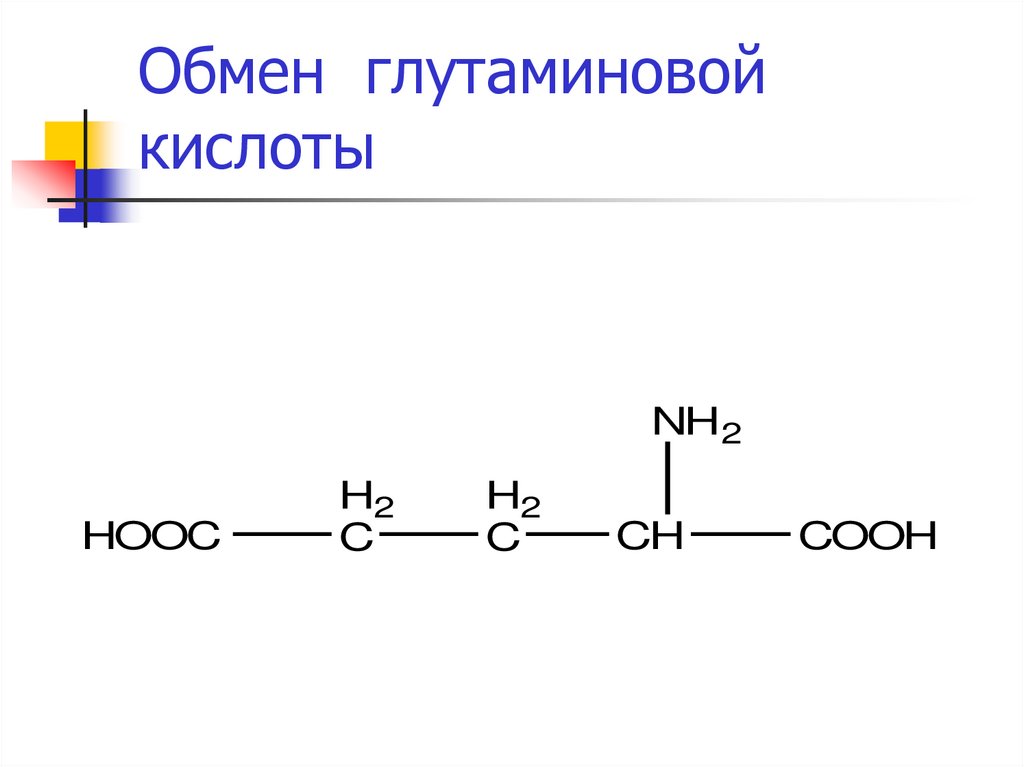
31. Обмен глутаминовой кислоты
NH2HOOC
H2
C
H2
C
CH
COOH
32. Пути обмена глутамата
В составе белковОкислительное дезаминирование- превращение в
а-кетоГЛУ
Трансаминирование- синтез заменимых АК
Синтез пуринового цикла (А, Г, АТФ, ГТФ, НК )
Синтез глутамина( транспорт аммиака из тканей
в печень, поддержание КОС в почке)
Синтез ГАМК и ГОМК( медиаторы торможения )
33.
Синтез аминокислот:орнитина( цикл мочевины)
гистидина
пролина
гидроксиролина
Синтез глутатиона
Источник аминогруппы для аминосахаров
( синтез ГАГ)
Источник НАД(Ф)Н в МСО и АОЗ
34. Синтез глутамата.
1.2.
Восстановительное аминирование aкетоглутарата глутаматдегидрогеназой:
а- кетоГЛУ + NH3 + NAДН + Н+
глутаматдегидрогеназа
2.
ГЛУ + NAД+
Реакция переаминирования с участием
аминотрансфераз:
АК
a-КГ
аминотрансфераза
кетокислота
глутамат
35. Нарушения обмена глутамата.
Эпилепсия - хроническое заболеваниеголовного мозга человека. Характеризуется
повторными припадками
Расстройства вестибулярной системы;
Ишемия – заболевание, характеризующееся
уменьшением кровоснабжения участка тела,
органа или ткани вследствие ослабления или
прекращения притока к нему артериальной крови;
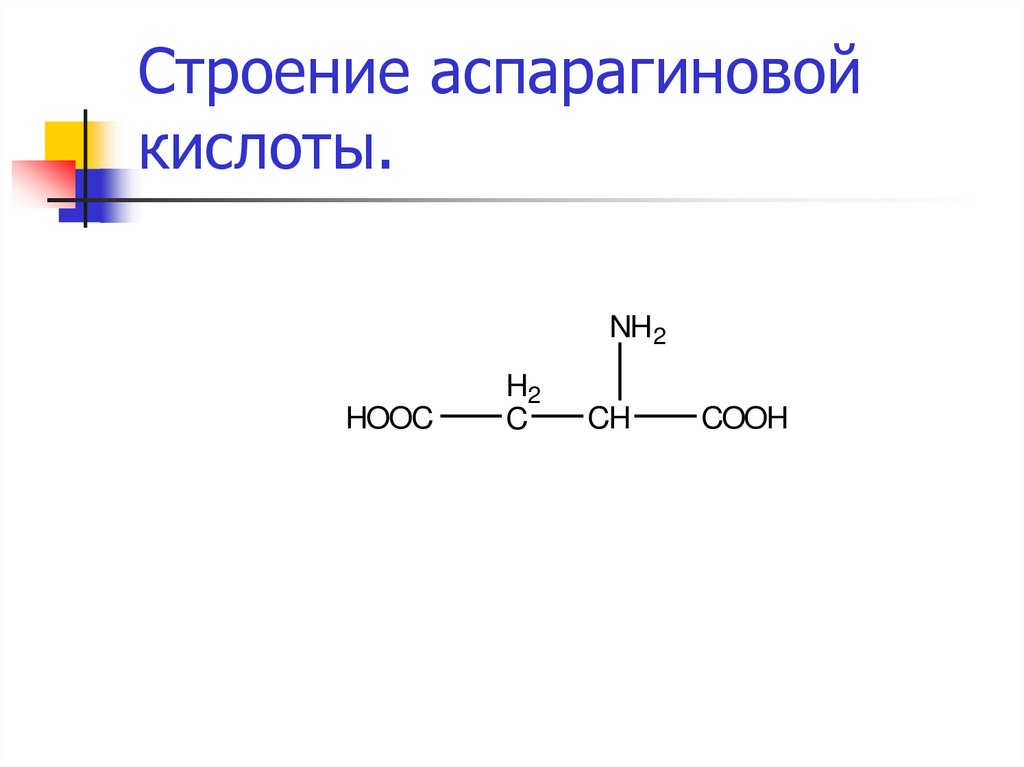
36. Строение аспарагиновой кислоты.
NH2HOOC
H2
C
CH
COOH
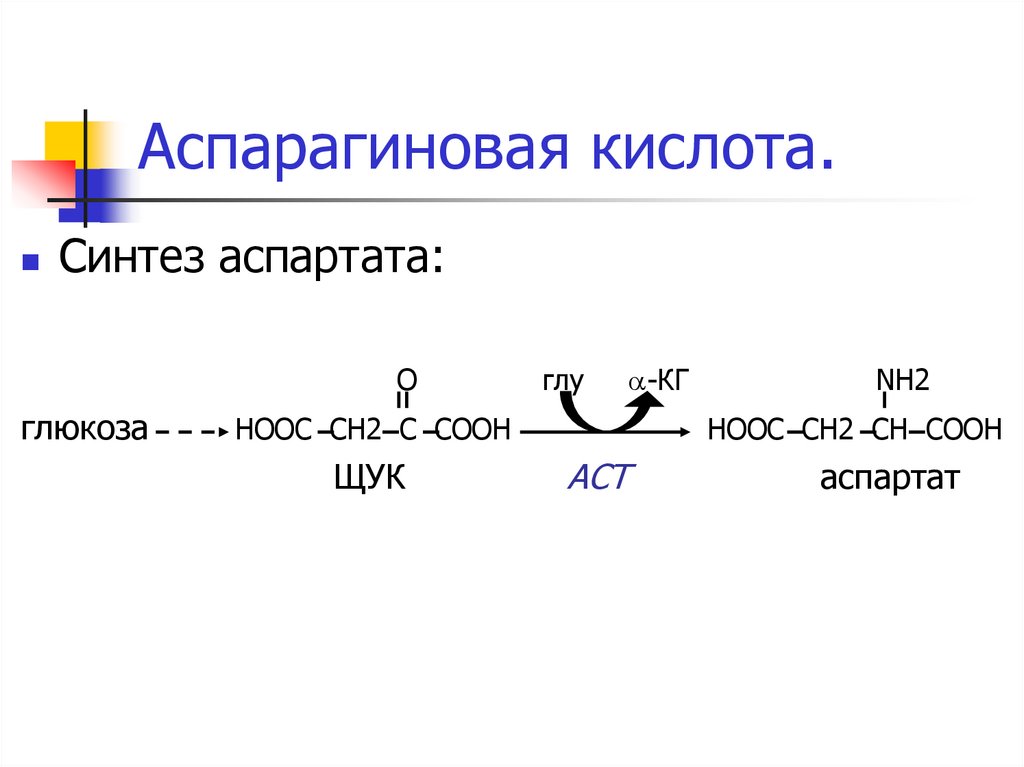
37. Аспарагиновая кислота.
Синтез аспартата:О
глюкоза
глу
НООС СН2 С СООН
ЩУК
a-КГ
NH2
НООС СН2 СН СООН
АСТ
аспартат
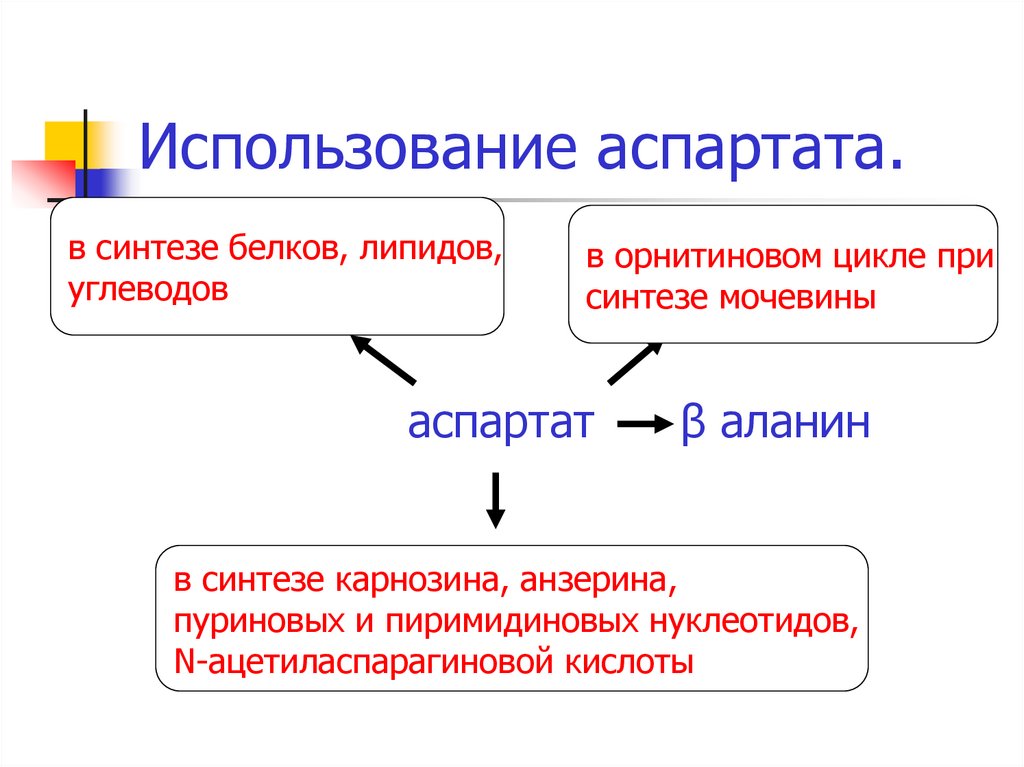
38. Использование аспартата.
в синтезе белков, липидов,углеводов
в орнитиновом цикле при
синтезе мочевины
аспартат
β аланин
в синтезе карнозина, анзерина,
пуриновых и пиримидиновых нуклеотидов,
N-ацетиласпарагиновой кислоты
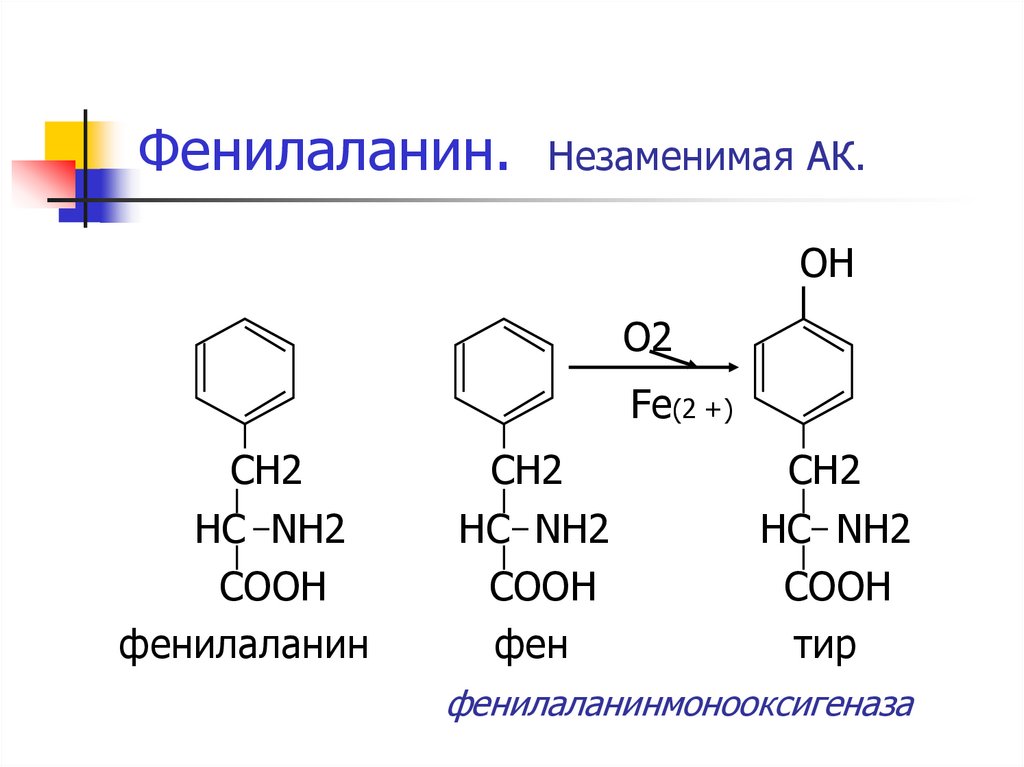
39. Фенилаланин. Незаменимая АК.
ОНО2
Fe(2 +)
CH2
HC NH2
COOH
фенилаланин
СН2
НС NH2
COOH
фен
СН2
HC NH2
COOH
тир
фенилаланинмонооксигеназа
40. Фенилкетонурия.
Наследственное заболевание, связанное смутациями в гене фенилаланингидроксилазы
(частота 1:10000 новорожденных), которые
приводят к снижению активности фермента или
полной его инактивации.
При ФКУ концентрация фенилаланина
повышается в крови в 20-30 раз, в моче в 100-300
раз, по сравнению с нормой.
В крови и моче повышается содержание
метаболитов альтернативного пути:
фенилпирувата, фенилацетата, фениллактата и
фенилацетилглутамина.
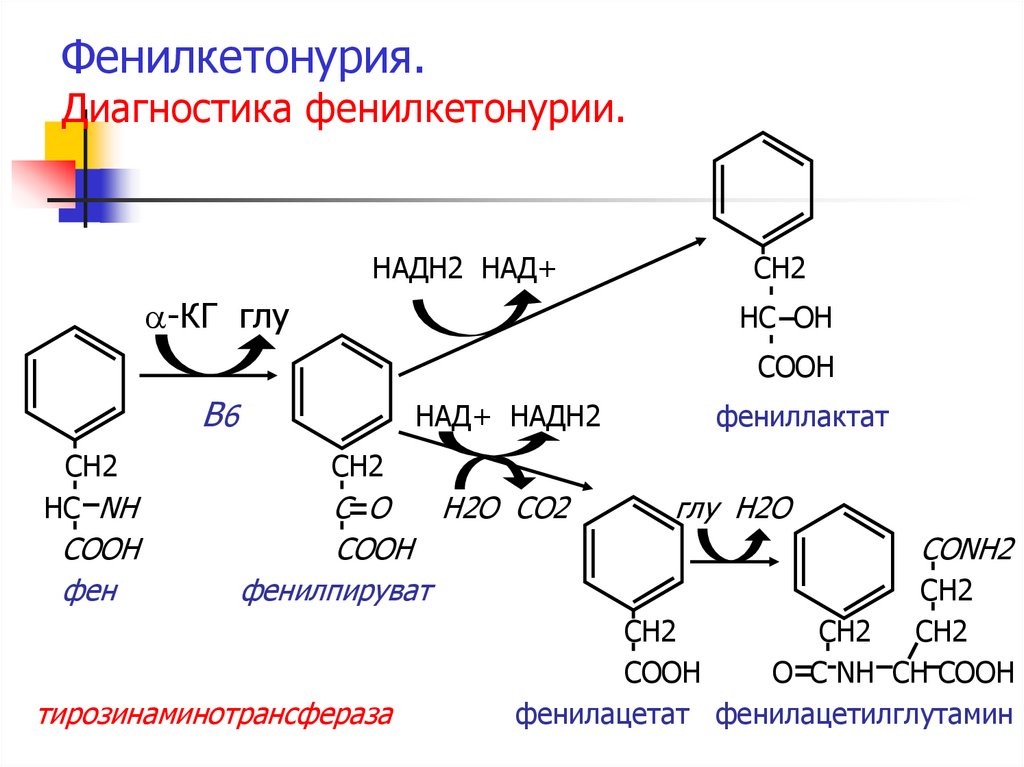
41. Фенилкетонурия. Диагностика фенилкетонурии.
НАДН2 НАД+a-КГ глу
СН2
НС ОН
СООН
В6
СН2
НС NH
COOH
фен
НАД+ НАДН2
фениллактат
CН2
С О
Н2О СО2
СООН
фенилпируват
тирозинаминотрансфераза
глу Н2О
CONH2
CH2
СН2
СН2
CH2
СООН
О С NH CH COOH
фенилацетат фенилацетилглутамин
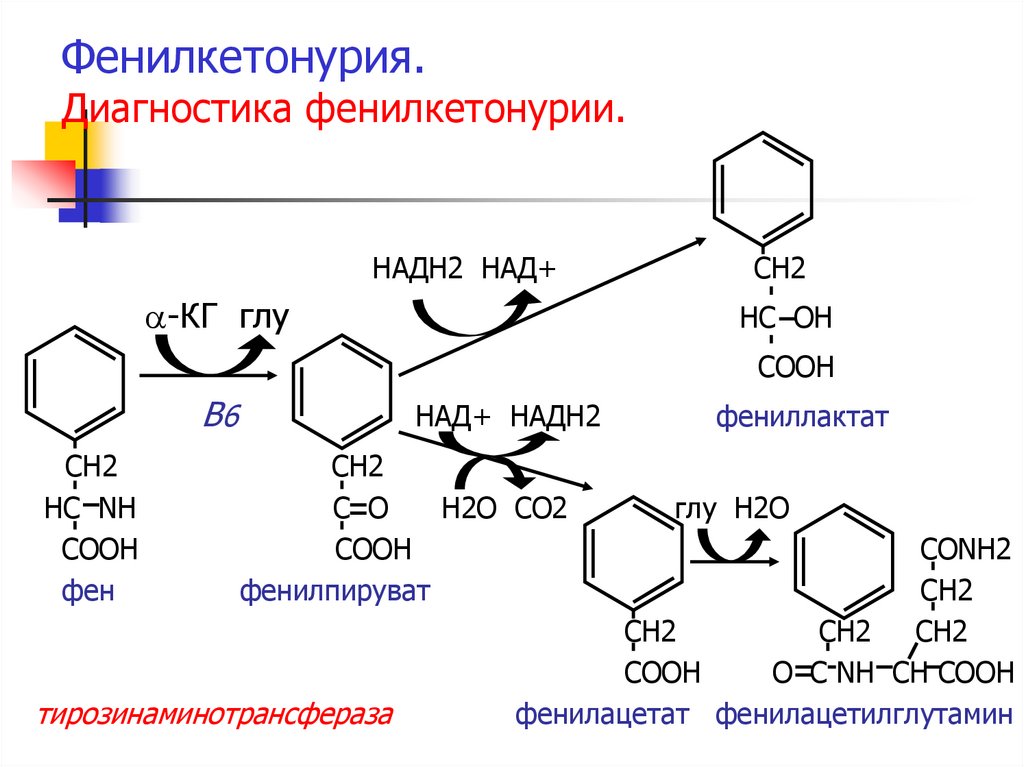
42. Фенилкетонурия. Диагностика фенилкетонурии.
НАДН2 НАД+a-КГ глу
СН2
НС ОН
СООН
В6
СН2
НС NH
COOH
фен
НАД+ НАДН2
CН2
С О
Н2О СО2
СООН
фенилпируват
тирозинаминотрансфераза
фениллактат
глу Н2О
CONH2
CH2
СН2
СН2
CH2
СООН
О С NH CH COOH
фенилацетат фенилацетилглутамин
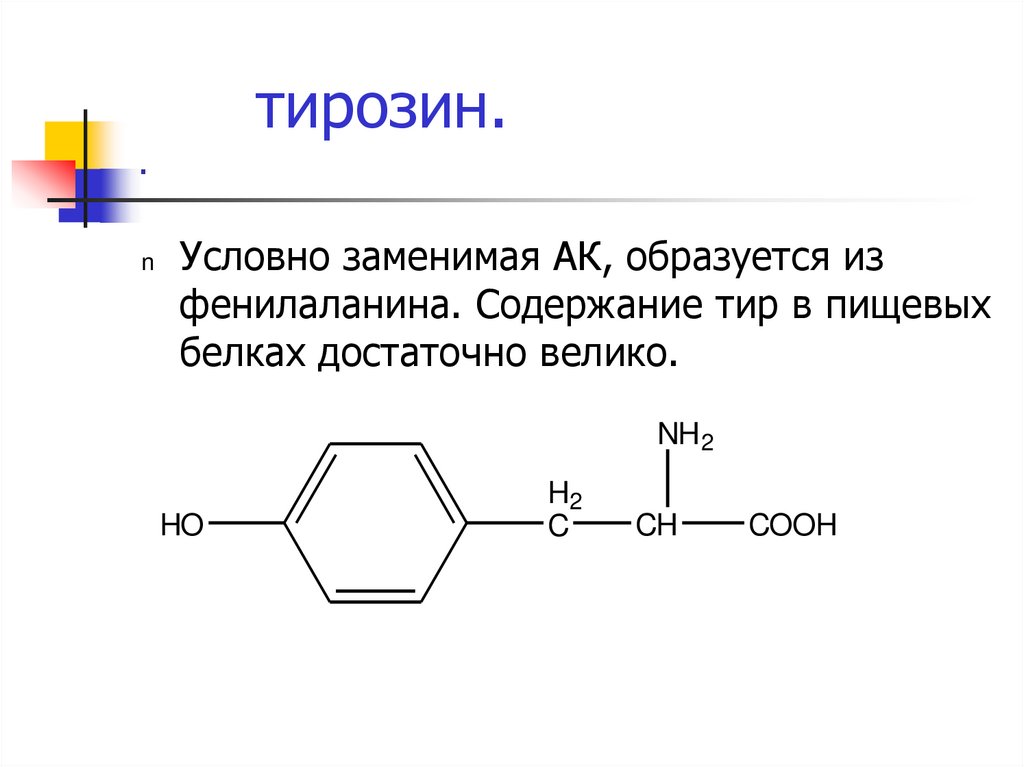
43. тирозин. .
nУсловно заменимая АК, образуется из
фенилаланина. Содержание тир в пищевых
белках достаточно велико.
NH 2
HO
H2
C
CH
COOH
44. ОБМЕН ТИРОЗИНА
1.2.
3.
4.
5.
в нервной ткани и надпочечниках:
синтез дофамина –
норадреналина - адреналина
в меланоцитах – синтез пигмента
меланина
щитовидная железа- синтез
тиреоидных гормонов
катаболизм в печени
45. Обмен в нервной ткани
Тирозин –(1) →ДОФА –(2) →
Дофамин –-(3) → норадреналин →
(4)- адреналин
46.
1)- тирозингидроксилаза ( Fe +2 )регуляторный ф-т, ингибиторадреналин(2)Дофадекарбоксилаза
(3)-Дофамингидроксилаза
( монооксигеназа, вит.С, Си+2)
(4)-N- метилтрансфераза( sаденозилметионин)
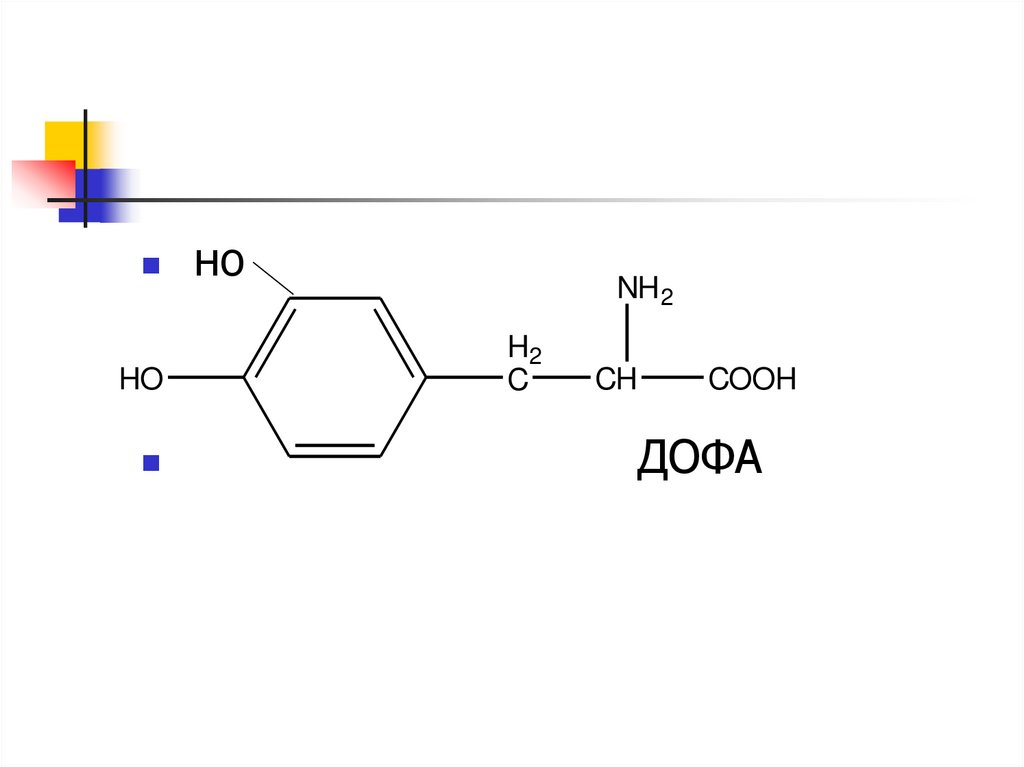
47.
HOно
NH 2
H2
C
CH
COOH
ДОФА
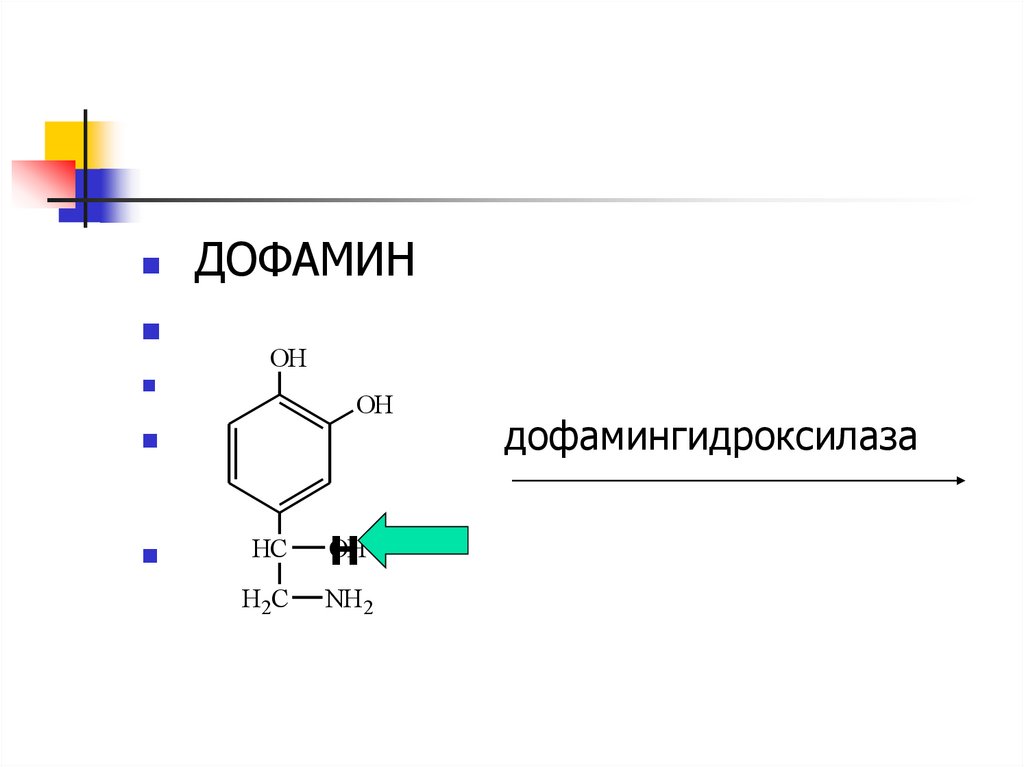
48.
ДОФАМИНOH
OH
HC
ОН
Н
H2C
NH2
дофамингидроксилаза
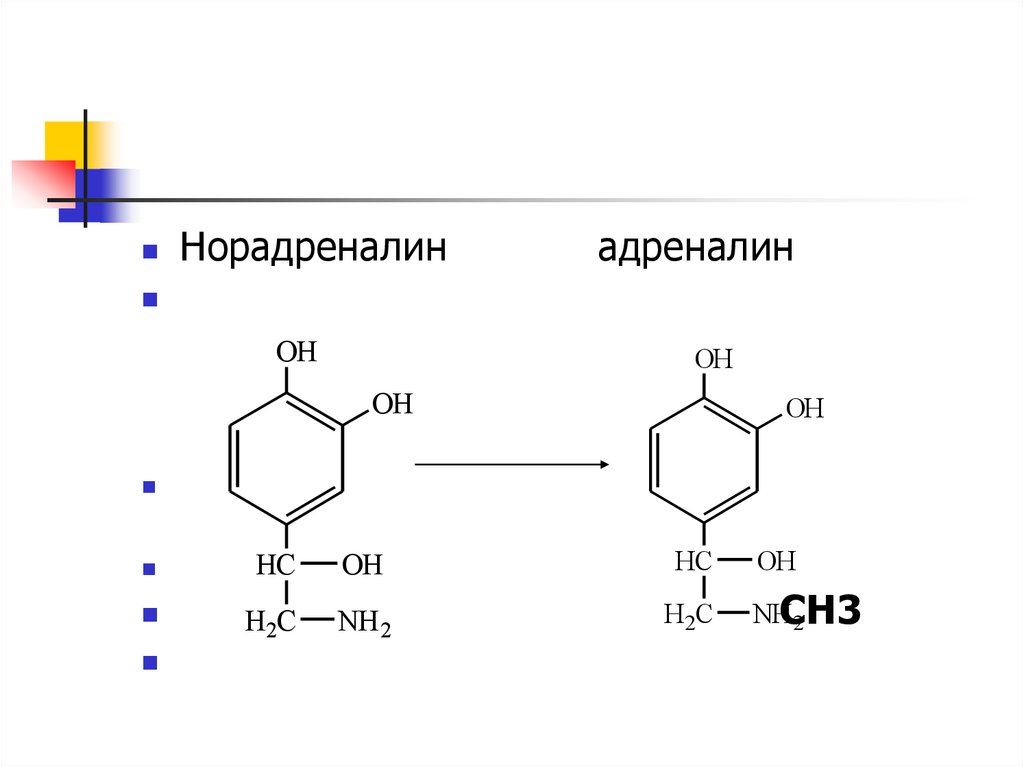
49.
Норадреналинадреналин
OH
OH
OH
OH
HC
ОН
HC
ОН
H2C
NH2
H2C
NHСН3
2
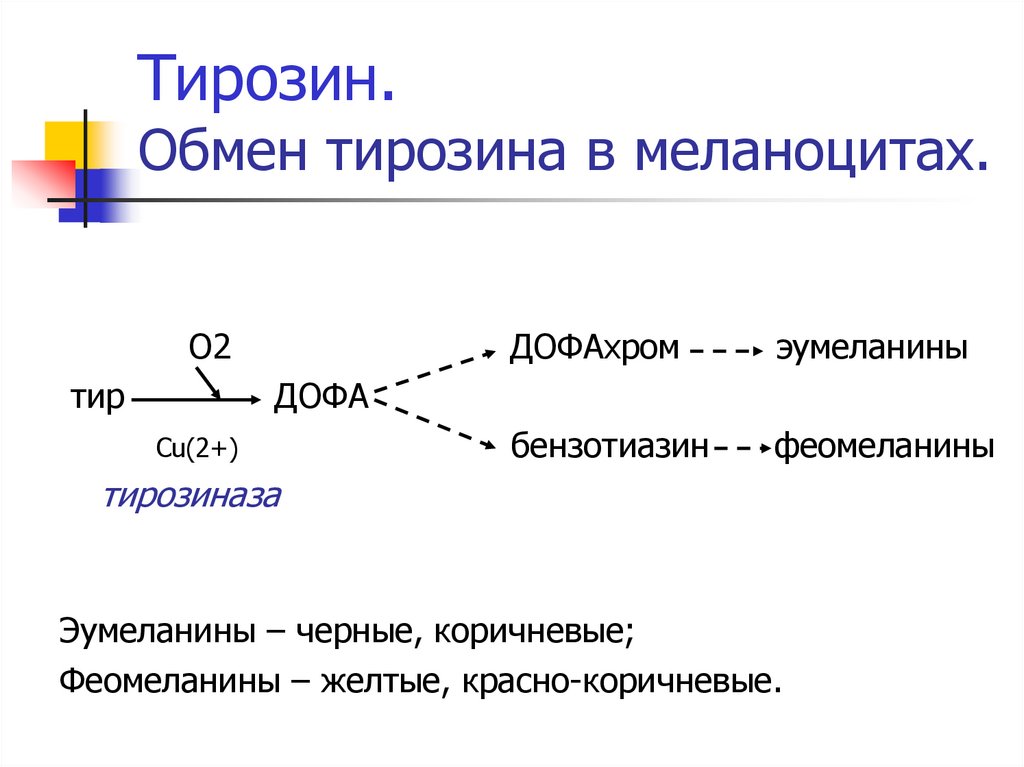
50. Тирозин. Обмен тирозина в меланоцитах.
О2тир
ДОФАхром
эумеланины
бензотиазин
феомеланины
ДОФА
Cu(2+)
тирозиназа
Эумеланины – черные, коричневые;
Феомеланины – желтые, красно-коричневые.
51. Обмен до АцАцКоА и Фумарата. Алкаптонурия
Тирозинх
п-гидроксифенилпируват
Гомогентизиновая кислота
АцАцКоА + фумарат
отсутствует фермент диоксигеназа
гомогентизиновой кислоты
52. Нарушения обмена тирозина.
Болезнь Паркинсона – развивается приснижении активности
тирозинмонооксигеназы и ДОФАдекарбоксилазы (частота 1:200 среди
людей старше 60 лет). Сопровождается
акинезией, регидностью и тремором;
Альбинизм – развивается при
наследственном дефекте тирозиназы
(1:20000). Проявляется отсутствием
пигментации кожи, сетчатки глаз и волос;
53. Нарушения обмена тирозина.
Болезнь Паркинсона – развивается приснижении активности
тирозинмонооксигеназы и ДОФАдекарбоксилазы (частота 1:200 среди
людей старше 60 лет). Сопровождается
акинезией, регидностью и тремором;
Альбинизм – развивается при
наследственном дефекте тирозиназы
(1:20000). Проявляется отсутствием
пигментации кожи, сетчатки глаз и волос;
54. Нарушения обмена тирозина.
Алкаптонурия – развивается при дефекте диоксигеназыгомогентизиновой кислоты. Клиническим проявлением является
потемнение мочи на воздухе, охроноз, артрит;
Тирозинемии:
I-типа(тирозиноз) – развивается при дефекте
фермента фумарилацетоацетатгидролазы;
II-типа(синдром РихнераХанхорта) – развивается при дефекте фермента
тирозинаминотрансферазы;
тирозинемия
новорожденных(кратковременная) - возникает в
результате понижения активности
n-гидроксифенилпируватдиоксигеназы, превращающего
n-гидроксифенилпируват в гомогентизиновую кислоту.
55. обмен триптофана
Незаменимая АК для человека и животных.Является предшественником ряда важных
биологически активных веществ, в частности
серотонина и рибонуклеотида никотиновой
кислоты.
NH 2
C
H2
N
H
CH
COOH
56.
серотонинТри
НАД+
мелатонин
57. кинурениновый путь
.NH 2
C
H2
N
H
CH
COOH
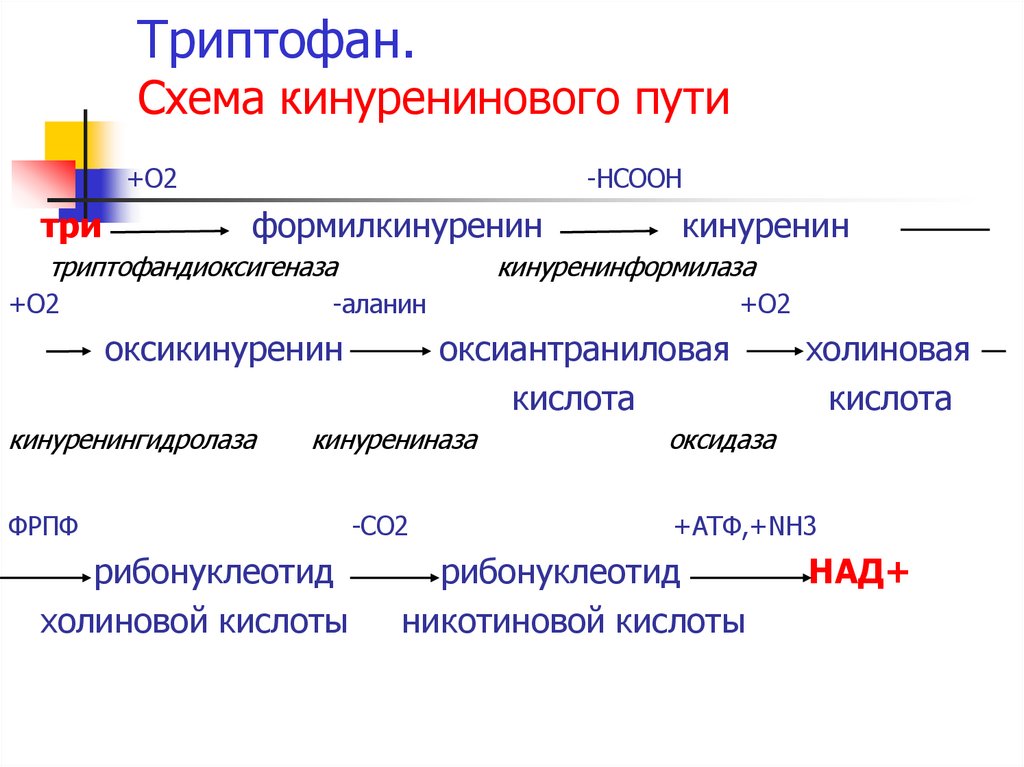
58. Триптофан. Схема кинуренинового пути
+О2три
-НСООН
формилкинуренин
триптофандиоксигеназа
+О2
кинуренин
кинуренинформилаза
-аланин
оксикинуренин
кинуренингидролаза
+О2
оксиантраниловая
кислота
кинурениназа
ФРПФ
рибонуклеотид
холиновой кислоты
-СО2
холиновая
кислота
оксидаза
+АТФ,+NH3
рибонуклеотид
никотиновой кислоты
НАД+
59. Триптофан.
Схема серотонинового пути:OH
три
O2
CН2 СН2 NH2
5-окситриптофан
H2O
НАДФН2 НАДФ
СО2
фенилгидроксилаза
CH3O
NH
серотонин
декарбоксилаза
СН2 СН2 NH CO CH3
NH
мелатонин
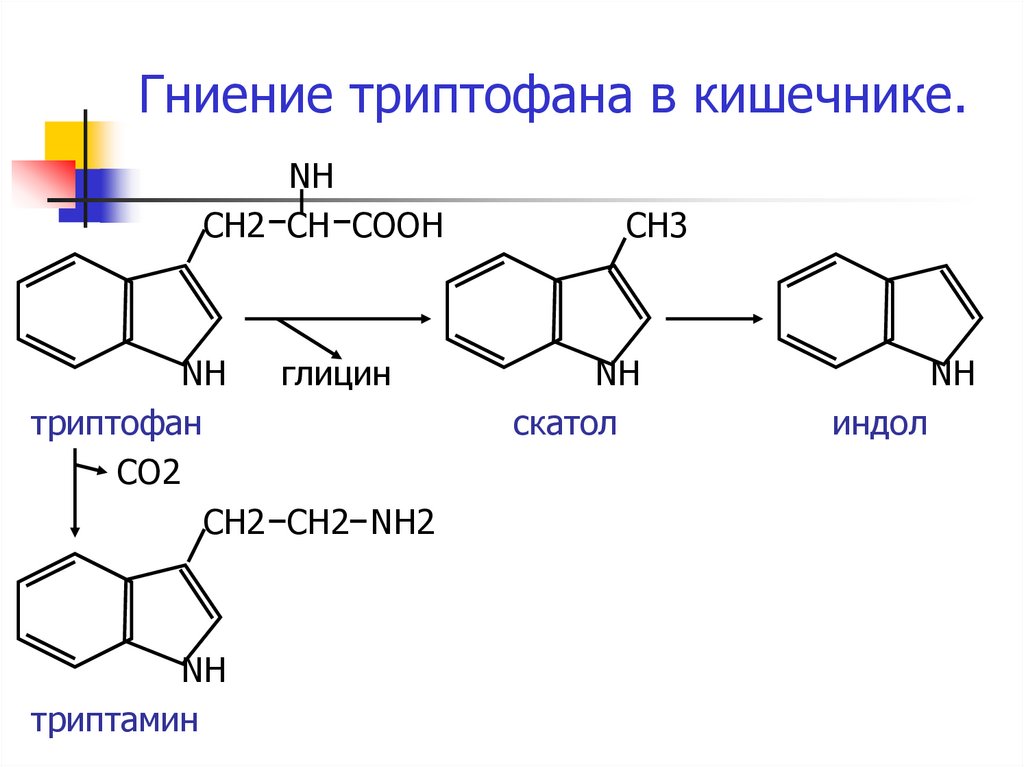
60. Гниение триптофана в кишечнике.
NHСН2 СН СООН
NH
глицин
триптофан
СО2
СН2 СН2 NH2
NH
триптамин
СН3
NH
скатол
NH
индол
61. Нарушения обмена триптофана.
Болезнь Хартнупа – происходит увеличениеконцентрации индолилацетата и
индолилацетилглутамина в моче. Возникает
метаболический блок связанный с первой
реакцией нормального пути обмена триптофана,
т.е. превращение его в формилкенуренин;
Наследственный «порок» обмена
триптофана – болезнь «моча с запахом
кленового сиропа» - происходит увеличение
индолилацетата в моче.






























 biology
biology








