Similar presentations:
Индивидуальные пути обмена аминокислот (1 занятие)
1.
ИНДИВИДУАЛЬНЫЕ ПУТИОБМЕНА АМИНОКИСЛОТ
(первое занятие)
2. ПЛАН ЛЕКЦИИ
1. Биологическая роль серина и глицина.2. Биологическая роль серосодержащих
аминокислот.
3. Значение метионина как донора метильной
группы для синтеза различных соединений.
4. Биологическая роль триптофана, гистидина и
аргинина.
5. Врожденные нарушения обмена
серосодержащих аминокислот.
3.
Гликогенные аминокислоты образуют пируват идругие промежуточные продукты ОПК (α-кетоглутарат,
сукцинил-КоА, фумарат, оксалоацетат), превращаются в
оксалоацетат и используются в процессе глюконеогенеза
Кетогенные аминокислоты (Лиз, Лей) превращаются
в ацетил-КоА и могут быть источником кетоновых тел
(ацетоацетат, β-гидроксибутират)
Гликокетогенные, или смешанные, аминокислоты
распадаются на два продукта – определенные метаболит
ОПК и ацетил-КоА (Иле) или ацетоацетат (Три, Фен,
Тир) и могут использоваться для синтеза как глюкозы,
так и кетоновых тел
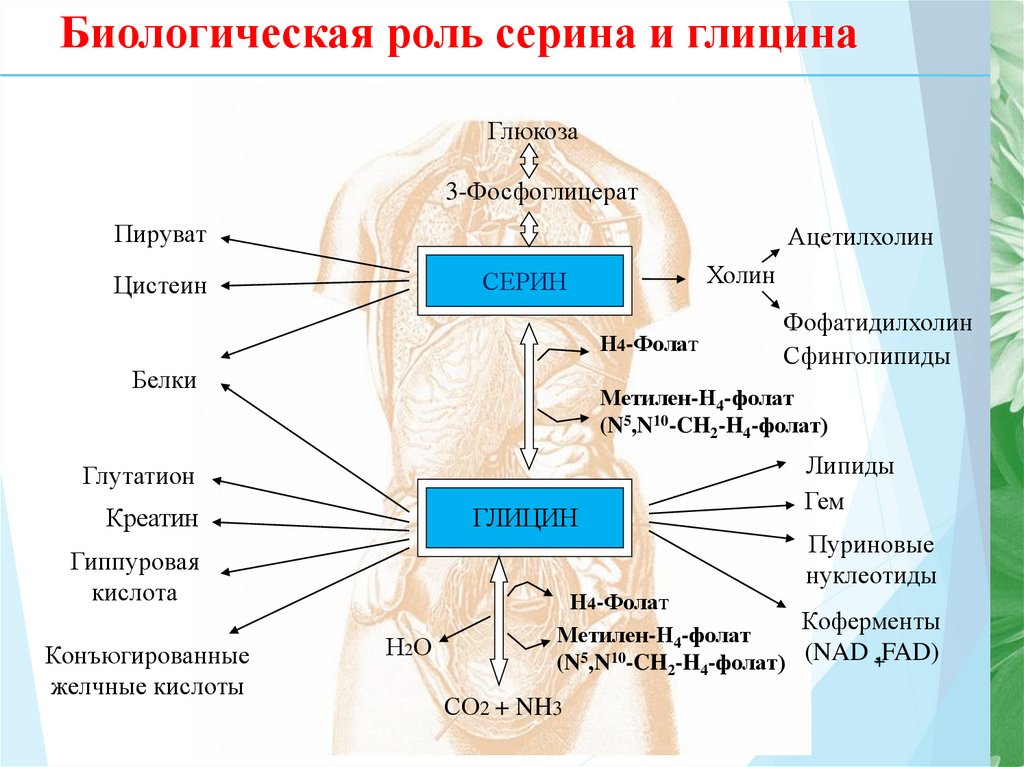
4. Биологическая роль серина и глицина
Глюкоза3-Фосфоглицерат
Пируват
Ацетилхолин
Холин
СЕРИН
Цистеин
Н4-Фолат
Белки
Метилен-Н4-фолат
(N5,N10-CH2-H4-фолат)
Глутатион
Креатин
ГЛИЦИН
Гиппуровая
кислота
Конъюгированные
желчные кислоты
Фофатидилхолин
Сфинголипиды
Н2О
Липиды
Гем
Пуриновые
нуклеотиды
Н4-Фолат
Коферменты
Метилен-Н4-фолат
(N5,N10-CH2-H4-фолат) (NAD +,FAD)
СО2 + NH3
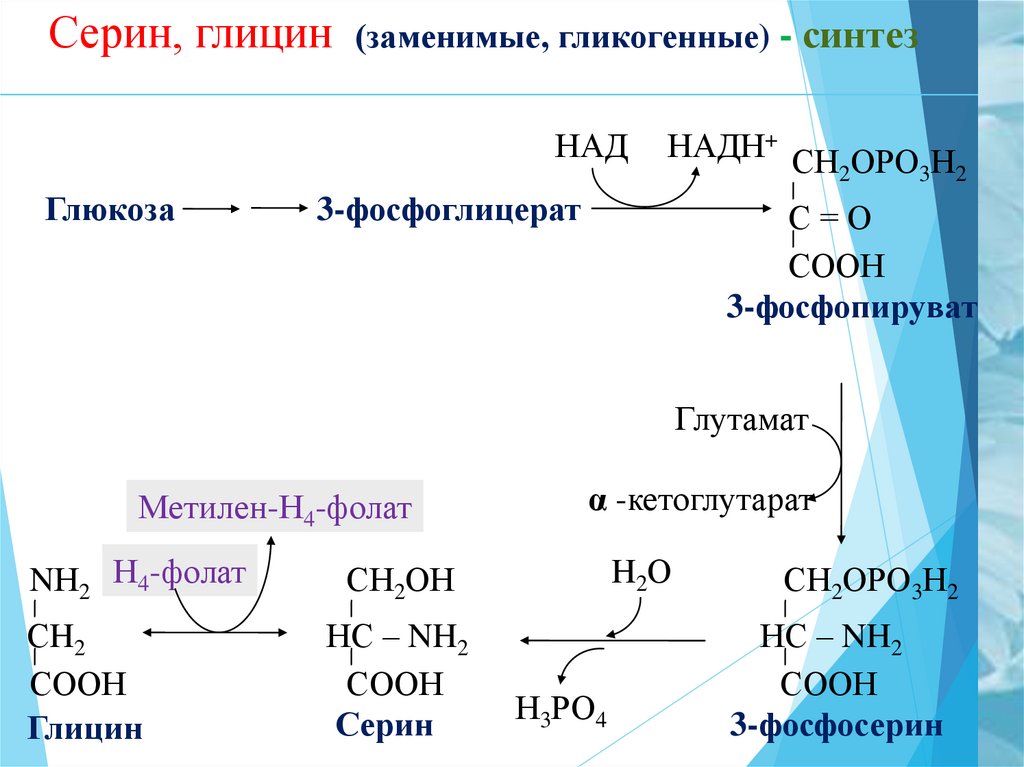
5. Серин, глицин (заменимые, гликогенные) - синтез
НАДНАДН+ СН ОРО Н
2
Глюкоза
3-фосфоглицерат
3
2
С=О
СООН
3-фосфопируват
Глутамат
Метилен-Н4-фолат
NН2 Н4-фолат
СН2ОН
СH2
СООН
Глицин
НС – NH2
СООН
Серин
α -кетоглутарат
H2О
Н3РО4
СН2ОРО3Н2
НС – NH2
СООН
3-фосфосерин
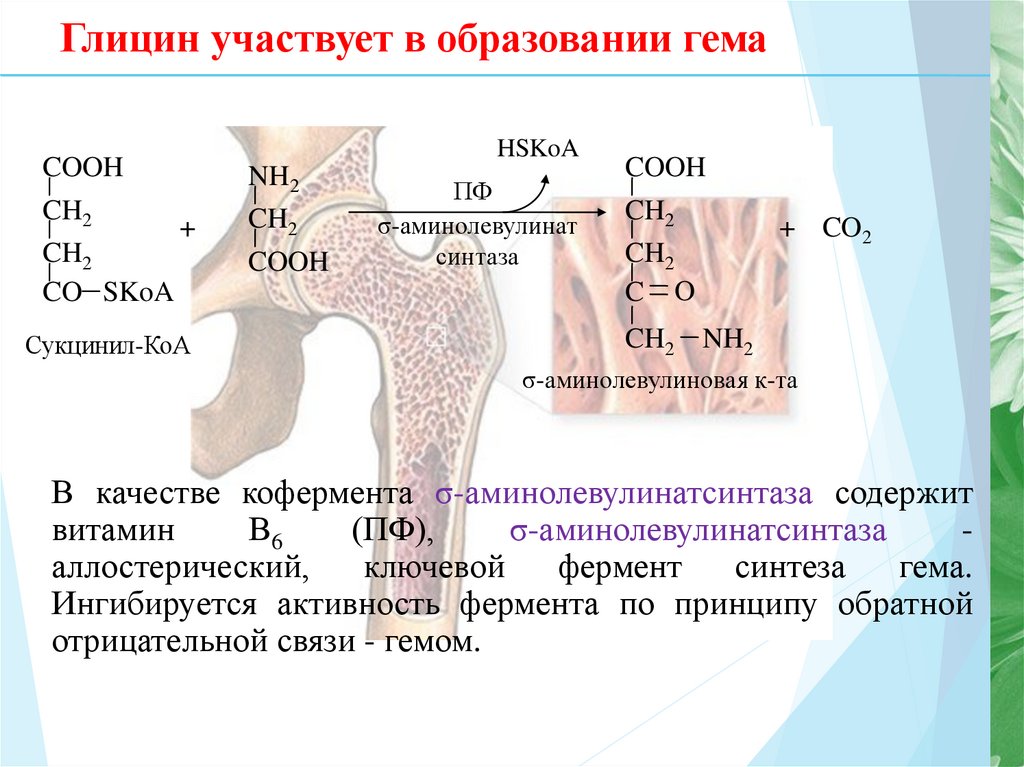
6. Глицин участвует в образовании гема
COOHCH2
+
CH2
CO SKoA
Сукцинил-КоА
HSKoA
NH2
CH2
COOH
ПФ
σ-аминолевулинат
синтаза
COOH
CH2
CH2
C O
+ CO2
CH2 NH2
σ-аминолевулиновая к-та
В качестве кофермента σ-аминолевулинатсинтаза содержит
витамин
В6
(ПФ),
σ-аминолевулинатсинтаза
аллостерический,
ключевой
фермент
синтеза
гема.
Ингибируется активность фермента по принципу обратной
отрицательной связи - гемом.
7.
Синтез креатинаКреатин используется в мышцах и мозге для образования креатинфосфата высокоэнергетического соединения.
1. В почках образуется гуанидинацетат:
NH2
C=NH
NH
(CH2)3
CH-NH2
COOH
Аргинин
+
NH2
CH2
COOH
Глицин
Глицинамидинотрансфераза
NH2
(CH2)3
CH-NH2
COOH
Орнитин
+
NH2
C=NH
NH
CH2
COOH
Гуанидинацетат
8.
2. Гунидинацетат с кровотоком поступаетв печень, где образуется креатин
NН2
NН2
C = NH
NH
CH2
SAM
CH3
Гуанидинацетатметилтрансфераза
COOH
Гуанидинацетат
C = NH
N – CH3
CH2
COOH
Креатин
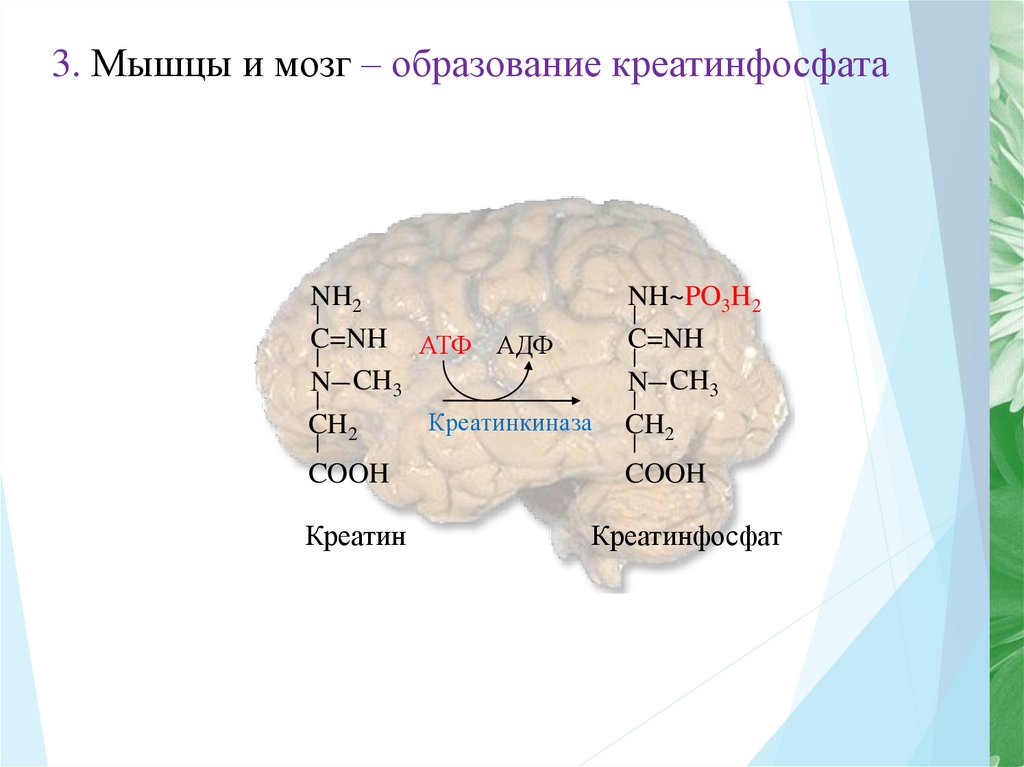
9.
3. Мышцы и мозг – образование креатинфосфатаNH2
C=NH АТФ АДФ
N CH3
CH2
COOH
Креатин
NH~PO3H2
C=NH
N CH3
Креатинкиназа
CH2
COOH
Креатинфосфат
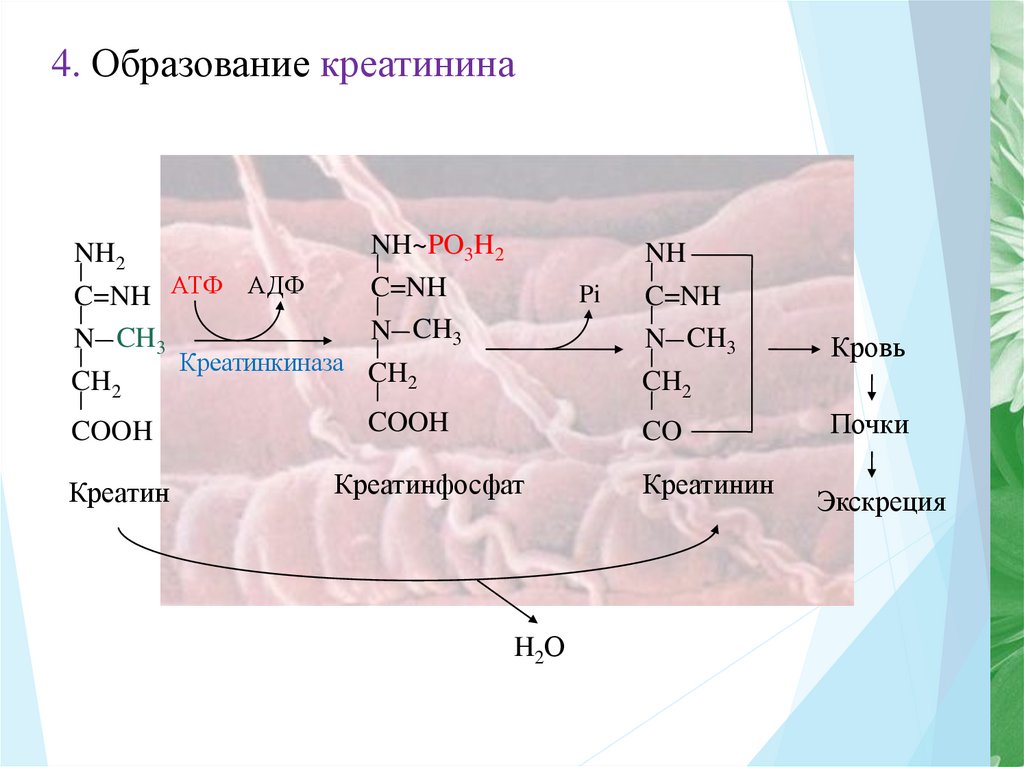
10.
4. Образование креатининаNH2
C=NH АТФ АДФ
N CH3
CH2
COOH
Креатин
NH~PO3H2
C=NH
N CH3
Pi
Креатинкиназа CH
2
NH
C=NH
N CH3
Кровь
CH2
COOH
CO
Креатинфосфат
H2О
Креатинин
Почки
Экскреция
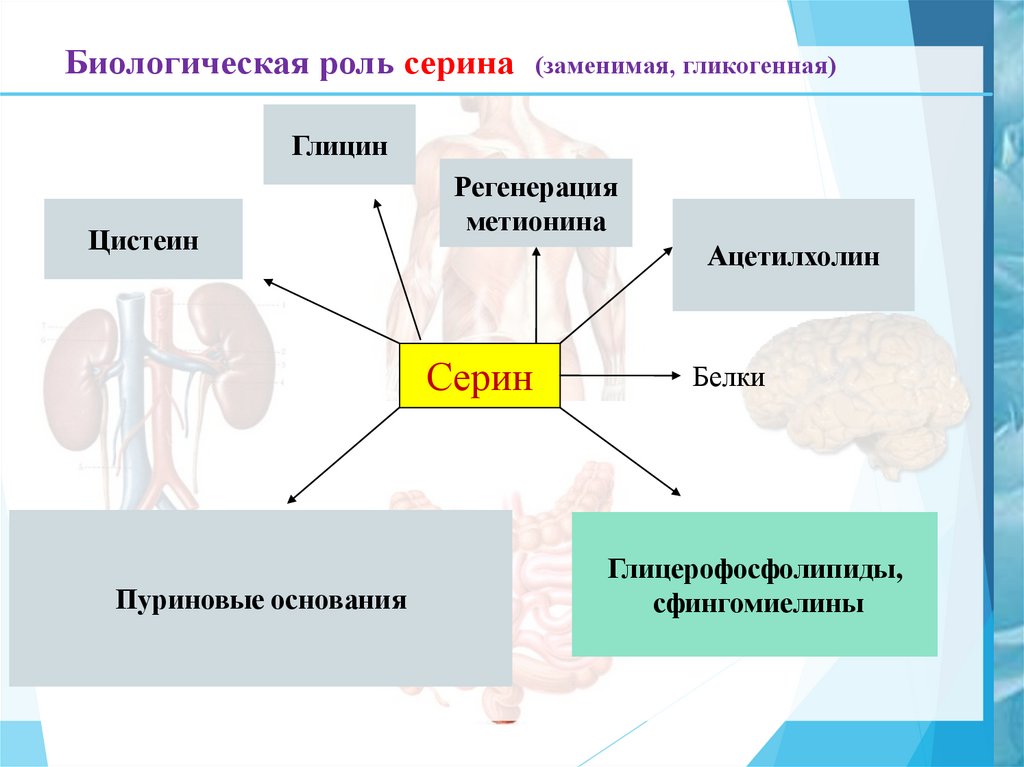
11. Биологическая роль серина (заменимая, гликогенная)
ГлицинЦистеин
Регенерация
метионина
Ацетилхолин
Серин
Пуриновые основания
Белки
Глицерофосфолипиды,
сфингомиелины
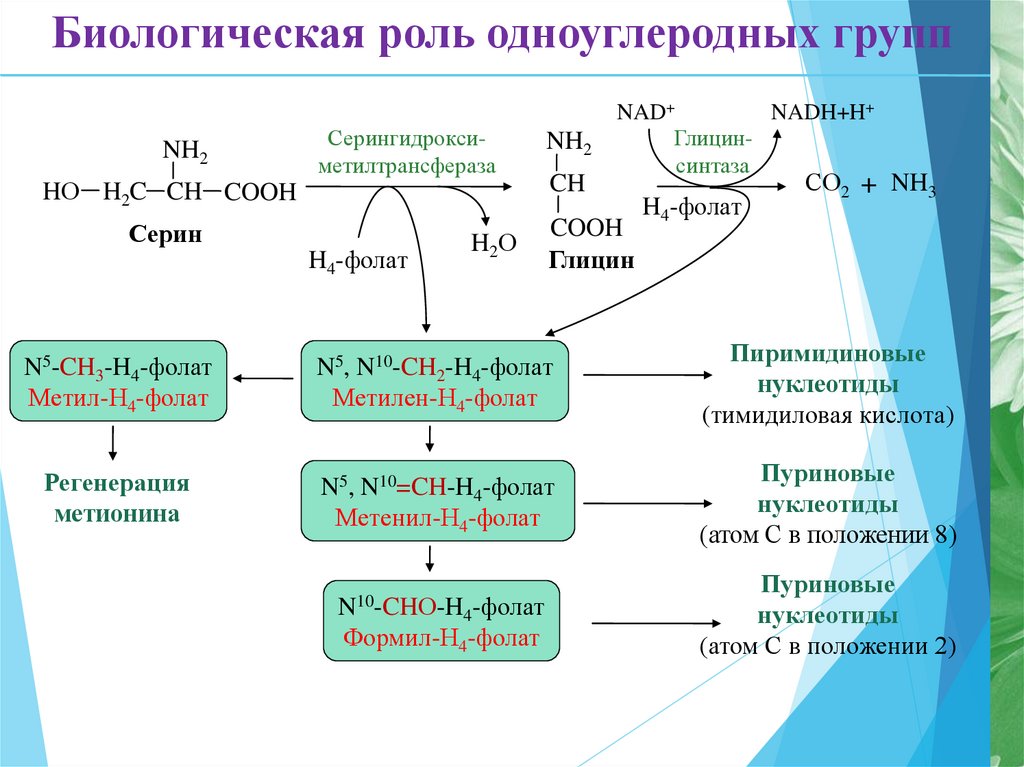
12. Биологическая роль одноуглеродных групп
NH2Серингидроксиметилтрансфераза
HО H2C CH COOH
Серин
H4-фолат
H2О
NH2
CH
NAD+
NADH+H+
Глицинсинтаза
COOH
Глицин
H4-фолат
СО2 + NH3
N5-CH3-H4-фолат
Метил-Н4-фолат
N5, N10-CH2-H4-фолат
Метилен-Н4-фолат
Пиримидиновые
нуклеотиды
(тимидиловая кислота)
Регенерация
метионина
N5, N10=CH-H4-фолат
Метенил-Н4-фолат
Пуриновые
нуклеотиды
(атом С в положении 8)
N10-CHО-H4-фолат
Формил-Н4-фолат
Пуриновые
нуклеотиды
(атом С в положении 2)
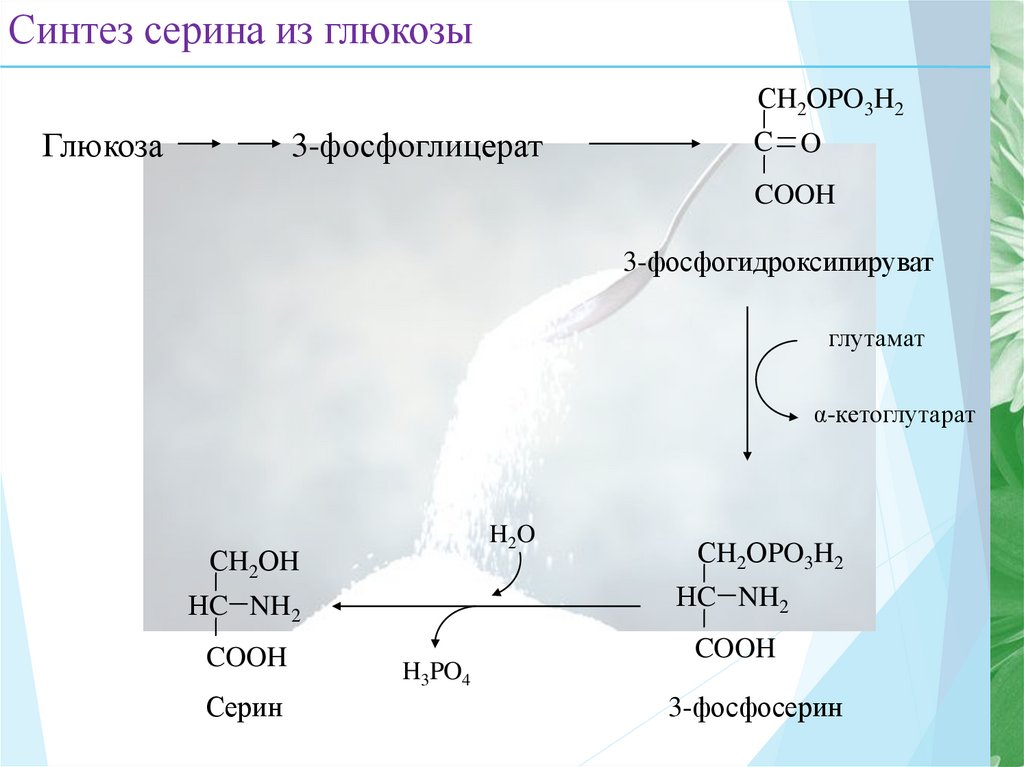
13. Синтез серина из глюкозы
Глюкоза3-фосфоглицерат
СH2ОPO3H2
C O
COOH
3-фосфогидроксипируват
глутамат
α-кетоглутарат
H2O
СH2ОH
СH2ОPO3H2
НC NH2
НC NH2
COOH
COOH
Серин
H3PO4
3-фосфосерин
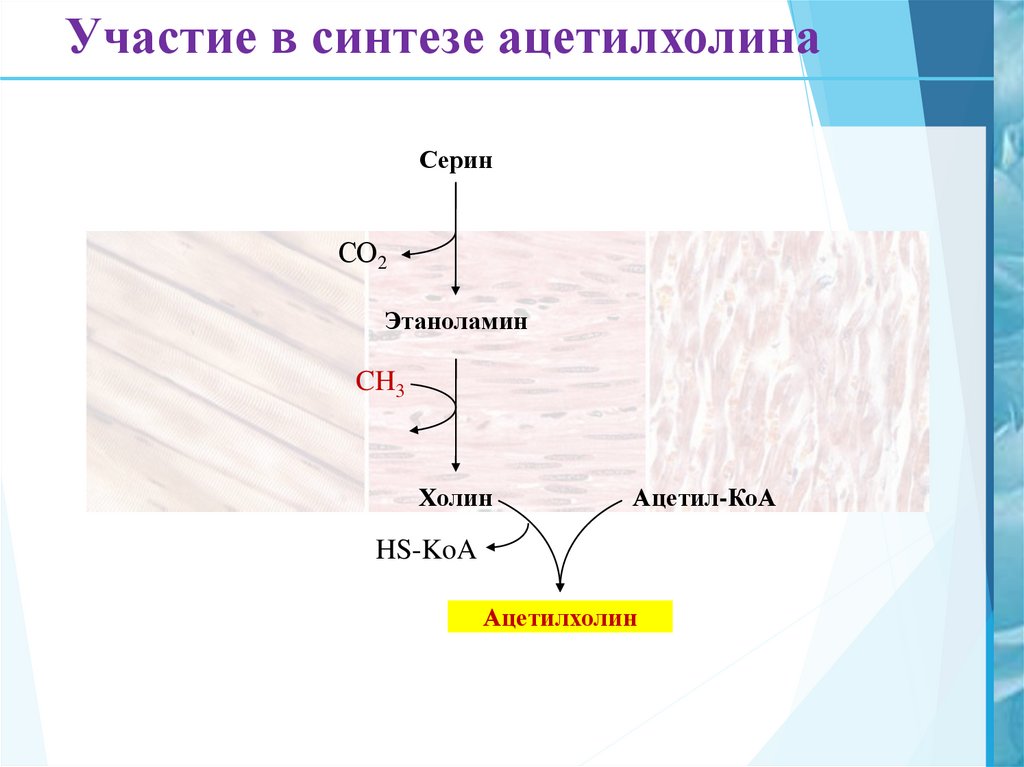
14. Участие в синтезе ацетилхолина
СеринСО2
Этаноламин
CH3
Холин
Ацетил-КоА
HS-KoA
Ацетилхолин
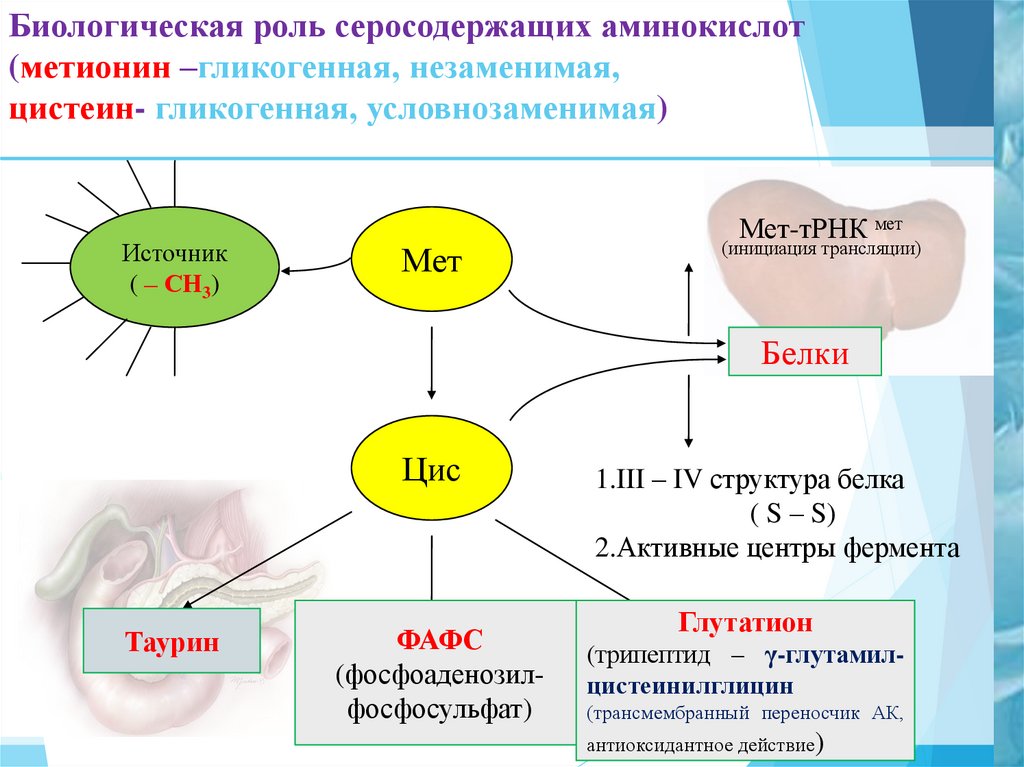
15. Биологическая роль серосодержащих аминокислот (метионин –гликогенная, незаменимая, цистеин- гликогенная, условнозаменимая)
Источник( – СН3)
Мет
Мет-тРНК мет
(инициация трансляции)
Белки
Цис
Таурин
ФАФС
(фосфоаденозилфосфосульфат)
1.III – IV структура белка
( S – S)
2.Активные центры фермента
Глутатион
(трипептид – γ-глутамилцистеинилглицин
(трансмембранный переносчик АК,
антиоксидантное действие)
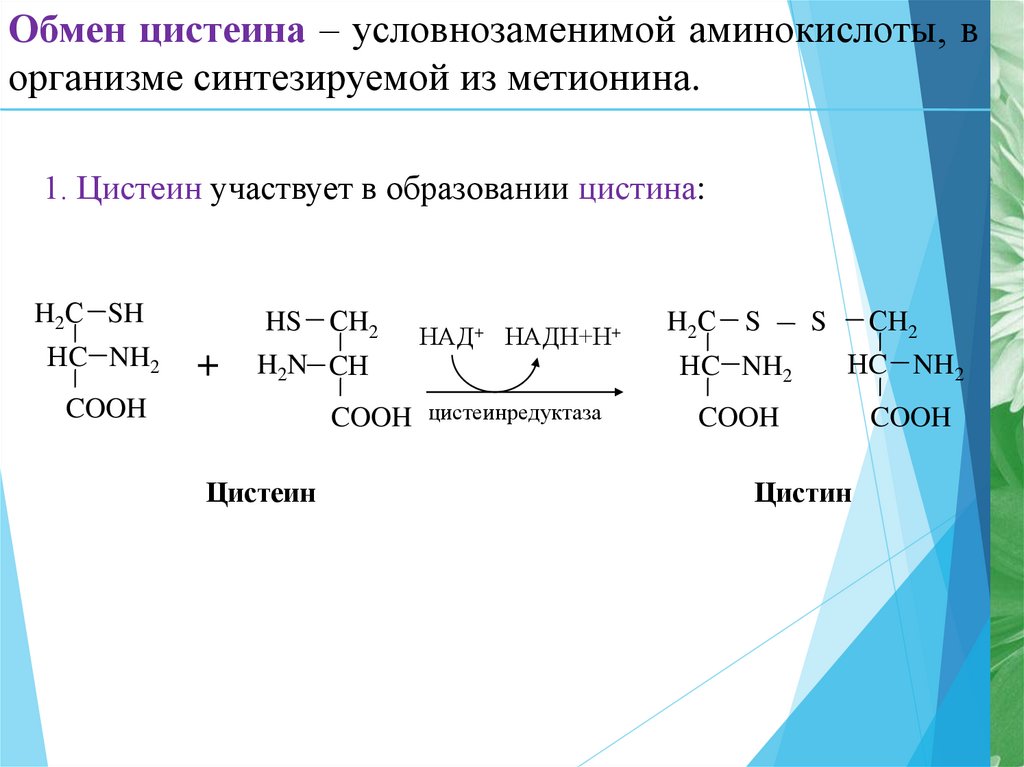
16.
Обмен цистеина – условнозаменимой аминокислоты, ворганизме синтезируемой из метионина.
1. Цистеин участвует в образовании цистина:
H2С SH
НC NH2
+
HS СH2
H2N CН
COOH
НАД+ НАДH+H+
COOH цистеинредуктаза
Цистеин
H2С
НC NH2
СH2
НC NH2
COOH
COOH
S
S
Цистин
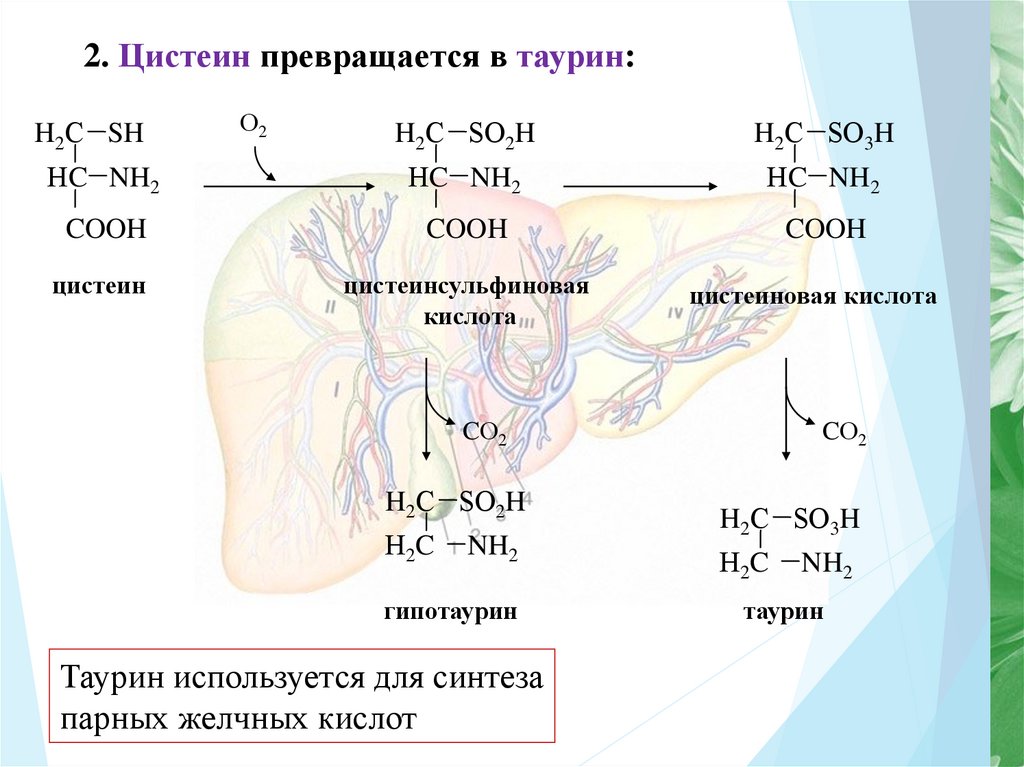
17.
2. Цистеин превращается в таурин:H2С SH
О2
H2С SО2H
H2С SО3H
НC NH2
НC NH2
НC NH2
COOH
COOH
COOH
цистеин
цистеинсульфиновая
кислота
цистеиновая кислота
CО2
H2С SО2H
Н2C
NH2
гипотаурин
Таурин используется для синтеза
парных желчных кислот
CО2
H2С SО3H
Н 2C
NH2
таурин
18.
3. При образовании цистина возникает дисульфидная связь S– S между двумя полипептидными цепями, что способствует
стабилизации третичной структуры белка.
4. Цистеин входит в состав трипептида глутатиона.
Глутатион обеспечивает сохранение ферментов в активной
восстановительной
форме.
Глутатион
участвует
в
ингибировании белков, например, инсулина.
5. Цистеин входит в состав активных центров ферментов.
19.
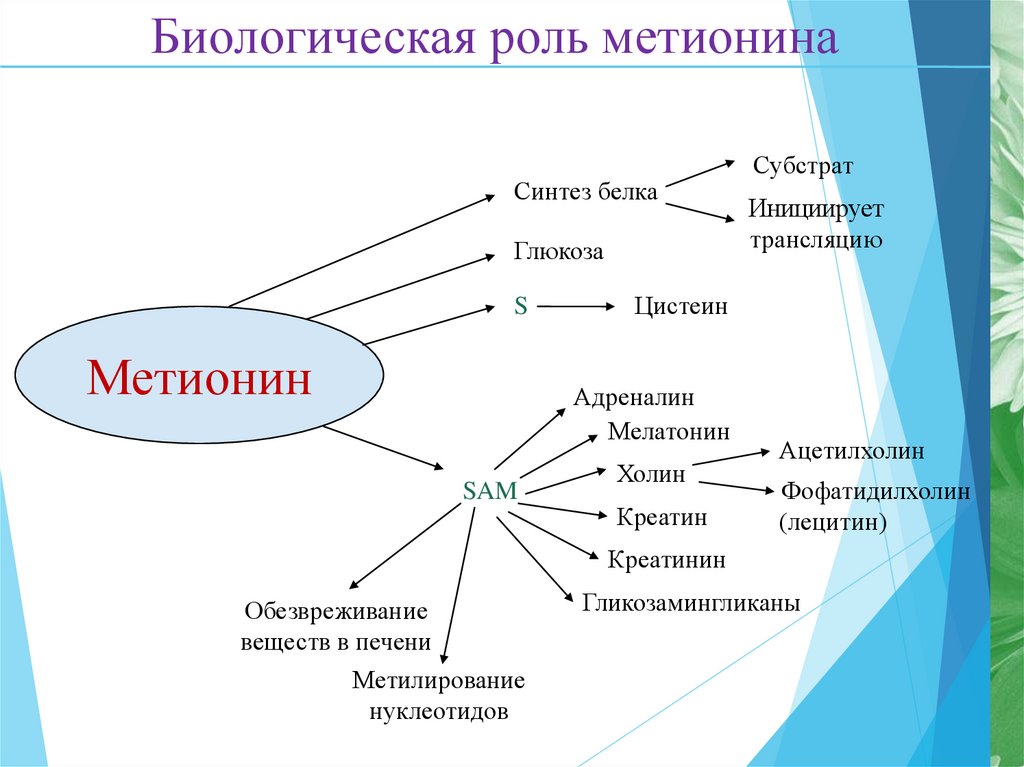
Биологическая роль метионинаСинтез белка
Глюкоза
S
Метионин
Инициирует
трансляцию
Цистеин
Адреналин
Мелатонин
SAM
Субстрат
Холин
Креатин
Ацетилхолин
Фофатидилхолин
(лецитин)
Креатинин
Обезвреживание
веществ в печени
Метилирование
нуклеотидов
Гликозамингликаны
20.
Обмен метионина – незаменимая аминокислота.1. Метионин является источником одноуглеродного
радикала – метила, который используется в реакциях
трансметилирования.
Донором метильной группы в реакциях трансметилирования служит производное метионина S – аденозилметионин.
2. Метионин участвует в синтезе креатина. Синтез креатина
происходит в почках и печени.
3. Метионин участвует в реакциях трансметилирования в
синтезе: адреналина, мелатонина, азотистых оснований.
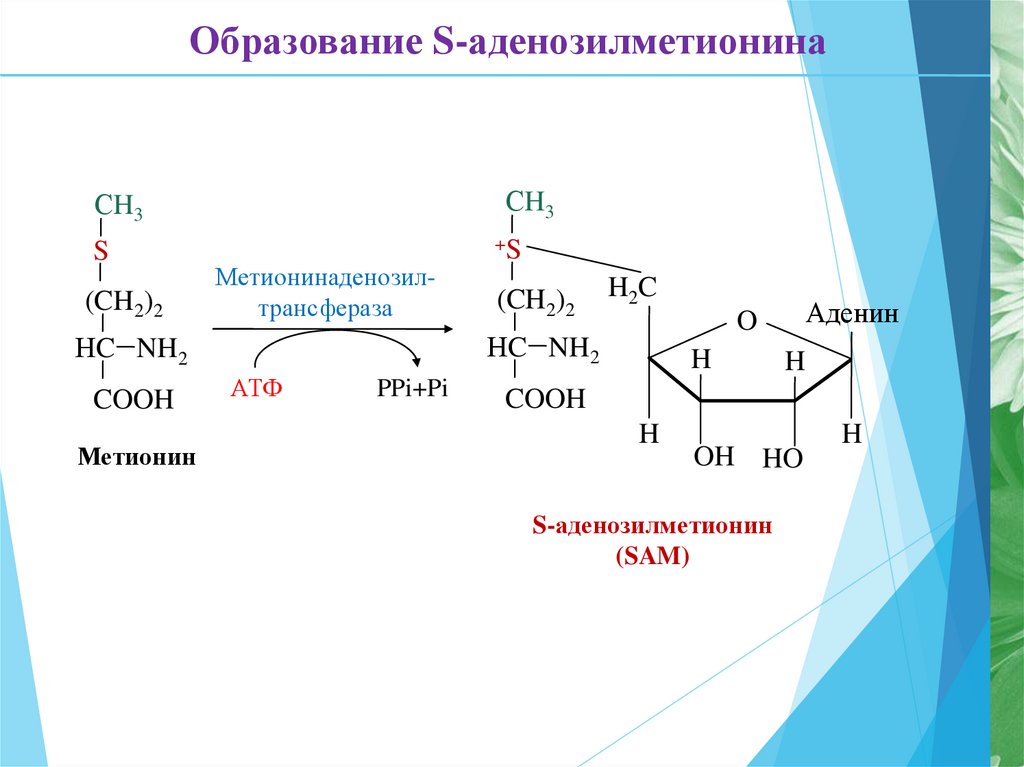
21.
Образование S-аденозилметионинаСH3
СH3
S
+S
(CH2)2
Метионинаденозилтрансфераза
Метионин
H2C
АТФ
PPi+Pi
Аденин
O
НC NH2
НC NH2
COOH
(CH2)2
H
H
COOH
H
OH HO
S-аденозилметионин
(SAM)
H
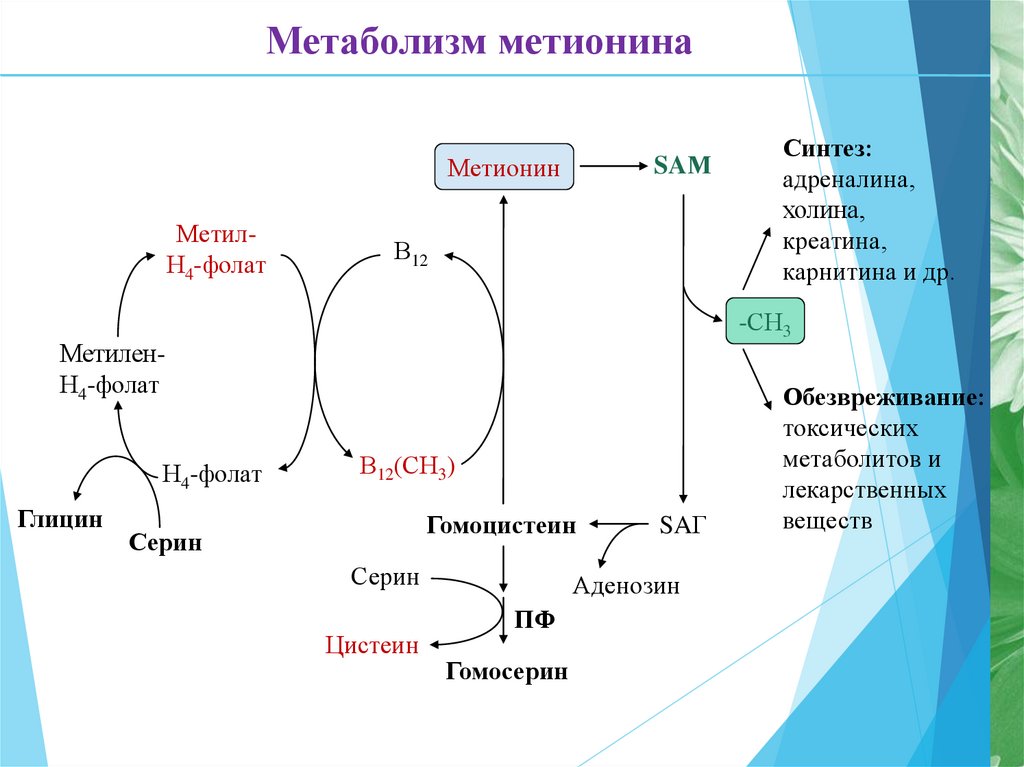
22.
Метаболизм метионинаМетионин
МетилН4-фолат
SAМ
В12
-СН3
МетиленН4-фолат
Н4-фолат
Глицин
Синтез:
адреналина,
холина,
креатина,
карнитина и др.
В12(СН3)
Гомоцистеин
Серин
Серин
Цистеин
SAГ
Аденозин
ПФ
Гомосерин
Обезвреживание:
токсических
метаболитов и
лекарственных
веществ
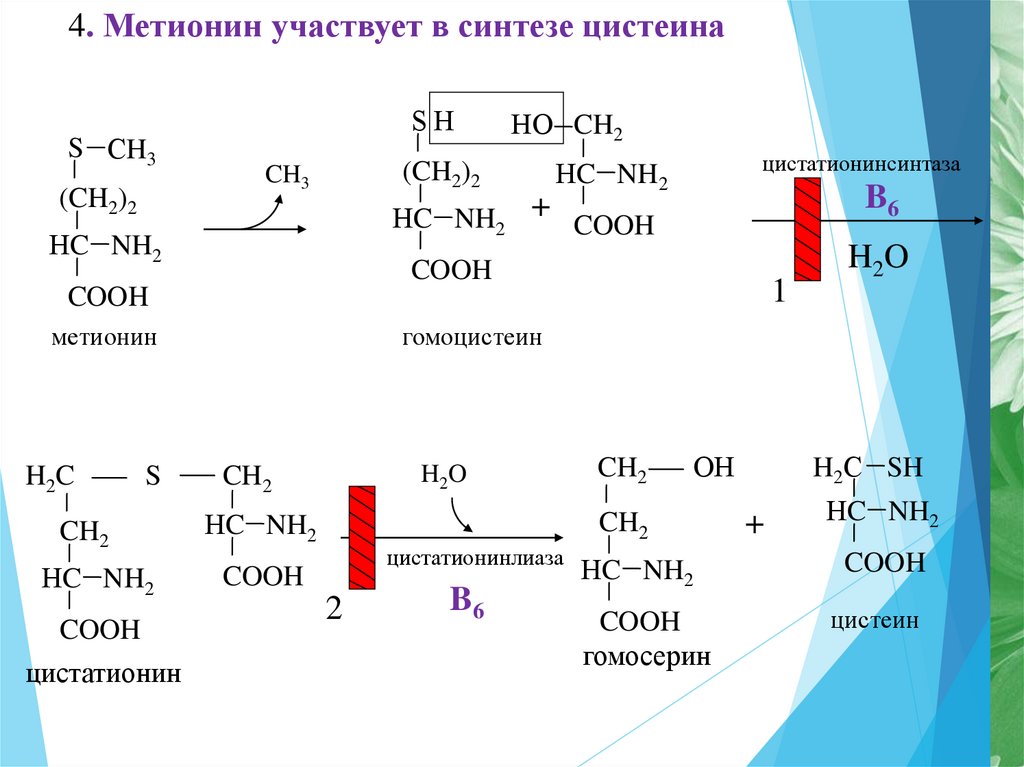
23.
4. Метионин участвует в синтезе цистеинаS СH3
(CH2)2
SН
НО CH2
(CH2)2
CH3
НC NH2
НC NH2
+
цистатионинсинтаза
НC NH2
B6
COOH
COOH
1
COOH
метионин
H2C
S
гомоцистеин
H2O
CH2
CH2
НC NH2
НC NH2
COOH
COOH
цистатионин
H2O
CH2
ОН
CH2
цистатионинлиаза
2
B6
H2С SH
+
НC NH2
НC NH2
COOH
COOH
гомосерин
цистеин
24.
В обмене метионина на 2-х этапах возможнынарушения, т. е. возникновение блоков, приводящих к
развитию патологии.
Выделяют 2 причины возникновения блоков:
1. Наследственная
недостаточность
ферментов,
участвующих в обмене.
2. Недостаточность (гиповитаминоз) В6.
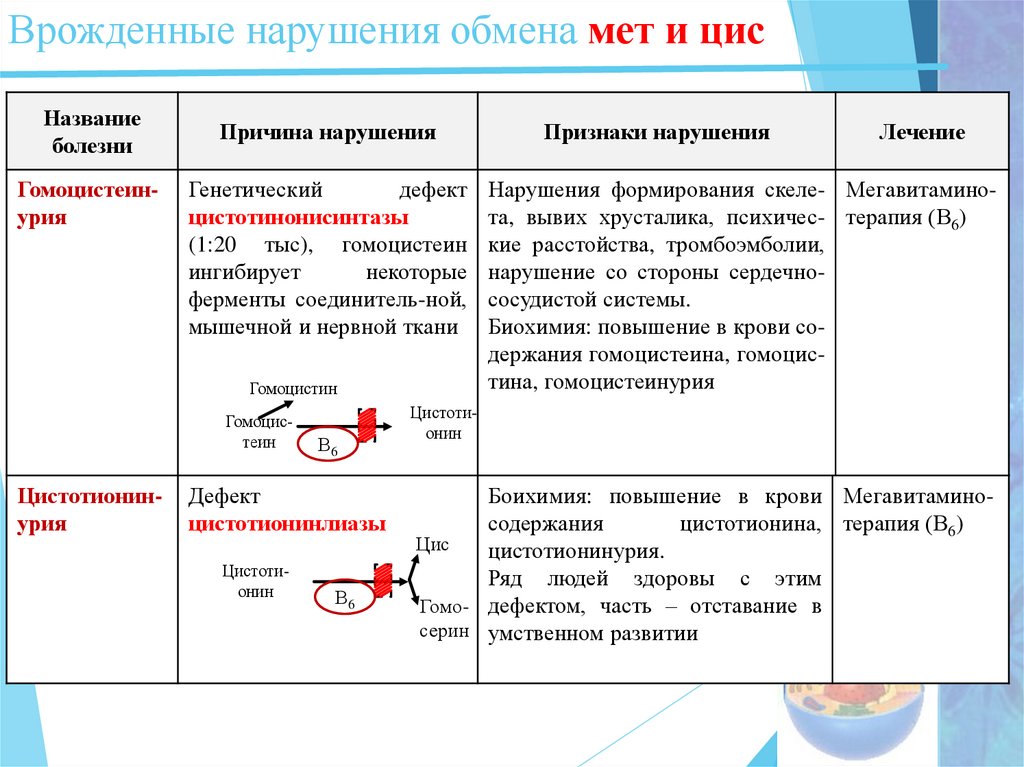
25. Врожденные нарушения обмена мет и цис
Названиеболезни
Гомоцистеинурия
Причина нарушения
Генетический
дефект
цистотинонисинтазы
(1:20 тыс), гомоцистеин
ингибирует
некоторые
ферменты соединитель-ной,
мышечной и нервной ткани
Гомоцистин
Гомоцистеин
Цистотионинурия
В6
Дефект
цистотионинлиазы
Цистотионин
В6
Признаки нарушения
Лечение
Нарушения формирования скеле- Мегавитаминота, вывих хрусталика, психичес- терапия (В6)
кие расстойства, тромбоэмболии,
нарушение со стороны сердечнососудистой системы.
Биохимия: повышение в крови содержания гомоцистеина, гомоцистина, гомоцистеинурия
Цистотионин
Боихимия: повышение в крови Мегавитаминосодержания
цистотионина, терапия (В6)
Цис
цистотионинурия.
Ряд людей здоровы с этим
Гомо- дефектом, часть – отставание в
серин умственном развитии
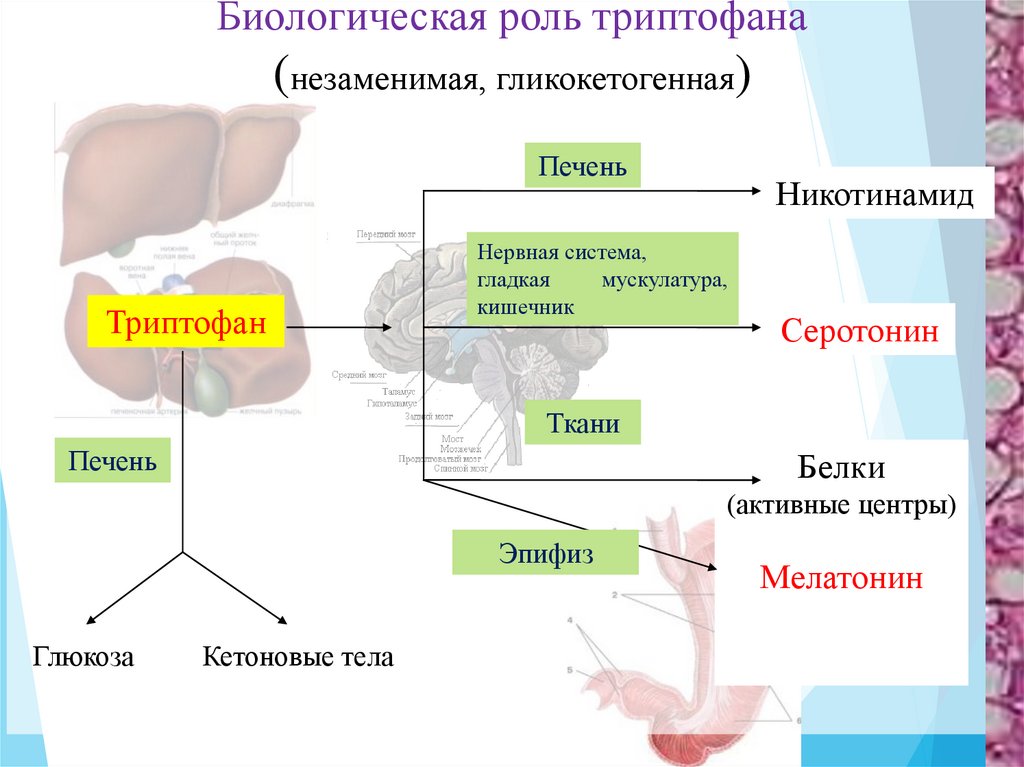
26.
Биологическая роль триптофана(незаменимая, гликокетогенная)
Печень
Триптофан
Никотинамид
Нервная система,
гладкая
мускулатура,
кишечник
Серотонин
Ткани
Печень
Белки
(активные центры)
Эпифиз
Глюкоза
Кетоновые тела
Мелатонин
27. Серотонин и его биологическая роль
1.Стимулирует сокращения гладкой
мускулатуры, перистальтику
кишечника;
2.
Оказывает сосудосуживающее
действием, регулирует АД, t,
дыхание;
3.
Обладает антидепрессивным
действием;
4.
Участвует в аллергической реакции;
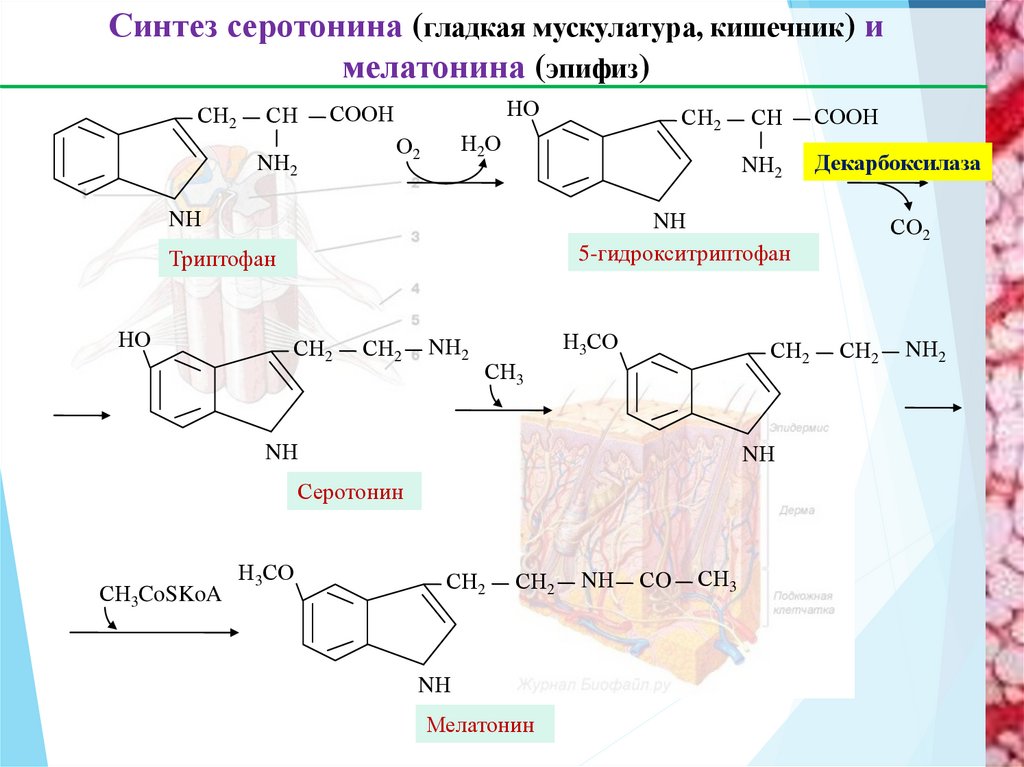
28.
Синтез серотонина (гладкая мускулатура, кишечник) имелатонина (эпифиз)
СН2
СН
НО
СООН
NН2
Н2О
О2
NН
СН2
СН2
NН2
Н3СО
СООН
NН2
Декарбоксилаза
СН2
СН3
NН
NН
Серотонин
СН3CoSKoA
СН
NН
5-гидрокситриптофан
Триптофан
НО
СН2
Н3СО
СН2
СН2
NН
Мелатонин
NН
СO
СН3
СО2
СН2
NН2
29.
Роль аргинина и орнитина в синтезебиологически активных молекул
Обмен аминокислоты аргинина связан с
реакциями орнитинового цикла, которые можно
рассматривать как путь синтеза аргинина. Под
действием аргиназы в цикле происходит распад
аргинина на орнитин и мочевину.
30.
Аргинин выполняет в организме важные функции:1. Используется в синтезе креатина, который в виде
креатинфосфата способен служить источником энергии для
работы мышц человека и млекопитающих.
2. В мышцах беспозвоночных аргининосукцинат выполняет
энергетическую функцию.
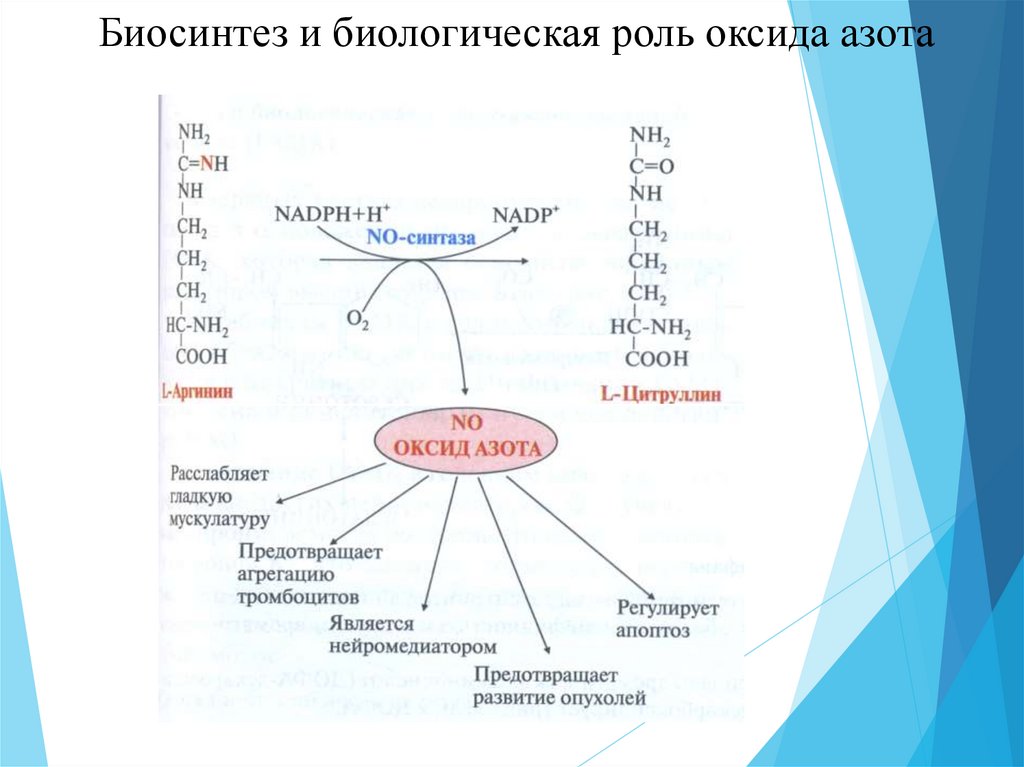
3. Аргинин служит источником NO в организме.
4. Аргинин служит предшественниеом орнитина, из которого
синтезируются полиамины.
31.
Гистидин (гликогенная, частично заменимая)Гистидин включается в два разных метаболических
пути (кроме синтеза белка):
- катаболизм до конечных продуктов;
- синтез гистамина.
В печени и коже гистидин подвергается дезаминированию
фермента
гистидазы
с
образованием
уроканиновой кислоты.
Наследственный дефект гистидазы вызывает накопление
гистидина и развитие гистидинемии, которая прявляется
задержкой в умственом и физическом развитии детей.
32. Биологическая роль гистамина
ГисГистамин
1.
Стимулирует секрецию желудочного сока, слюны;
2.
Повышает проницаемость капилляров, вызывает
отеки;
3.
Снижает АД, но увеличивает внутричерепное давление;
4.
Сокращает гладкую мускулатуру легких, вызывая
удушье;
5.
Участвует в воспалении – расширяет сосуды,
покраснение кожи, отёк;
6.
Вызывает аллергическую реакцию;
7.
Выполняет роль нейромедиатора;
8.
Медиатор боли.
33.
Биосинтез и биологическая роль оксида азота34.
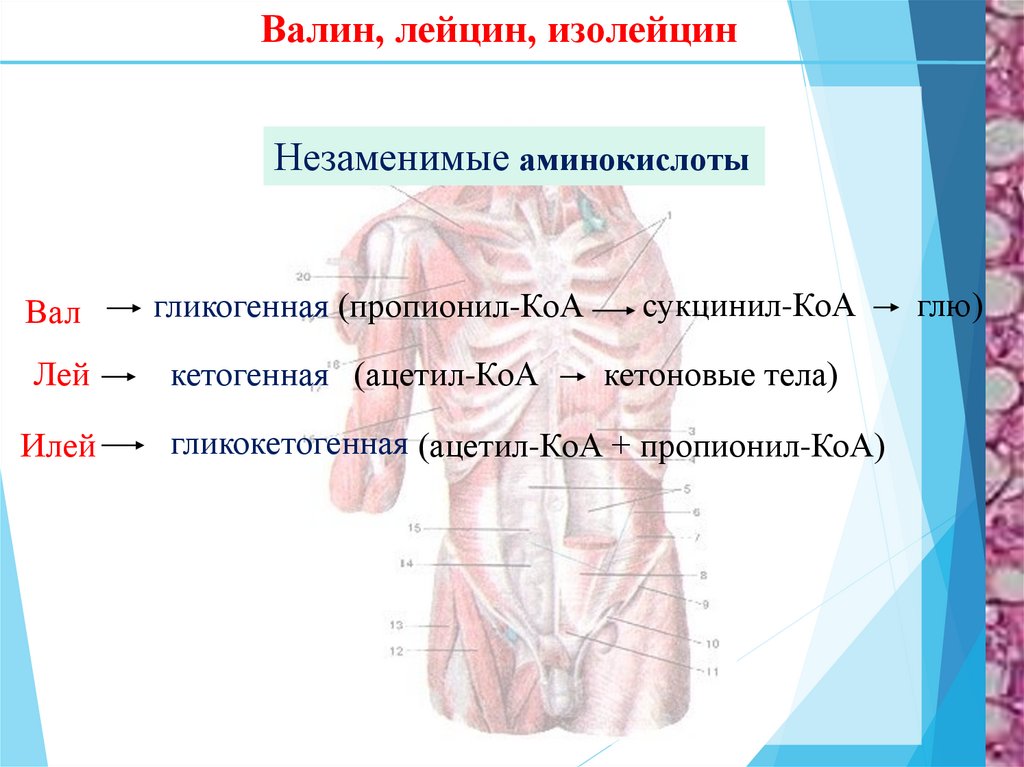
Валин, лейцин, изолейцинНезаменимые аминокислоты
сукцинил-КоА
Вал
гликогенная (пропионил-КоА
Лей
кетогенная (ацетил-КоА
Илей
гликокетогенная (ацетил-КоА + пропионил-КоА)
кетоновые тела)
глю)
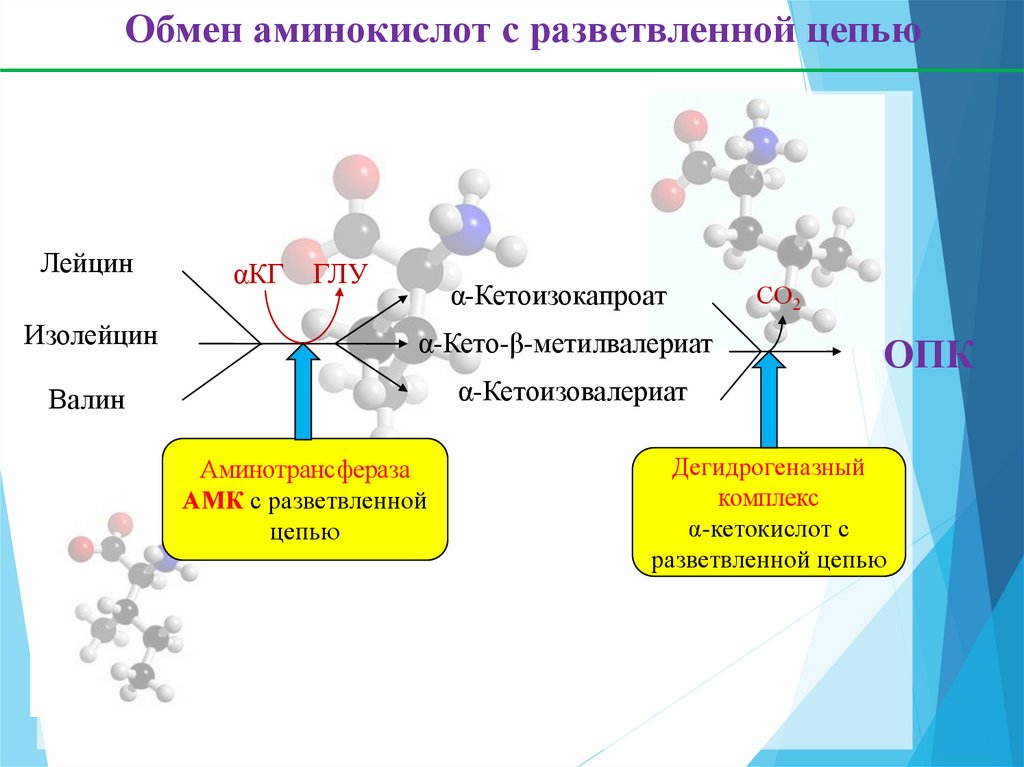
35.
Обмен аминокислот с разветвленной цепьюЛейцин
αКГ
ГЛУ
α-Кетоизокапроат
Изолейцин
α-Кето-β-метилвалериат
Валин
α-Кетоизовалериат
Аминотрансфераза
АМК с разветвленной
цепью
CО2
ОПК
Дегидрогеназный
комплекс
α-кетокислот с
разветвленной цепью
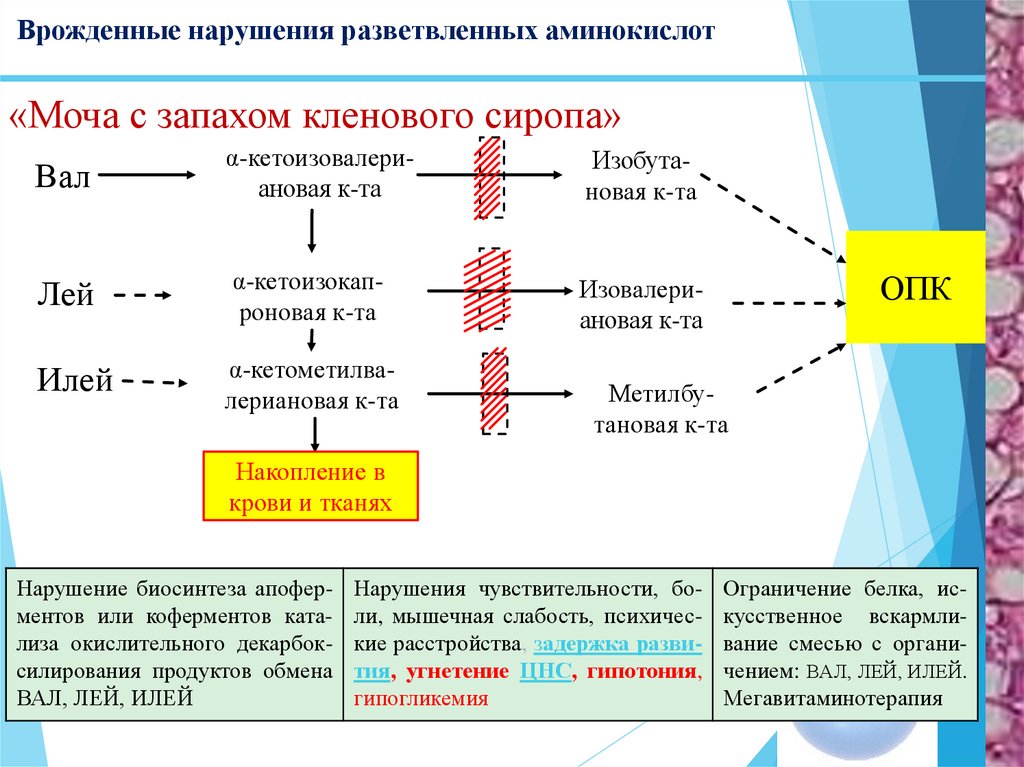
36. Врожденные нарушения разветвленных аминокислот
«Моча с запахом кленового сиропа»Вал
α-кетоизовалериановая к-та
Изобутановая к-та
Лей
α-кетоизокапроновая к-та
Изовалериановая к-та
Илей
α-кетометилвалериановая к-та
ОПК
Метилбутановая к-та
Накопление в
крови и тканях
Нарушение биосинтеза апоферментов или коферментов катализа окислительного декарбоксилирования продуктов обмена
ВАЛ, ЛЕЙ, ИЛЕЙ
Нарушения чувствительности, боли, мышечная слабость, психические расстройства, задержка развития, угнетение ЦНС, гипотония,
гипогликемия
Ограничение белка, искусственное вскармливание смесью с органичением: ВАЛ, ЛЕЙ, ИЛЕЙ.
Мегавитаминотерапия














 biology
biology








