Similar presentations:
Специфические пути обмена отдельных аминокислот. Патология. (Лекция 12)
1. ЛЕКЦИЯ № 12
ФГБОУ ВО УГМУ Минздрава РоссииКафедра биохимии
Дисциплина: Биохимия
ЛЕКЦИЯ № 12
Специфические пути обмена
отдельных аминокислот.
Патология
Лектор: Гаврилов И.В.
Факультет: лечебно-профилактический,
Курс: 2
Екатеринбург, 2016г
2. План:
Серин и глицин. Роль ТГФК и витамина В12 в этих процессах, их нарушение(мегалобластическая анемия).
Цистеин. Образование сульфат-иона, образование ФАФС.
Метионин. Образование S -аденозилметионина (SАМ), его участие в реакциях
трансметилирования. Ресинтез метионина, роль ТГФК и витамина В12 в этом
процессе. Связь обменов метионина и цистеина. Метионин как липотропное
вещество. Схема путей обмена глутаминовой и аспарагиновой кислот, их
биосинтез, участие в обезвреживании аммиака. Глутамин как донор
аминогруппы при синтезе ряда соединений.
Образование и использование в организме ГАМК и ГОМК. Антиоксидантные,
антигипоксические и адаптогенные свойства Глу, Асп, их клинико –
фармакологическое значение. Фенилаланин: схема обмена, реакции
образования тирозина. Катехоламиновый и меланиновый пути, реакции,
регуляция. Гомогентизиновый путь (схема). Фенилкетонурия, альбинизм,
алкаптонурия как энзимопатии обмена фенилаланина (механизмы
биохимических нарушений, диагностические показатели крови и мочи).
Триптофан: схема основных путей обмена. Реакции биосинтеза серотонина,
биологическое значение. Схема кинуренинового пути, и его роль в
образовании НАД и снижении потребности в витамине РР.
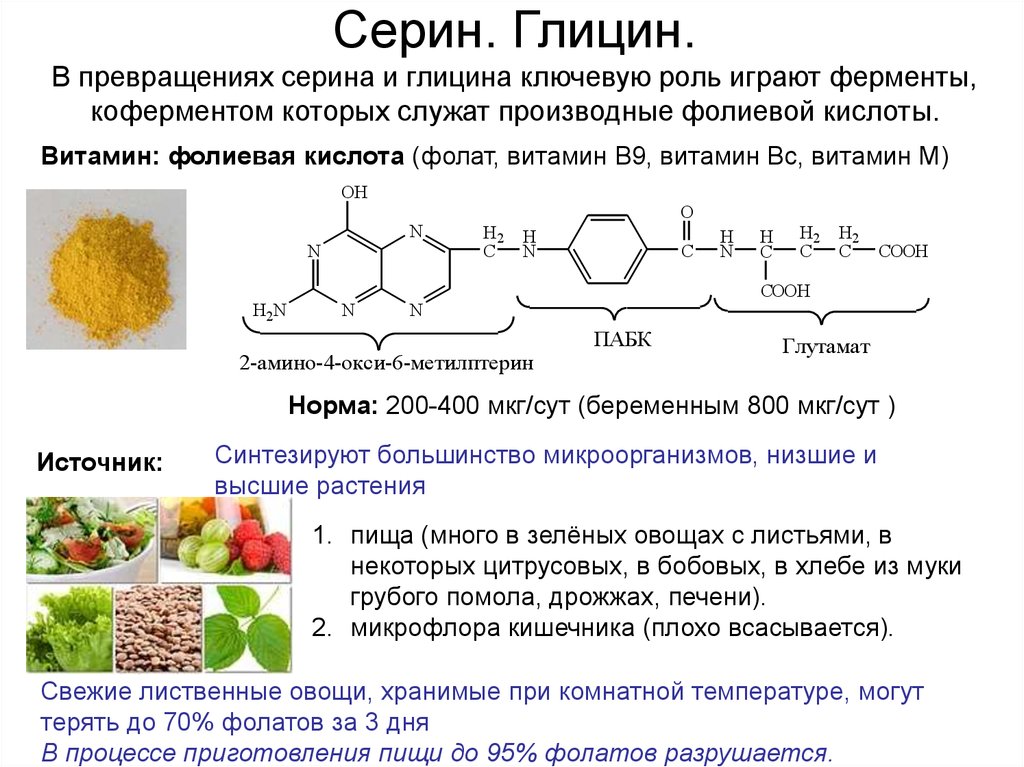
3. Серин. Глицин. В превращениях серина и глицина ключевую роль играют ферменты, коферментом которых служат производные фолиевой кислоты.
Витамин: фолиевая кислота (фолат, витамин B9, витамин Bc, витамин M)OH
N
N
H2N
N
O
H2
C
H
N
C
H
C
H2
C
H2
C
COOH
COOH
N
2-амино-4-окси-6-метилптерин
H
N
ПАБК
Глутамат
Норма: 200-400 мкг/сут (беременным 800 мкг/сут )
Источник:
Синтезируют большинство микроорганизмов, низшие и
высшие растения
1. пища (много в зелёных овощах с листьями, в
некоторых цитрусовых, в бобовых, в хлебе из муки
грубого помола, дрожжах, печени).
2. микрофлора кишечника (плохо всасывается).
Свежие лиственные овощи, хранимые при комнатной температуре, могут
терять до 70% фолатов за 3 дня
В процессе приготовления пищи до 95% фолатов разрушается.
4. Активация фолиевой кислоты
ЖКТСвязывание
Фолиевая кислота + фактор Касла
Фолиевая кислота + белки крови
Всасывание: тощая кишка, 50%
OH
Печень
O
N
N
H2N
N
H2
C
H
N
H2N
N
ПАБК
N
H H
2
C C
CH
H2
C
COOH
Глутамат
O
H
N
H
H
C
H
N
H
C
H2
C
H2
C
COOH
COOH
Тетрагидрофолиевая кислота (ТГФК)
1% от общего запаса / сут
Моча
H2
C
Фолиевая кислота
H
N
H
C
Дегидрофолатредуктаза
- метотрексат
2НАДФ+
2/3 в печени
H
N
COOH
2НАДФН2
OH
C
N
2-амино-4-окси-6-метилптерин
N
Кровь
5 - 20 мкг/литр
1/3 в ткани
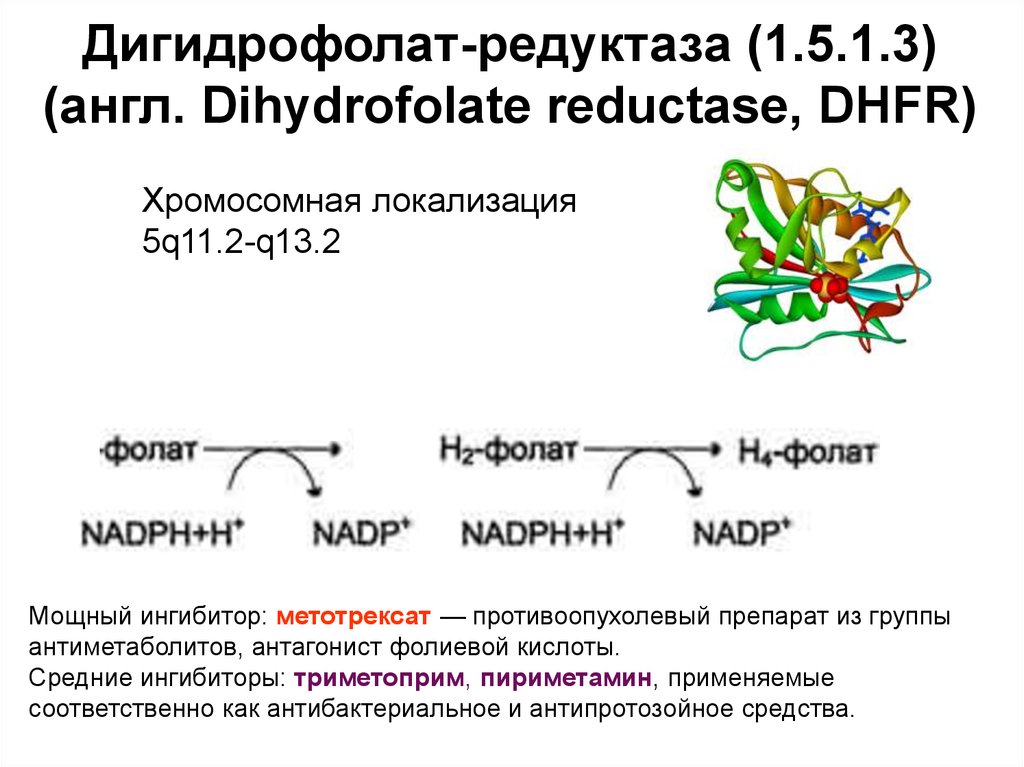
5. Дигидрофолат-редуктаза (1.5.1.3) (англ. Dihydrofolate reductase, DHFR)
Хромосомная локализация5q11.2-q13.2
Мощный ингибитор: метотрексат — противоопухолевый препарат из группы
антиметаболитов, антагонист фолиевой кислоты.
Средние ингибиторы: триметоприм, пириметамин, применяемые
соответственно как антибактериальное и антипротозойное средства.
6. Роль ТГФК
Участвует:• в метаболизме аминокислот
(серин
глицин, гомоцистеин
метионин),
• в синтез нуклеиновых кислот (пуриновые
основания, тимидиловая кислота),
• в образовании эритроцитов
• в образовании ряда компонентов нервной ткани
7.
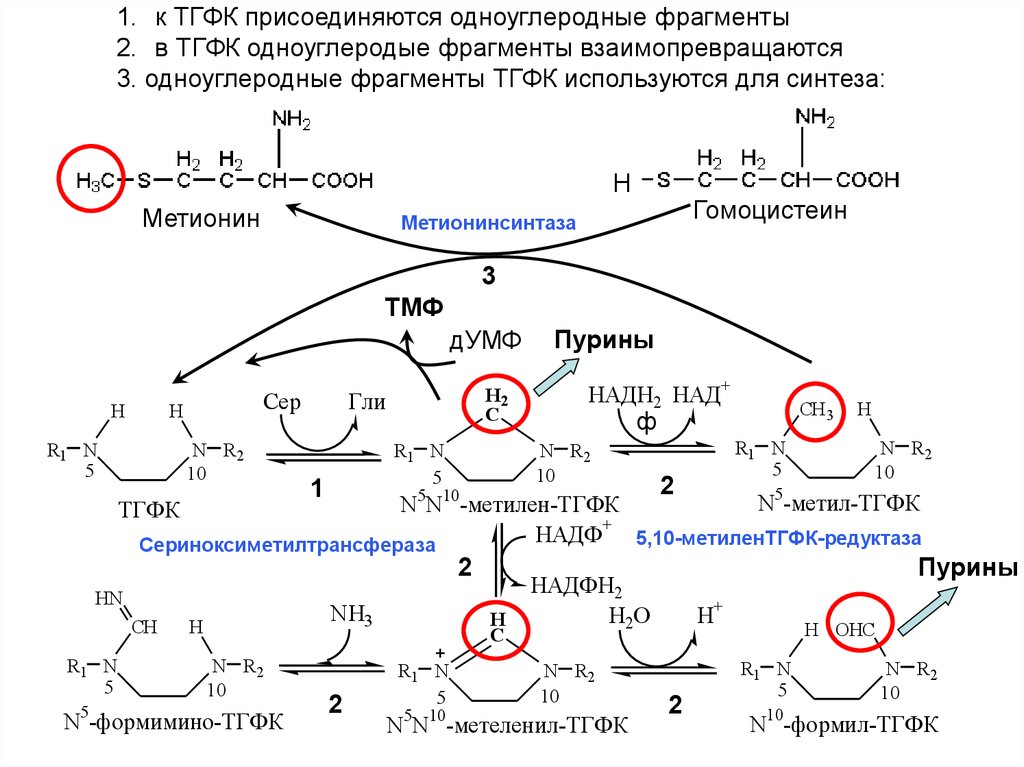
1. к ТГФК присоединяются одноуглеродные фрагменты2. в ТГФК одноуглеродые фрагменты взаимопревращаются
3. одноуглеродные фрагменты ТГФК используются для синтеза:
Н
Метионин
Гомоцистеин
Метионинсинтаза
3
ТМФ
дУМФ
H
Сер
H
R1 N
5
N R2
10
H2
C
Гли
R1 N
5
1
Пурины
НАДН2 НАД+
CH 3
ф
N R2
10
R1 N
5
2
H
N R2
10
N5-метил-ТГФК
N N -метилен-ТГФК
+
НАДФ
5,10-метиленТГФК-редуктаза
Сериноксиметилтрансфераза
ТГФК
5 10
2
HN
CH
R1 N
5
NH3
H
N R2
10
N5-формимино-ТГФК
2
H
C
R1 N
5
Пурины
НАДФН2
Н2О
N R2
10
N5N10-метеленил-ТГФК
Н+
2
H OHC
R1 N
5
N R2
10
N10-формил-ТГФК
8.
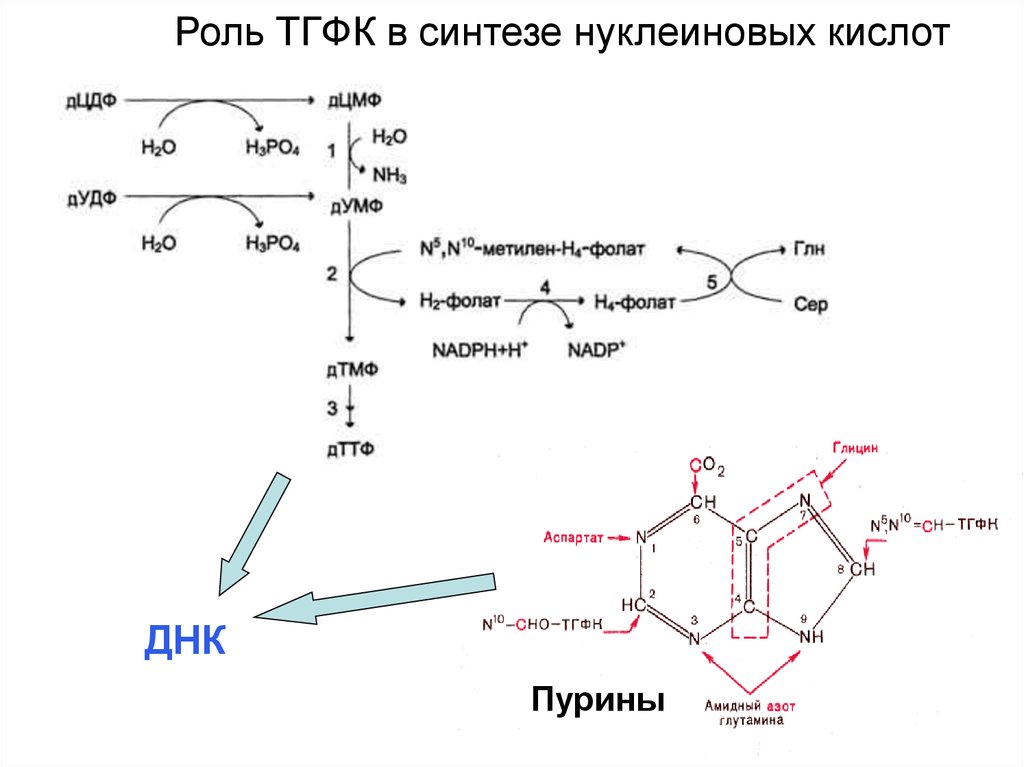
Роль ТГФК в синтезе нуклеиновых кислотДНК
Пурины
9. Дефицит фолиевой кислоты
Причины1. Пищевая недостаточность
2. кислые продукты и тепловая обработка пищи
3. алкоголизм
4. беременность
5. прием лекарств (сульфаниламиды и антибиотики, некоторые цитостатики –
аминоптерин, метотрексат – гибель микрофлоры кишечника, барбитураты,
антиконвульсанты карбамазепин и вальпроевая кислота - активируют
микросомальное окисление в печени и разрушение фолатов)
Гиповитаминоз фолиевой кислоты приводит к:
1. мегалобластической (макроцитарной) анемии. уменьшение количества
Er, Hb, увеличение размера Er. Причина — нарушение синтеза ДНК и
РНК из-за недостатка тимидиловой кислоты и пуриновых нуклеотидов.
2. лейкопении;
3. задержке роста.
4. поражению ЖКТ (связано с недостатком нуклеотидов для синтеза ДНК
в постоянно делящихся клетках слизистой оболочки).
5. конъюнктивиту,
6. ухудшению заживления ран,
7. иммунодефициты, оживление хронических инфекций.
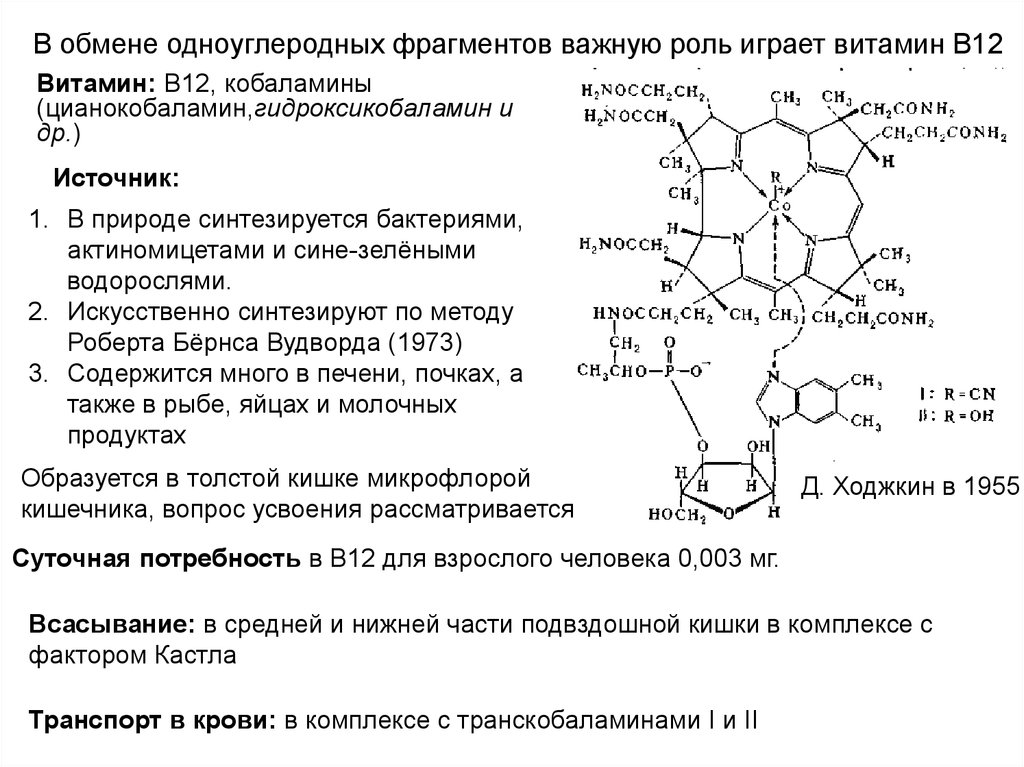
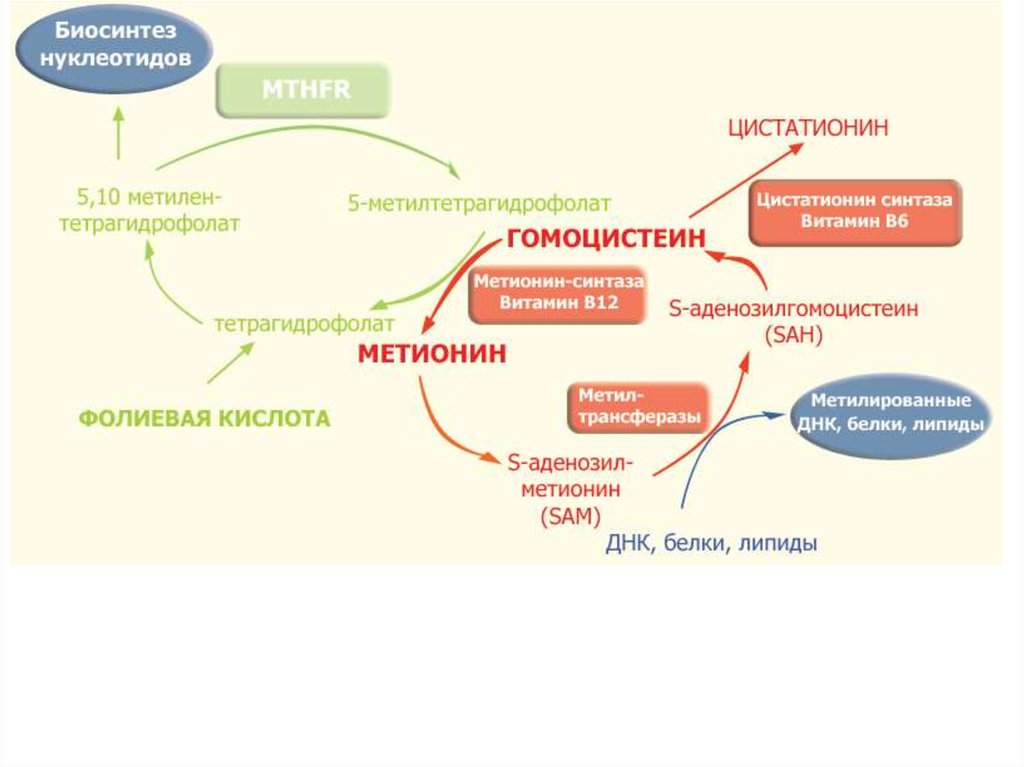
10. В обмене одноуглеродных фрагментов важную роль играет витамин В12
Витамин: В12, кобаламины(цианокобаламин,гидроксикобаламин и
др.)
Источник:
1. В природе синтезируется бактериями,
актиномицетами и сине-зелёными
водорослями.
2. Искусственно синтезируют по методу
Роберта Бёрнса Вудворда (1973)
3. Содержится много в печени, почках, а
также в рыбе, яйцах и молочных
продуктах
Образуется в толстой кишке микрофлорой
кишечника, вопрос усвоения рассматривается
Д. Ходжкин в 1955
Суточная потребность в В12 для взрослого человека 0,003 мг.
Всасывание: в средней и нижней части подвздошной кишки в комплексе с
фактором Кастла
Транспорт в крови: в комплексе с транскобаламинами I и II
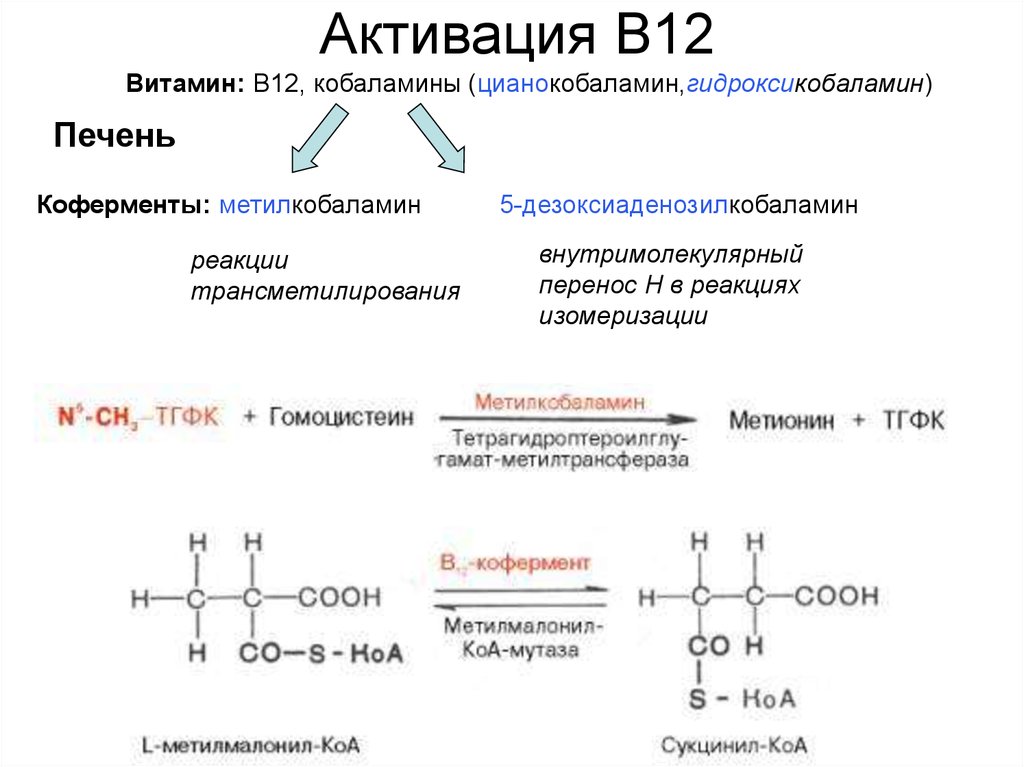
11. Активация В12
Витамин: В12, кобаламины (цианокобаламин,гидроксикобаламин)Печень
Коферменты: метилкобаламин
реакции
трансметилирования
5-дезоксиаденозилкобаламин
внутримолекулярный
перенос Н в реакциях
изомеризации
12. Дефицит В12
Причины1. Недостаток витамина В12 в пищевых продуктах,
2. голодание или вегетарианство
3. дефицит фактора Касла при пониженной кислотности желудочного
сока
Клиника
1. макроцитарная (мегалобластическая) анемия: снижение числа
эритроцитов, гемоглобина, увеличение размера эритроцитов.
Причина — нарушение синтеза ДНК в эритрокариоцитах.
2. расстройство деятельности нервной системы (бред,
галлюцинации, шаткая походка, парестезии, болевые ощущения,
онемение конечностей и др.). Нарушается синтез миелина. При
распаде жирных кислот с нечетным количеством атомов С и
разветвленных АК из-за дефицита В12 накапливается
нейротоксичная метилмалоновая кислота.
3. Нарушения ЖКТ глоссит, формирование "полированного" языка
(в связи с атрофией его сосочков); стоматит; гастроэнтероколит
13. Мегалобластическая анемия
нормаМегалобластическая анемия
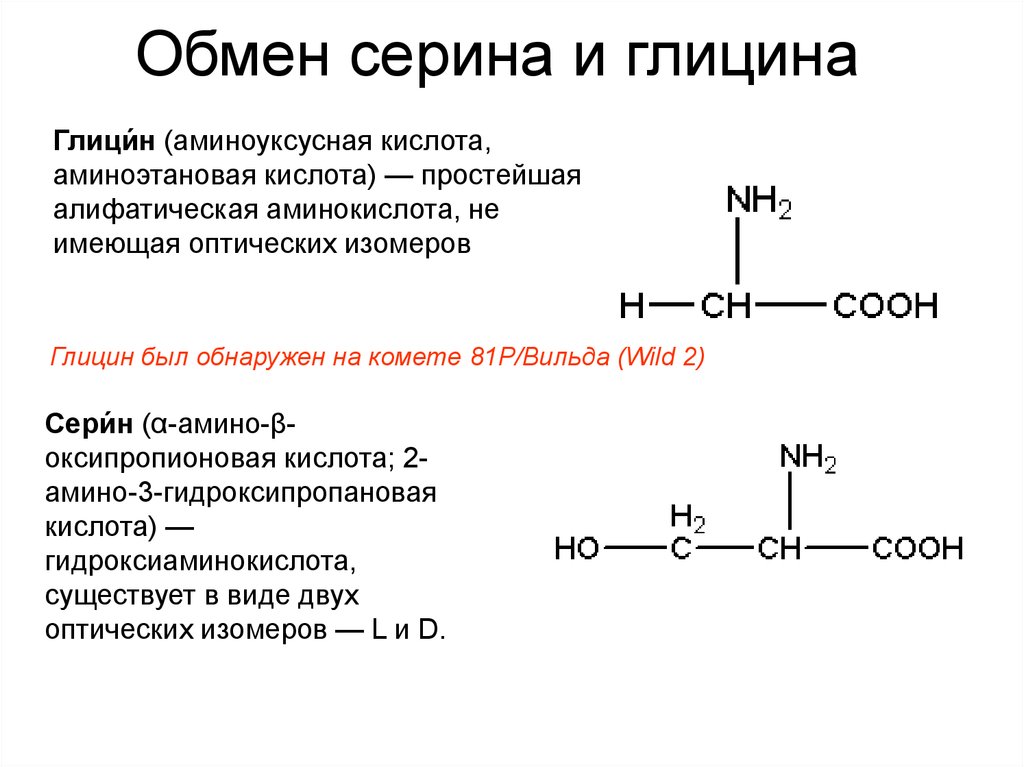
14. Обмен серина и глицина
Глици́н (аминоуксусная кислота,аминоэтановая кислота) — простейшая
алифатическая аминокислота, не
имеющая оптических изомеров
Глицин был обнаружен на комете 81P/Вильда (Wild 2)
Сери́н (α-амино-βоксипропионовая кислота; 2амино-3-гидроксипропановая
кислота) —
гидроксиаминокислота,
существует в виде двух
оптических изомеров — L и D.
15. Серин. Глицин.
Синтез серина:COOH
глюкоза
НАД+ НАДН2 COOH
HC OH
H2C OPO 3H2
3-фосфоглицерат
ДГ
C O
Глу
а-КГ
COOH
HC NH 2
H2O
Аминотранс- H C OPO H
2
3 2
фераза
3-Фосфосерин
3-фосфооксипируват
H2C OPO 3H2
Фн
фосфотаза
COOH
HC NH 2
H2C OH
Серин
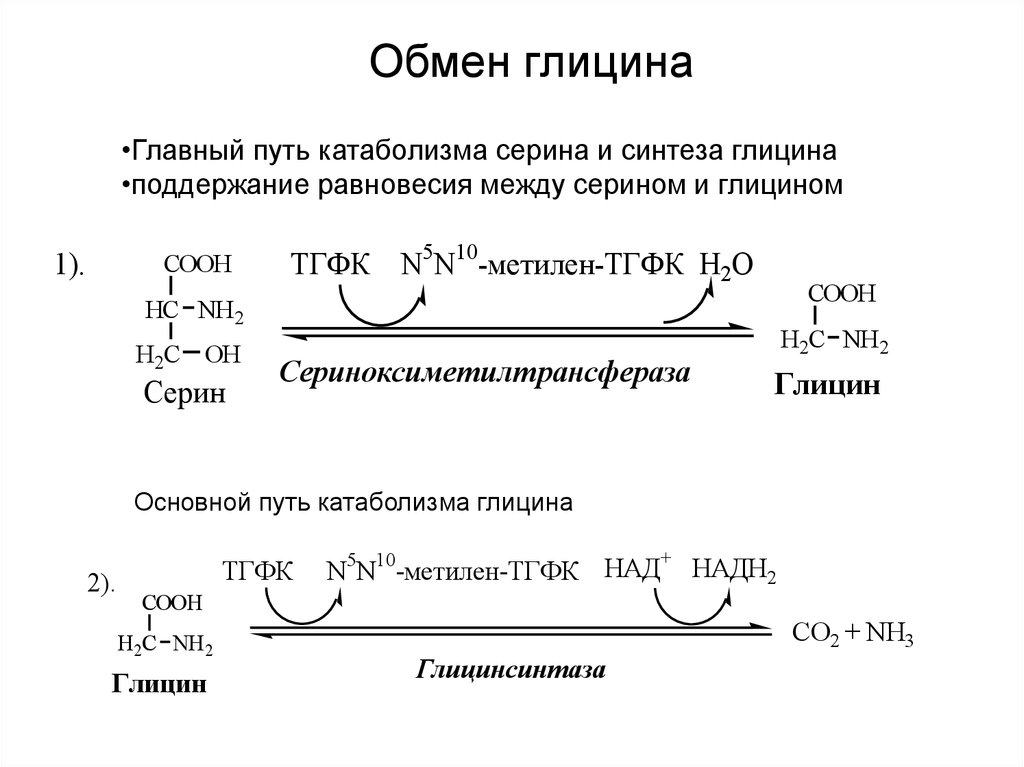
16.
Обмен глицина•Главный путь катаболизма серина и синтеза глицина
•поддержание равновесия между серином и глицином
1).
COOH
ТГФК N5N10-метилен-ТГФК Н2О
COOH
HC NH2
H2C OH
Серин
Сериноксиметилтрансфераза
H2C NH2
Глицин
Основной путь катаболизма глицина
2).
ТГФК
+
N5N10-метилен-ТГФК НАД НАДН2
COOH
H2C NH2
Глицин
СО2 + NH3
Глицинсинтаза
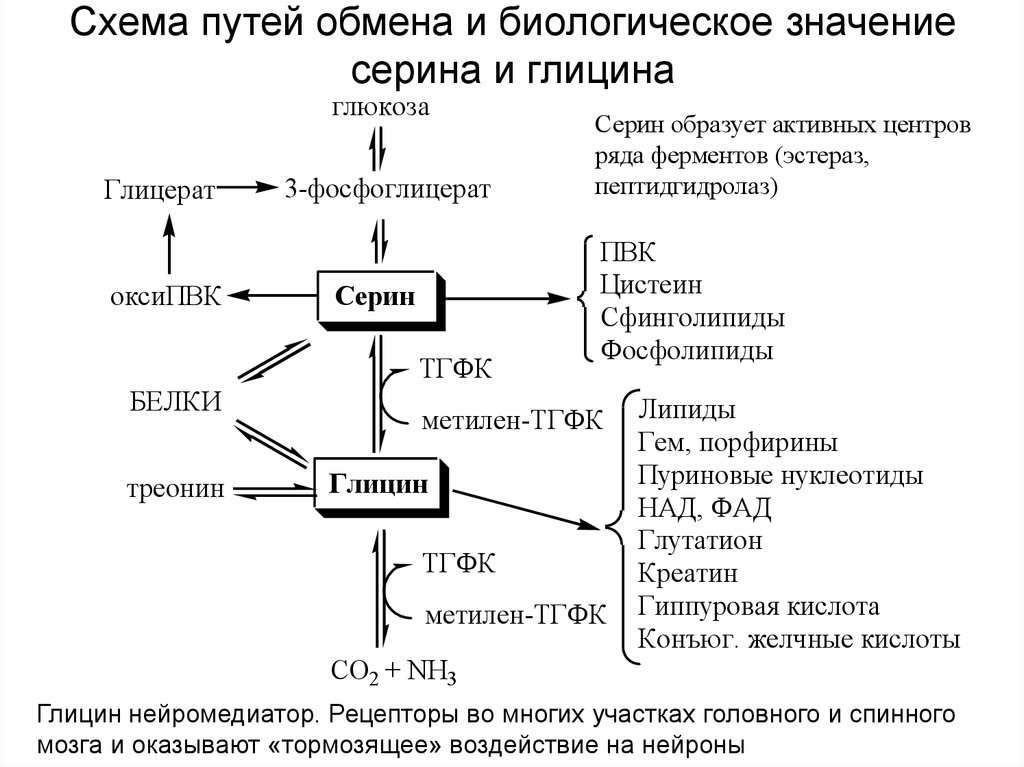
17. Схема путей обмена и биологическое значение серина и глицина
глюкозаГлицерат
оксиПВК
3-фосфоглицерат
Серин
ТГФК
БЕЛКИ
треонин
Серин образует активных центров
ряда ферментов (эстераз,
пептидгидролаз)
ПВК
Цистеин
Сфинголипиды
Фосфолипиды
метилен-ТГФК
Глицин
ТГФК
метилен-ТГФК
Липиды
Гем, порфирины
Пуриновые нуклеотиды
НАД, ФАД
Глутатион
Креатин
Гиппуровая кислота
Конъюг. желчные кислоты
СО2 + NH3
Глицин нейромедиатор. Рецепторы во многих участках головного и спинного
мозга и оказывают «тормозящее» воздействие на нейроны
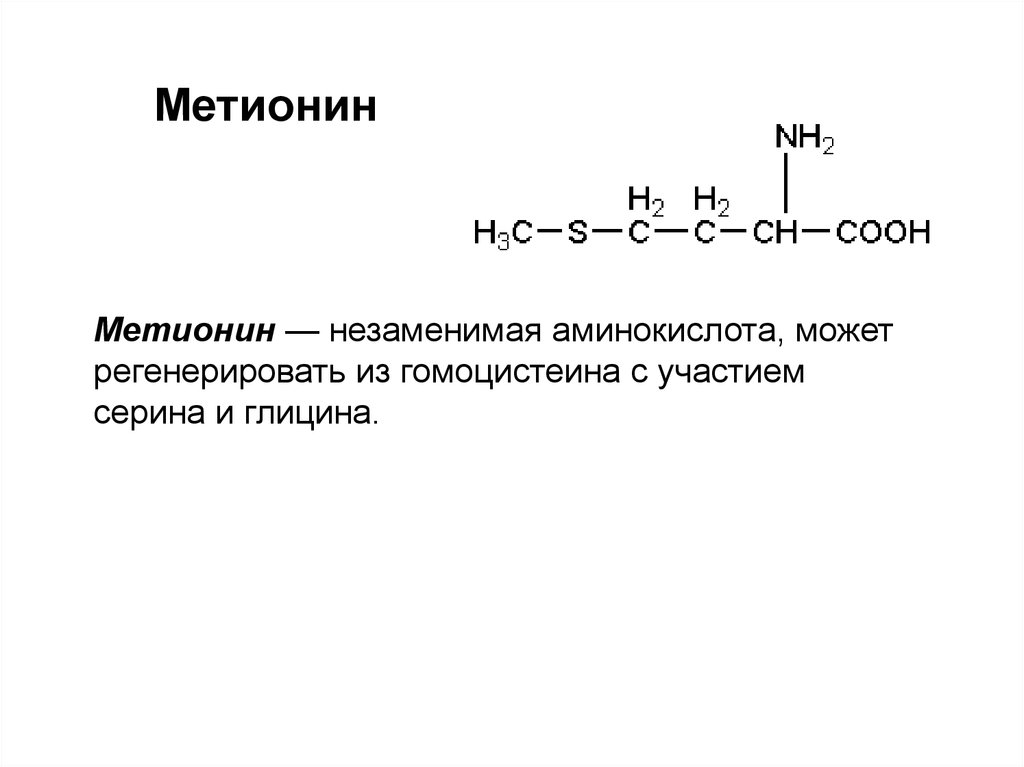
18. Метионин
Метионин — незаменимая аминокислота, можетрегенерировать из гомоцистеина с участием
серина и глицина.
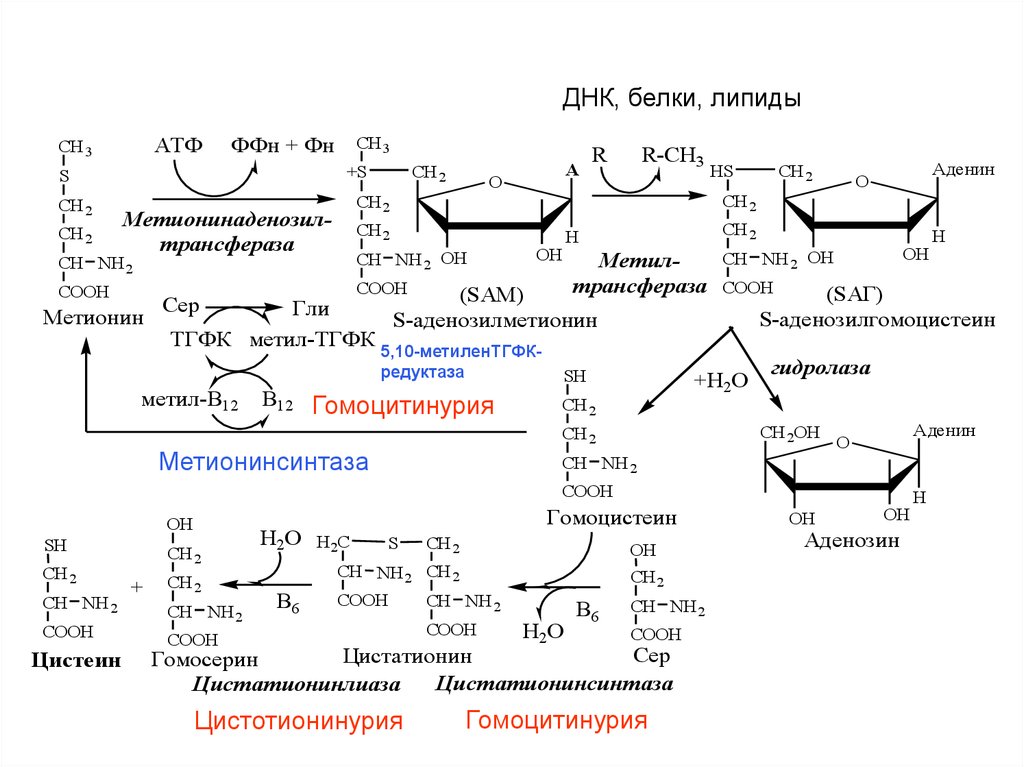
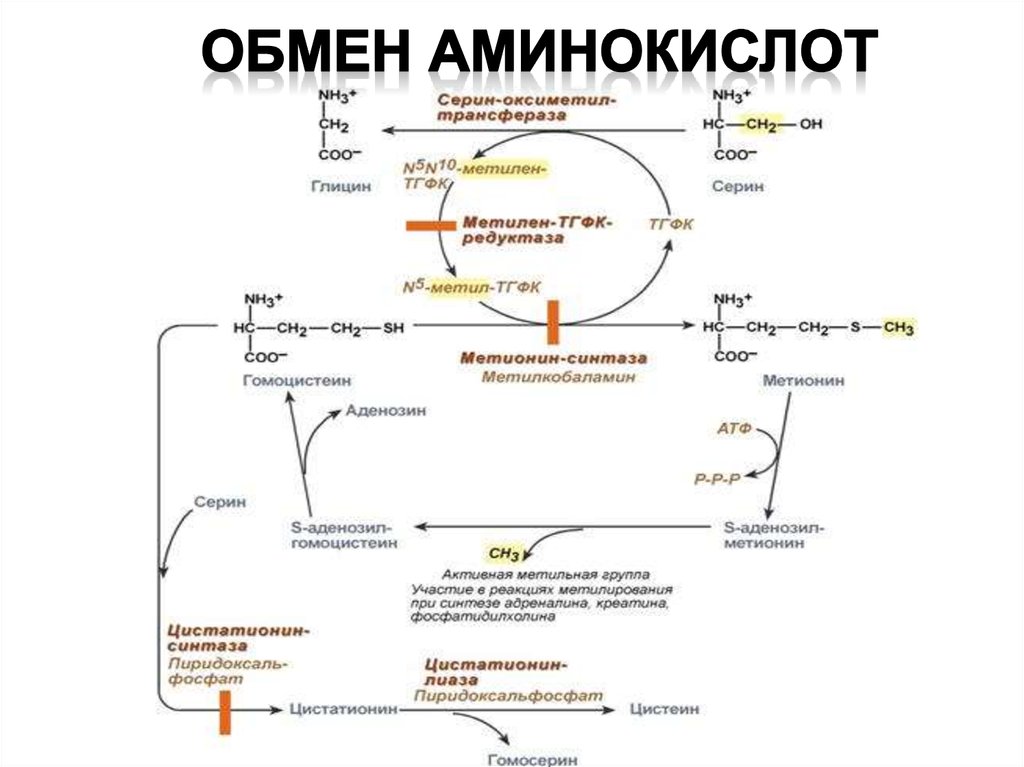
19.
ДНК, белки, липидыАТФ
CH 3
CH 3
ФФн + Фн
+S
S
CH 2
А
О
R
R-CH3
HS
СН 2
Аденин
О
CH 2
CH 2
Метионинаденозилтрансфераза
CH 2
СН 2
CH 2
ОН
CH 2
Н
ОН
Н
CH NH 2 ОН
Метилтрансфераза CООН
CООН
CООН
(SAГ)
(SAM)
Сер
Гли
Метионин
S-аденозилгомоцистеин
S-аденозилметионин
ТГФК метил-ТГФК 5,10-метиленТГФКгидролаза
редуктаза
SH
+Н2О
метил-В12 В12 Гомоцитинурия
CH 2
CH NH 2 ОН
CH NH 2
Гомоцистеинметилтрансфераза
Метионинсинтаза
СН 2ОН
CH 2
Аденин
О
CH NH 2
CООН
ОH
SH
CH 2
CH 2
CH NH 2
+
CООН
Цистеин
а-КГ
глу
CH 2
CH NH 2
Н2О H2C
Гомоцистеин
S
CH 2
ОH
CH NH 2 CH 2
В6
CООН
CООН
CH 2
CH NH 2
CООН
Н2О
В6
CH NH 2
CООН
Сер
Цистатионин
Гомосерин
Цистатионинсинтаза
Цистатионинлиаза
Цистотионинурия
Гомоцитинурия
ОН
ОН
Аденозин
Н
20. Значение метионина
• участвует в синтезе белков организма;• является источником метильной группы, используемой
в реакциях трансметилирования (метилирование ДНК,
белков, синтез фосфолипидов, нейромедиаторов и др.);
• является источником атома серы, необходимого для
синтеза цистеина из него ФАФС и других
серосодержащих соединений;
• Метионил-тРНК участвует в инициации процесса
трансляции.
• Метионин обеспечивает транспорт липидов из
печени. Дефицит приводит к жировому
перерождению печени
• Необходим для антиоксидантной системы (синтез
глутатиона). Дефицит активирует ПОЛ и старение
• Обеспечивает формирование основного вещества
межклеточного матрикса (ГАГ)
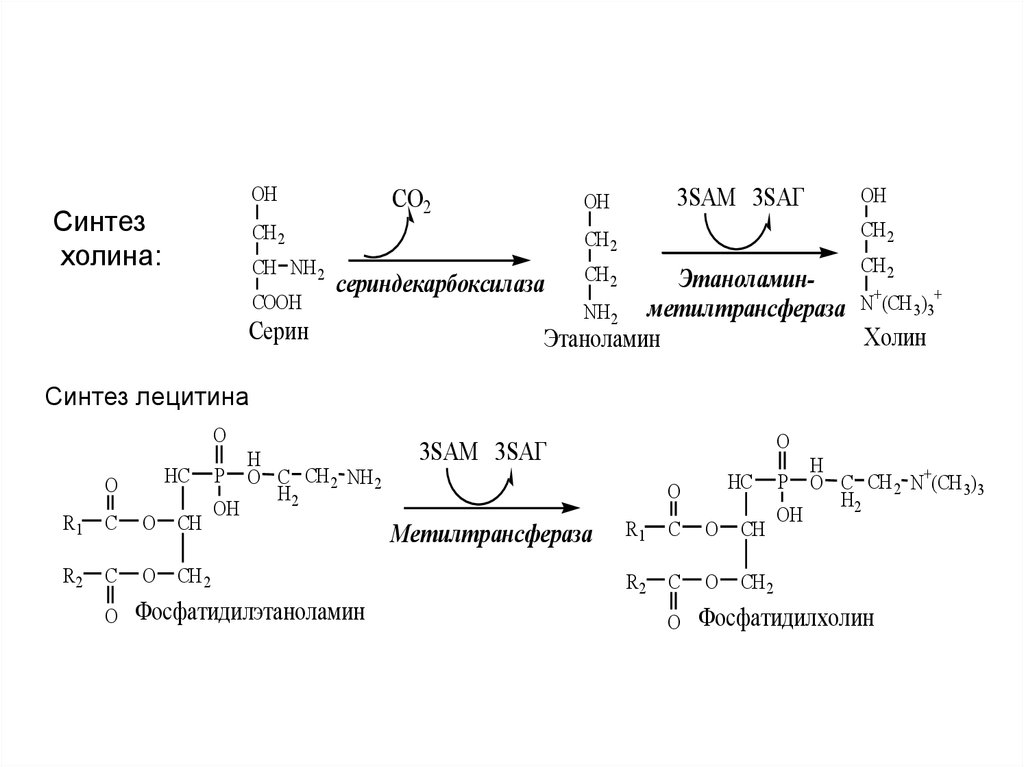
21.
ОНСинтез
холина:
CO2
CH 2
CH NH 2
CООН
3SAM 3SAГ
ОН
CH 2
CH 2
CH
CH 2
2
Этаноламин+
+
N
(CH
)
3
3
метилтрансфераза
NH 2
Холин
Этаноламин
сериндекарбоксилаза
Серин
ОН
Синтез лецитина
O
HC
O
R1
C
O
CH
R2
C
O
CH 2
O
P
OH
Н
О C CH 2 NH2
H2
Фосфатидилэтаноламин
O
3SAM 3SAГ
HC
O
Метилтрансфераза
R1
C
O
CH
R2
C
O
CH 2
O
Н
P О C CH 2 N+(CH 3)3
H2
OH
Фосфатидилхолин
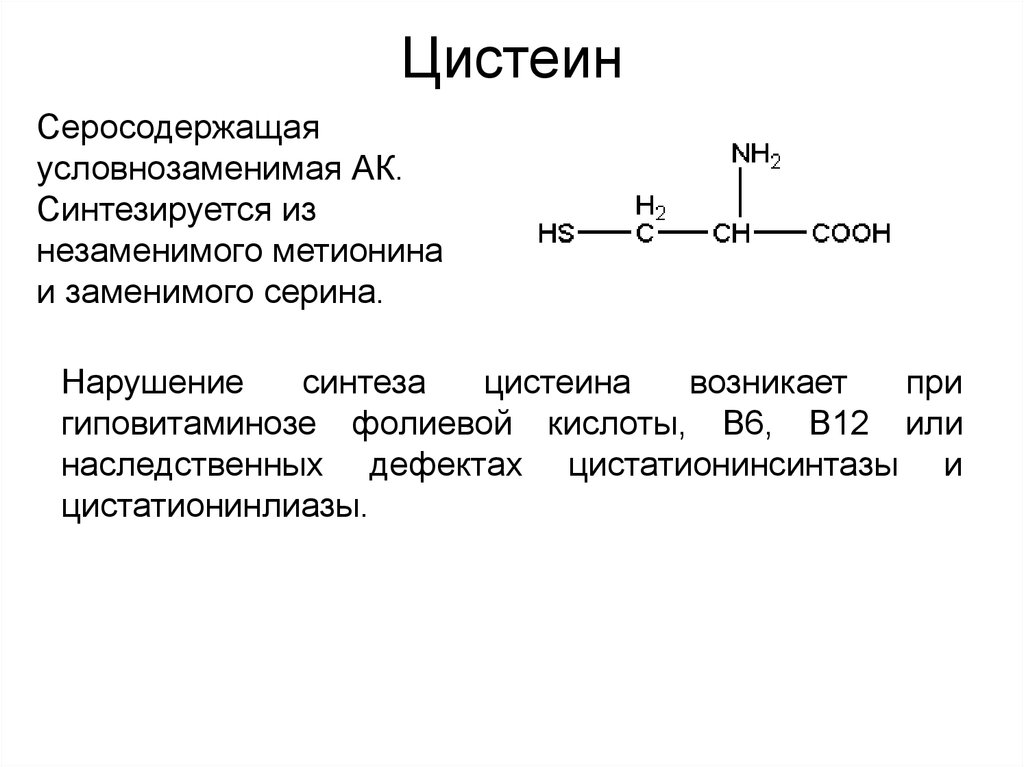
22. Цистеин
Серосодержащаяусловнозаменимая АК.
Синтезируется из
незаменимого метионина
и заменимого серина.
Нарушение
синтеза
цистеина
возникает
при
гиповитаминозе фолиевой кислоты, В6, В12 или
наследственных дефектах цистатионинсинтазы и
цистатионинлиазы.
23. Использование цистеина
1. используется в белках для формированиятретичной структуры (дисульфидные мостики);
2. SH группы цистеина формируют активный центр
многих ферментов;
3. идет на синтез глутатиона, таурина (парные
желчные кислоты), НS-КоА, ПВК (глюкоза);
4. Является источником сульфатов, которые идут на
синтез ФАФС или выделяются с мочой.
24. Образование сульфат-иона, его утилизация
SHH2C
CH NH 2
CООН
Цистеин
О2
а-КГ
SO 2H
глу
SO 2H
H2C
CH NH 2
Цистеиндиоксигеназа
CООН
О2
CH 3
H2C
аминотрансфераза
H2C
CH NH 2
CООН
Цистеиновая
кислота
O
CООН
сульфинилпируват
Цистеинсульфинат
SO 3H
C
C
АТФ
СО2
CООН
пируват
SO32SO42-
АТФ
АДФ
ФАС
SO 3H
CH 2
CH NH 2
Таурин
O
парные желчные кислоты
ФАФС
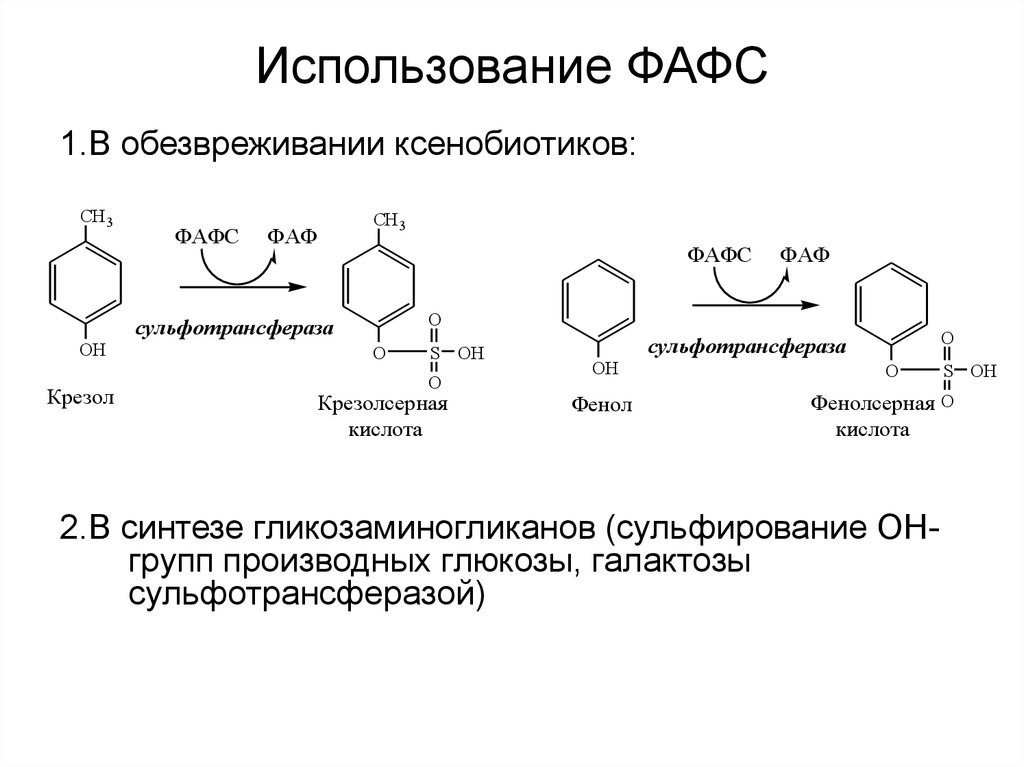
25. Использование ФАФС
1.В обезвреживании ксенобиотиков:CH 3
ФАФС
CH 3
ФАФ
ФАФС
O
сульфотрансфераза
OH
Крезол
ФАФ
O
S OH
O
Крезолсерная
кислота
O
сульфотрансфераза
OH
Фенол
O
S OH
Фенолсерная O
кислота
2.В синтезе гликозаминогликанов (сульфирование ОНгрупп производных глюкозы, галактозы
сульфотрансферазой)
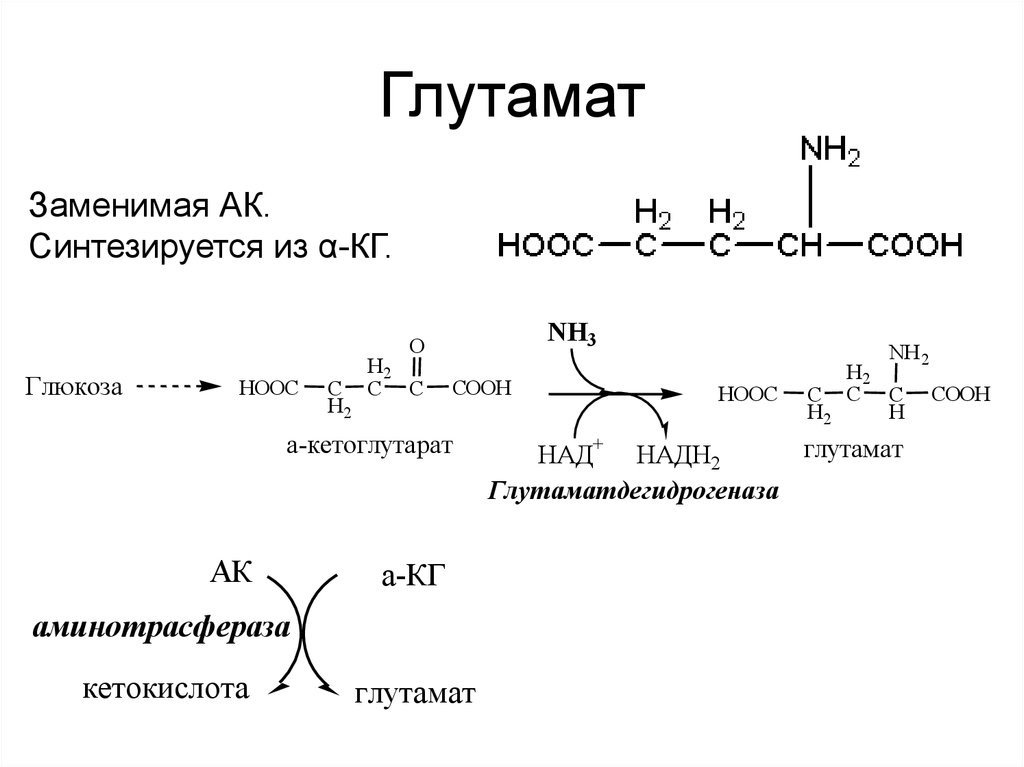
26. Глутамат
Заменимая АК.Синтезируется из α-КГ.
NH3
O
Глюкоза
HOOC
C
H2
H2
C C
COOH
а-кетоглутарат
АК
а-КГ
аминотрасфераза
кетокислота
глутамат
HOOC
C
H2
NH 2
H2
C C COOH
H
глутамат
НАД+ НАДН2
Глутаматдегидрогеназа
27.
Глутамат1. возбуждающий нейромедиатор в коре, гиппокампе, полосатом теле
и гипоталамусе, участвует в регуляции процессов памяти.
2. Используется в синтезе белков, липидов, углеводов;
3. источник α-КГ (для ЦТК и синтеза АТФ);
4. Входит в состав глутатиона;
5. используется для синтеза тормозного нейромедиатора ГАМК;
6. входит в состав нейропептидов — люлиберина, тиролиберина,
нейротензина, бомбезина и др.;
7. глутамат служит источником янтарной кислоты (сукцинат)
8. Ведущая роль в интеграции азотистого обмена:
• Обеспечивает реакции переаминирования АК: глутамат
универсальный донор аминогруппы для синтеза заменимых АК
(Ала, Асп, Асн, Сер, Гли, Глн, Про).
• Обеспечивает непрямое дезаминирование большинства АК.
• Участвует в обезвреживании аммиака с образованием глутамина;
28. Глутамин
NH3NH2
HOOC
C
H2
H2
C C
H
глутамат
COOH
NH2
2+
Mg
H2NOC
C
H2
H2
C CH
COOH
глутамин
АТФ
АДФ + Фн
Глутаминсинтаза
АМФ, глюкозо-6ф, гли, ала и гис
1. Используется в синтезе белков, углеводов;
2. Источник азота в синтезе пуриновых и
пиримидиновых оснований, аспарагина,
аминосахаров;
3. Обеспечивает транспорт азота из тканей
29. Аспарагиновая кислота
Заменимая АК.Синтезируется из ЩУК
Глу
O
Глюкоза
HOOC
H2
C C
ЩУК
а-КГ
NH 2
HOOC
COOH
АСТ
H2
C C
H
COOH
аспартат
1. Используется в синтезе белков, липидов, углеводов;
2. Участвует в орнитиновом цикле при синтезе мочевины;
3. Участвует в синтезе карнозина, анзерина, пуриновых и
пиримидиновых нуклеотидов, N-ацетиласпарагиновой
кислоты.
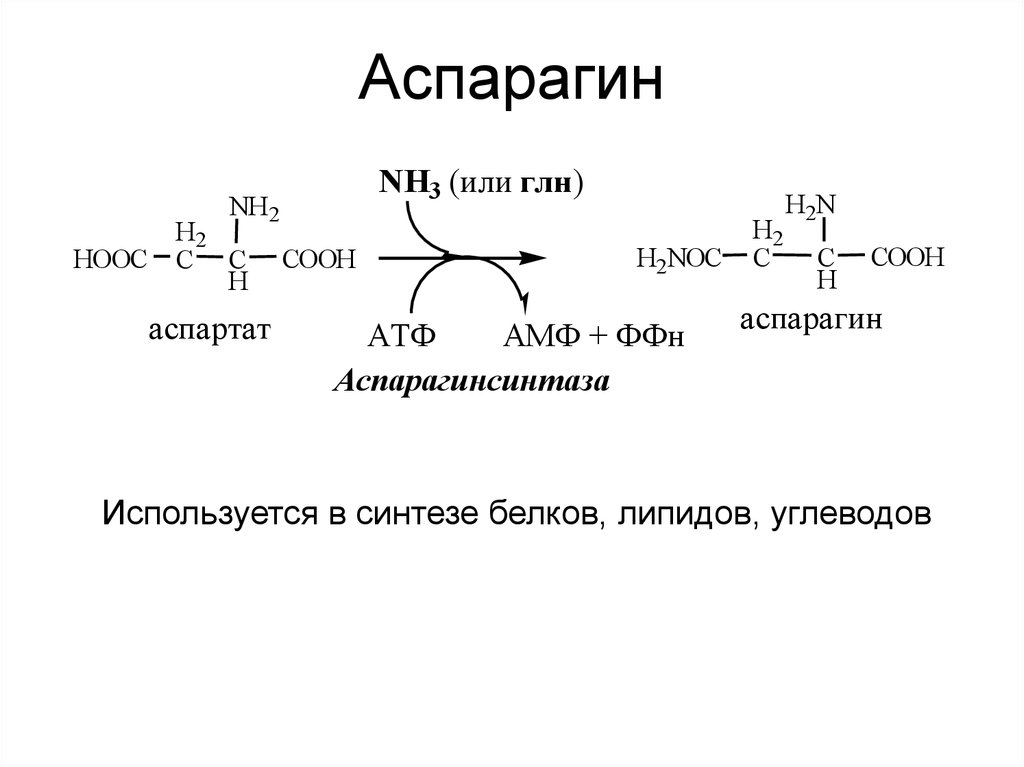
30. Аспарагин
NH3 (или глн)NH 2
HOOC
H2
C C
H
аспартат
COOH
H2NOC
АТФ
АМФ + ФФн
Аспарагинсинтаза
H2
C
H2N
C
H
COOH
аспарагин
Используется в синтезе белков, липидов, углеводов
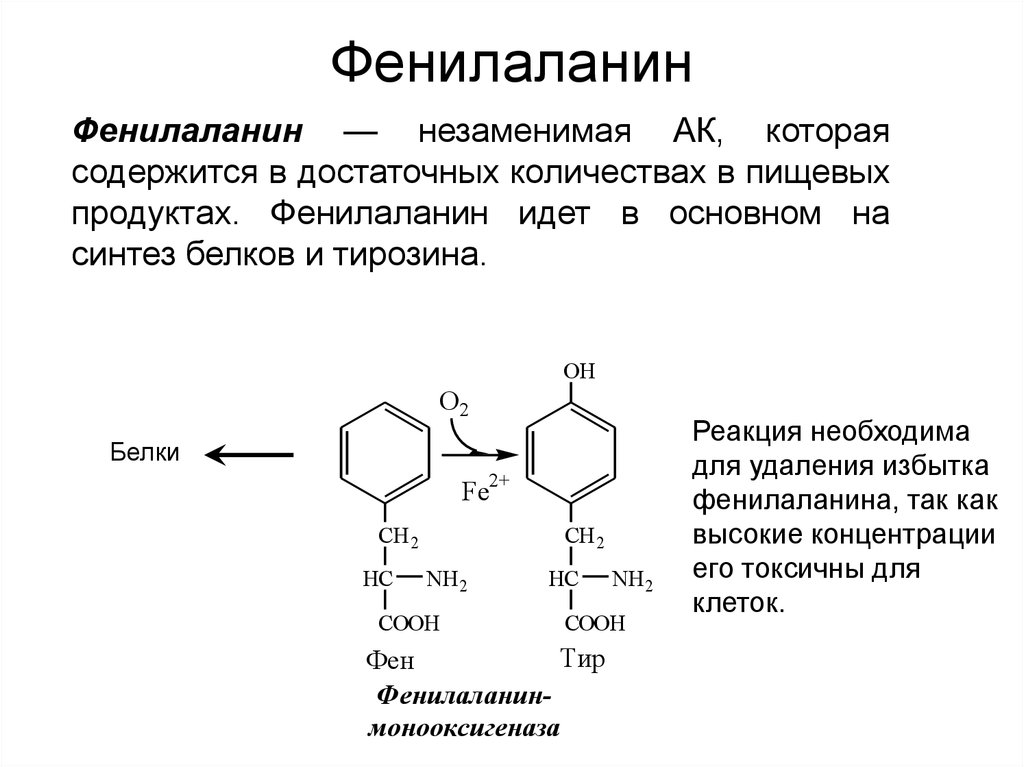
31. Фенилаланин
Фенилаланин — незаменимая АК, котораясодержится в достаточных количествах в пищевых
продуктах. Фенилаланин идет в основном на
синтез белков и тирозина.
OH
О2
Белки
Fe2+
CH 2
HC
CH 2
NH 2
COOH
HC
NH 2
COOH
Тир
Фен
Фенилаланинмонооксигеназа
Реакция необходима
для удаления избытка
фенилаланина, так как
высокие концентрации
его токсичны для
клеток.
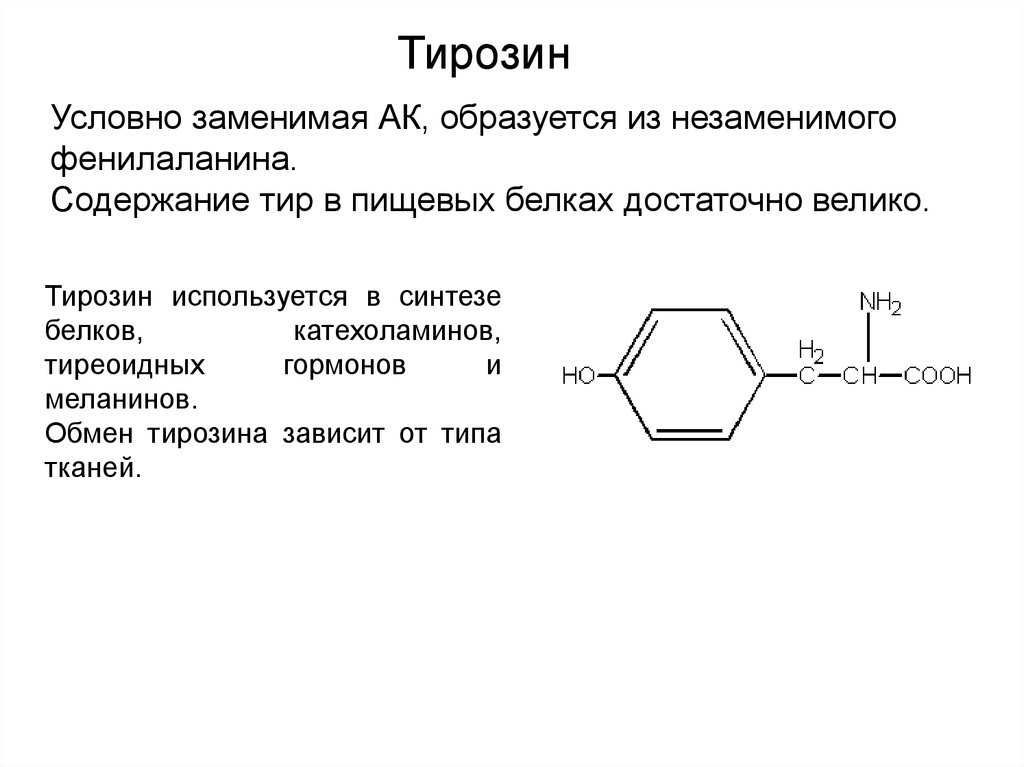
32. Условно заменимая АК, образуется из незаменимого фенилаланина. Содержание тир в пищевых белках достаточно велико.
ТирозинУсловно заменимая АК, образуется из незаменимого
фенилаланина.
Содержание тир в пищевых белках достаточно велико.
Тирозин используется в синтезе
белков,
катехоламинов,
тиреоидных
гормонов
и
меланинов.
Обмен тирозина зависит от типа
тканей.
33.
Обмен тир в надпочечниках и нервной тканиOH
норадреналин
OH
О2
OH
Fe2+
CH 2
HC
COOH
Тир
OH
OH
HC
CH 2
NH 2
COOH
H2C
О2
вит. С
Cu2+
B6
CH 2
NH 2
СО2
NH 2
дофамин
OH
OH
OH
OH
SAM SAГ
HC
ОН
HC
H2C
NH 2
H2C
норадреналин
ДОФА
ДОФАТирозиндофаминмонооксигеназа декарбоксилаза монооксигеназа
ОН
NНCH 3
адреналин
метилтрансфераза
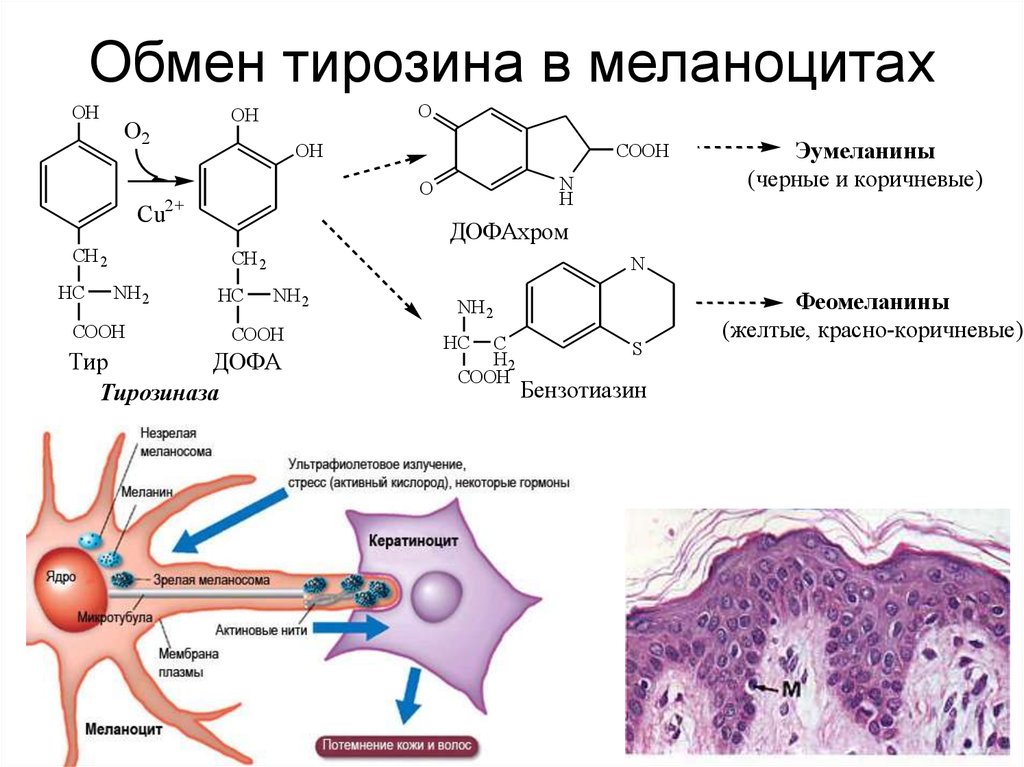
34. Обмен тирозина в меланоцитах
OHО2
O
OH
OH
HC
N
H
O
Cu2+
CH 2
COOH
ДОФАхром
CH 2
NH 2
COOH
Эумеланины
(черные и коричневые)
HC
N
NH 2
COOH
Тир
ДОФА
Тирозиназа
NH 2
HC
C
H2
COOH
S
Бензотиазин
Феомеланины
(желтые, красно-коричневые)
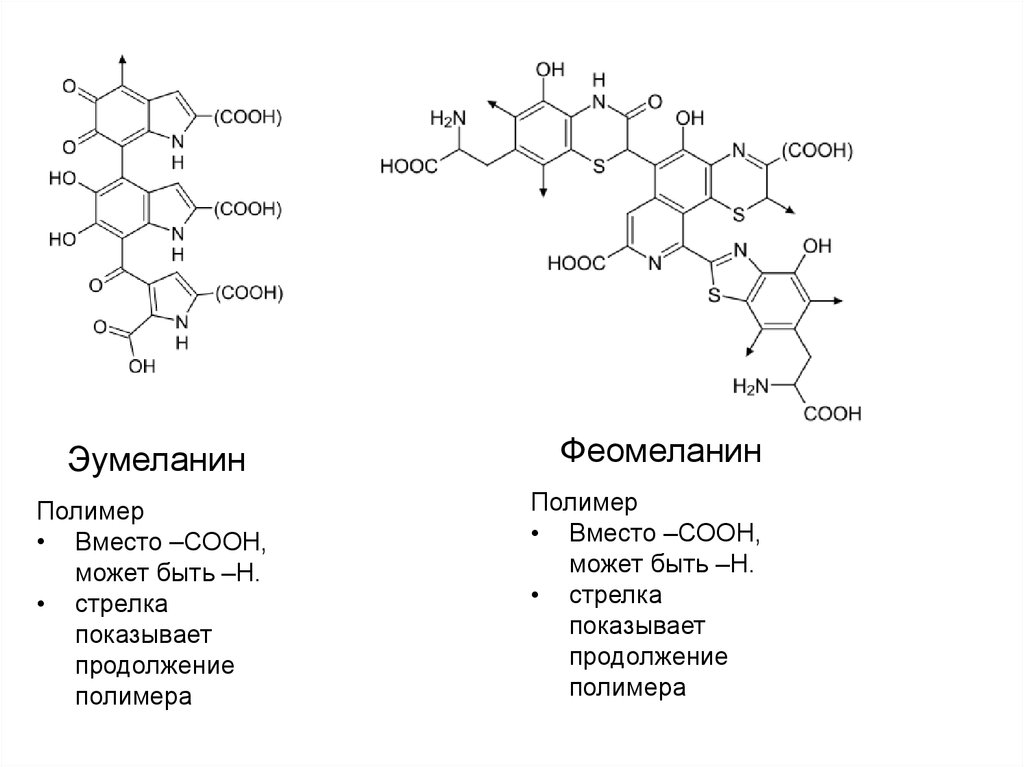
35.
ЭумеланинПолимер
• Вместо –СООН,
может быть –Н.
• стрелка
показывает
продолжение
полимера
Феомеланин
Полимер
• Вместо –СООН,
может быть –Н.
• стрелка
показывает
продолжение
полимера
36.
Цвет волос в зависимости от соотношения пигментов37. Катаболизм тирозина в печени
Тирозингидроксифенилпируватаминотрансферазадиоксигеназа
OH
OH
OH
O2 CO2
а-КГ глу
В6
CH 2
CH 2
HC
NH 2
COOH
Тир
C
вит. С, Fe2+
O
COOH
п-гидроксифенилпируват
OH
диоксигеназа
гомогентизиновой
кислоты
О2
Fe2+
C COOH
H2
Гомогентизиновая
кислота
HOOC
OH
C COOH
H2
O
Фумарилацетоацетат
COOH
CH 3
CH
C
CH
CH 2
COOH
COOH
O
Фумарат
Ацетоацетат
Фумарилацетоацетатгидролаза
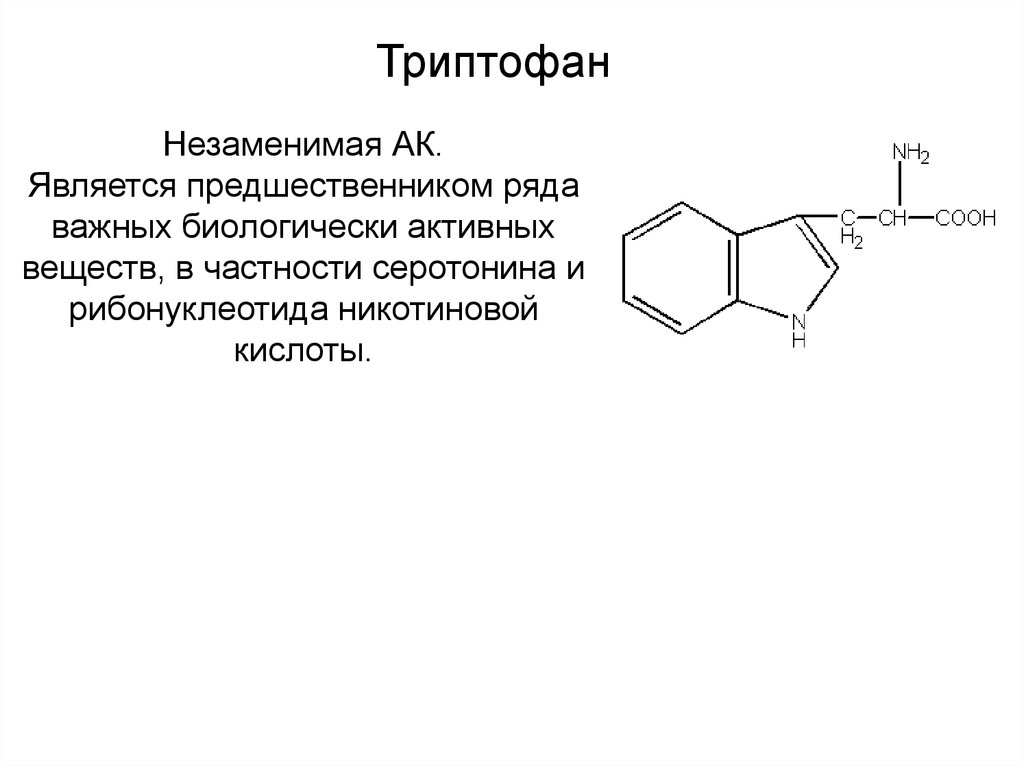
38. Незаменимая АК. Является предшественником ряда важных биологически активных веществ, в частности серотонина и рибонуклеотида никотиново
ТриптофанНезаменимая АК.
Является предшественником ряда
важных биологически активных
веществ, в частности серотонина и
рибонуклеотида никотиновой
кислоты.
39.
В физиологических условиях >95% триптофана метаболизирует покинурениновому пути и 1% по серотониновому пути.
NH 2
H2
C CH COOH
NH 2
H2
C CH COOH
C
C
O
Три
N
H
O
O
O2
триптофандиоксигеназа
НАДН2 НАД+
НСООН
Кинуренинформилаза
N C
H
H
Формилкинуренин
NH 2
H2
C CH COOH
C
NH 2
H2
C CH COOH
NH 2
Кинуренин
COOH
COOH
O
O2
Кинуренингидроксилаза
Аланин
NH 2
Кинурениназа
OH
Оксикинуренин
COOH
ФРПФ
N
COOH
рибозо-5ф
Рибонуклеотид
холиновой кислоты
СО2
NH 2
O2
N
COOH
Оксидаза
Холиновая
Оксиантраниловая
кислота
кислота
COOH
OH
АТФ NH3
CONH 2
N
N
рибозо-5ф
рибозо-5ф-О-ф-аденозин
Рибонуклеотид
холиновой кислоты
НАД+
40.
• Схема серотонинового пути:NH 2
H2
HO
C CH COOH
N
H
Триптофан
NH 2
H2
C CH COOH HO
N
H
В6
CO2
O2
H2O
НАДФН2 НАДФ+ 5-окситриптофан
фен-гидроксилаза
Декарбоксилаза
1. Серотонин образуется в
надпочечниках, ЦНС и тучных
клетках.
2. Возбуждающий нейромедиатор
средних отделов мозга
(проводящих путей) и гормон.
3. Стимулирует сокращение гладкой
мускулатуры, вазоконстриктор,
регулирует АД, температуру тела,
дыхание, антидепрессант.
H2
C
N
H
серотонин
Мелатонин
NH 2
CH 2
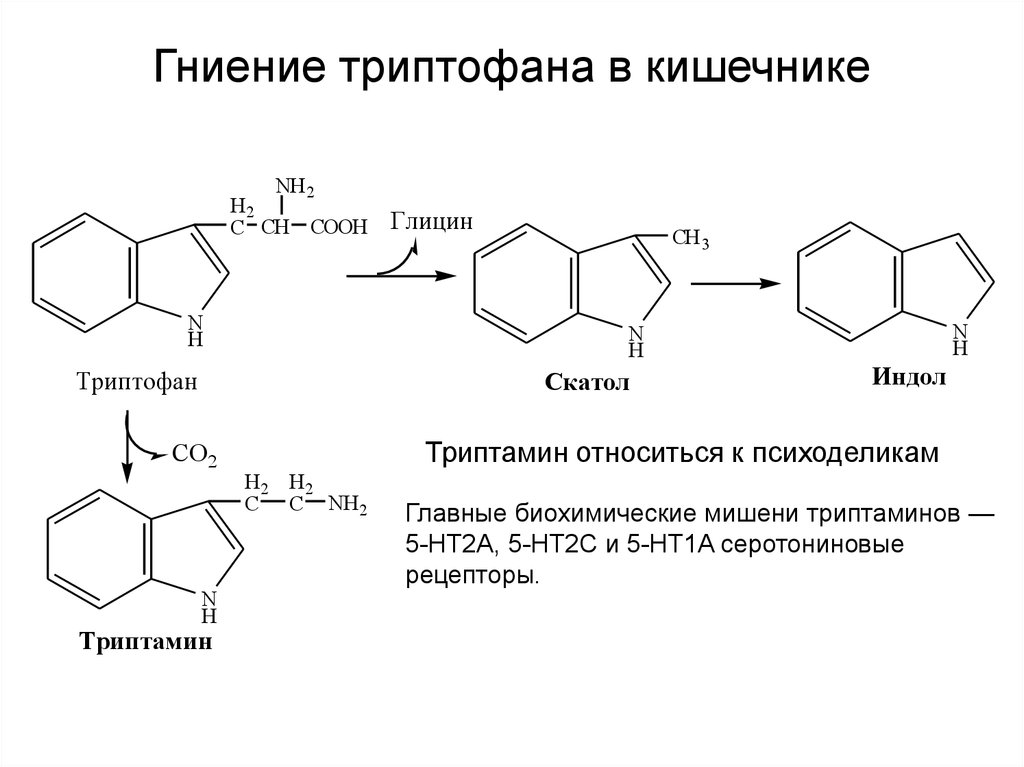
41. Гниение триптофана в кишечнике
NH 2H2
C CH COOH
N
H
Глицин
CH 3
N
H
Триптофан
Скатол
CO2
N
H
Триптамин
N
H
Индол
Триптамин относиться к психоделикам
H2 H2
C C NH 2
Главные биохимические мишени триптаминов —
5-HT2A, 5-HT2C и 5-HT1A серотониновые
рецепторы.




















 biology
biology chemistry
chemistry








