Similar presentations:
Альдегиды. Строение молекул, функциональная группа. Номенклатура, изомерия. Свойства и применение альдегидов
1.
10 КЛАСС«Альдегиды. Строение молекул, функциональная
группа. Номенклатура, изомерия. Свойства и
применение альдегидов.»
2.
Цель урока:Сформировать представление о составе, строении
физических свойствах альдегидов, закрепить навыки
в названии веществ по систематической
номенклатуре химических свойств веществ, о
способах получения на примере уксусного альдегида;
Познакомиться с качественными реакциями на
альдегидную группу.
Продолжить формирование умений и навыков в
составлении формул изомеров и гомологов
3.
Химический тренажерhttp://him.1september.ru/2008/11/2c.jpg
• К какому классу органических соединений
относится это вещество?
• Дать название этому веществу.
4.
Экспресс-опрос• 1.Сформулируйте определение понятия фенолы
• 2.Опишите физические свойства фенола
• 3.что общего в химических свойствах спиртов и
фенолов, в чем различие?
• 4.Какие типы реакций характерны для фенола?
• 5.В чем заключается взаимное влияние атомов в
молекуле фенола ?
• 6.Какие качественные реакции на фенол вам
известны ?
• 7.Какие кислородсодержащие группы вам известны?
5.
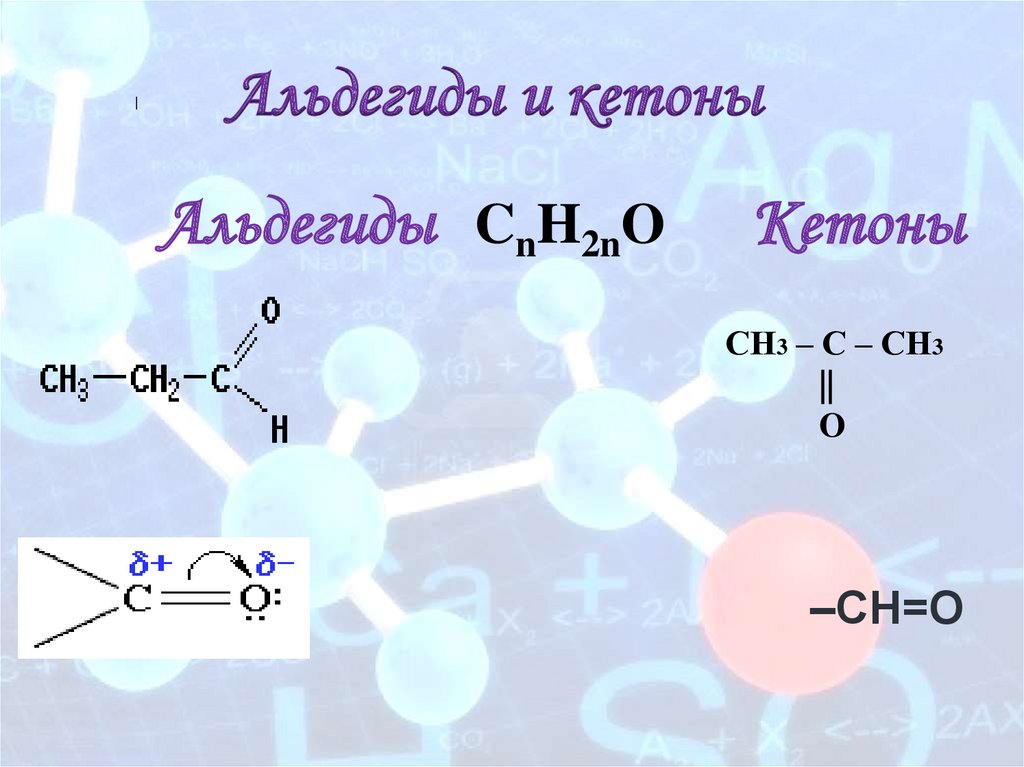
Альдегиды и кетоныАльдегиды CnH2nO
Кетоны
СН3 – С – СН3
||
O
–СН=O
6.
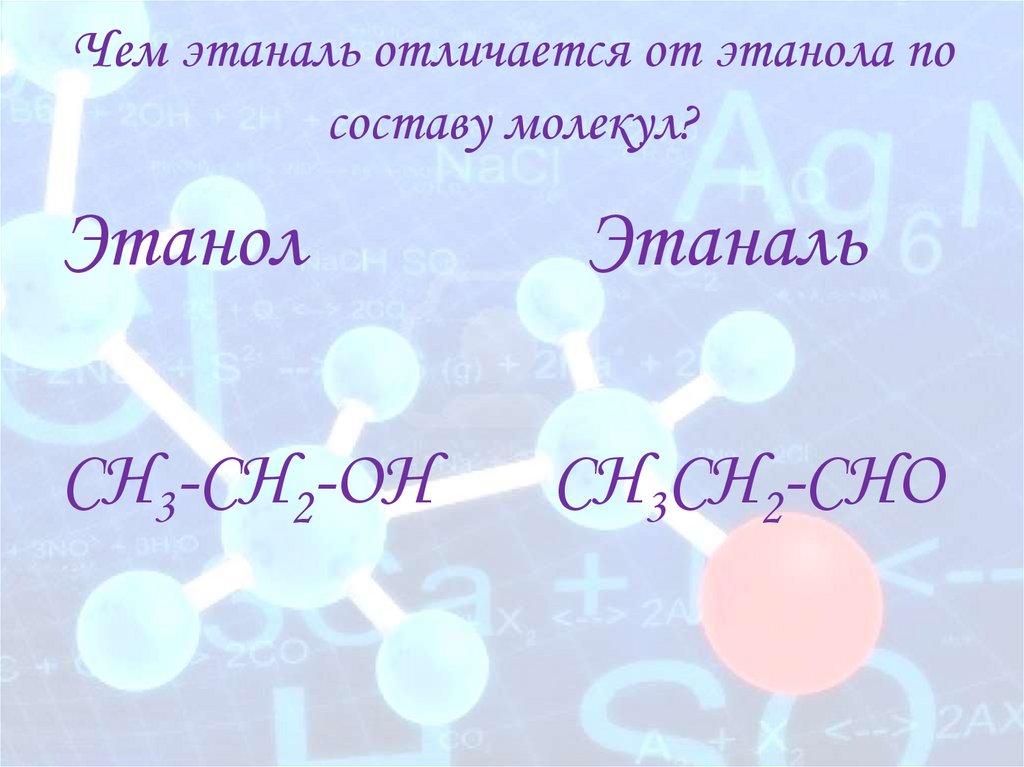
Чем этаналь отличается от этанола посоставу молекул?
Этанол
СH3-CH2-OH
Этаналь
СH3CH2-CHO
7.
Альдегиды - это органическиевещества, молекулы которых
содержат альдегидную группу,
связанную с углеводородным
радикалом.
8.
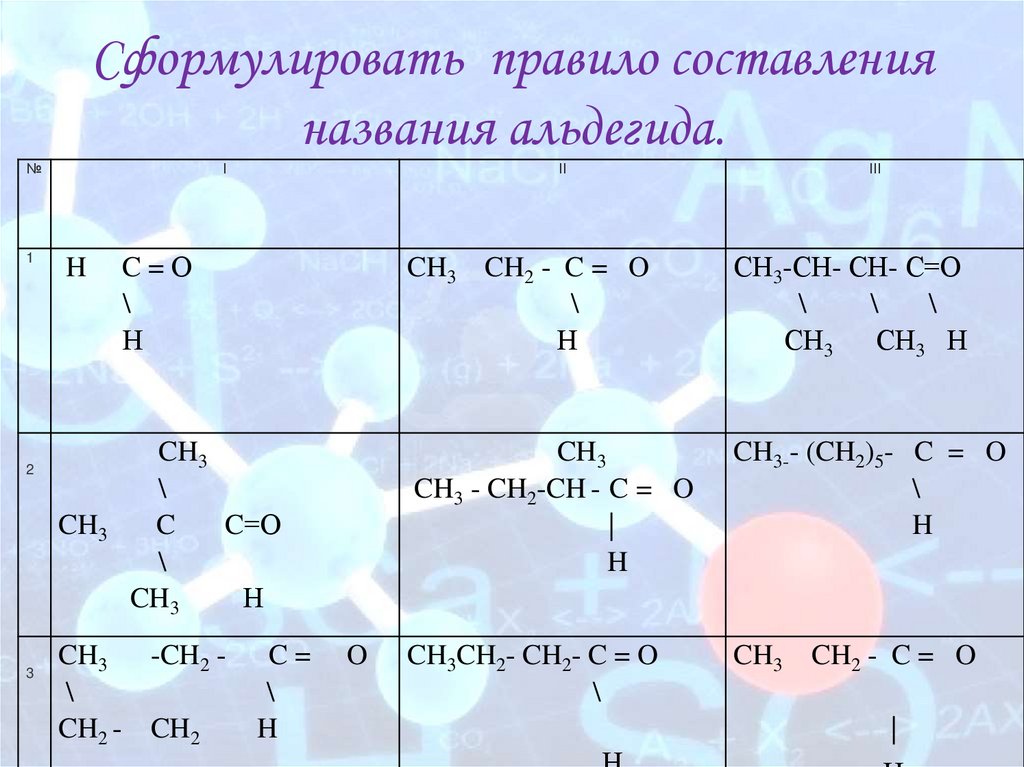
Сформулировать правило составленияназвания альдегида.
№
1
I
H
2
CH3
3
II
III
C=О
\
Н
CH3 CH2 - C = O
\
Н
СН3-СН- СН- С=О
\
\
\
СН3 СН3 Н
CH3
\
C
C=О
\
CH3
Н
CH3
CH3 - CH2-CH - C = O
|
H
CH3-- (CH2)5- C = O
\
H
CH3CH2- CH2- C = O
\
CH3 CH2 - C = O
CH3 -CH2 \
CH2 - CH2
C=
\
H
O
|
9.
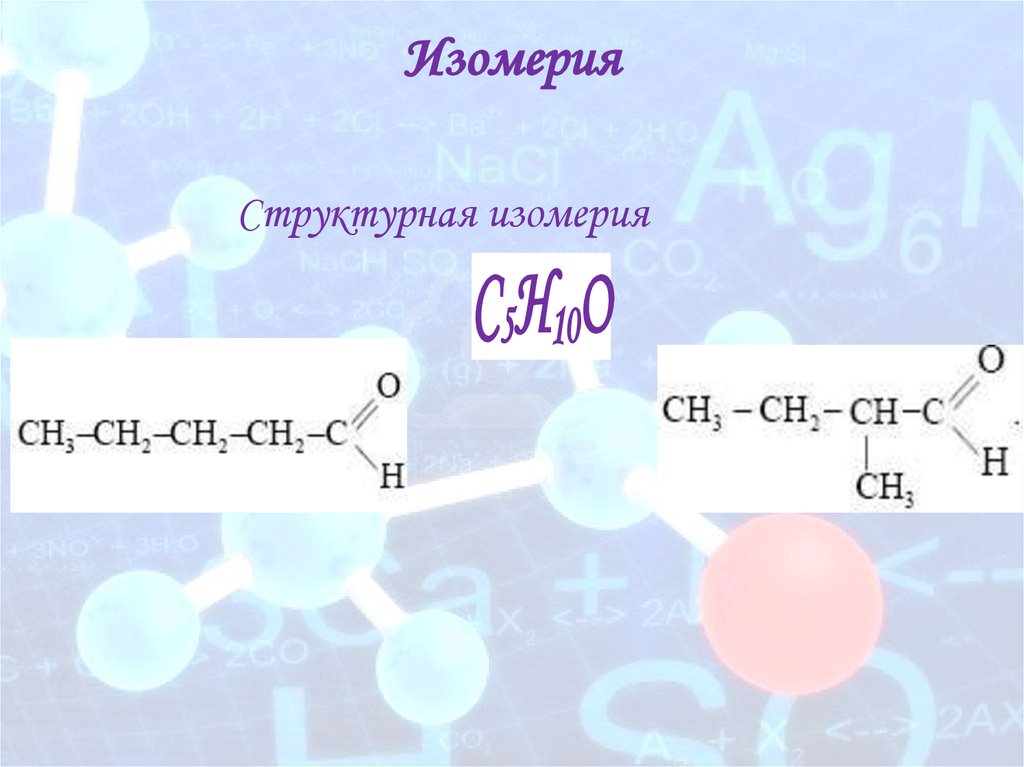
ИзомерияСтруктурная изомерия
С5Н10О
10.
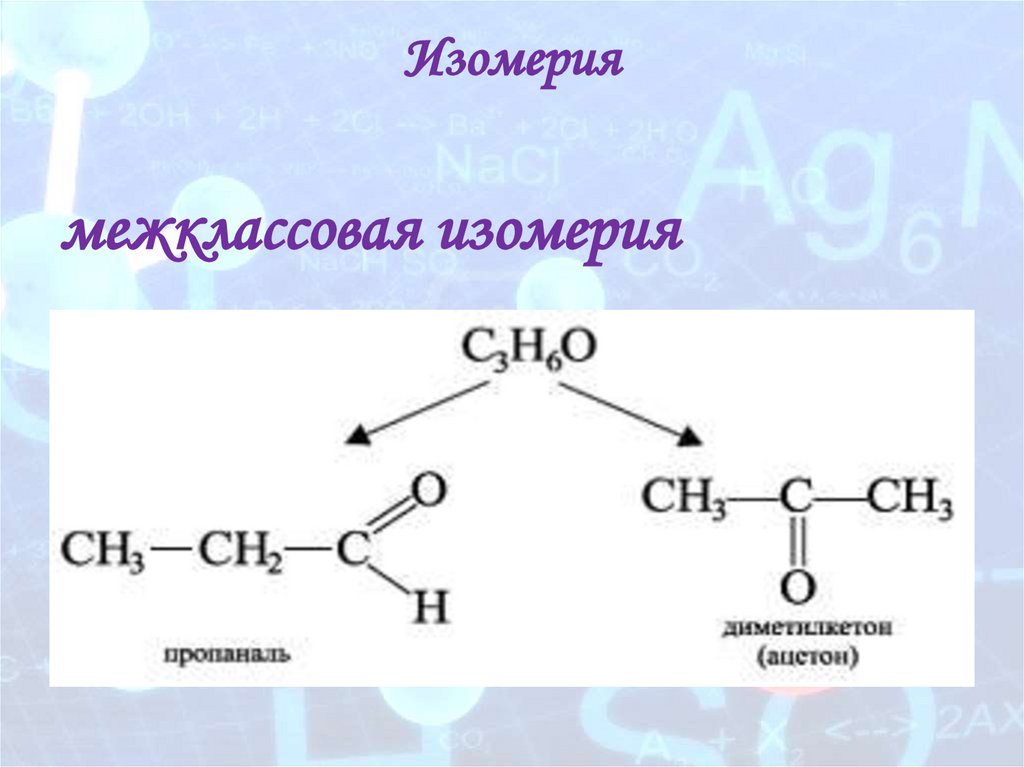
Изомериямежклассовая изомерия
11.
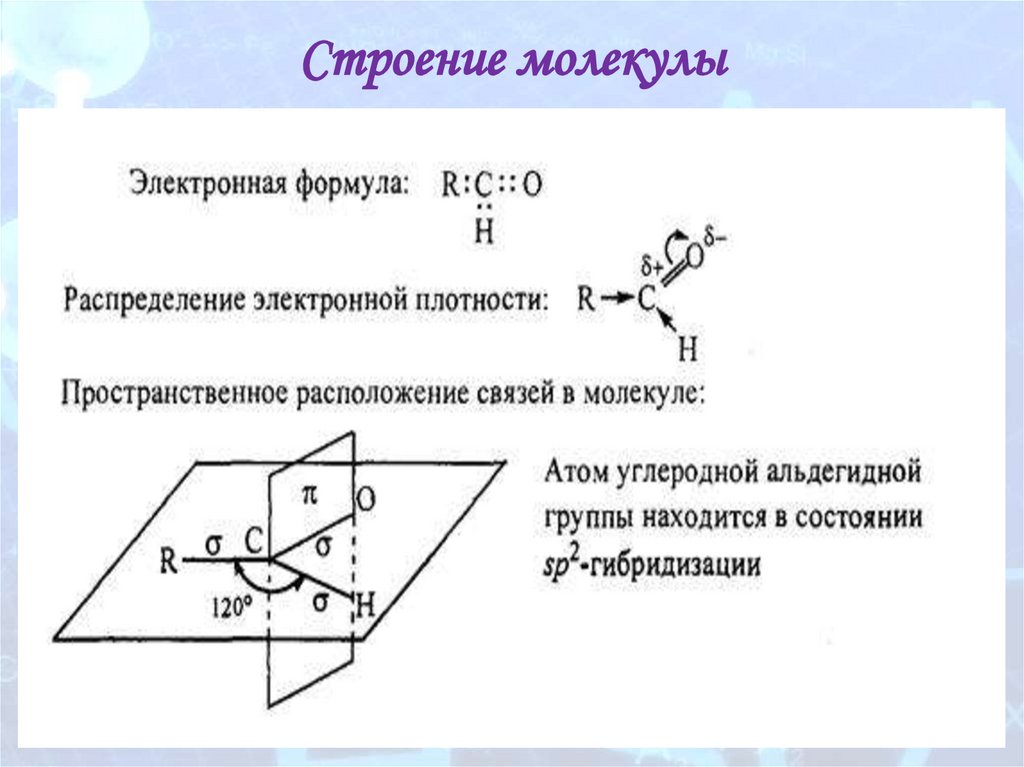
Строение молекулы12.
Физические свойства альдегидов• Метаналь (формальдегид) – газ, альдегиды С2-C5 и кетоны
С3-С4 – жидкости, высшие – твердые вещества. Низшие
гомологи растворимы в воде, благодаря образованию
водородных связей между атомами водорода молекул воды
и карбонильными атомами кислорода. С увеличением
углеводородного радикала растворимость в воде падает.
• Альдегиды обладают удушливым запахом, который при
многократном разведении становится приятным,
напоминая запах плодов. Альдегиды кипят при более
низкой температуре, чем спирты с тем же числом
углеродных атомов. Это cвязано с отсутствием в
альдегидах водородных связей. В то же время температура
кипения альдегидов выше, чем у соответствующих по
молекулярной массе углеводородов, что связано с высокой
полярностью альдегидов.
13.
14.
Видео «Реакция серебрянного зеркала»http://orgchem.ru/chem4/vid/mirror_CH2O.ht
m
15.
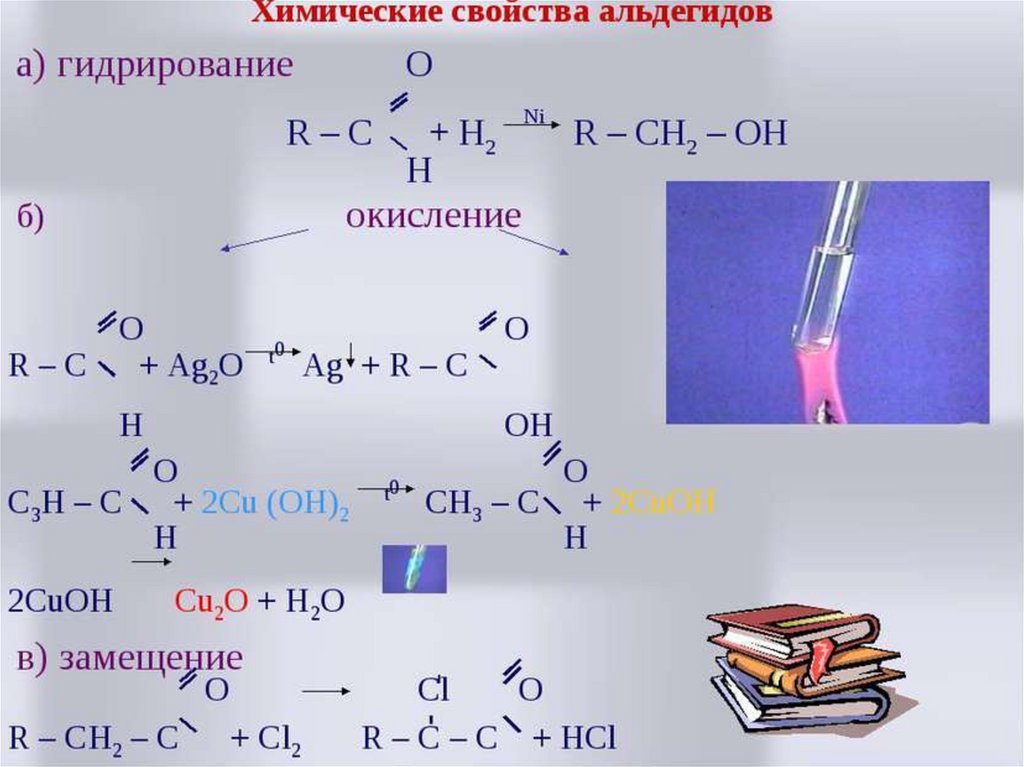
Качественная реакция на альдегиды сгидроксидом меди
https://www.youtube.com/watch?v=Nipbnb1Ya
AI&feature=youtu.be
16.
17.
18.
Применение альдегидов• Формальдегид (метаналь, муравьиный альдегид) H2C=O:
а) для получение фенолформальдегидных смол;
б) получение мочевино-формальдегидных (карбамидных)
смол;
в) полиоксиметиленовые полимеры;
г) синтез лекарственных средств (уротропин);
д) дезинфицирующее средство;
е) консервант биологических препаратов (благодаря
способности свертывать белок).
• Уксусный альдегид (этаналь, ацетальдегид) СН3СН=О:
а) производство уксусной кислоты;
б) органический синтез.









 chemistry
chemistry








