Similar presentations:
Кислоты. Повторение
1.
Урок 8 класса.Повторение
Кислоты
2.
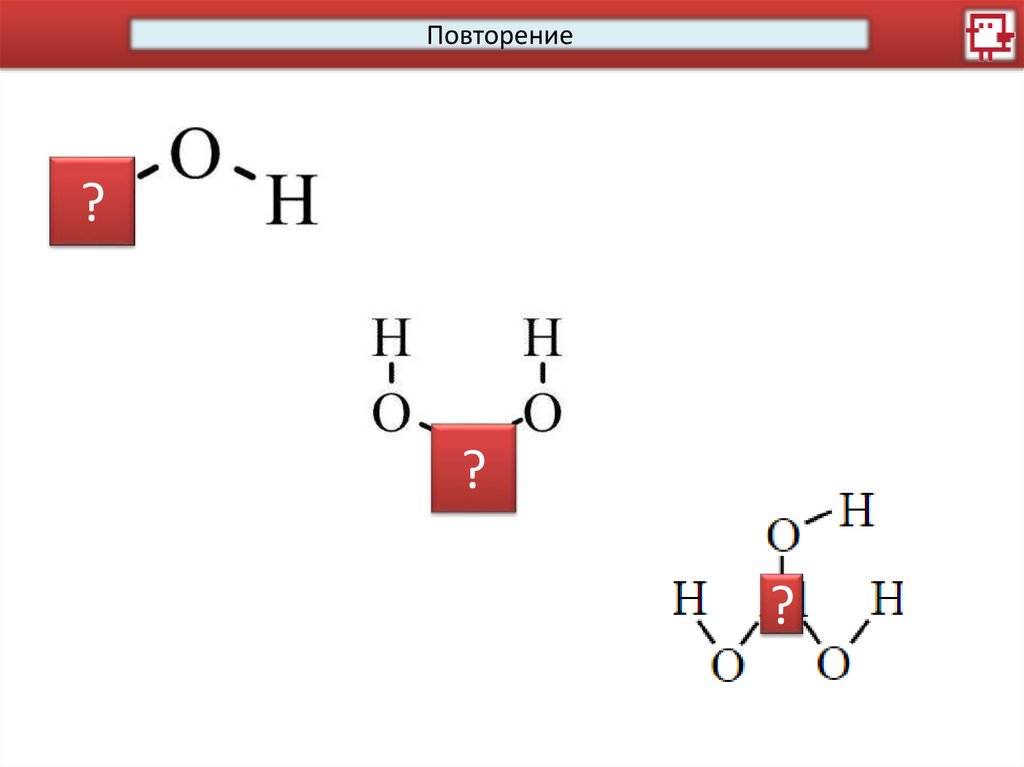
Повторение?
?
?
3.
ПовторениеCaO + H2O
CuCl2 + NaOH
Li2O + H2O
CaCO3 + SiO2
Cu(OH)2
Ca(OH)2 + CO2
CO2 + KOH
4.
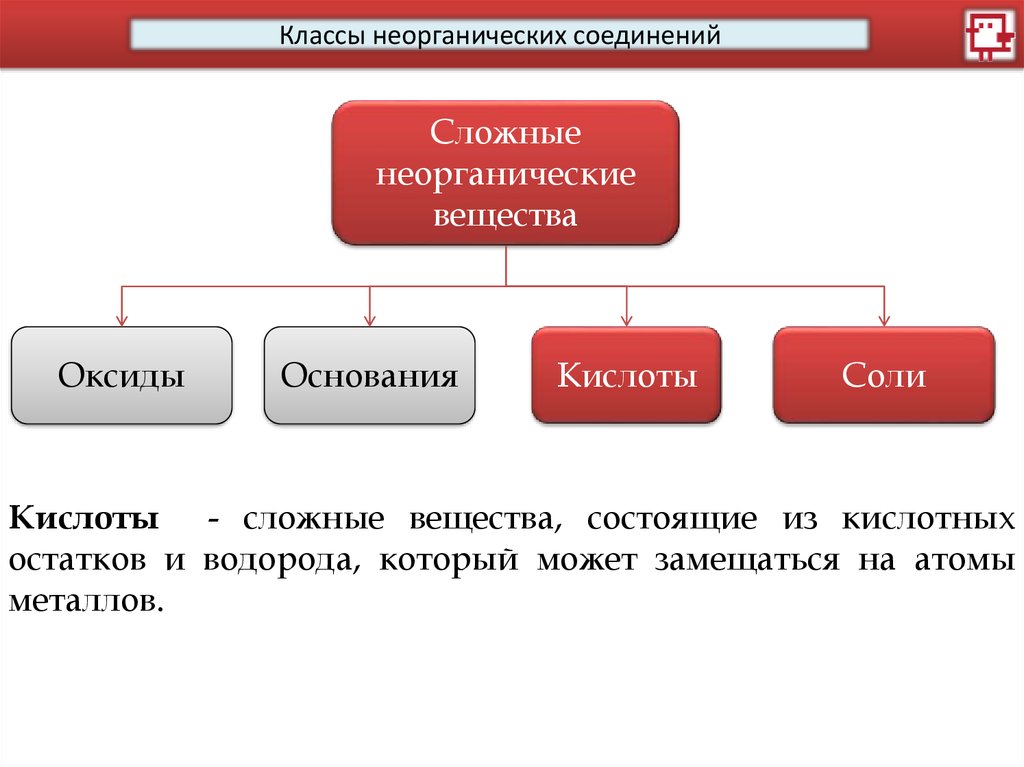
Классы неорганических соединенийСложные
неорганические
вещества
Оксиды
Основания
Кислоты
Соли
Кислоты - сложные вещества, состоящие из кислотных
остатков и водорода, который может замещаться на атомы
металлов.
5.
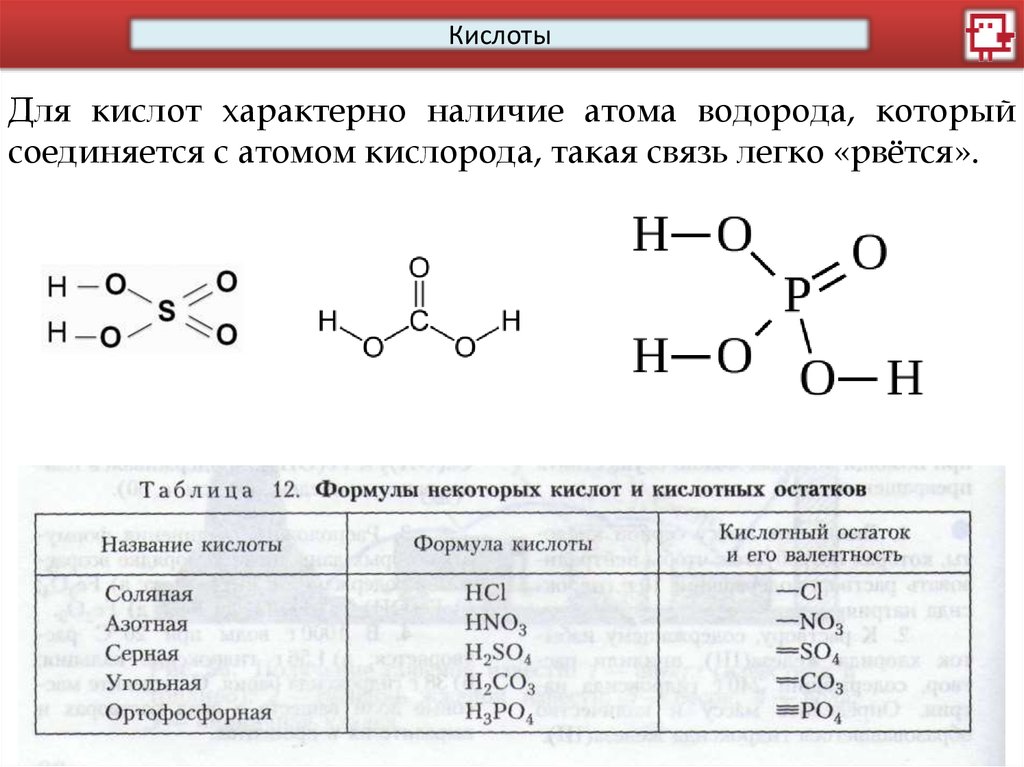
КислотыДля кислот характерно наличие атома водорода, который
соединяется с атомом кислорода, такая связь легко «рвётся».
6.
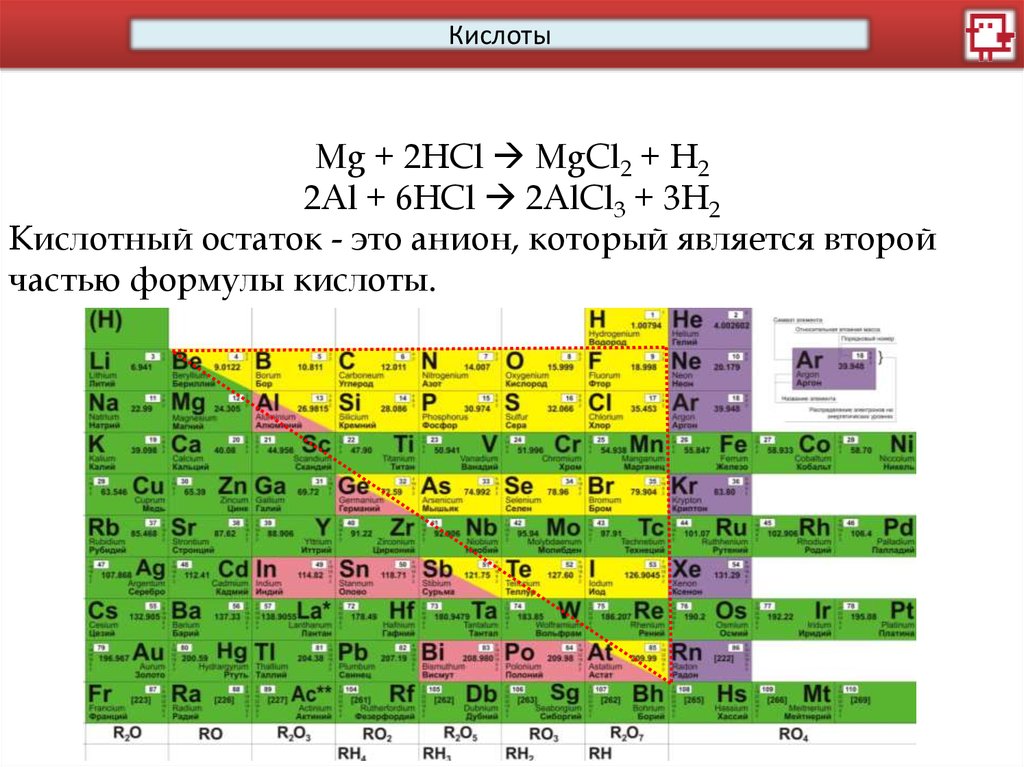
КислотыMg + 2HCl MgCl2 + H2
2Al + 6HCl 2AlCl3 + 3H2
Кислотный остаток - это анион, который является второй
частью формулы кислоты.
7.
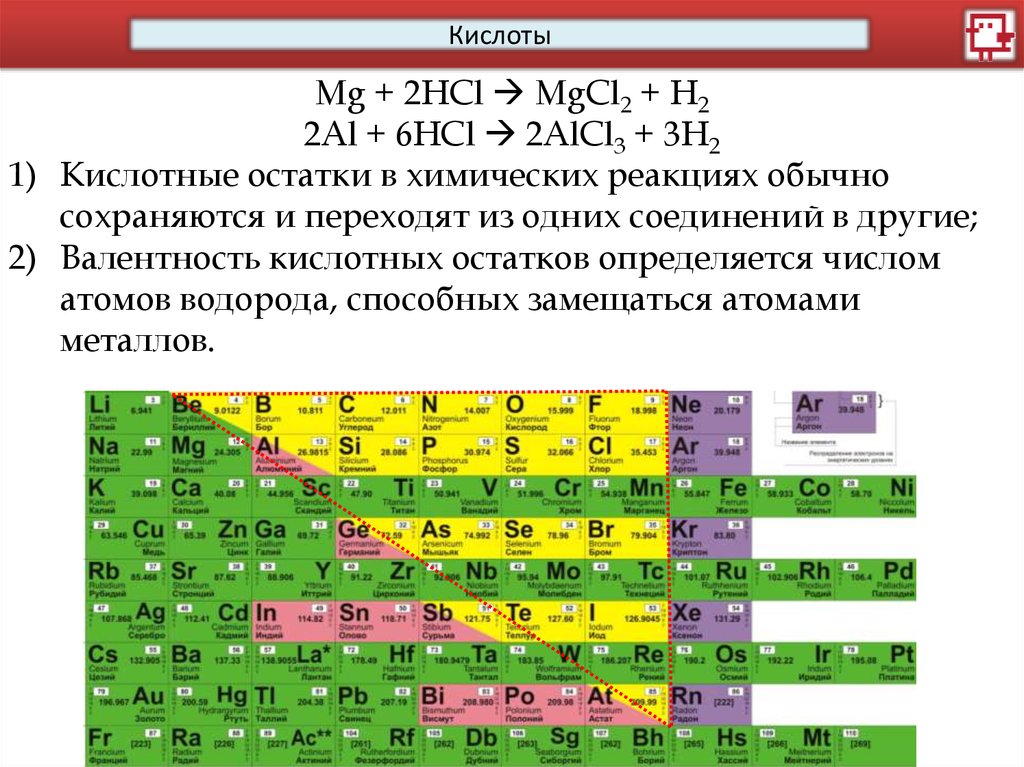
КислотыMg + 2HCl MgCl2 + H2
2Al + 6HCl 2AlCl3 + 3H2
1) Кислотные остатки в химических реакциях обычно
сохраняются и переходят из одних соединений в другие;
2) Валентность кислотных остатков определяется числом
атомов водорода, способных замещаться атомами
металлов.
8.
КислотыФизические свойства.
Многие кислоты – жидкости: серная, азотная и т.д.
Некоторые твёрдые: кремниевая H2SiO3, ортофосфорная
H3PO4, метафосфорная HPO3, борная H3BO3.
Многие из них растворимые, кроме …
9.
КислотыФизические свойства.
Многие кислоты – жидкости: серная, азотная и т.д.
Некоторые твёрдые: кремниевая H2SiO3, ортофосфорная
H3PO4, метафосфорная HPO3, борная H3BO3.
Многие из них растворимые, кроме кремниевой.
Вспоминаем: Na2SiO3 + 2HCl = H2SiO3↓ +2NaCl
10.
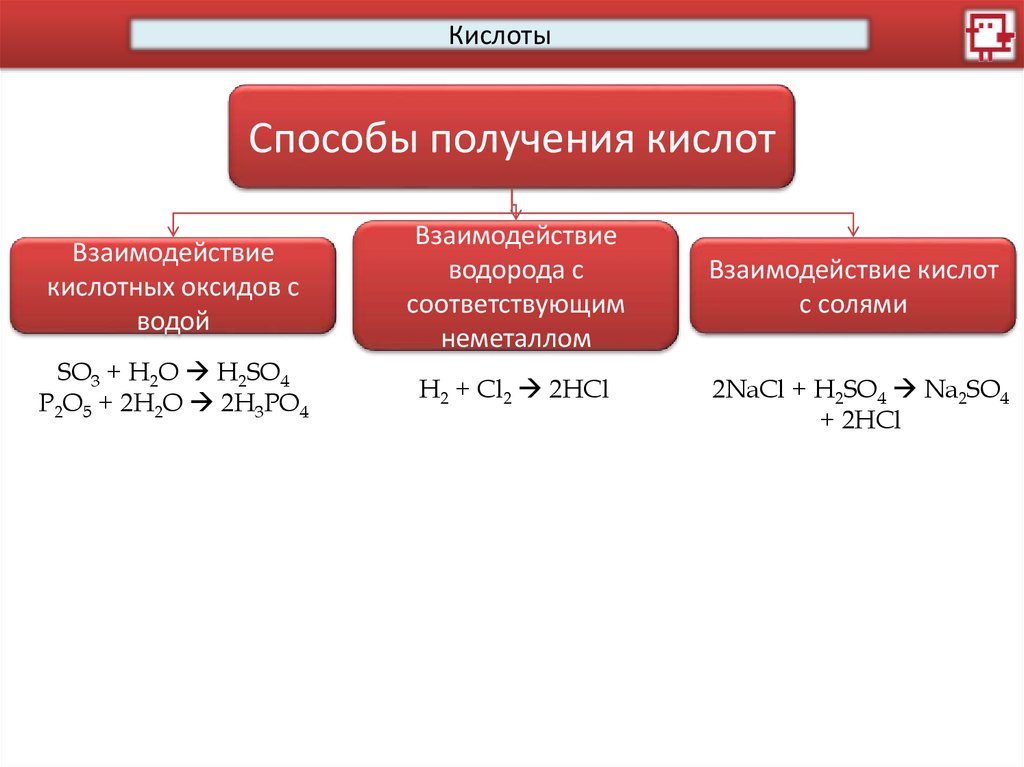
КислотыСпособы получения кислот
Взаимодействие
кислотных оксидов с
водой
Взаимодействие
водорода с
соответствующим
неметаллом
SO3 + H2O H2SO4
P2O5 + 2H2O 2H3PO4
H2 + Cl2 2HCl
Взаимодействие кислот
с солями
2NaCl + H2SO4 Na2SO4
+ 2HCl
11.
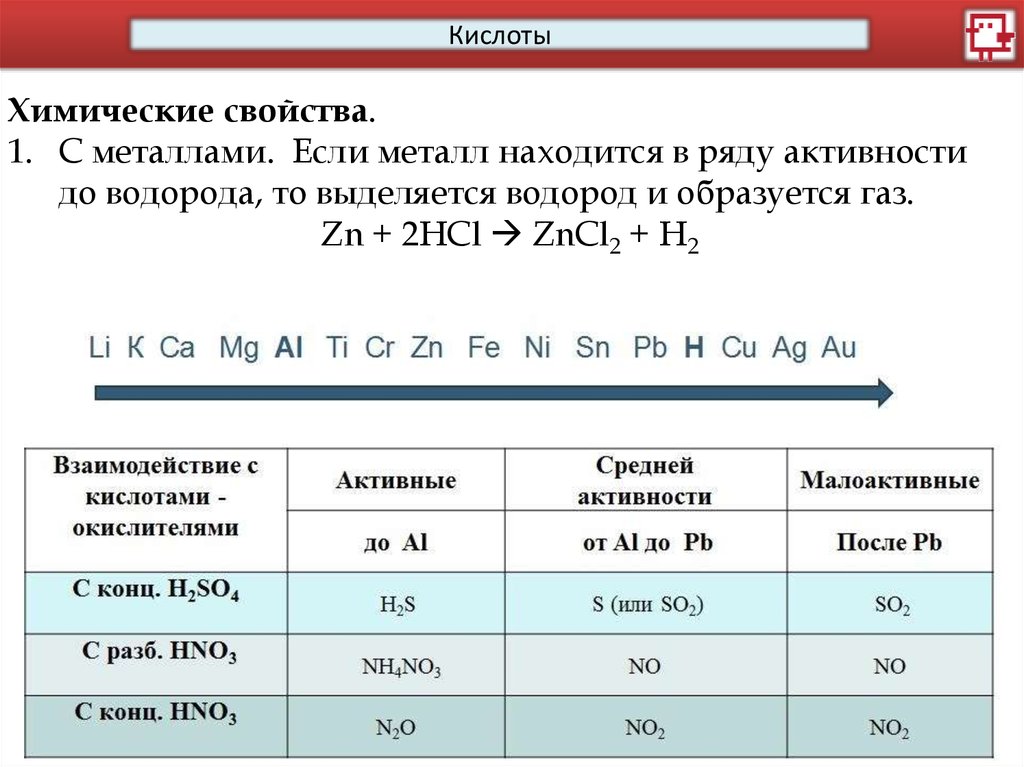
КислотыХимические свойства.
1. C металлами. Если металл находится в ряду активности
до водорода, то выделяется водород и образуется газ.
Zn + 2HCl ZnCl2 + H2
12.
КислотыХимические свойства.
2. C основными оксидами. Образуется соль и вода.
CuO + H2SO4 CuSO4 + H2O
13.
КислотыХимические свойства.
3. С основаниями. Образуется соль и вода.
NaOH + HCl NaCl + H2O
14.
КислотыХимические свойства.
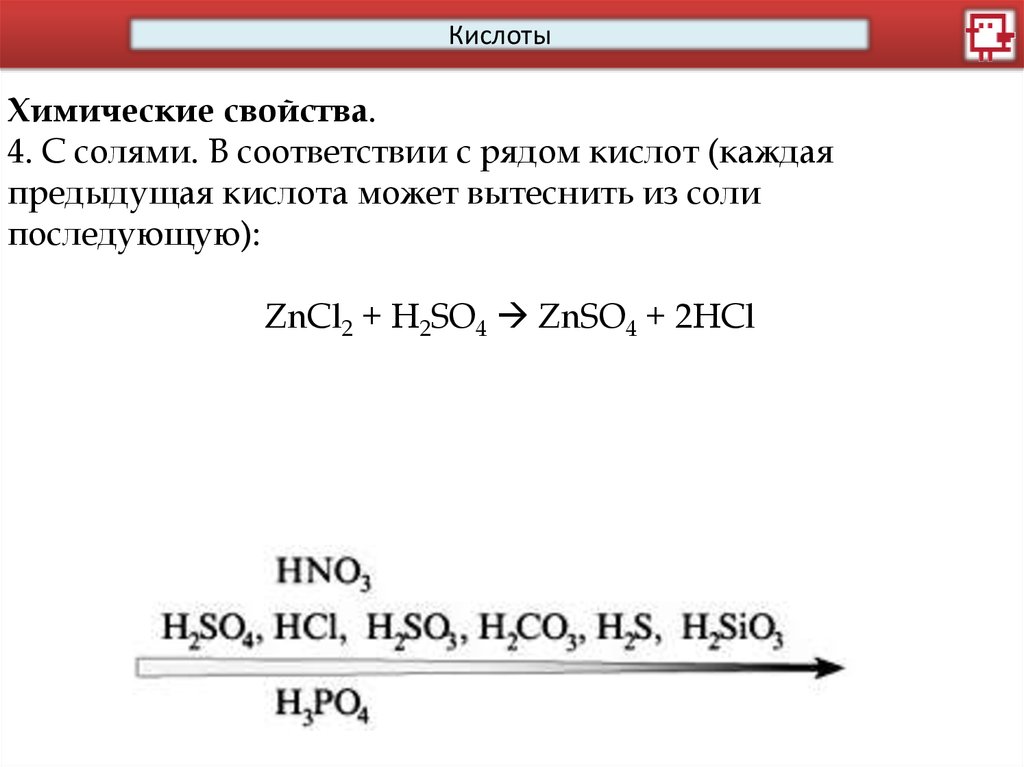
4. С солями. В соответствии с рядом кислот (каждая
предыдущая кислота может вытеснить из соли
последующую):
ZnCl2 + H2SO4 ZnSO4 + 2HCl
15.
КислотыХимические свойства.
5. При нагревании некоторые кислоты разлагаются.
H2SO3 H2O + SO2






 chemistry
chemistry








