Similar presentations:
Кислоты: классификация, номенклатура, физические и химические свойства
1.
2.
«Их получают путем горенияИли сложных веществ разложения.
В них два элемента, один – кислород.
Я отнесу к ним и известь, и лед».
Какие это вещества?
3.
Из предложенного списка выпишите формулы оксидов и основанийСaCl2; BaO; Fe(OH)2; H2SO4; HNO3; CaO;
CO2; Ca(OH)2; ZnSO4; H2SiO3; NaOH; KNO3.
Оксиды BaO; CaO; CO2,
Основания Fe(OH)2Ca(OH)2, NaOH
4.
«Ониимеют кислый вкус.
В них изменяет цвет лакмус.
с фиолетового на красный».
5.
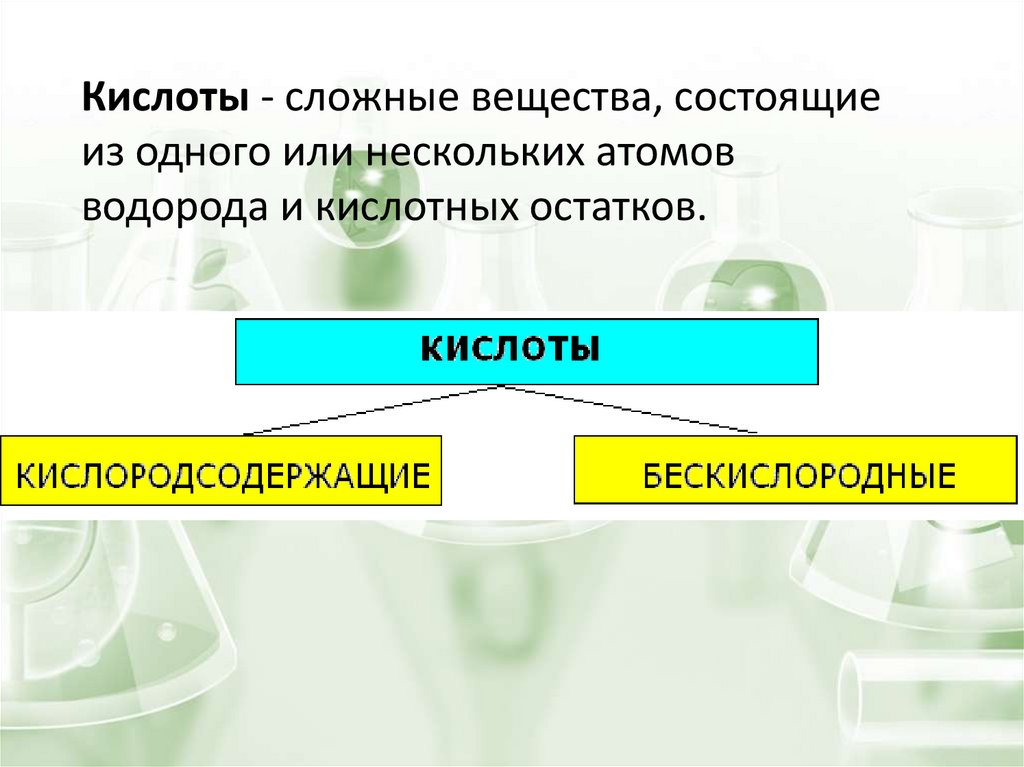
Кислоты - сложные вещества, состоящиеиз одного или нескольких атомов
водорода и кислотных остатков.
6.
Физические свойства кислотМногие кислоты, например серная, азотная,
соляная – это бесцветные жидкости. Известны
также твёрдые кислоты: ортофосфорная,
метафосфорная HPO3, борная H3BO3. Почти все
кислоты растворимы в воде. Пример
нерастворимой кислоты – кремниевая H2SiO3.
Растворы кислот имеют кислый вкус. Так,
например, многим плодам придают кислый вкус
содержащиеся в них кислоты. Отсюда названия
кислот: лимонная, яблочная и т.д.
7.
Способы получения кислотбескислородные
кислородсодержащие
HCl, HBr, HI, HF, H2S HNO3, H2SO4 и другие
ПОЛУЧЕНИЕ
1. Прямое
1. Кислотный оксид +
вода = кислота
взаимодействие
неметаллов
SO3 + H2O = H2SO4
H2 + Cl2 = 2 HCl
2. Реакция обмена между солью и менее
летучей кислотой
2 NaCl (тв.) + H2SO4(конц.) = Na2SO4 + 2HCl
8.
ИНДИКАТОРЫ (от лат. indicator –указатель) – вещества, позволяющие
следить за составом среды или за
протеканием химической реакции
9.
Химические свойства кислот1. Изменяют окраску индикаторов
10.
2.Реагируют с металлами в ряду активности до H2(искл. HNO3 –азотная кислота)
Ме + КИСЛОТА =СОЛЬ + H2↑
Zn + 2 HCl = ZnCl2 + H2
11.
3. С основными (амфотерными) оксидами –оксидами металлов
МехОу + КИСЛОТА= СОЛЬ + Н2О
CuO + H2SO4 = Cu SO4 + H2O
12.
4. Реагируют с основаниямиКИСЛОТА + ОСНОВАНИЕ= СОЛЬ+ H2O
H3PO4 + 3NaOH = Na3PO4 + 3H2O
13.
5. Реагируют с солями слабых, летучих кислот - еслиобразуется соль, выпадающая в осадок или выделяется
газ:
2 NaCl (тв.) + H2SO4(конц.) = Na2SO4 + 2HCl↑
( р. обмена)
Сила кислот убывает в ряду:
HI > HClO4 > HBr > HCl > H2SO4 > HNO3 > HMnO4 >
H2SO3 > H3PO4 > HF > HNO2 >H2CO3 > H2S > H2SiO3 .
Каждая предыдущая кислота может
вытеснить из соли последующую
14.
6. Разложение кислородсодержащих кислотпри нагревании
( искл. H2SO4 ; H3PO4 )
КИСЛОТА = КИСЛОТНЫЙ ОКСИД + ВОДА
(р. разложения )
Запомните! Неустойчивые кислоты
(угольная и сернистая) – разлагаются на
газ и воду:
H2CO3 ↔ H2O + CO2↑
H2SO3 ↔ H2O + SO2↑
15.
ХИМИЧЕСКИЕ СВОЙСТВА СОЛЯНОЙ КИСЛОТЫ16.
Составьте уравнения реакций, назовитепродукты:
Na2O + H2CO3
ZnO + HCl
CaO + HNO3
Fe2O3 + H2SO4















 chemistry
chemistry








