Similar presentations:
Органическая химия
1. Органическая химия
Центр дистанционного обученияОрганическая химия
ФИО преподавателя: Коновалова Надежда Валерьевна
e-mail: nadejda_73@mail.ru
Online-edu.mirea.ru
online.mirea.ru
2. Консультация к экзамену
Центр дистанционного обученияКонсультация к экзамену
• Теоретические
основы органической химии
• Алканы и циклоалканы
• Алкены
• Диены и алкины
• Ароматические соединения
online.mirea.ru
3.
Центр дистанционного обученияТема 1. Теоретические основы органической химии
1.1. Электронные эффекты заместителей
• Изобразите и обозначьте электронные эффекты заместителей в
молекуле 1-метоксипропена
CH3O
-I, +M
CH
CH
CH3
CH3O CH CH CH3
+I
online.mirea.ru
4.
Центр дистанционного обученияТема 1. Теоретические основы органической химии
1.1. Электронные эффекты заместителей
• Изобразите и обозначьте электронные эффекты заместителей для
нитробензола, трихлорметилбензола и анилина.
online.mirea.ru
5.
Центр дистанционного обучения• Изобразите электронные эффекты заместителей для
фенола и бензальдегида.
online.mirea.ru
6.
Центр дистанционного обучения1. Теоретические основы органической химии
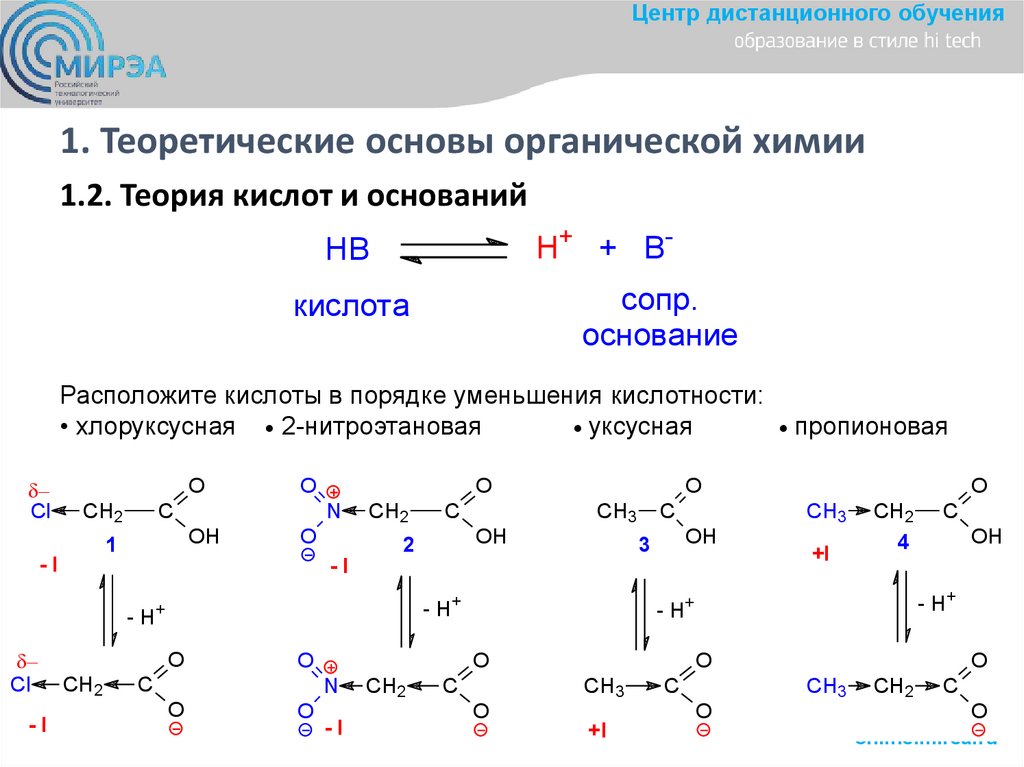
1.2. Теория кислот и оснований
H+ + B-
HB
сопр.
основание
кислота
Расположите кислоты в порядке уменьшения кислотности:
• хлоруксусная 2-нитроэтановая
уксусная
Cl
O
CH2
C
O
N
OH
1
-I
O
O
-I
CH2
-I
O
CH3
O
O
C
O
OH
-I
CH2
O
CH3
+I
CH2
4
C
O
C
OH
- H+
- H+
O
N
O
C
3
- H+
-H
CH2
OH
2
+
Cl
C
пропионовая
O
CH3
+I
C
O
O
CH3
CH2
C
O
online.mirea.ru
7.
Центр дистанционного обучения1. Теоретические основы органической химии
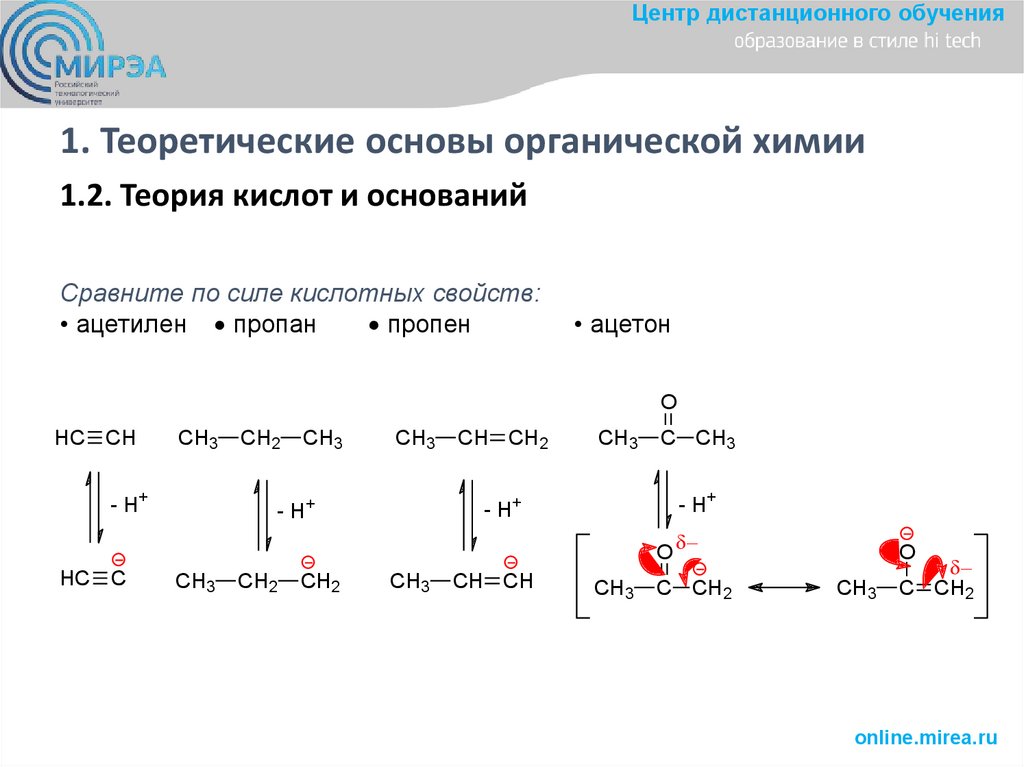
1.2. Теория кислот и оснований
Сравните по силе кислотных свойств:
• ацетилен пропан
пропен
• ацетон
O
HC CH
CH3
- H+
CH2
CH3
CH3
CH CH2
CH3
- H+
- H+
- H+
C CH3
O
HC C
CH3
CH2
CH2
CH3
CH CH
CH3
C CH2
O
CH3
C CH2
online.mirea.ru
8.
Центр дистанционного обучения1. Теоретические основы органической химии
1.2. Теория кислот и оснований
Сравните по основности (ответ обоснуйте):
• этанол
этиламин
этантиол
C2H5
OH
C2H5
NH2
C2H5
хлорэтан
SH
C2H5
Сравните по основности (ответ обоснуйте):
• ацетат натрия
этилат натрия
гидроксид натрия
O
CH3 C
O Na
O
CH3
C
O
C2H5
O Na
Na OH
Cl
амид Na
Na NH2
online.mirea.ru
9.
Центр дистанционного обучения1. Теоретические основы органической химии
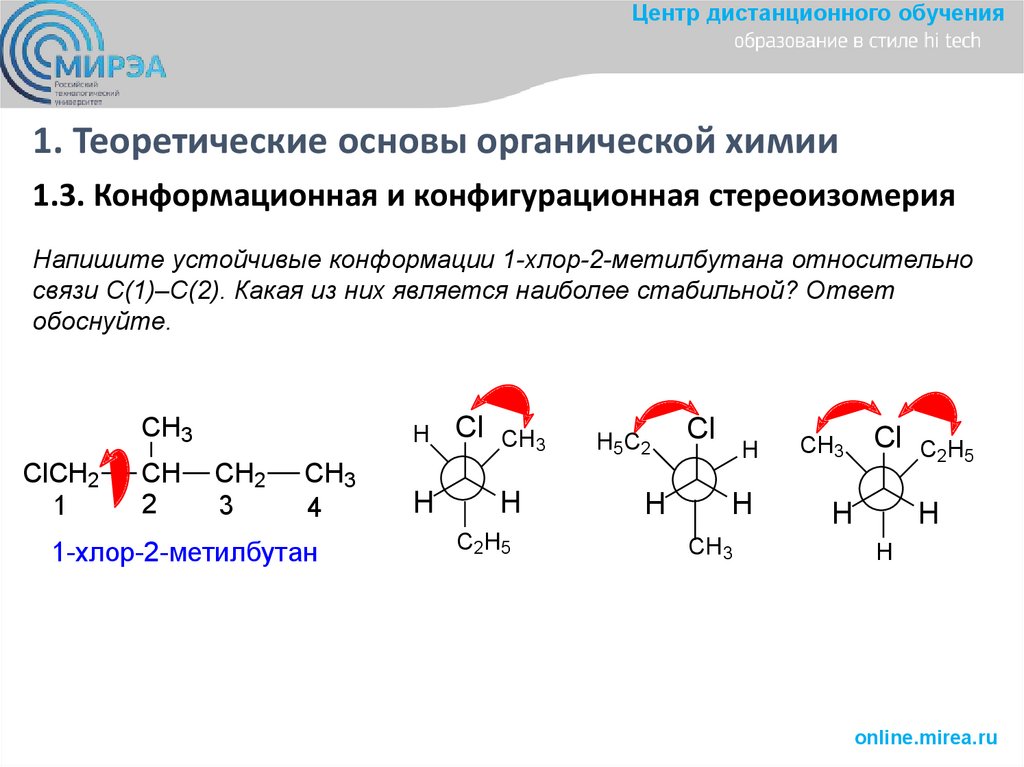
1.3. Конформационная и конфигурационная стереоизомерия
Напишите устойчивые конформации 1-хлор-2-метилбутана относительно
связи С(1)‒С(2). Какая из них является наиболее стабильной? Ответ
обоснуйте.
CH3
ClCH2
1
CH
2
H
CH2
3
CH3
4
1-хлор-2-метилбутан
H
Cl CH3
H
C2H5
H5C2
H
Cl
H
H
CH3
CH3
Cl C2H5
H
H
H
online.mirea.ru
10.
Центр дистанционного обучения1. Теоретические основы органической химии
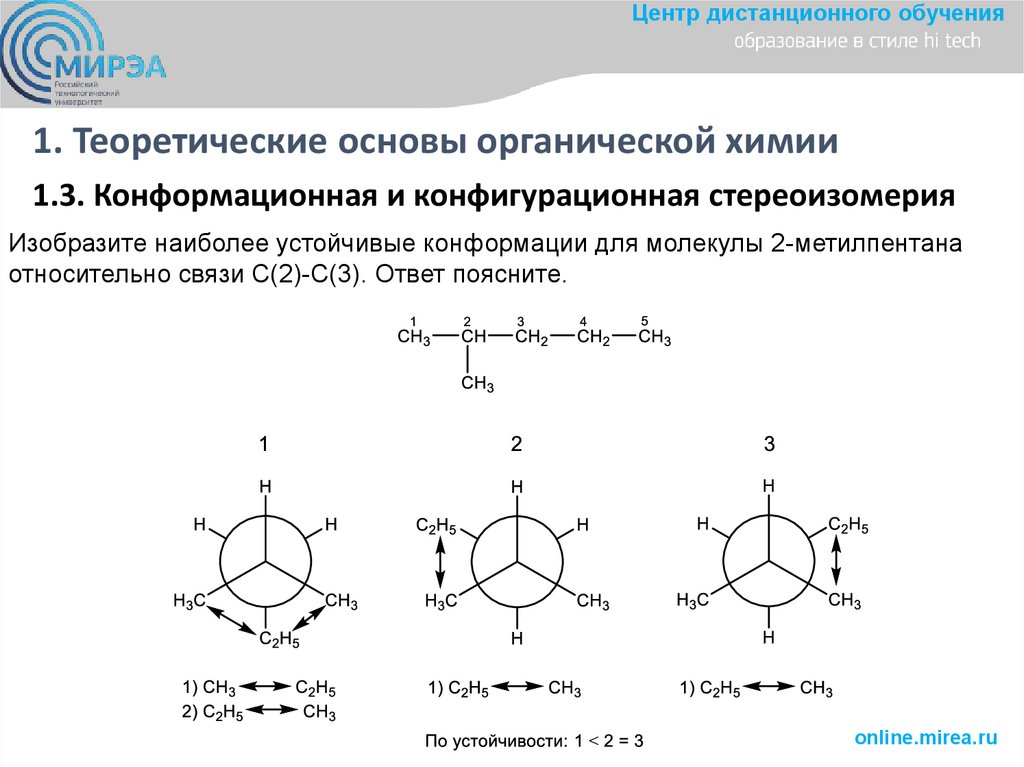
1.3. Конформационная и конфигурационная стереоизомерия
Изобразите наиболее устойчивые конформации для молекулы 2-метилпентана
относительно связи С(2)-С(3). Ответ поясните.
online.mirea.ru
11. 1. Теоретические основы органической химии 1.3. Конформационная и конфигурационная стереоизомерия
Центр дистанционного обучения1. Теоретические основы органической химии
1.3. Конформационная и конфигурационная стереоизомерия
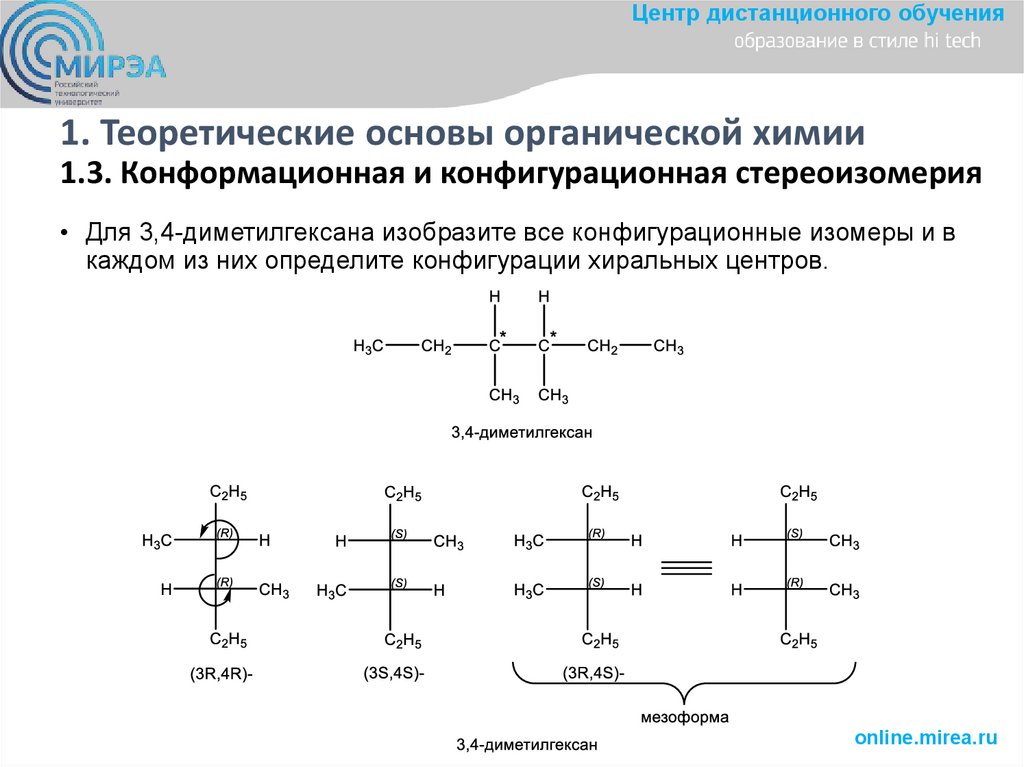
• Для 3,4-диметилгексана изобразите все конфигурационные изомеры и в
каждом из них определите конфигурации хиральных центров.
online.mirea.ru
12.
Центр дистанционного обученияТема 2. Алканы и циклоалканы
2.1. Алканы
Способы получения:
• каталитическое гидрирование алкенов и алкинов,
• из алкилгалогенидов восстановлением, реакцией Вюрца,
• из оксосоединений восстановлением по Кижнеру – Вольфу
и по Клемменсену,
• из карбоновых кислот декарбоксилированием.
online.mirea.ru
13.
Центр дистанционного обучения• Получите 2,5-диметилгексан: а) из соответствующего
алкена; б) из 2,5-диметил-3-гексанона.
А) из соответствующего алкена:
Б) из 2,5-диметил-3-гексанона:
online.mirea.ru
14.
Центр дистанционного обученияХимические свойства алканов
Характерны реакции SR
Механизм: цепная свободно-радикальная реакция
1 стадия – инициирование (образование радикалов)
2 стадия – рост цепи:
Cl• + H : CH3 → HCl + •CH3
•CH3 + Cl :Cl → Cl‒CH3 + •Cl
online.mirea.ru
15.
Центр дистанционного обучения• Хлорирование пропана
CH3CH2CH3
Cl2, hn
_ HCl CH3CH2CH2Cl + CH3CHCH3
1-хлорпропан
Cl
(пропилхлорид) 2-хлорпропан
(изопропилхлорид)
Соотношение продуктов
Условия
CH3
CH2 CH2Cl
(A)
CH3
CH CH3
Cl
hn, T = 20 °C
43%
57%
T = 300 °C
75%
25%
(B)
online.mirea.ru
16.
Центр дистанционного обученияСтабильность алкильных радикалов и скорость
разрыва связей растет в ряду:
СН4
< C(перв)‒Н < C(втор)‒Н < C(трет)‒Н
Условия
активность
(скорость)
падает
Соотношение скоростей
C(перв)‒Н
C(втор)‒Н
C(трет)‒Н
Cl• , 20 °C, hn
1
4
5
Br• , 20 °C, hn
1
100
200
селективность
растет
Cl , hn
CH3CH2CH3 _ 2
CH3CH2CH2Cl + CH3CHCH3
HCl
Cl
(А)
(В)
А / B = (1 6) / (4 2) = 6 / 8 = 3 / 4 – соотношение продуктов
online.mirea.ru
17.
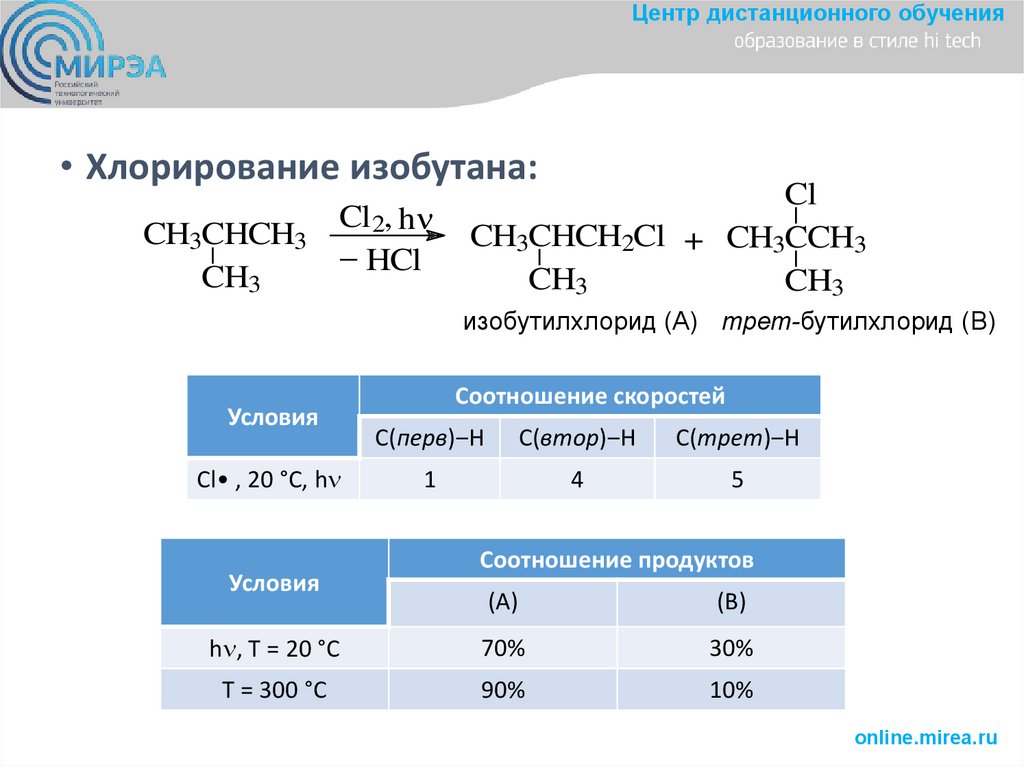
Центр дистанционного обучения• Хлорирование изобутана:
CH3CHCH3
CH3
Cl2, hn
_ HCl
Cl
CH3CHCH2Cl + CH3CCH3
CH3
CH3
изобутилхлорид (А) трет-бутилхлорид (В)
Условия
Cl• , 20 °C, hn
Условия
Соотношение скоростей
C(перв)‒Н
C(втор)‒Н
C(трет)‒Н
1
4
5
Соотношение продуктов
(A)
(B)
hn, T = 20 °C
70%
30%
T = 300 °C
90%
10%
online.mirea.ru
18.
Центр дистанционного обучения• Напишите реакцию 2,4-диметилпентана и хлора при облучении. Для
одного из продуктов этой реакции, имеющего асимметрический атом
углерода, изобразите проекционные формулы Фишера. Определите их
конфигурации.
online.mirea.ru
19.
Центр дистанционного обучения*
online.mirea.ru
20.
Центр дистанционного обучения• Получите 2,5-диметилгексан из 2-метилпропана
online.mirea.ru
21.
Центр дистанционного обучения• Бромирование изобутана
CH3
Br
Br2
CH CH3
CH3
0
hn, 20 C
CH3
C CH3
CH3
трет-бутилбромид
(96%)
0
Br2, 350 C
трет. / перв. = 200 1 / 1 9 = 96 / 4
CH3
CH CH2
Br
Региоселективный процесс
CH3
изобутилбромид
(90%)
Условия
Br• , 20 °C, hn
Соотношение скоростей
C(перв)‒Н
C(втор)‒Н
C(трет)‒Н
1
100
200
online.mirea.ru
22.
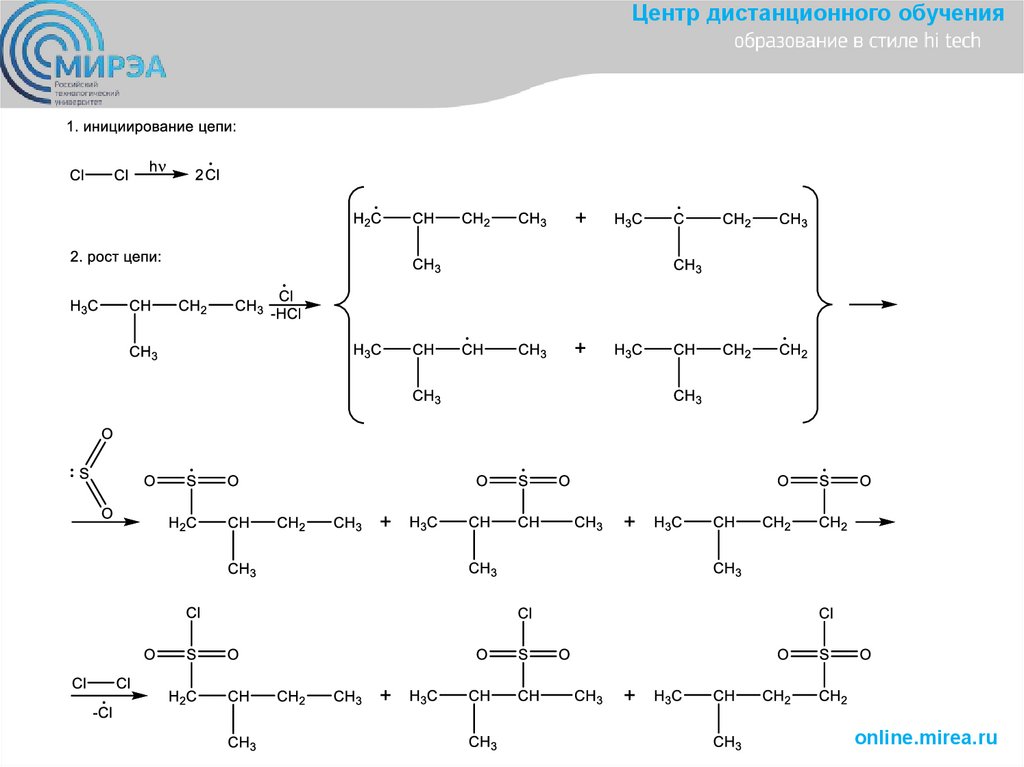
Центр дистанционного обучения• 1.2. Реакции сульфогалогенирования
(сульфохлорирования, сульфобромирования)
R H + Cl2 +
SO2
hn
или Т
R SO2Cl + HCl
алкансульфохлорид
• Особенность реакции сульфогалогенирования:
CH3
CH3
CH CH2 CH3
2-метилбутан
SO2, Cl2
0
hn, 20 C
Cl
O
CH3
CH3
S CH2
CH CH2 CH3
+ CH3 CH CH2 CH2 SOCl2 +
O
CH3
+ CH3 CH CH CH3
SOCl2
По третичному атому С продукт не образуется!!!
online.mirea.ru
23.
Центр дистанционного обученияonline.mirea.ru
24.
Центр дистанционного обученияonline.mirea.ru
25.
Центр дистанционного обучения• 1.4. Нитрование
А) Жидкофазное нитрование разбавленной азотной кислотой (15%) при t = 140 0С
(реакция М.И. Коновалова)
R H
HNO3
_
H2O
R NO2
Региоселективность:
Механизм:
CH3CHCH3
CH3
HNO3
_
H2O
NO2
CH3CCH3
CH3
2-метил-2-нитропропан
Б) Нитрование концентрированной азотной кислотой в газовой фазе (t = 400 0С)
CH3CH2CH3
HNO3, t
CH3CH2CH2NO2 + CH3CHCH3 + CH3CH2NO2 + CH3NO2
NO2
online.mirea.ru
26.
Центр дистанционного обучения3. Пиролиз и крекинг алканов
Крекинг – 600‒700 °С – более крупные фрагменты
Пиролиз – 700‒900 °С – более мелкие фрагменты
CH3CH2CH2CH3
CH3 +
CH3CH2CH2CH3
CH3CH2 + CH2CH3
CH3CH2 + CH2CH3CH3
CH4 + CH2=CHCH3
CH2CH2CH3
CH3CH3 + CH2=CH2
CH2=CH2 + CH3CH2CH3
Общая схема:
CH3CH2CH2CH3
t
CH4 + CH3CH3 + CH3CH2CH3 +
CH2=CH2 +
CH2=CHCH3
online.mirea.ru
27. 2.2. Циклоалканы
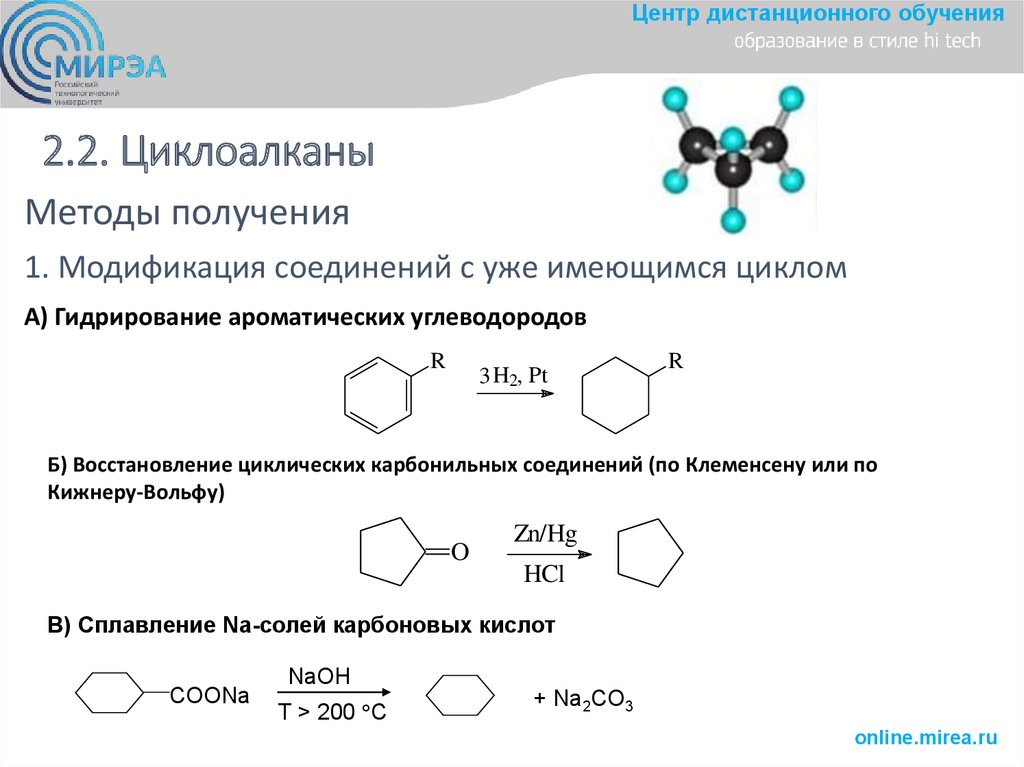
Центр дистанционного обучения2.2. Циклоалканы
Методы получения
1. Модификация соединений с уже имеющимся циклом
А) Гидрирование ароматических углеводородов
R
3 H2, Pt
R
Б) Восстановление циклических карбонильных соединений (по Клеменсену или по
Кижнеру-Вольфу)
O
Zn/Hg
HCl
В) Сплавление Na-солей карбоновых кислот
COONa
NaOH
T > 200 C
+ Na2CO3
online.mirea.ru
28.
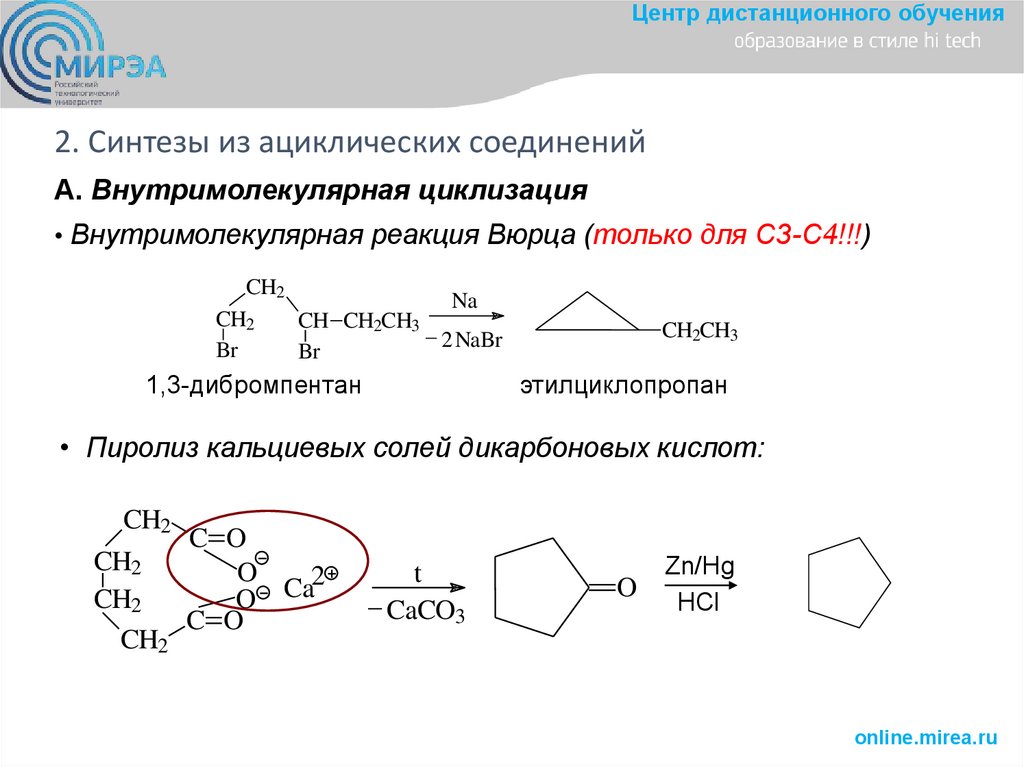
Центр дистанционного обучения2. Синтезы из ациклических соединений
А. Внутримолекулярная циклизация
• Внутримолекулярная реакция Вюрца (только для С3-С4!!!)
CH2
Na
CH2
CH CH2CH3 _
2 NaBr
Br
Br
CH2CH3
этилциклопропан
1,3-дибромпентан
• Пиролиз кальциевых солей дикарбоновых кислот:
CH2
CH2
CH2
CH2
C O
O
2
Ca
O
C O
t
_ CaCO
3
O
Zn/Hg
HCl
online.mirea.ru
29.
Центр дистанционного обученияБ) Межмолекулярная циклизация (циклоприсоединение)
• [2+1]-циклоприсоединение – реакция алкенов (С2) с карбенами (С1)
●
Карбены - нейтральные нестабильные частицы общей формулы R1-С -R2
диазометан
Синхронное взаимодействие:
#
Сохранение конфигурации
исходного алкена!!!
цис-2-бутен
цис-1,2-диметилциклопропан
online.mirea.ru
30.
Центр дистанционного обучения• [2+4]-циклоприсоединение – реакция Дильса-Альдера:
реакция диенов с алкенами циклогексены
+
T, C
переходное
состояние
транс-алкен
Н2/Pd
#
циклогексен
циклогексан
цис-алкен
транс-
Конфигурация алкена и диена сохраняются!!!
цисonline.mirea.ru
31.
Центр дистанционного обученияСтабильная конформация циклогексана - «кресло»
Ha
Ha
He
He
Ha
Ha
He
He
He
He
He
He
He
Ha
Ha
Ha
Ha
Ha
Ha
He
He
He
Ha
50%
а е
е а
Ha
50%
• Замещенные циклогексаны
Ha
R (а)
Ha
R (е)
Между аксиальными заместителями –
1,3-диаксиальные отталкивания –
конформация нестабильна
(5%)
Конформация стабильна
(95%)
online.mirea.ru
32.
Центр дистанционного обучения• Дизамещенные циклогексаны
транс-1-метил-2-изопропилциклогексан
Н
CH(CH3)2
Н
(а)
CH(CH3)2
Н
CH3
CH3 (а)
Н
два 1,3-диаксиальных отталкивания СН3 – Н;
два 1,3-диаксиальных отталкивания СН(СН3)2 – Н –
энергетически невыгодна
(е)
(е)
нет диаксиальных отталкиваний –
более устойчива
цис-1-метил-2-изопропилциклогексан
Н
Н
CH(CH3)2
CH3
два 1,3-диаксиальных отталкивания
СН(СН3)2 – Н
Н
H3C
Н
CH(CH3)2
два 1,3-диаксиальных отталкивания
online.mirea.ru
СН3 – Н
33.
Центр дистанционного обученияХимические свойства циклоалканов
1. Циклопропан и гомологи
А) реакции с разрывом С-С-связи (1,2-присоединение)
H2, Ni
50o C
Br2
t
HCl
CH3 CH2 CH3
CH2 CH2 CH2
Br
Br
CH3 CH2 CH2
Cl
Б) реакции с сохранением цикла (в мягких условиях) - SR
Cl2
hn, 20 C
Cl
+ HCl
В) реакции изомеризации
online.mirea.ru
34.
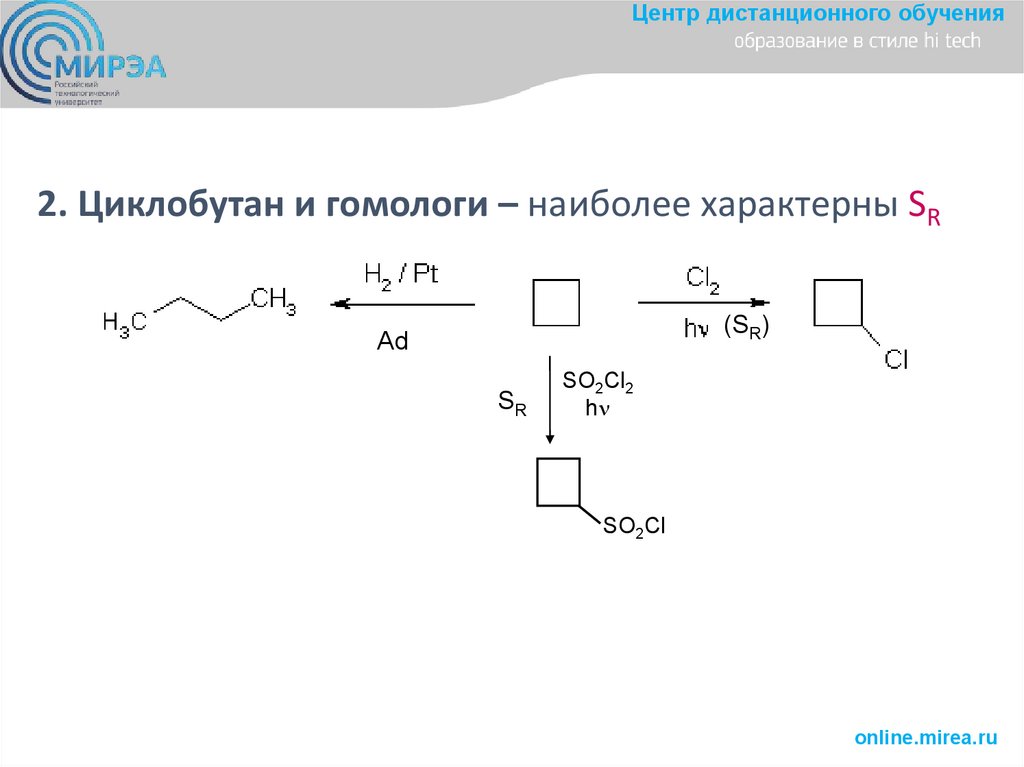
Центр дистанционного обучения2. Циклобутан и гомологи – наиболее характерны SR
(SR)
Ad
SR
SO2Cl2
hn
SO2Cl
online.mirea.ru
35.
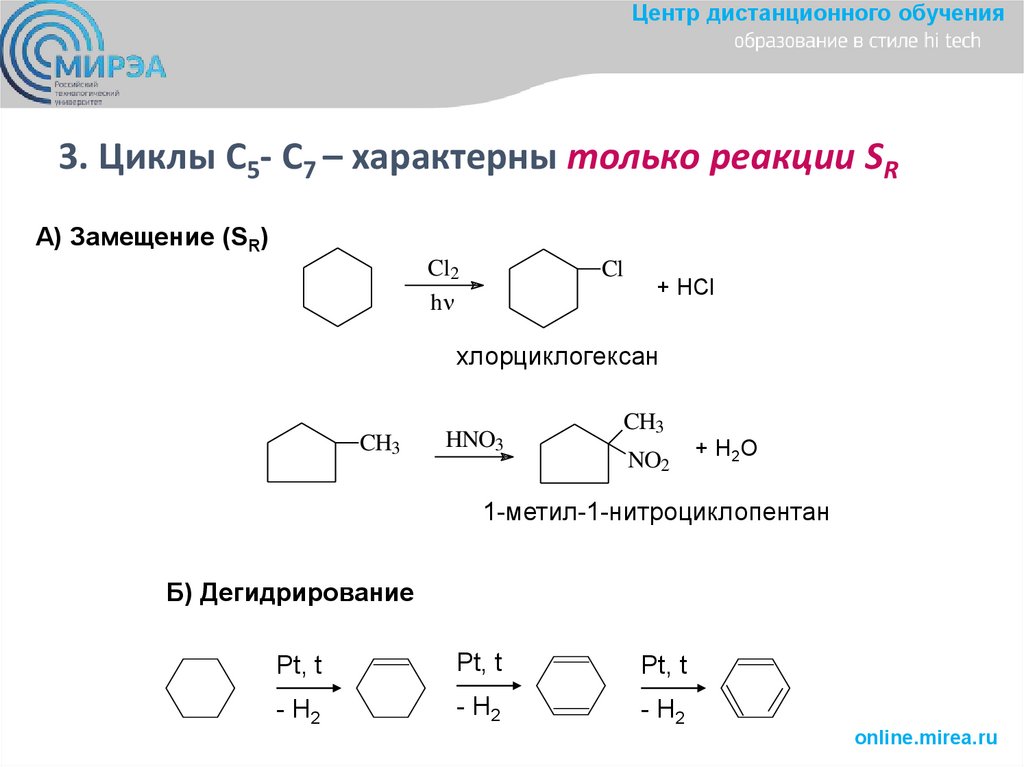
Центр дистанционного обучения3. Циклы С5- С7 – характерны только реакции SR
А) Замещение (SR)
Cl2
hn
Cl
+ HCl
хлорциклогексан
CH3
HNO3
CH3
NO2
+ H2O
1-метил-1-нитроциклопентан
Б) Дегидрирование
Pt, t
Pt, t
Pt, t
- H2
- H2
- H2
online.mirea.ru
36. Тема 3. Алкены
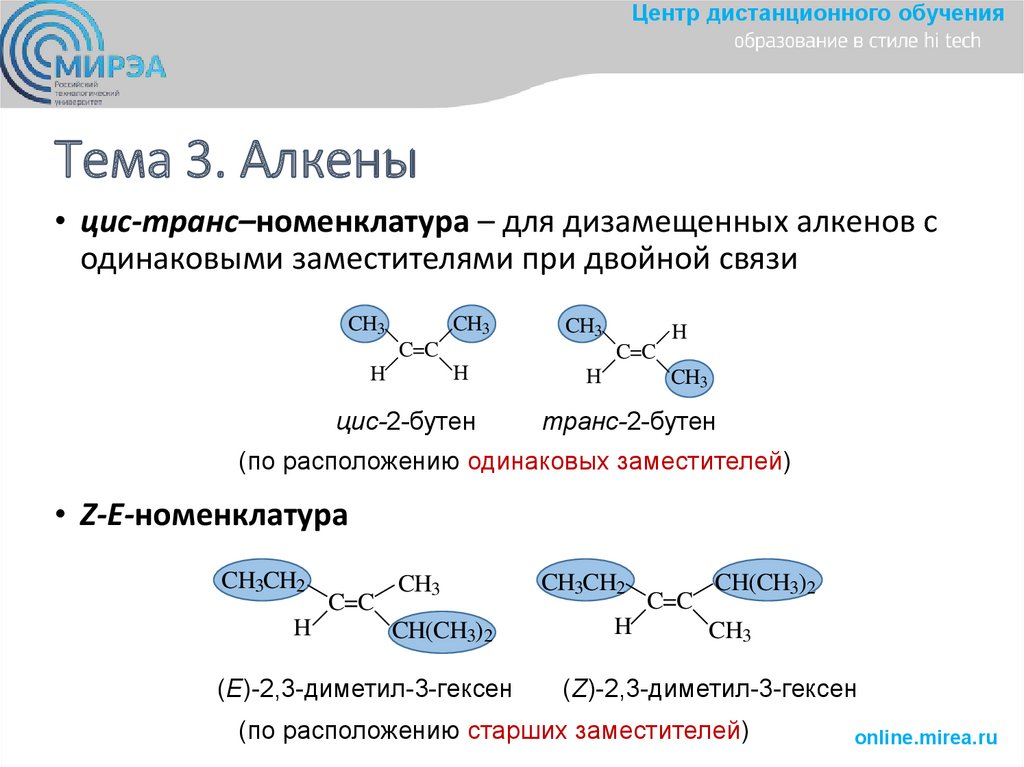
Центр дистанционного обученияТема 3. Алкены
• цис-транс–номенклатура – для дизамещенных алкенов с
одинаковыми заместителями при двойной связи
CH3
CH3
CH3
C=C
C=C
H
H
H
цис-2-бутен
H
CH3
транс-2-бутен
(по расположению одинаковых заместителей)
• Z-E-номенклатура
CH3CH2
H
C=C
CH3
CH(CH3)2
(Е)-2,3-диметил-3-гексен
CH3CH2
H
C=C
CH(CH3)2
CH3
(Z)-2,3-диметил-3-гексен
(по расположению старших заместителей)
online.mirea.ru
37.
Центр дистанционного обученияМетоды получения алкенов
1. Пиролиз и крекинг алканов
2. Дегидрирование алканов
3. Синтезы с использованием реакций элиминирования
С
С
Х
Y
- Х‒Y
С
С
Х = Н, Hal; Y = OH, Hal и др.
online.mirea.ru
38.
Центр дистанционного обучения• Дегидратация:
Cat = H2SO4, H3PO4 и др., t = 170
CH3‒CH‒CH3 H2SO4, t
OH
- H2O
CH2=CH‒CH3
пропен
H2SO4, t CH2 ‒CH2‒CH3
- H2O
2-пропанол
OH
1-пропанол
Скорость дегидратации: С(трет)‒ОН > C(втор)‒ОН > C(перв)‒ОН
CH2‒CH‒CH‒CH3
H
OH H
2-бутанол
H3PO4, t
- H2O
CH2=CH‒CH2‒CH3 + CH3‒CH=CH‒CH3
1-бутен
2-бутен
80‒90%
Преимущественно образуется алкен с более замещенной двойной связью –
более термодинамически стабильный (правило Зайцева)
online.mirea.ru
39.
Центр дистанционного обученияС
С
Х
Y
- Х‒Y
С
С
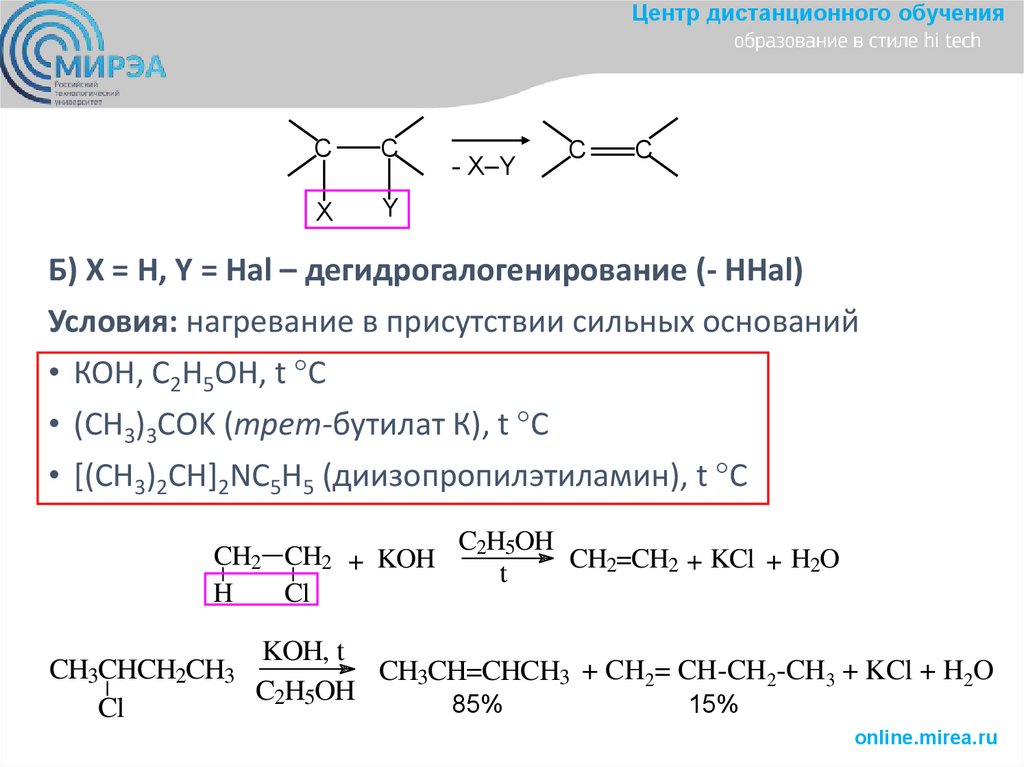
Б) X = H, Y = Hal – дегидрогалогенирование (- HHal)
Условия: нагревание в присутствии сильных оснований
• КОН, С2Н5ОН, t C
• (CH3)3COK (трет-бутилат К), t C
• [(CH3)2CH]2NC5H5 (диизопропилэтиламин), t C
CH2 CH2 + KOH
H
Cl
CH3CHCH2CH3
Cl
C2H5OH
CH2=CH2 + KCl + H2O
t
KOH, t
CH3CH=CHCH3 + CH2= CH-CH2-CH3 + KCl + H2O
C2H5OH
85%
15%
online.mirea.ru
40.
Центр дистанционного обученияС
С
Х
Y
- Х‒Y
С
С
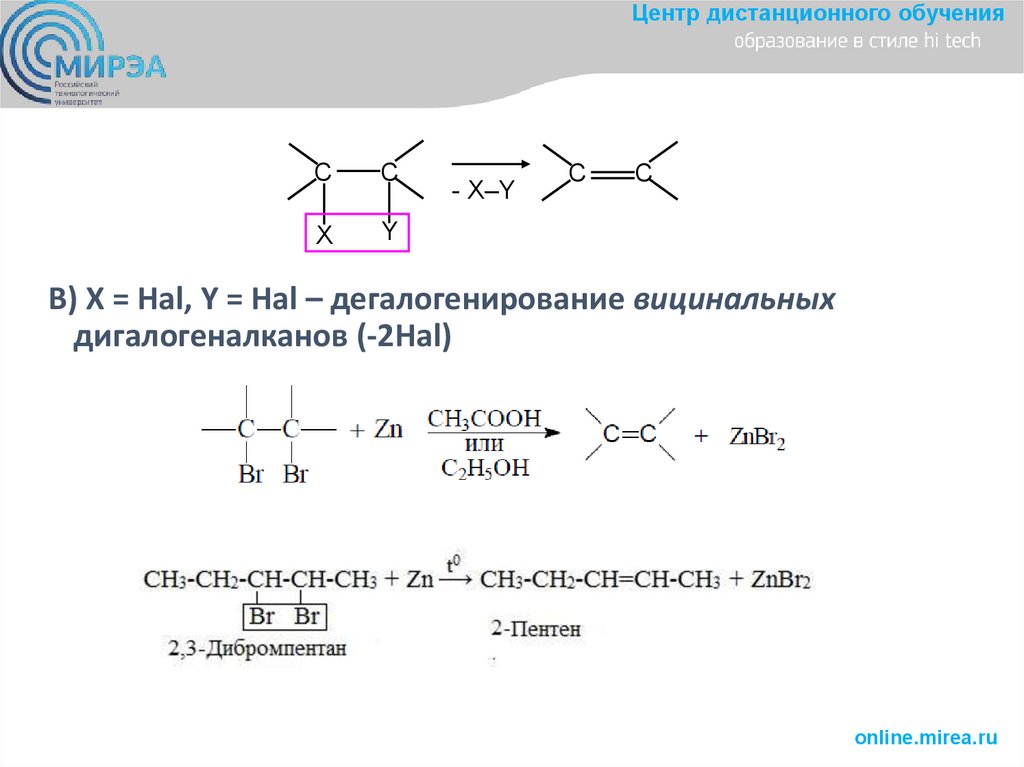
В) X = Hal, Y = Hal – дегалогенирование вицинальных
дигалогеналканов (-2Hal)
online.mirea.ru
41.
Центр дистанционного обучения4. Частичное восстановление алкинов
А) Гидрирование
R‒C C‒R’
алкин
H2
Cat
R‒CH=CH‒R’
алкен
Cat = Pd/S;
5%Pd/CaCO3/Pb(OCOCH3)2
(катализатор Линдлара)
H2
Cat
быстрее!
R‒CH2‒CH2‒R’
алкан
- дезактивированный катализатор!!!
цис-2-бутен
online.mirea.ru
42.
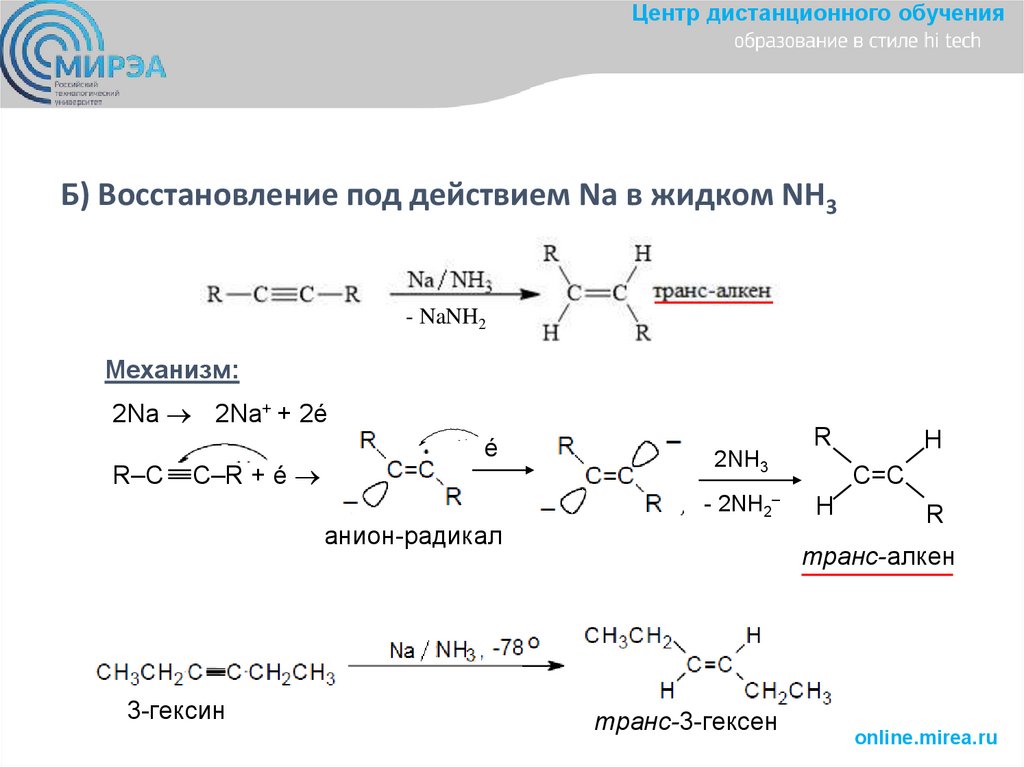
Центр дистанционного обученияБ) Восстановление под действием Na в жидком NH3
- NaNH2
Механизм:
2Na 2Na+ + 2é
R‒C
C‒R + é
é
2NH3
-
2NH2‒
анион-радикал
3-гексин
R
H
C=C
H
R
транс-алкен
транс-3-гексен
online.mirea.ru
43. Химические свойства алкенов 1. Реакции присоединения (Аd)
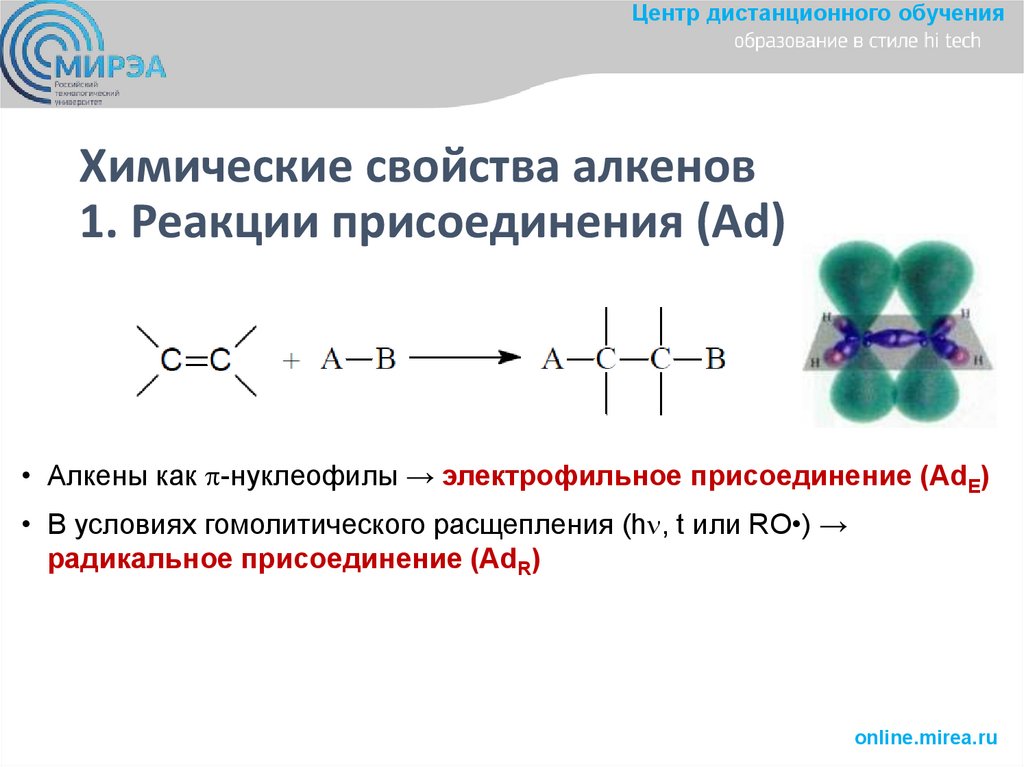
Центр дистанционного обученияХимические свойства алкенов
1. Реакции присоединения (Аd)
• Алкены как -нуклеофилы → электрофильное присоединение (AdE)
• В условиях гомолитического расщепления (hn, t или RO•) →
радикальное присоединение (AdR)
online.mirea.ru
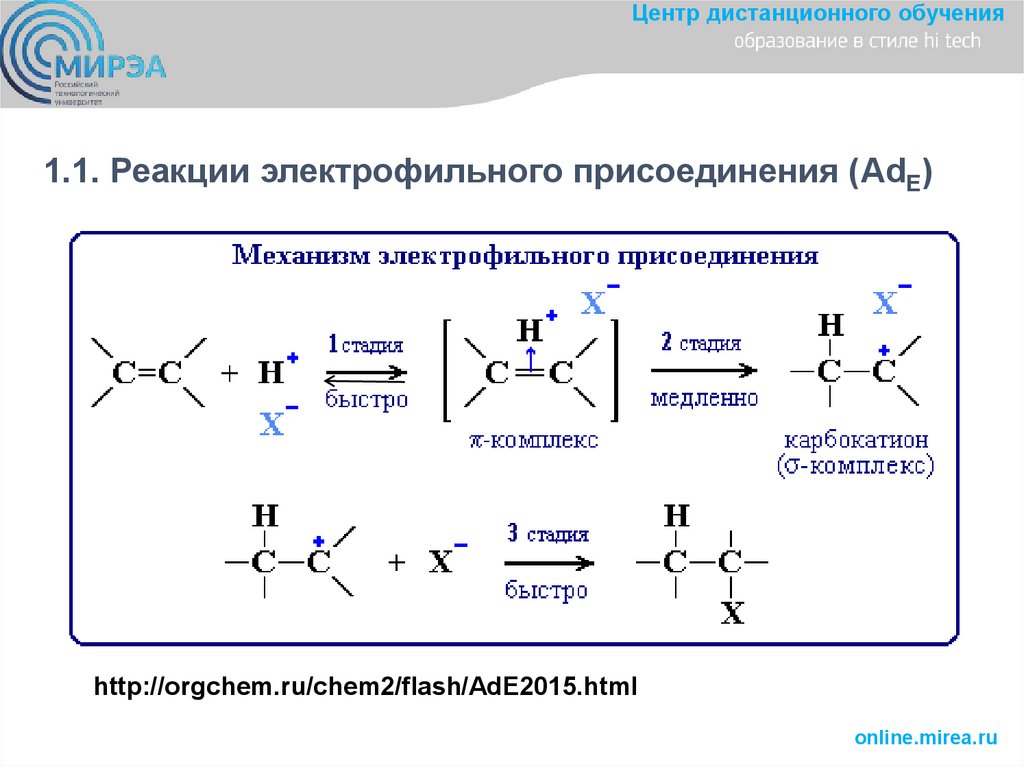
44. 1.1. Реакции электрофильного присоединения (AdE)
Центр дистанционного обучения1.1. Реакции электрофильного присоединения (AdE)
http://orgchem.ru/chem2/flash/AdE2015.html
online.mirea.ru
45.
Центр дистанционного обученияСкорость реакции AdE зависит от величины
электронной плотности на связи >C=C<
online.mirea.ru
46.
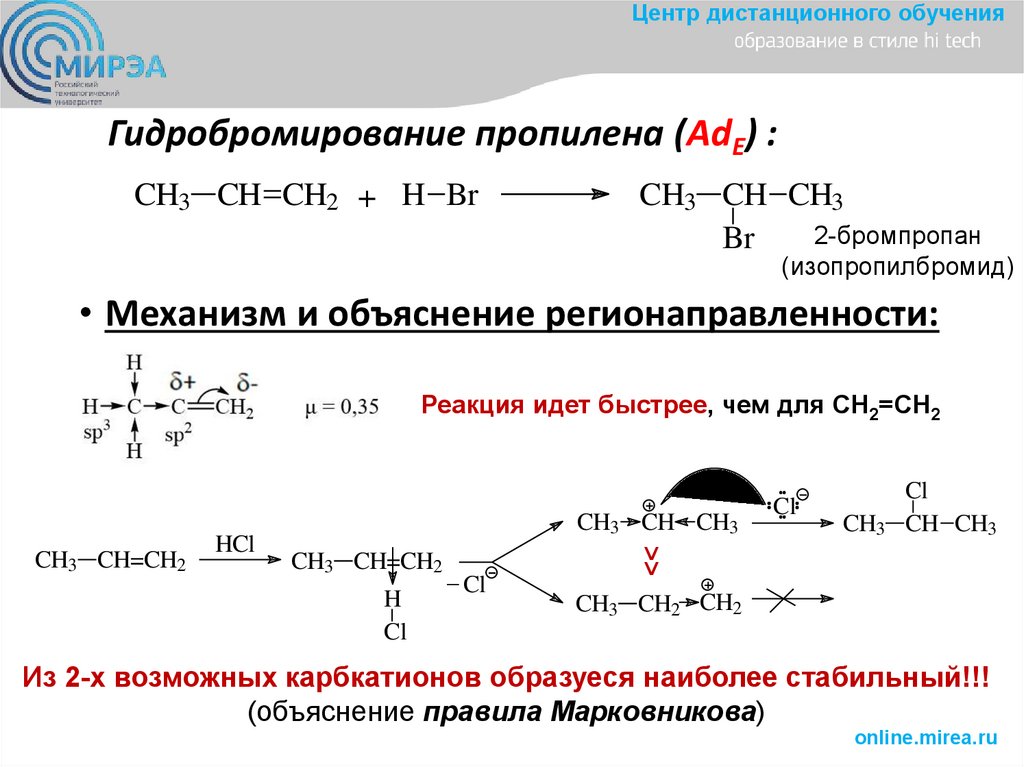
Центр дистанционного обученияГидробромирование пропилена (AdE) :
CH3 CH CH2 + H Br
CH3 CH CH3
2-бромпропан
Br
(изопропилбромид)
• Механизм и объяснение регионаправленности:
Реакция идет быстрее, чем для СН2=СН2
CH3 CH CH3
CH3 CH=CH2
H
Cl
_ Cl
CH3
Cl
CH CH3
>>
CH3 CH=CH2
HCl
Cl
CH3 CH2 CH2
Из 2-х возможных карбкатионов образуеся наиболее стабильный!!!
(объяснение правила Марковникова)
online.mirea.ru
47.
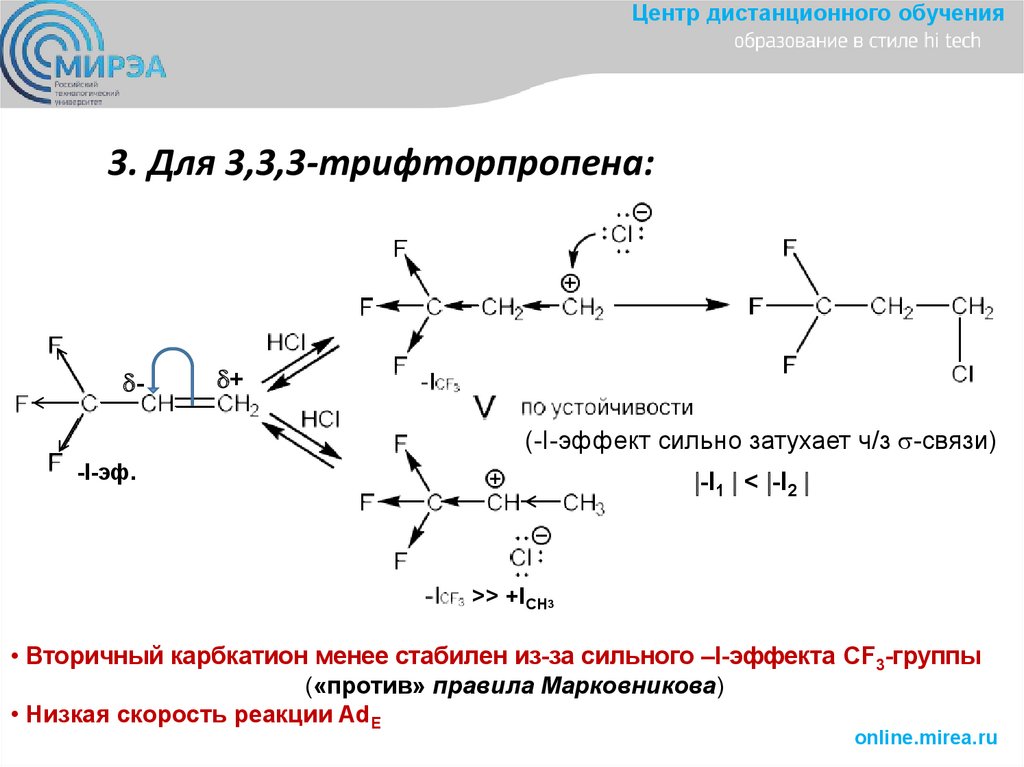
Центр дистанционного обучения3. Для 3,3,3-трифторпропена:
-
+
Реакция идет быстрее, чем для СН2=СН2
(-I-эффект сильно затухает ч/з -связи)
-I-эф.
-I1 < -I2
>>
>> +ICH3
• Вторичный карбкатион менее стабилен из-за сильного –I-эффекта CF3-группы
(«против» правила Марковникова)
• Низкая скорость реакции AdE
online.mirea.ru
48.
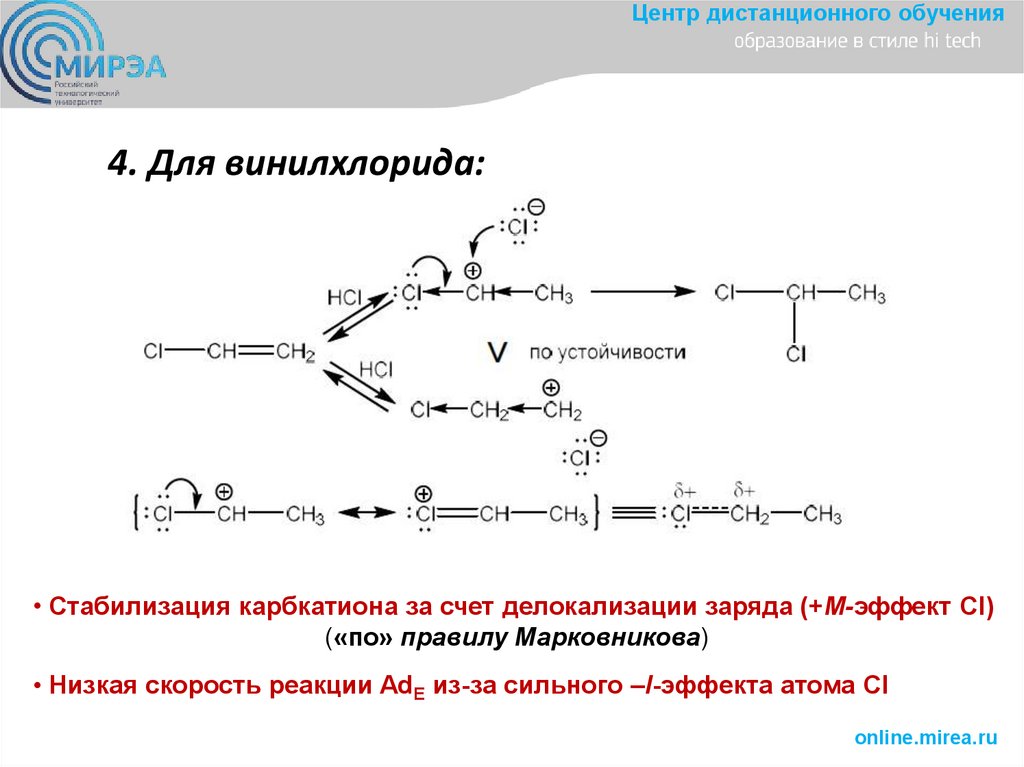
Центр дистанционного обучения4. Для винилхлорида:
• Стабилизация карбкатиона за счет делокализации заряда (+M-эффект Cl)
(«по» правилу Марковникова)
• Низкая скорость реакции AdE из-за сильного –I-эффекта атома Cl
online.mirea.ru
49.
Центр дистанционного обучения• Присоединение Н2SO4 и других протонных кислот
AdE
online.mirea.ru
50.
Центр дистанционного обучения• Гидратация алкенов (+Н2О)
- прямая гидратация в присутствии катализаторов: H2SO4, Н3PO4, CF3COOH
H2SO4 – каталитическое кол-во
Н2О – реагент (в избытке)
online.mirea.ru
51.
Центр дистанционного обучения• Галогенирование (+ Hal2)
F2 >> Cl2 > Br2 > I2
(анти-присоединение)!!!
online.mirea.ru
52.
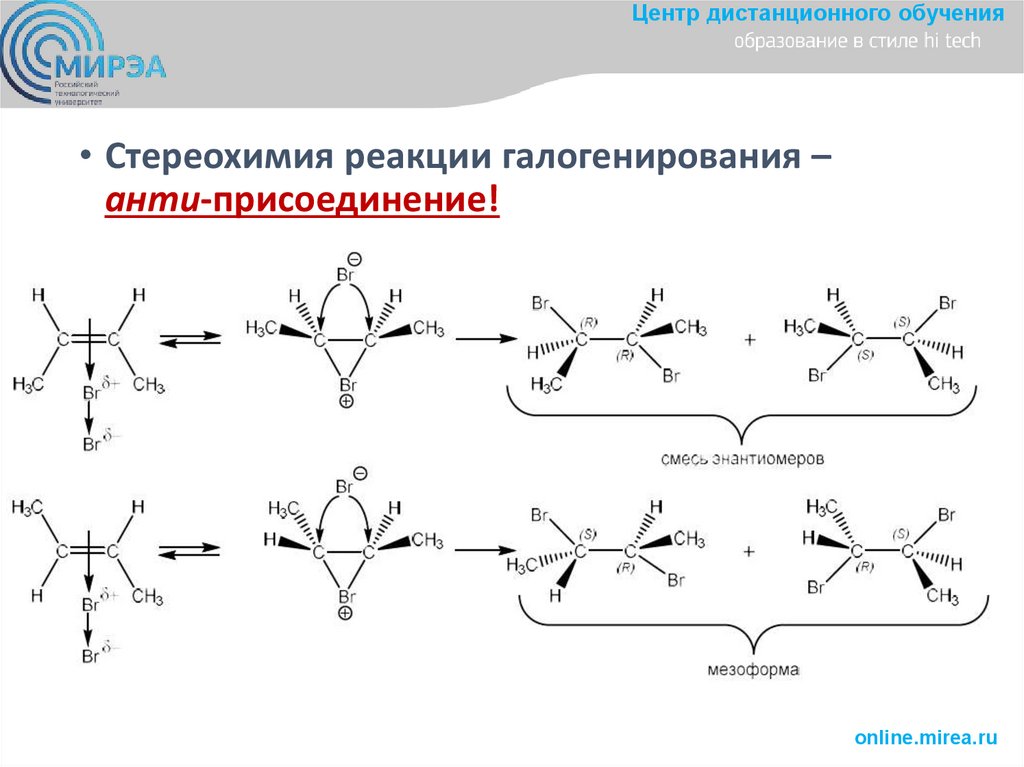
Центр дистанционного обучения• Стереохимия реакции галогенирования –
анти-присоединение!
online.mirea.ru
53.
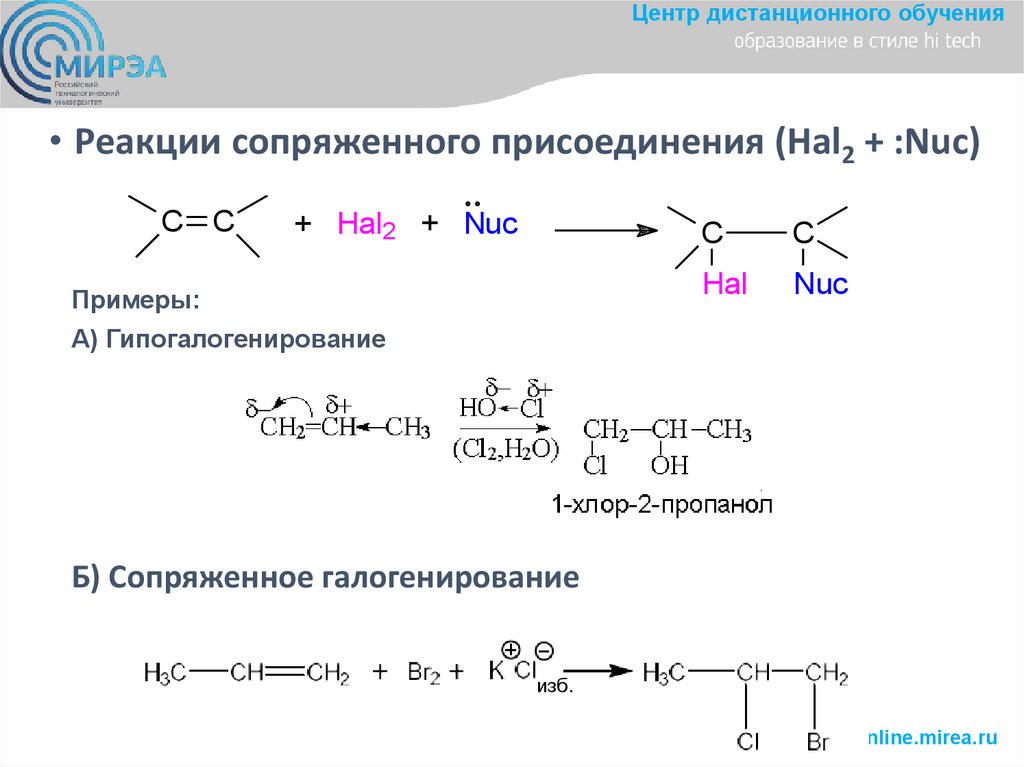
Центр дистанционного обучения• Реакции сопряженного присоединения (Hal2 + :Nuc)
C C
+ Hal2 + Nuc
Примеры:
C
C
Hal
Nuc
А) Гипогалогенирование
Б) Сопряженное галогенирование
изб.
online.mirea.ru
54.
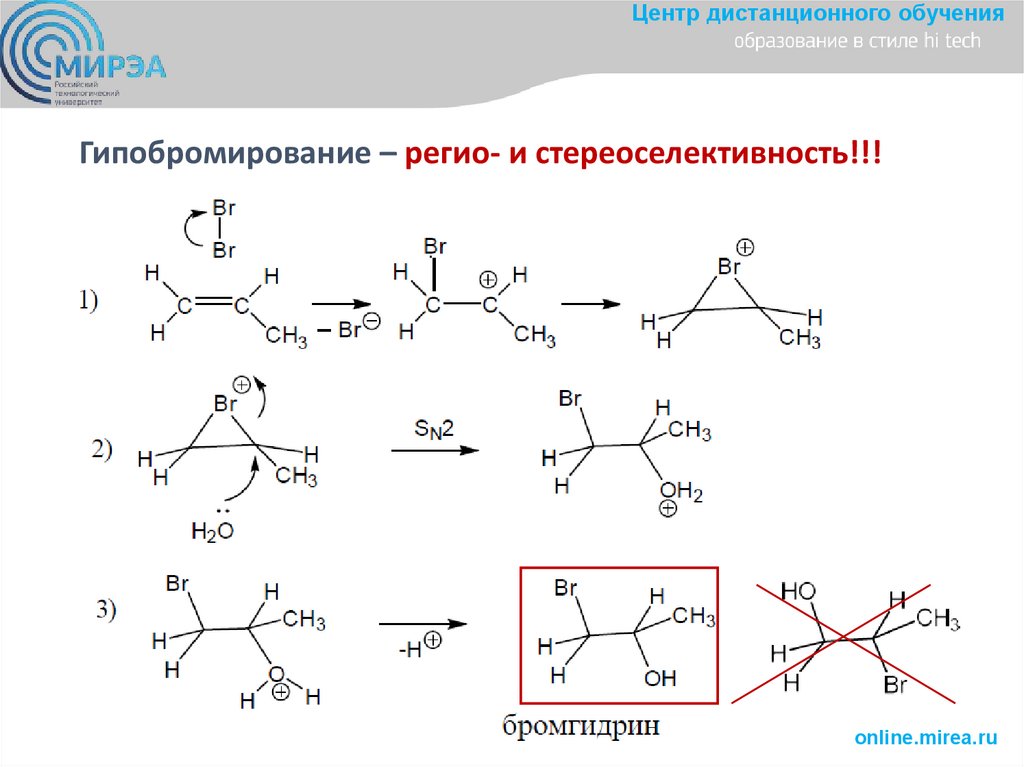
Центр дистанционного обученияГипобромирование – регио- и стереоселективность!!!
online.mirea.ru
55.
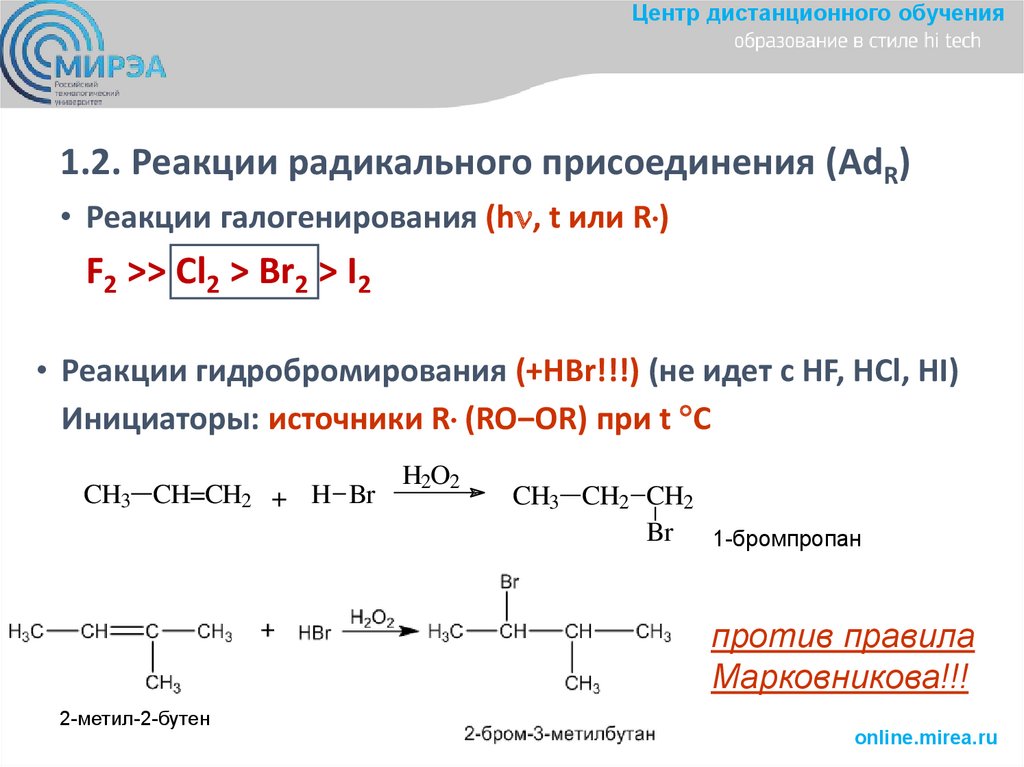
Центр дистанционного обучения1.2. Реакции радикального присоединения (AdR)
• Реакции галогенирования (hn, t или R )
F2 >> Cl2 > Br2 > I2
• Реакции гидробромирования (+HBr!!!) (не идет с HF, HCl, HI)
Инициаторы: источники R (RO‒OR) при t C
CH3 CH=CH2 + H Br
H2O2
CH3 CH2 CH2
Br 1-бромпропан
против правила
Марковникова!!!
2-метил-2-бутен
online.mirea.ru
56.
Центр дистанционного обучения1.3. Реакция гидрирования
CH3
H2, Ni
CH3
1,2-диметилциклогексен
H
CH3
H
CH3
цис-1,2-диметилциклогексан
2. Реакции радикального замещения (SR)
в аллильное положение
CH3 CH=CH2
Cl2
ClCH2 CH=CH2 + H Cl
o
400 C
3-хлорпропен
(аллилхлорид)
online.mirea.ru
57.
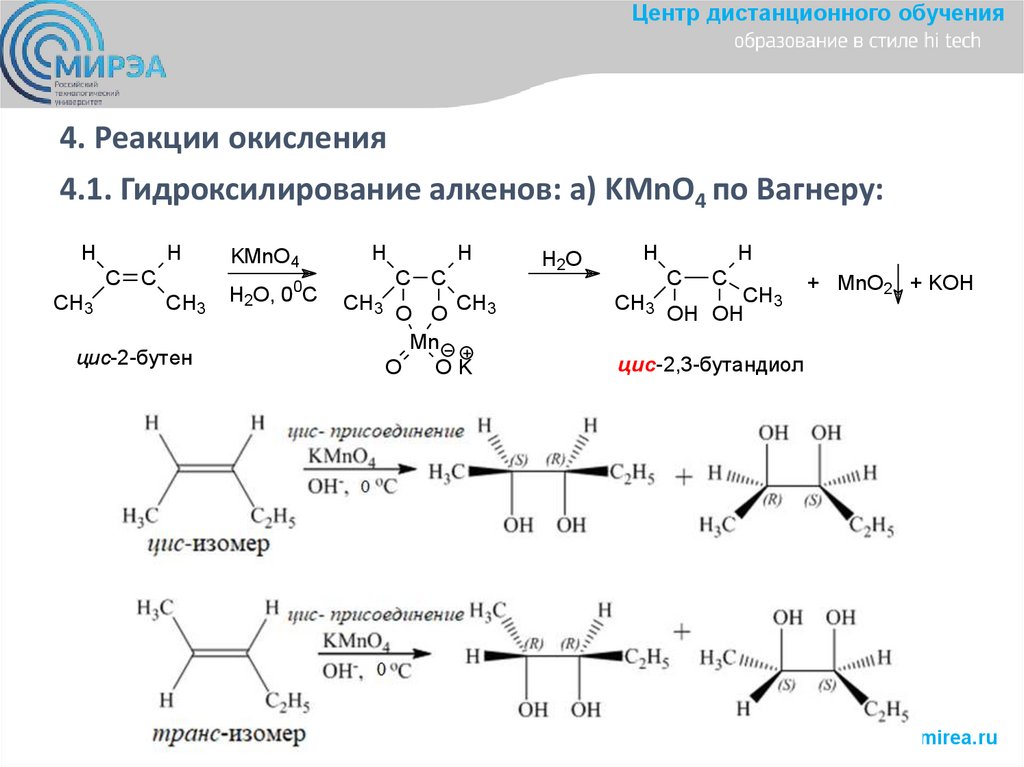
Центр дистанционного обучения4. Реакции окисления
4.1. Гидроксилирование алкенов: а) KMnO4 по Вагнеру:
H
H
KMnO4
CH3
H2O, 00C
C C
CH3
цис-2-бутен
H
H
C C
CH3 O O CH3
Mn
O
OK
H2O
H
H
C
C
CH3 OH OHCH3
+ MnO2 + KOH
цис-2,3-бутандиол
online.mirea.ru
58.
Центр дистанционного обучения• Предложите одностадийный метод синтеза рацемического 2,3-бутандиола из
соответствующего алкена. Напишите уравнение этой реакции. Изобразите
проекционные формулы Фишера всех конфигурационных изомеров продукта
реакции и определите конфигурации каждого из хиральных центров.
online.mirea.ru
59.
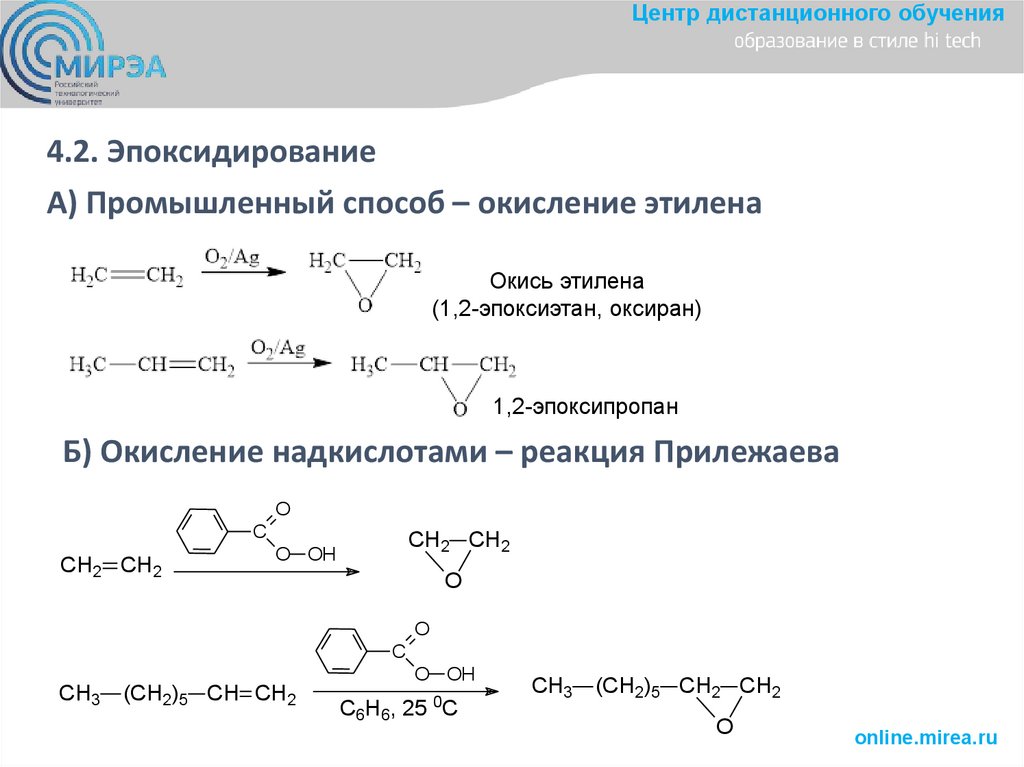
Центр дистанционного обучения4.2. Эпоксидирование
А) Промышленный способ – окисление этилена
Окись этилена
(1,2-эпоксиэтан, оксиран)
1,2-эпоксипропан
Б) Окисление надкислотами – реакция Прилежаева
O
C
CH2 CH2
CH2 CH2
O OH
O
O
C
CH3
(CH2)5 CH CH2
O OH
0
C6H6, 25 C
CH3 (CH2)5 CH2 CH2
O
online.mirea.ru
60.
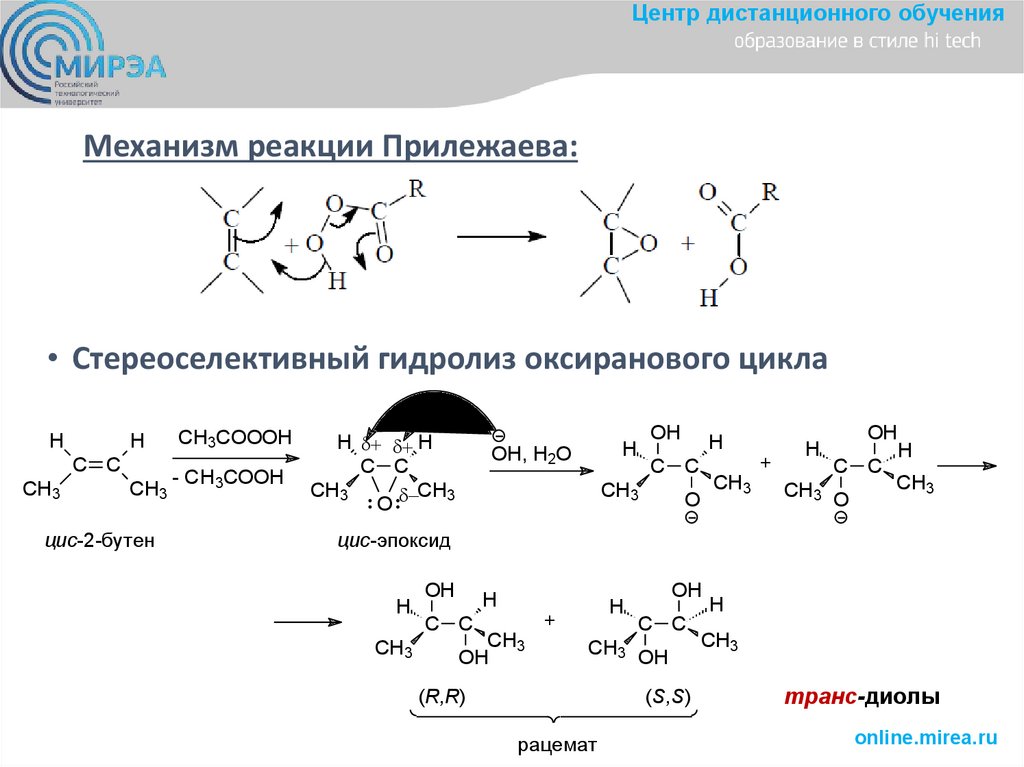
Центр дистанционного обученияМеханизм реакции Прилежаева:
• Стереоселективный гидролиз оксиранового цикла
H
H
C C
CH3
CH3
цис-2-бутен
CH3COOOH
- CH3COOH
H H
C C
CH3
CH3
O
OH
H
OH, H2O
H
C C
CH3
CH3
O
+
H
CH3
OH
H
C C
CH3
O
цис-эпоксид
H
CH3
OH
H
C C
CH3
OH
H
+
OH
C C
CH3 OH
(R,R)
(S,S)
рацемат
H
CH3
транс-диолы
online.mirea.ru
61.
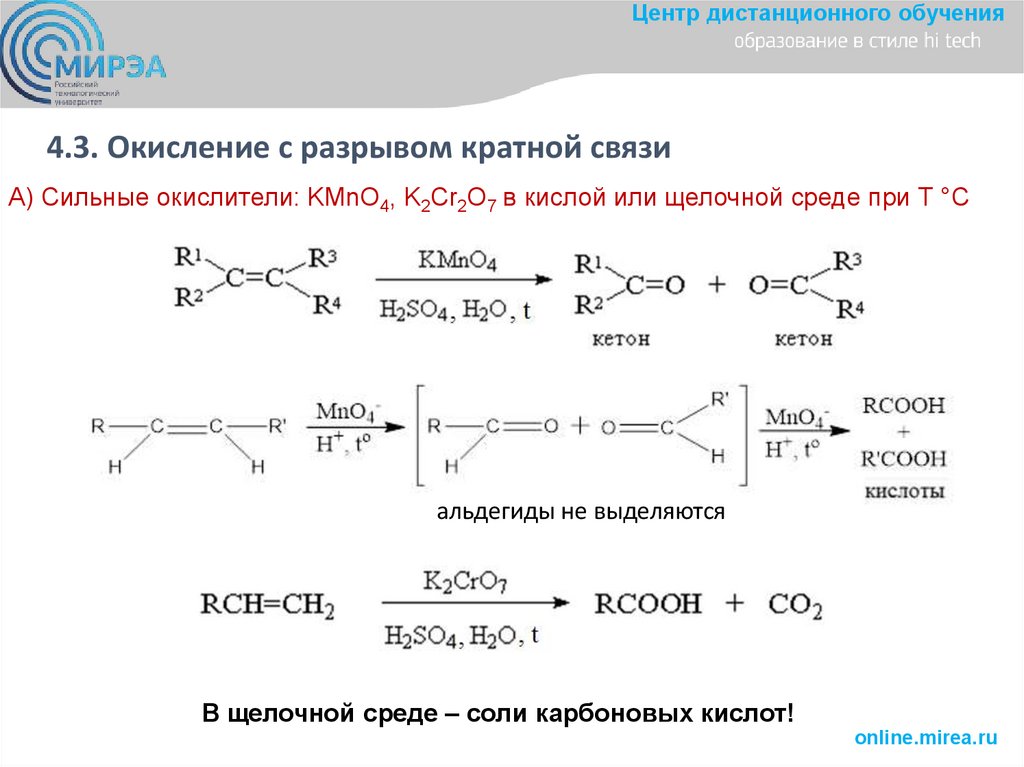
Центр дистанционного обучения4.3. Окисление с разрывом кратной связи
А) Сильные окислители: KMnO4, K2Cr2O7 в кислой или щелочной среде при Т °С
альдегиды не выделяются
В щелочной среде – соли карбоновых кислот!
online.mirea.ru
62.
Центр дистанционного обученияБ) Озонолиз алкенов
R1
R2
C C
R3
O O O
R4
AdE
R1
R2
C C
O
O
R3
R1
CH CH CH3
бутен
2-метил-2-бутен
2) H2O, Zn
C
R3
O O R4
озонид
моль-озонид
CH3
C
R2
OR4
1) O3
O
H2O, Zn, H+
- ZnO
R1
R2
C O O C
R3
R4
восстановительное
расщепление
O
2 CH3
C
H
ацетальдегид
online.mirea.ru
63.
Центр дистанционного обучения5. Реакции полимеризации
Полимер – макромолекула, состоит из большого числа
повторяющихся звеньев
Мв ~ 107
Инициаторы:
• Источники радикалов (радикальная полимеризация)
• Катионы (катионная полимеризация)
• Анионы (анионная полимеризация)
• Соли переходных металлов (координационная полимеризация)
online.mirea.ru
64. Структура диенов
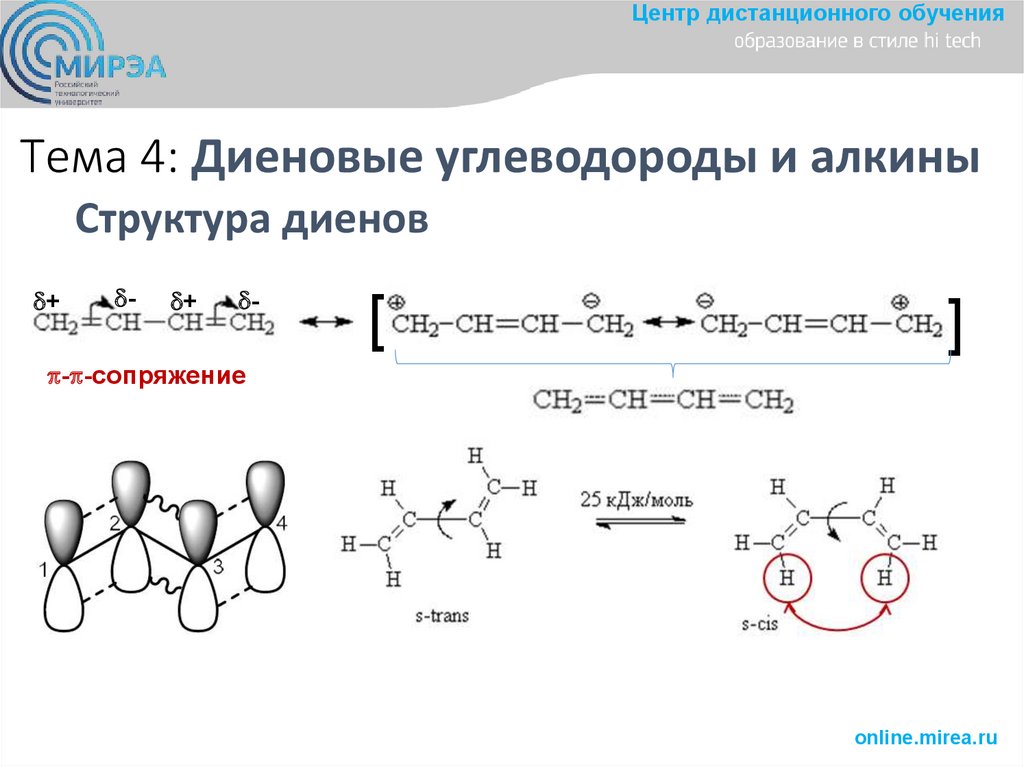
Центр дистанционного обученияТема 4: Диеновые углеводороды и алкины
Структура диенов
+
-
+
-
[
]
- -сопряжение
online.mirea.ru
65.
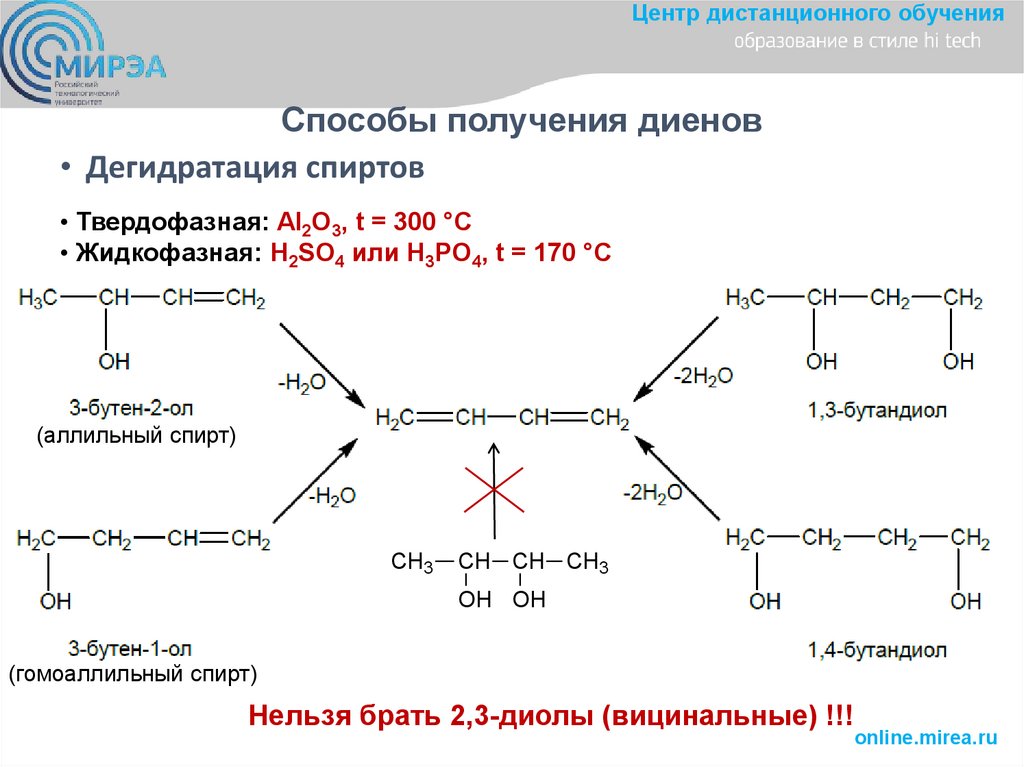
Центр дистанционного обученияСпособы получения диенов
• Дегидратация спиртов
• Твердофазная: Al2O3, t = 300 °C
• Жидкофазная: H2SO4 или H3PO4, t = 170 °C
(аллильный спирт)
CH3
CH CH CH3
OH OH
(гомоаллильный спирт)
Нельзя брать 2,3-диолы (вицинальные) !!!
online.mirea.ru
66.
Центр дистанционного обучения• Реакции дегидрогалогенирования (-HHal) (Hal = Cl, Br, I)
Условия: KOH/C2H5OH, t °C
3-бром-1-бутен
(аллилгалогенид)
4-бром-1-бутен
(гомоаллилгалогенид)
1,3-дибромбутан
1,4-дибромбутан
online.mirea.ru
67.
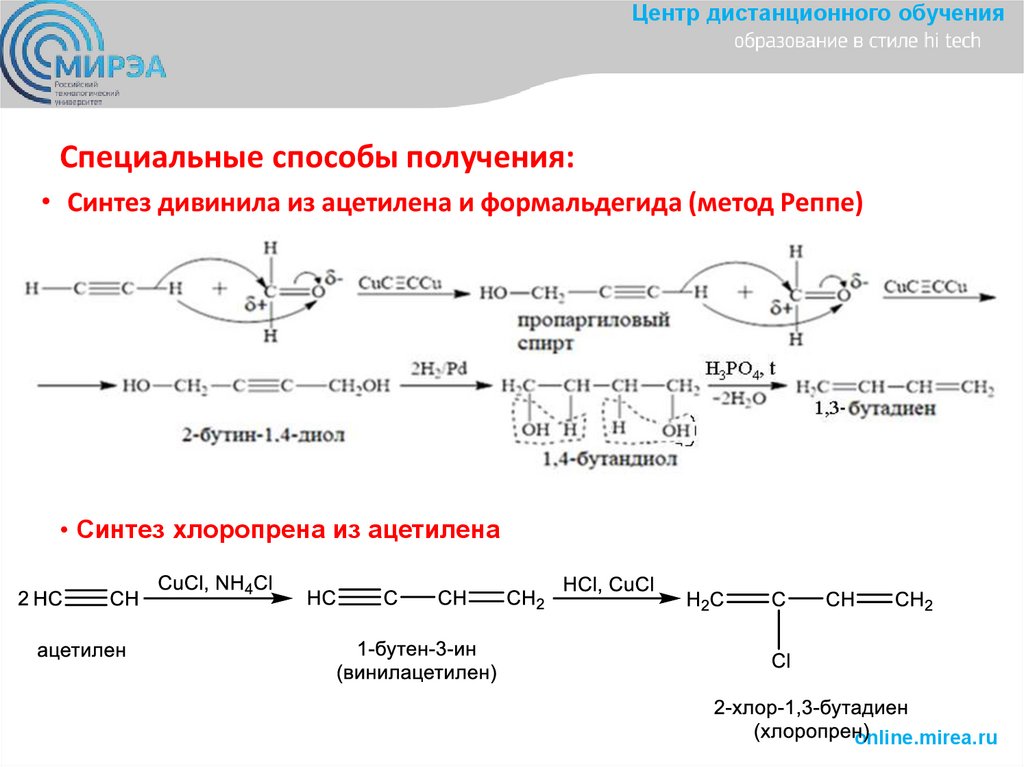
Центр дистанционного обученияСпециальные способы получения:
• Синтез дивинила из ацетилена и формальдегида (метод Реппе)
• Синтез хлоропрена из ацетилена
online.mirea.ru
68.
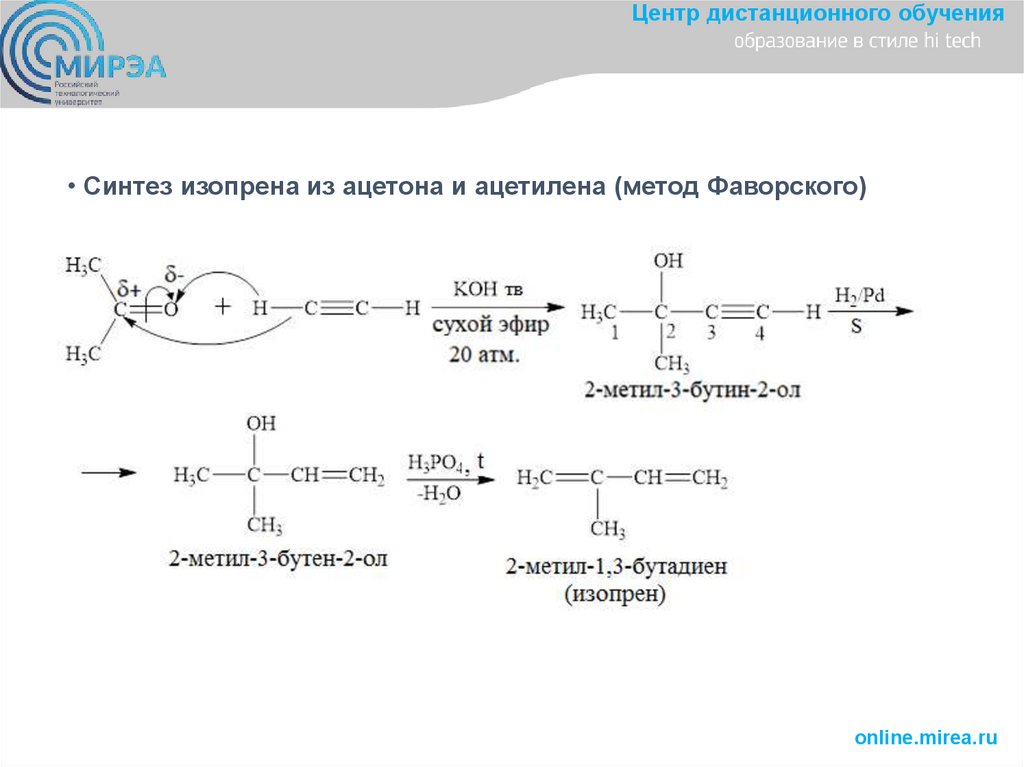
Центр дистанционного обучения• Синтез изопрена из ацетона и ацетилена (метод Фаворского)
online.mirea.ru
69.
Центр дистанционного обученияХимические свойства сопряженных диенов
1. Реакции присоединения (Аd)
• Диены как -нуклеофилы → электрофильное присоединение (AdE)
• В условиях гомолитического расщепления (hn, t или RO•) →
радикальное присоединение (AdR)
С=С‒С=С
1,2-присоединение
1,4-присоединение
online.mirea.ru
70.
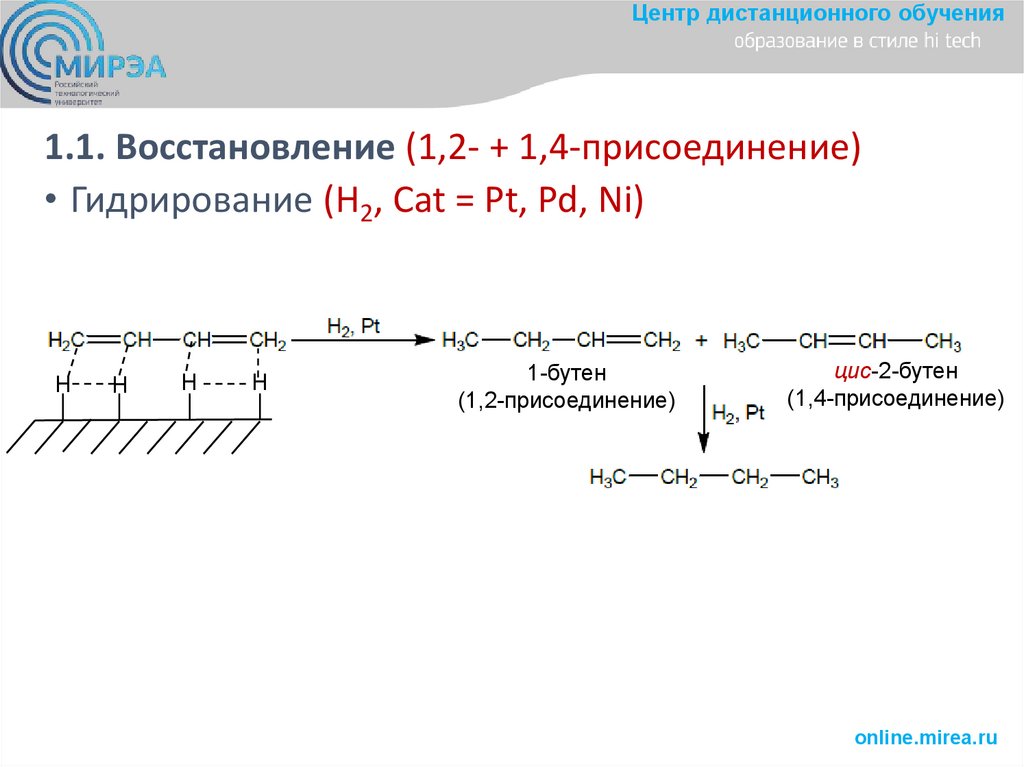
Центр дистанционного обучения1.1. Восстановление (1,2- + 1,4-присоединение)
• Гидрирование (Н2, Cat = Pt, Pd, Ni)
Н
Н
Н
Н
1-бутен
(1,2-присоединение)
цис-2-бутен
(1,4-присоединение)
online.mirea.ru
71.
Центр дистанционного обучения1.2. Реакции электрофильного присоединения (AdE)
• Галогенирование
F2 >> Cl2 > Br2 > I2
3,4-дихлор-1-бутен
1,4-дихлор-2-бутен
Механизм электрофильного галогенирования:
-I (Cl) << +M
амбидентный
электрофил
аллильный карбкатион
online.mirea.ru
72.
Центр дистанционного обученияСоотношение продуктов галогенирования
Т, °С
Продукт 1,2присоединения
Продукт 1,4присоединения
Т = 40 °С
20%
80%
Т = ‒80 °С
80%
20%
• При 40 °С – термодинамический контроль →
более стабильный алкен
• При ‒80 °С – кинетический контроль →
преобладает продукт, скорость образования
которого выше
online.mirea.ru
73.
Центр дистанционного обучения• Сравните скорости взаимодействия 1,3-бутадиена
бутадиена с хлором в темноте. Ответ обоснуйте.
и
2-этил-1,3-
online.mirea.ru
74.
Центр дистанционного обучения• Гидрогалогенирование
А) для дивинила
аллильный карбкатион
Низкие Т – 1,2 > 1,4
«Высокие» Т – 1,4 > 1,2
3-бром-1-бутен
1-бром-2-бутен
online.mirea.ru
75.
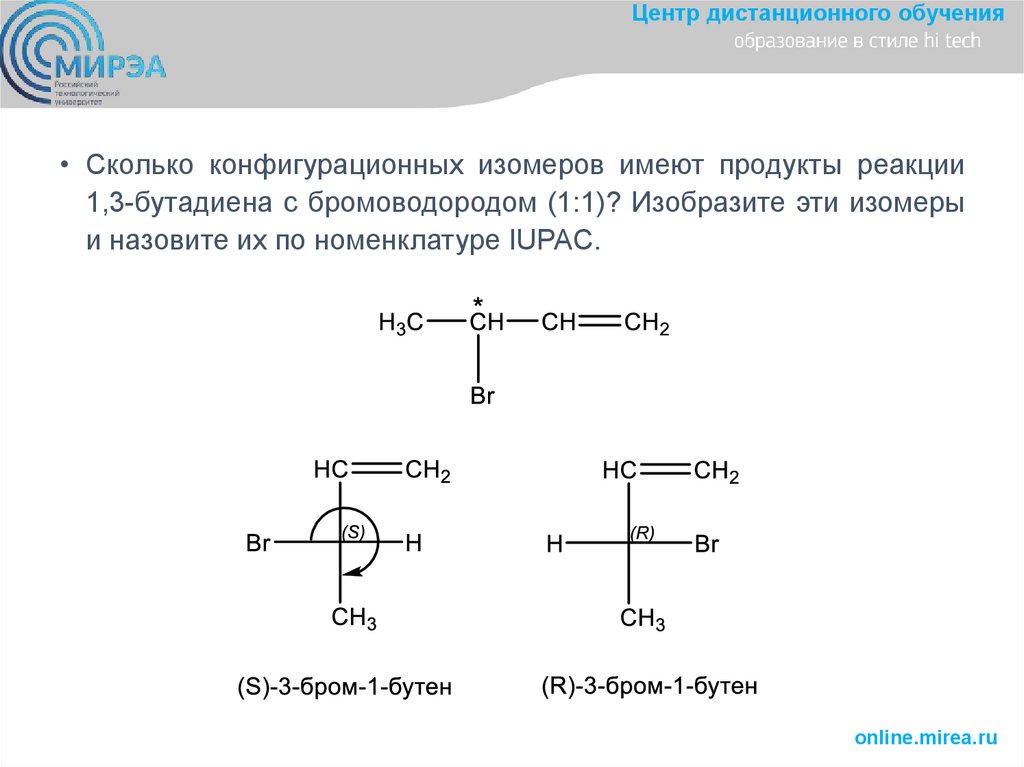
Центр дистанционного обучения• Сколько конфигурационных изомеров имеют продукты реакции
1,3-бутадиена с бромоводородом (1:1)? Изобразите эти изомеры
и назовите их по номенклатуре IUPAC.
online.mirea.ru
76.
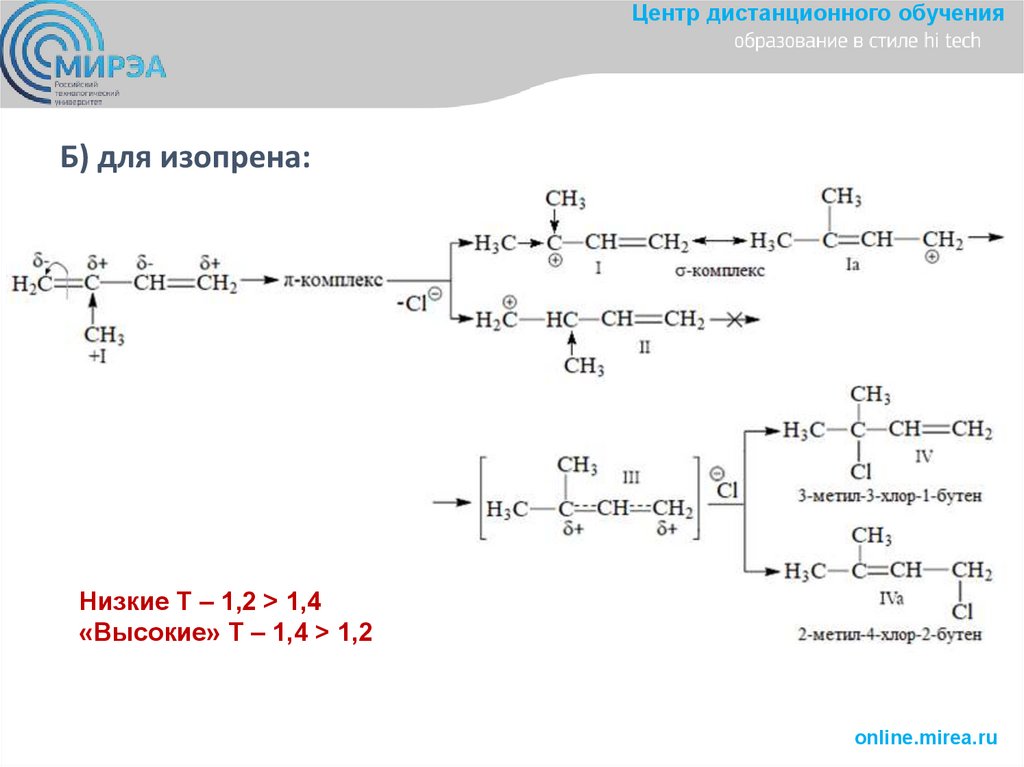
Центр дистанционного обученияБ) для изопрена:
Низкие Т – 1,2 > 1,4
«Высокие» Т – 1,4 > 1,2
online.mirea.ru
77.
Центр дистанционного обученияВ) Для хлоропрена:
Низкие Т – 1,2 > 1,4
«Высокие» Т – 1,4 > 1,2
online.mirea.ru
78.
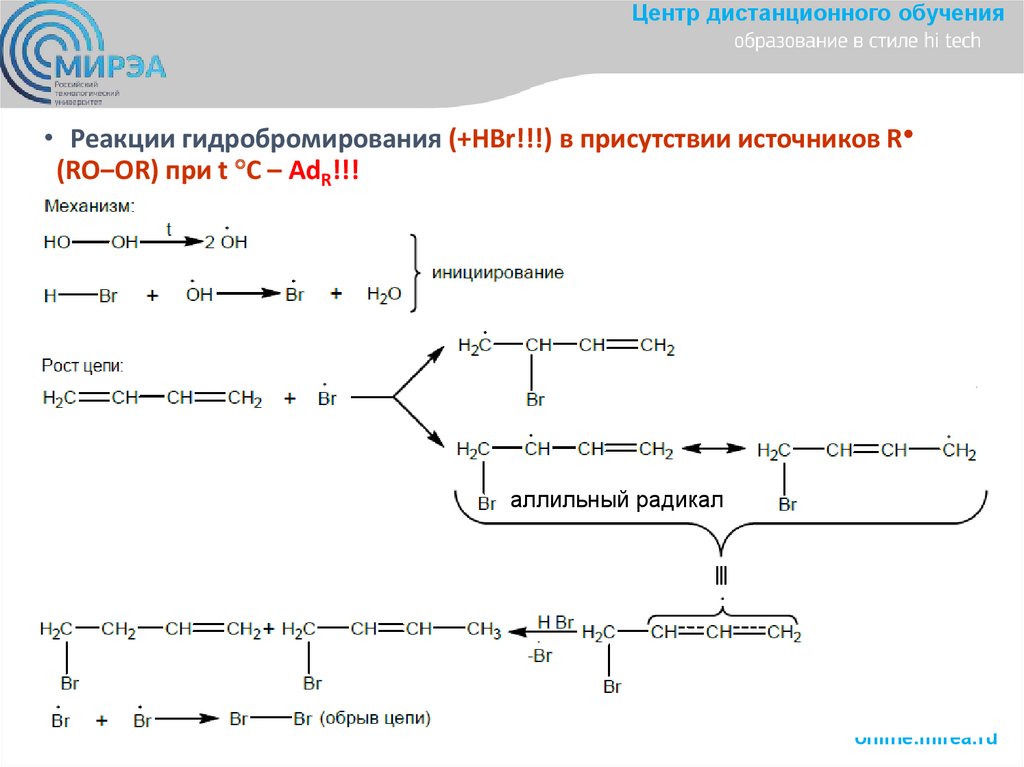
Центр дистанционного обучения• Реакции гидробромирования (+HBr!!!) в присутствии источников R
(RO‒OR) при t C – AdR!!!
аллильный радикал
online.mirea.ru
79.
Центр дистанционного обучения3. Реакции окисления
а) Эпоксидирование
O
H3C
H3C
CH3C
С CH CH CH2
4-метил-1,3-пентадиен
O OH
O
H3C
H3C
CH3C
С CH CH CH2
O
4-метил-3,4-эпокси-1-пентен
O OH
H3C
H3C
С CH CH CH2
O
O
4-метил-1,2;3,4-диэпоксипентан
б) Озонолиз
online.mirea.ru
80.
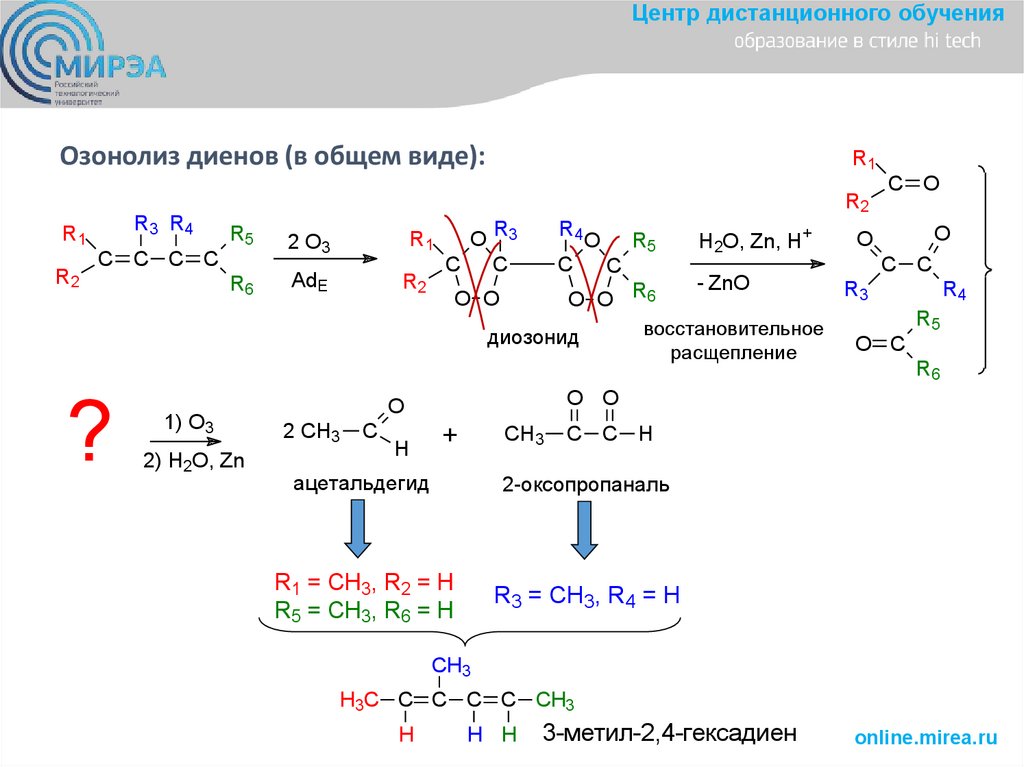
Центр дистанционного обученияОзонолиз диенов (в общем виде):
R1
R2
R3 R4
C C C C
R1
R2
R5
2 О3
R6
AdE
R1
R2
O R3
C
C
R4
C
O
C
O O R6
O O
диозонид
?
1) O3
2) H2O, Zn
C
H
H2O, Zn, H+
- ZnO
восстановительное
расщепление
О
О
С С
R3
O C
R4
R5
R6
O O
O
2 CH3
R5
C O
+
СH3
C C H
ацетальдегид
2-оксопропаналь
R1 = CH3, R2 = H
R5 = CH3, R6 = H
R3 = CH3, R4 = H
CH3
H3C C C C C CH3
H
H H
3-метил-2,4-гексадиен
online.mirea.ru
81.
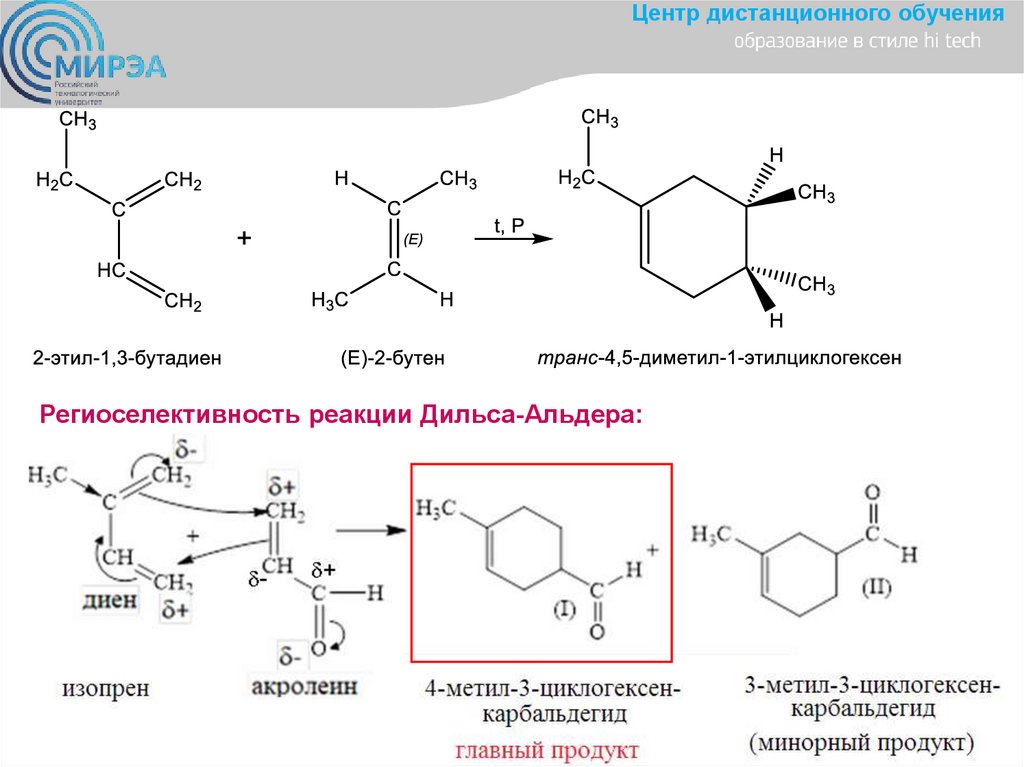
Центр дистанционного обучения4. [2+4]-циклоприсоединение – реакция Дильса-Альдера:
реакция диенов с алкенами циклогексены
#
переходное
состояние
online.mirea.ru
82.
Центр дистанционного обученияРегиоселективность реакции Дильса-Альдера:
online.mirea.ru
83.
Центр дистанционного обучения5. Реакции полимеризации
+
+ смешанные
продукты (1,2-, 1,4-)
1,4-присоединение
1,2-присоединение
Инициаторы:
• Источники радикалов (радикальная полимеризация)
• Катионы (катионная полимеризация)
• Анионы (анионная полимеризация)
• Соли переходных металлов (координационная полимеризация)
online.mirea.ru
84.
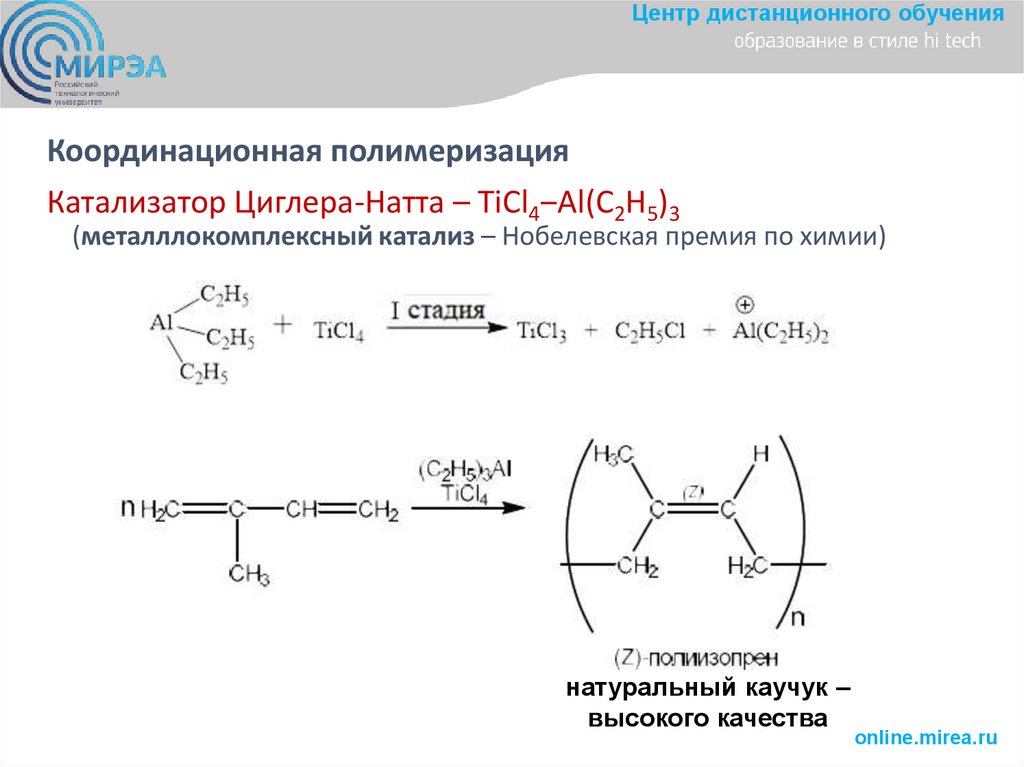
Центр дистанционного обученияКоординационная полимеризация
Катализатор Циглера-Натта – TiCl4‒Al(C2H5)3
(металллокомплексный катализ – Нобелевская премия по химии)
натуральный каучук –
высокого качества
online.mirea.ru
85.
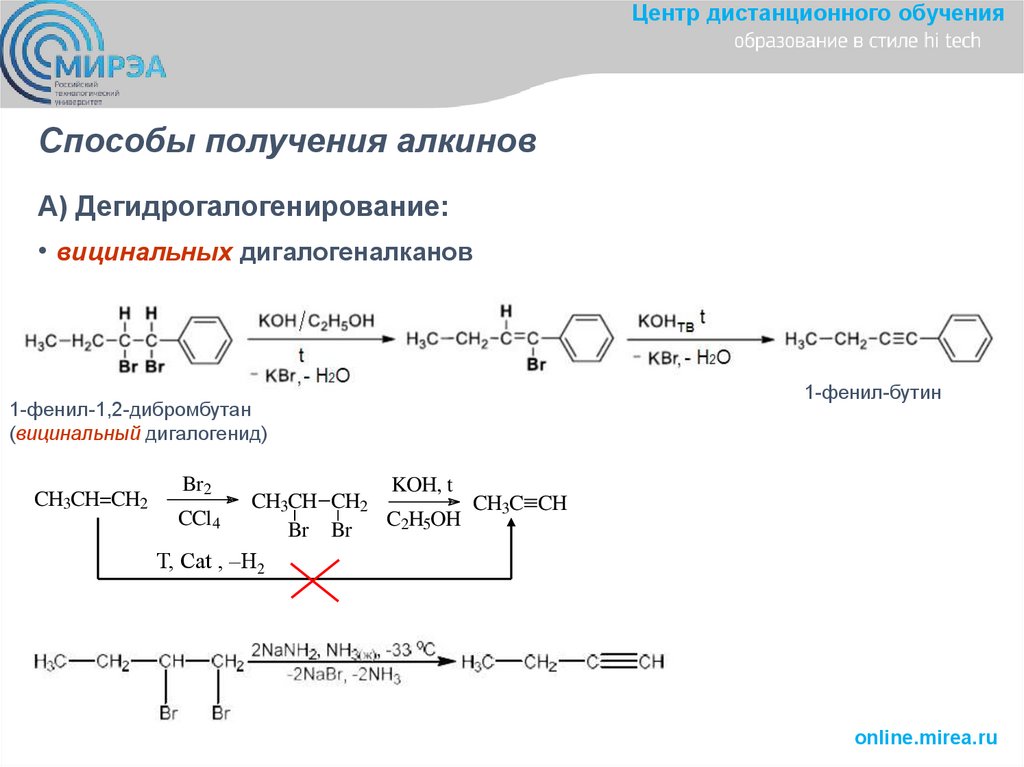
Центр дистанционного обученияCпособы получения алкинов
А) Дегидрогалогенирование:
• вицинальных дигалогеналканов
1-фенил-1,2-дибромбутан
(вицинальный дигалогенид)
CH3CH=CH2
Br2
CCl4
1-фенил-бутин
KOH, t
CH3CH CH2
CH3C CH
C2H5OH
Br Br
T, Cat , ‒H2
online.mirea.ru
86.
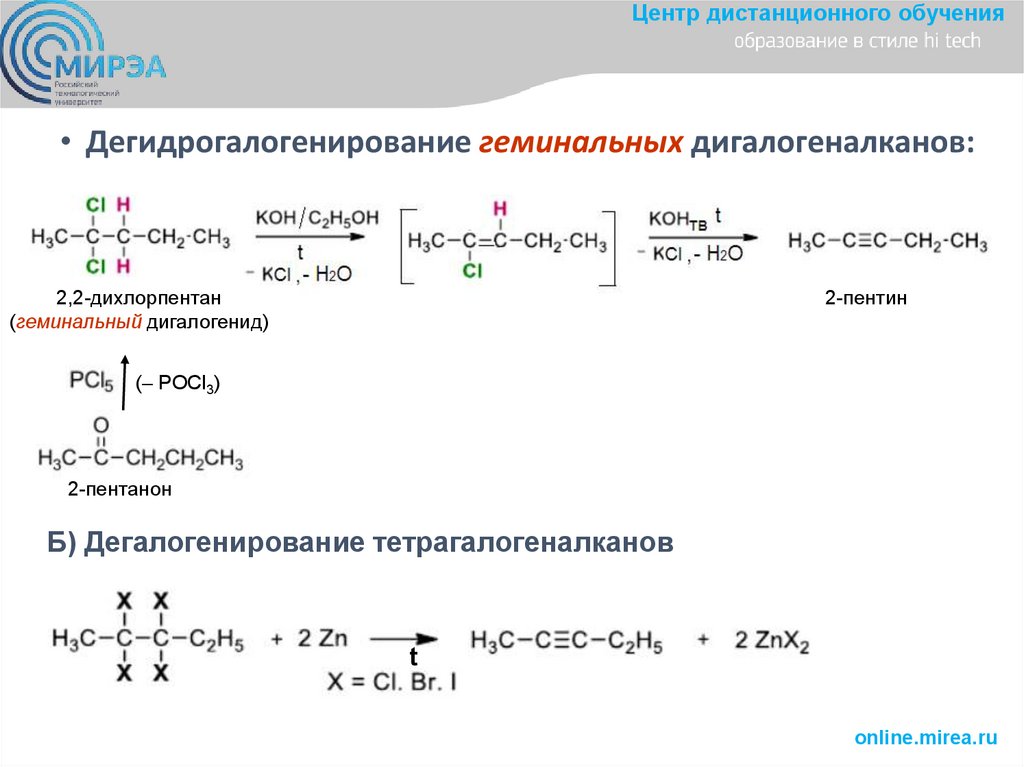
Центр дистанционного обучения• Дегидрогалогенирование геминальных дигалогеналканов:
2,2-дихлорпентан
(геминальный дигалогенид)
2-пентин
(‒ POCl3)
2-пентанон
Б) Дегалогенирование тетрагалогеналканов
t
online.mirea.ru
87.
Центр дистанционного обученияВ) Алкилирование алкинов с терминальной тройной связью
• через образование ацетиленидов металлов
• с использованием Mg-органических соединений
online.mirea.ru
88.
Центр дистанционного обученияХимические свойства алкинов
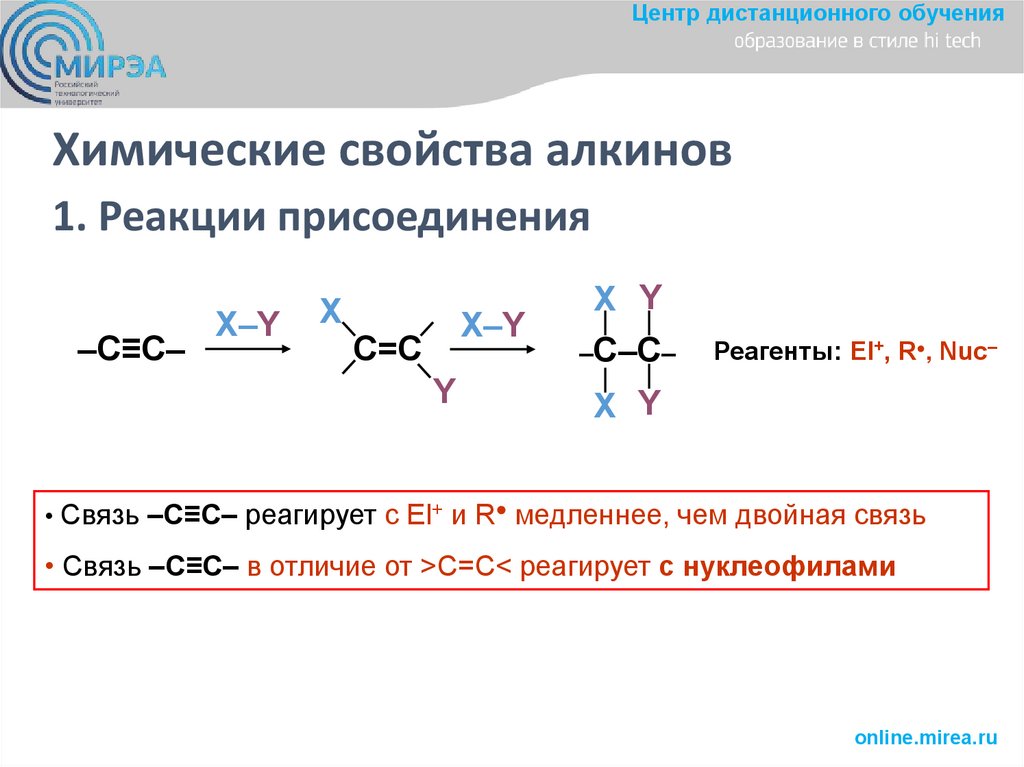
1. Реакции присоединения
‒С≡С‒
X‒Y
X
X‒Y
С=С
Y
X Y
‒С‒С‒
Реагенты: El+, R●, Nuc‒
X Y
• Связь ‒С≡С‒ реагирует с El+ и R● медленнее, чем двойная связь
• Связь ‒С≡С‒ в отличие от >C=C< реагирует с нуклеофилами
online.mirea.ru
89.
Центр дистанционного обучения1) Реакции галогенирования (+ Hal2)
Условия:
Hal2 в полярном растворителе - AdE
• Hal2, hn, t C или R● - AdR
AdR
(Z + E)!!!
online.mirea.ru
90.
Центр дистанционного обучения2) Реакции гидрогалогенирования (+ НHal)
Условия:
НCl, HBr, HI - AdE
• HBr, t C и R● - AdR
AdE
1) реакция протекает ступенчато
2) по правилу Марковникова
3) образуются продукты транс-присоединения
online.mirea.ru
91.
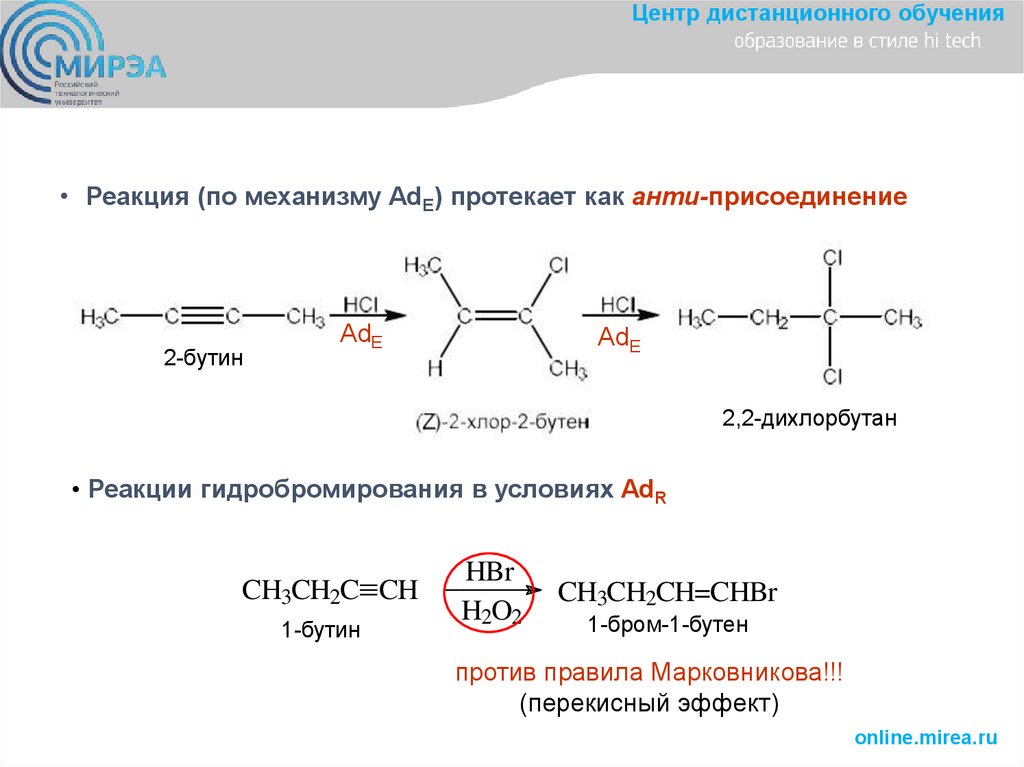
Центр дистанционного обучения• Реакция (по механизму AdE) протекает как анти-присоединение
2-бутин
AdE
AdE
2,2-дихлорбутан
• Реакции гидробромирования в условиях AdR
CH3CH2C CH
1-бутин
HBr
H2O2
CH3CH2CH=CHBr
1-бром-1-бутен
против правила Марковникова!!!
(перекисный эффект)
online.mirea.ru
92.
Центр дистанционного обучения3) Реакция гидратации (+ Н2О) – реакция Кучерова
AdE
-комплекс
енол
Кето-енольная таутомерия
Из замещенного ацетилена образуются кетоны!!!
online.mirea.ru
93.
Центр дистанционного обучения4) Реакции со спиртами (+ ROH)
А) AdE: ROH, HgSO4 или H+
AdE
AdE
винилэтиловый эфир –
очень реакционноспособный!!!
диэтилацеталь этаналя
(1,1-диэтоксиэтан)
• реакция идет по правилу Марковникова
• конечные продукты – диалкилацетали карбонильных соединений
online.mirea.ru
94.
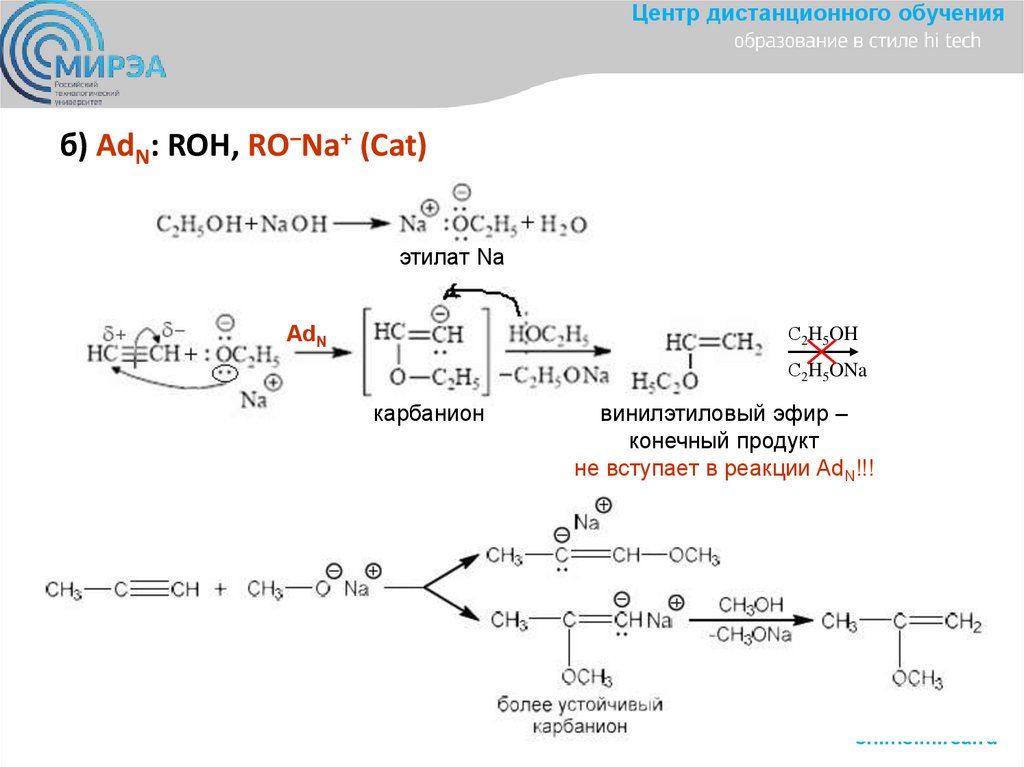
Центр дистанционного обученияб) AdN: ROH, RO‒Na+ (Cat)
этилат Na
С2H5OH
AdN
С2H5ONa
карбанион
винилэтиловый эфир –
конечный продукт
не вступает в реакции AdN!!!
online.mirea.ru
95. 2. Реакции окисления
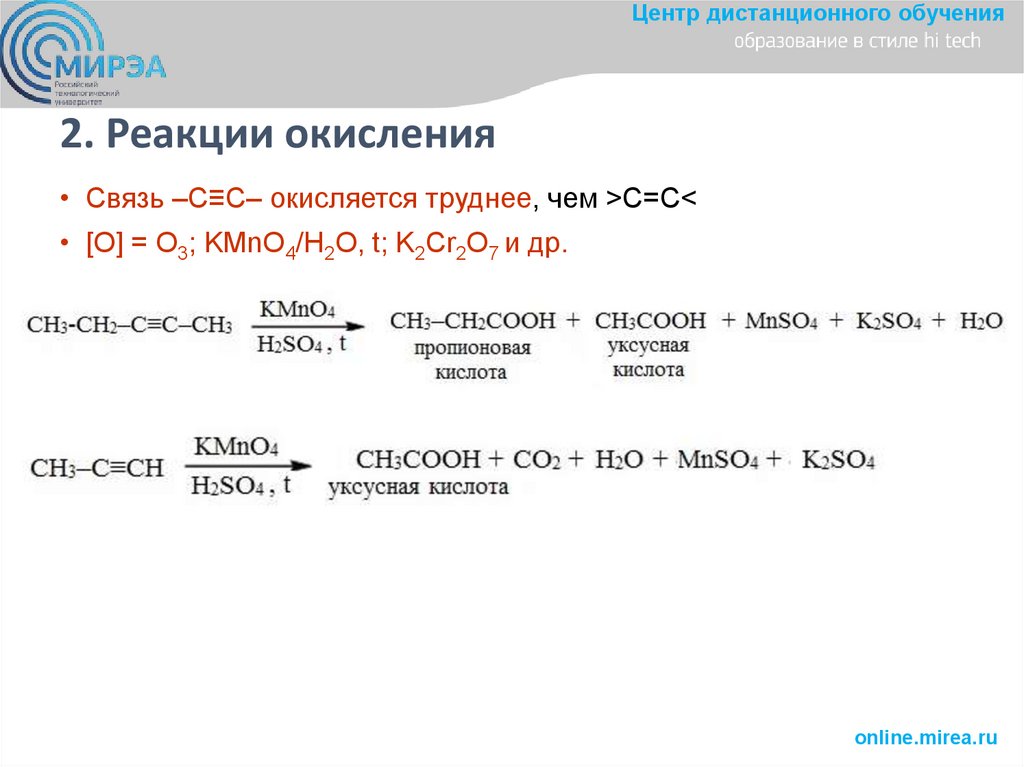
Центр дистанционного обучения2. Реакции окисления
• Связь ‒С≡С‒ окисляется труднее, чем >C=C<
• [O] = O3; KMnO4/H2O, t; K2Cr2O7 и др.
online.mirea.ru
96.
Центр дистанционного обучения• Реакции с комплексными солями тяжелых металлов – качественные
на терминальную тройную связь
реактив Толленса
online.mirea.ru
97.
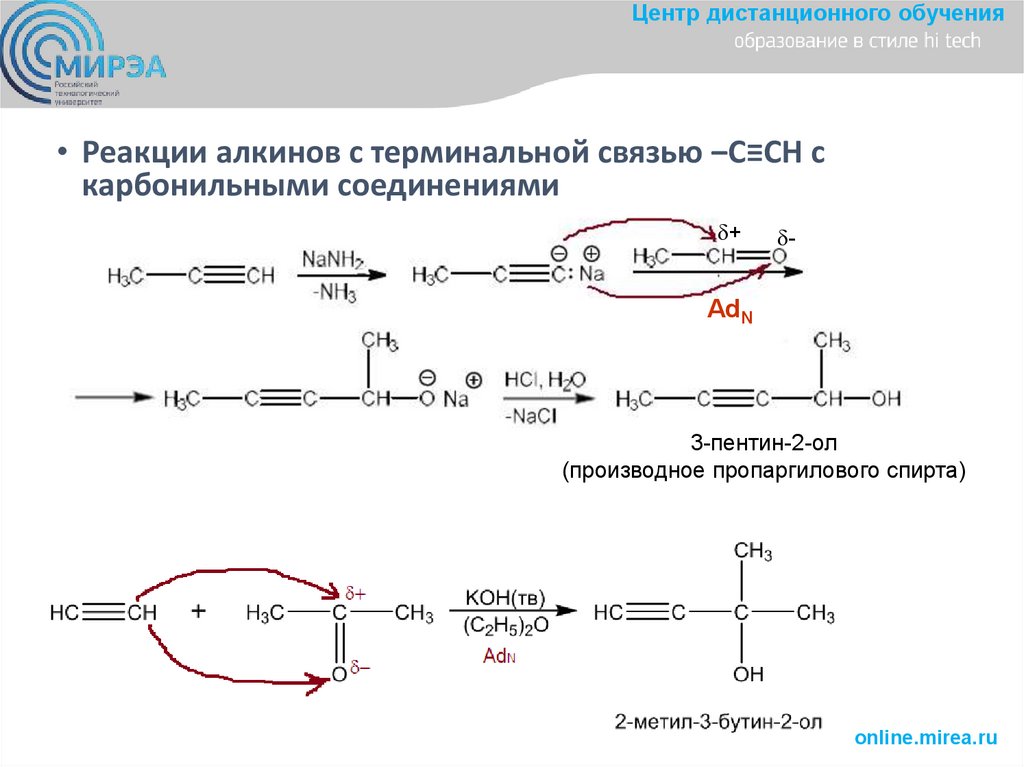
Центр дистанционного обучения• Реакции алкинов с терминальной связью ‒С≡СН с
карбонильными соединениями
+
-
AdN
3-пентин-2-ол
(производное пропаргилового спирта)
online.mirea.ru
98. Тема 5: Ароматические соединения
Центр дистанционного обученияТема 5: Ароматические соединения
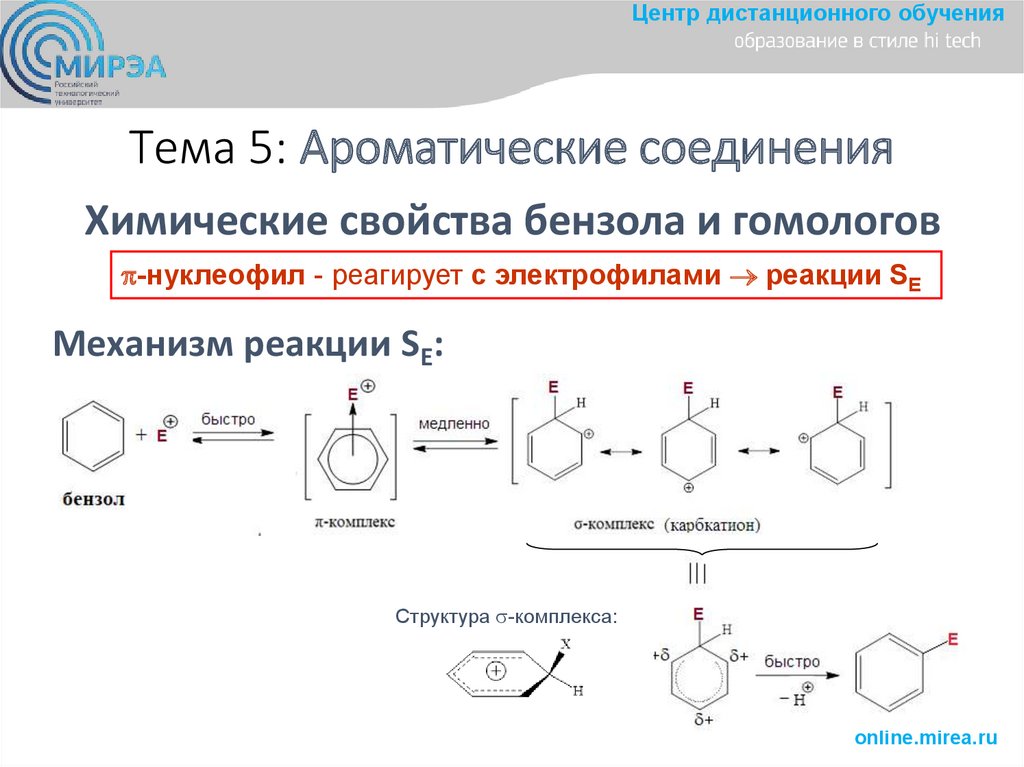
Химические свойства бензола и гомологов
-нуклеофил - реагирует с электрофилами реакции SE
Механизм реакции SE:
Структура -комплекса:
online.mirea.ru
99. Реакции SE для монозамещенных производных бензола
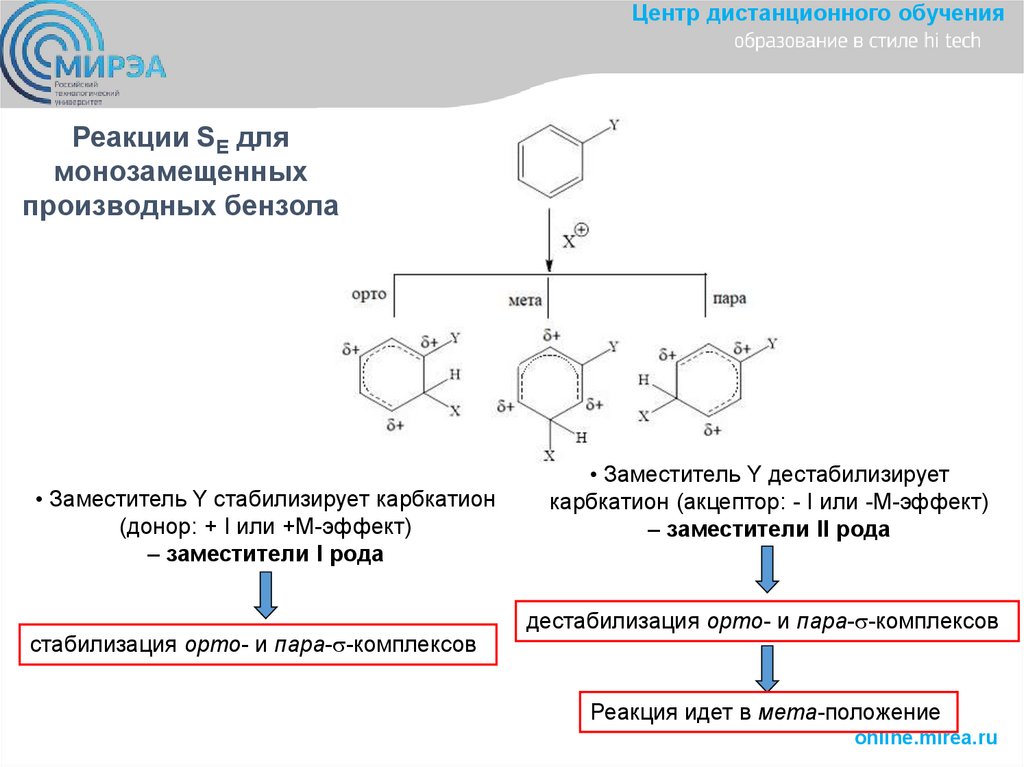
Центр дистанционного обученияРеакции SE для
монозамещенных
производных бензола
• Заместитель Y стабилизирует карбкатион
(донор: + I или +M-эффект)
– заместители I рода
стабилизация орто- и пара- -комплексов
• Заместитель Y дестабилизирует
карбкатион (акцептор: - I или -M-эффект)
– заместители II рода
дестабилизация орто- и пара- -комплексов
Реакция идет в мета-положение
online.mirea.ru
100.
Центр дистанционного обученияonline.mirea.ru
101.
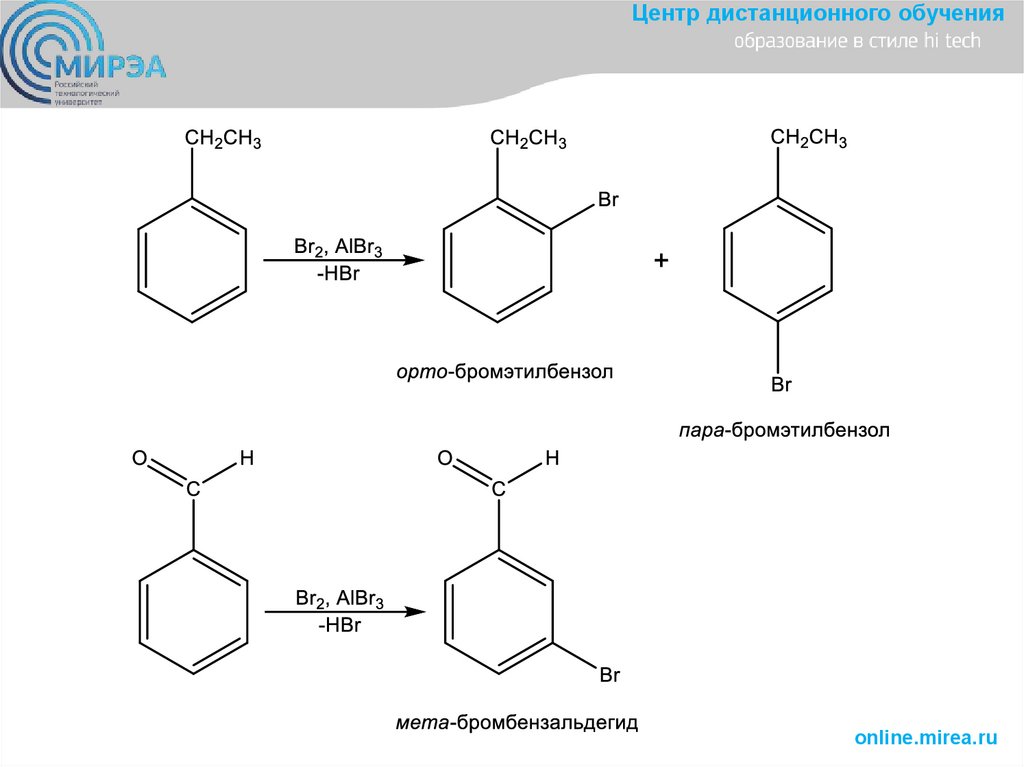
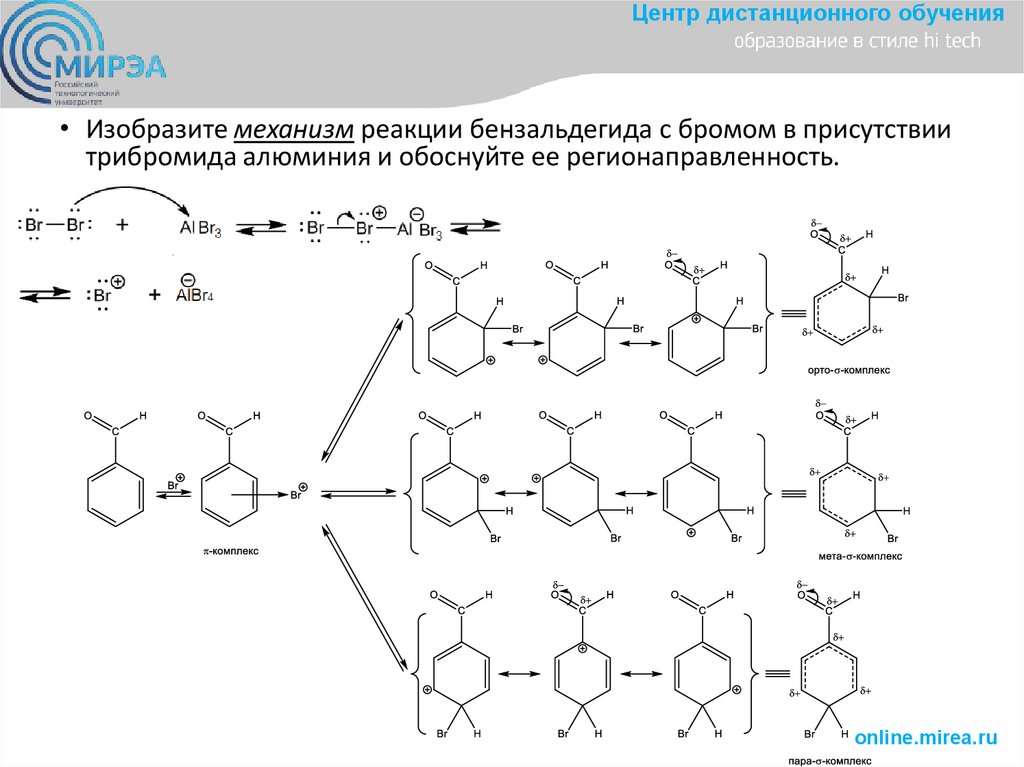
Центр дистанционного обучения• Изобразите механизм реакции бензальдегида с бромом в присутствии
трибромида алюминия и обоснуйте ее регионаправленность.
online.mirea.ru
102.
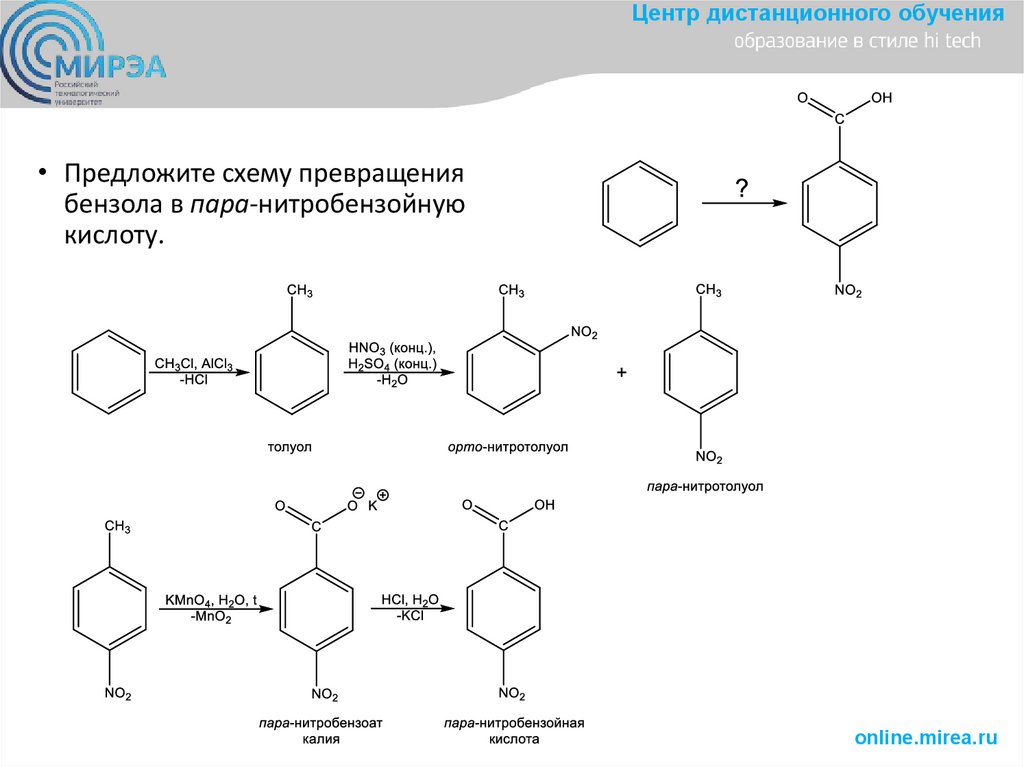
Центр дистанционного обучения• Предложите схему превращения
бензола в пара-нитробензойную
кислоту.
online.mirea.ru
103.
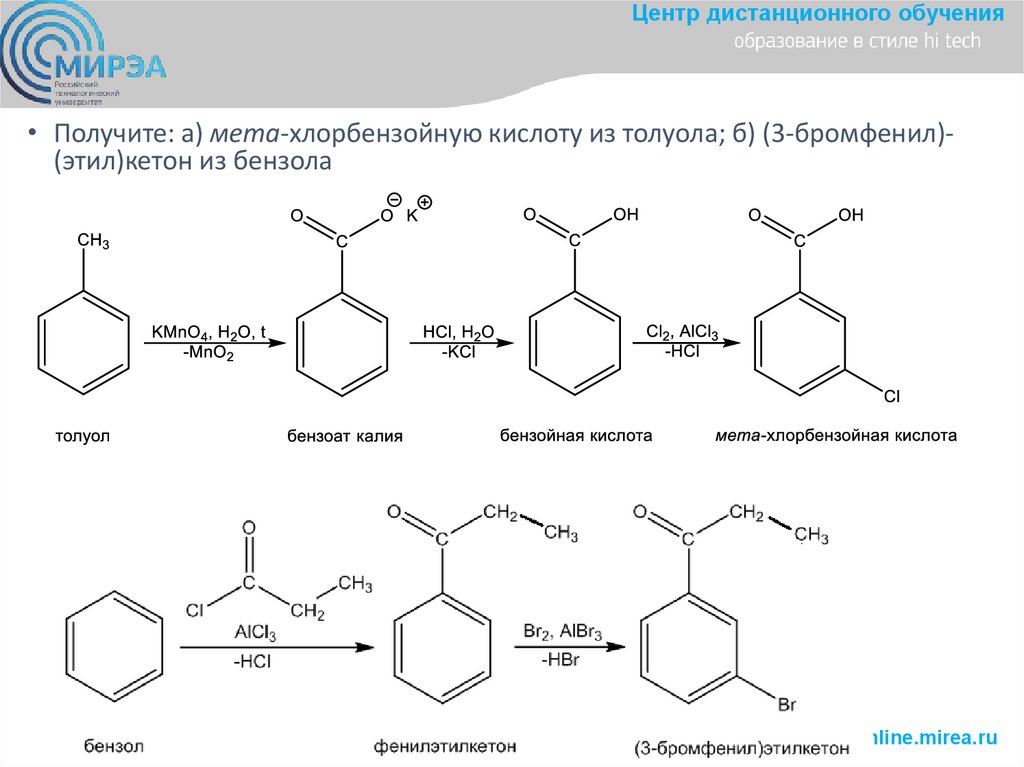
Центр дистанционного обучения• Получите: а) мета-хлорбензойную кислоту из толуола; б) (3-бромфенил)(этил)кетон из бензола
online.mirea.ru
104.
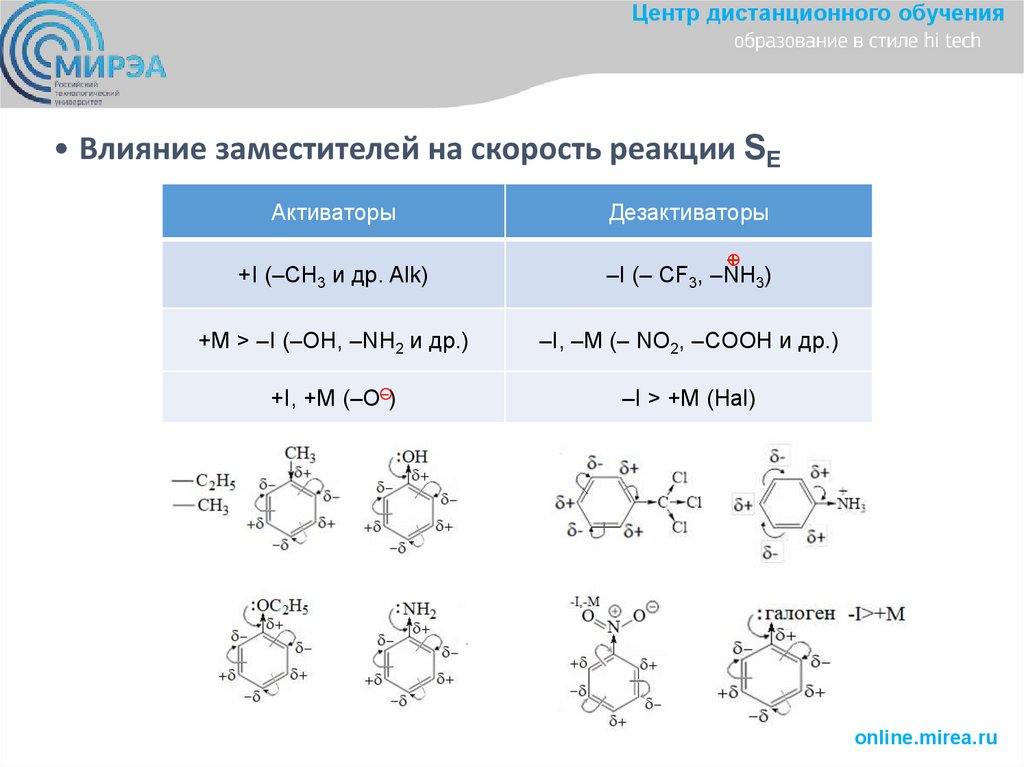
Центр дистанционного обучения• Влияние заместителей на скорость реакции SE
Активаторы
Дезактиваторы
+I (‒CH3 и др. Alk)
‒I (‒ CF3, ‒NH3)
+M > ‒I (‒ОН, ‒NH2 и др.)
‒I, ‒M (‒ NO2, ‒COOH и др.)
+I, +M (‒O‒)
‒I > +M (Hal)
+
online.mirea.ru
105.
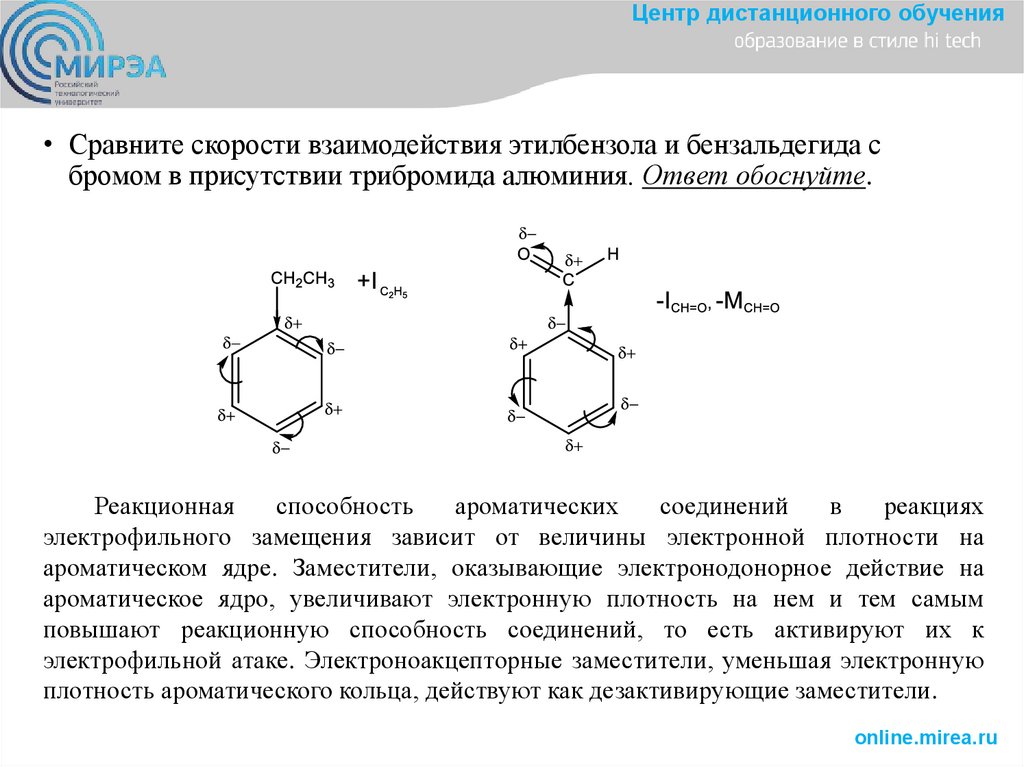
Центр дистанционного обучения• Сравните скорости взаимодействия этилбензола и бензальдегида с
бромом в присутствии трибромида алюминия. Ответ обоснуйте.
Реакционная
способность
ароматических
соединений
в
реакциях
электрофильного замещения зависит от величины электронной плотности на
ароматическом ядре. Заместители, оказывающие электронодонорное действие на
ароматическое ядро, увеличивают электронную плотность на нем и тем самым
повышают реакционную способность соединений, то есть активируют их к
электрофильной атаке. Электроноакцепторные заместители, уменьшая электронную
плотность ароматического кольца, действуют как дезактивирующие заместители.
online.mirea.ru
106. Правила ориентации в дизамещенных производных бензола
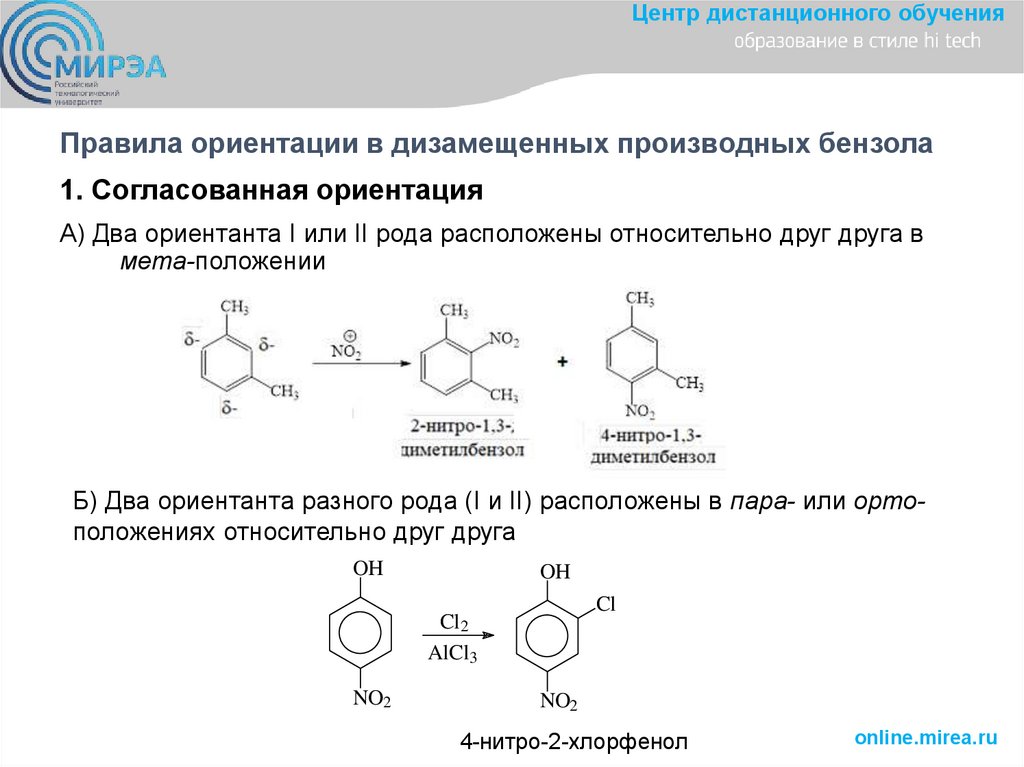
Центр дистанционного обученияПравила ориентации в дизамещенных производных бензола
1. Согласованная ориентация
А) Два ориентанта I или II рода расположены относительно друг друга в
мета-положении
Б) Два ориентанта разного рода (I и II) расположены в пара- или ортоположениях относительно друг друга
OH
OH
Cl
Cl2
AlCl3
NO2
NO2
4-нитро-2-хлорфенол
online.mirea.ru
107.
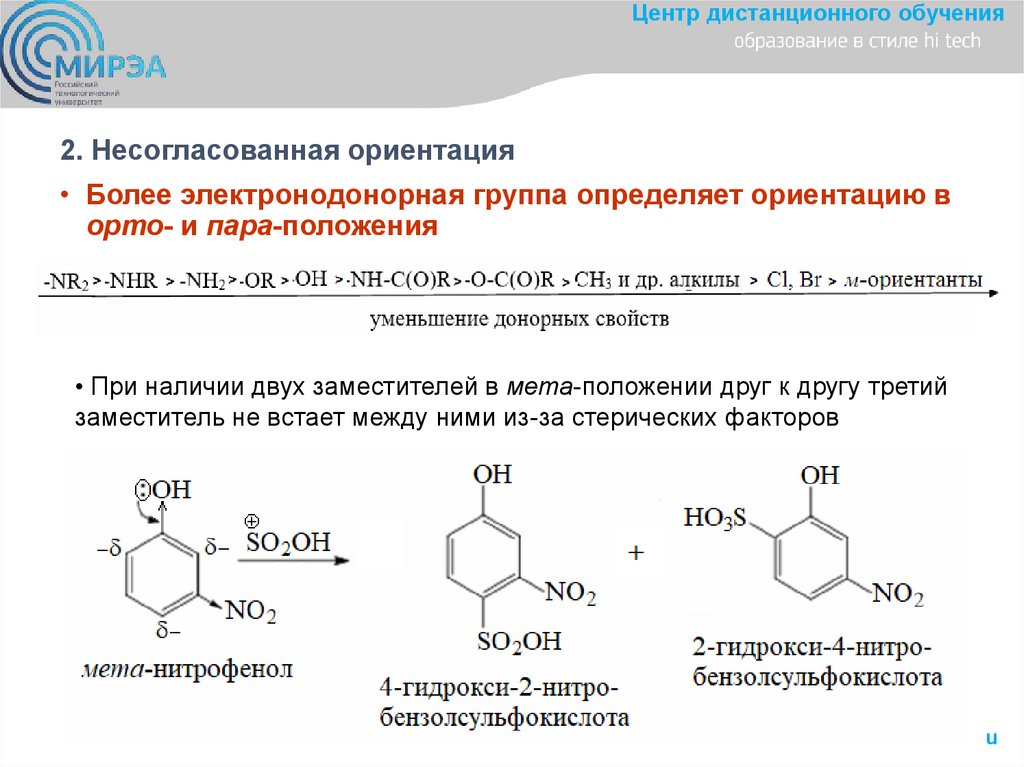
Центр дистанционного обучения2. Несогласованная ориентация
• Более электронодонорная группа определяет ориентацию в
орто- и пара-положения
• При наличии двух заместителей в мета-положении друг к другу третий
заместитель не встает между ними из-за стерических факторов
online.mirea.ru
108.
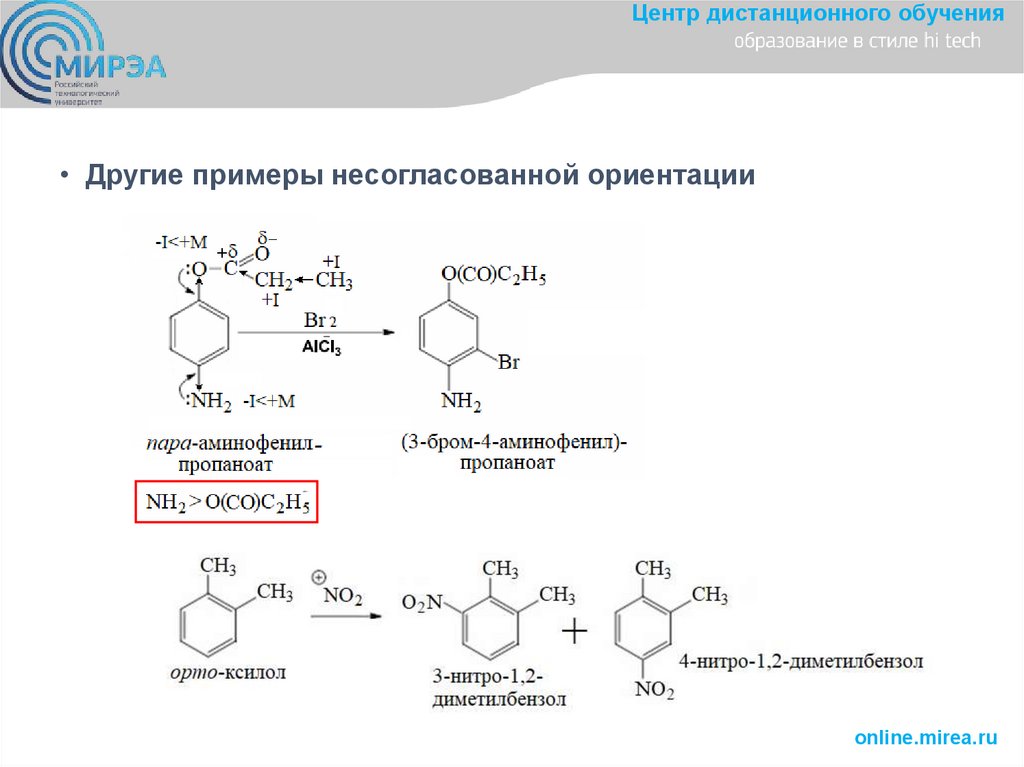
Центр дистанционного обучения• Другие примеры несогласованной ориентации
online.mirea.ru
109. Реакции радикального замещения (SR) по боковым цепям гомологов бензола
Центр дистанционного обученияРеакции радикального замещения (SR) по
боковым цепям гомологов бензола
• Галогенирование (Cl2, Br2)
Условия: hn, t C или R● (SR)
по -положению!!!
CH2
CH3
CH
CH3
CH
CH3
CH
CH3
CH
CH3
Cl2
hn
- HCl
этилбензол
бензильный радикал
online.mirea.ru
110. Химические свойства нафталина
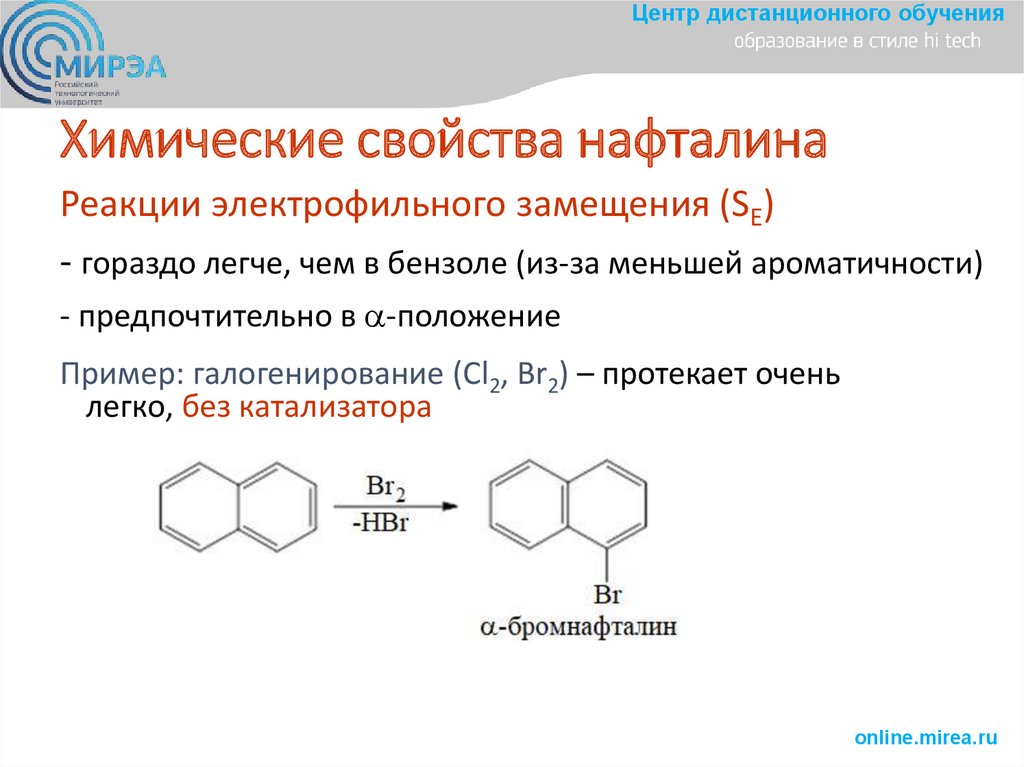
Центр дистанционного обученияХимические свойства нафталина
Реакции электрофильного замещения (SE)
- гораздо легче, чем в бензоле (из-за меньшей ароматичности)
- предпочтительно в -положение
Пример: галогенирование (Cl2, Br2) – протекает очень
легко, без катализатора
online.mirea.ru
111.
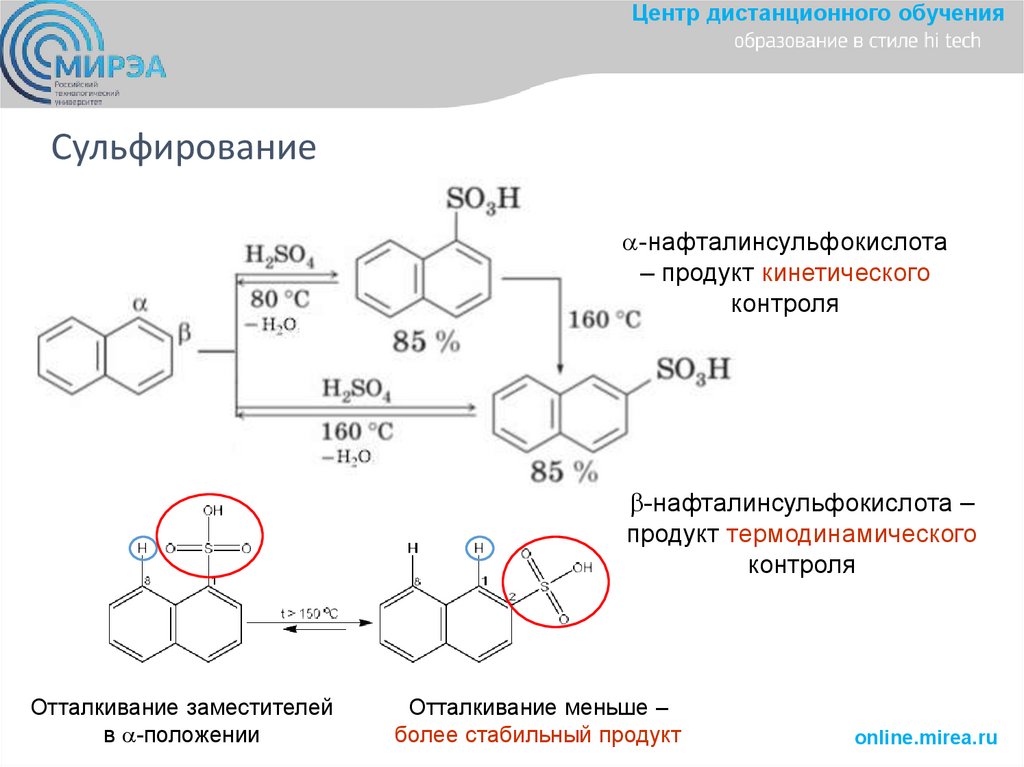
Центр дистанционного обученияСульфирование
-нафталинсульфокислота
– продукт кинетического
контроля
-нафталинсульфокислота –
продукт термодинамического
контроля
Отталкивание заместителей
в -положении
Отталкивание меньше –
более стабильный продукт
online.mirea.ru
112.
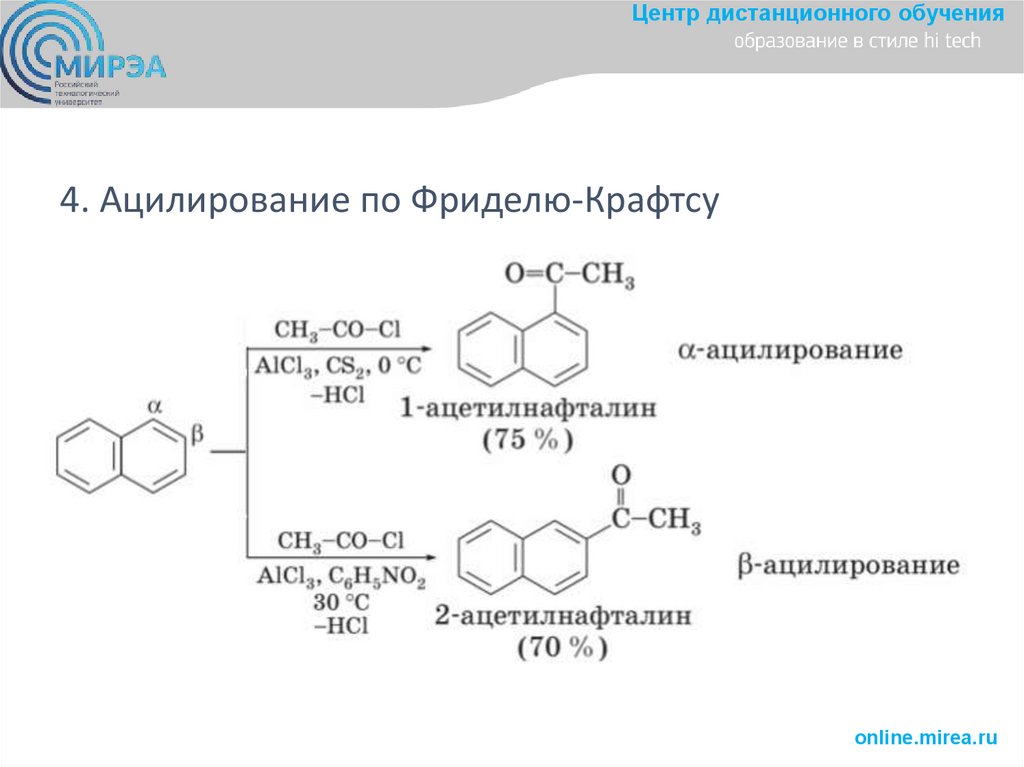
Центр дистанционного обучения4. Ацилирование по Фриделю-Крафтсу
online.mirea.ru
113.
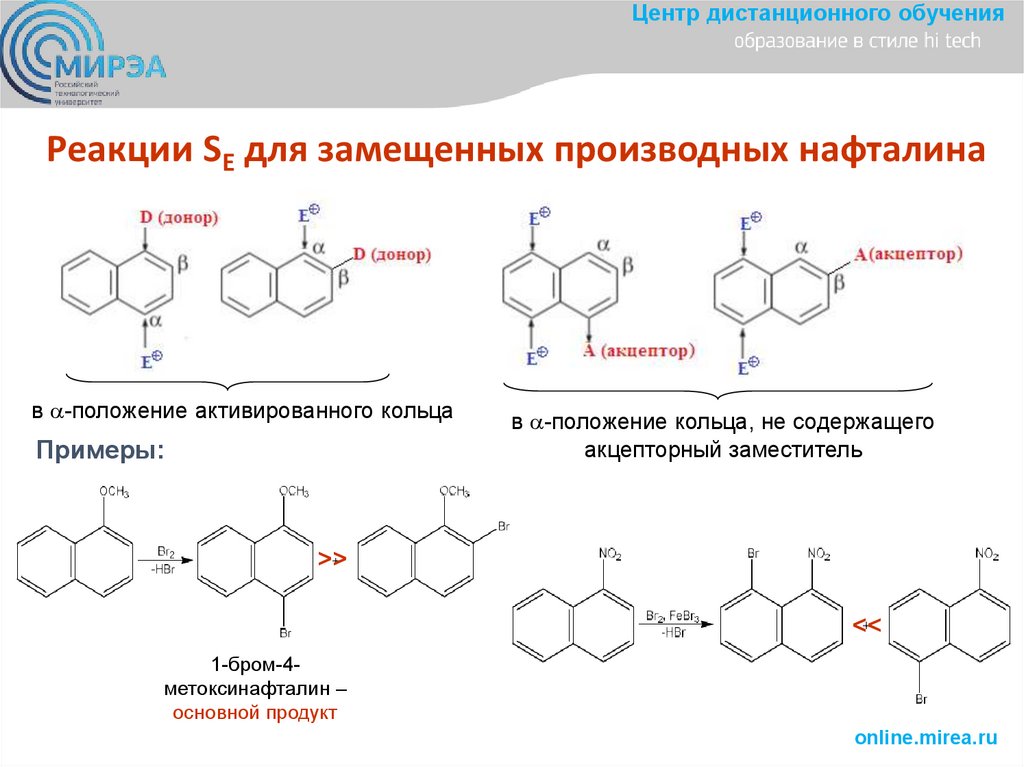
Центр дистанционного обученияРеакции SE для замещенных производных нафталина
в -положение активированного кольца
Примеры:
в -положение кольца, не содержащего
акцепторный заместитель
>>
<<
1-бром-4метоксинафталин –
основной продукт
online.mirea.ru
114. Способы получения пятичленных гетероциклов
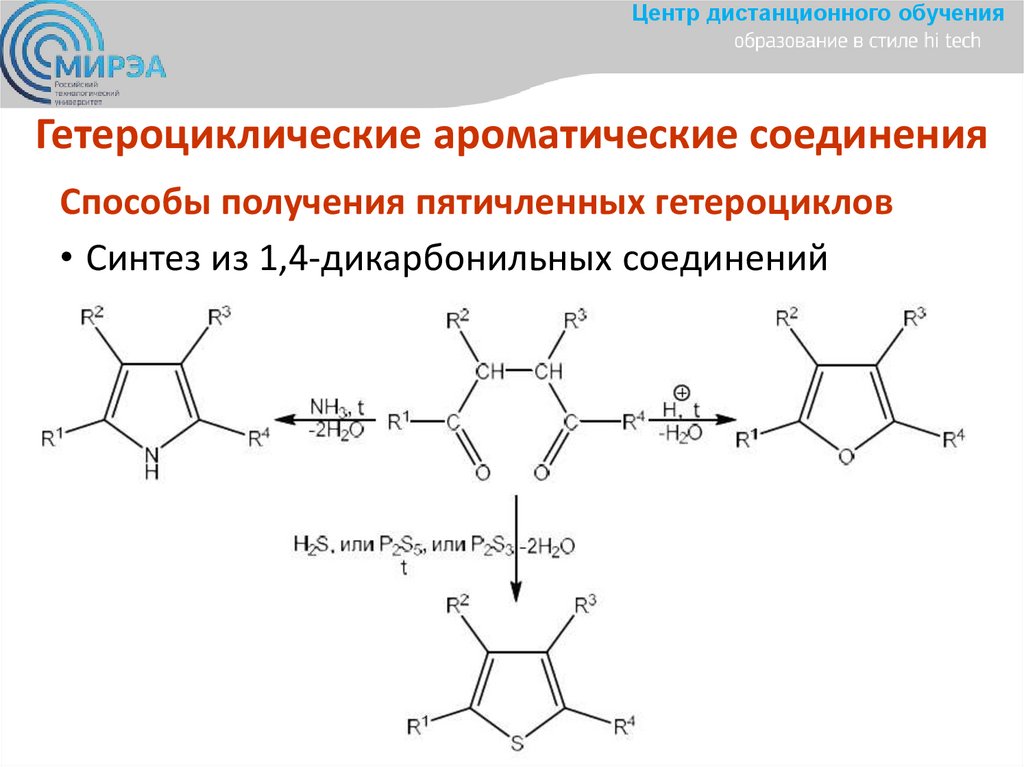
Центр дистанционного обученияГетероциклические ароматические соединения
Способы получения пятичленных гетероциклов
• Синтез из 1,4-дикарбонильных соединений
online.mirea.ru
115.
Центр дистанционного обучения• Напишите уравнения реакции 4-оксопентаналя с
аммиаком
4-оксопентаналь
2-метилпиррол
online.mirea.ru
116. Способы получения производных пиридина
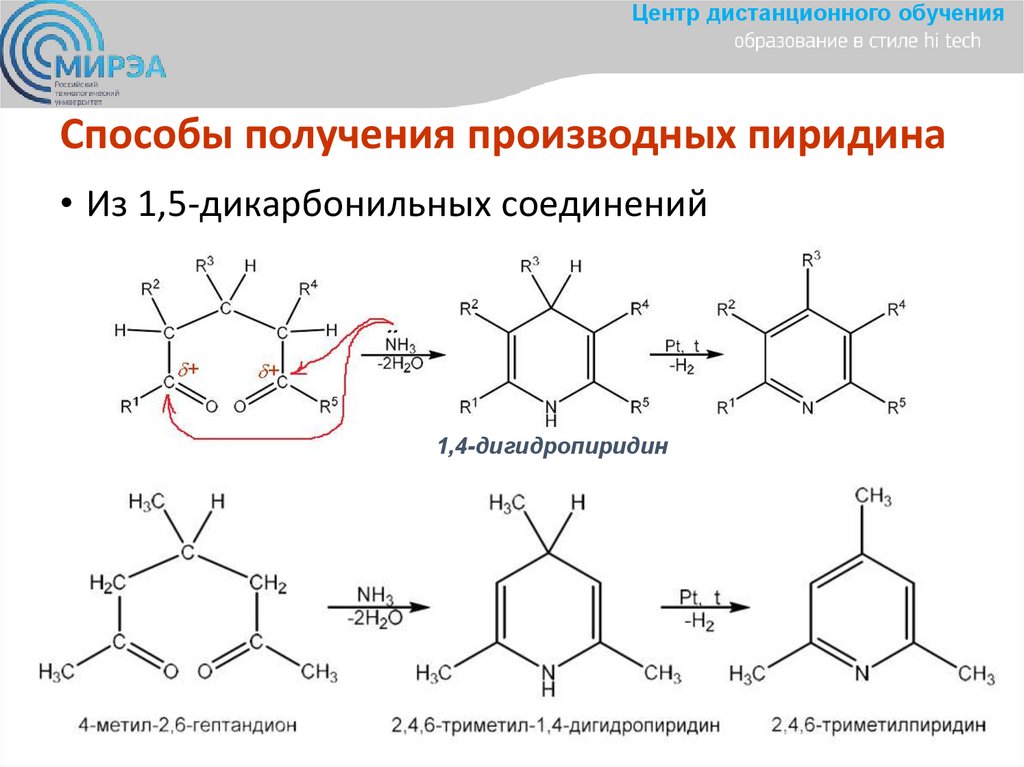
Центр дистанционного обученияСпособы получения производных пиридина
• Из 1,5-дикарбонильных соединений
1,4-дигидропиридин
online.mirea.ru
117. Химические свойства пятичленных гетероциклов
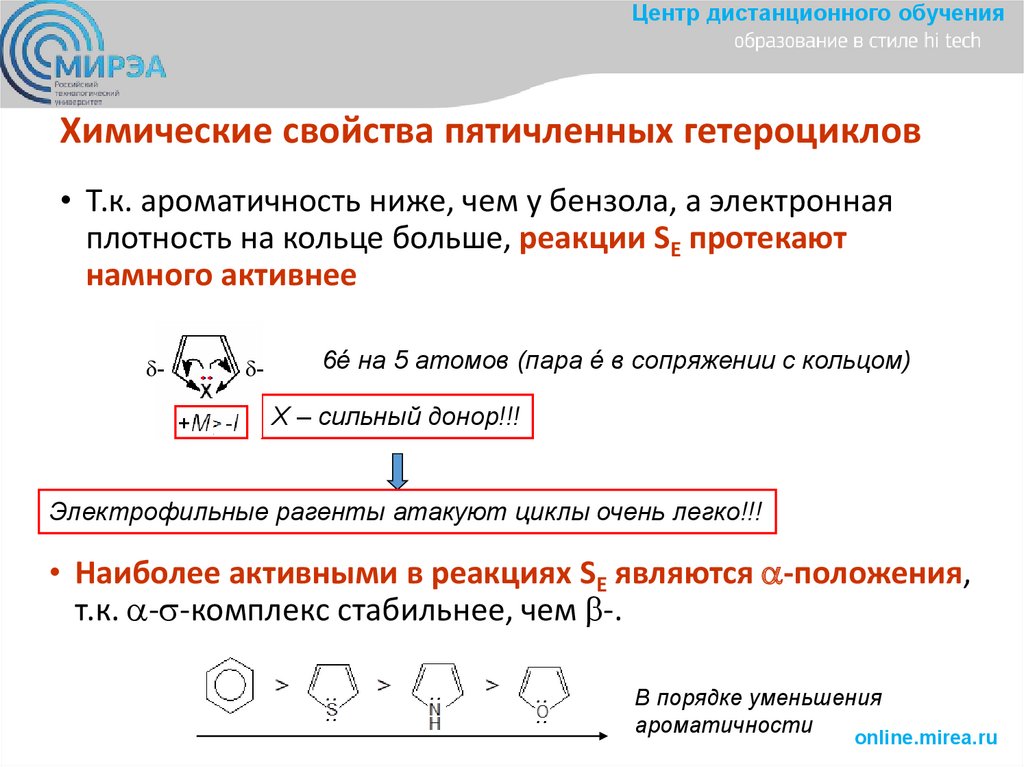
Центр дистанционного обученияХимические свойства пятичленных гетероциклов
• Т.к. ароматичность ниже, чем у бензола, а электронная
плотность на кольце больше, реакции SE протекают
намного активнее
-
-
6é на 5 атомов (пара é в сопряжении с кольцом)
Х – сильный донор!!!
Электрофильные рагенты атакуют циклы очень легко!!!
• Наиболее активными в реакциях SE являются -положения,
т.к. - -комплекс стабильнее, чем -.
..
..
..
..
..
В порядке уменьшения
ароматичности
online.mirea.ru
118.
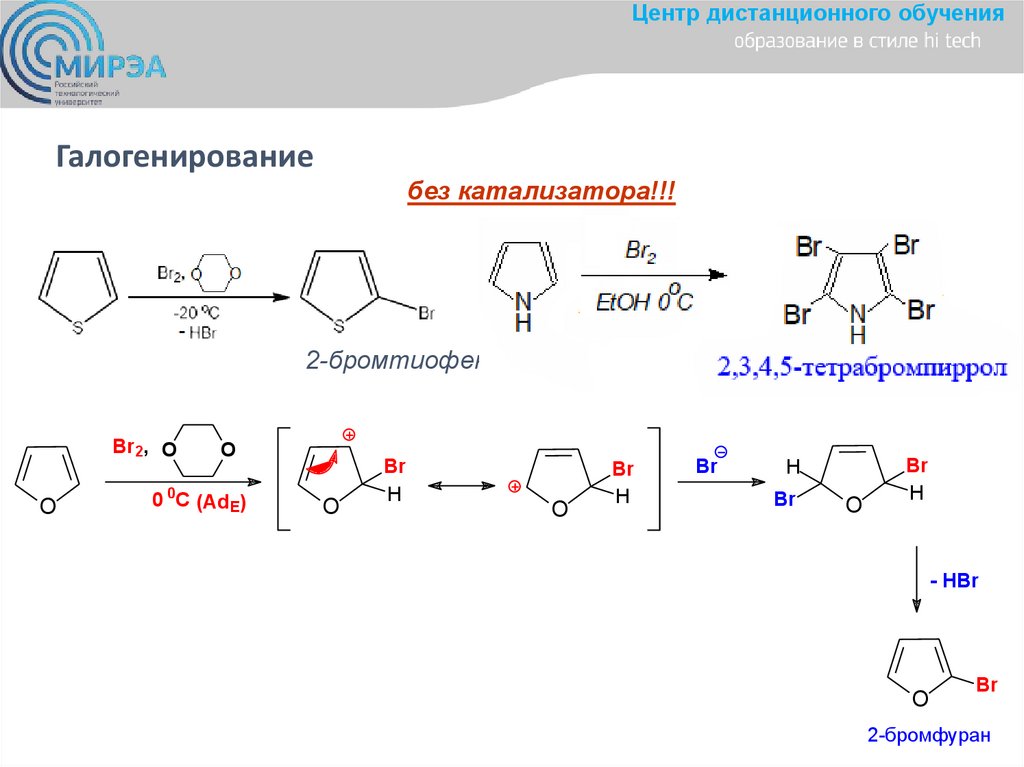
Центр дистанционного обученияГалогенирование
без катализатора!!!
2-бромтиофен
Br2, O
O
O
0 0C (AdE)
O
Br
H
O
Br
H
Br
H
Br
O
Br
H
- HBr
O
Br
2-бромфуран
online.mirea.ru
119.
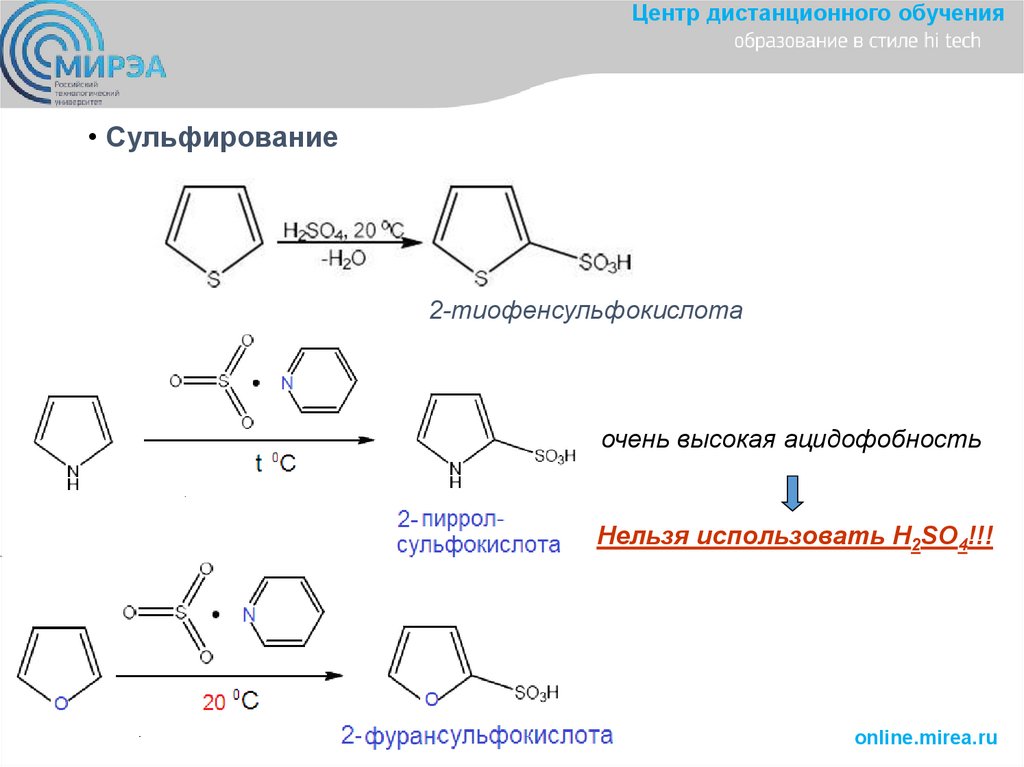
Центр дистанционного обучения• Сульфирование
2-тиофенсульфокислота
очень высокая ацидофобность
Нельзя использовать H2SO4!!!
online.mirea.ru
120.
Центр дистанционного обучения• Нитрование
Механизм реакции:
online.mirea.ru
121.
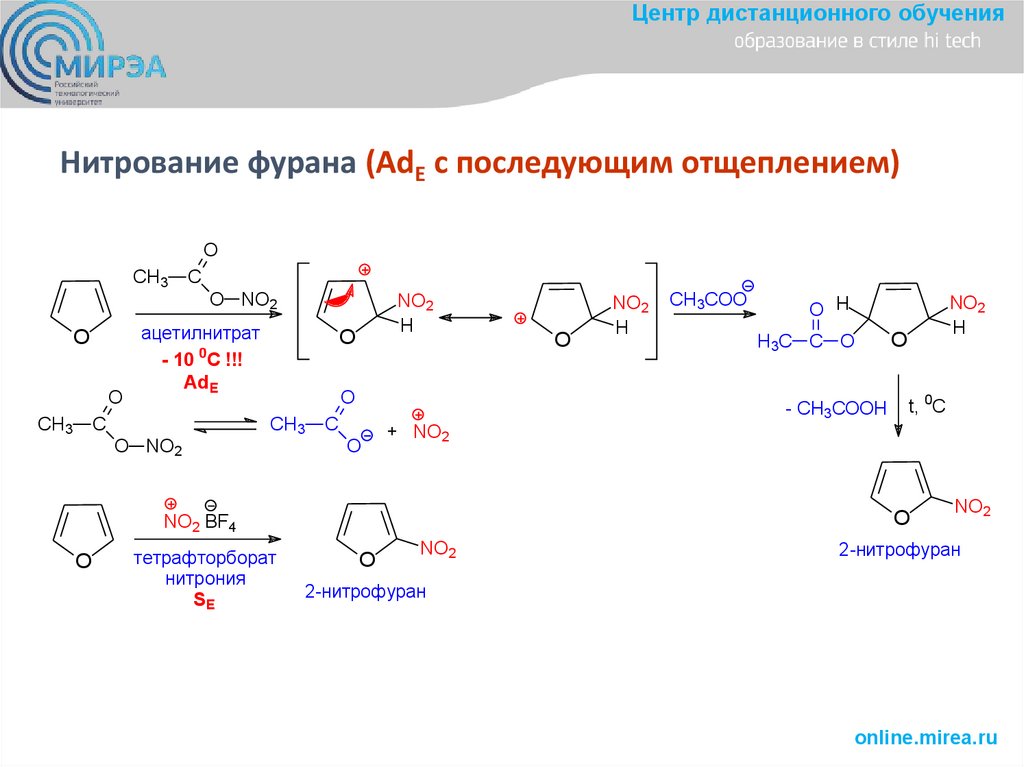
Центр дистанционного обученияНитрование фурана (AdE с последующим отщеплением)
O
CH3
O
O
CH3
C
O NO2
ацетилнитрат
- 10 0C !!!
AdE
C
O NO2
NO2
H
O
O
CH3
тетрафторборат
нитрония
SE
CH3COO
C
O
NO2
H
O H
H 3C C O
- CH3COOH
O
t, 0C
+ NO2
O
NO2 BF4
O
O
NO2
H
O
NO2
NO2
2-нитрофуран
2-нитрофуран
online.mirea.ru
122.
Центр дистанционного обучения• Ацилирование по Фриделю-Крафтсу
• Алкилирование по Фриделю-Крафтсу
+ продукты
полиалкилирования
2-изопропилтиофен
online.mirea.ru
123.
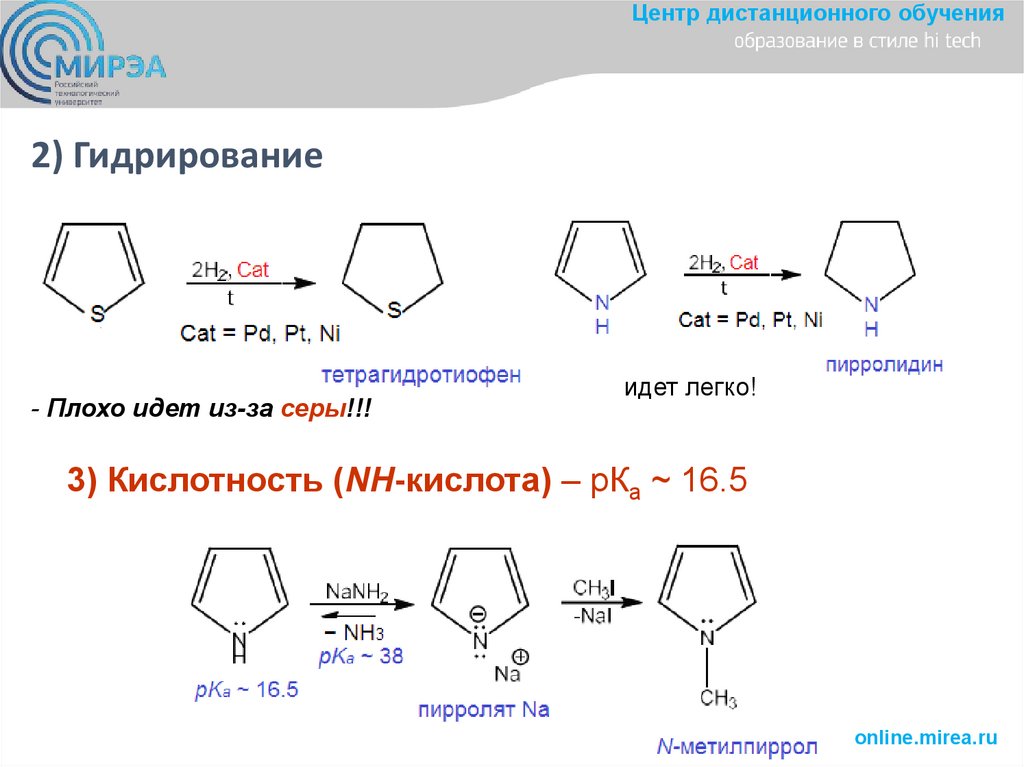
Центр дистанционного обучения2) Гидрирование
- Плохо идет из-за серы!!!
идет легко!
3) Кислотность (NH-кислота) – рКа ~ 16.5
online.mirea.ru
124.
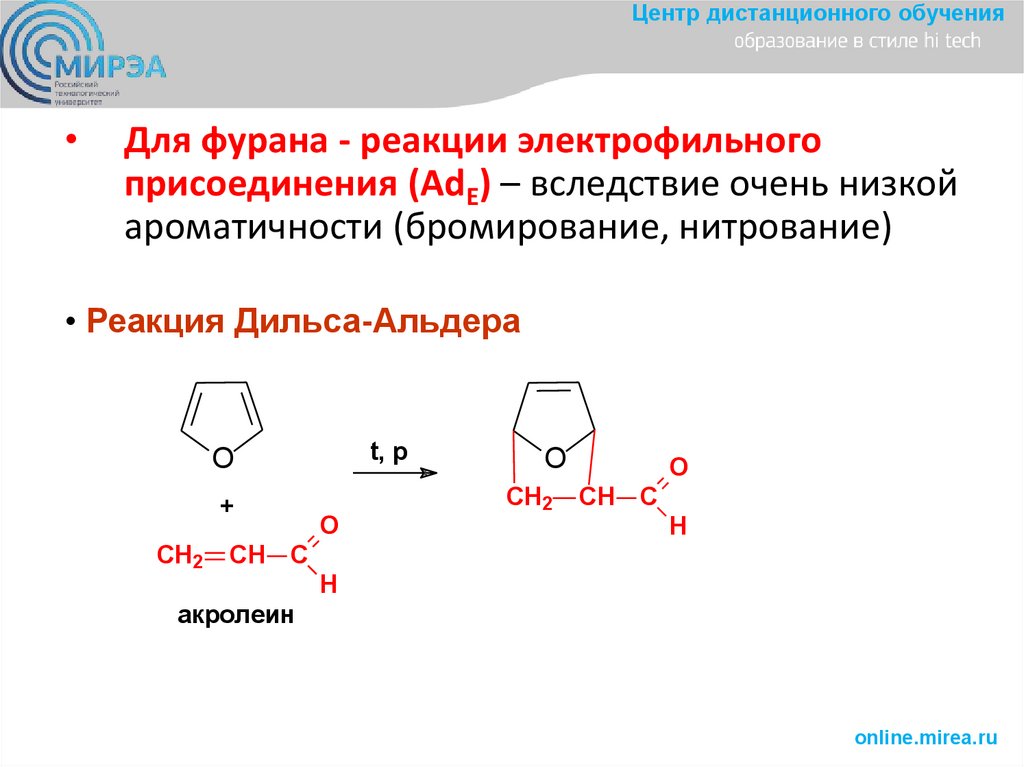
Центр дистанционного обученияДля фурана - реакции электрофильного
присоединения (AdE) – вследствие очень низкой
ароматичности (бромирование, нитрование)
• Реакция Дильса-Альдера
t, p
O
+
CH2
O
O
CH2
O
CH C
H
CH C
H
акролеин
online.mirea.ru
125. Химические свойства пиридина
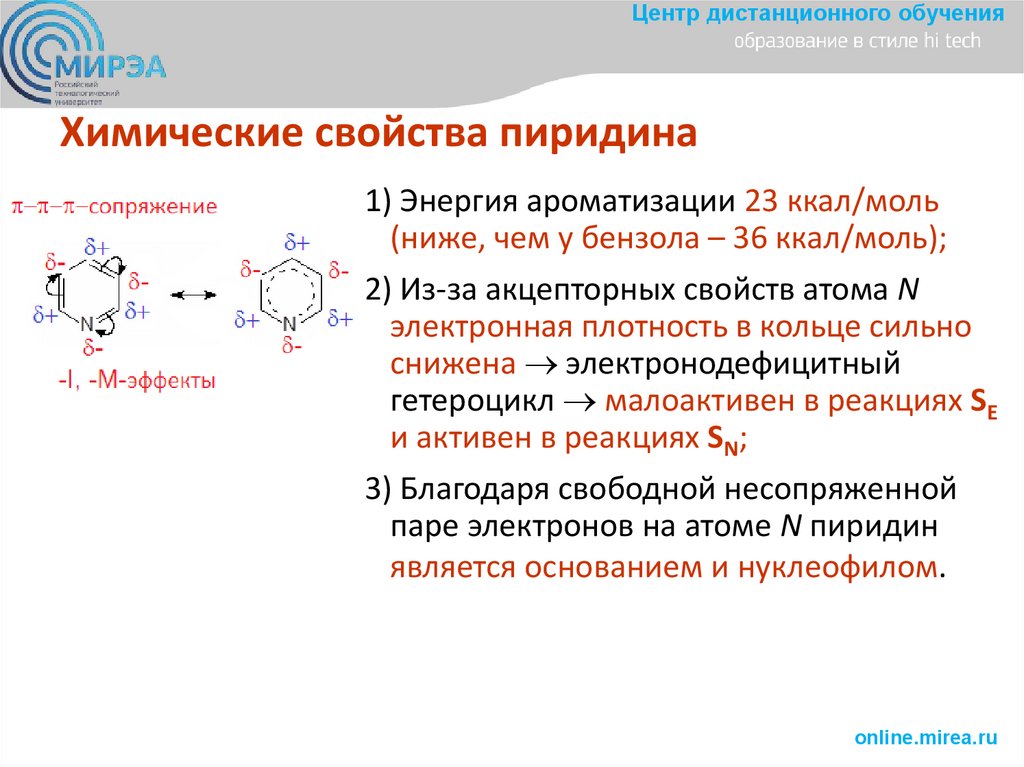
Центр дистанционного обученияХимические свойства пиридина
1) Энергия ароматизации 23 ккал/моль
(ниже, чем у бензола – 36 ккал/моль);
2) Из-за акцепторных свойств атома N
электронная плотность в кольце сильно
снижена электронодефицитный
гетероцикл малоактивен в реакциях SE
и активен в реакциях SN;
3) Благодаря свободной несопряженной
паре электронов на атоме N пиридин
является основанием и нуклеофилом.
online.mirea.ru
126. 1) Реакции SE
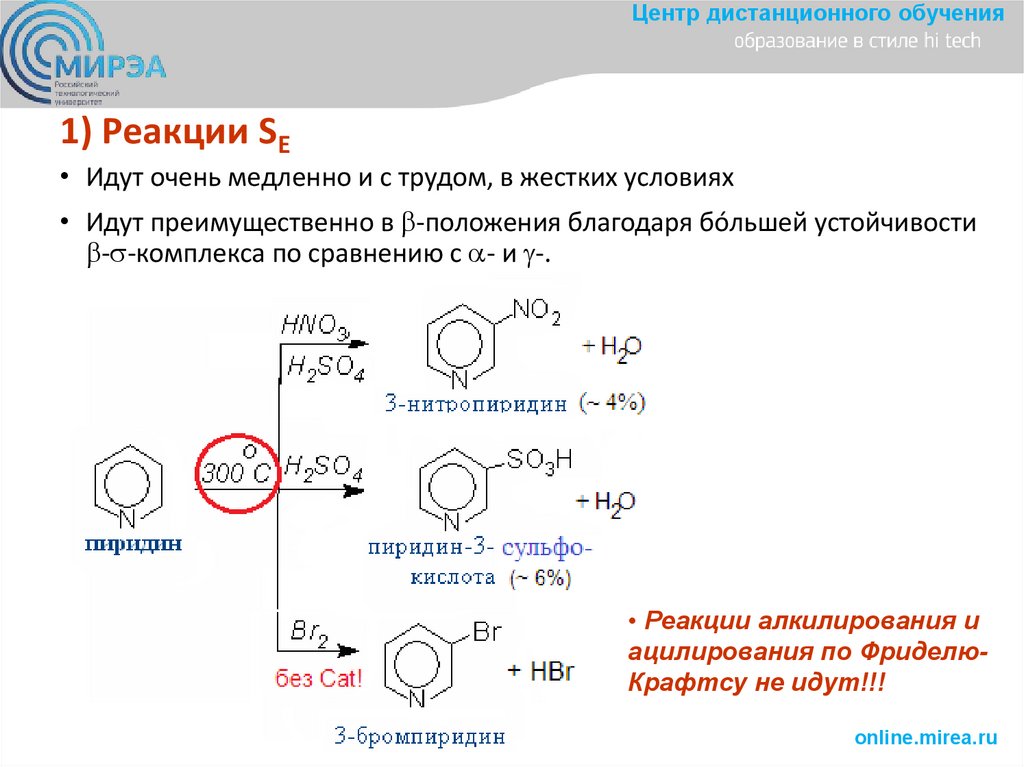
Центр дистанционного обучения1) Реакции SE
• Идут очень медленно и с трудом, в жестких условиях
• Идут преимущественно в -положения благодаря бóльшей устойчивости
- -комплекса по сравнению с - и -.
• Реакции алкилирования и
ацилирования по ФриделюКрафтсу не идут!!!
online.mirea.ru
127. 3) Основные свойства пиридина
Центр дистанционного обучения3) Основные свойства пиридина
- Не атакуется электрофилами
4) Нуклеофильные свойства пиридина
online.mirea.ru
128. Спасибо за внимание!
Центр дистанционного обученияСпасибо за внимание!
online.mirea.ru

























































 chemistry
chemistry








