Similar presentations:
Физические величины
1.
12.
23.
34.
45.
56. ОТНОСИТЕЛЬНАЯ АТОМНАЯ МАССА Ar
6ОТНОСИТЕЛЬНАЯ АТОМНАЯ
МАССА Ar
7.
78.
8m м лы (в ва)
Mr (в ва)
1 m 12 C
a
12
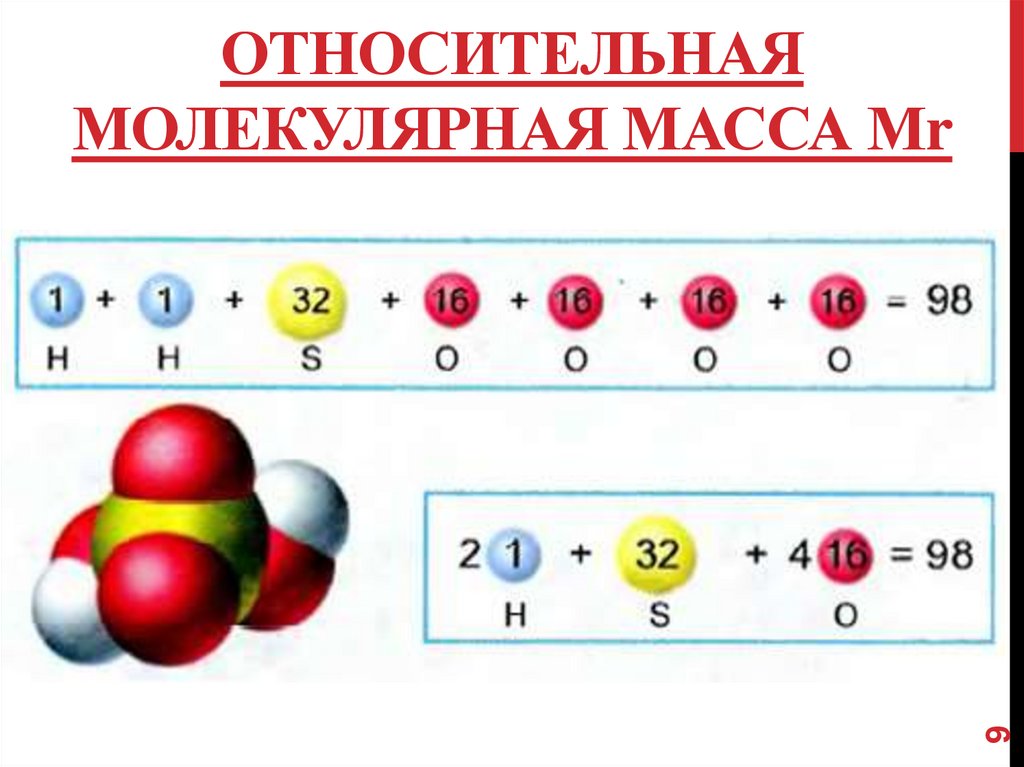
9. ОТНОСИТЕЛЬНАЯ молекулярная МАССА Мr
9ОТНОСИТЕЛЬНАЯ
МОЛЕКУЛЯРНАЯ МАССА Мr
10.
1011.
1112.
1213.
1314.
1415.
1516.
1617.
m – масса вещества;n – число молей вещества.
17
Молярная масса М
18.
mM
n
m
n
M
m n M
18
Молярная масса М
19.
1920.
Нормальные условия:T=
или 273 К
P = 1 атм. = 760 мм.рт.ст.
= 101,3 кПа
20
o
0 C
21.
Молярный объем газа Vm(л/моль)
V n Vm
21
m
Vm
V
M
22.
2223.
2324.
24D=
М газа1
М газа2
25. относительная плотность любого газа по водороду
ОТНОСИТЕЛЬНАЯПЛОТНОСТЬ ЛЮБОГО ГАЗА ПО
ВОДОРОДУ
М
М
газа
газа
М
М
газа
газа; М
Дн
22 Дн
Дн22 Мн 2 ; Мгаза
Дн22
газа
Мн2
2
25
2
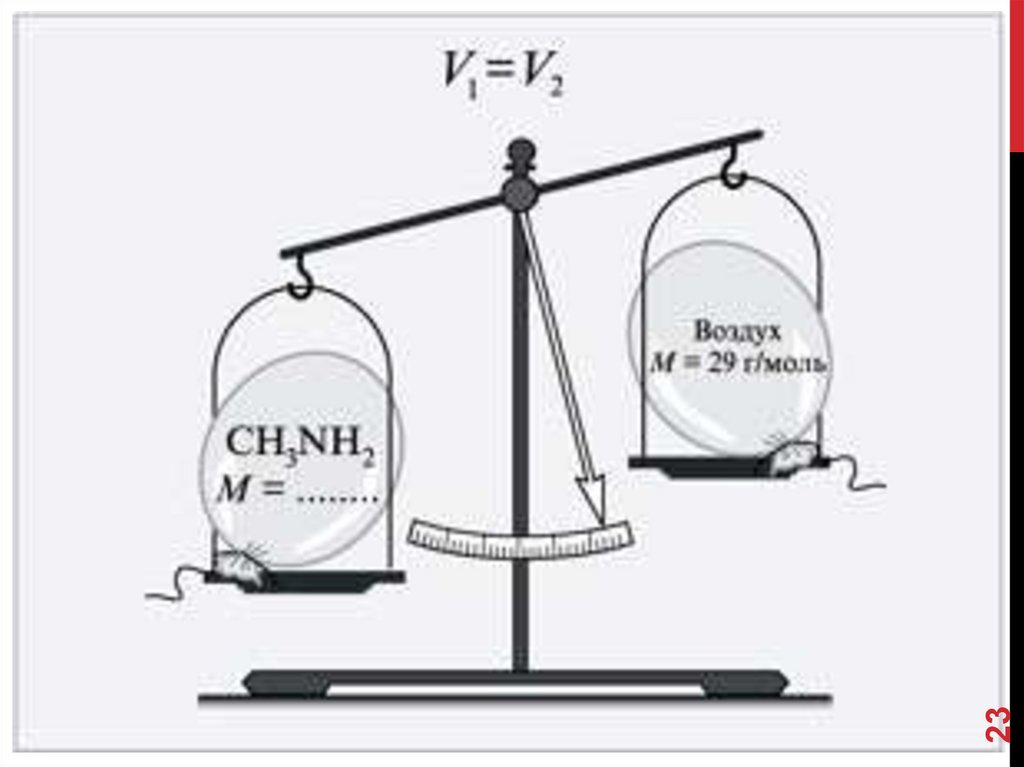
26. относительная плотность по воздуху
ОТНОСИТЕЛЬНАЯПЛОТНОСТЬ ПО ВОЗДУХУ
Д в озд
М газа
М газа
;
М в озд
29
26
М газа 29 Д возд
27.
Массовая доля элемента всоединении
27
Ar ( элемента) n( эл та)
(%)
100%
Mr (в ва)
28.
Основное уравнение газовогосостояния
(уравнение объединенного закона
Клайперона):
P, V, T – при данных условиях
P0, V0, T0 – при нормальных условиях
28
P0 V0
P V
T
T0
29.
Уравнение КлайперонаМенделееваm
PV
RT
M
29
PV nRT
30.
ДжR 8,314
моль K
(если P в Па, а V в м3)
л атм
R 0,082
( P(атм),V ( л))
моль К
30
R – универсальная газовая постоянная
31.
3132. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА (МЭ) ВЕЩЕСТВА
это масса 1 моль эквивалентавещества,
произведению
она
равна
фактора
эквивалентности на молярную
массу вещества:
32
33. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА (МЭ) ВЕЩЕСТВА
33Мэ (в-ва) = fэ *М (в-ва)
34. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА ЭЛЕМЕНТА
молярнойк
его
34
равна отношению
массы
элемента
валентности.
35. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА ОСНОВАНИЯ
равнаотношению
основания
к
молярной
числу
массы
замещенных
гидроксогрупп (ч3ОН-):
35
36. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА КИСЛОТЫ
равнаотношению
молярной
массы
кислоты к числу замещенных катионов
водорода (ч3Н+).
36
37. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА СОЛИ
молярной массы соли к произведениючисла катионов соли на его валентность.
37
МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА
СОЛИ
в обменных реакциях равна отношению
38.
3839.
3940.
4041.
4142.
4243.
4344.
М Э2V mЭ
1
V mЭ
2
m1 М Э1
m 2 М Э2
44
М Э1
m1 Э1
m 2 Э2
45. Домашнее задание
ДОМАШНЕЕ ЗАДАНИЕ1. В рабочей тетради ТЕМА № 2,
(з. 1, 2)
2. Выучить лекции № 1, 2.
45
3. Химический диктант № 1




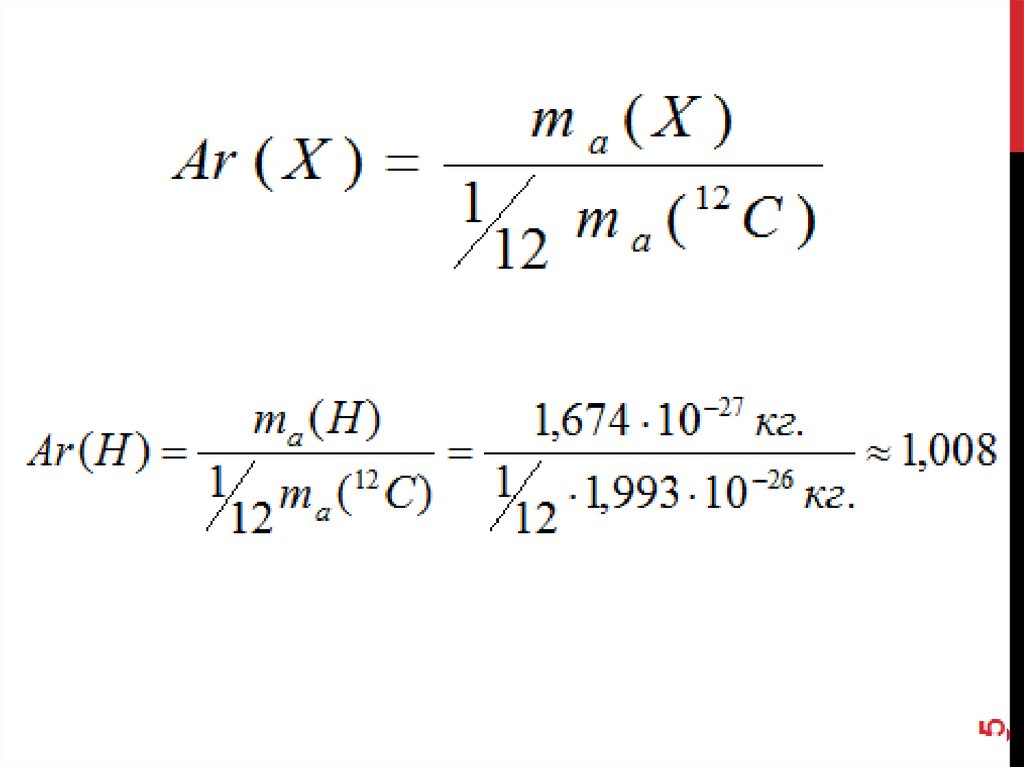


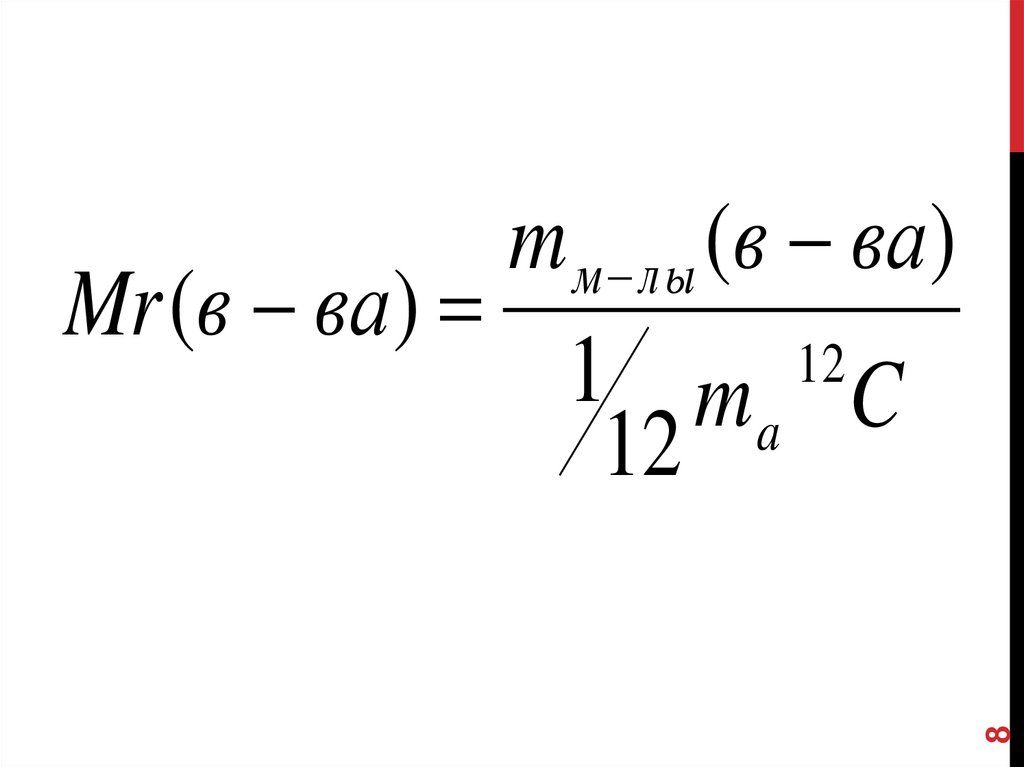





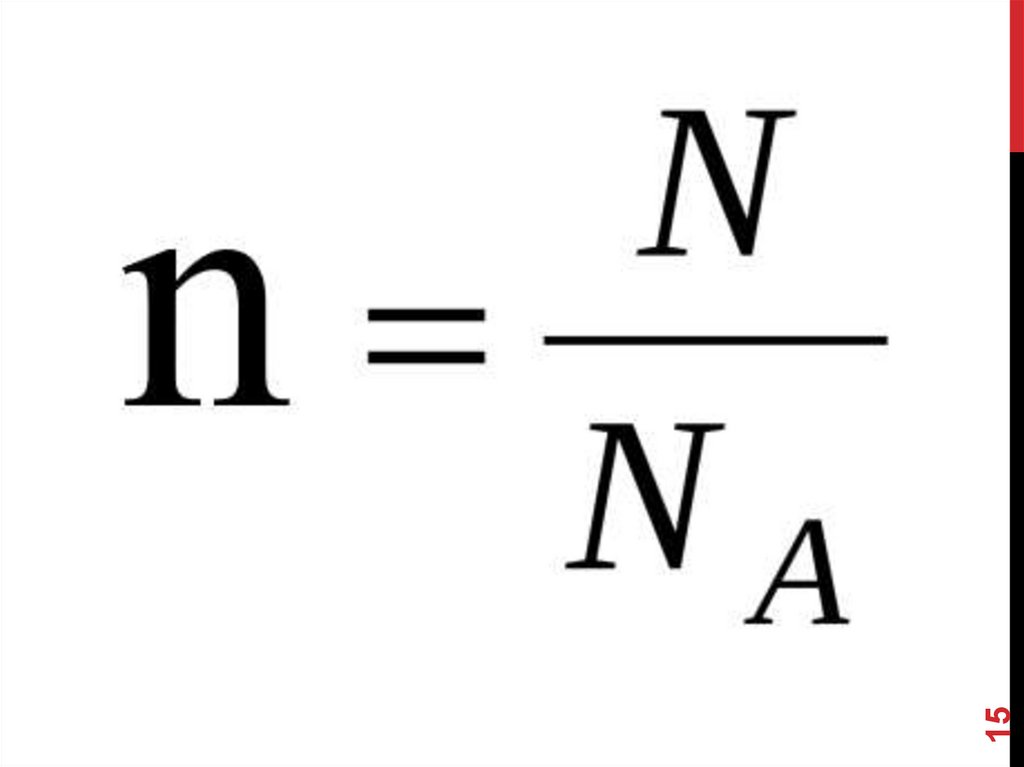







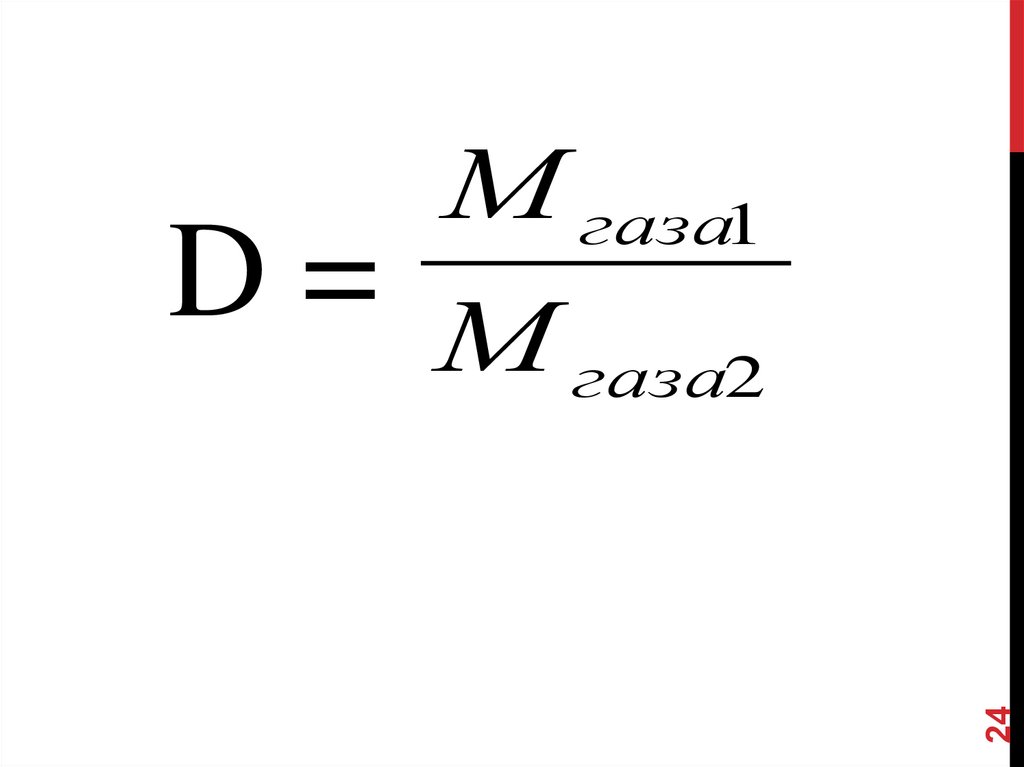



















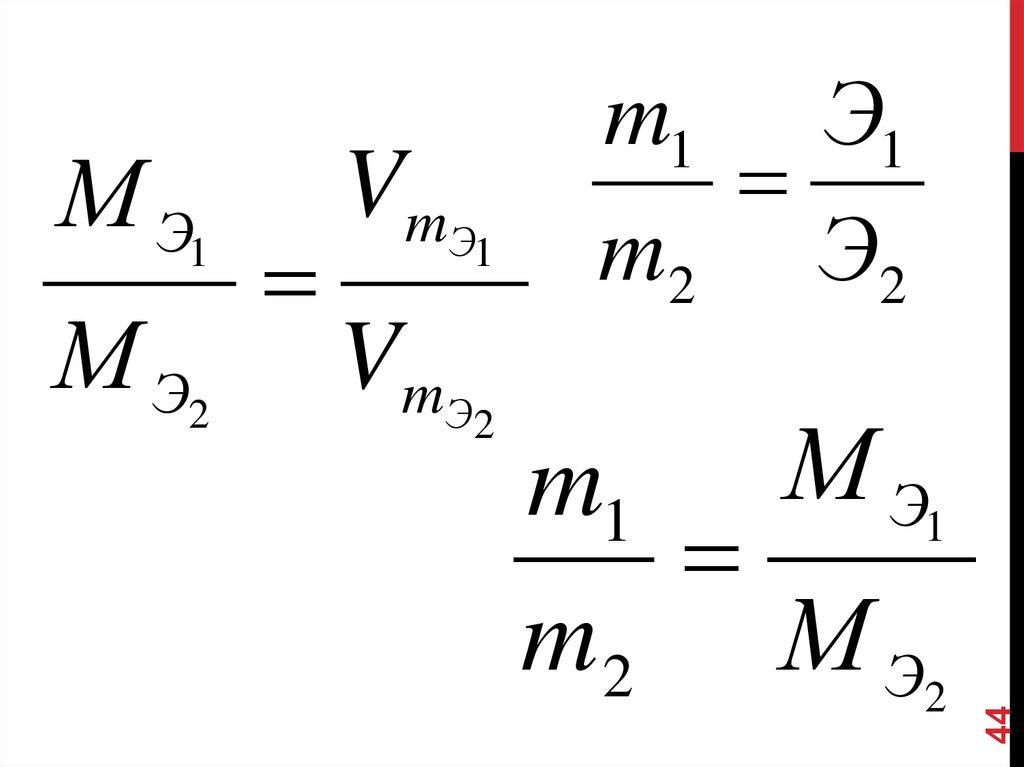

 chemistry
chemistry








