Similar presentations:
Алкены (CnH2n)
1.
2.
НоменклатураСтроение
молекулы
Изомерия
Физические
свойства
CnH2n
Химические
свойства
Получение
Проверка
знаний
Применение
3.
CnH2nАлкены – ациклические
углеводороды, в молекуле
которых кроме одинарных
связей содержится одна двойная
связь между атомами углерода.
Общая формула: СnH2n
4.
sp2-гибридизацияСтроение
молекулы
Cπ
δC
Угол связи – 1200
Форма молекулы – плоский треугольник
н
с
н
н
н
с
с
н
н
н
с
н
5.
1. Выбор главной цепи.С Н3 С Н С Н С Н С Н3
Номенклатура
СН3
2. Нумерация атомов главной
2
1
3
5
4
цепи.
С Н3 С Н С Н С Н С Н3
СН3
3. Формирование названия.
С Н3 С Н С Н С Н С Н3
СН3
4пенте - 2
метил н
6.
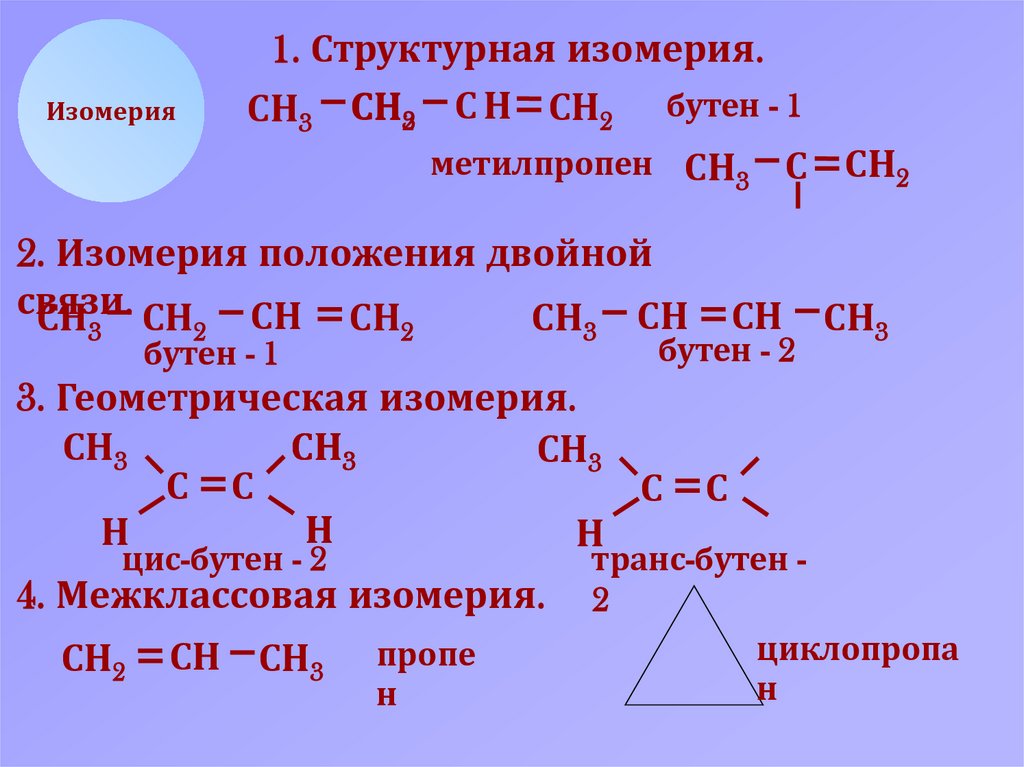
1. Структурная изомерия.СН3 СН32 С Н СН2 бутен - 1
метилпропен СН3 С СН2
Изомерия
2. Изомерия положения двойной
связи.
СН СН СН СН
СН СН
3
2
бутен - 1
2
3
бутен - 2
3. Геометрическая изомерия.
СН3
СН3
СН3
С С
С
Н
Н
Н
цис-бутен - 2
4. Межклассовая изомерия.
СН2
СН СН3
пропе
н
СН
СН3
С
транс-бутен 2
циклопропа
н
7.
Физическиесвойства
Агрегатное состояние:
С2Н4 – С4Н8
газообразные
вещества;
жидкости;
С5Н10 – С18Н36
с С19Н38
твердые вещества
С увеличением молекулярной массы соединений
температуры кипения и плавления закономерно
повышаются.
Г, З нефтяной, Ц
Этилен С2Н4
Tпл = - 169,20С
Tкип = -
103,70С
Плохо в
Н2О
8.
этиленХимические
свойства
+ Н2, t0, Ni
+ Hal2
+ HHal
+ H2O, t0, H+
СnH2n
+ H2O + [O]
+ O2, t0 (горение)
- H2, t0, Ni
+ nCnH2n
CnH2n+2
дигалогеналканы, СnH2nHal2
галогеналканы, СnH2n+1Hal
CnH2n+1OH
CnH2n(OH)2
CO2 + H2O
CnH2n-2
полимер
9.
главная1.
СН2
СН2 + Н2 Pt, t
Гидрирование:
2. Галогенирование: СН2
СН2 + Br2
3. Гидрогалогенирование:СН2
4. Гидратация:СН2
СН2 + Н2О
5. Мягкое окисление:СН2
6. Горение: СН2
СН2 + НСl
t, Н3РО4
СН2
СН2
t, Ni
CН3
cat
СН
(…
СН2Вr
CН3
2Н2О
2СО2
СН3
СН2Вr
СН2 + [О] +Н2О
СН2 + 3О2
7.
СН2
Дегидрирование:
8. Полимеризация:nСН2
СН3
СН2Сl
СН2ОН
СН2
СН2
ОН
ОН
СН + Н2
СН2
СН2
…)n
10.
1. Крекинг нефтепродуктов:С16Н34
С8Н18 + С8Н16
Получение
2. Дегидрирование предельных углеводородов:
СН СН2 СН3 + Н2
СН2
СН3
СН2 СН2 СН3
СН
СН СН3 + Н2
СН3
3. Дегидратация спиртов (отщепление воды):
Н2SО4 , 140 – 1500С
СН3
СН2 ОН
СН2
СН2 + Н2О
4. Дегидрогалогенирование (отщепление
галогеноводорода):
спирт, t
СН3 СН СН СН3 +NaBr +Н2О
+
NaОН
СН
СН3
СН2 СН3
Br
5. Дегалогенирование:
СН3 СН СН СН3 +Zn
Br
Br
СН3
СН
СН
СН3 +ZnBr2
11.
ПрименениеАцетальдегид
Этанол
Бутадиен-1,3
Синтетический
каучук
Этилен
О
Уксусная кислота
Н2С
СН2
Оксид этилена
Стирол
1,2-дихлорэтан
Полистирол
Хлорвинил
Этиленгликоль
Полиэтилен
Поливинилхлорид
Антифриз
12.
Типгибридизации
Алкен
массой 4,2 г
Алкенам
Какой
тип
не
характерны
изомерии
способен
присоединить
8 г брома.
атомов
углерода
Общая
формула
алкенов
отсутствует
реакции
у алкенов
Молекулярная
формула
в пропене алкена:
Вопрос 1
Вопрос 3
Вопрос 2
Проверка
знаний
Вопрос 5
Вопрос 4
углеродного
Попробуй
Попробуй
2С
2,sp2
spCскелета
,sp
H
Н
А замещения
УРА!
6
n 6 2n+2
еще
еще
положения
Попробуй
2Попробуй
3
функциональной
Вприсоединения
УРА!
Сn10еще
Н
20
2n
еще
группы
положения
Попробуй
2
окисления
Бкратной
sp,sp,sp
CСn6H
НУРА!
12
2n-6
связи
еще
Попробуй
Попробуй
2
2,sp3
геометрическая
полимеризации
С
Н
Г spC,sp
H
УРА!
24
n 12еще
2n-2
еще
spC,sp,sp
H











 chemistry
chemistry








