Similar presentations:
Строение атома и ПСХЭ. Повторение 9 класс
1. Повторение 9 класс
ХИМИЯО.А.Лацкова
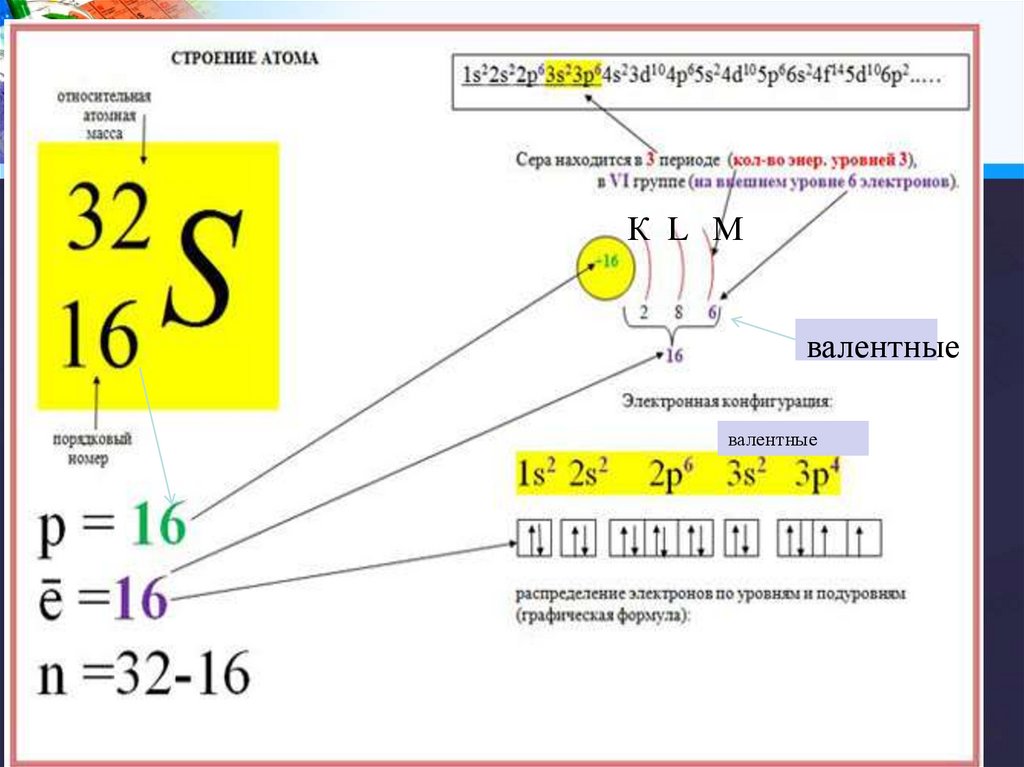
2. Т1 Строение атома и ПСХЭ
Числовое значение в ПСХЭФизический смысл
Порядковый (
атомный ) номер Z
Число протонов и
электронов в атоме ,
заряд ядра
Число энергетических
уровней
K L M N…
Номер периода
Номер группы
Число валентных
электронов
Для ГП – число е на
внешнем уровне
3. А1 Строение атома
Атомная масса Ar =2727
Al
+13
13
Z=13
• Р (е)=13
• N = 27-13=14
K
2,8,3
2+8+3=13
L
M
3 период
4.
К L Мвалентные
валентные
5.
• 4 период 6 группа главная подгруппаK L M N
• 34Se +34 2, 8, 18, 6
• 4период 7 группа побочная подгруппа
K L M N
• 25Mn +25 2, 8, 13, 2 =
(25-2-2)
2,8,?,2 элемент побочной п/г
• Порядок заполнения уровней в 4 периоде
• K L N M
6.
7.
8. №1
Ответ 1-борОтвет -2
9.
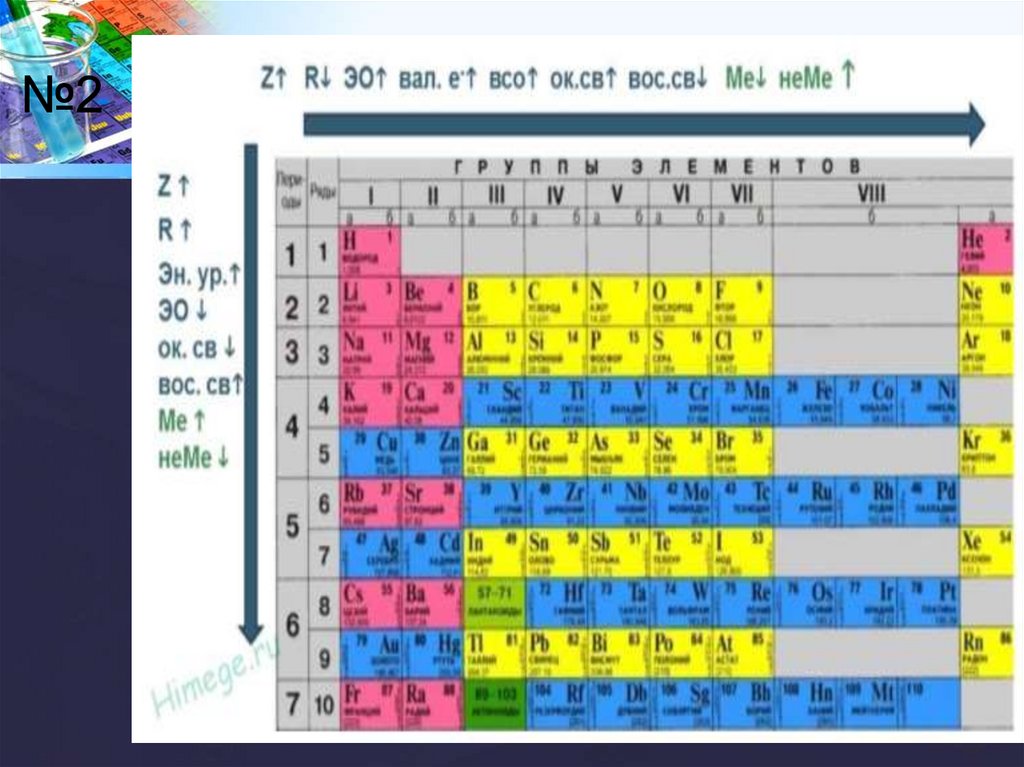
Закономерности изменения химических свойств элементов и их соединений
по периодам и группам.
Необходимо запомнить:
Физический смысл порядкового номера, номера периода и номера группы.
порядковый номер равен числу протонов и электронов, заряду ядра;
номер периода равен числу заполняемых электронных слоёв( энергетических уровней);
номер А - группы равен числу электронов на внешнем слое (валентных электронов), высшей степени
окисления( валентности)
Горизонтальная периодичность.
В периоде слева направо:
заряды атомных ядер увеличиваются;
число электронов на внешнем электронном слое увеличивается;
число электронных слоёв не изменяется;
радиус атомов уменьшается;
ЭО увеличивается;
металлические свойства уменьшаются, неметаллические свойства увеличиваются;
основные свойства соединений (оксидов, гидроксидов) уменьшаются, сменяются амфотерными,
кислотные свойства (оксидов, кислородных кислот) увеличиваются.
Вертикальная периодичность.
В А - группе сверху вниз:
заряды атомных ядер увеличиваются;
число электронов на внешнем электронном слое не изменяется;
число электронных слоёв увеличивается;
радиус атомов увеличивается;
ЭО уменьшается;
металлические свойства увеличиваются, неметаллические свойства уменьшаются;
основные свойства соединений (оксидов, гидроксидов) увеличиваются, кислотные свойства соединений
(оксидов, кислородных кислот) уменьшаются;
кислотные свойства бескислородных кислот увеличиваются.
10. №2
11.
Ответ 3Ответ 1
12.
13.
Ответ 3414.
1. Учебный тренажер содержит 20 заданий В-1 с краткимответом.
2. Задание считается выполненным верно, если
правильно указана последовательность цифр.
3. За полный правильный ответ ставится 2 балла; если
допущена одна ошибка, то ответ оценивается в 1 балл.
4. Каждое задание имеет 5 варианта ответа.
5. Необходимо выбрать два ответа, нажав при этом на
рисунок/Менделеев/ рядом с цифрой.
6. Если ответы правильные, то цифры «займут свои
места» в клеточках ответа и вы услышите аплодисменты.
15.
уменьшается радиус атомауменьшается электроотрицательность
усиливаются неметаллические свойства
увеличиваются заряды ядер атомов
уменьшается число заполненных
электронных слоев
16.
числа нейтронов в ядрах атомоввосстановительных свойств
степени окисления в высших оксидах
радиуса атома
металлических свойств
17.
уменьшаются заряды ядер атомоввозрастают кислотные свойства летучих
водородных соединений
высшая степень окисления уменьшается
уменьшается радиус атомов
усиливаются металлические свойства
18.
уменьшается валентность в высшихоксидах
возрастают радиусы атомов элементов
усиливаются неметаллические свойства
увеличивается электроотрицательность
увеличивается число электронных слоев в
атомах
19.
уменьшается число протонов в ядреуменьшается электроотрицательность
увеличивается радиус атомов
увеличивается число электронов во внешнем
электронном слое
усиливаются неметаллические свойства
20.
уменьшается радиус атомоввозрастает способность атомов отдавать
электроны
увеличиваются заряды ядер атомов
уменьшается относительная атомная масса
увеличивается степень окисления в высших
гидроксидах
21.
уменьшается электроотрицательностьуменьшаются радиусы атомов
ослабевают неметаллические свойства
увеличивается валентность в высших
оксидах
уменьшается число заполненных
электронных слоев атомов
22.
Be → Mg → CaNa → Mg → Al
Rb → K → Na
B → Be → Li
Mg → Ca → Sr
23.
уменьшается число протонов в ядреуменьшается электроотрицательность
увеличивается радиус атомов
увеличивается число электронов во внешнем
электронном слое
усиливаются неметаллические свойства
24.
усиливается электроотрицательностьусиливаются металлические свойства
усиливается основный характер их высших
оксидов
уменьшается радиус атомов
усиливается кислотный характер их высших
оксидов
25.
увеличивается число протонов в ядреувеличивается электроотрицательность
уменьшается радиус атомов
уменьшается число электронов во внешнем
электронном слое
ослабевают неметаллические свойства
26.
N→O→FС → Si → Ge
P → Si → Al
C→N→O
Br → Se → As
27.
увеличивается радиус атомаослабевают металлические свойства простых
веществ
ослабевает основный характер высших оксидов
возрастает валентность высших оксидах
увеличивается число электронных слоёв в атомах
28.
увеличиваются неметаллические свойствауменьшается радиус атома
увеличивается число электронов во внешнем
электронном слое
уменьшается низшая степень окисления
ослабевают неметаллические свойства
29.
уменьшается электроотрицательностьувеличиваются заряды ядер атомов
ослабевают неметаллические свойства
уменьшаются радиусы атомов
увеличивается число заполненных
электронных слоев атомов
30.
уменьшаются заряды ядер атомовуменьшается число электронных слоев
увеличивается атомный радиус
уменьшается низшая степень окисления
усиливаются неметаллические свойства
31.
увеличивается степень окисления в высшихоксидах
уменьшается число валентных электронов
увеличиваются заряды ядер атомов
усиливаются неметаллические свойства
уменьшается радиус атомов
32.
увеличивается число электронных слоевуменьшаются заряды ядер атомов
усиливаются неметаллические свойства
уменьшается радиус атомов
уменьшается число электронов во внешнем
электронном слое
33.
увеличивается электроотрицательностьуменьшаются заряды ядер атомов
возрастают металлические свойства
уменьшаются радиусы атомов
уменьшается число электронов во внешнем
электронном слое
34.
увеличивается электроотрицательностьуменьшаются металлические свойства
уменьшаются заряды ядер атомов
уменьшается число электронов во внешнем
электронном слое
увеличивается число заполненных
электронных слоев
































 chemistry
chemistry








