Similar presentations:
ПСХЭ и строение атома
1.
ТЕМА УРОКА: ПСХЭ и строение атома..
Учитель химии:Халько З.А
2. ТДЦ урока:
Обучающая: закрепить знания о строении атомовхимических элементов, определить закономерности
изменения свойств атомов с увеличением
порядкового номера в пределах одного периода и
главных подгрупп
Развивающая: учить сравнивать, описывать
наблюдаемые явления, делать соответствующие
выводы; продолжить формирование информационных
умений через организацию работы с различными
источниками информации
Воспитательная: формирование
коммуникативных качеств и чувства ответственности
за результат общей работы через организацию их
работы в парах; умений самоконтроля и
взаимоконтроля
3.
Средства обучения: компьютер, мультимедийный проектор,презентация к уроку, индивидуальные комплекты для
работы
Методы ведения урока:
• 1. Фронтальный;
• 2. Парный;
• 3.Индивидуальный;
Методы обучения: объяснительно-иллюстративные,
репродуктивные, частично-поисковые, проблемнообобщающие.
Приемы: беседа, анализ предмета наблюдения,
самостоятельная работа.
4.
Компетенции развиваемые на уроке.Учебно-познавательные:
• способность видеть и понимать окружающий мир,
ориентироваться в нем;
• умение задавать вопросы к наблюдаемым фактам, отыскивать
причины явлений, обозначать свое понимание или непонимание
по отношению к изучаемой теме;
Информационные:
• умение работать с разными источниками информации;
• способность следовать предложенной инструкции ;
Комуникативные:
• навыки работы в паре, способы взаимодействия с людьми;
• способность к совместной работе ради достижения цели;
• способность слушать других людей и принимать во внимание то,
что они говорят.
5. Структура урока:
Вводная часть: 10-15 минут• I. Организационный момент
• II. Актуализация знаний, полученных на предыдущих уроках темы
• III. Проблема, выход на тему урока
Основная часть: 25-30 минут
• IV. Формирование новых знаний
1. Представление программы деятельности для самостоятельной
индивидуальной и парной работы по изучению материала
2. Индивидуальная работа по вариантам
3. Обсуждение результатов работы в парах
4. Сравнение результатов с эталонными ответами, взаимооценка
5. Обсуждение результатов работы, первичное закрепление изученного
материала
Заключительная часть: 5 минут
• V. Домашнее задание
• VI. Рефлексия
6. Подготовительный этап:
1. Вынесение вопросов для повторения ксеминару:
а) Знаки химических элементов
б)Строение электронных оболочек атомов
в)Структура ПСХЭ
2. «Техническая подготовка»: подготовка
индивидуальных комплектов для работы
(оценочные листы, матрицы, программы
деятельности и пр.)
7.
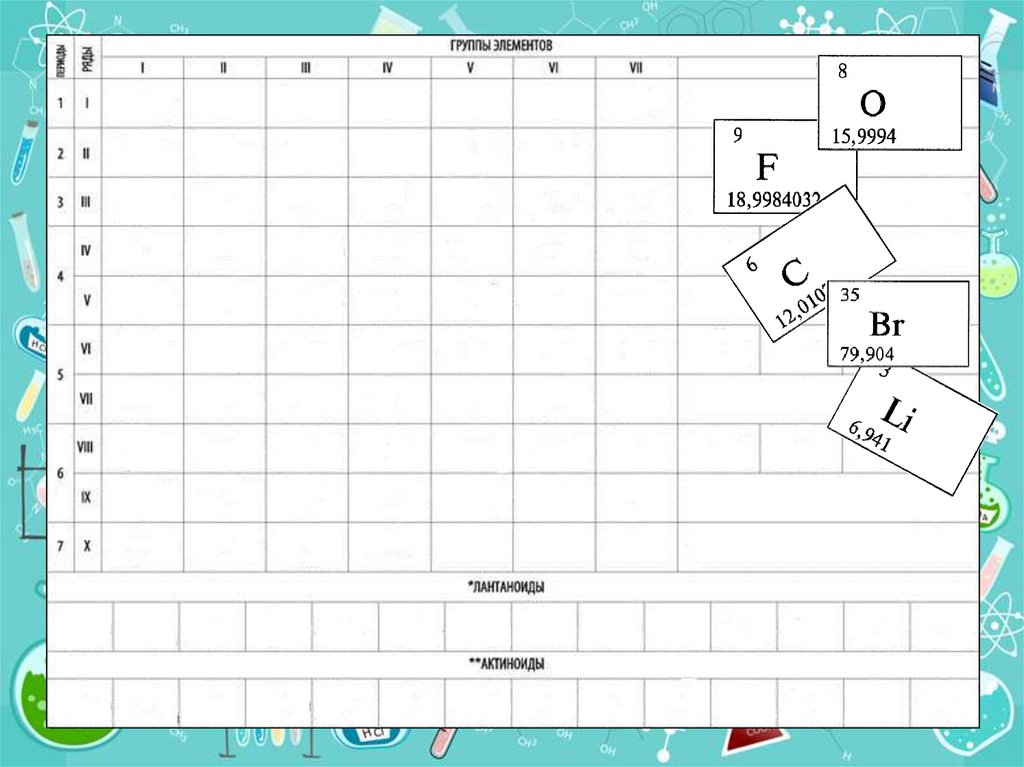
8. Определите место химического элемента в ПСХЭ, если о нем известно следующее:
• Электронная оболочка атома лития имеет2 энергетических уровня, на внешнем
расположен 1 электрон
9. Определите место химического элемента в ПСХЭ, если о нем известно следующее:
• Электронная формула атома кислородаимеет вид: 1s22s2p4
10. Определите место химического элемента в ПСХЭ, если о нем известно следующее:
• До завершения внешнего (второго отядра) энергетического уровня атому
фтора не хватает одного электрона
11. Определите место химического элемента в ПСХЭ, если о нем известно следующее:
• Схема строения электронной оболочкиатома азота выглядит так:
12. Определите место химического элемента в ПСХЭ, если о нем известно следующее:
• Бром расположен в нечетном ряду ПСХЭ.35 электронов атома брома
распределены в 4 энергетических уровня
и на внешнем два s- и пять р- электронов
13.
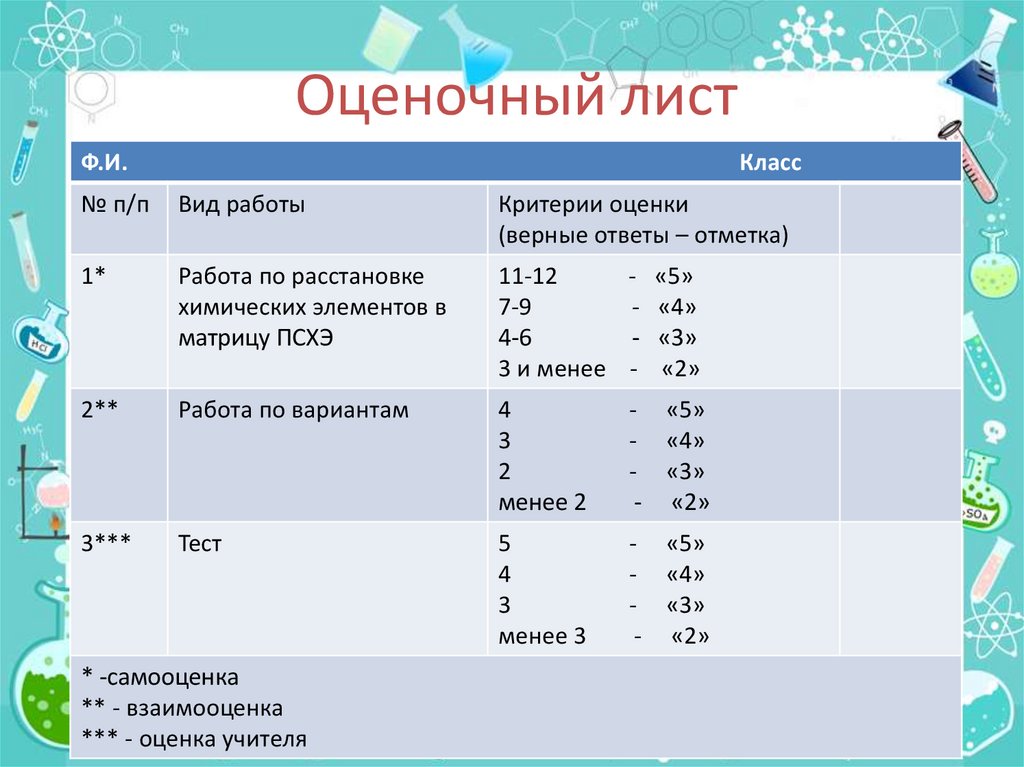
14. Оценочный лист
Ф.И.Класс
№ п/п
Вид работы
Критерии оценки
(верные ответы – отметка)
1*
Работа по расстановке
химических элементов в
матрицу ПСХЭ
11-12
- «5»
7-9
- «4»
4-6
- «3»
3 и менее - «2»
2**
Работа по вариантам
4
3
2
менее 2
- «5»
- «4»
- «3»
- «2»
3***
Тест
5
4
3
менее 3
- «5»
- «4»
- «3»
- «2»
* -самооценка
** - взаимооценка
*** - оценка учителя
15.
Проблема, выход на темуурока:
Выбран один ряд и одна
подгруппа химических
элементов. Необходимо:
-сравнить атомы элементов
одного периода и одной
подгруппы
-найти сходство и различие в
их строении
-определить закономерности
изменений, происходящих в
пределах периода и группы
16.
Программа деятельности:(в случае затруднений, обращайтесь к учителю)
• 1 вариант
• 1. Сравни строение атомов
элементов одного периода по
следующим характеристикам:
• а)заряд ядра
• б)число электронных слоев
• в)число электронов на внешнем
слое
• г)радиус атома
• 2. Расскажи о своих выводах
партнеру.
• 3. Выслушай рассказ своего соседа,
если ты считаешь иначе, скажи ему.
• 4. Сравните свои ответы с
правильными.
• 2 вариант
• 1. Сравни строение атомов
элементов одной группы по
следующим характеристикам:
• а)заряд ядра
• б)число электронных слоев
• в)число электронов на внешнем
слое
• г)радиус атома
• 2. Выслушай рассказ своего соседа,
если ты считаешь иначе, скажи ему.
• 3. Расскажи о своих выводах
партнеру.
• 4. Сравните свои ответы с
правильными.
17.
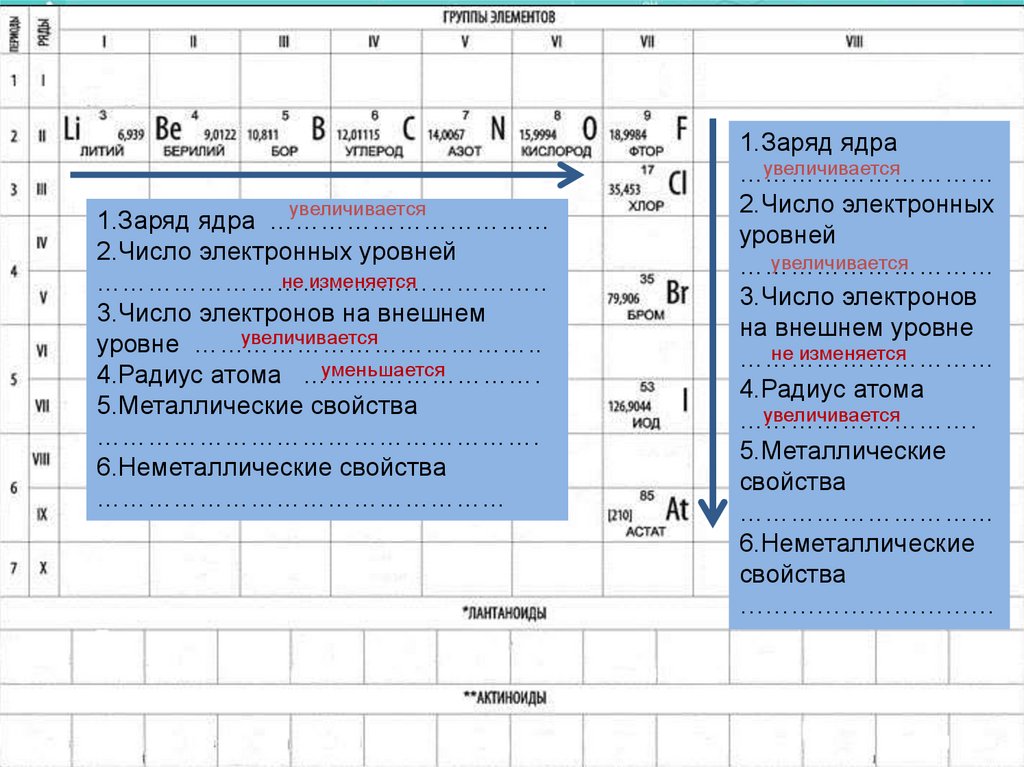
увеличивается1.Заряд ядра ……………………………
2.Число электронных уровней
не изменяется
……………………………………………..
3.Число электронов на внешнем
увеличивается
уровне …………………………………..
уменьшается
4.Радиус атома ……………………….
5.Металлические свойства
…………………………………………….
6.Неметаллические свойства
…………………………………………
1.Заряд ядра
увеличивается
…………………………
2.Число электронных
уровней
увеличивается
…………………………
3.Число электронов
на внешнем уровне
не изменяется
…………………………
4.Радиус атома
увеличивается
……………………….
5.Металлические
свойства
…………………………
6.Неметаллические
свойства
…………………………
18. Тест
• 1. Металличность элементов в пределаходного периода с увеличением
порядкового номера:
• а)увеличивается
• б)уменьшается
• в)не изменяется
19. Тест
• 2. В паре кислород-фтор больший радиусатома имеет
• а)кислород
• б)фтор
• в)радиусы атомов одинаковые
20. Тест
• 3. В ряду фтор-хлор-бромнеметалличность
• а)усиливается
• б)ослабевает
• в)не изменяется
• г)скачет
21. Тест
• 5. Среди элементов бериллий, литий,бор, углерод наиболее сильно
металлические свойства выражены у
• а)бериллия
• б)бора
• в)лития
• г)углерода
22.
Заключительнаячасть: 5 минут.
Домашнее
задание: § 10, стр.
61-63 (по таблицу)
Найди сходство
Периодической
системы с
географической
картой, попробуй
убедить в этом
сходстве
родителей.




















 chemistry
chemistry








