Similar presentations:
Нуклеиновые кислоты. (Лекция 17)
1.
ЛЕКЦИЯ 17НУКЛЕИНОВЫЕ КИСЛОТЫ
2. План
17.1. Строение нуклеиновых кислот17.2. Нуклеозиды
17.3. Нуклеотиды
17.4. Первичная структура
нуклеиновых кислот
17.5. Адениндинуклеотиды
17.6. АТФ
3.
17.1. Строение нуклеиновых кислотНуклеиновые кислоты играют
важную роль в переносе
генетической информации в
живых существах от одного
поколения к другому посредством
управления точным ходом
биосинтеза белков в клетках
4. Открытие нуклеиновых кислот
Принадлежит швейцарскому биохимику Ф.Мишеру. В 1868 году он обнаружил новое
химическое соединение в лейкоцитах, которое
назвал нуклеин. Впервые нуклеиновую кислоту,
свободную от белков получил Р. Альтман в 1876
году, который и предложил термин
нуклеиновые кислоты. Впоследствии
нуклеиновые кислоты были обнаружены во
всех растительных и животных клетках,
бактериях и вирусах
5.
Нуклеиновые кислоты – этовысокомолекулярные органические
соединения, конечными продуктами
полного гидролиза которых
являются азотистые основания
(пуриновые или пиримидиновые)
пентоза и фосфорная кислота. В
состав нуклеиновых кислот входят:
С, О, Н, Р ≈ 8-10 %, N ≈ 15-16%.
6.
Нуклеиновые кислоты –высокомолекулярные соединения,
построенные из блоков
(мономерных единиц), которыми
являются мононуклеотиды.
Принцип построения
нуклеиновых кислот был выяснен
при изучении продуктов гидролиза
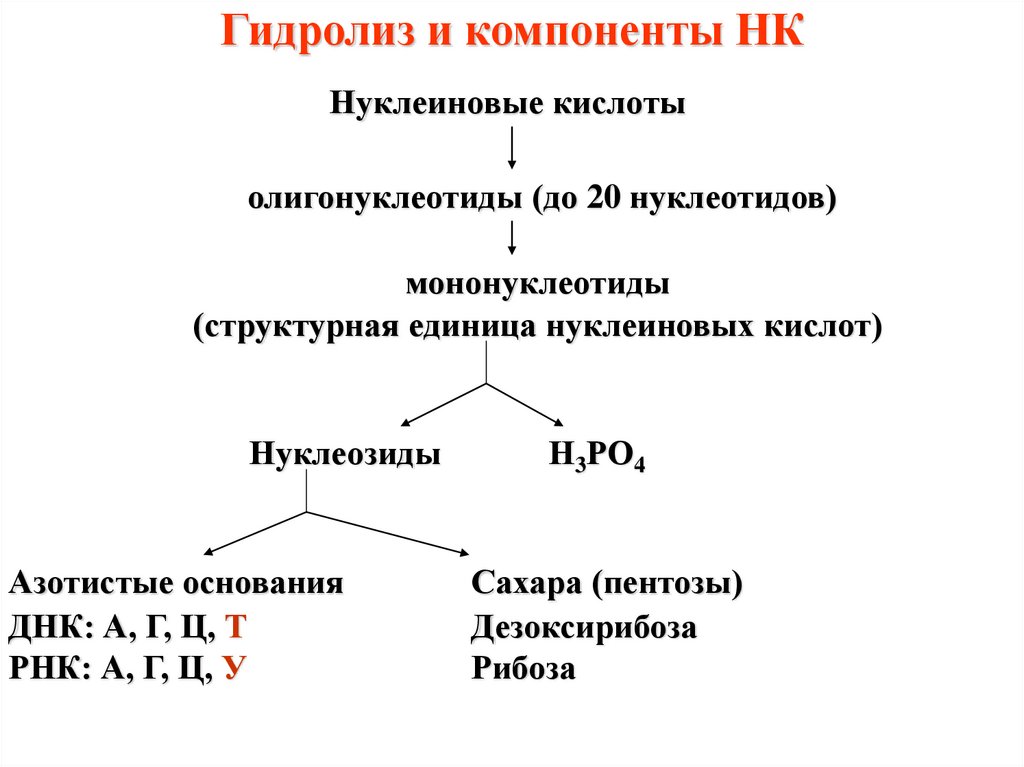
7. Гидролиз и компоненты НК
Нуклеиновые кислотыолигонуклеотиды (до 20 нуклеотидов)
мононуклеотиды
(структурная единица нуклеиновых кислот)
Нуклеозиды
Азотистые основания
ДНК: А, Г, Ц, Т
РНК: А, Г, Ц, У
Н3РО4
Сахара (пентозы)
Дезоксирибоза
Рибоза
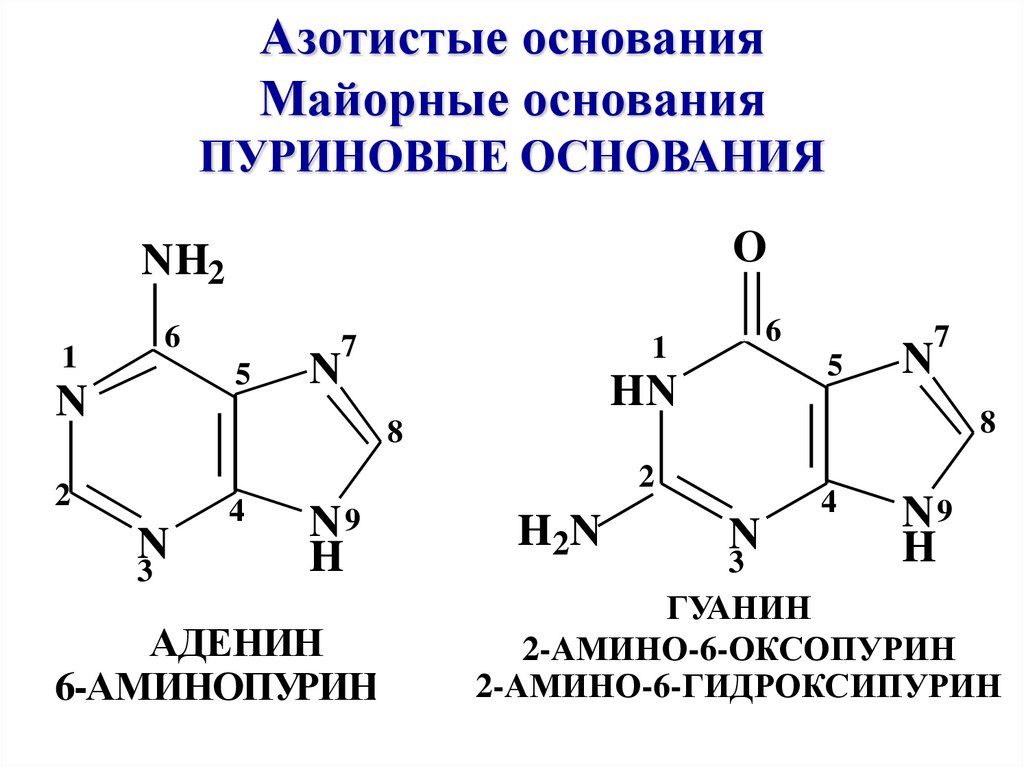
8. Азотистые основания Майорные основания ПУРИНОВЫЕ ОСНОВАНИЯ
ONH2
6
1
5
N
N
7
6
1
5
HN
N
7
8
8
2
2
N
3
4
N9
H
АДЕНИН
6-АМИНОПУРИН
H2N
N
3
4
N9
H
ГУАНИН
2-АМИНО-6-ОКСОПУРИН
2-АМИНО-6-ГИДРОКСИПУРИН
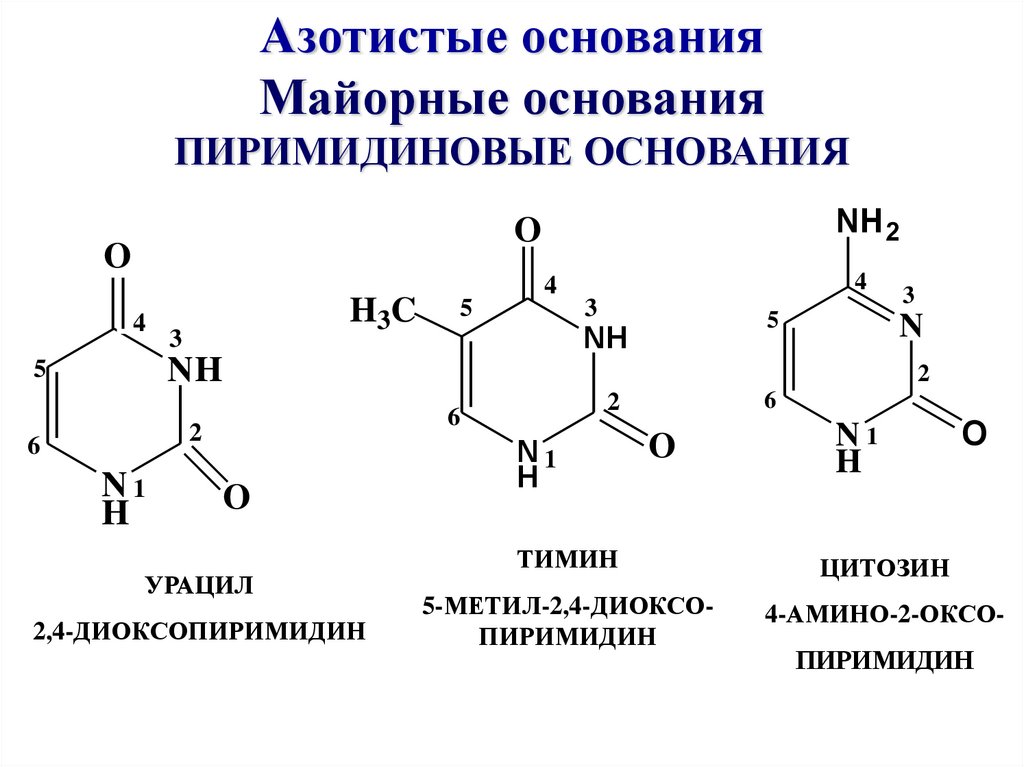
9. Азотистые основания Майорные основания ПИРИМИДИНОВЫЕ ОСНОВАНИЯ
NH 2O
O
4
H3C
3
4
4
5
3
5
NH
N
NH
5
2
N1
H
O
УРАЦИЛ
2,4-ДИОКСОПИРИМИДИН
6
2
6
2
6
3
N1
H
O
N1
H
O
ТИМИН
ЦИТОЗИН
5-МЕТИЛ-2,4-ДИОКСОПИРИМИДИН
4-АМИНО-2-ОКСО-
ПИРИМИДИН
10.
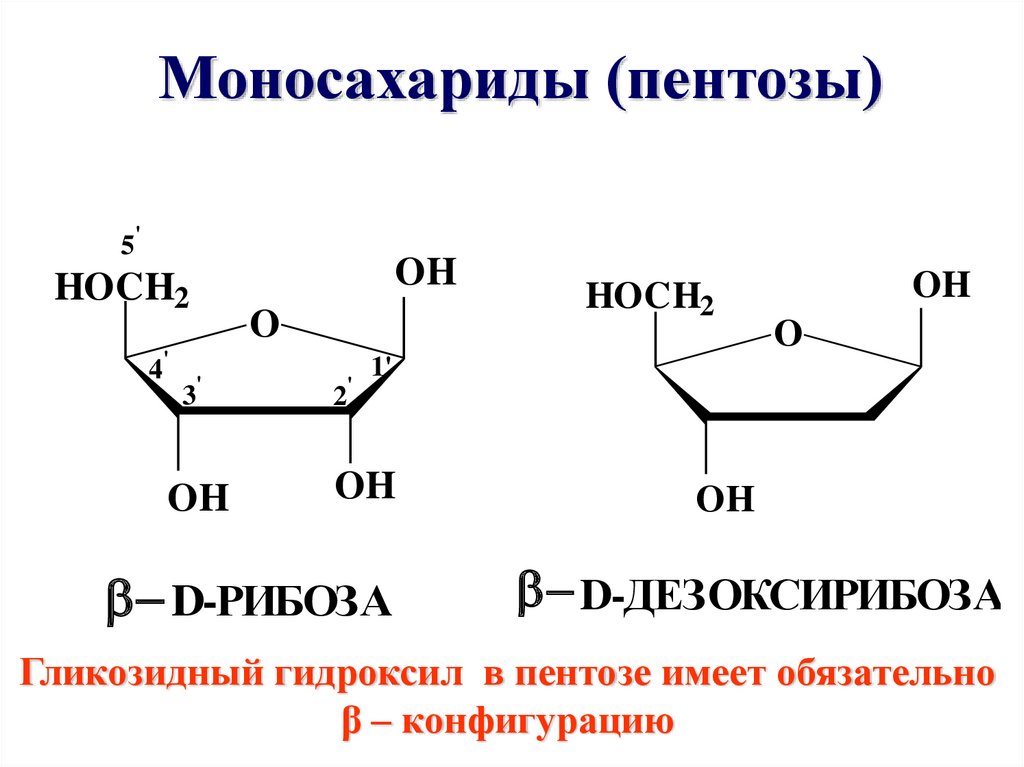
Моносахариды (пентозы)5'
OH
HOCH2
4'
3
O
'
OH
2
'
HOCH2
OH
O
1'
OH
D-РИБОЗА
OH
D-ДЕЗОКСИРИБОЗА
Гликозидный гидроксил в пентозе имеет обязательно
β – конфигурацию
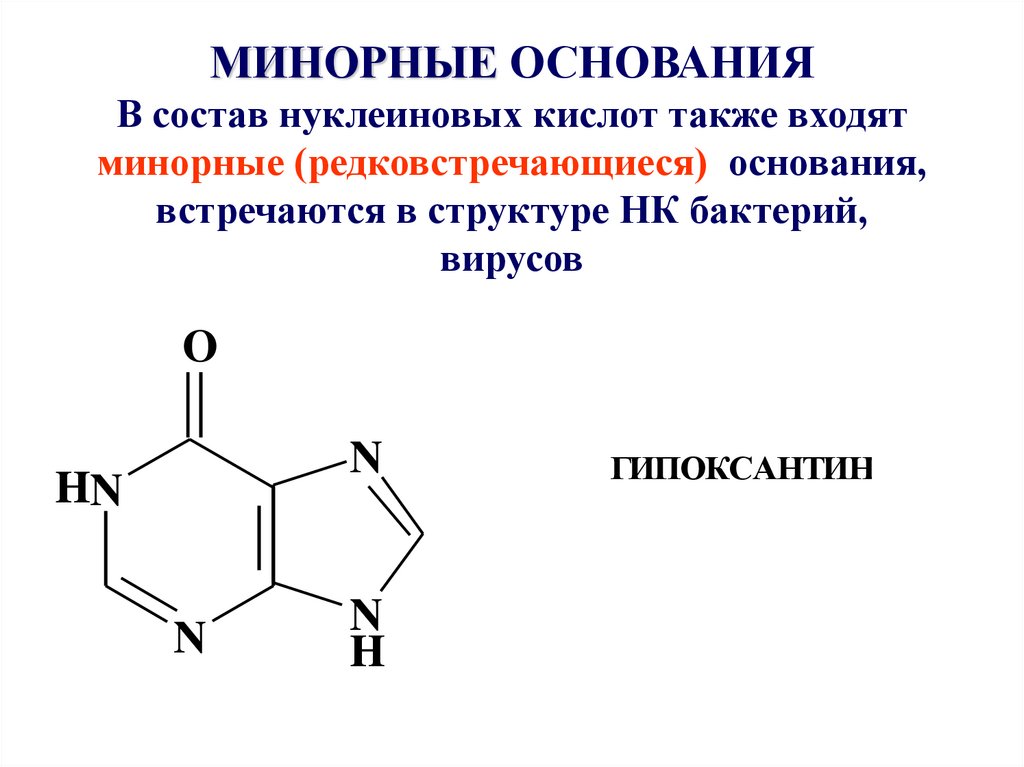
11. МИНОРНЫЕ ОСНОВАНИЯ В состав нуклеиновых кислот также входят минорные (редковстречающиеся) основания, встречаются в структуре НК
бактерий,вирусов
O
N
HN
N
N
H
ГИПОКСАНТИН
12.
OH3C
N
N
H2N
1-N-МЕТИЛГУАНИН
N
H
N
O
N
N
H
CH3
O
3-N-МЕТИЛУРАЦИЛ
13.
Пиримидиновые и пуриновыеоснования – ароматические
системы, имеют плоское строение,
в структуре НК азотистые
основания присутствуют в
энергетически более выгодной
форме (более устойчивой)
лактамной форме
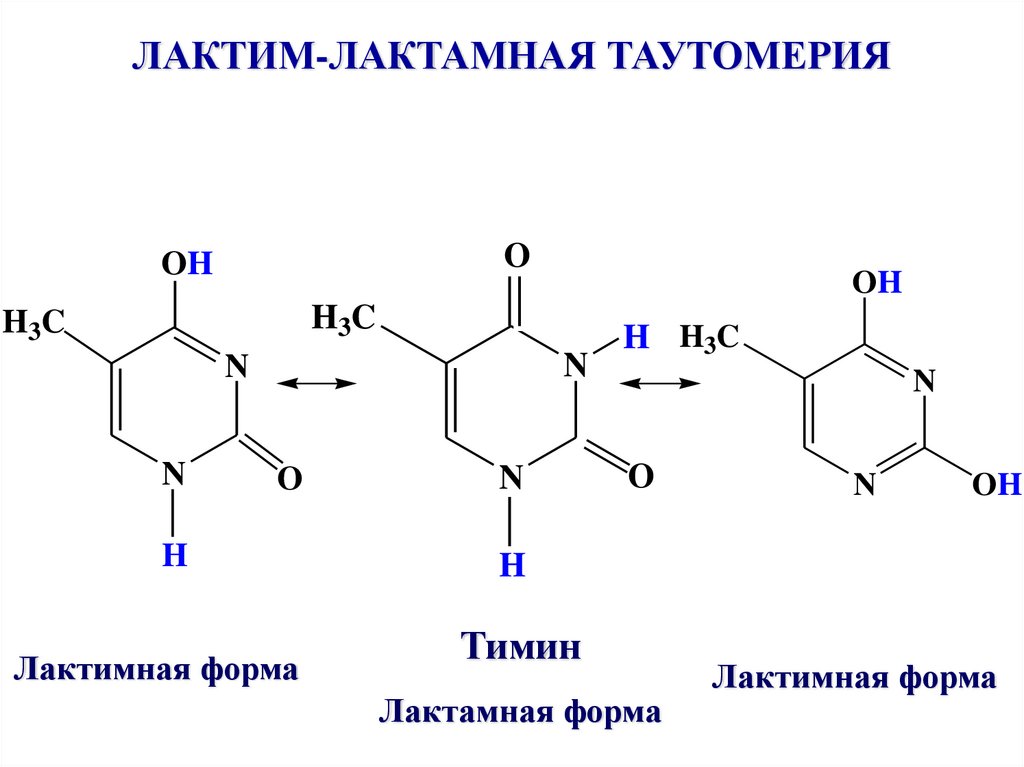
14. ЛАКТИМ-ЛАКТАМНАЯ ТАУТОМЕРИЯ
OOH
OH
H3 C
H3 C
N
N
N
O
H
Лактимная форма
N
H H3C
N
O
N
OH
H
Тимин
Лактамная форма
Лактимная форма
15. ЕНАМИНО –ИМИННАЯ ТАУТОМЕРИЯ возможна для аминопроизводных
NH 2N
N
NH
NH 2
N
N
OH
N
H
енаминные
формы
NH
O
N
H
N
O
N
H
иминные
формы
H
OH
16. ПРОТОТРОПНАЯ ТАУТОМЕРИЯ
NH2NH2
7
N
N
N
N9
H
H
N7
N
N
N9
17. При физиологических условиях нуклеиновые основания существуют только в лактамной и аминной формах
18.
Урацил, тимин и цитозин –твердые высокоплавкие
вещества, растворимые в воде,
нерастворимые в неполярных
органических растворителях.
Для них характерно наличие
прочных межмолекулярных
водородных связей
19.
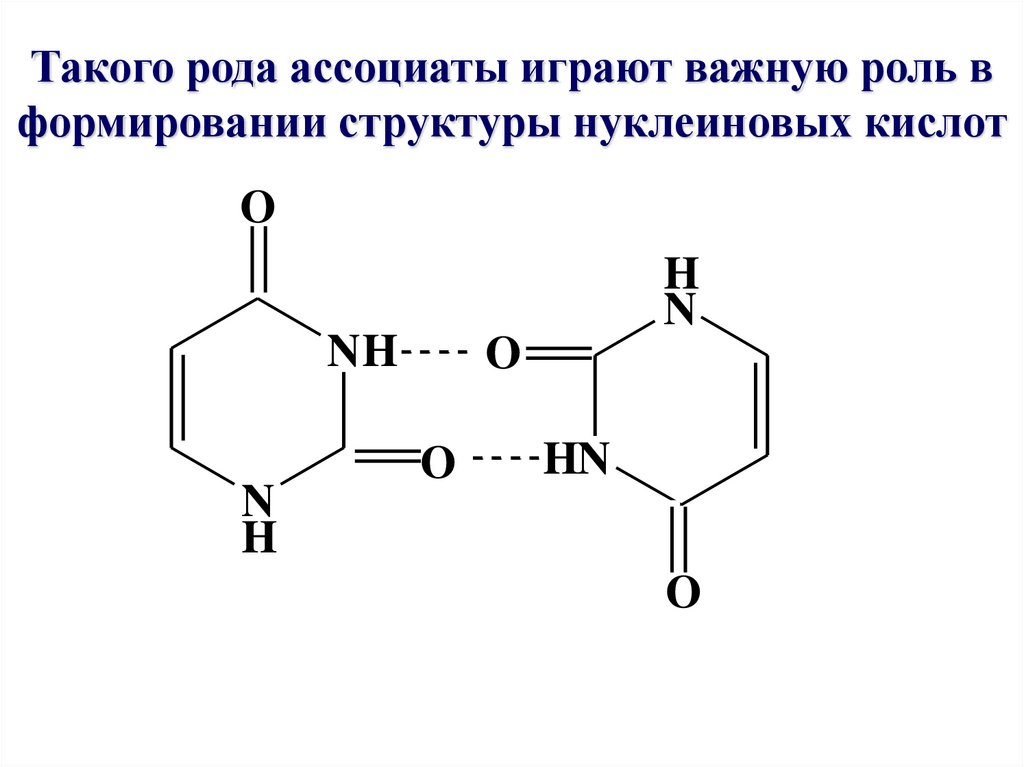
Такого рода ассоциаты играют важную роль вформировании структуры нуклеиновых кислот
O
H
N
NH
N
H
O
O
HN
O
20.
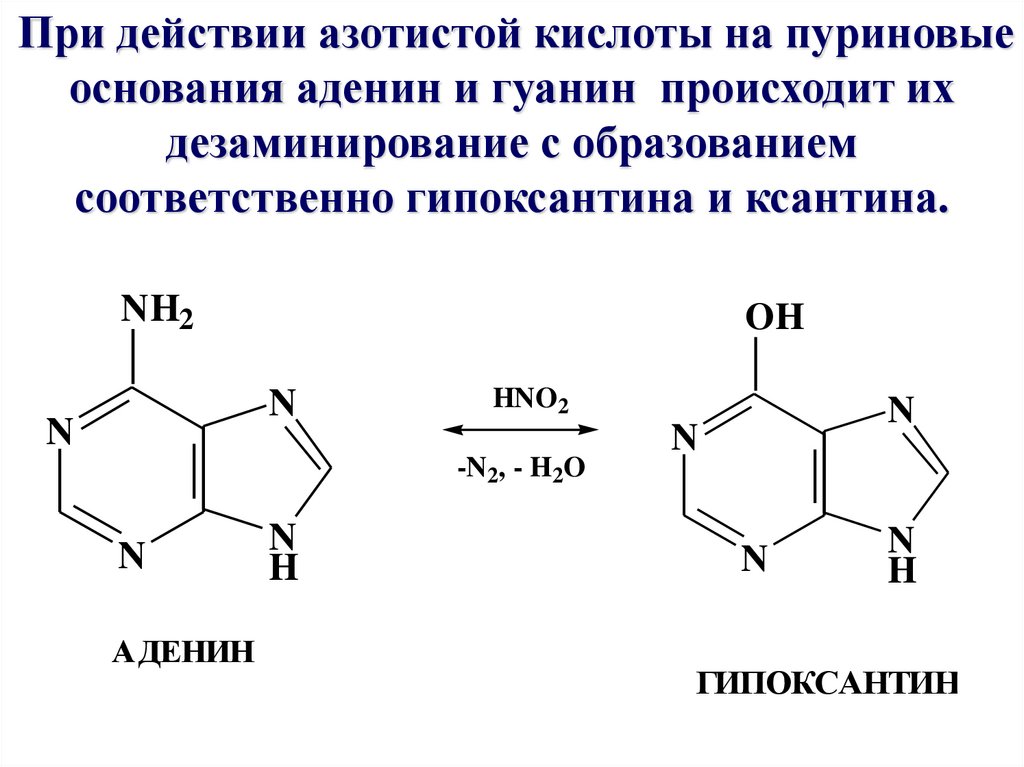
При действии азотистой кислоты на пуриновыеоснования аденин и гуанин происходит их
дезаминирование с образованием
соответственно гипоксантина и ксантина.
NH2
OH
N
N
HNO2
-N2, - H2O
N
АДЕНИН
N
H
N
N
N
N
H
ГИПОКСАНТИН
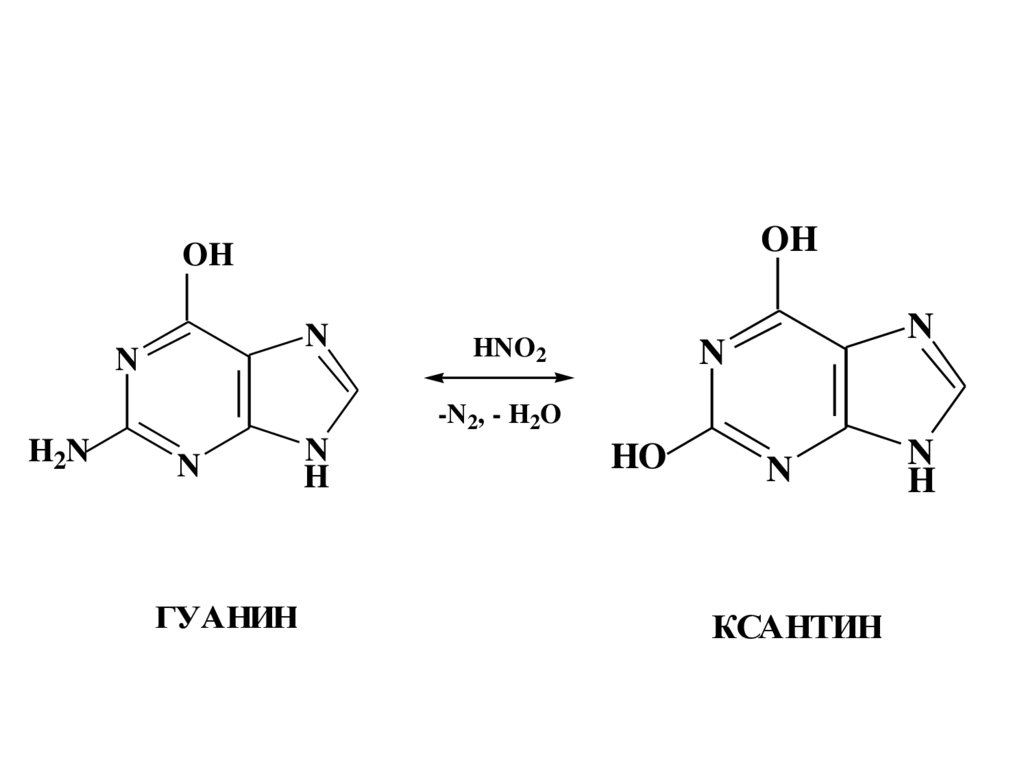
21.
OHOH
N
N
HNO2
N
N
-N2, - H2O
H2N
N
ГУАНИН
N
H
HO
N
КСАНТИН
N
H
22.
Пуриновые и пиримидиновыеоснования ДНК несут
генетическую информацию,
углеводные и фосфатные
группы выполняют
структурную роль
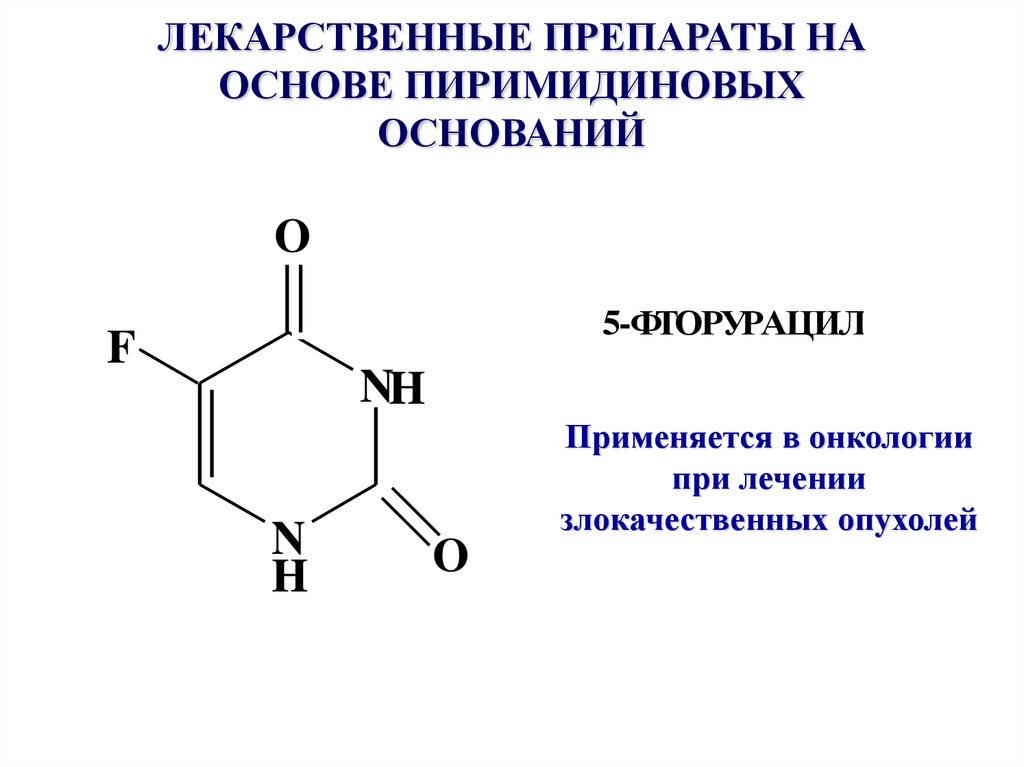
23. ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ НА ОСНОВЕ ПИРИМИДИНОВЫХ ОСНОВАНИЙ
O5-ФТОРУРАЦИЛ
F
NH
N
H
Применяется в онкологии
при лечении
злокачественных опухолей
O
24. Нуклеозиды – это азотистые аналоги О-гликозидов, т.е. N-гликозиды, образованные гетероциклическими основа-ниями и
17.2. НуклеозидыНуклеозиды – это азотистые
аналоги О-гликозидов, т.е.
N-гликозиды, образованные
гетероциклическими основаниями и полуацетальным
гидроксилом пентозы
25.
Нуклеозиды бывают двух типов –пуриновые и пиримидиновые.
У пуриновых нуклеозидов
N-гликозидная связь осуществляется между С-1’-D-рибозы или
дезоксирибозы и N-9 азотистого
основания, а у пиримидиновых –
между С-1’-D-рибозы или
дезоксирибозы и N-1 основания.
N-гликозидная связь имеет βконфигурацию
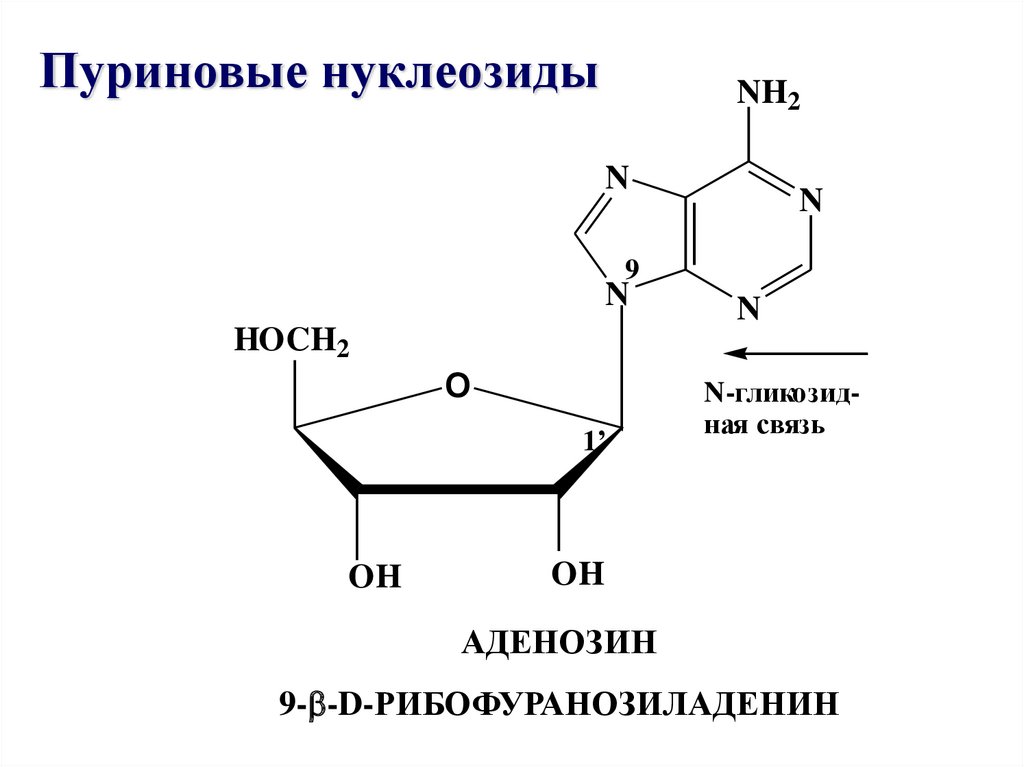
26.
Пуриновые нуклеозидыNH2
N
N
9
N
N
HOCH2
O
1’
OH
N-гликозидная связь
OH
АДЕНОЗИН
9- -D-РИБОФУРАНОЗИЛАДЕНИН
27.
Пуриновые нуклеозидыO
N
NH
9
N
N
NH2
HOCH2
O
1’
N-гликозидная связь
OH
ДЕЗОКСИГУАНОЗИН
9- -D-ДЕЗОКСИРИБОФУРАНОЗИЛГУАНИН
28.
NH2Пиримидиновые
нуклеозиды
N
1
N
O
HOCH2
O
1’
OH
N-гликозидная связь
OH
ЦИТИДИН
1- -D-РИБОФУРАНОЗИЛЦИТОЗИН
29.
Пиримидиновыенуклеозиды
O
H3C
NH
1
N
O
HOCH2
O
1’
OH
N-гликозидная связь
ТИМИДИН
1- -D-ДЕЗОКСИРИБОФУРАНОЗИЛТИМИН
30.
N-гликозидная связь стабильна поотношению к щелочам, но легко
подвергается гидролизу в кислой
среде. Пуриновые нуклеозиды легко
гидролизуются в кислой среде, а
пиримидиновые нуклеозиды
гидролизуются в более жестких
условиях (после продолжительной
обработки концентрированными
кислотами)
31.
17.3. НуклеотидыНуклеотиды –
фосфорилированные нуклеозиды по
С-2’, C-3’ и С-5’
Нуклеотиды являются сильными
кислотами. При физиологических
значениях рН (7,35) фосфатная
группа ионизирована
32.
Нуклеотиды находятся вионизированном состоянии, поэтому
их называют как сложные ионы с
окончанием ат. АМФ – аденилат,
ТМФ – тимидилат и т.д. Также
сохранились и используются старые
названия : АМФ- 5’-адениловая
кислота, ТМФ - 5’-тимидиловая
кислота. Сокращения АМФ, ТМФ
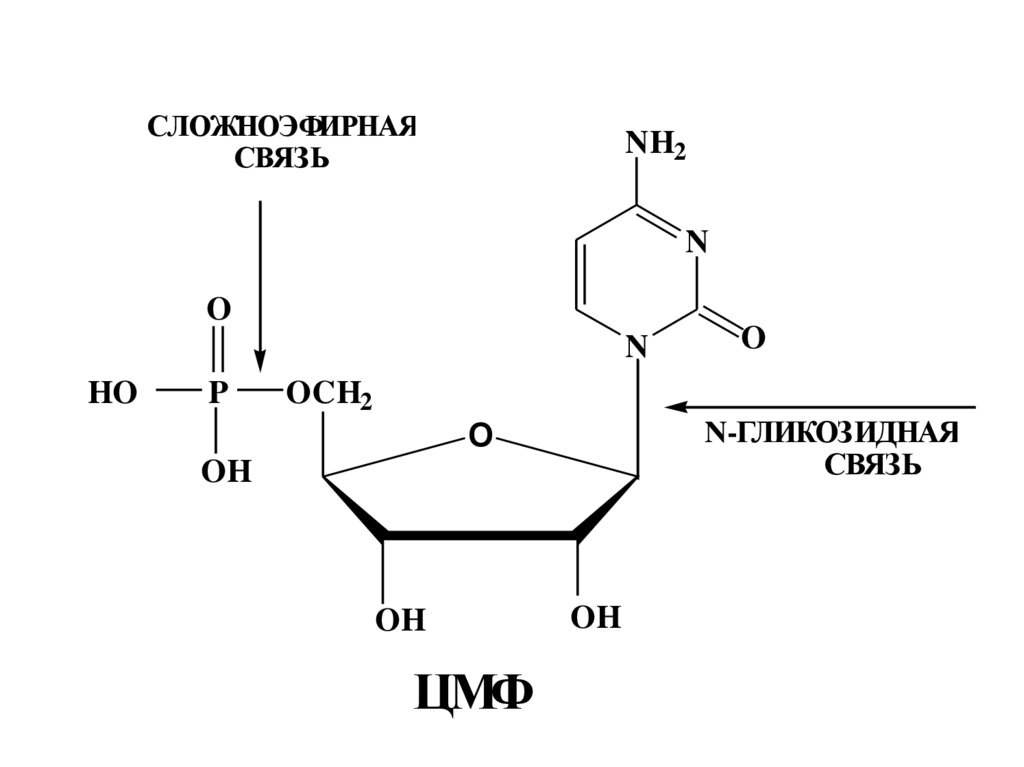
33.
NH2СЛОЖНОЭФИРНАЯ
СВЯЗЬ
N
N
O
N
HO
P
N
OCH2
O
N-ГЛИКОЗИДНАЯ
СВЯЗЬ
OH
OH
OH
АДЕНОЗИН-5 -МОНОФОСФАТ
АМФ
34.
СЛОЖНОЭФИРНАЯСВЯЗЬ
NH2
N
O
N
HO
P
O
OCH2
N-ГЛИКОЗИДНАЯ
СВЯЗЬ
O
OH
OH
ЦМФ
OH
35.
Гидролизу подвергается какN-гликозидная, так и
сложноэфирная связи, в
зависимости от этого могут
образовываться нуклеозиды или
компоненты нуклеотида –
азотистое основание, пентоза и
фосфорная кислота
36. СХЕМА ГИДРОЛИЗА
АДЕНОЗИН + Н3РО4ЩЕЛОЧНАЯ
СРЕДА
СЛАБОКИСЛАЯ
СРЕДА
АМФ
АДЕНОЗИН + Н3РО4
КИСЛАЯ СРЕДА
рН = 1
АДЕНИН + D - РИБОЗА +
Н3РО4
37.
Нуклеотиды помимо того что входятв состав НК, встречаются в клетке в
свободном состоянии.
Кроме фосфатов основных
нуклеозидов известны и фосфаты
минорных нуклеозидов, например,
5’-инозиновая кислота – монофосфат
инозита
38.
ON
NH
O
N
HO
P
OCH2
O
OH
OH
OH
5-ИНОЗИНОВАЯ КИСЛОТА
N
39.
Нуклеотиды, в которых фосфорнаякислота одновременно этерифицирует
две гидроксильные группы пентозы
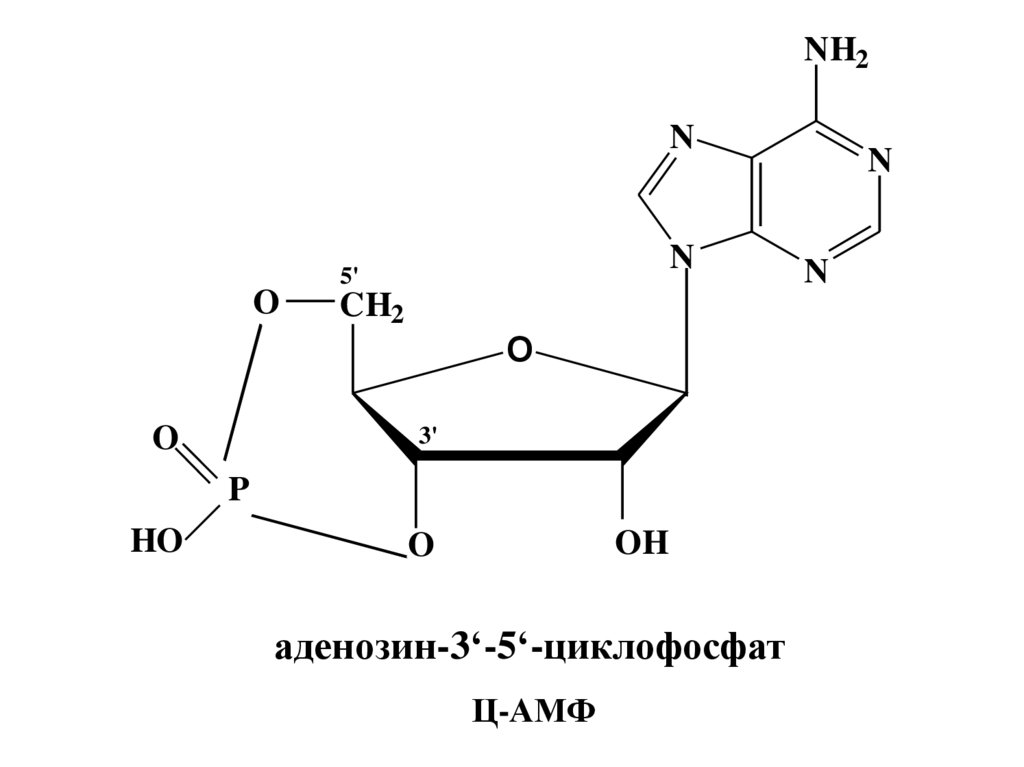
называют циклические нуклеотиды. Они
являются регуляторами внутриклеточных процессов. цАМФ относится к
вторичным посредникам, способствует
превращению инертных белков в ферменты, под действием которых происходит ряд биохимических реакций, лежащих в основе проведения нервного
импульса
40.
NH2N
N
5'
O
CH2
O
O
3'
P
HO
OH
O
аденозин-3‘-5‘-циклофосфат
Ц-АМФ
N
N
41.
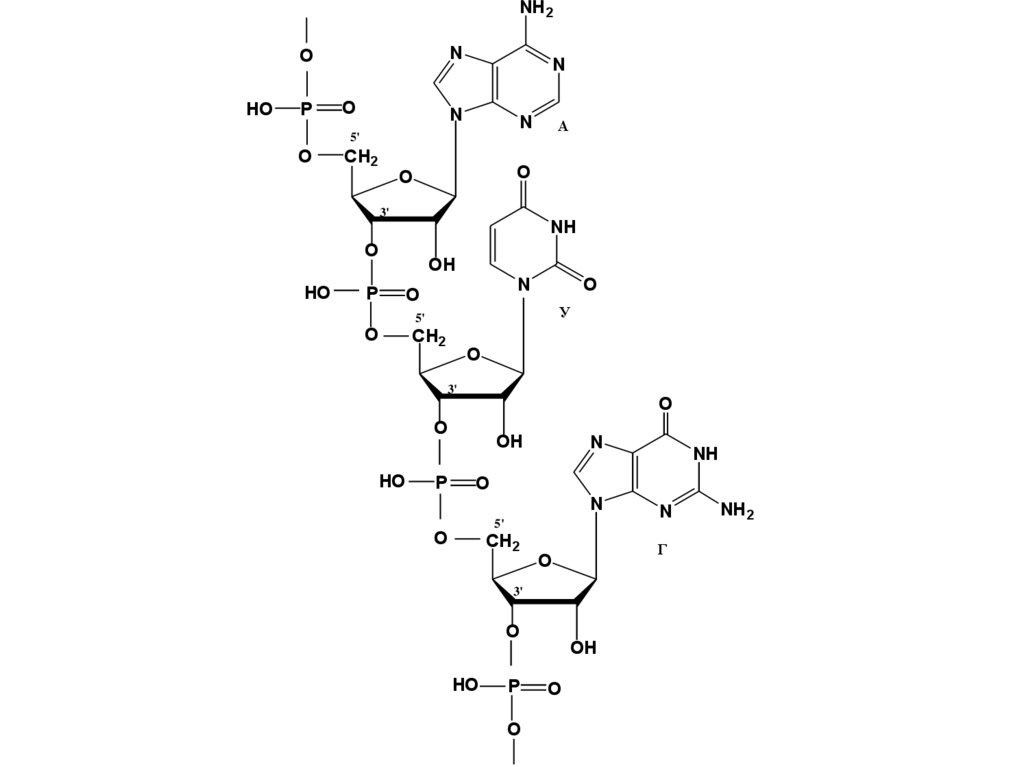
17.4. Первичная структурануклеиновых кислот
Первичная структура нуклеиновых
кислот – это последовательность
нуклеотидных звеньев, связанных
ковалентными связями в
непрерывную цепь полинуклеотида.
Мононуклеотиды соединены
фосфодиэфирной связью 3’-5’
42.
NH 2N
O
HO
P
O
N
N
N
А
5'
O
CH2
O
O
3'
NH
O
HO
OH
P
N
O
O
У
5'
O
CH2
O
3'
O
O
HO
P
OH
N
NH
O
N
5'
O
CH2
Г
O
3'
O
OH
HO
P
O
O
N
NH 2
43.
Вторичная структура ДНК – двеспиральные полинуклеотидные
цепи, закрученные вокруг общей
оси. Удерживаются две спирали
друг относительно друга
водородными связями между
пуриновыми и пиримидиновыми
основаниями противоположных
цепей
44.
Водородные связи возникаютмежду двумя парами оснований
А–Т и
Г–Ц
45.
Дополнение аденина – тимином,гуанина – цитозином называют
комплементарностью, за счет чего
обеспечивается одинаковое по всей
длине двойной спирали расстояние
между цепями и образование между
противоположными основаниями
максимального числа водородных
связей, что придает молекуле
одновременно устойчивость и
подвижность
46.
HO
H 3C
4
..................... H
N
N
7
6
5
3N
6
2
1
N
9
H ................. N
1
4
2
O
8
5
N
3
N
Цепь
Цепь
Т
A
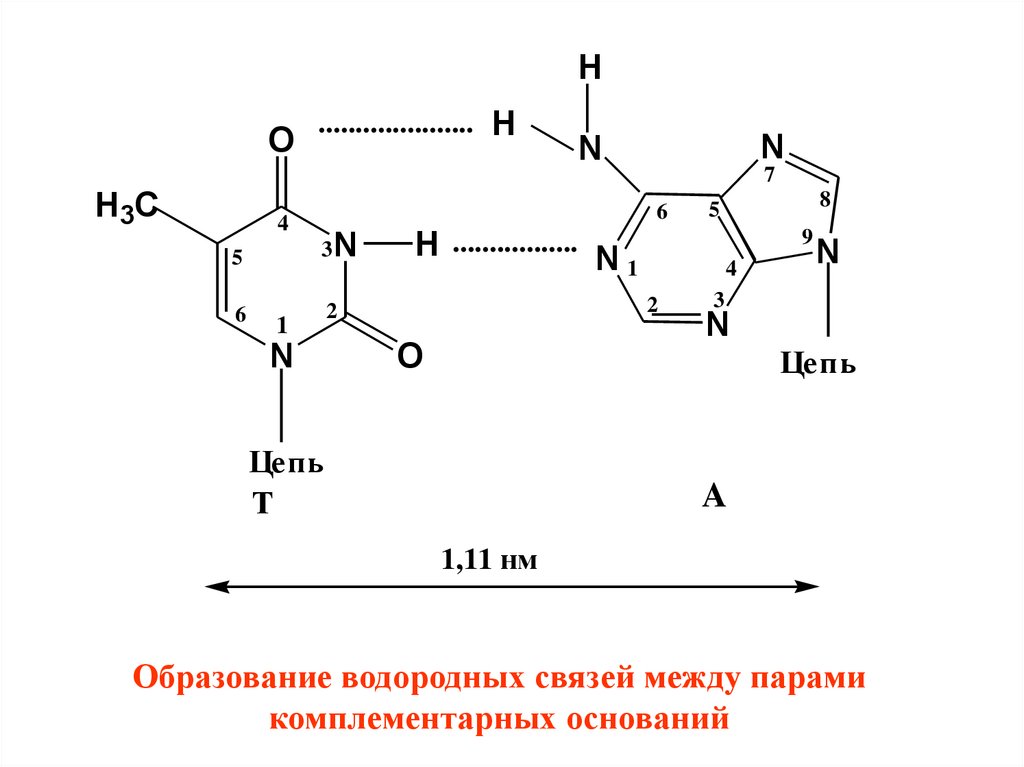
1,11 нм
Образование водородных связей между парами
комплементарных оснований
47.
HH
N
O
N
7
5
6
4
5
6
1
N
3N
H
2
O
H
9
4
N
3
2
N
N
Цепь
H
Цепь
Ц
N1
8
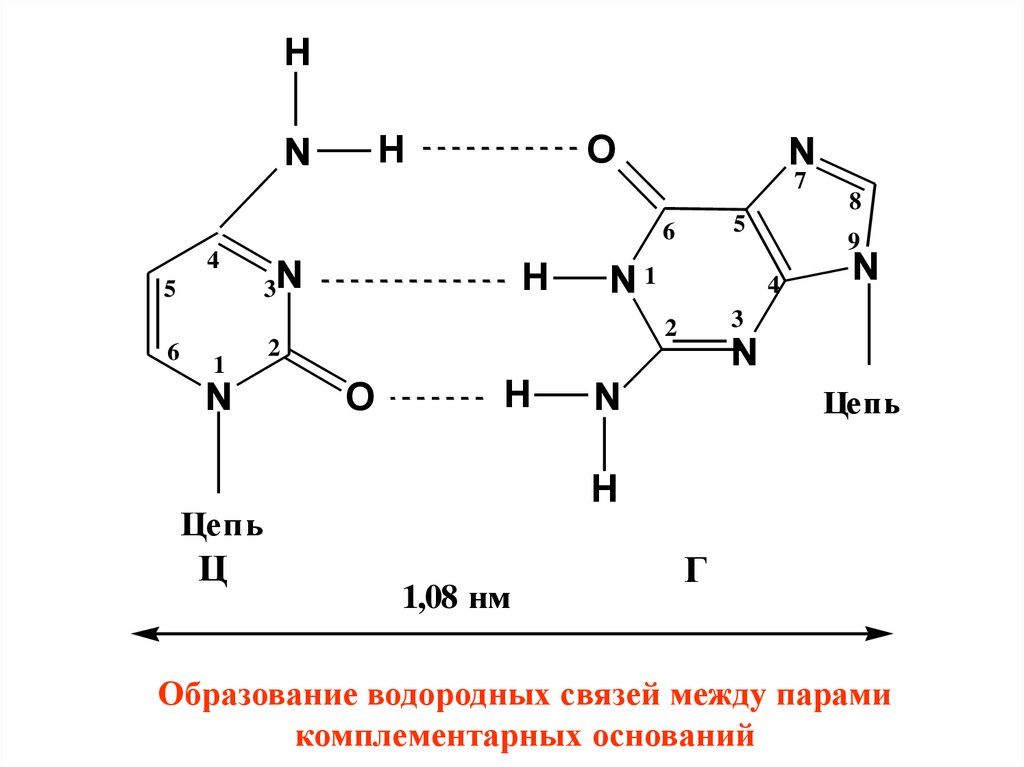
1,08 нм
Г
Образование водородных связей между парами
комплементарных оснований
48.
49.
Дж.Уотсон иФ. Крик в 1962
году стали
Нобелевскими
лауреатами в
области физиологии и медицины,
за расшифровку
структуры двойной
спирали молекулы
ДНК
50.
51.
52.
ДНК содержится в ядрах клеток, вхромосомах, незначительное ее
количество обнаружено в митохондриях.
ДНК обладает большой молекулярной
массой. В молекуле ДНК обязательно
количество молекул аденина должно
быть равно количеству молекул тимина,
а количество молекул гуанина равно
количеству молекул цитозина, т.е. сумма
пуриновых оснований равна сумме
пиримидиновых оснований
(правила Чаргафа)
53.
В молекуле ДНК зафиксированы всенаследственные свойства организма.
Важнейшей особенностью ДНК
является репликация – создание себе
подобной структуры. Репликация
заключается в том, что двойная спираль раскручивается и разделяется на
две части и на каждой из цепей молекулы ДНК синтезируется парная ей
цепь новой ДНК. В результате
создаются две новые дочерние ДНК
54.
55.
РНК повсеместно распространена вживой природе, она находится во
всех микроорганизмах,
растительных и животных клетках.
Биологическая роль РНК
обусловлена тем, что она
обеспечивает реализацию в клетке
наследственной информации,
которая передается с помощью ДНК
56.
В клетке существуют 3 главных типаРНК: матричная (информационная)
РНК (2-10%), рибосомная РНК (8090%) и транспортная РНК (15-16%).
В отличие от ДНК молекулы всех
трех типов РНК – одноцепочечные.
Содержание РНК в клетке в
пересчете на массу в 5-10- раз выше,
чем ДНК
57. 17.5. Адениндинуклеотиды
17.5. АдениндинуклеотидыАдениндинуклеотиды являются
компонентами трех коферментов
(небелковая часть фермента)
НАД+, ФАД, КоА
58.
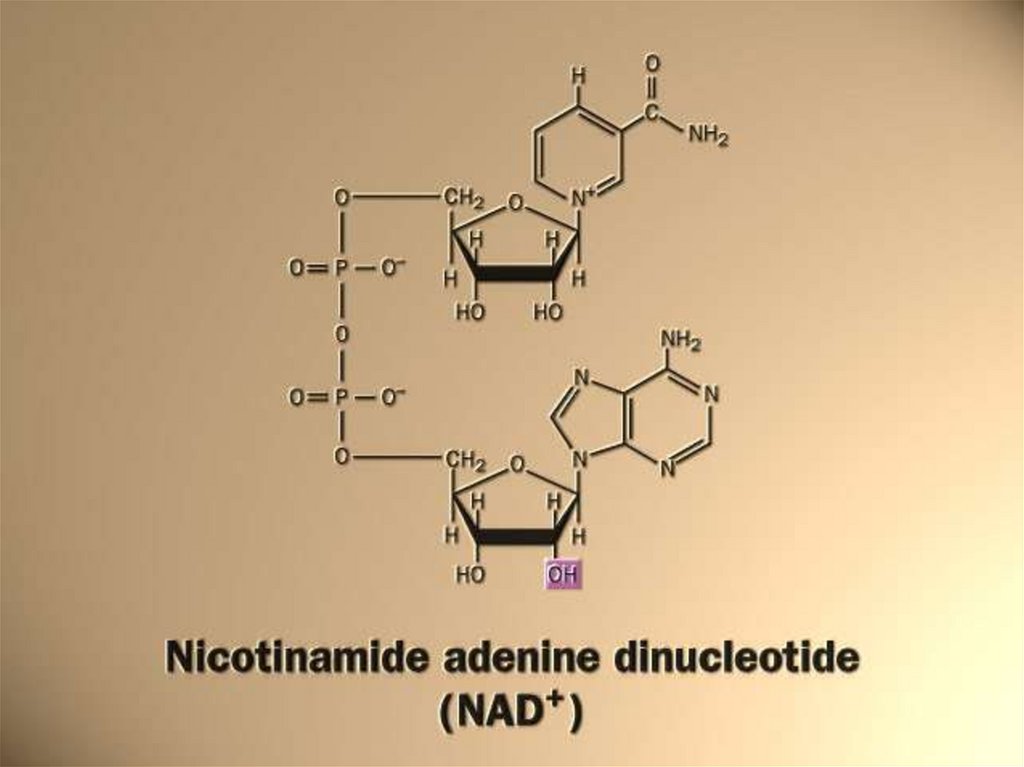
НАД+ и НАДФ+ - динуклеотиды, вкоторых мононуклеотиды связаны
между собой через остатки фосфорной
кислоты. В состав одного из
нуклеотидов входит амид
никотиновой кислоты (Витамин РР),
другой мононуклеотид представляет
собой адениловую кислоту
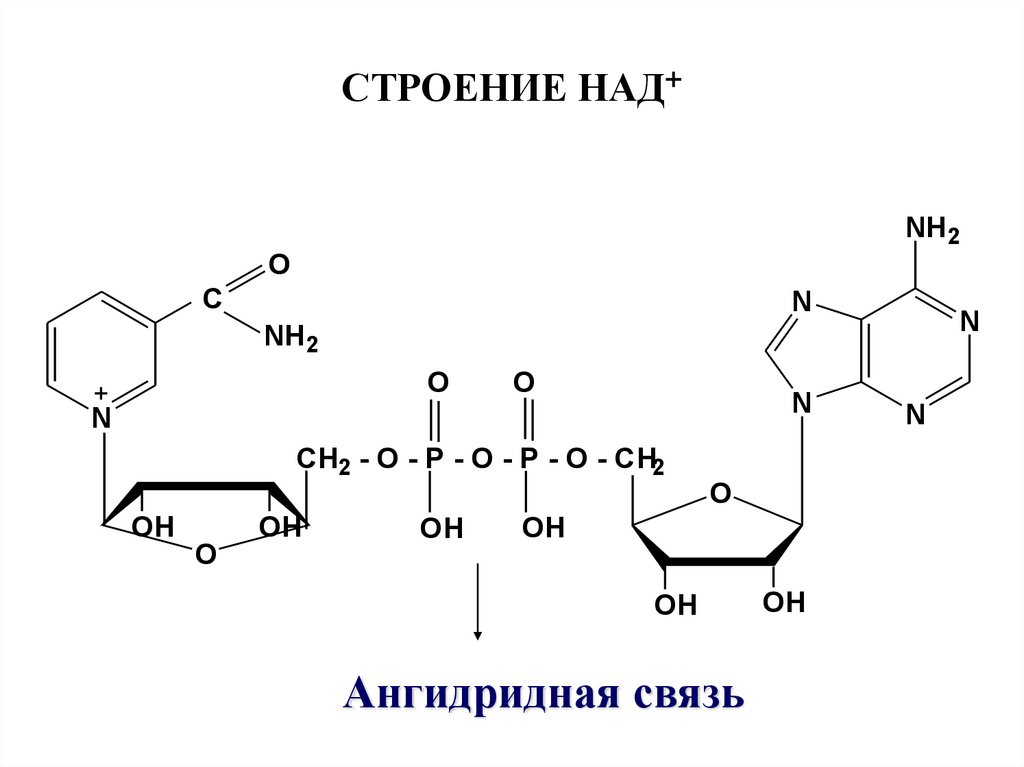
59. СТРОЕНИЕ НАД+
NH 2O
C
N
N
NH 2
O
+
O
N
N
CH2 - O - P - O - P - O - CH2
O
OH
OH
O
OH
OH
OH
Ангидридная связь
OH
N
60.
61. НАД+ и НАДФ+ участвуют в реакциях биологического окисления
HH
CONH 2
CONH 2
+
N
R
+ Н - субстрат - Н
+
+H
N
R
+
субстрат
окисленный
62.
γ- положение никотинамидногофрагмента акцептирует гидрид ион
(Н‾). В результате присоединения Н‾
происходит восстановление НАД+ и
его пиридиновое кольцо переходит в
1,4-дигидропиридиновый фрагмент
63.
Схема окисления молочной кислоты до ПВКпод действием фермента лактатдегидрогеназа
H
CONH2
CONH2
+
+
H
ЛДГ
CH3-CH-COOH
N
N
OH
R
НАД+
+ H+ + CH3-C-COOH
O
R
НАД Н
64.
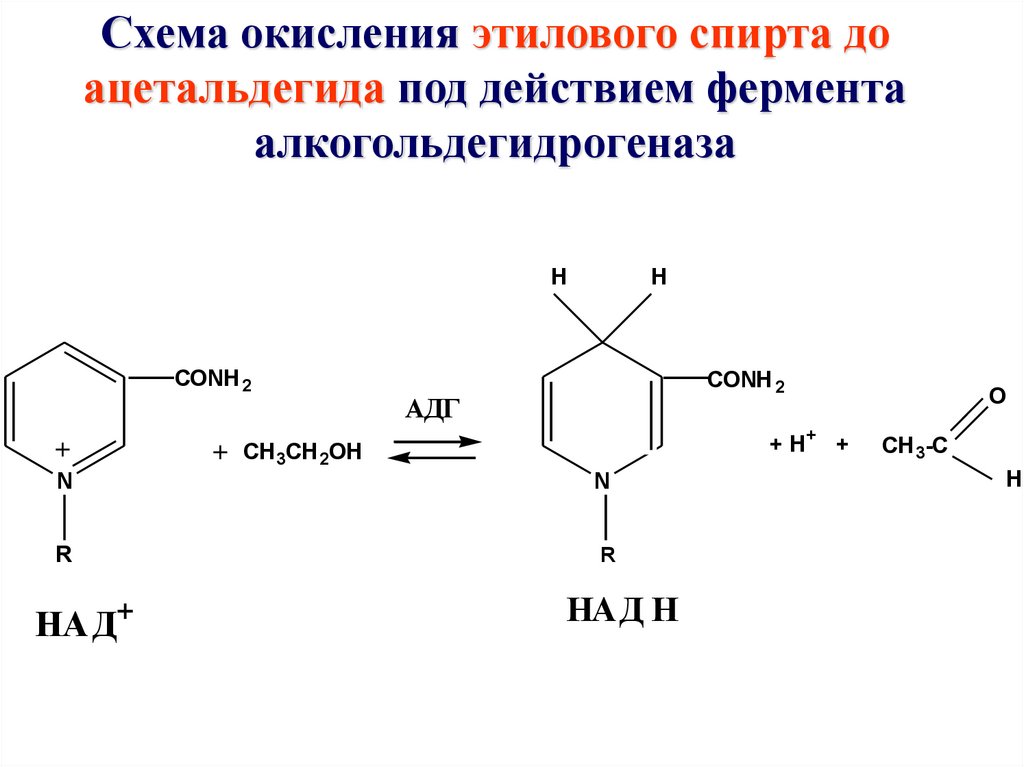
Схема окисления этилового спирта доацетальдегида под действием фермента
алкогольдегидрогеназа
H
CONH 2
+
H
CONH 2
АДГ
+ H+ +
+ CH 3CH2OH
N
N
R
R
НАД+
НАД Н
O
CH 3-C
H
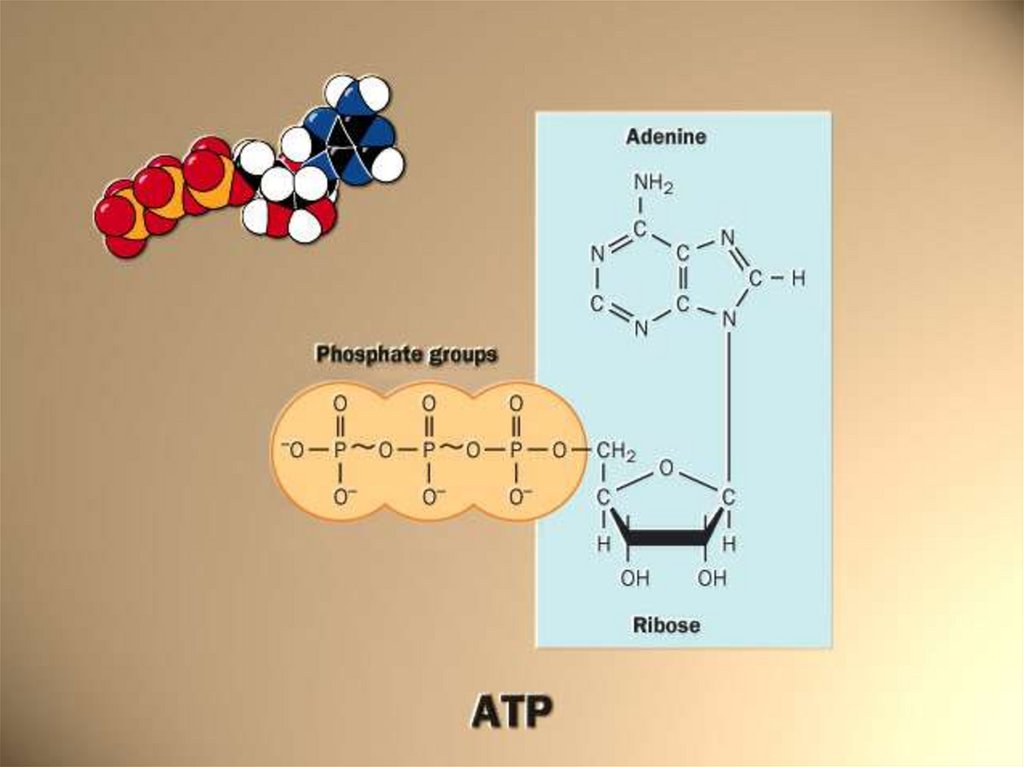
65. 17.6. Аденозинтрифосфорная кислота
АТФ выполняет роль аккумулятора(накопителя) и передатчика энергии
в клетке, обеспечивает синтез
донора метильных групп S – аденозилметионина из АТФ и
метионина, участвует в переносе
фосфатных групп
66.
АТФ содержит богатые энергиейангидридные макроэргические связи
O
O
- P - O ~ P OH
OH
При расщеплении этой связи выделяется
энергия ≈ 32 кДж/моль
67.
Процессы, связанные срасходованием энергии,
сопровождаются расщеплением
АТФ до АДФ и Н3РО4, а затем до
АМФ. Наоборот в процессах
распада питательных веществ часть
освобождающейся энергии
расходуется на образование АТФ из
АДФ и АМФ
68.
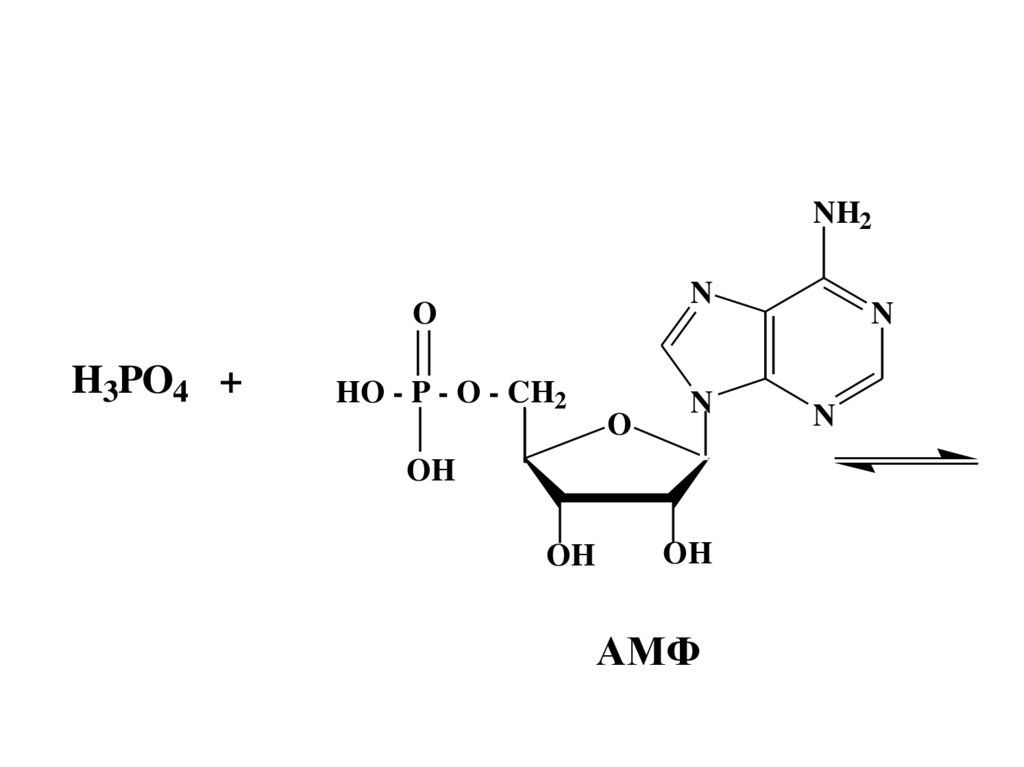
NH2N
O
H3PO4 +
HO - P - O - CH2
O
N
OH
OH
OH
АМФ
N
N
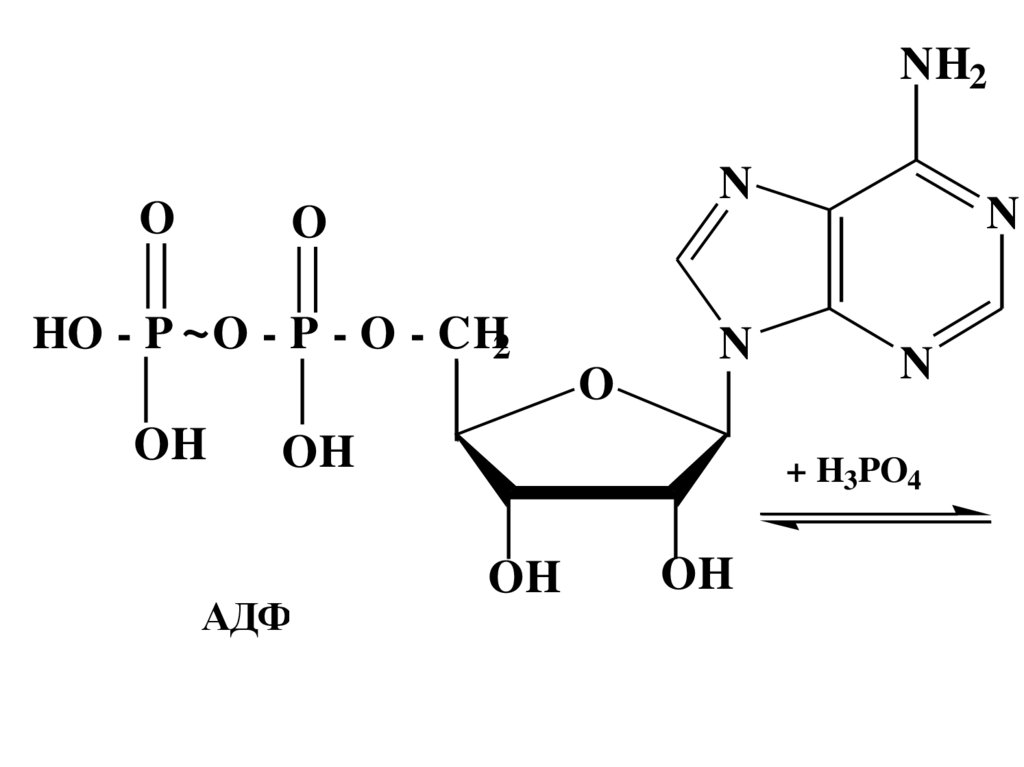
69.
NH2O
N
O
HO - P ~ O - P - O - CH2
O
OH
N
OH
АДФ
N
N
+ H3PO4
OH
OH
70.
OO
O
HO - P ~O - P ~ O - P - O - CH2
OH
OH
АТФ
O
A
OH
OH
OH
71.
72.
Нуклеозидная часть молекулы важнадля узнавания и связывания с
различными ферментами
При физиологических значениях рН
АТФ находится в ионизированном
состоянии и в клетке связывается с
Mg2+, Са2+. АТФ способна переносить
потенциальную энергию на множество
важных биологических соединений
73.
С участием АТФосуществляется активный
транспорт ионов через
биологические мембраны,
активирование аминокислот
перед их связыванием
74. Схема реакции взаимодействия АТФ с аминокислотами (SN)
OO
A
O
HO - P - O - P - O - P - O - CH2
O
OH
OH
OH
+
OH
АТФ
OH
HOOC - CH - CH3
NH2
АЛАНИН
75.
OO
A
H3C - CH - C - O - P - O - CH2
NH2
O
OH
OH
АЛАНИЛАДЕНИЛАТ
+
H4P2O7
OH
ДИФОСФОРНАЯ
КИСЛОТА
76.
Благодаримза внимание !






















































 biology
biology








