Similar presentations:
Синтез индолов по Неницеску
1. Работу выполнил студент 4 курса факультета химии и высоких технологий Прокопенко Иван
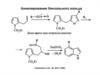
Синтез индолов по Неницеску2. Синтез Неницески
служит исключительнодля получения 5-гидроксииндолов,
некоторые из которых проявляют
биологическую активность.Реакция
представляет собой сопряженное
присоединение винилогов первичных или
вторичных амидов к бензохинону с
последующей циклизацией
3. Реакция Неницески
COR3O
R3CO
O
HO
R2
O
R2
NHR1
O
COR3
R2
NR1
NR1
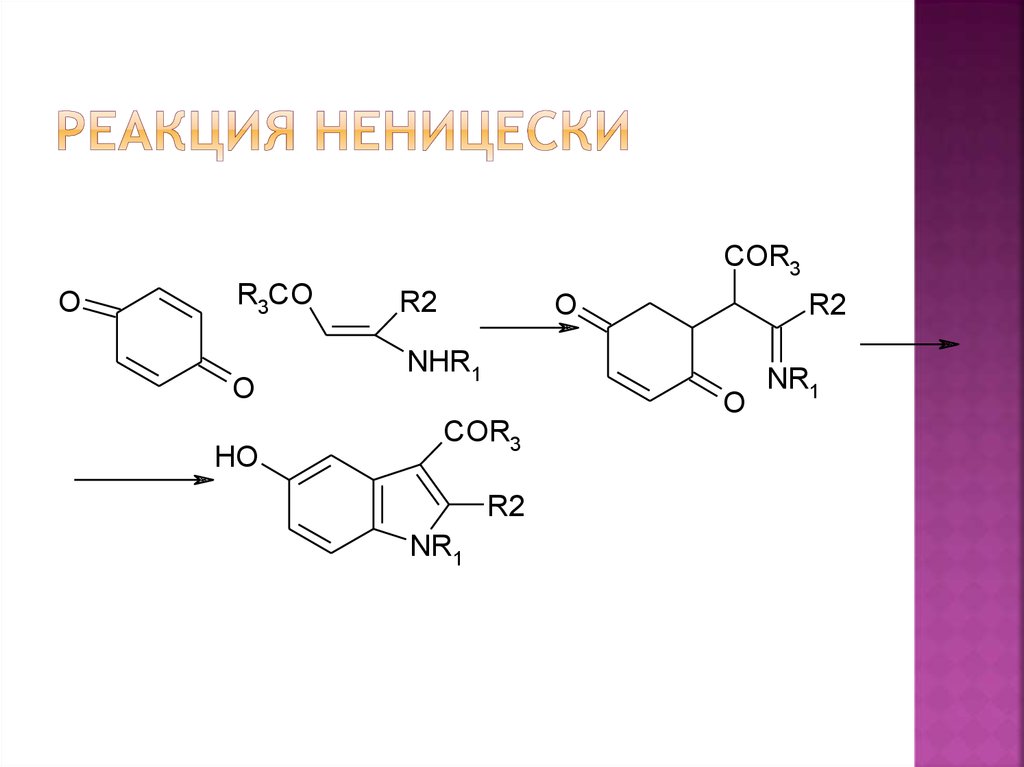
4. Производные 5-гидроксииндолов,проявляющие биологическую активность
Средиродственных природных индолов можно назвать
триптамин (66),серотонин (67) и N,N-диметиламины 6870,каждый из которых обладает галлюценогенным
действием.
R1 NH
2
R2
H
N
H
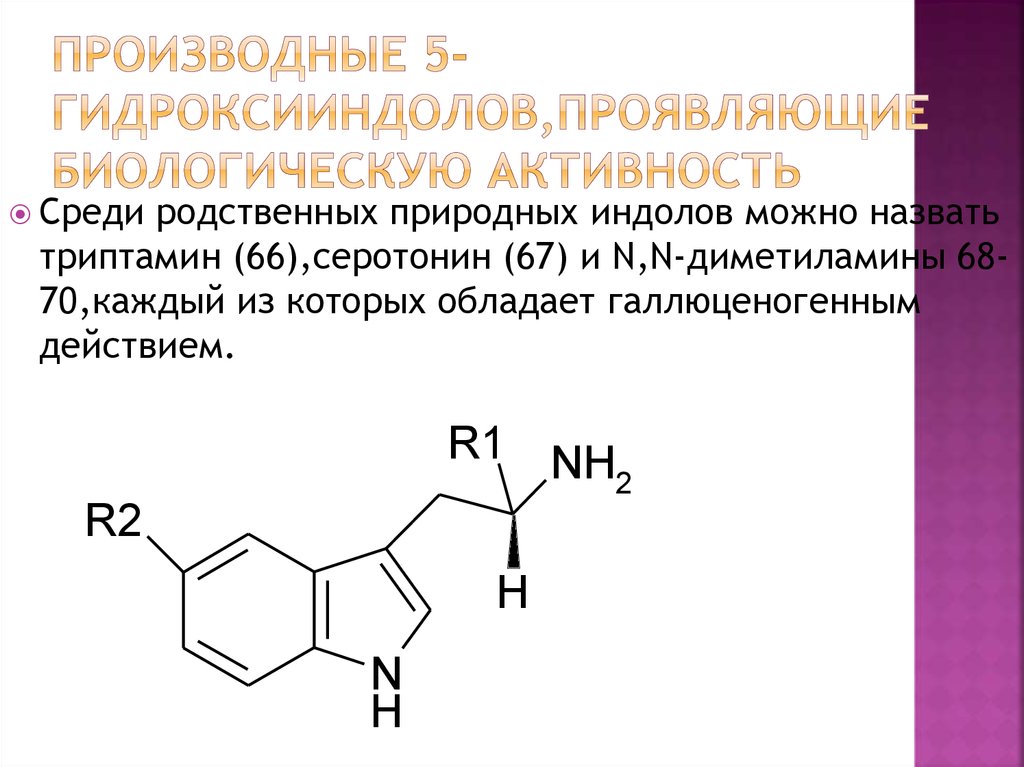
5. Производные 5-гидроксииндолов,проявляющие биологическую активность
65;66;
67;
68;
R1=CO2H,R2=H
R1=R2=H
R1
NMe2
R2
R1 =H,R2 =OH
69;
R1=H,R2=OH
70;
R1=OH,R2=H
R1=H,R2=OMe
N
H
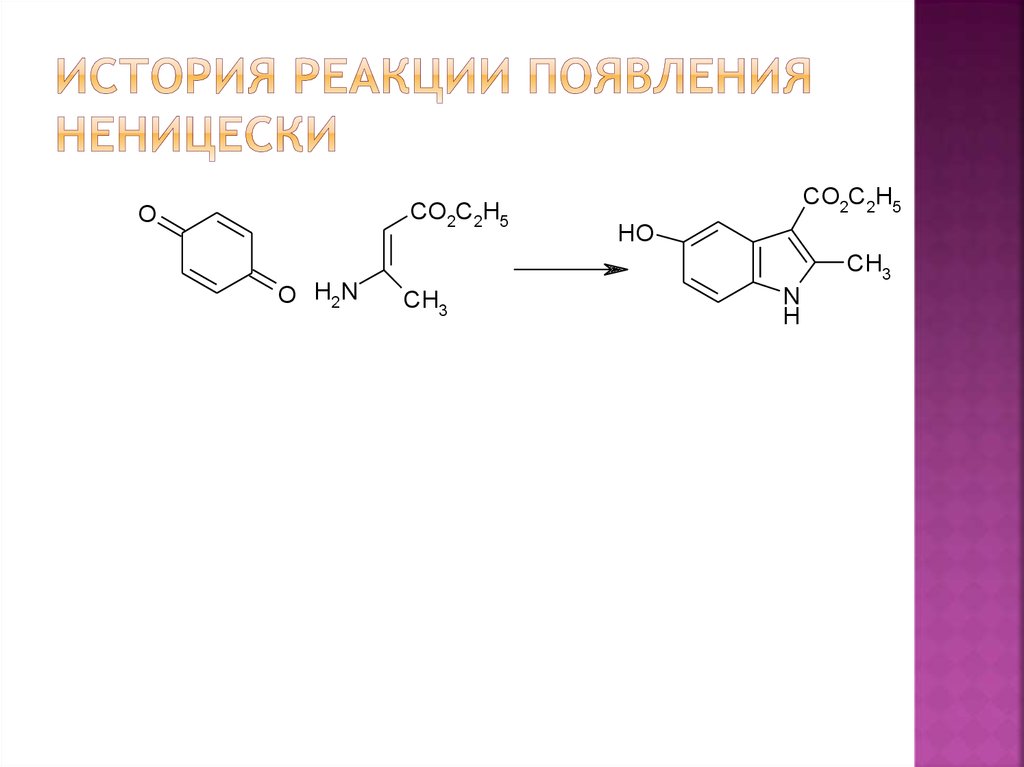
6. История реакции появления Неницески
В1929г. К. Неницески впервые обнаружил,
что при взаимодействии п-бензохинона с
этиловым эфиром3-аминокротоновой
кислоты в кипящем
ацетоне образуется этиловый эфир5гидрокси-2-метилиндол-3-карбоновой
кислоты[73].
7. История реакции появления Неницески
CO2C2H5O
O H2N
CO2C2H5
HO
CH3
CH3
N
H
8. История реакции появления Неницески
Этареакция была незаслуженно забыта
до1950-х гг., когда интерес
к химии меланина, серотонина и
родственных производных 5-гидроксииндола стимулировал исследование
разнообразных способов синтеза соединений этого класса. Публикация этого
подробного обзора[74] хорошо отра-жает
возросший интерес исследователей к
реакции Неницески.
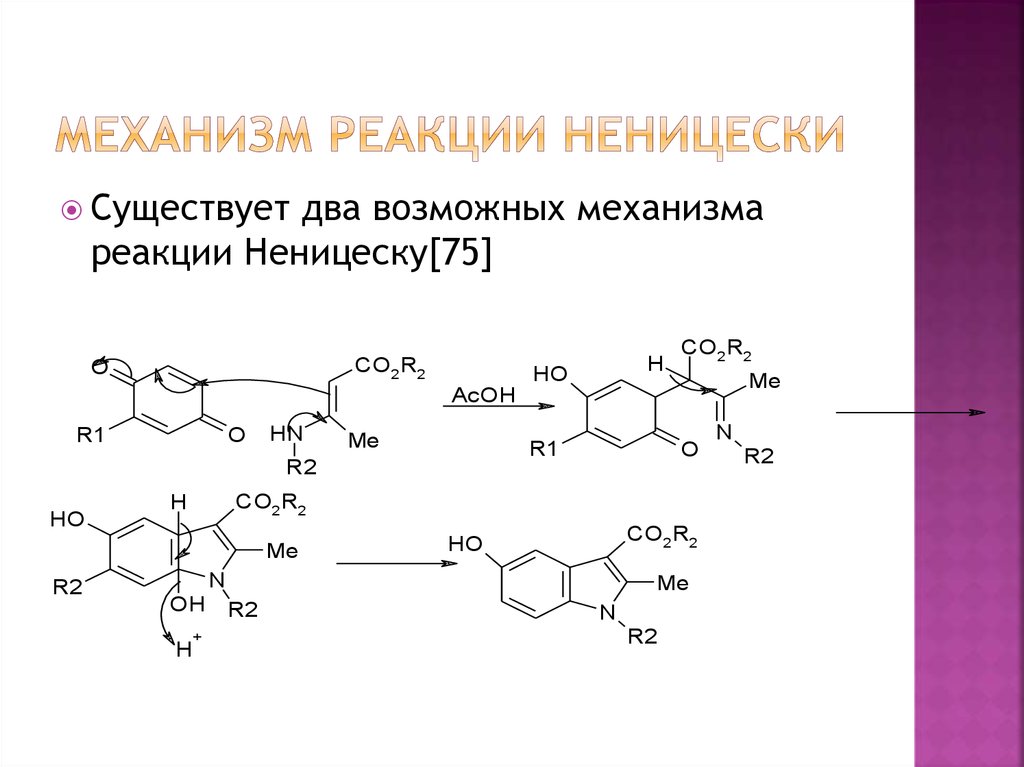
9. Механизм реакции Неницески
Существуетдва возможных механизма
реакции Неницеску[75]
CO2R2
O
H
HO
CO2R2
Me
AcOH
R1
O
HN
Me
R1
R2
HO
CO2R2
H
Me
R2
O
CO2R2
HO
N
OH
+
H
Me
R2
N
R2
N
R2
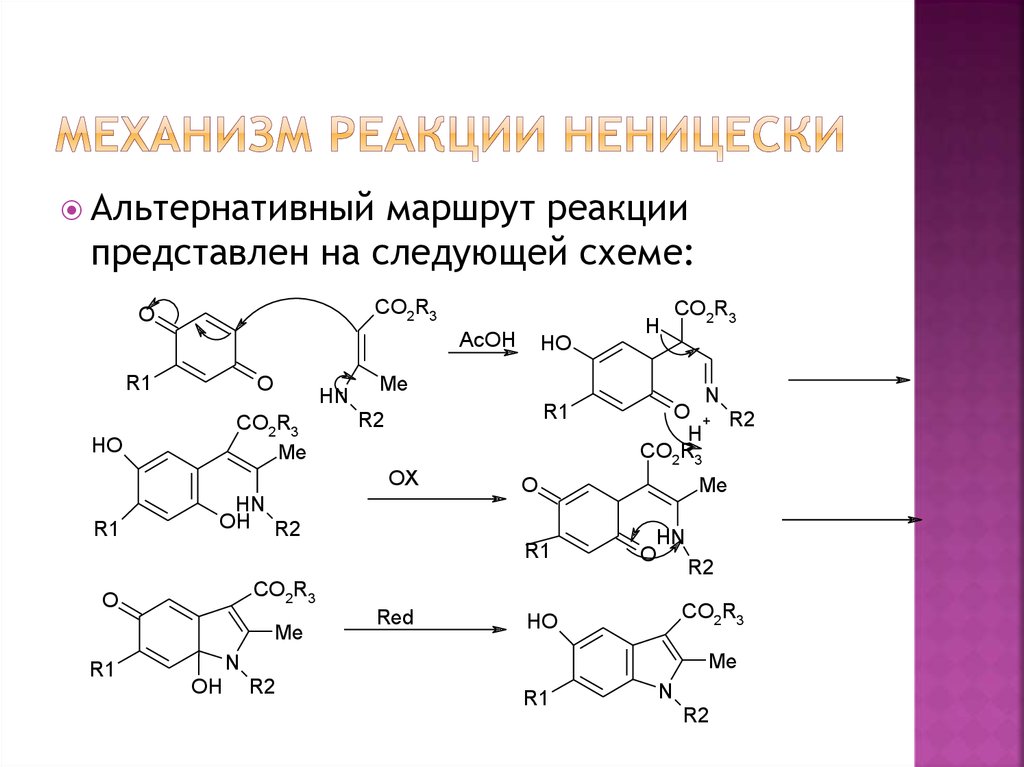
10. Механизм реакции Неницески
Альтернативныймаршрут реакции
представлен на следующей схеме:
CO2R3
O
AcOH
R1
O
HN
CO2R3
Me
HO
Me
R1
R2
OX
R1
HO
HN
OH R2
N
O + R2
H
CO2R3
Me
HN
O
CO2R3
O
Me
Red
R2
CO2R3
HO
Me
N
OH
CO2R3
O
R1
R1
H
R2
R1
N
R2
11. Реакции Неницески
Где Ox- окислитель, Red- восстановительМежмолекулярный процесс окисления–
восстановления, по-видимому,
включает в себя бимолекулярный комплекс с
переносом заряда[76].
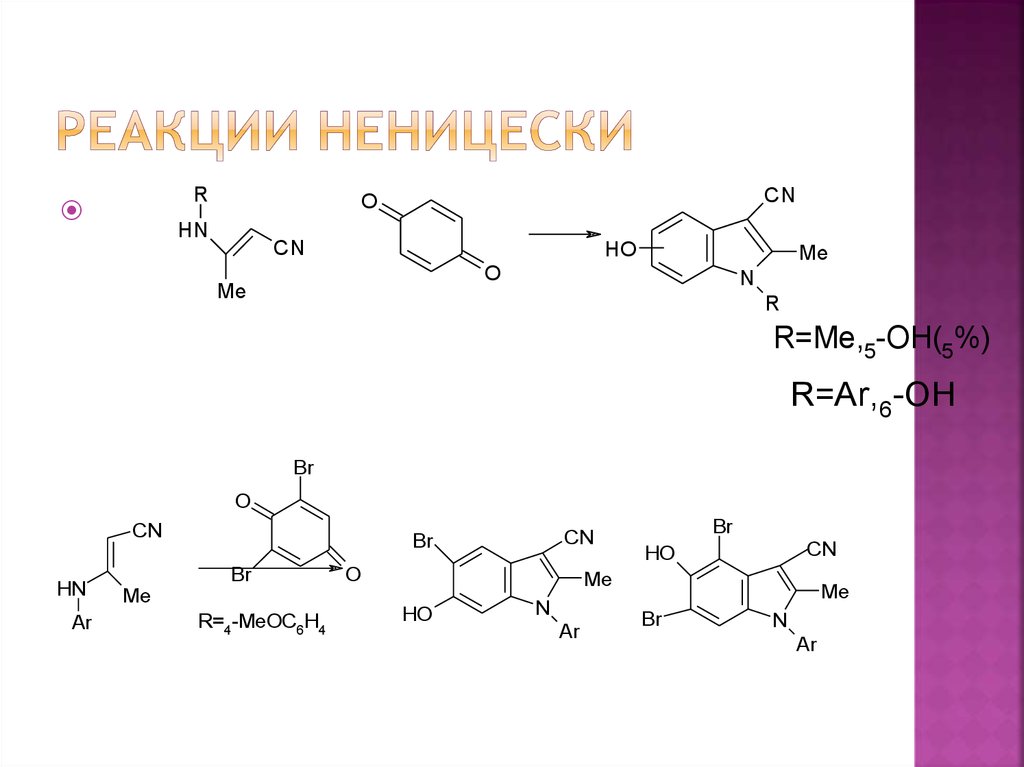
Направление реакции Неницески в значительной
степени зависит от
строения енамина и гораздо меньше от
структуры кетона[74]. Так, на
примере2,6-дибромхинона было показано[77], что
при переходе от N-метилк N-арил-β-цианоенаминам направление реакции
меняется: в первом случае
преимущественно образуются5-гидроксииндолы,
во втором– 6-гидрокси-производные.
12. Реакции Неницески
По мере роста электроноакцепторности βзаместителя в исход-ном енаминеувеличивается склонность к образованию6гидроксиизомеров.
В случае β-нитроенаминов это
направление становится доминирующим
не только для N-арил-, но и для Nметиленаминов.
13. Реакции Неницески
RCN
O
HN
CN
HO
Me
O
Me
N
R
R=Me,5-OH(5%)
R=Ar,6-OH
Br
O
CN
HN
Ar
CN
Br
Br
Me
R=4-MeOC6H4
O
Br
CN
HO
Me
HO
N
Ar
Me
Br
N
Ar
14. Реакции Неницели
Замена N-метильного заместителя на арильныйпрежде всего сказывается
на снижении электронной плотности в βположении енамина. Это в свою
очередь приводит к уменьшению скорости
присоединения енамина к хинону,
причём менее электронодефицитное положение2
более чувствительно
к такому снижению скорости, чем атом углерода
карбонильной группы. По-скольку первый тип
присоединения ответственен за образование5гидрокси-индолов, а второй– 6-гидроксииндолов,
то доминирующим процессом стано-вится
образование последних. Образование6гидроксииндола можно пред-ставить следующей
схемой:
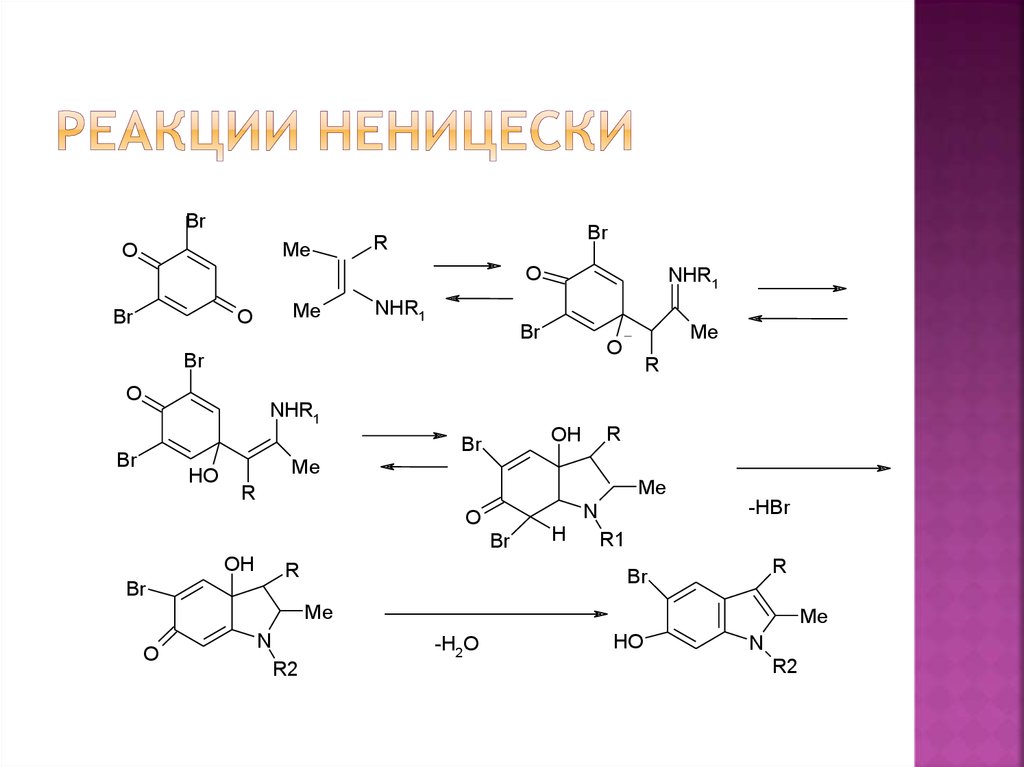
15. Реакции Неницески
BrMe
O
Br
R
O
Br
Me
O
NHR1
NHR1
Br
Br
O
Me
O
R
NHR1
Br
HO
R
OH
Br
Me
Me
R
Br
OH
R
Br
-HBr
N
O
H
R1
R
Br
Me
O
N
Me
-H2O
R2
HO
N
R2
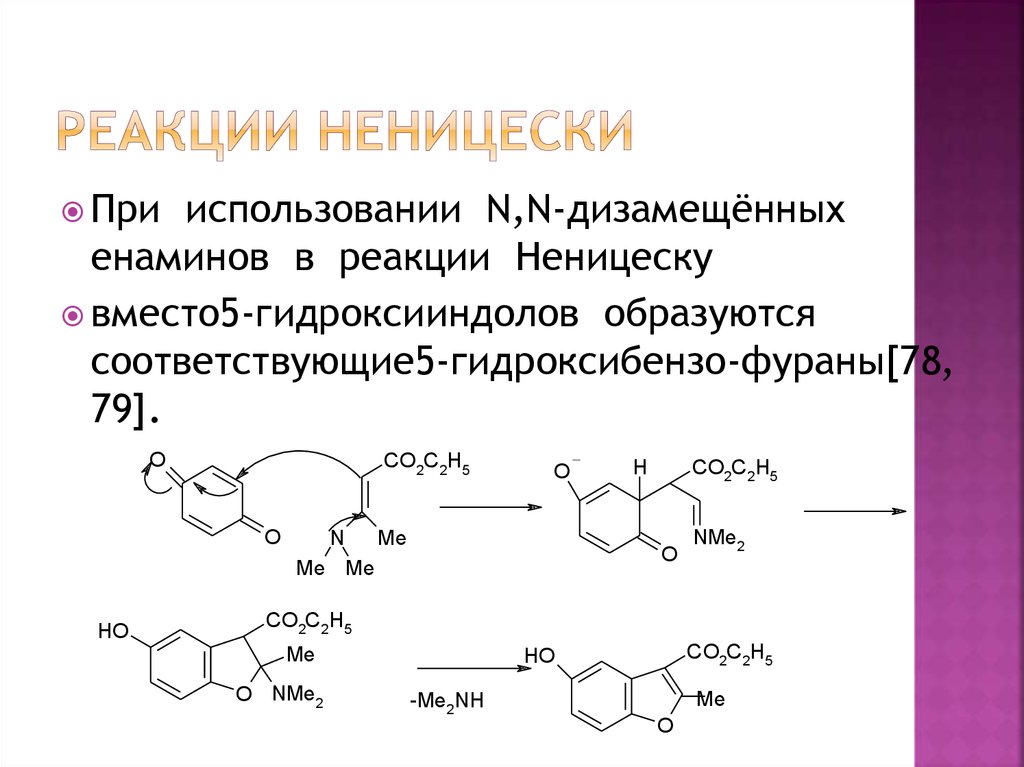
16. Реакции Неницески
Прииспользовании N,N-дизамещённых
енаминов в реакции Неницеску
вместо5-гидроксииндолов образуются
соответствующие5-гидроксибензо-фураны[78,
79].
O
CO2C2H5
O
N
O
Me
O
Me Me
HO
CO2C2H5
H
NMe2
CO2C2H5
Me
O NMe2
CO2C2H5
HO
Me
-Me2NH
O
17. Реакции Неницески
Альтернативой реакции Неницеску можносчитать весьма интересный
метод получения1,2,3,4-тетрагидро-γкарболинов, основанный на катализи-руемой
кислотами Льюиса циклоконденсации
еноловых эфиров пиперидона-4
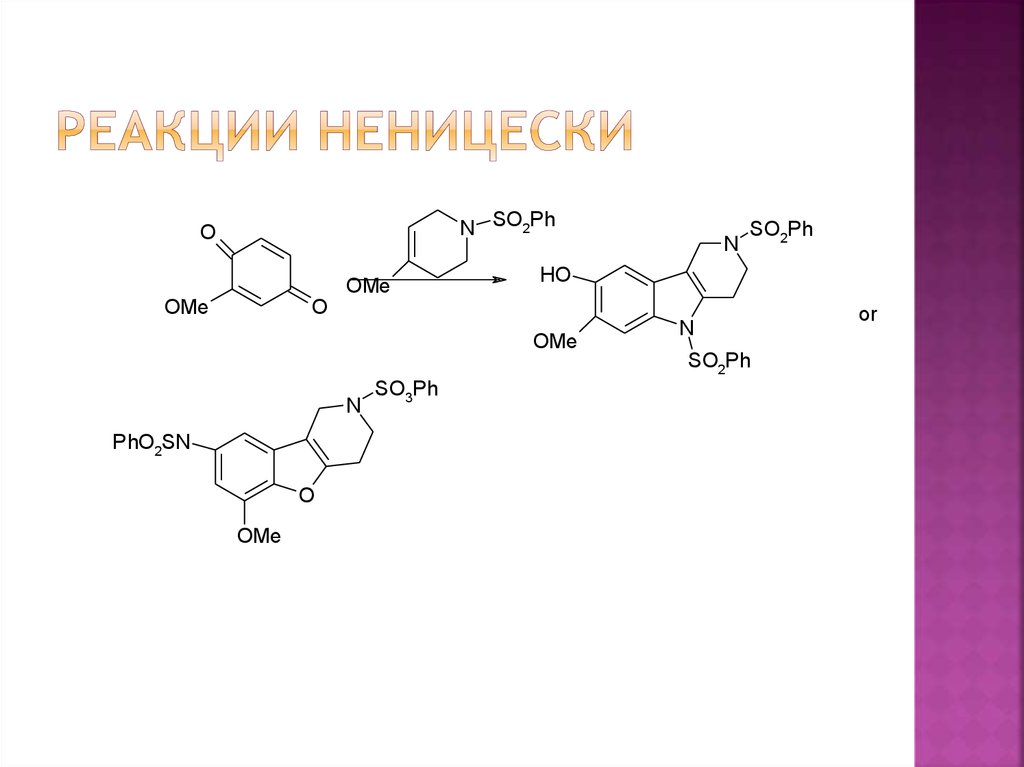
с2-метокси-4-(N-фенилсульфонил)-1,4бензохинониминами[80]. Моноимины
бензохинона взаимодействуют с еноловым
эфиром пиперидона-4 с образова-нием как γкарболиновых производных 32, так и
тетрагидробензо[4,5]фуро-[3,2-c]пиридинов 33
в зависимости от используемой кислоты
Льюиса.
18. Реакции Неницески
N SO2PhO
OMe
OMe
N
SO2Ph
HO
O
OMe
N
SO2Ph
N
PhO2SN
O
OMe
SO3Ph
or
19. Реакции Неницески
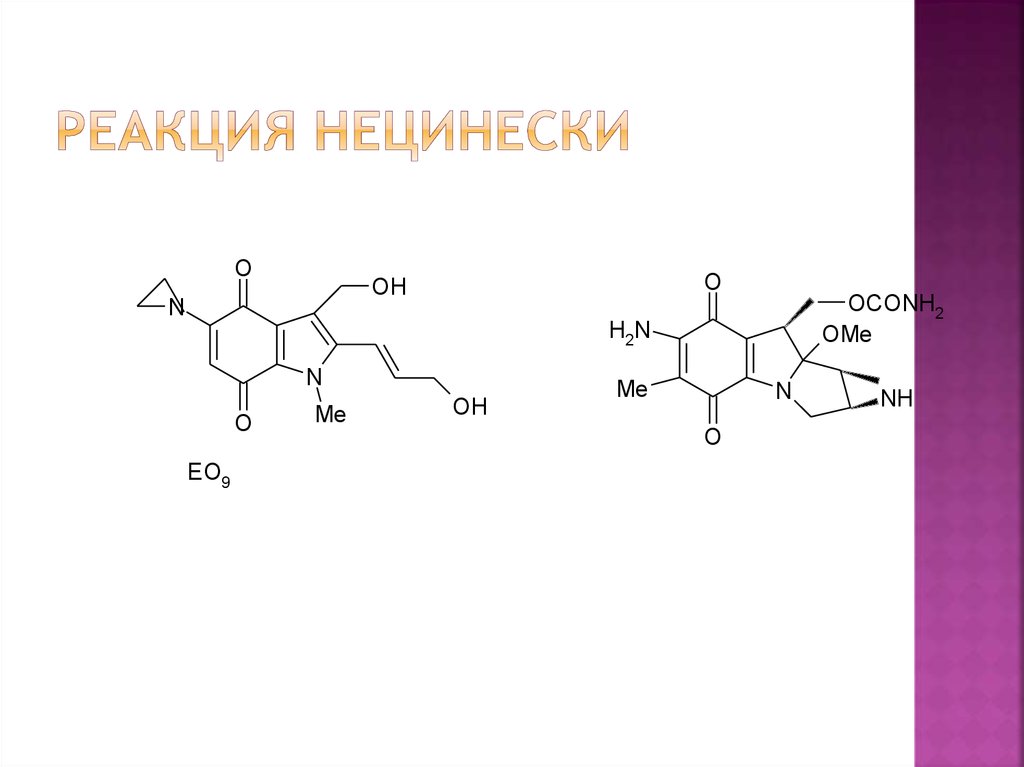
В1995г. реакция Неницеску была
использована для синтеза ключевого
интермедиата при получении нового
синтетического индолохинона ЕО9,
структура и функции которого близки
Митомицину С– антибиотику с противоопухолевой активностью, выделенному
из культуры гриба Streptomyces
caespitosus[81]
20. Реакция Нецинески
OO
OH
N
OCONH2
OMe
H2N
N
O
EO9
Me
OH
Me
N
O
NH










 chemistry
chemistry