Similar presentations:
Фенолы. Классификация и номенклатура фенолов
1.
Фенолы1
26.11.2018
2.
Фенол – соединение, в молекуле которогогидроксильная группа находится при углероде
ароматического кольца.
OH
2
26.11.2018
3.
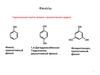
фенолы+M
+M
ароматические спирты
-I
: OH
CH2
-I
-I
OH
-I
3
26.11.2018
4.
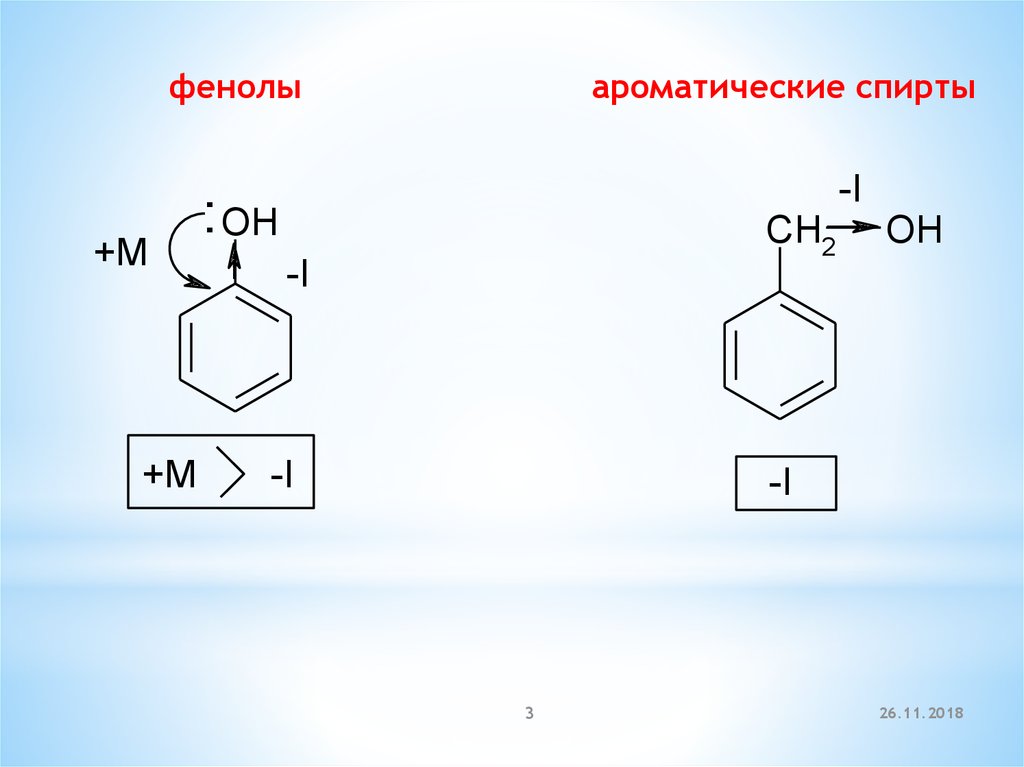
I. Классификация и номенклатура фенолов1. Одноатомные фенолы
OH
фенол
гидроксибензол
CH3
CH3
CH3
OH
о – крезол
ортометилгидроксибензол
2 – метилгидроксибензол
OH
м – крезол
метаметилгидроксибензол
3 – метилгидроксибензол
4
OH
п – крезол
параметилгидроксибензол
4 – метилгидроксибензол
26.11.2018
5.
2. Двухатомные фенолыOH
OH
OH
OH
OH
пирокатехин
1,2 – дигидроксибензол
резорцин
1,3 – дигидроксибензол
5
OH
гидрохинон
1,4 – дигидроксибензол
26.11.2018
6.
3. Трехатомные фенолыOH
OH
OH
OH
OH
OH
OH
OH
пирогаллол
1,2,3 – тригидроксибензол
OH
оксигидрохинон
1,2,4 – тригидроксибензол
флороглюцин
1,3,5 – тригидроксибензол
6
26.11.2018
7.
4. Многоатомные фенолы (от 4 до 6 групп -OH).OH
HO
OH
HO
OH
OH
гексагидроксибензол
7
26.11.2018
8.
II. Способы получения фенолов1. Получение фенолов из каменноугольной смолы
(промышленный способ)
При коксовании 1тонны угля получают 55кг
каменноугольной смолы. В состав входит:
1) 1,6% - бензол;
2) 0,4% - толуол;
3) 0,08% - ксилолы;
4) 0,4% - фенол;
5) 1,6% - крезолы;
6) 4,2% - нафталин.
8
26.11.2018
9.
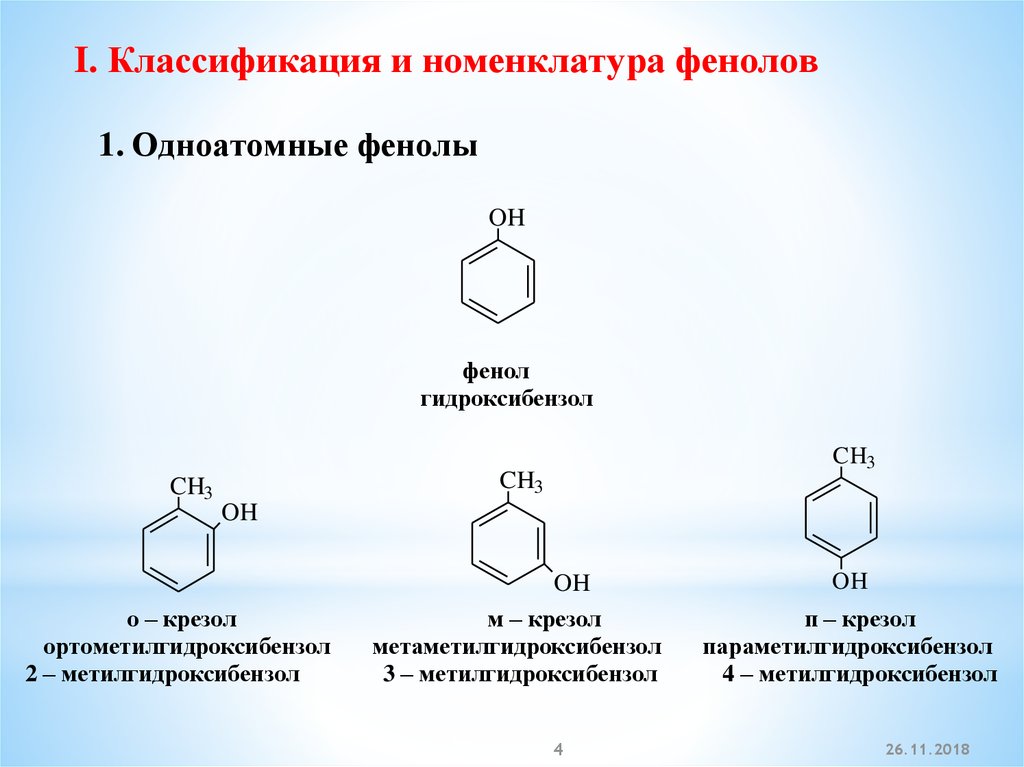
2. Гидролиз галогенопроизводных бензолаCl
OH
+
NaOH
+
9
NaCl
26.11.2018
10.
:ClВозникает эффект сопряжения, за счет которого связь C –
Cl становится прочной . Чтобы разорвать эту связь, нужны
жёсткие условия
:Cl
300º
C
NaOH(конц
)
Образуется тройная связь. Новая π – связь находится в
плоскости нахождения атомов бензольного кольца
10
26.11.2018
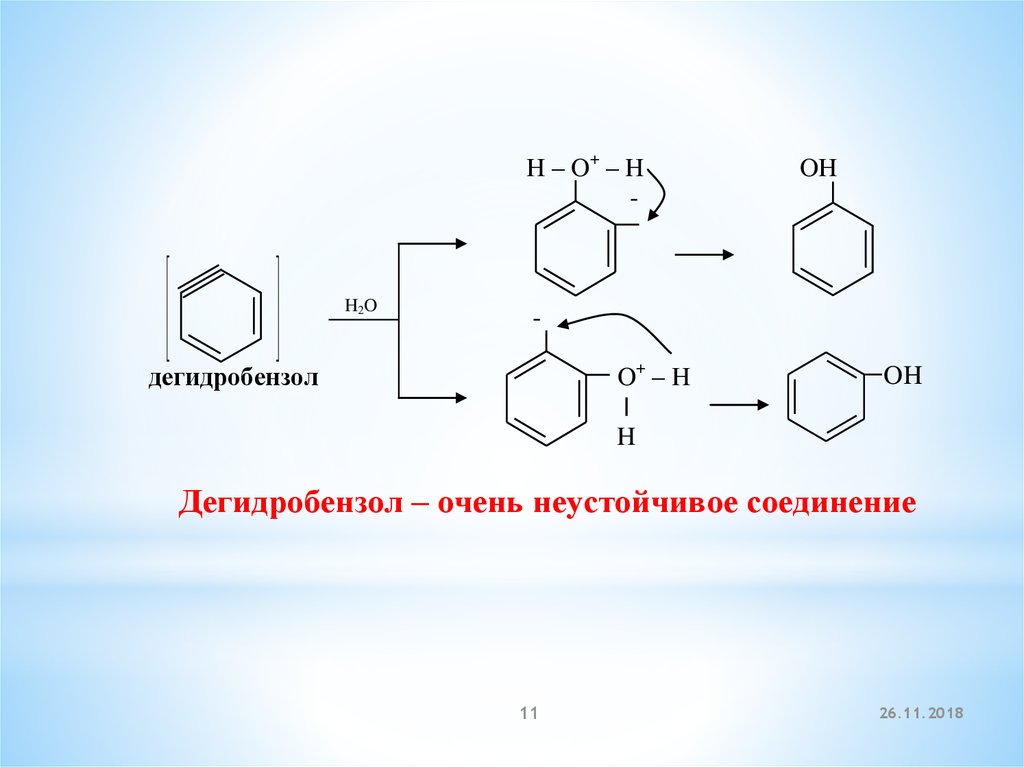
11.
H – O+ – H-
H2O
OH
O+ – H
|
H
дегидробензол
OH
Дегидробензол – очень неустойчивое соединение
11
26.11.2018
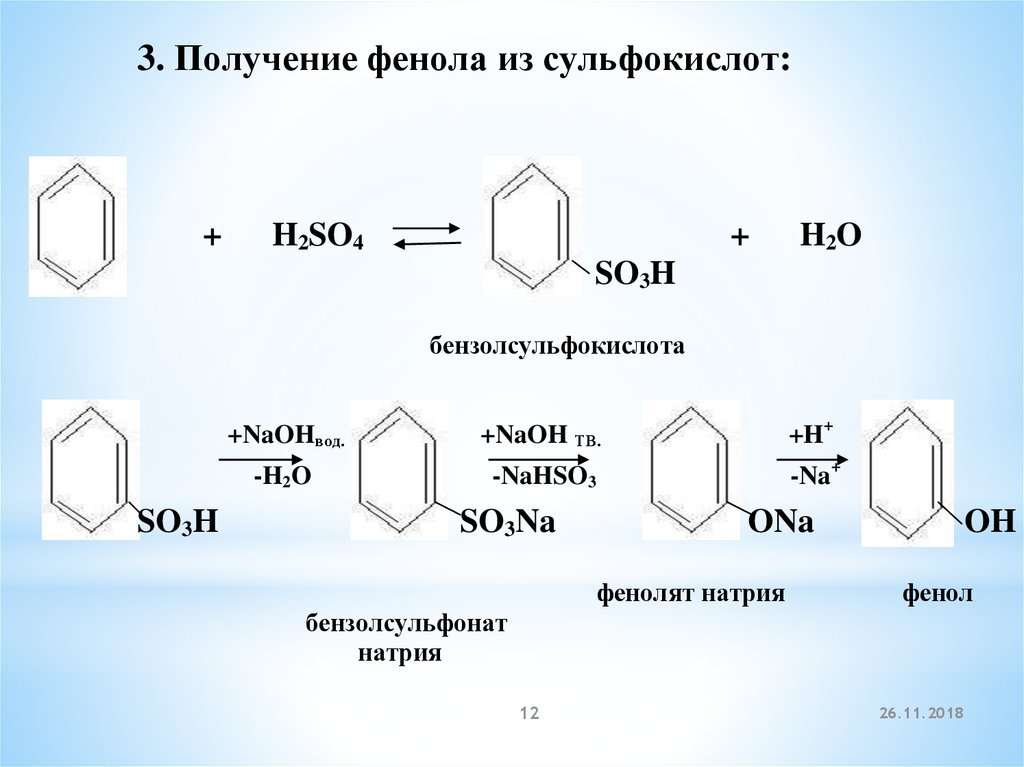
12.
3. Получение фенола из сульфокислот:+
H2SO4
+
H2O
SO3H
бензолсульфокислота
SO3H
+NaOHвод.
+NaOH ТВ.
+H+
-H2O
-NaHSO3
-Na+
SO3Na
ONa
фенолят натрия
OH
фенол
бензолсульфонат
натрия
12
26.11.2018
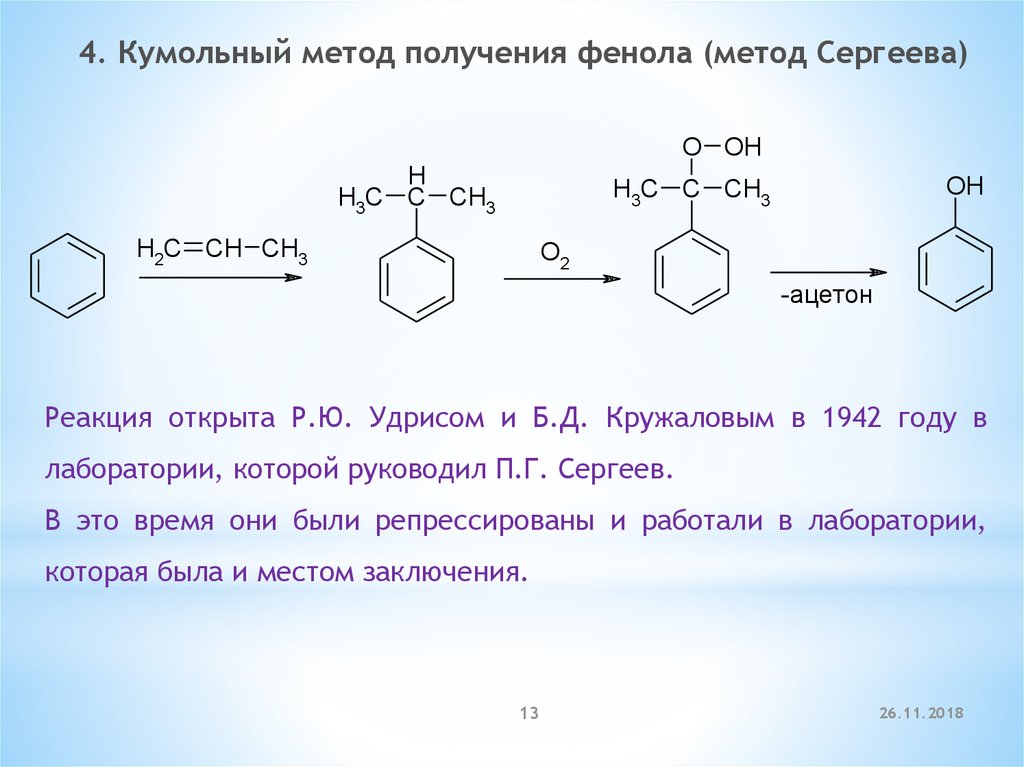
13.
4. Кумольный метод получения фенола (метод Сергеева)O OH
H
H3C C CH3
OH
H3C C CH3
H2C CH CH3
O2
-ацeтон
Реакция открыта Р.Ю. Удрисом и Б.Д. Кружаловым в 1942 году в
лаборатории, которой руководил П.Г. Сергеев.
В это время они были репрессированы и работали в лаборатории,
которая была и местом заключения.
13
26.11.2018
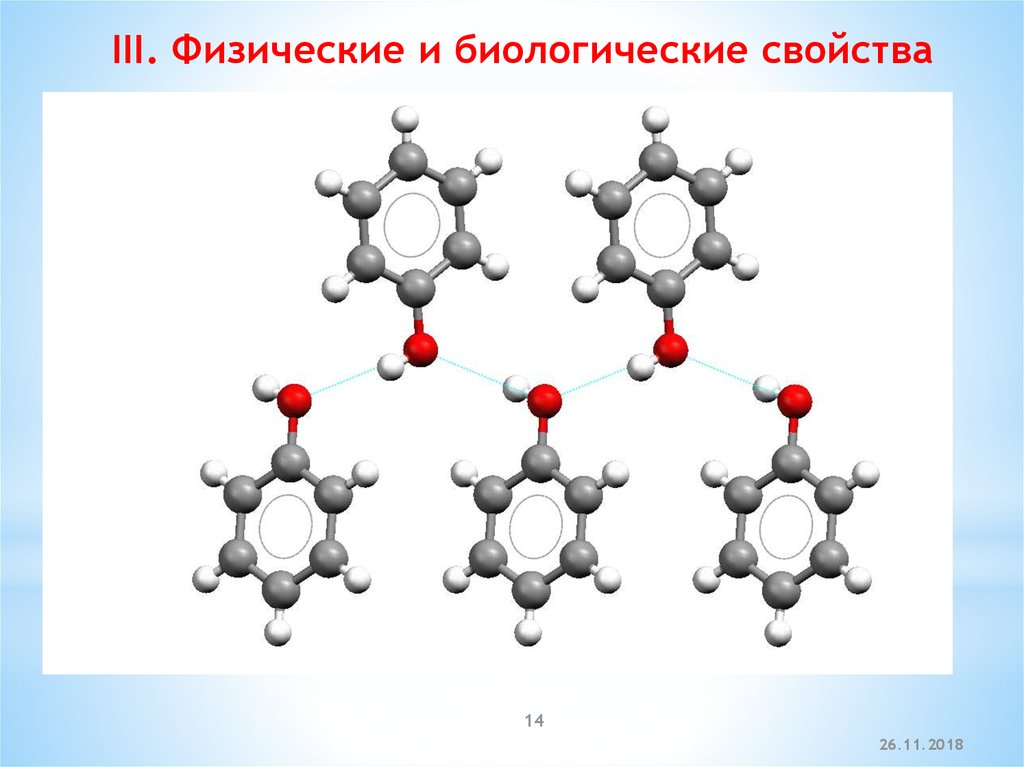
14.
III. Физические и биологические свойства14
26.11.2018
15.
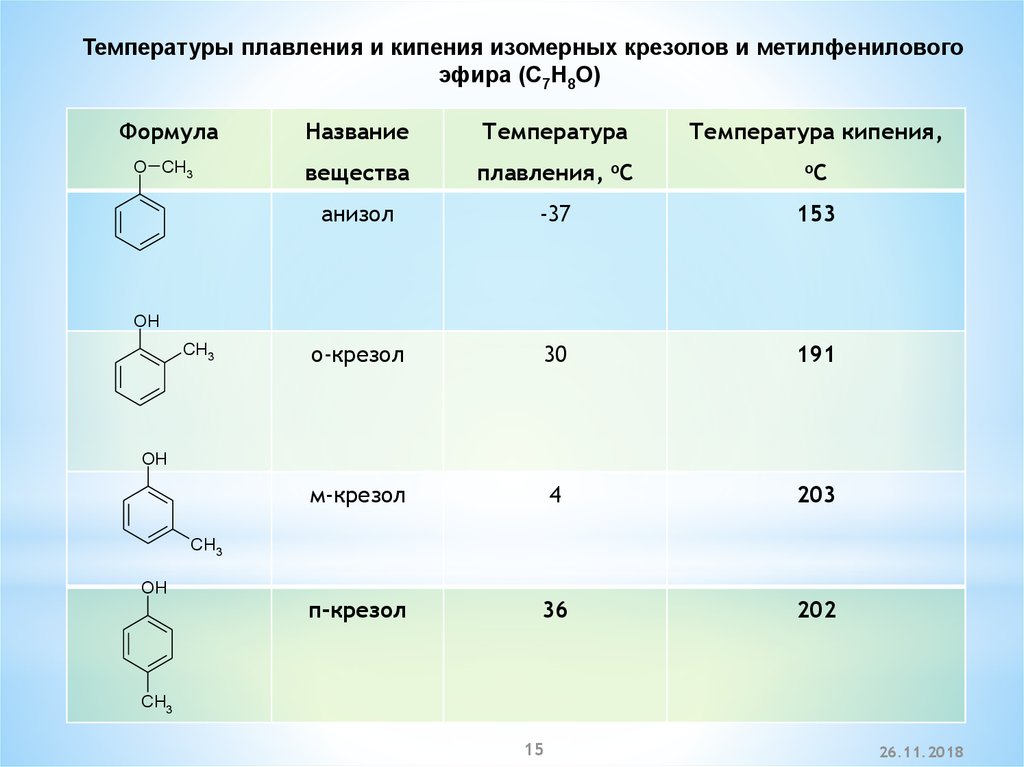
Температуры плавления и кипения изомерных крезолов и метилфениловогоэфира (C7H8O)
Формула
O CH3
Название
Температура
Температура кипения,
вещества
плавления, oC
oC
анизол
-37
153
о-крезол
30
191
м-крезол
4
203
п-крезол
36
202
OH
CH3
OH
CH3
OH
CH3
15
26.11.2018
16.
* Фенол очень токсичен, при попадании на кожу вызываетожоги. Фенол обладает хорошими дезинфицирующими
свойствами; это было первое вещество, которое
использовалось для дезинфекции (Дж. Листер, 1867)
* Фенолы входят в состав креозота – жидкости, получаемой
из каменноугольной смолы и используемой для пропитки
шпал для предотвращения их гниения. Очищенный
креозот используется как антисептик в медицине.
* Пентахлорфенол применяется для пропитки древесины
как антисептик, инсектицид и фунгицид.
16
26.11.2018
17.
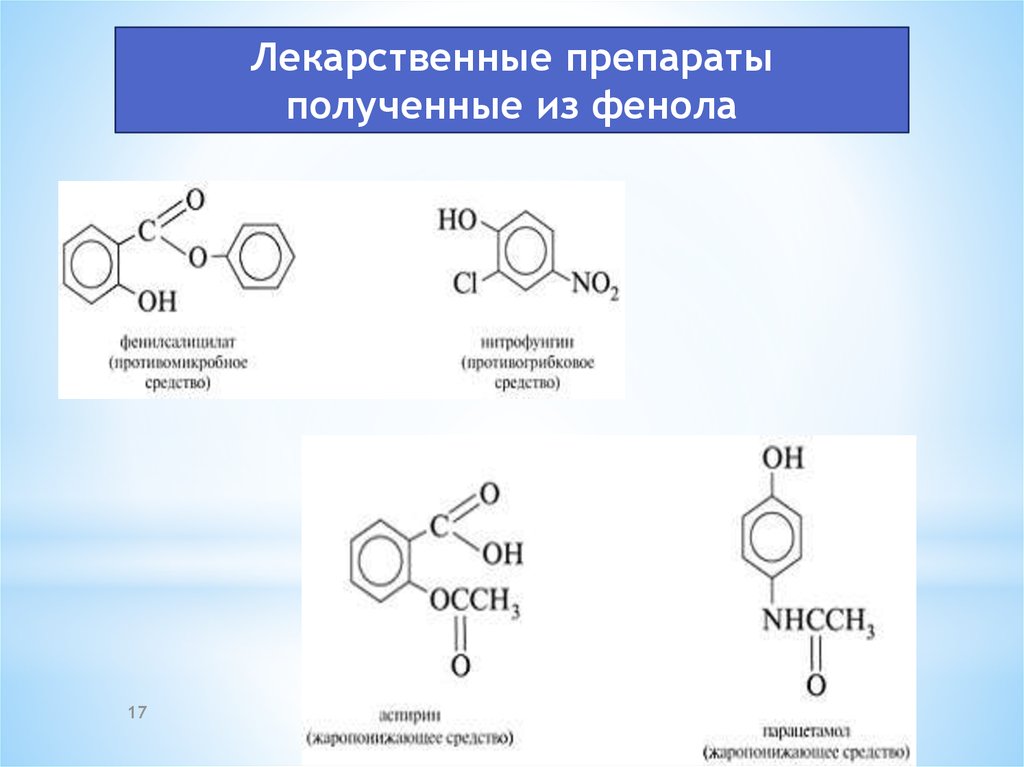
Лекарственные препаратыполученные из фенола
17
18.
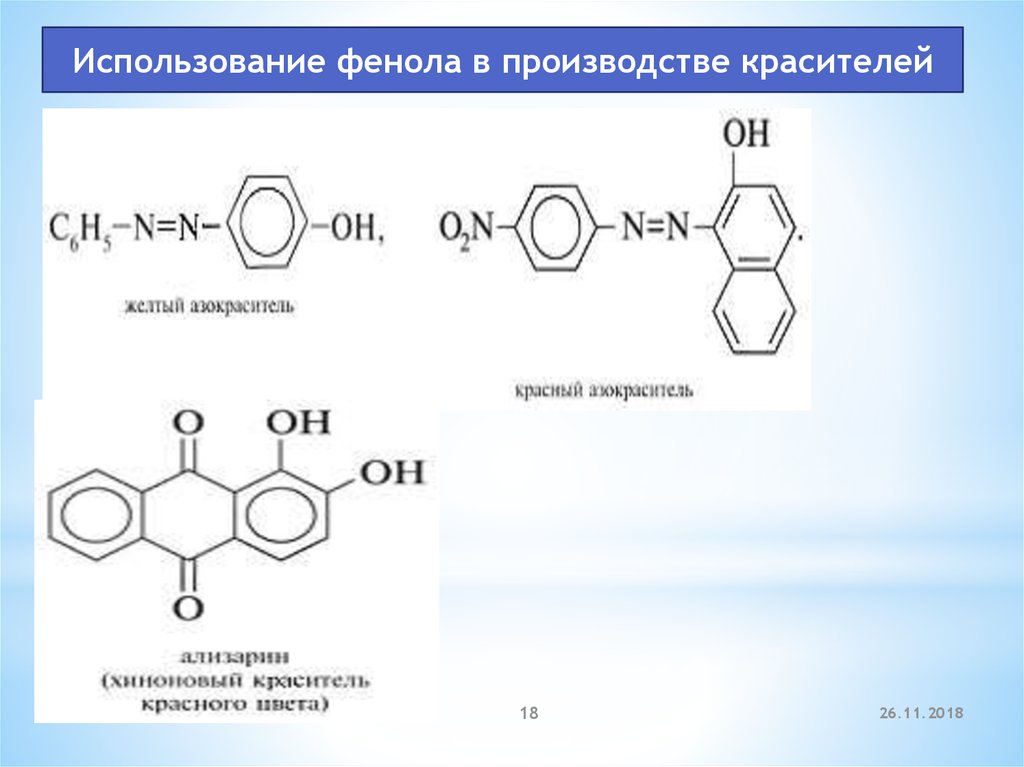
Использование фенола в производстве красителей18
26.11.2018
19.
IV. Химические свойства1. Кислотные свойства:
1) образование фенолятов
O Na
OH
+
+
+
NaOH
Фенол
H2O
фенолят натрия
19
26.11.2018
20.
Опыт: взаимодействие фенола с гидроксидом натрияС6Н5ОН +
NaOH
C6H5ONa
фенол
фенолят натрия
20
+
H2O
26.11.2018
21.
22.
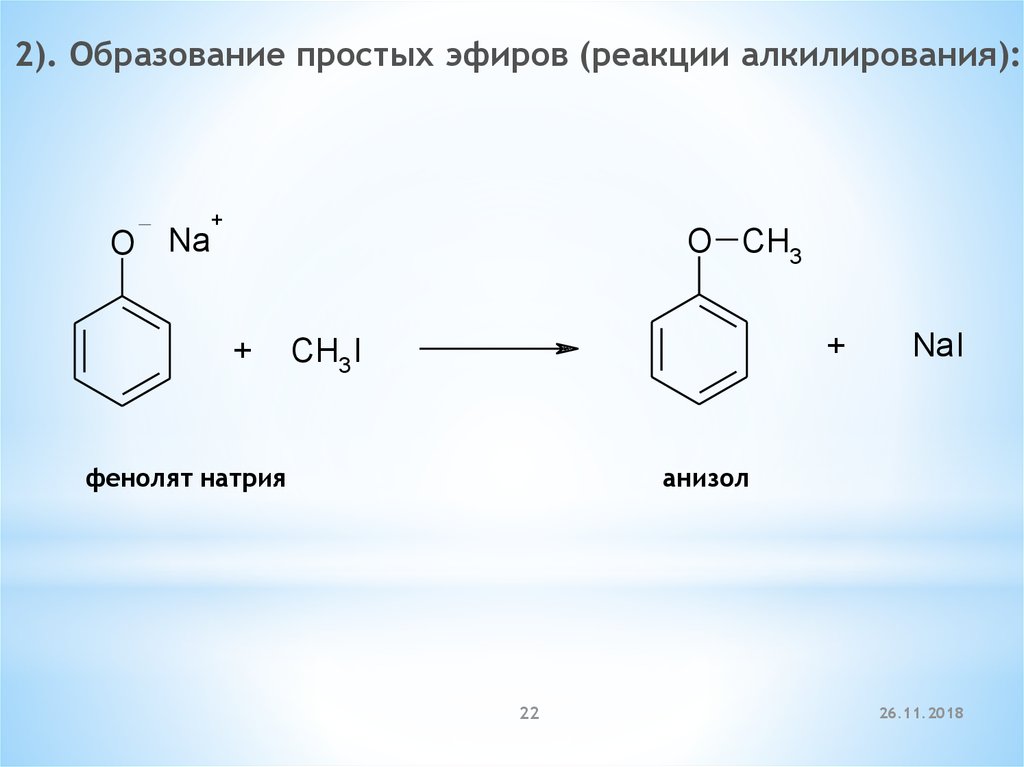
2). Образование простых эфиров (реакции алкилирования):O Na
+
O CH3
+
+
CH3 I
фенолят натрия
NaI
анизол
22
26.11.2018
23.
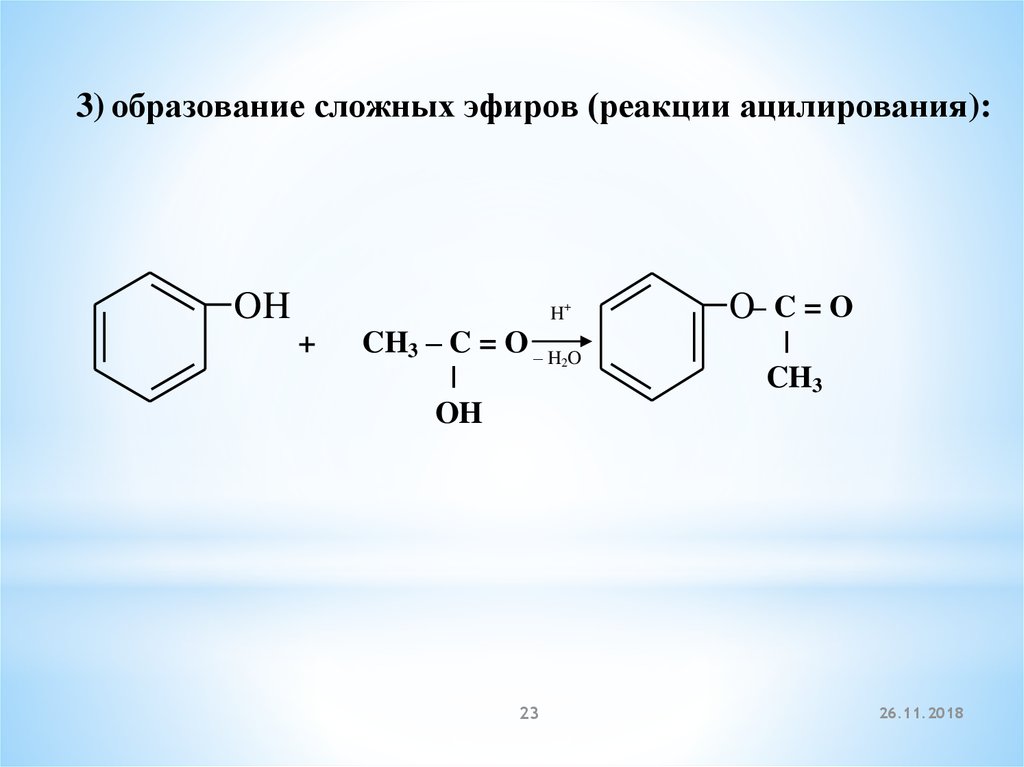
3) образование сложных эфиров (реакции ацилирования):OH
H+
+
CH3 – C = O – H2O
|
OH
23
O– C = O
|
CH3
26.11.2018
24.
Опыт: качественная реакция на фенол3C6H5OH
+
FeCl3
(C6H5O)3Fe
+
3HCl
Образуется комплексная соль фиолетового цвета
24
26.11.2018
25.
26.
2. Реакциибензольного
замещения):
кольца
(электрофильного
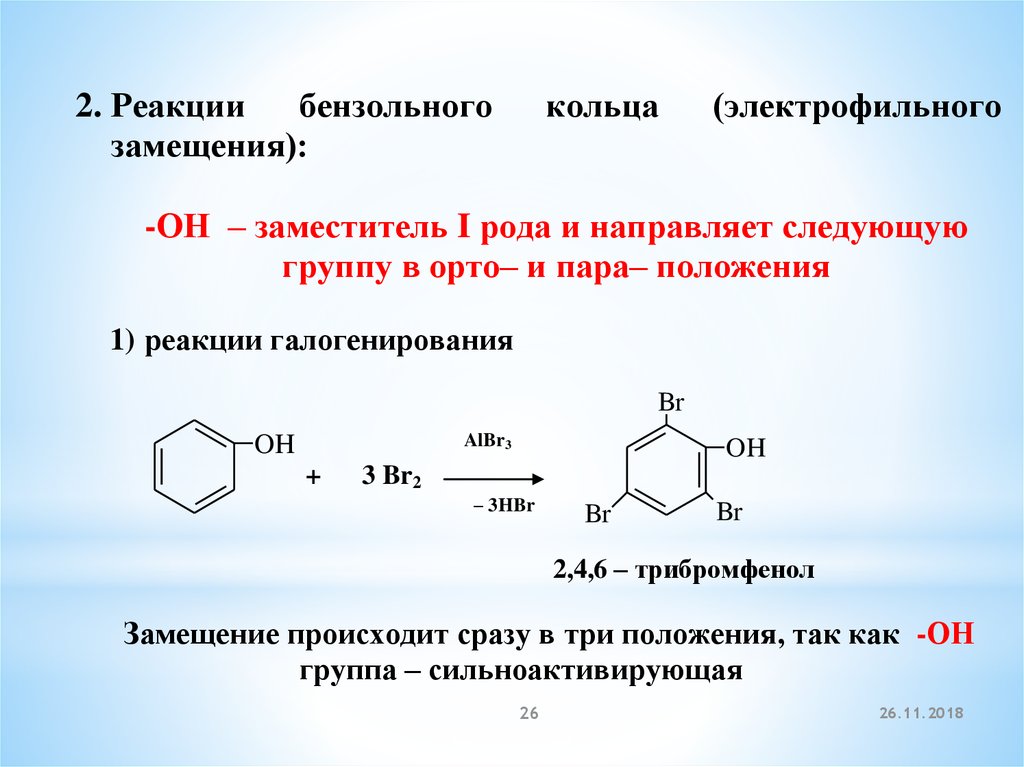
-ОН – заместитель I рода и направляет следующую
группу в орто– и пара– положения
1) реакции галогенирования
Br
AlBr3
OH
+
OH
3 Br2
– 3HBr
Br
Br
2,4,6 – трибромфенол
Замещение происходит сразу в три положения, так как -ОН
группа – сильноактивирующая
26
26.11.2018
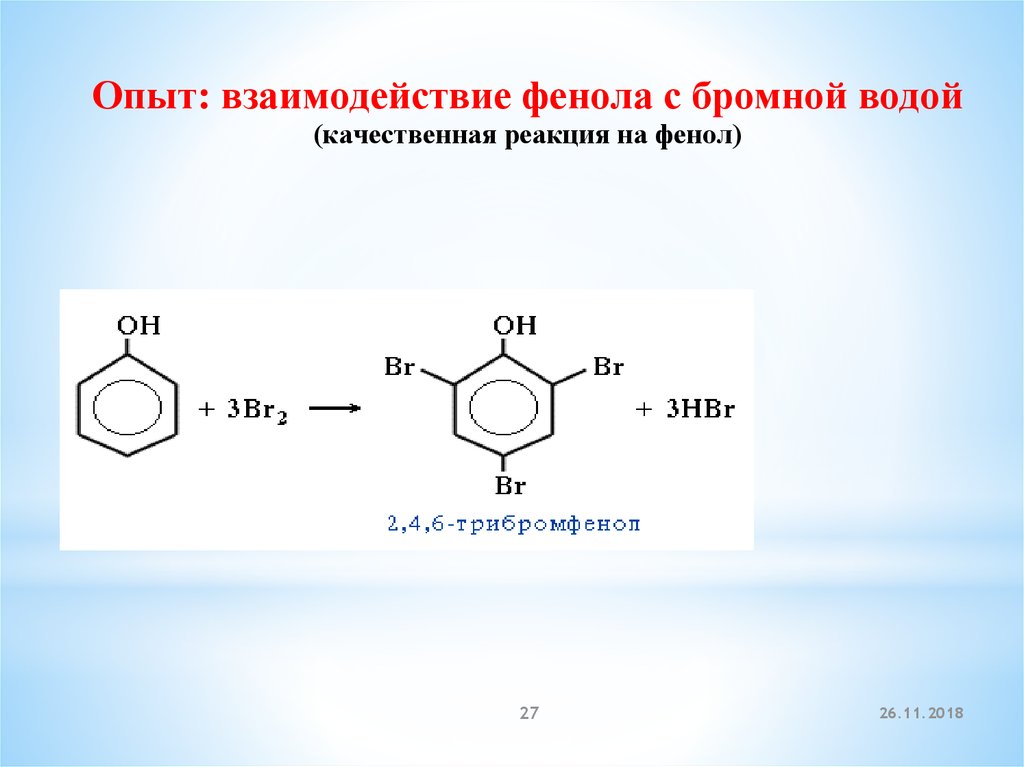
27.
Опыт: взаимодействие фенола с бромной водой(качественная реакция на фенол)
27
26.11.2018
28.
29.
Для получения моногалогенопроизводных нуженмалополярный растворитель
Br
OH
CCl4
+
OH
Br2
орто-бромофенол
OH
Br
пара-бромофенол
29
26.11.2018
30.
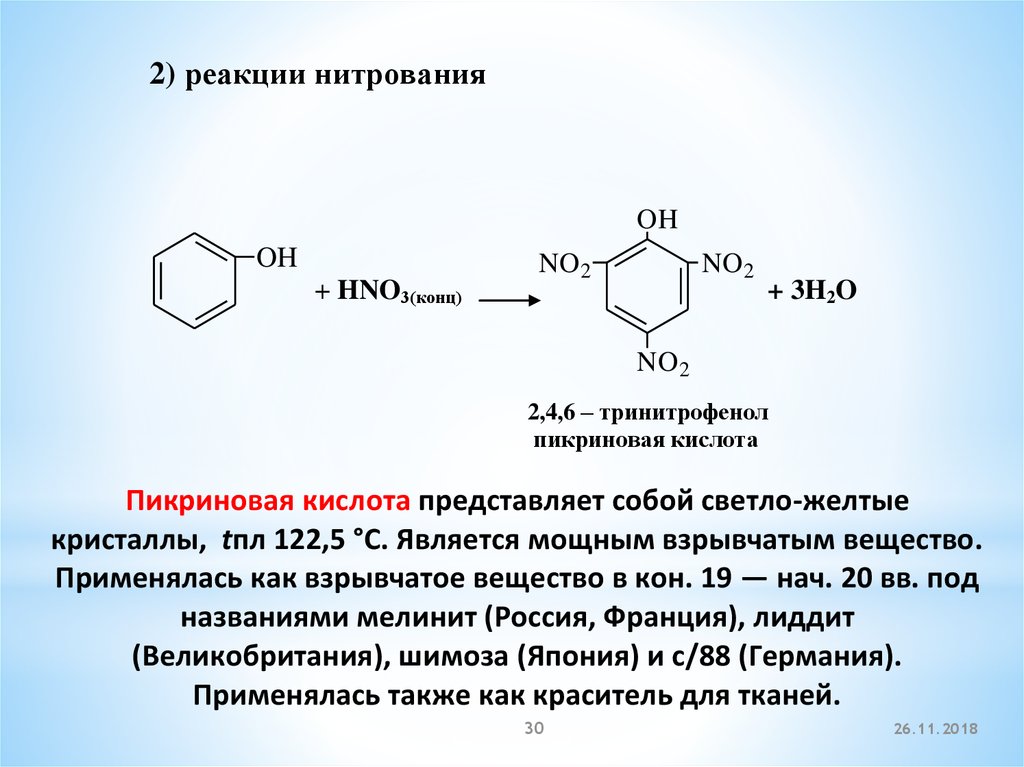
2) реакции нитрованияOH
OH
+ HNO3(конц)
NO2
NO2
+ 3H2O
NO2
2,4,6 – тринитрофенол
пикриновая кислота
Пикриновая кислота представляет собой светло-желтые
кристаллы, tпл 122,5 °С. Является мощным взрывчатым вещество.
Применялась как взрывчатое вещество в кон. 19 — нач. 20 вв. под
названиями мелинит (Россия, Франция), лиддит
(Великобритания), шимоза (Япония) и с/88 (Германия).
Применялась также как краситель для тканей.
30
26.11.2018
31.
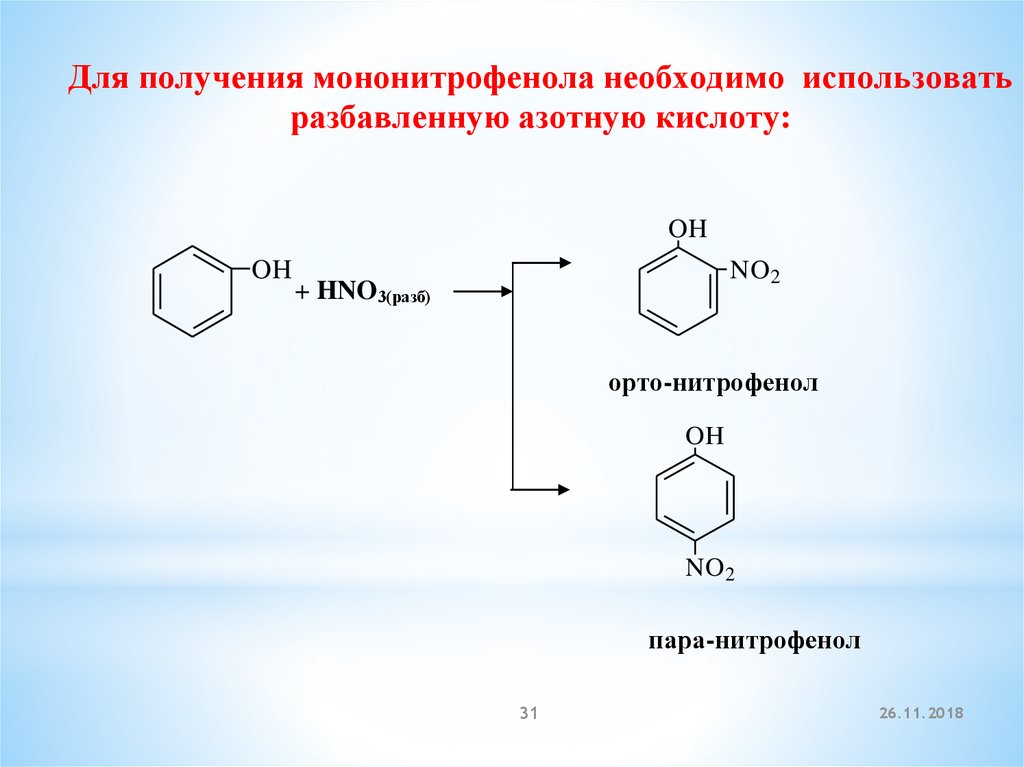
Для получения мононитрофенола необходимо использоватьразбавленную азотную кислоту:
OH
OH
NO 2
+ HNO3(разб)
орто-нитрофенол
OH
NO 2
пара-нитрофенол
31
26.11.2018
32.
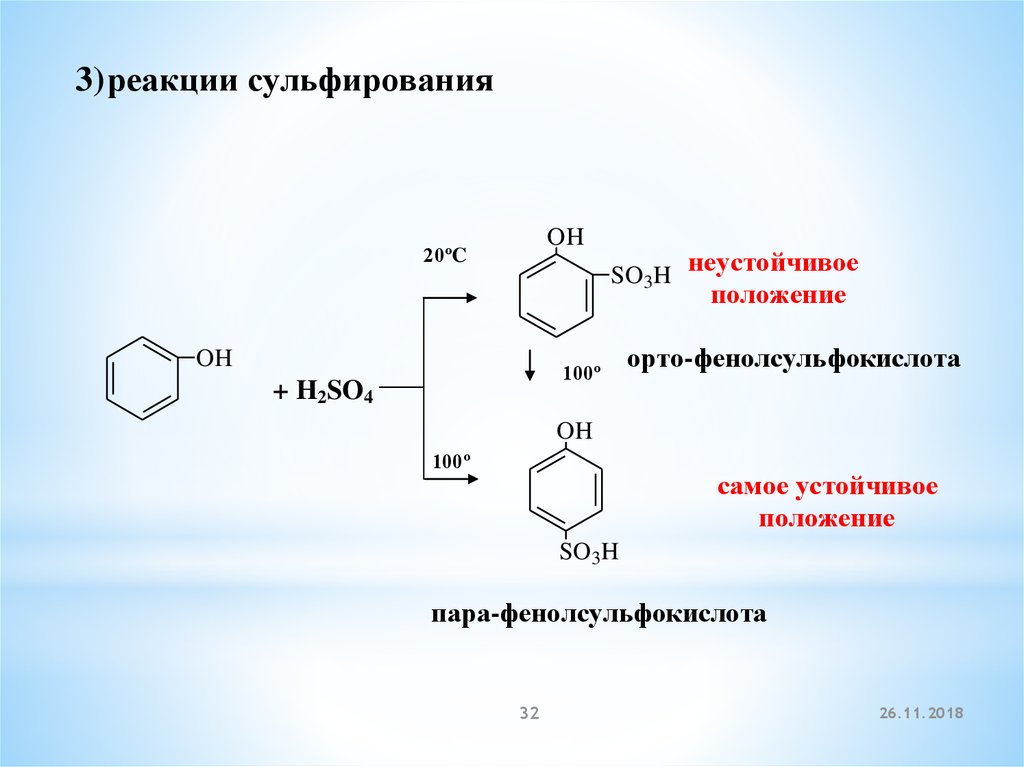
3) реакции сульфированияOH
20ºC
SO3H неустойчивое
положение
OH
100º
C
+ H2SO4
орто-фенолсульфокислота
OH
100º
C
самое устойчивое
положение
SO 3H
пара-фенолсульфокислота
32
26.11.2018
33.
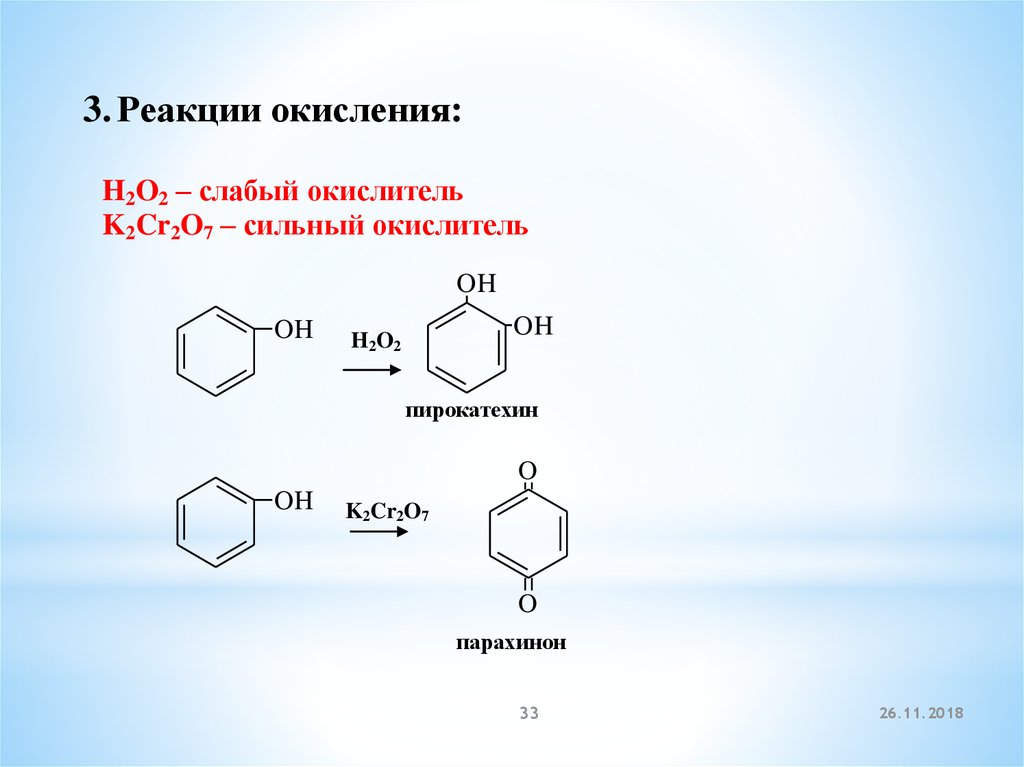
3. Реакции окисления:H2O2 – слабый окислитель
K2Cr2O7 – сильный окислитель
OH
OH
OH
H2O2
пирокатехин
O
OH
K2Cr2O7
O
парахинон
33
26.11.2018
34.
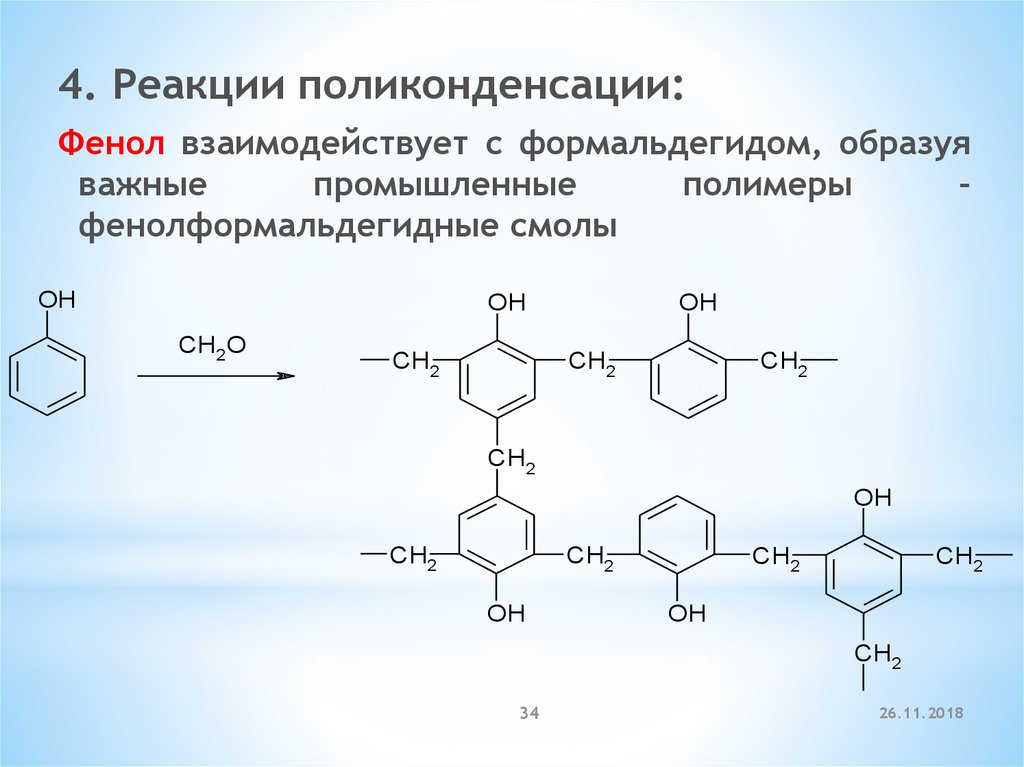
4. Реакции поликонденсации:Фенол взаимодействует с формальдегидом, образуя
важные
промышленные
полимеры
–
фенолформальдегидные смолы
OH
OH
CH2O
CH2
OH
CH2
CH2
CH2
OH
CH2
CH2
OH
CH2
CH2
OH
CH2
34
26.11.2018
35.
* Фенолформальдегидные смолы являются вязкими жидкостями илитвердыми веществами. Отвержденные фенолоформальдегидные
смолы обладают электроизоляционными и механическими
свойствами. Применяются в производстве фенопластов, клеев,
лаков, герметиков, фанеры, фенолформальдегидного волокна
(кайнол).
*
Фенолформальдегидные
смолы
являлись
первыми
промышленными синтетическими смолами; их производство под
названием “бакелит” было начато в 1909 году.
* Также,
в
промышленности
используются
крезолоформальдегидные смолы, резорцино-формальдегидные смолы,
феноло-анилино-формальдегидные
смолы,
фенологексаметилентетраминовые смолы, феноло-фурфурольные смолы
и смешанные смолы.
35
26.11.2018
36. Спасибо за Ваше внимание!
3626.11.2018

















 chemistry
chemistry