Similar presentations:
Ферменты - 2. Эффекторы
1. КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ
Лекция по теме:«ФЕРМЕНТЫ - 2»
КРАСНОДАР
2009
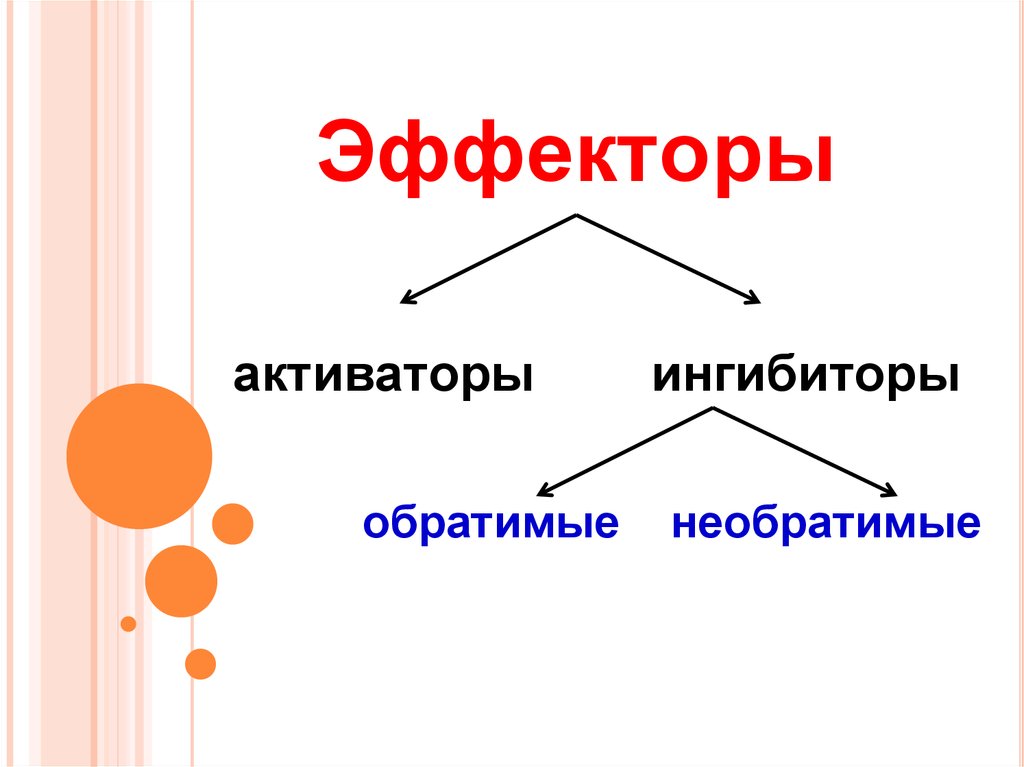
2. Эффекторы
активаторыобратимые
ингибиторы
необратимые
3. Активаторы
Неорганическиевещества
Низкомолекулярн
ые органические
вещества
Белки
4. Основные механизмы действия активаторов
Площадкадля
взаимодействия
фермента и
субстрата
Повышение
сродства фермента и
субстрата
Отщепление
5. Механизмы ингибирования
КонкурентноеНеконкурентное
Бесконкурентное
Субстратное
Аллостерическое
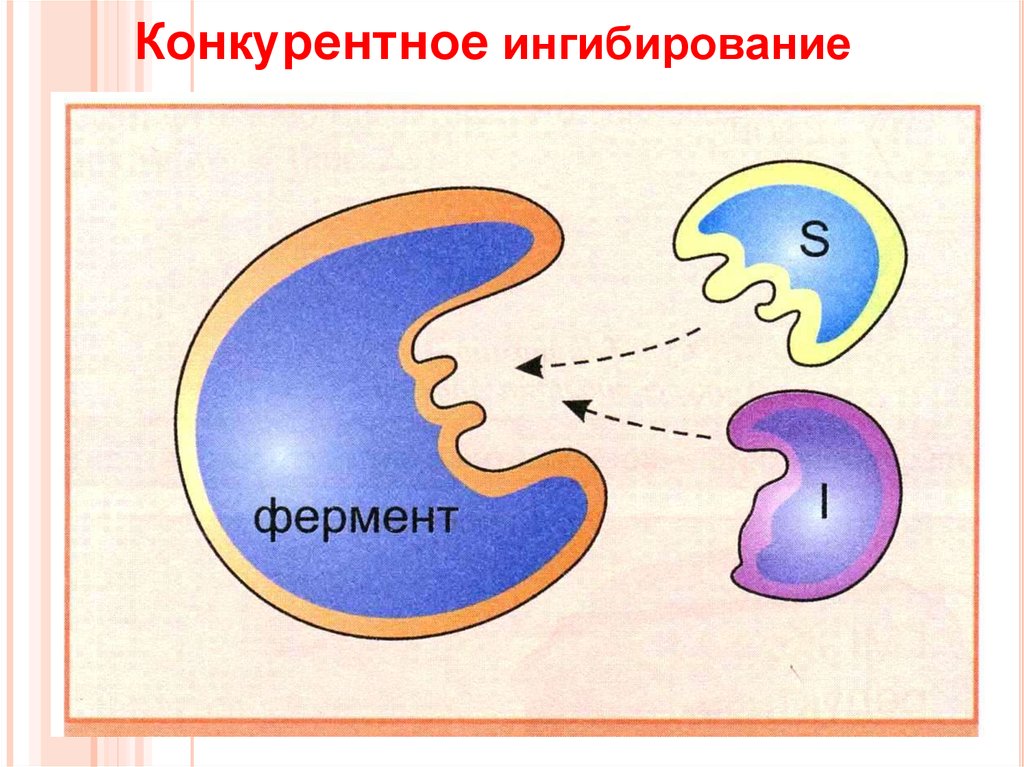
6. Конкурентное ингибирование
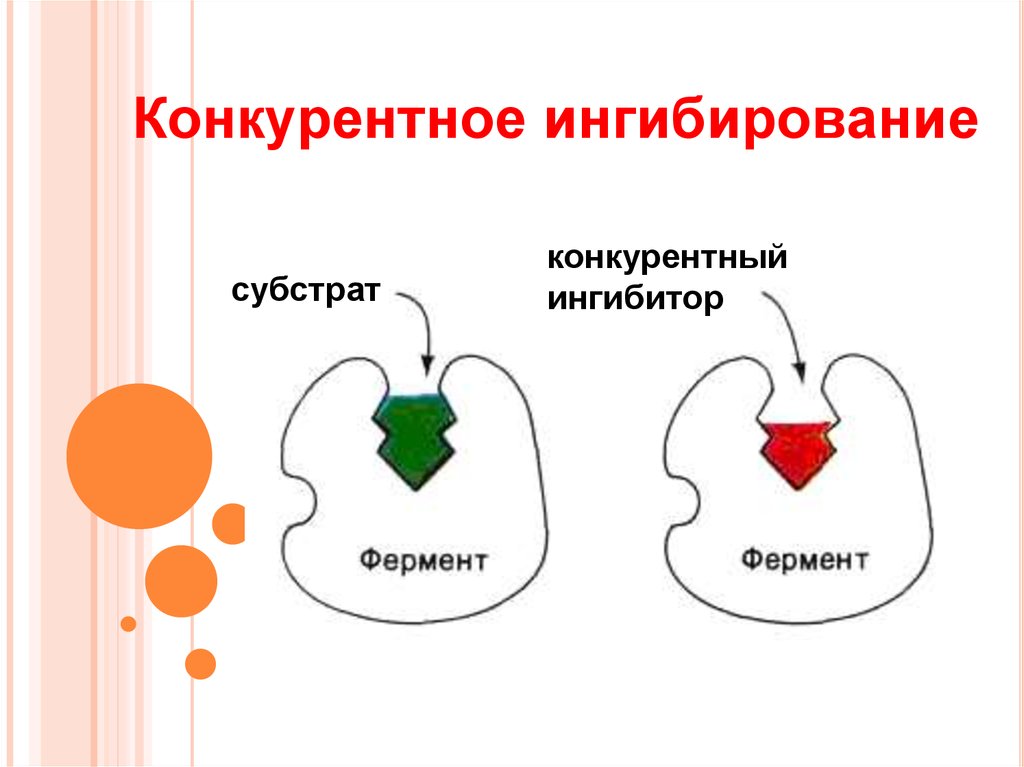
7. Конкурентное ингибирование
субстратконкурентный
ингибитор
8. и антивитамины витамина К
Витамин Ки антивитамины витамина К
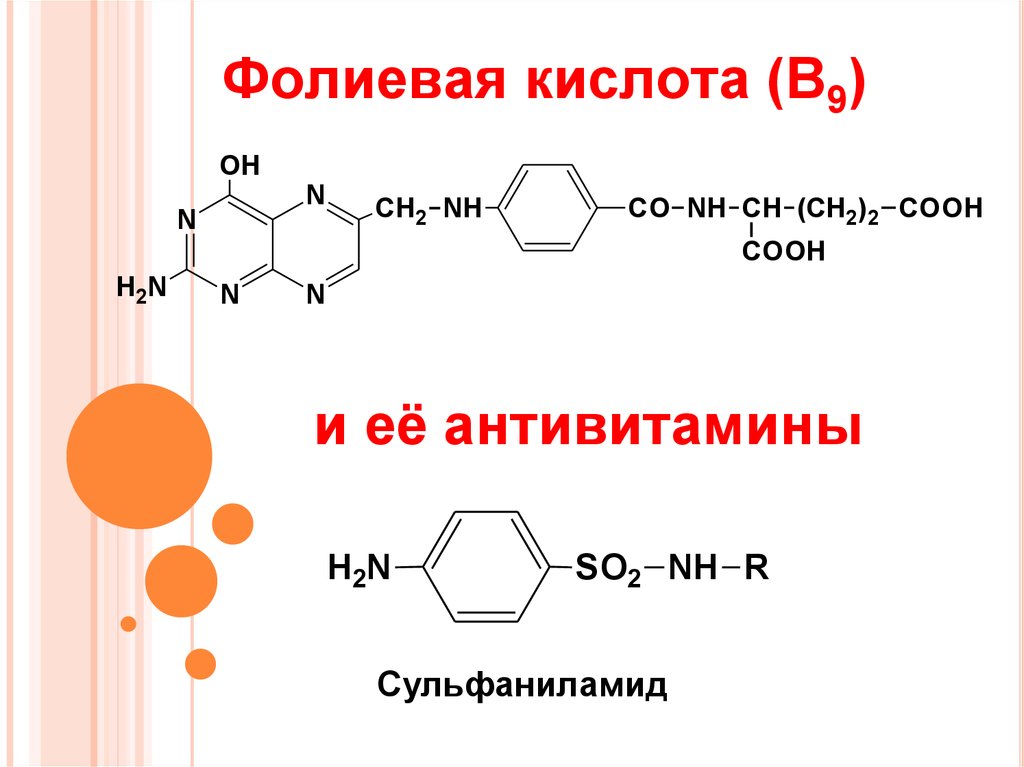
9. Фолиевая кислота (В9)
OHN
N
СН2 NH
СО NH СН (СН2)2 COOH
COOH
H2N
N
N
и её антивитамины
H2N
SО2 NH R
Сульфаниламид
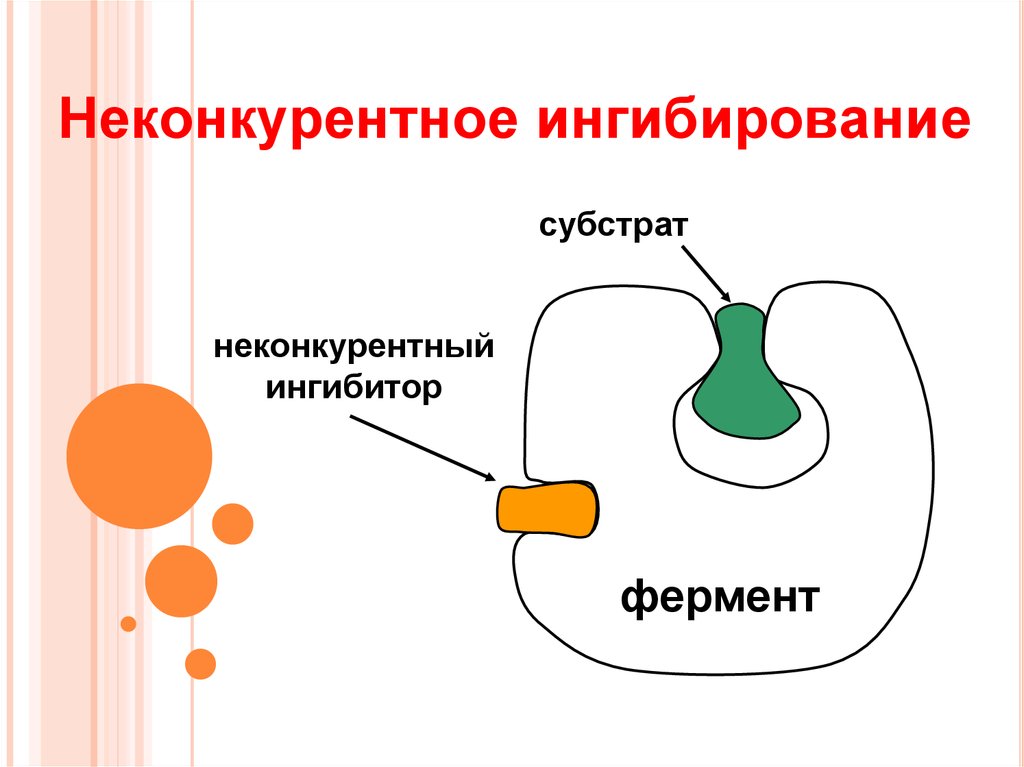
10. Неконкурентное ингибирование
субстратнеконкурентный
ингибитор
фермент
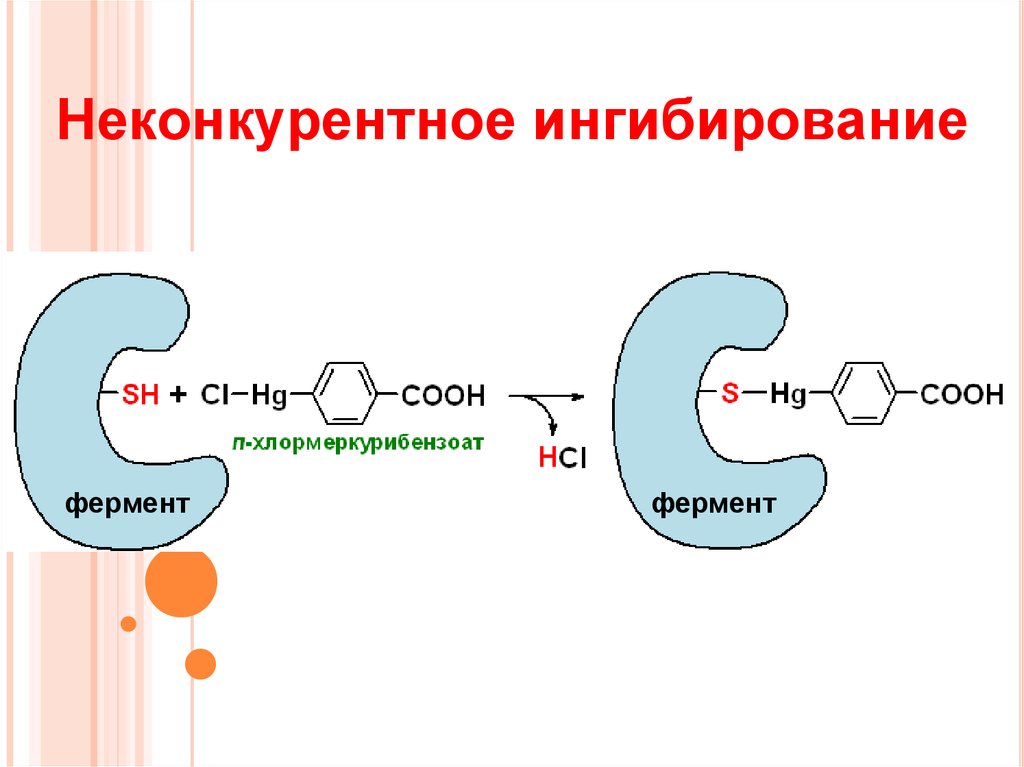
11. Неконкурентное ингибирование
12. Неконкурентное ингибирование
+фермент
фермент
13. Бесконкурентное ингибирование
E+SES
ES + I
EP
ESI
E+P
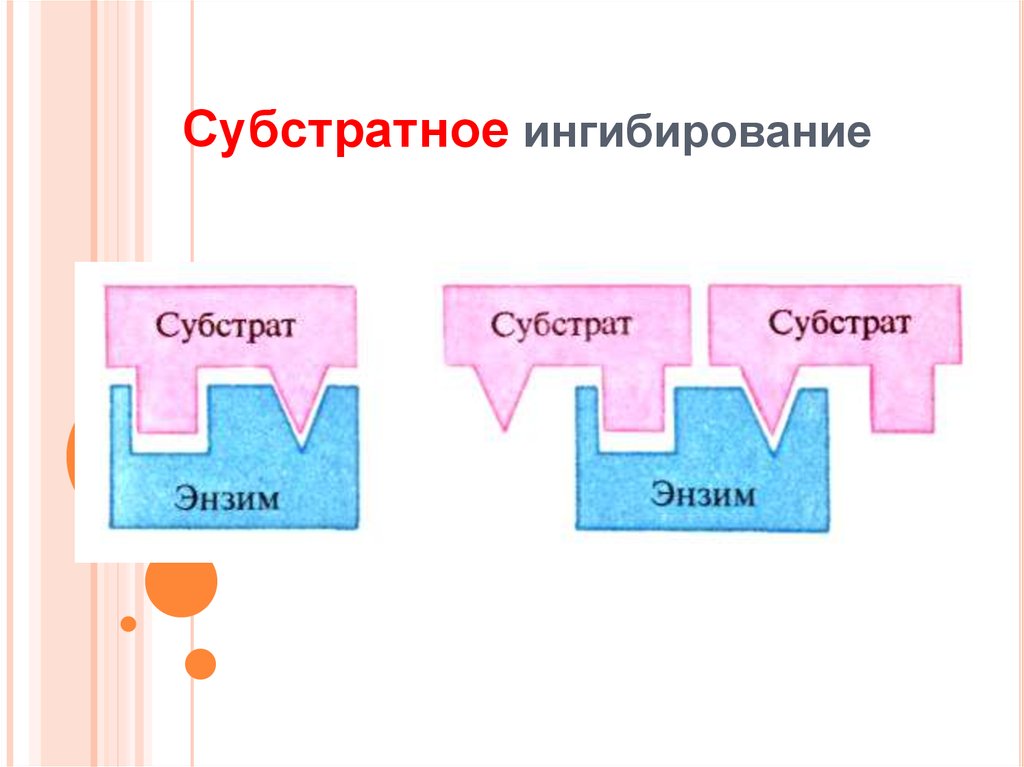
14. Субстратное ингибирование
15. Аллостерическое ингибирование
аллостерическийцентр
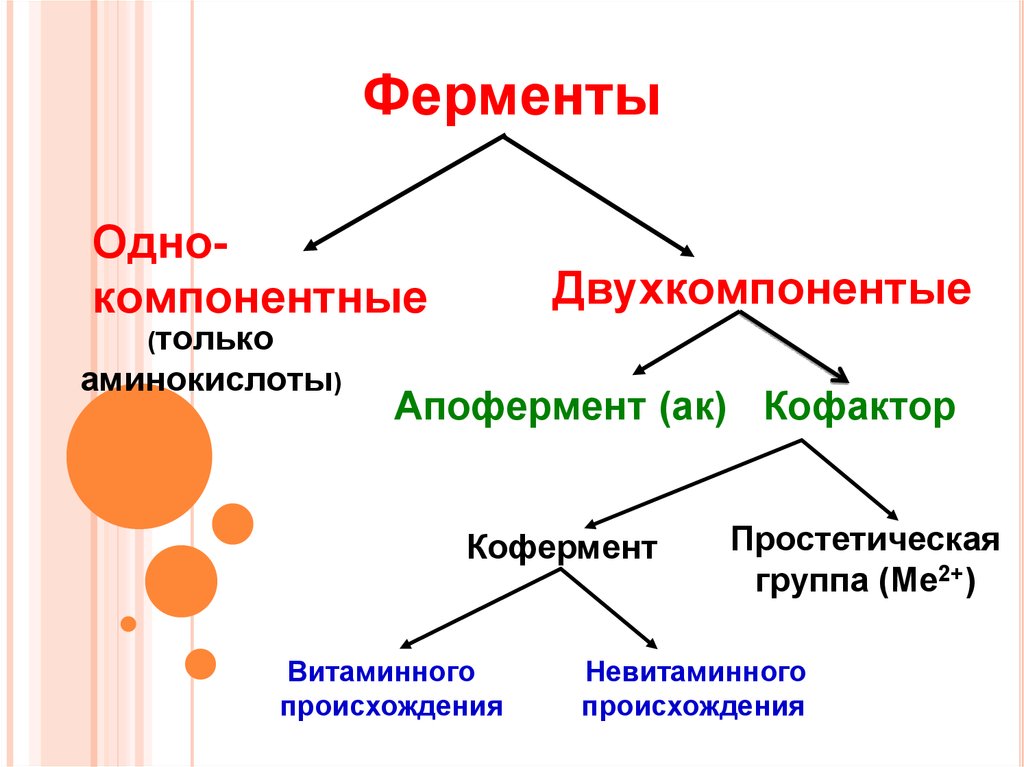
16. Ферменты
ОднокомпонентныеДвухкомпонентые
(только
аминокислоты)
Апофермент (ак) Кофактор
Кофермент
Витаминного
происхождения
Простетическая
группа (Ме2+)
Невитаминного
происхождения
17. Металлы, содержащиеся в ферментах
Алкогольдегидрогеназа,карбоангидраза
Аргиназа, аминопептидаза
Дипептидаза
Mn
Co
Фосфатаза, фосфокиназа
Mg
Тирозиназа
Cu
Сукцинатдегидрогеназа
Fe
Ксантиноксидаза
Mo
Zn
18. Классификация коферментов
По химическомустроению
1. Алифатические (липоевая
кислота);
2. Ароматические (коэнзим Q);
3. Гетероциклические (ТПФ,
ПФ);
4. Нуклеотиды (НАД, НАДФ,
ФАД, ФМН)
19. Липоевая кислота
CH2СН2
СН
S
S
(СН2)4
COOH
20. КоQ (коэнзим Q, убихинон)
Н3СОO
CH3
CH3
Н3СО
O
(СН2
СН
С
СН2)n
Н
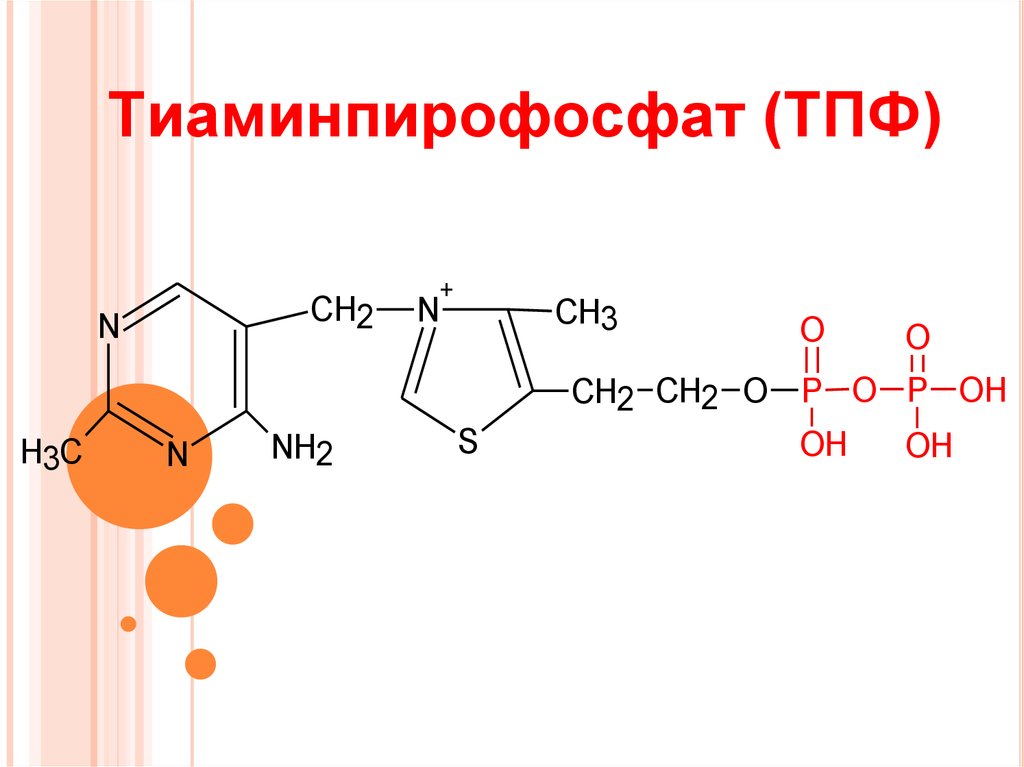
21. Тиаминпирофосфат (ТПФ)
CH2N
H3C
N
NH2
+
N
CH3
S
O
O
CH2 CH2 O P O P OH
OH
OH
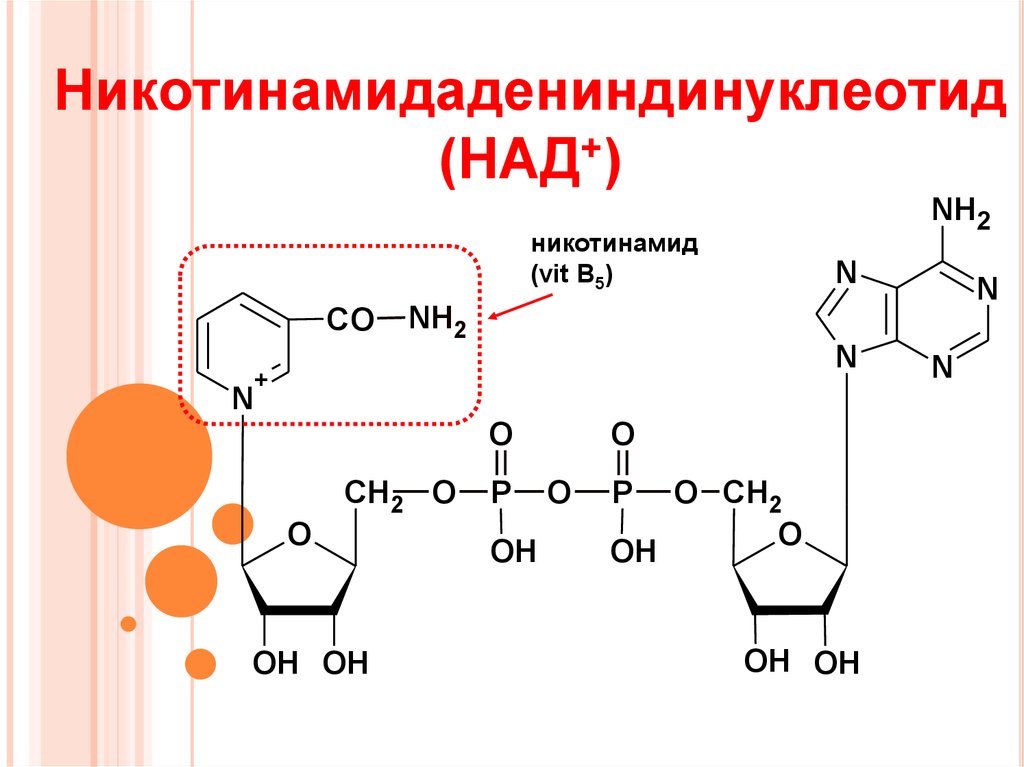
22. Никотинамидадениндинуклеотид (НАД+)
NH2никотинамид
(vit B5)
CO
N
N
NH2
N
+
O
СН2 O
O
OH OH
N
P
OH
O
O
P
OH
O СН2
O
OH OH
N
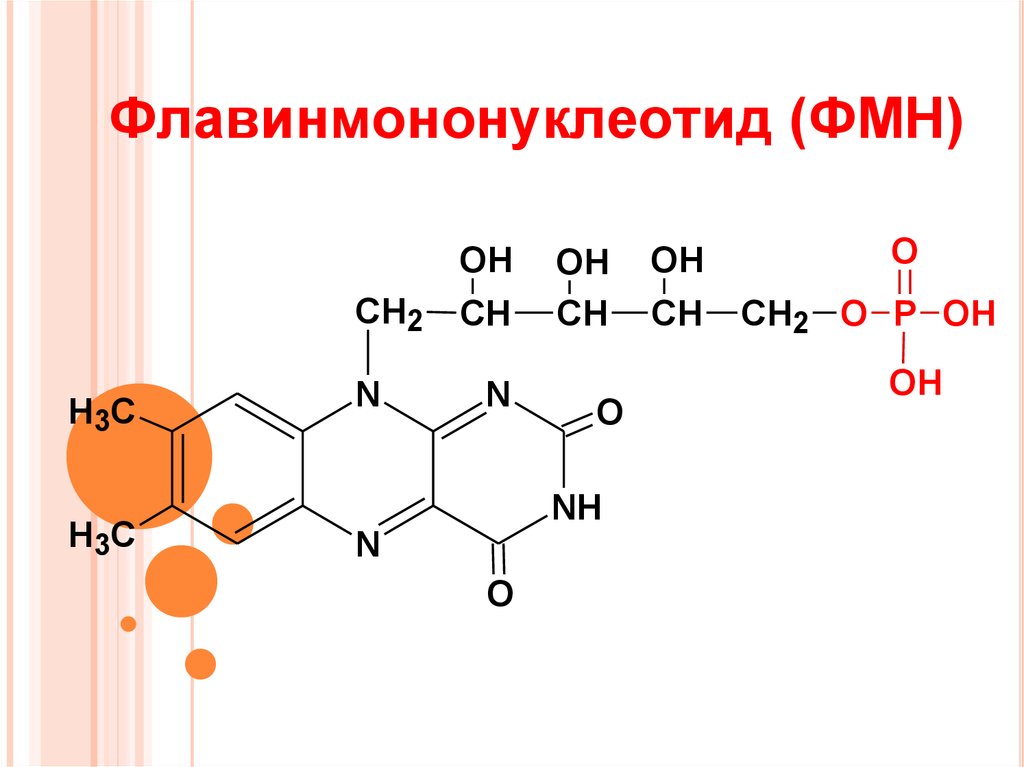
23. Флавинмононуклеотид (ФМН)
OHCH2
H3C
H3C
N
CH
N
OH
CH
O
NH
N
O
OH
CH
O
CH2 O P OH
OH
24. По выполняемым функциям
1. Переносчики протонов иэлектронов (НАД, ФАД, Ко Q);
2. Переносчики групп (ТПФ,
ПФ, КоА);
3. Коферменты синтеза и
изомеризации
25. По механизму действия
1. Коферменты с высокимпотенциалом переноса энергии
(переносчики энергии);
2. Коферменты, участвующие в
окислительновосстановительных реакциях;
3. Коферменты, формирующие
активный центр фермента.
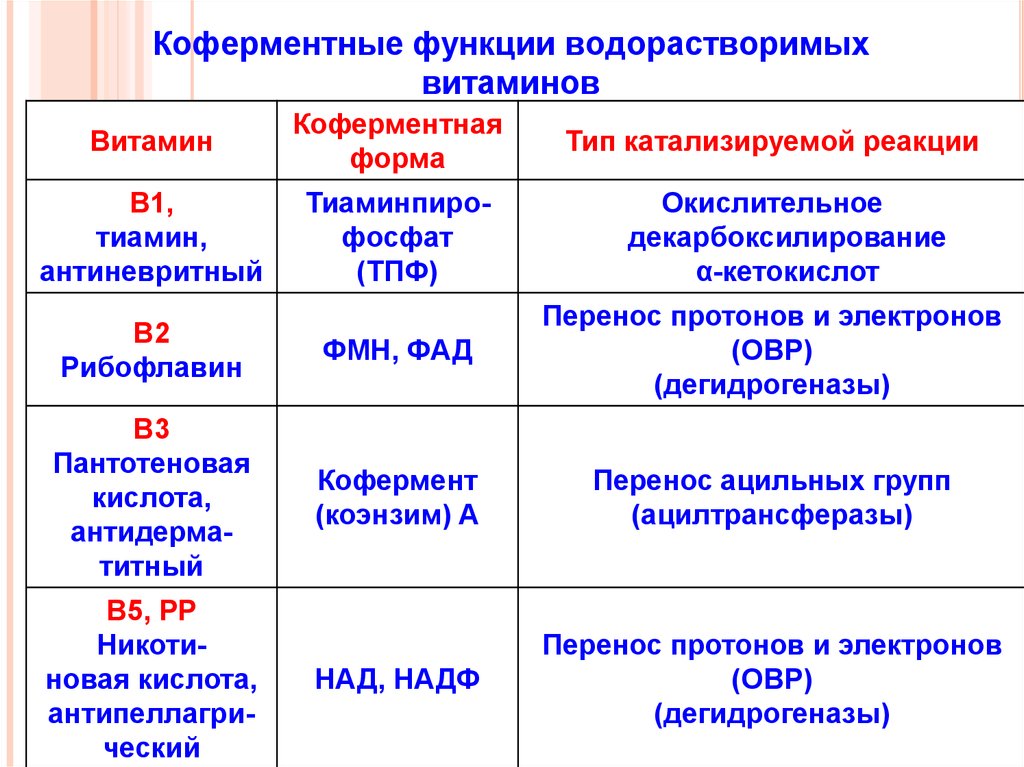
26. Коферментные функции водорастворимых витаминов
ВитаминКоферментная
форма
В1,
тиамин,
антиневритный
Тиаминпирофосфат
(ТПФ)
Тип катализируемой реакции
Окислительное
декарбоксилирование
α-кетокислот
В2
Рибофлавин
ФМН, ФАД
Перенос протонов и электронов
(ОВР)
(дегидрогеназы)
B3
Пантотеновая
кислота,
антидерматитный
Кофермент
(коэнзим) А
Перенос ацильных групп
(ацилтрансферазы)
НАД, НАДФ
Перенос протонов и электронов
(ОВР)
(дегидрогеназы)
B5, PP
Никотиновая кислота,
антипеллагрический
27.
В6Пиридоксин,
антидерматитный
Пиридоксальфосфат
(ПФ)
Перенос аминогрупп
(трансаминазы) и
декарбоксилирование
(декарбоксилазы)
B 9, B c
Фолиевая
кислота,
антианемический
Тетрагидрофолат
(ТГФК)
Перенос
одноуглеродных групп
(метитрансферазы)
В12
Кобаламин,
антианемический
Дезоксиаденозилкобаламин,
метилкобаламин
Изомеразы,
метилтрансферазы
С
Аскорбиновая
кислота,
антискорбутный
Не известна
Реакции
гидроксилирования
(гидроксилазы)
H
Биотин,
антисеборейный
Биотин кофермент
Фиксация СО2
(карбоксилазы)
28. Классификация ферментов
1. ОксидоредуктазыА Н2 + В
А + В Н2
2. Трансферазы
А Х +В
А+ В Х
3. Гидролазы
А В + Н2О
А Н + В ОН
29.
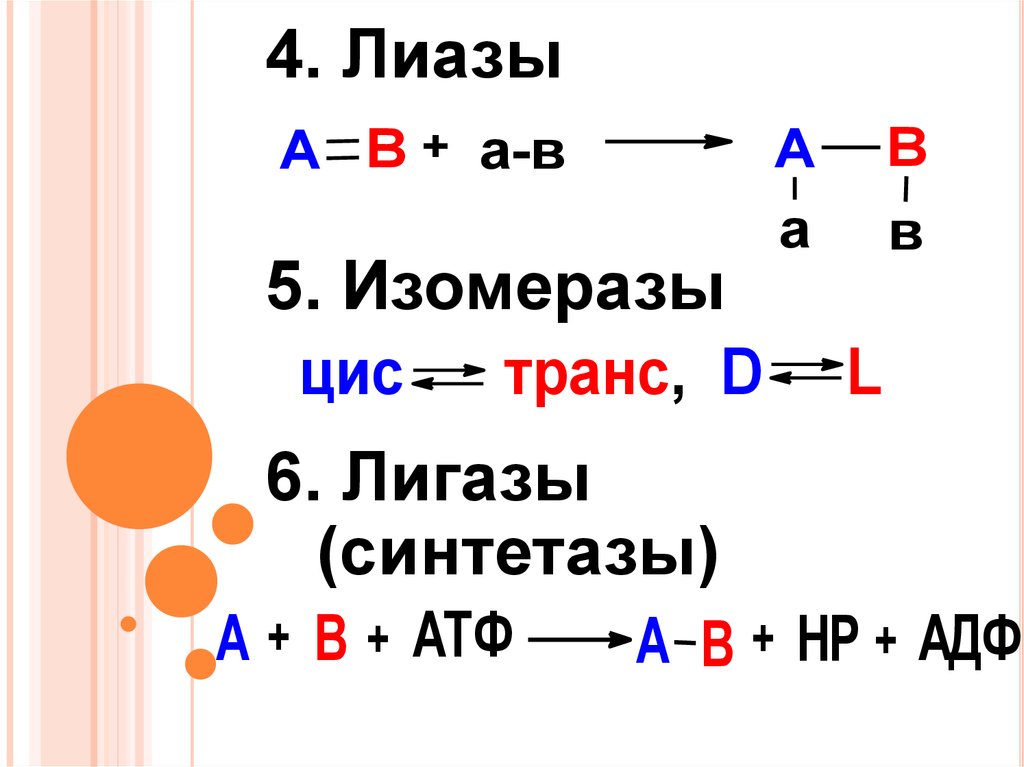
4. ЛиазыА В + а-в
5. Изомеразы
цис
транс, D
В
А
а
в
L
6. Лигазы
(синтетазы)
А + В + АТФ
А В + НР + АДФ
30.
класспод- катализируемая
класс
реакция
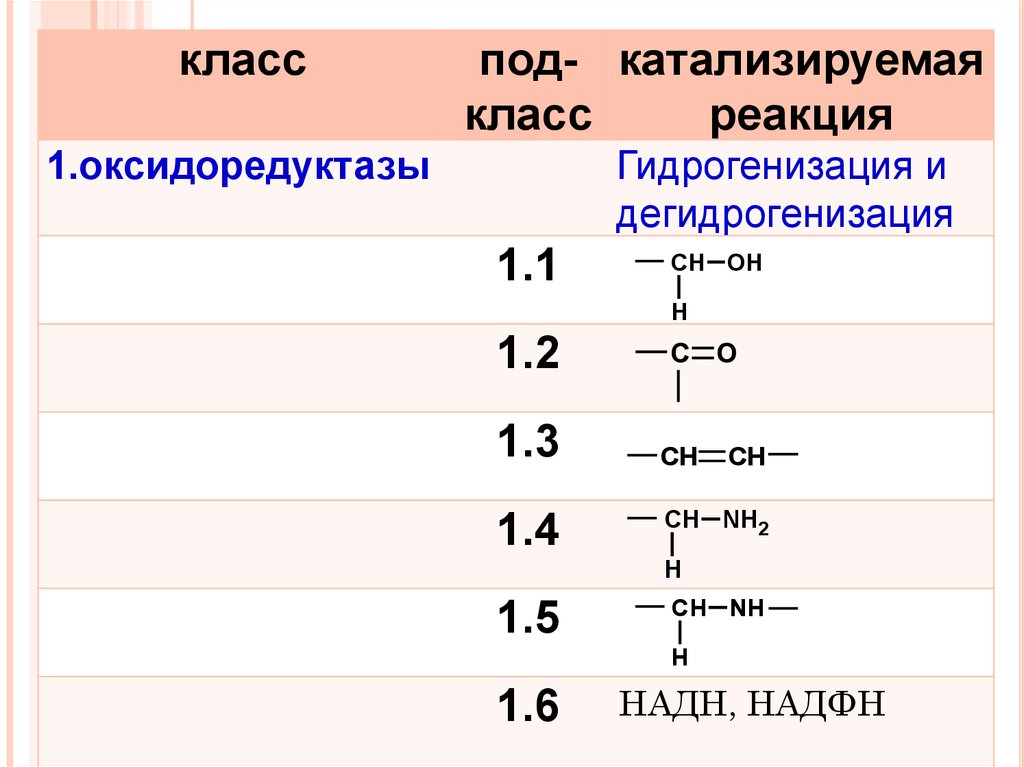
1.оксидоредуктазы
Гидрогенизация и
дегидрогенизация
1.1
СН OH
H
1.2
С O
1.3
СН
1.4
СН NH2
СН
H
1.5
СН NН
H
1.6
НАДН, НАДФН
31.
класспод- катализируемая реакция
класс
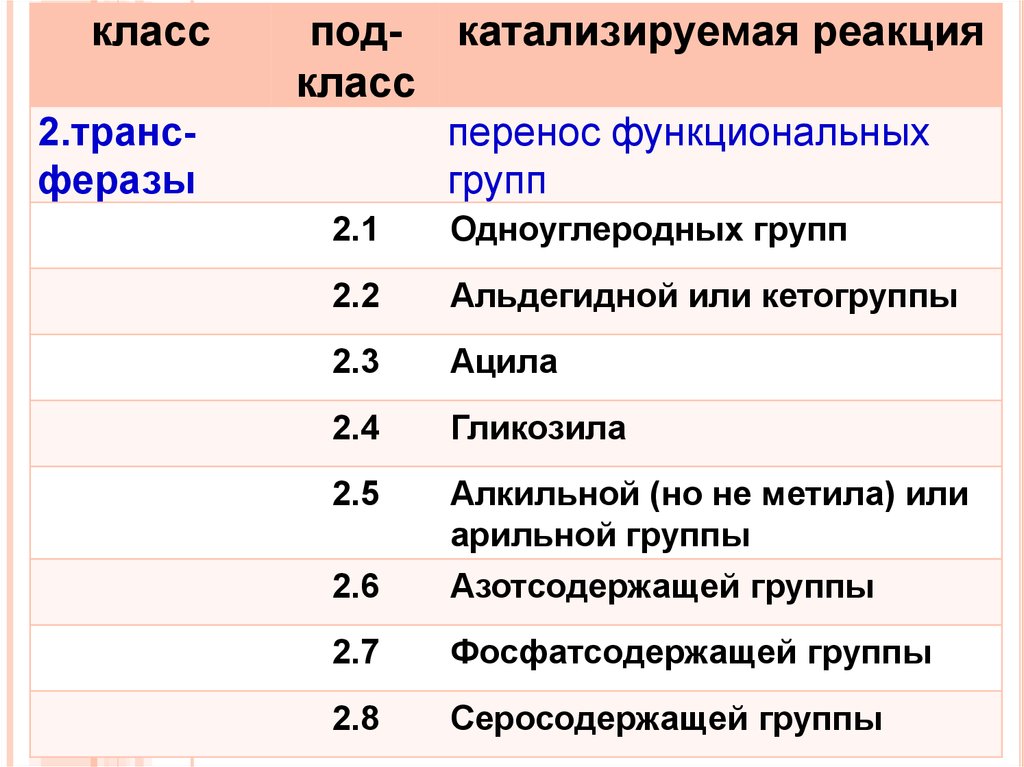
2.трансферазы
перенос функциональных
групп
2.1
Одноуглеродных групп
2.2
Альдегидной или кетогруппы
2.3
Ацила
2.4
Гликозила
2.5
Алкильной (но не метила) или
арильной группы
2.6
Азотсодержащей группы
2.7
Фосфатсодержащей группы
2.8
Серосодержащей группы
32.
классподкласс
3.гидролазы
катализируемая
реакция
гидролитические реакции
3.1
Сложных эфиров
3.2
Гликозидов
3.3
Простых эфиров
3.4
Пептидов
3.5
Других С—N-связей
3.6
Ангидридов кислот
33.
34.
OСН2О
СН2ОН
O
O
+ АТФ
OH
HO
HO
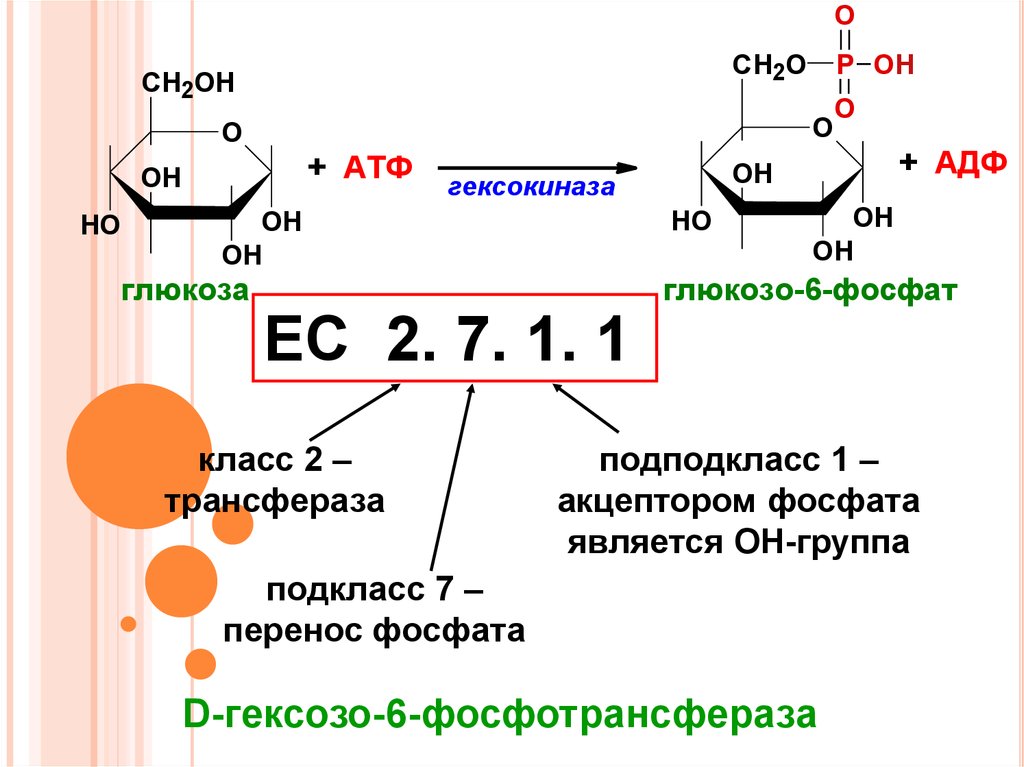
ЕС 2. 7. 1. 1
класс 2 –
трансфераза
O
+ АДФ
OH
гексокиназа
OH
OH
глюкоза
P OH
OH
OH
глюкозо-6-фосфат
подподкласс 1 –
акцептором фосфата
является ОН-группа
подкласс 7 –
перенос фосфата
D-гексозо-6-фосфотрансфераза
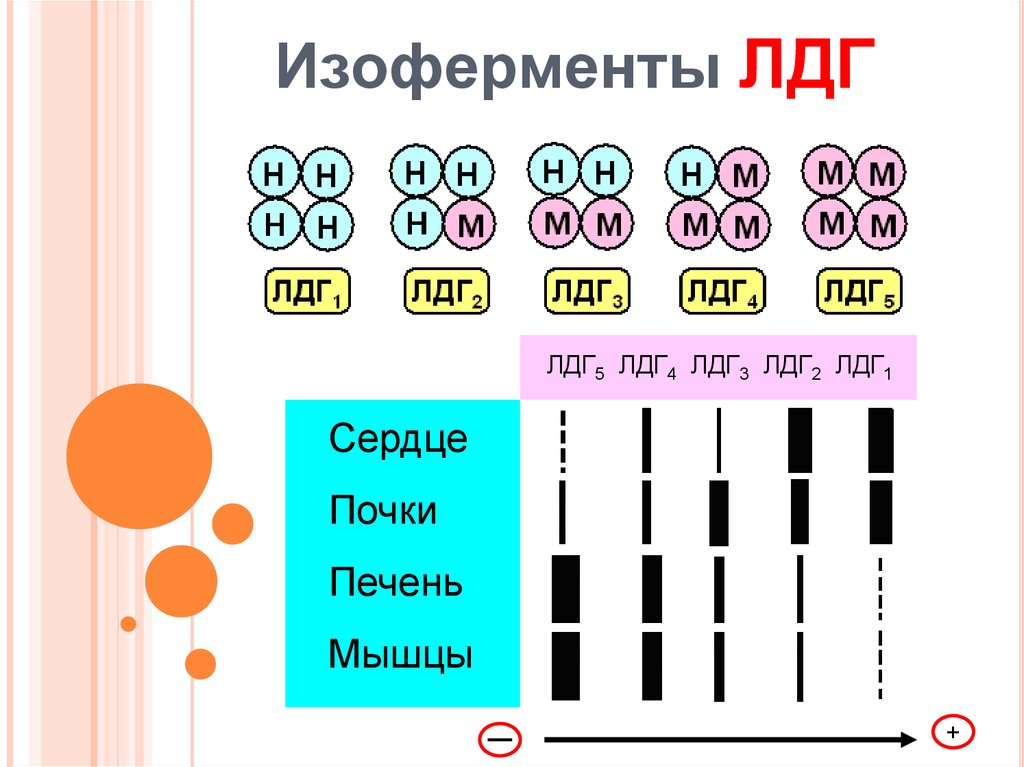
35. Изоферменты ЛДГ
ЛДГ5 ЛДГ4 ЛДГ3 ЛДГ2 ЛДГ1Сердце
Почки
Печень
Мышцы
+
36. Изоферменты креатинкиназы
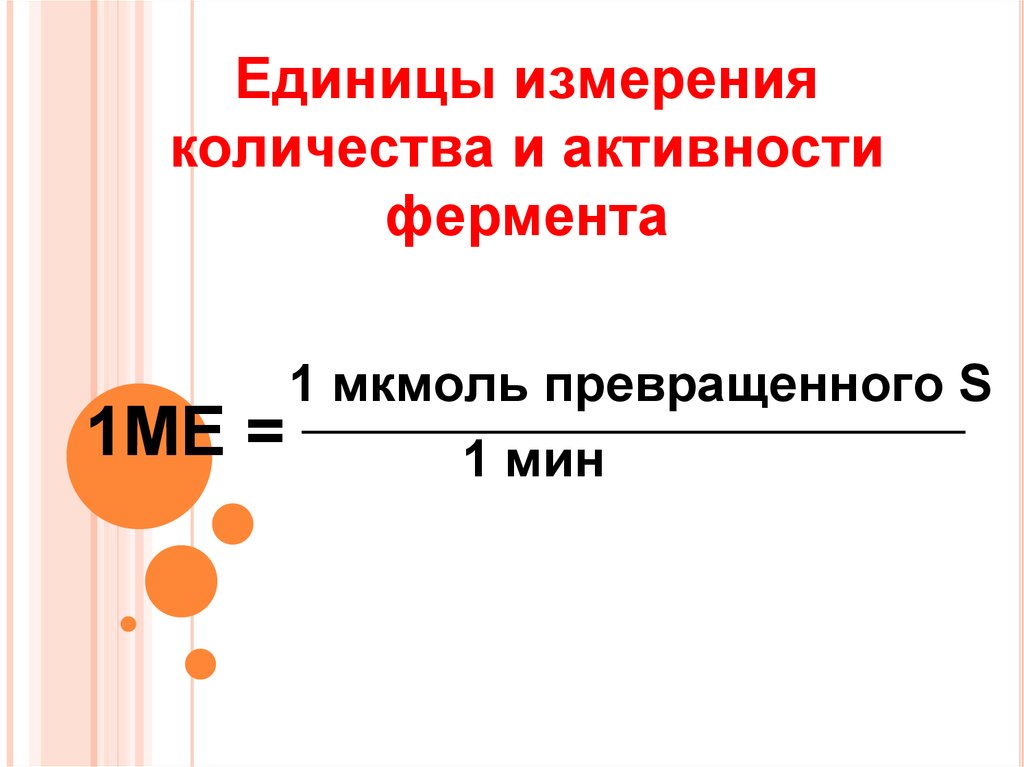
37. Единицы измерения количества и активности фермента
1МЕ1 мкмоль превращенного S
=
1 мин
38. nМЕ – количество единиц активности
Кол-во превращенного S (мкмоль)nМЕ =
Время (мин)
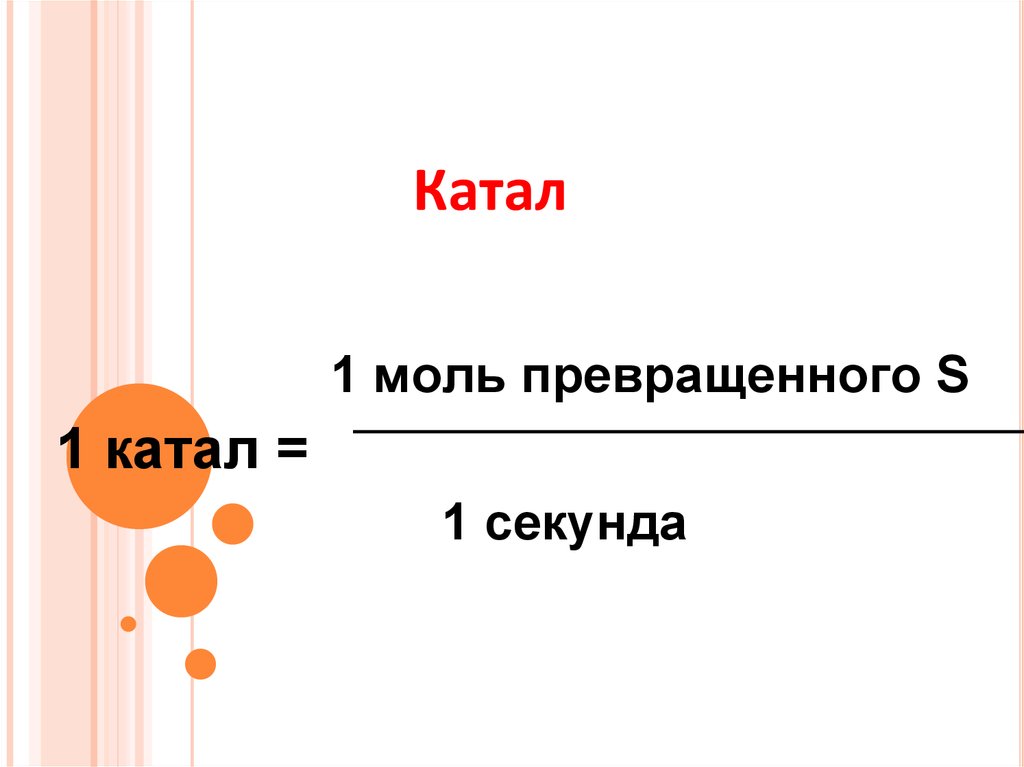
39. Катал
1 моль превращенного S1 катал =
1 секунда





















 biology
biology








