Similar presentations:
не ме
1. Неметаллы: общая характеристика.
2. Неметаллы – хим.элементы, для атомов которых характерна способность принимать электроны и малый атомный радиус по сравнению с
металлами.3.
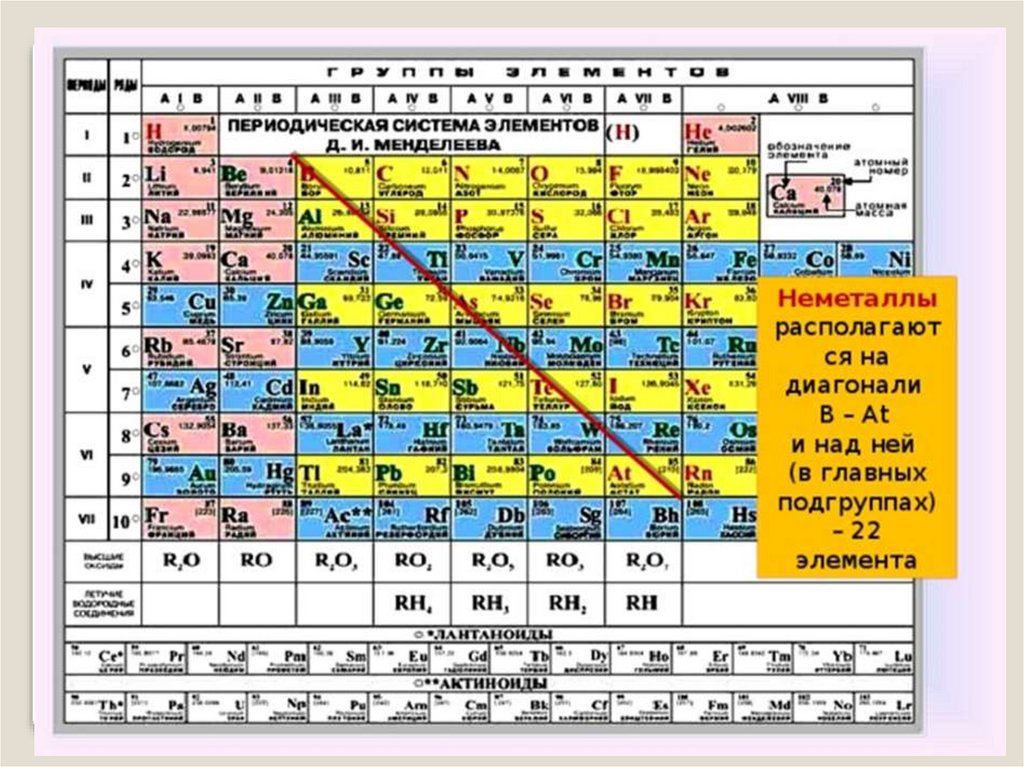
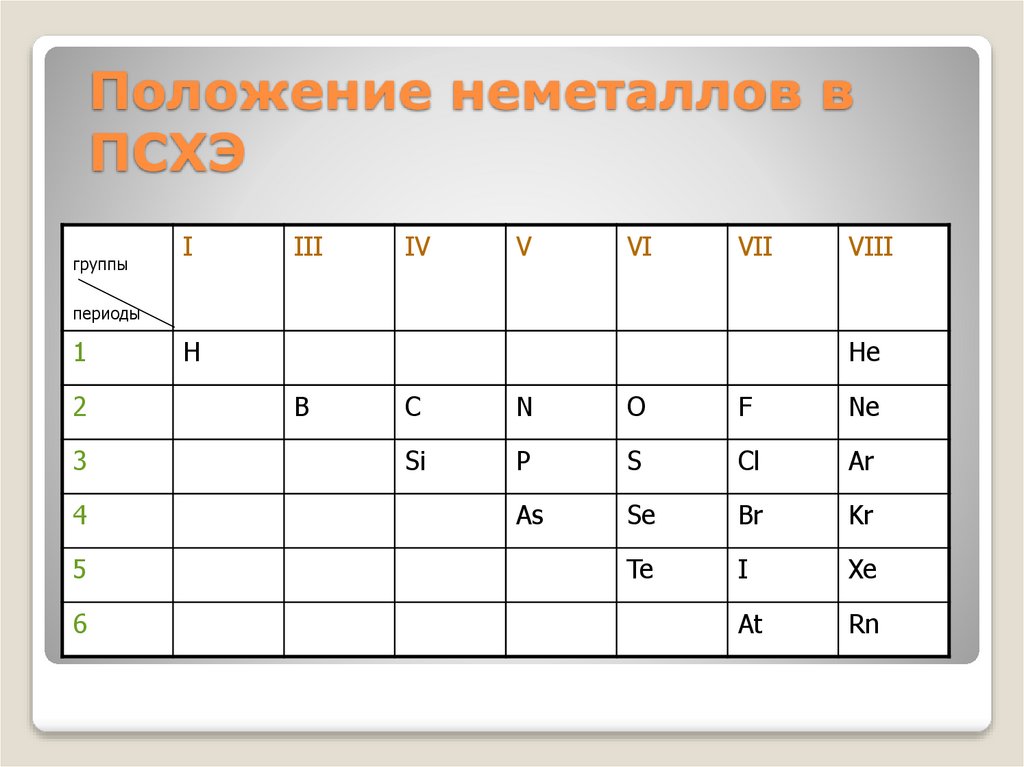
4. Положение неметаллов в ПСХЭ
группыI
III
IV
V
VI
VII
VIII
периоды
1
2
3
4
5
6
H
He
B
C
N
O
F
Ne
Si
P
S
Cl
Ar
As
Se
Br
Kr
Te
I
Xe
At
Rn
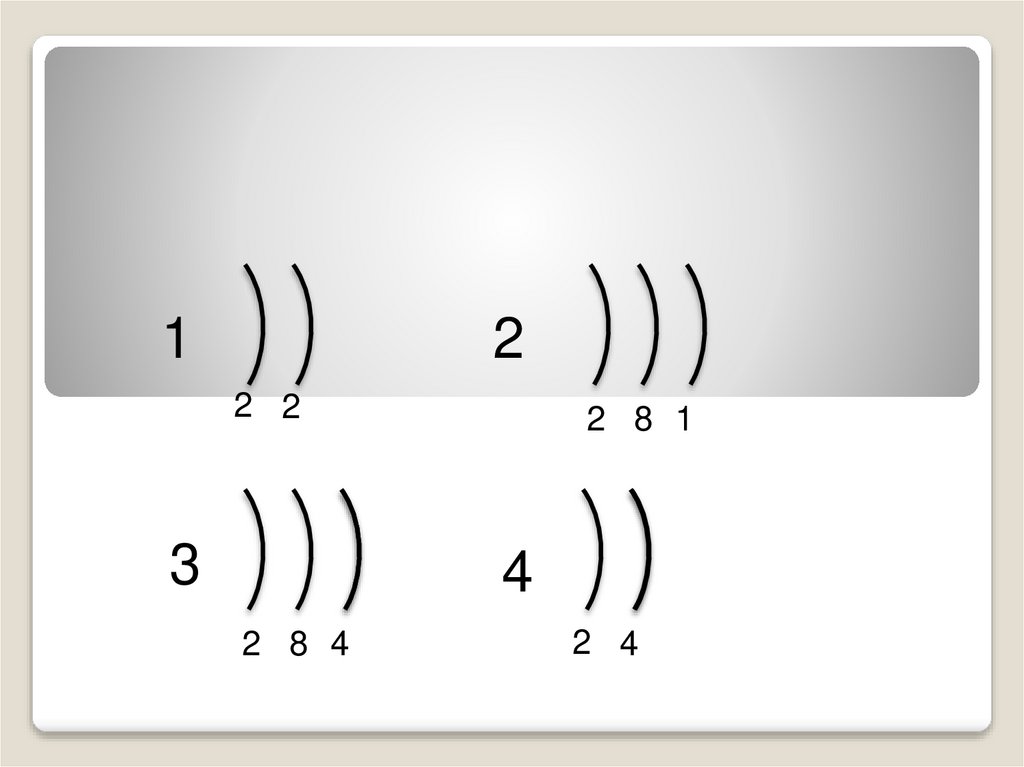
5.
12
2 2
3
2 8 1
4
2 8 4
2 4
6.
Небольшой атомный радиусНа внешнем уровне 4-8 электронов
Характерно высокое значение ЭО
Являются окислителями
7. Электронная формула атомов неметаллов
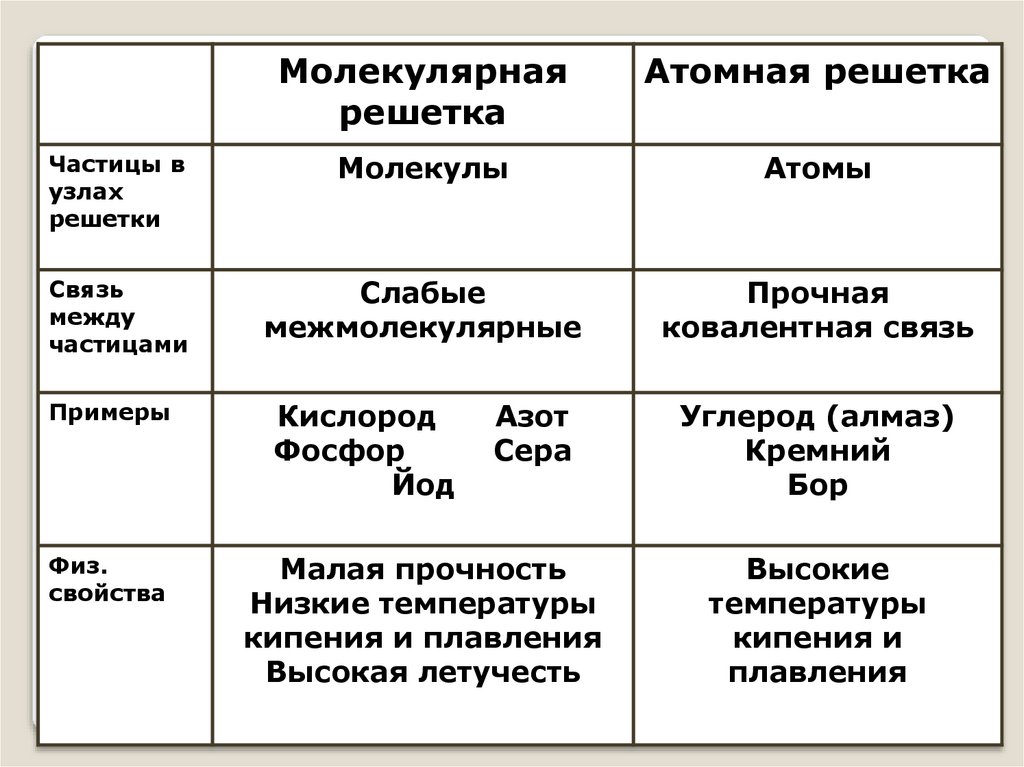
8. Типы кристаллических решеток
Молекулярнаярешетка
Атомная решетка
Частицы в
узлах
решетки
Молекулы
Атомы
Связь
между
частицами
Слабые
межмолекулярные
Прочная
ковалентная связь
Примеры
Кислород
Фосфор
Йод
Углерод (алмаз)
Кремний
Бор
Азот
Сера
Малая прочность
Высокие
Низкие температуры
температуры
кипения и плавления
кипения и
Типы кристаллических
решеток
Высокая летучесть
плавления
Физ.
свойства
9. ФИЗИЧЕСКИЕ СВОЙСТВА ПРОСТЫХ ВЕЩЕСТВ неМе
10.
КРАСНЫЙЖЕЛТЫЙ
ФИОЛЕТОВЫЙ
ФОСФОР
СЕРА
ЙОД
БЕСЦВЕТНЫЙ
УГЛЕРОД
11.
БЕЛЫЙЧЕРНЫЙ
ФОСФОР
ГРАФИТ
ФОСФОР
ЖЕЛТО-ЗЕЛЕНЫЙ
ХЛОР
12.
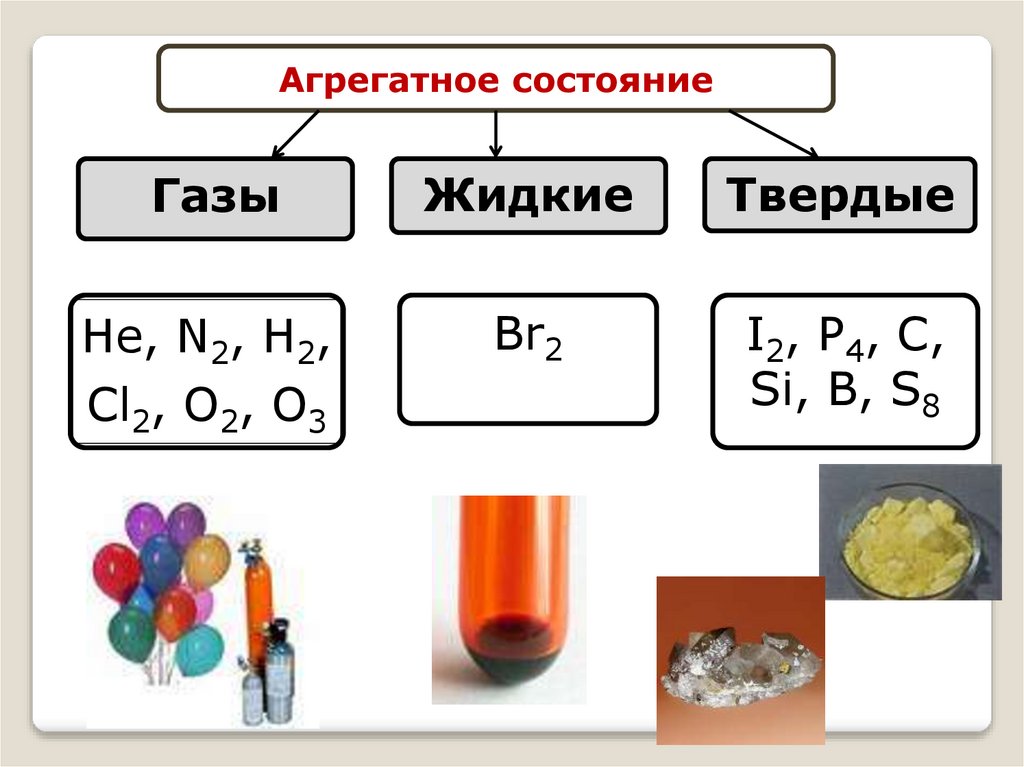
Агрегатное состояниеГазы
Жидкие
Твердые
Не, N2, Н2,
Cl2, O2, O3
Br2
I2, P4, C,
Si, B, S8
13. Газы – неметаллы – двухатомные молекулы
Н2О2
Cl2
N2
F2
Газы – неметаллы –
двухатомные молекулы
14. Температура плавления
3 8000 С – у графита- 2100 С - азота
Температура плавления
15. Способность атомов одного хим. элемента образовывать несколько простых веществ называют аллотропией, а эти простые вещества –
аллотропнымимодификациями
16.
Разное типыкристаллических решеток
Р - фосфор
Красный фосфор - атомная
Белый фосфор - молекулярная
17.
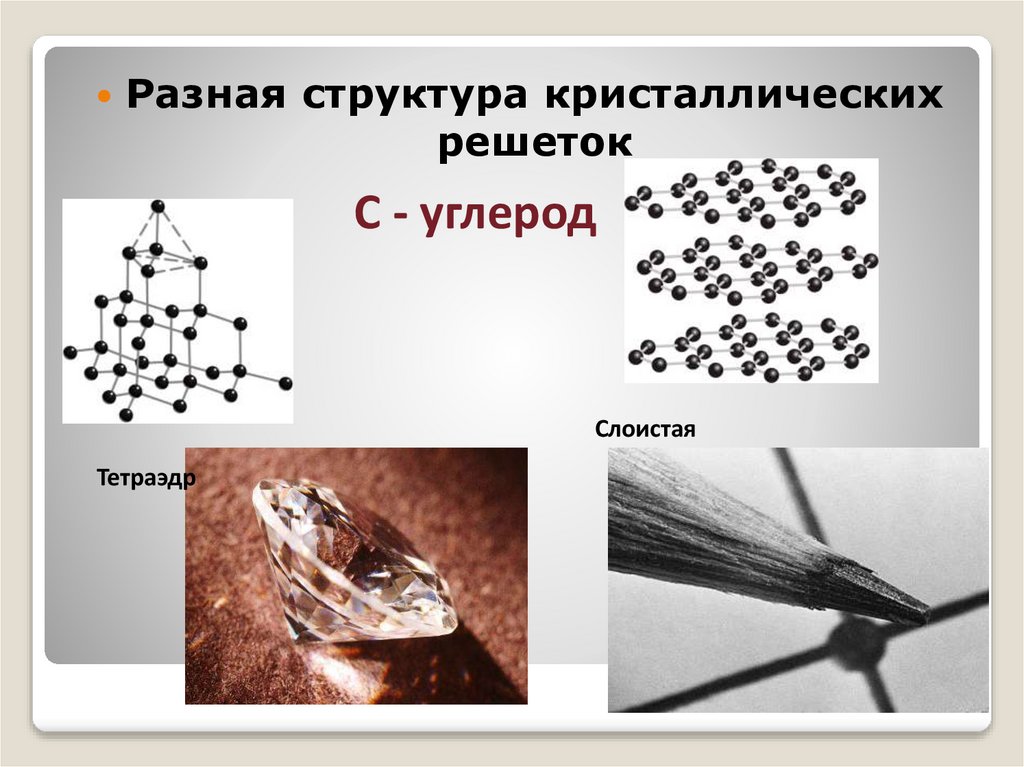
Разная структура кристаллическихрешеток
С - углерод
Слоистая
Тетраэдр
18.
Разный состав молекулО - кислород
Кислород
Озон
19.
• Задерживает ультрафиолетовыелучи, которые разрушительно
действуют на клетки живых
организмов
• Озоновый слой расположен на
высоте 20 – 25 км
20. Озон О3
Светло - синий газ с сильнымзапахом
Имеет запах свежести
Появляется после грозы
Озон О3
21. Озон в природе
Содержится в воздухе сосновыхлесов и морского побережья
Озон в природе
22. Получение озона в лаборатории
Получают в специальных приборах– озонаторах при действии на
кислород электрическим разрядом
без искр
Получение озона в лаборатории
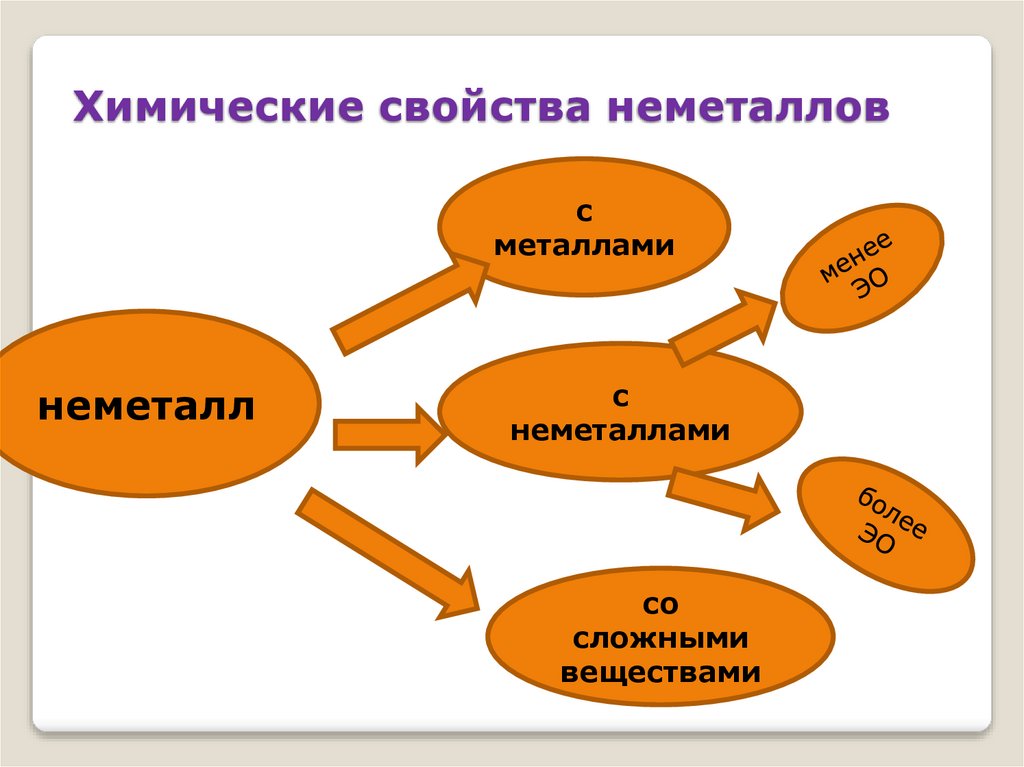
23. Химические свойства неметаллов
сметаллами
неметалл
с
неметаллами
со
сложными
веществами
24.
Характерными для большинстванеметаллов являются окислительные
свойства. Как окислители они
реагируют
с металлами:
Ca + Cl2 = CaCl2
4Li + O2 = 2Li2O
2Na + S = Na2S
25.
с неметаллами:H2 + S = H2S
P4 + 5O2 = 2P2O5
2P + 5Cl2 = 2PCl5
со сложными веществами:
2FeCl2 + Cl2 = 2FeCl3
СН4 + Cl2
=СН3Cl+НCl
26.
ДОМАШНЕЕ ЗАДАНИЕСоставить сообщение по одной
из тем (по выбору)
«Распространение неметаллов
в природе»
«Биологическая роль
неметаллов»
«Применение неметаллов»



















 chemistry
chemistry








