Similar presentations:
UF-spektroskopia
1.
Оптическая спектроскопия – УФ2. УФ спектроскопия
ИсторияВ 1801 году немецкий физик Иоганн
Вильгельм Риттер начал поиски излучения с
противоположного конца видимого спектра, с
длинами волн короче, чем у излучения
фиолетового цвета.
Ученые, пришли к соглашению, что свет состоит
из трех отдельных компонентов: окислительного
или теплового (инфракрасного) компонента,
осветительного компонента (видимого света), и
восстановительного
(ультрафиолетового)
компонента.
3. УФ спектроскопия
Источники УФ-излученияОсновной естественный источник УФ-излучения на Земле – Солнце.
Искусственные источники УФ-излучения:
Лампа
• Эритемные лампы
• Ртутно-кварцевые лампы
• Люминесцентные лампы
• Эксилампы
Светодиод
Лазер
4. УФ спектроскопия
ИсторияВ начале 1940-х годов вышла серия статей
Роберта Бёрнса Вудворда, описывающая
применение УФ-спектроскопии в объяснении
структуры природных продуктов.
Вудворд собрал большое количество
эмпирических данных и разработал ряд
правил, позднее названных «правилами
Вудворда», которые могли применяться
для выяснения структур как природных
веществ, так и синтезированных молекул.
5. УФ спектроскопия
γ-лучирентген
видимый
свет
(электронная)
УФ
радио
микро
волны
волны
спектроскопия
– раздел
ИК
УФ-В
Ультрафиолетовая
оптической спектроскопии, который включает получение,
УФ
в
исследование ивакууме
применение
спектров испускания, поглощения
УФ-С
УФ-А
и отражения в ультрафиолетовой области.
В УФ-области поглощают все органические вещества.
Если вещество окрашено, то в его спектре наблюдаются
полосы поглощения в видимой области.
Необходимые для исследования
невелики – около 0,1 мг.
количества
вещества
6.
УФ спектроскопия7.
УФ спектроскопия8.
9.
10. УФ спектроскопия
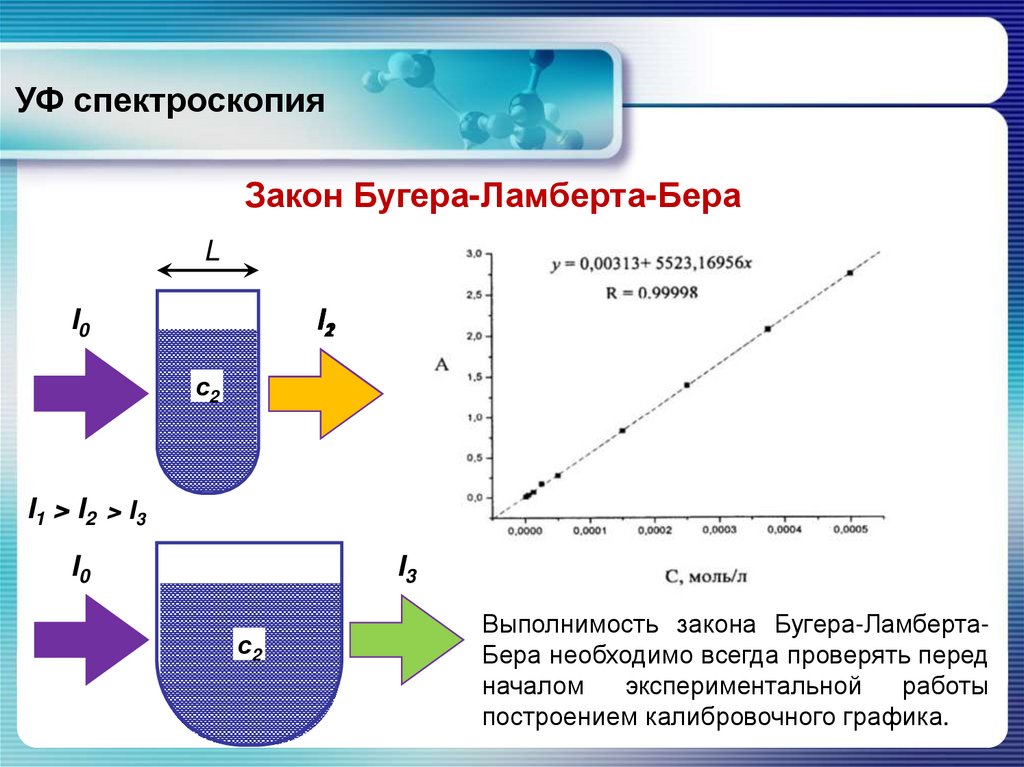
Закон Бугера-Ламберта-БераL
lg(I0/I) = e L c – закон Бугера-Ламберта-Бера
I0
I21
где e – молярный коэффициент поглощения,
L – толщина (путь), c – концентрация
сс2
T=I/I0 – коэффициент пропускания
А= –lg(T) = –lg(I/I0) – оптическая плотность
I1 > I2 > I3
А = e L c - закон светопропускания
I0
I3
с2
Выполнимость закона Бугера-ЛамбертаБера необходимо всегда проверять перед
началом
экспериментальной
работы
построением калибровочного графика.
11. УФ спектроскопия
Закон Бугера-Ламберта-БераЗакон Бугера-Ламберта-Бера строго справедлив
разбавленных растворов и в определенных условиях:
только
для
• постоянство состава и неизменность поглощающих частиц в
растворе
• исследуемые молекулы должны быть диспергированы до
молекулярного уровня, они не должны рассеивать свет и
взаимодействовать друг с другом
• монохроматичность и параллельность проходящего через раствор
лучистого потока небольшой интенсивности
• постоянство температуры
12. Спектрофотометры видимого и ультрафиолетового диапазонов
13. Спектрофотометры видимого и ультрафиолетового диапазонов
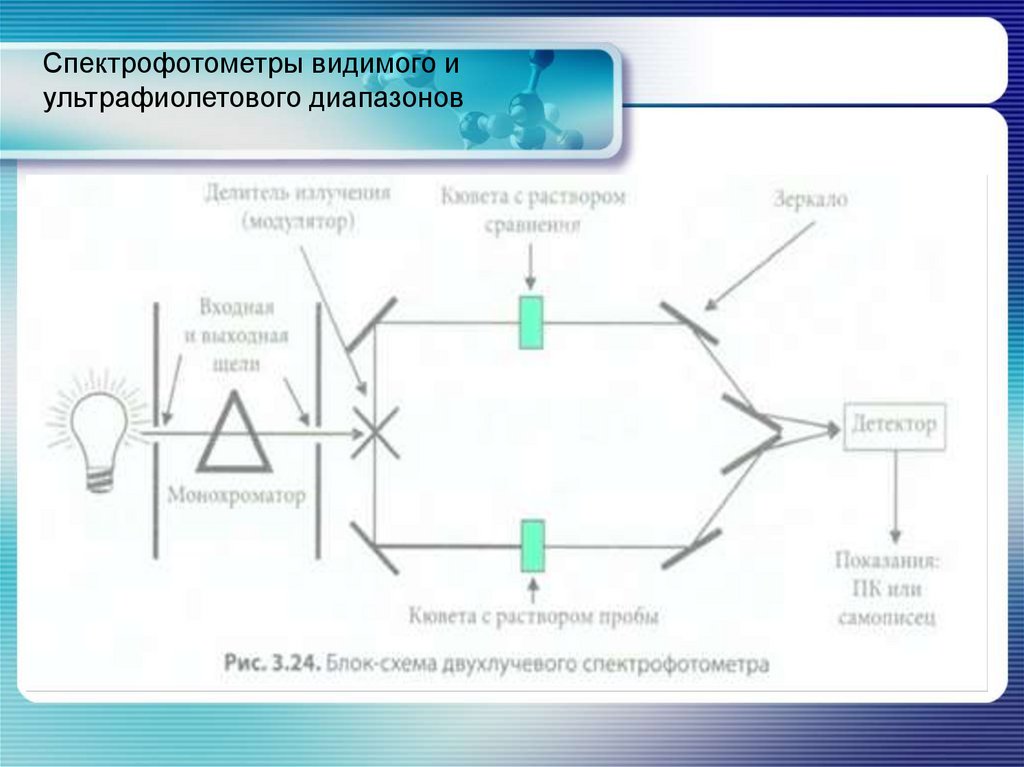
Для измерения абсорбции излучения в зависимости от длины волныпадающего света в настоящее время обычно применяют двухлучевые
спектрофотометры (рис. 3.24). Из испускаемого полихроматического
излучения (непрерывного спектра в широком диапазоне длин волн) с
помощью монохроматора выделяют излучение только с определенной
длиной волны λ (монохроматическое излучение) и интенсивностью l0,
после чего специальными приспособлениями направляют его на образец.
Образец при этом помещают в маленькую емкость, кювету. В этом
растворе излучение частично поглощается, а интенсивность излучения /,
прошедшего через раствор, регистрируется детектором. На
регистрирующее устройство передается значение величины оптической
плотности, которое по закону Ламберта — Бера пропорционально
концентрации аналита.
14. Источники излучения, применяемые в современных спектрофотометрах
В качестве источников излучения в современных спектрофотометрах, какправило, используют две разновидности ламп:
газоразрядную дейтериевую лампу, используемую для излучения УФдиапазона
(дейтерий D2; длины волн между 180 и 370 нм);
галогенную вольфрамовую лампу, испускающую излучение видимого
диапазона (X = 360-800 нм).
В зависимости от положения зеркала на пробу подается излучение либо
видимого, либо УФ-диапазона.
15. Кюветы, применяемые в спектроскопии видимого и ультрафиолетового диапазонов
Так как в спектроскопии видимого и УФ-диапазонов проводят анализ толькожидких проб, то для последних требуются специальные емкости — кюветы. Их
изготовляют из материала, который не поглощает излучение в исследуемом
диапазоне длин волн.
Кюветы, изготовленные из полимерных материалов и стекла,
можно использовать в диапазоне длин волн λ > 350 нм (видимый
диапазон).
В УФ-диапазоне (λ = 200-400 нм) следует использовать кварцевые
кюветы, так как обычное оконное стекло или органические полимеры
обладают слишком высокой собственной абсорбцией.
Специальные полимерные кюветы можно использовать в
диапазоне длин волн от λ = 220 нм.
Кюветы являются составной частью оптической системы и требуют крайне
бережного обращения (впрочем, как и любые другие элементы оптической
системы).
16. Детекторы
Детекторы предназначены для измерения интенсивностипоступающего излучения.
В спектроскопии видимого и УФ-диапазонов в их качестве чаще
всего выступают фотоэлектронные умножители (также
называемые вторичными электронными умножителями (ВЭУ) и
фотодиоды.
Современные технологии позволяют производить очень компактные
фотодиоды, что делает возможным изготовление фотодиодной
матрицы. Так, в настоящее время один конструктивный элемент
может содержать от 64 до 4096 фотодиодов. Поскольку каждый
фотодиод способен измерять интенсивность / определенных длин
волн λ, то при использовании фотодиодной матрицы можно
одновременно определять интенсивности большого количества
длин волн.
17. Растворители, применяемые в спектроскопии видимого и ультрафиолетового диапазонов
Как правило, для проведения анализаРастворители для спектроскопии
определяемое вещество растворяют в
видимого и УФ-диапазонов (нижнее
подходящем растворителе.
значение длины волны)
Растворители, применяемые в спектроскопии
видимого и УФ-диапазонов, должны отвечать
Растворитель
Наименьшее значение
следующим требованиям:
длины волны λ в нм
Вода
190 не содержать взвесей во избежание
рассеивания излучения на частицах;
Этанол
210
(неденатурированный)
не поглощать слишком сильно излучение в
н-Гексан
195
диапазоне измерений.
Диэтиловый
215
К сожалению, большинство растворителей
эфир
Ацетон
330 сильно абсорбируют излучение в
1,4-Диоксан
220 коротковолновом УФ-диапазоне (табл. 3.12).
Приведенные в таблице растворители не могут
Метанол
205
быть использованы при длинах волн
Ацетонитрил
190
излучения, меньших некоторого предельного
Хлороформ
240 значения, поскольку в этих пределах они
обладают слишком интенсивной собственной
абсорбцией.
18. Спектрофотометры видимого и ультрафиолетового диапазонов
Спектрофотометрия используется для:идентификации соединений,
исследования состава,
исследования строения,
количественного анализа индивидуальных веществ
и многокомпонентных систем.
Кривая зависимости поглощения (функция поглощения)
от длины волны или волнового числа называется
спектром поглощения вещества и является
специфической характеристикой данного вещества
19. Спектрофотометры видимого и ультрафиолетового диапазонов
Однако главным достоинствомспектрофотометра является возможность
сканировать полный диапазон длин волн в УФ
и видимой области и получать спектры
поглощения.
Спектры отражают зависимость поглощения
от длины волны.
Спектры поглощения – это результат
определенных электронных переходов. Чаще
всего это π-электроны, участвующие в
образовании двойных связей углерод-углерод,
а также электроны неподеленных электронных
пар азота и кислорода.
Длина волны поглощаемого света
определяется соответствующими электронными
переходами, поэтому специфические пики
поглощения можно связать с известными
молекулярными фрагментами
20. УФ спектроскопия
Электронная спектроскопия изучает электронные переходы междувалентными молекулярными орбиталями.
Поглощение фотонов УФ диапазона атомами или молекулами,
приводит к переходам между их энергетическими состояниями.
Разность энергий ΔЕ между этими состояниями квантована, поэтому
молекулы поглощают фотоны только строго определенной энергии.
Молекулы в возбужденном состоянии, могут терять избыток энергии:
• Разрыв связи
• Испускание
• Флуоресценция
• Фосфоресценция
• Безизлучательные переходы
21. УФ спектроскопия
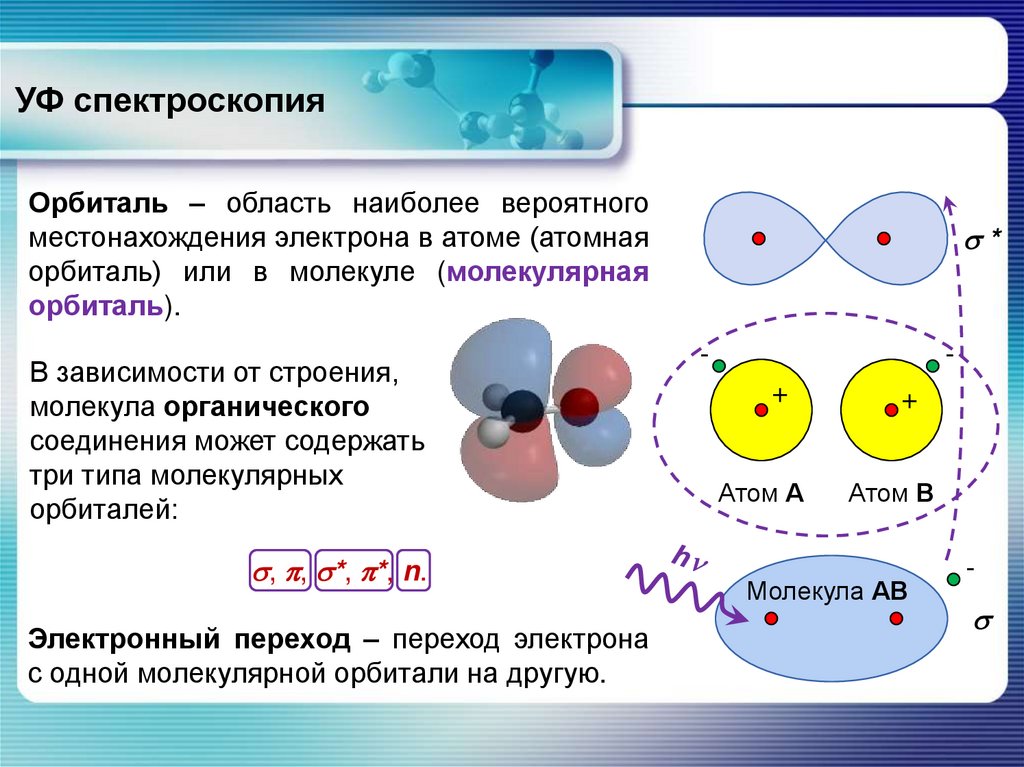
Орбиталь – область наиболее вероятногоместонахождения электрона в атоме (атомная
орбиталь) или в молекуле (молекулярная
орбиталь).
В зависимости от строения,
молекула органического
соединения может содержать
три типа молекулярных
орбиталей:
,, *,, *,
, **,иn.
n.
Электронный переход – переход электрона
с одной молекулярной орбитали на другую.
*
-
+
+
Атом А
Атом В
Молекула АВ
-
22. УФ спектроскопия
Типы молекулярных орбиталейСвязывающие орбитали. Образуются в результате перекрывания
атомных орбиталей двух соседних атомов. На связывающих - и орбиталях, соответственно, находятся -электроны одинарных (C–C,
C–H, C–O, C–N, C–S, C–Hal и др.) и -электроны кратных связей (С=С,
С=N, C=O, C≡C, C≡N и др.).
Несвязывающие орбитали. Молекулы, содержащие гетероатомы с
неподелёнными электронными парами (O:, N:, S:, Hal: и др.), имеют nорбитали несвязывающих неподелённых пар электронов, существенно
не участвующих в образовании химической связи.
Разрыхляющие орбитали. Связывающим орбиталям соответствуют
разрыхляющие орбитали * и *. Электроны на них «разрыхляют»
химическую связь (т.е. способствуют разъединению молекулы).
23.
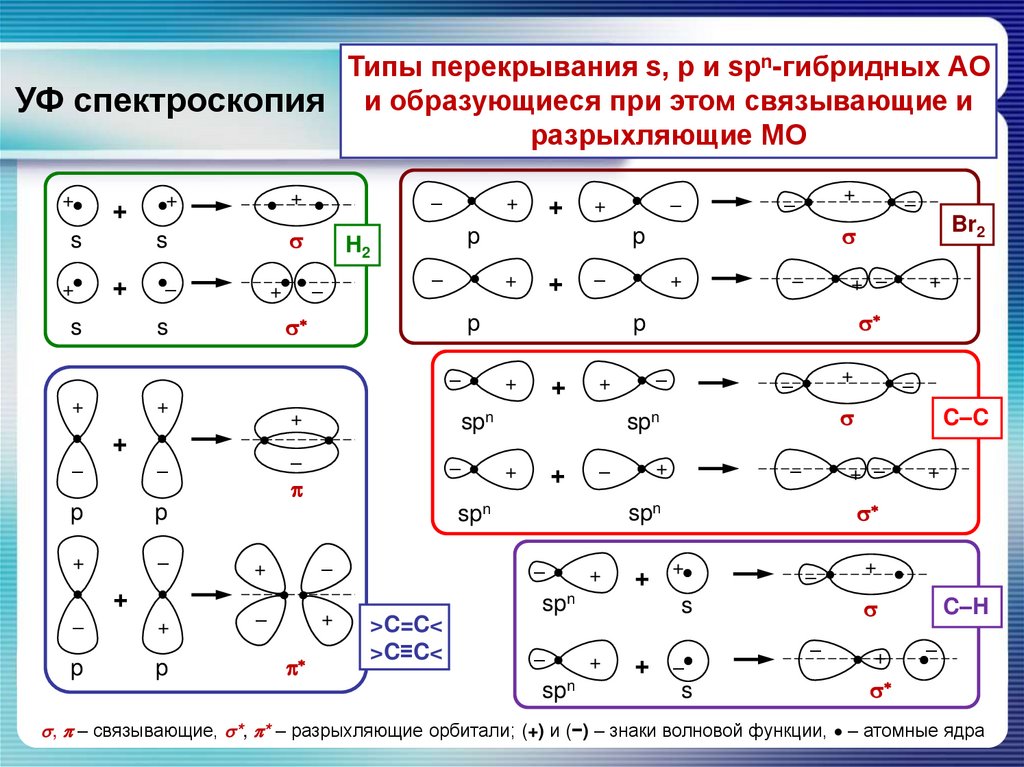
Типы перекрывания s, p и spn-гибридных АОУФ спектроскопия и образующиеся при этом связывающие и
разрыхляющие МО
+
+
s
+
+
s
+
+
s
–
–
–
+
+
+
+
–
–
–
p
p
+
–
+
–
–
+
–
+
p
p
*
+
–
+
+
+
–
+
–
–
+
+
+
spn
–
spn
+
C–C
+
*
+
–
–
s
+
s
+
–
+ –
spn
–
+
spn
+
Br2
*
–
+
–
+ –
p
spn
>C=C<
>C≡C<
+
–
–
spn
–
+
+
p
–
–
+
p
+
*
s
+
p
H2
–
+
+
–
+
C–H
–
*
, – связывающие, *, * – разрыхляющие орбитали; (+) и (−) – знаки волновой функции, • – атомные ядра
24. УФ спектроскопия
Электронные переходыЕ
→ *, → *, n→ *, n→ *
* - МО
* - МО
*
Возбужденное
состояние
*
*
n
*
n
n - МО
Е
- МО
- МО
Основное
состояние
В результате
поглощения
ультрафиолетового
и видимого излучения
происходит переход
валентного электрона с
занимаемого им уровня
на уровень с более
высокой энергией.
Е=1.8-6.2 эВ
=100-800 нм
25. УФ спектроскопия
Электронные переходы – правила отбора1. По симметрии: разрешены переходы между орбиталями такой симметрии,
которые могут перекрываться в пространстве; если орбитали ортогональны,
то переходы между ними запрещены (например, n→ * в соединениях с
группами C=O, C=S, C=N, NO).
2. По спину: запрещены переходы с изменением спина электрона, т.е. между
состояниями различной мультиплетности (с поворотом электрона).
3. По числу возбужденных электронов: запрещены переходы, при которых
происходит возбуждение более чем одного электрона.
26.
УФ спектроскопияУФ-спектроскопия является одним из распространенных физикохимических методов исследования органических и неорганических
соединений.
Спектрофотометрический анализ может быть проведен для
органических веществ, обладающих определенными особенностями
строения (ароматические соединения, соединения с сопряженными
кратными связями, соединения ряда металлов и др.).
Величина поглощенного излучения прямо пропорциональна числу
молекул растворенного вещества и поэтому возрастает с увеличением
концентрации.
Электронные спектры (спектры в ультрафиолетовой и видимой
областях) представляют собой зависимость поглощения излучения от
длины волны излучения.
27. УФ спектроскопия
Оптическая плотностьУФ спектроскопия
1
макс
полоса
поглощения
2
Длина волны, нм
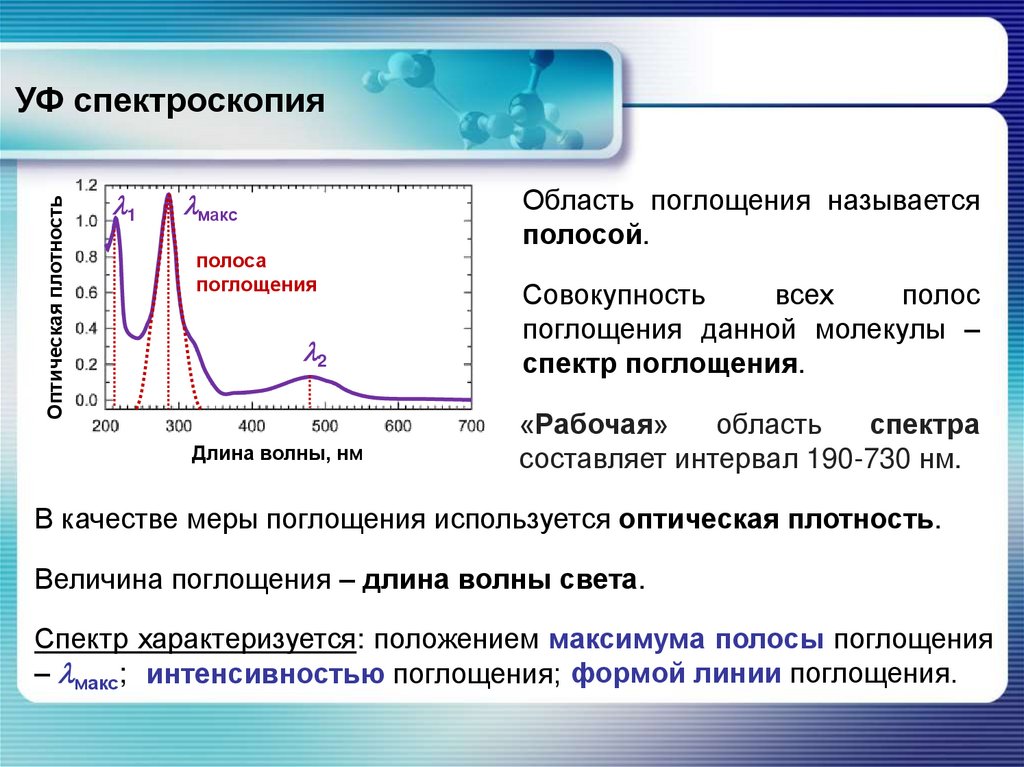
Область поглощения называется
полосой.
Совокупность
всех
полос
поглощения данной молекулы –
спектр поглощения.
«Рабочая»
область
спектра
составляет интервал 190-730 нм.
В качестве меры поглощения используется оптическая плотность.
Величина поглощения – длина волны света.
Спектр характеризуется: положением максимума полосы поглощения
– макс; интенсивностью поглощения; формой линии поглощения.
28. УФ спектроскопия
184Полоса поглощения – область спектра, в
которой имеется детектируемый сигнал с
одним или несколькими максимумами.
Тонкая колебательная структура – сложный
контур полосы поглощения, возникающий за счет
перехода на разные уровни одного и того же
электронного состояния.
Хромофор – структурная группа в органическом
соединении, которая обуславливает избирательное
поглощение света в электронном спектре. Обычно
это группы C=C, C≡C, C=O, N=N, N=O, NO2,
ароматические системы и т.д.
Ауксохром
–
насыщенная
группа
в
органическом
соединении,
присоединение
которой к хромофору изменяет положение и
интенсивность полосы поглощения последнего в
спектре. Типичные группы: –Alk, –SH, –NH2, –
OH, –Hal
204
бензол
255
29. УФ спектроскопия
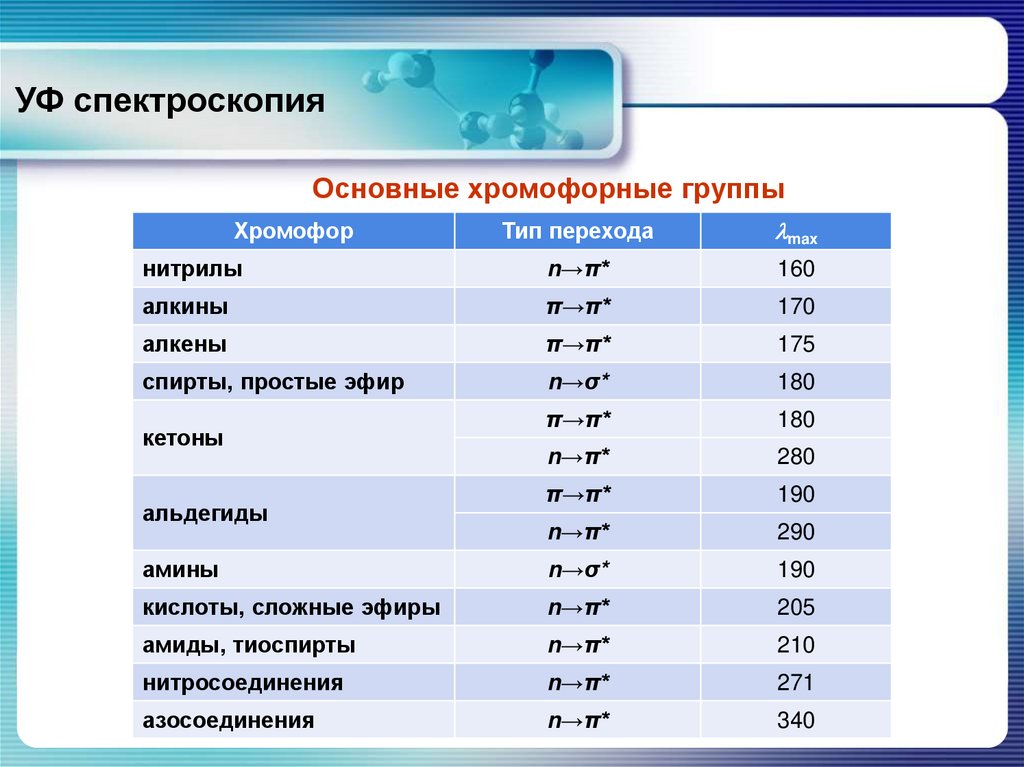
Основные хромофорные группыТип перехода
max
нитрилы
n→π*
160
алкины
π→π*
170
алкены
π→π*
175
спирты, простые эфир
n→σ*
180
π→π*
180
n→π*
280
π→π*
190
n→π*
290
амины
n→σ*
190
кислоты, сложные эфиры
n→π*
205
амиды, тиоспирты
n→π*
210
нитросоединения
n→π*
271
азосоединения
n→π*
340
Хромофор
кетоны
альдегиды
30. УФ спектроскопия
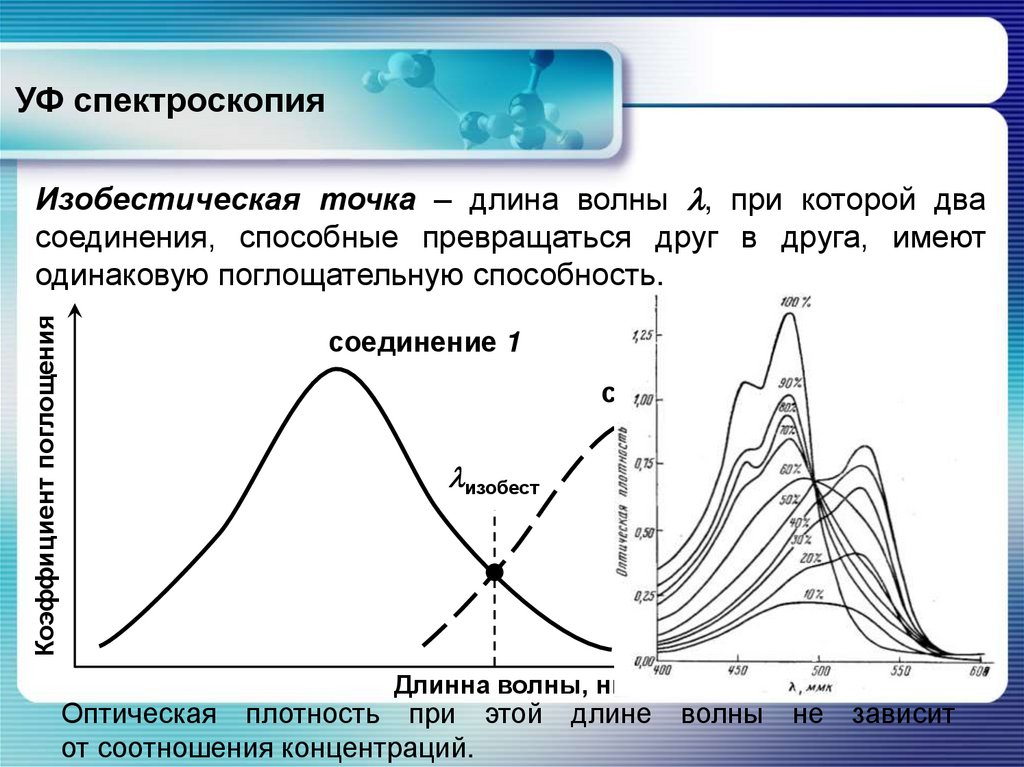
Коэффициент поглощенияИзобестическая точка – длина волны , при которой два
соединения, способные превращаться друг в друга, имеют
одинаковую поглощательную способность.
соединение 1
соединение 2
изобест
Длинна волны, нм
Оптическая плотность при этой длине волны не зависит
от соотношения концентраций.
31. УФ спектроскопия
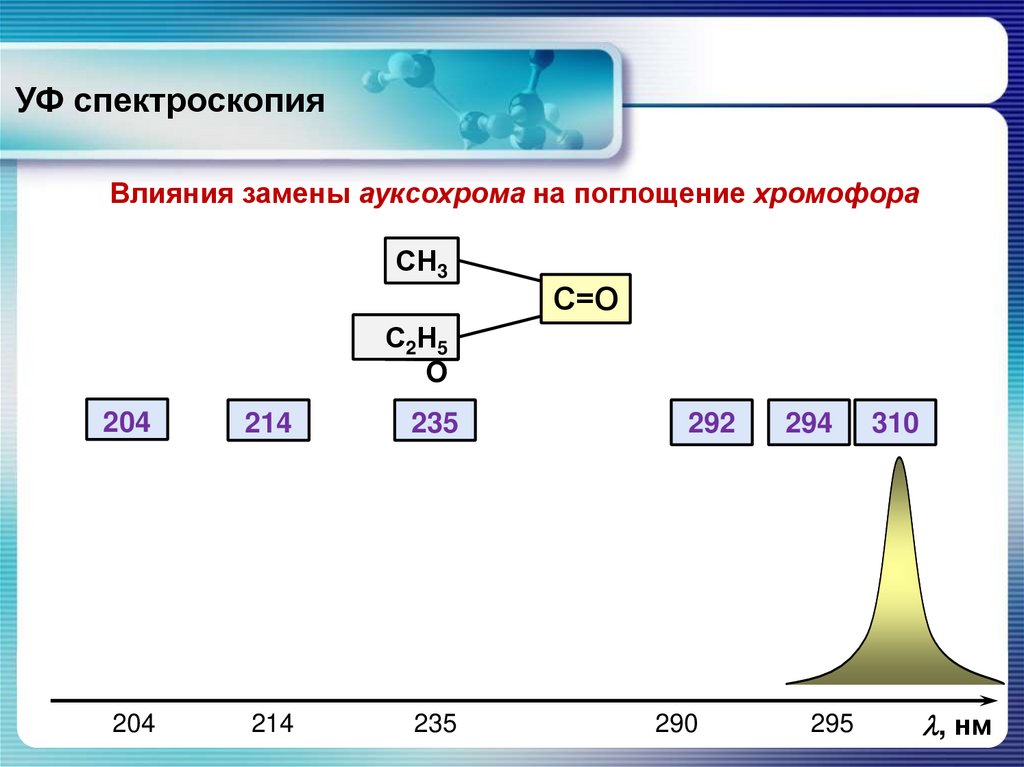
Влияния замены ауксохрома на поглощение хромофораСНН3
С=О
СNН
СН
Сl
Н235
2Н
O
204
214
235
204
214
235
292
290
294
295
310
, нм
32. УФ спектроскопия
Взаимосвязь электронных спектров и структурыорганических молекул
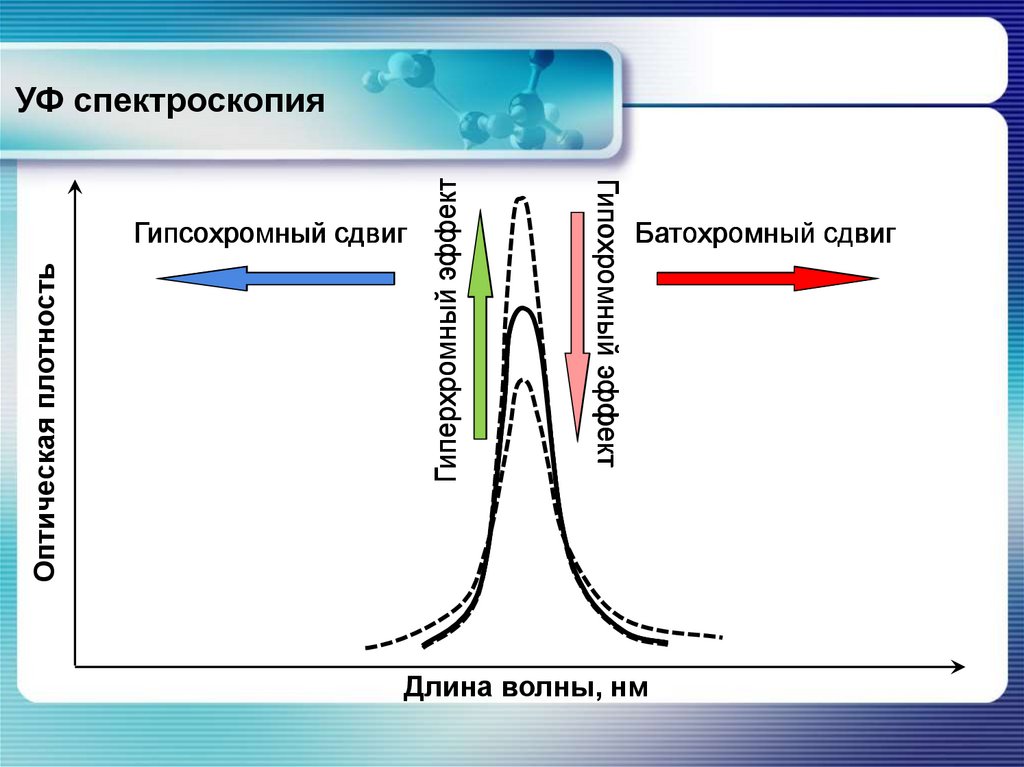
Гипсохромный сдвиг – смещение полосы поглощения в
коротковолновую область спектра;
Батохромный сдвиг – смещение полосы поглощения в
область длинных волн;
Гиперхромный эффект – увеличение интенсивности полосы
поглощения;
Гипохромный эффект – уменьшение интенсивности полосы
поглощения.
33. УФ спектроскопия
Оптическая плотностьГипохромный эффект
Гипсохромный сдвиг
Гиперхромный эффект
УФ спектроскопия
Батохромный сдвиг
Длина волны, нм
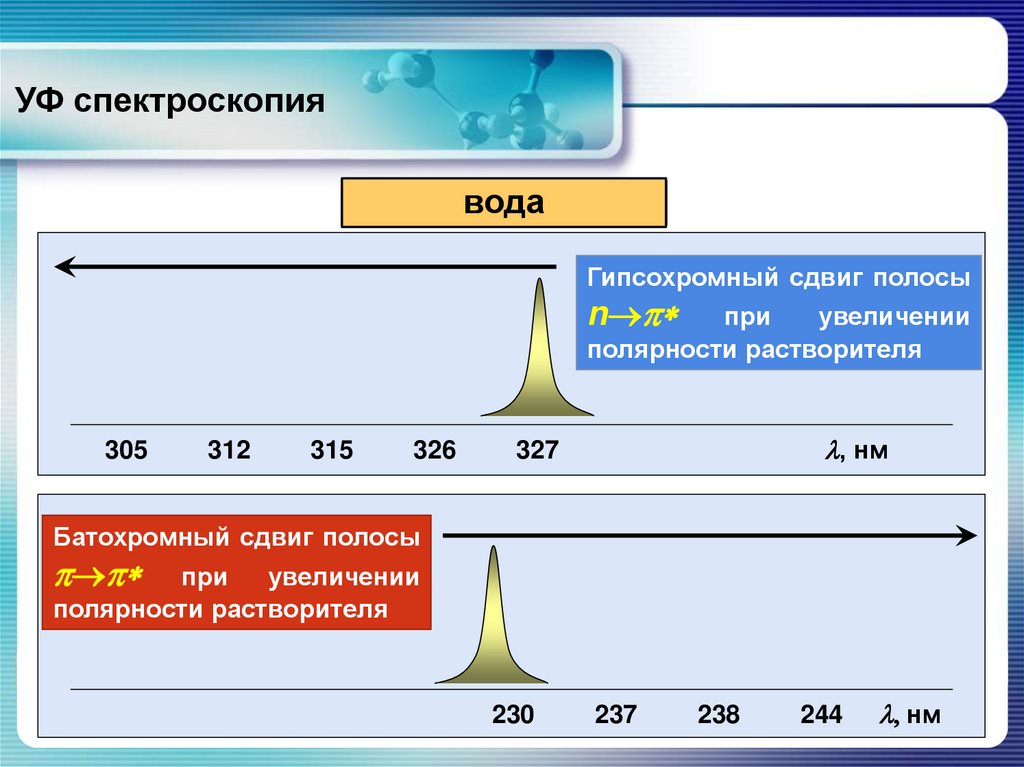
34.
УФ спектроскопиявода эфир
диэтиловый
метанол
этанол
гексан
Гипсохромный сдвиг полосы
n *
при
увеличении
полярности растворителя
305
312
315
326
, нм
327
Батохромный сдвиг полосы
*
при
увеличении
полярности растворителя
230
237
238
244
, нм
35. УФ спектроскопия
Применение УФ-спектроскопии1. Идентификация
органических
соединений,
хромофорные группировки - доказательство
исследуемом веществе группировок-хромофоров.
содержащих
наличия в
2. Исследование
деталей
строения,
используя
величины
коэффициента молярной экстинкции и длины волны в максимуме
полосы поглощения. Относительное расположение хромофорных
групп у кратных связей влияет на спектры поглощения, что
позволяет различить цис- и транс-изомеры.
3. Количественный анализ, включая контроль за ходом реакций и
определение примесей в образце органического вещества,
исследования процессов комплексообразования.
36. УФ спектроскопия
В настоящее время для структурного анализа органических соединенийэлектронная спектроскопия имеет ограниченное применение.
УФ-спектроскопия − широко применяется, как количественный анализ.
Количественное определение вещества проводится на основании спектра, в
котором измеряется интенсивность поглощения света этим веществом при
выбранной длине волны.
При проведении такого количественного анализа длина волны должна
соответствовать следующим требованиям:
• выбранная полоса должна быть по возможности свободна от наложения
полос поглощения других компонентов анализируемой системы.
• выбранная
полоса
должна
обладать
достаточно
высоким
коэффициентом поглощения для индивидуального соединения.
Такие полосы поглощения называются аналитическими.
37.
Инструментальныеметоды анализа
Вопросы к лекции:
1. Что такое спектроскопия, виды электромагнитного излучения?
2. Характеристики электромагнитной волны, единицы их измерения?
3. Виды спектров, их классификация?
4. Понятия фотона и энергетических состояний?
5. Что такое УФ-спектроскопия?
6. Закон светопоглощения?
7. Что такое молекулярные орбитали; типы молекулярных орбиталей?
8. Виды электронных переходов?
9. Основные характеристики УФ-спектра?
10. Основные понятия УФ-спектроскопии?
11. Применение УФ-спектроскопии?



























 physics
physics








