Similar presentations:
Урок 16. Одноатомные спирты
1.
Тема урока:Одноатомные спирты
2.
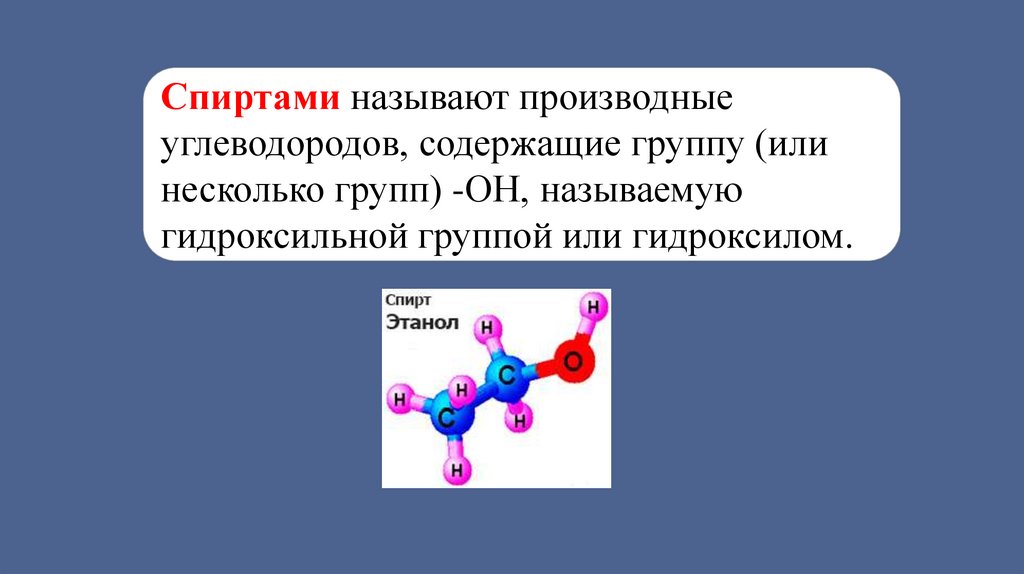
Спиртами называют производныеуглеводородов, содержащие группу (или
несколько групп) -ОН, называемую
гидроксильной группой или гидроксилом.
3.
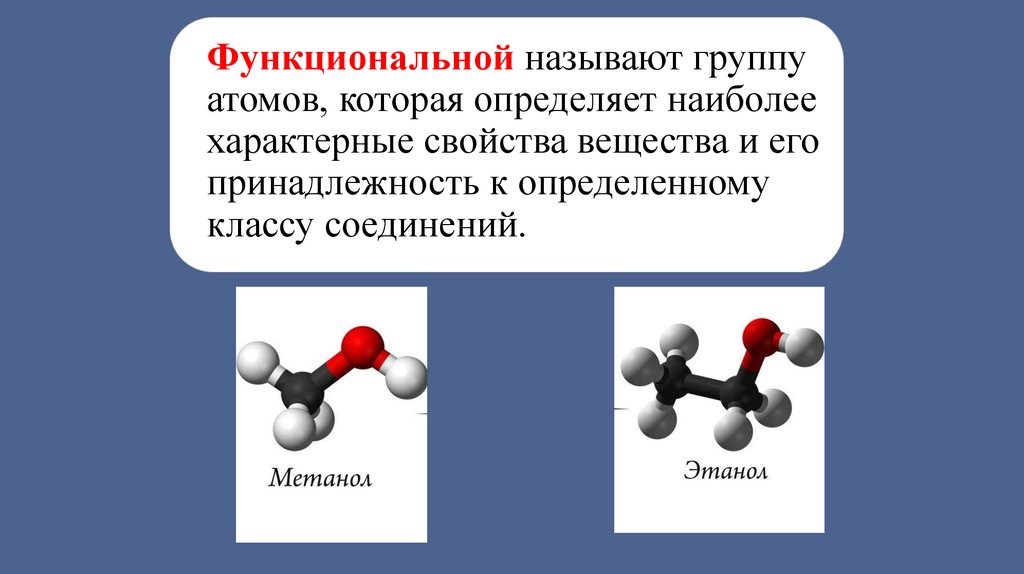
Функциональной называют группуатомов, которая определяет наиболее
характерные свойства вещества и его
принадлежность к определенному
классу соединений.
4.
Предельными одноатомными спиртамиили, алканолами называют органические
соединения, в молекулах которых алкильный
радикал (R) связан с гидроксильной группой.
Состав их соответствует формуле
R – ОН или СnH2n+1 OH
5.
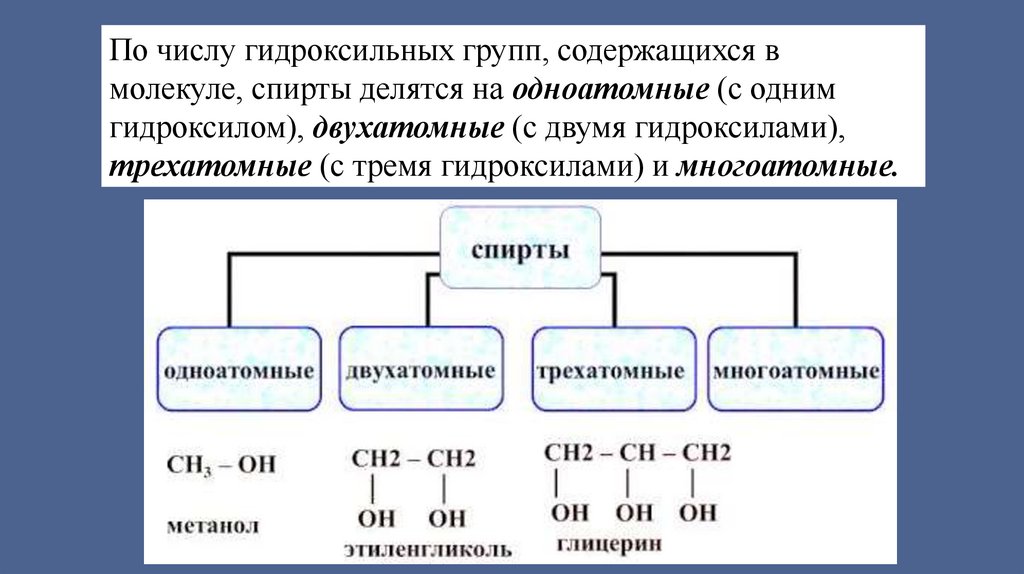
По числу гидроксильных групп, содержащихся вмолекуле, спирты делятся на одноатомные (с одним
гидроксилом), двухатомные (с двумя гидроксилами),
трехатомные (с тремя гидроксилами) и многоатомные.
6.
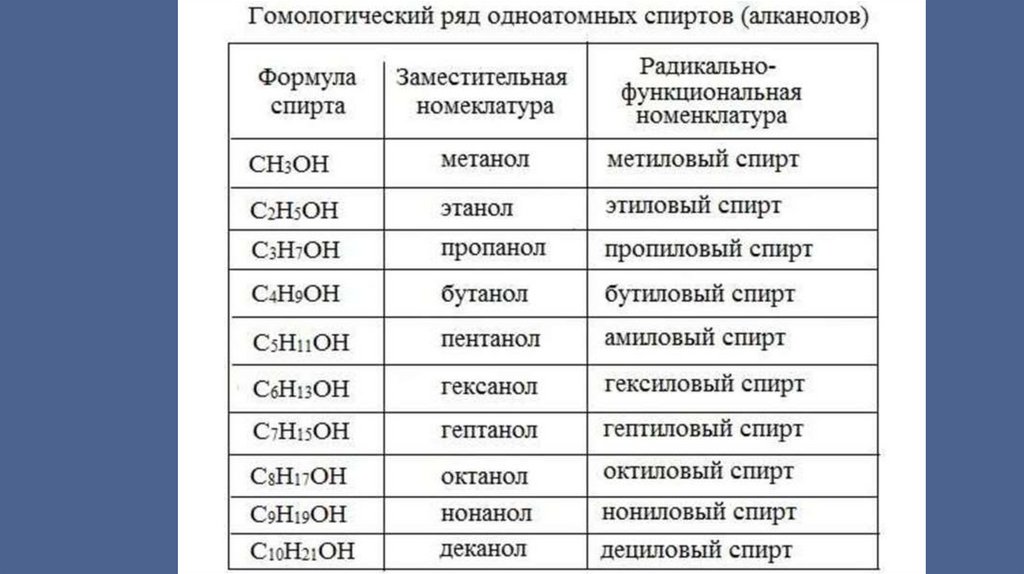
Номенклатура спиртовСистематические названия даются по названию углеводорода с
добавлением суффикса -ол и цифры, указывающей положение
гидроксигруппы (если это необходимо). Например:
Нумерация ведется от ближайшего к ОН-группе конца цепи.
7.
8.
Изомерия спиртов1. Для спиртов характерна структурная изомерия:
изомерия положения ОН-группы (начиная с С3)
2. углеродного скелета (начиная с С4)
3. межклассовая изомерия с простыми эфирами СН3-CH2–OH и CH3–O–CH3
9.
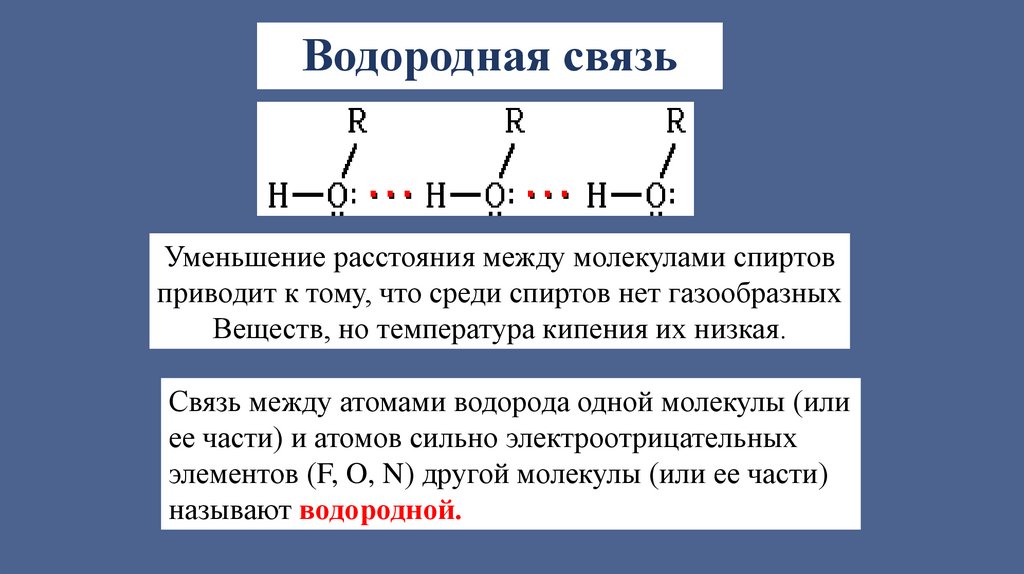
Водородная связьУменьшение расстояния между молекулами спиртов
приводит к тому, что среди спиртов нет газообразных
Веществ, но температура кипения их низкая.
Связь между атомами водорода одной молекулы (или
ее части) и атомов сильно электроотрицательных
элементов (F, O, N) другой молекулы (или ее части)
называют водородной.
10.
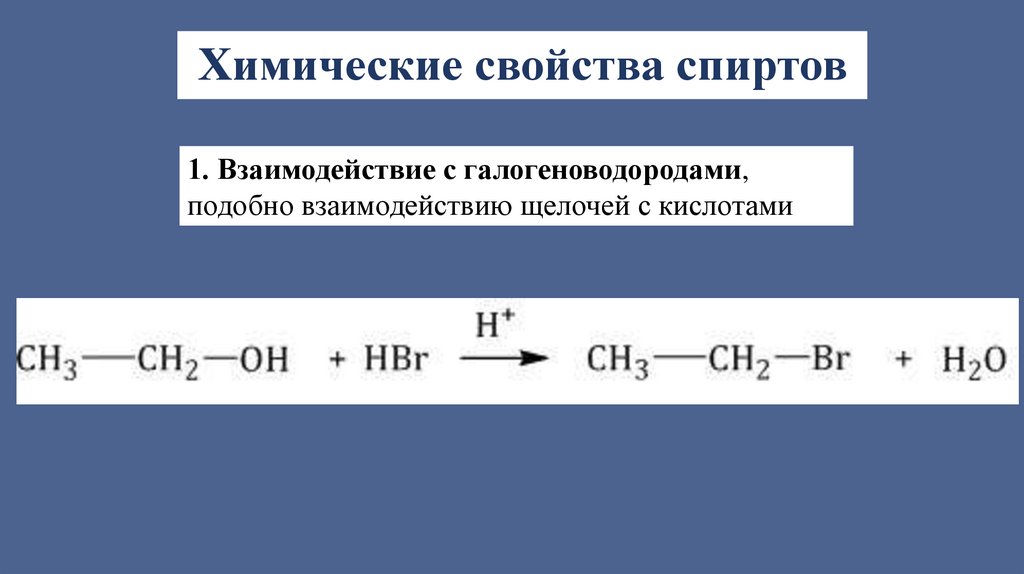
Химические свойства спиртов1. Взаимодействие с галогеноводородами,
подобно взаимодействию щелочей с кислотами
11.
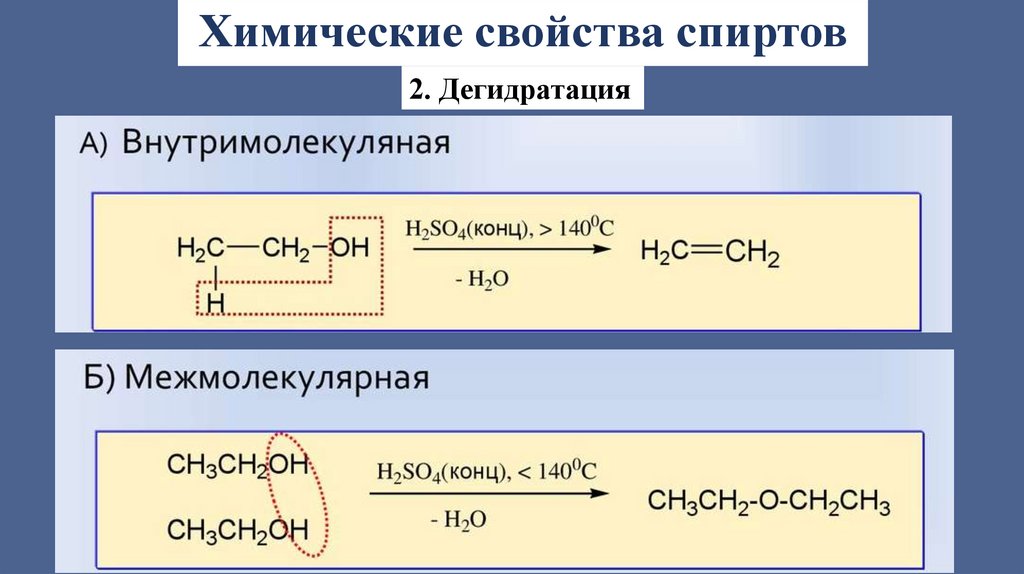
Химические свойства спиртов2. Дегидратация
12.
Химические свойства спиртов3. Горение
С2Н5ОН + 3 О2 → 2 СО2 + 3 Н2О
С3Н7ОН + 4,5 О2 → 3 СО2 + 4 Н2О
С3Н7ОН + 9 О2 → 6 СО2 + 8 Н2О
13.
4. Спирты взаимодействуют со щелочными ищелочно-земельными металлами
2СН3-СН2-ОН + 2К → 2СН3-СН2-ОК + Н2↑
2СН3-СН2-ОН + Са → (СН3-СН2-О)2Са + Н2↑
14.
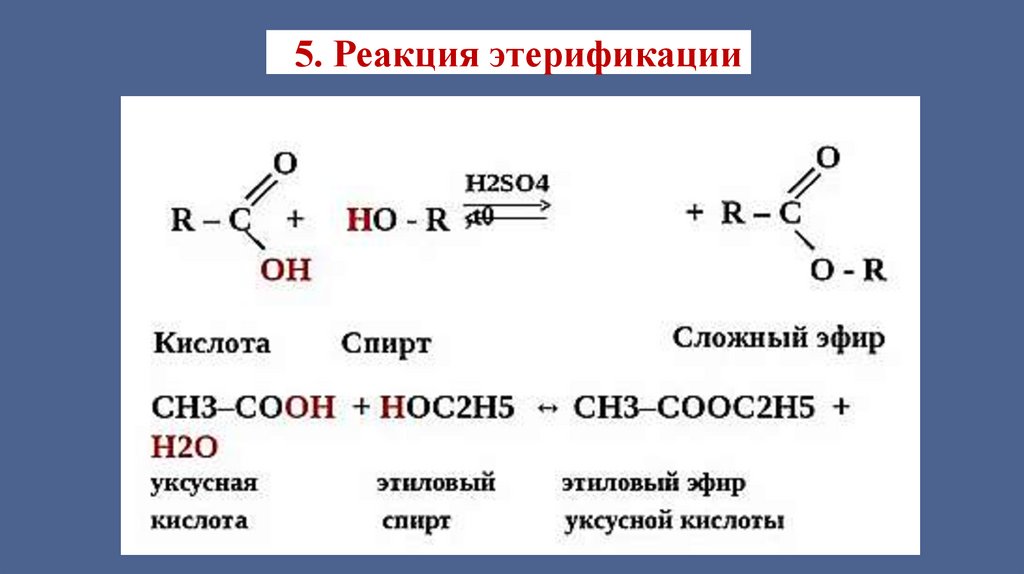
5. Реакция этерификации15.
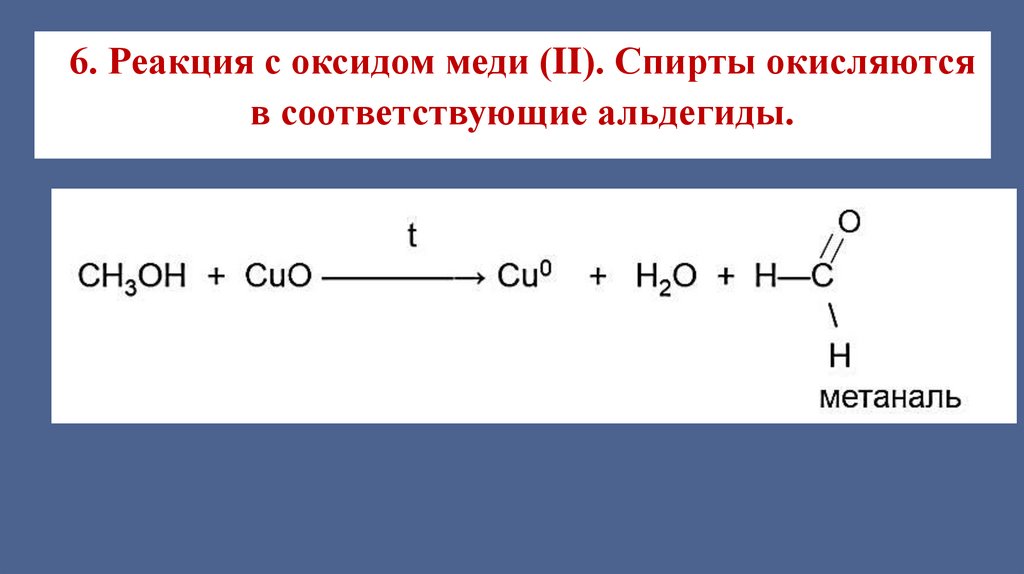
6. Реакция с оксидом меди (II). Спирты окисляютсяв соответствующие альдегиды.
16.
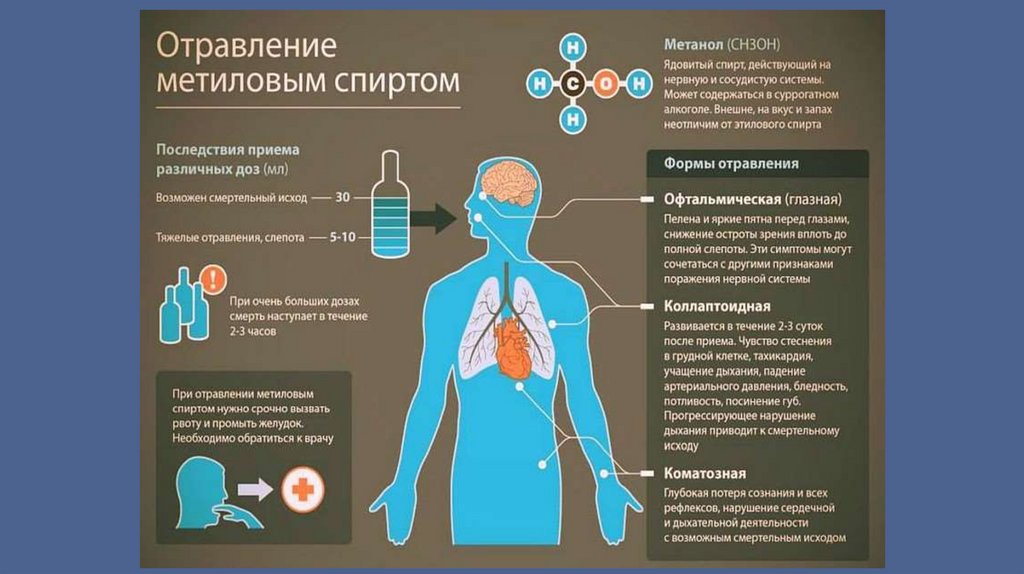
ПредставителиМЕТАНОЛ (древесный спирт)
СН3ОН – жидкость (tкип = 64,5; tпл
=- 98; ρ = 0,793 г/см3), с запахом
алкоголя, хорошо растворяется в
воде. Ядовит – вызывает слепоту,
смерть наступает от паралича
верхних дыхательных путей.
17.
Применение метанола• Метанол СН3ОН используют как
растворитель, а также в производстве
формальдегида, применяемого для
получения фенолформальдегидных смол, в
последнее время метанол рассматривают
как перспективное моторное топливо.
• Большие объемы метанола используют при
добыче и транспорте природного газа.
• Метанол – наиболее токсичное соединение
среди всех спиртов, смертельная доза при
приеме внутрь – 100 мл.
18.
19.
ЭТАНОЛ (винный спирт)С2Н5ОН – бесцветная
жидкость, с запахом спирта,
хорошо смешивается с водой,
ядовитое наркотическое
вещество.
20.
Применение этанолаЭтанол С2Н5ОН – исходное
соединение для получения
ацетальдегида, уксусной кислоты,
а также для производства
сложных эфиров карбоновых
кислот, используемых в качестве
растворителей.
Кроме того, этанол – основной
компонент всех спиртных
напитков, его широко применяют
и в медицине как
дезинфицирующее средство.
21.
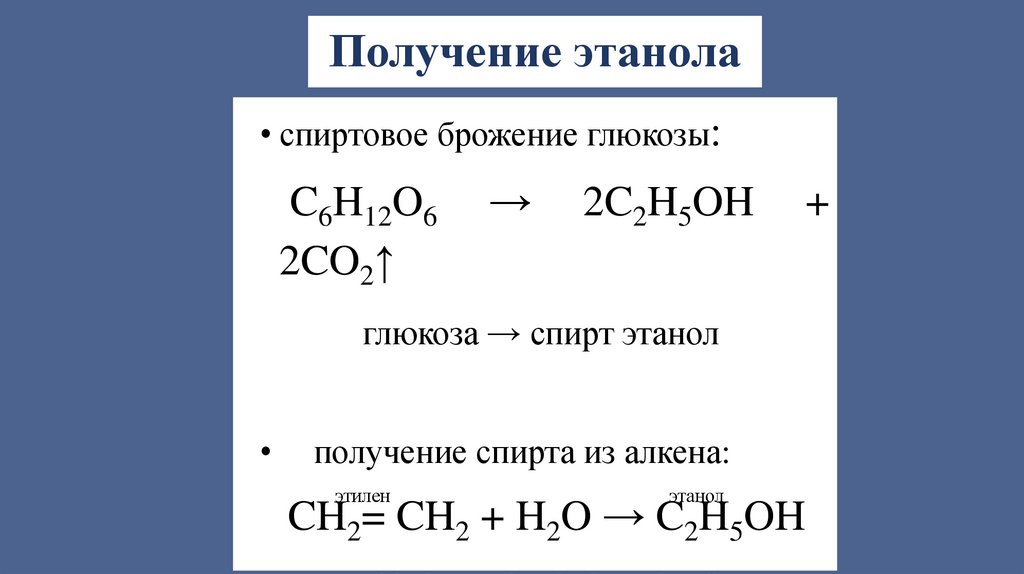
Получение этанола• спиртовое брожение глюкозы:
C6H12O6
2CO2↑
→
2C2H5OH
+
глюкоза → спирт этанол
получение спирта из алкена:
этилен
этанол
CH2= CH2 + H2O → C2H5OH
22.
Вопросы для закрепления22
23.
Домашнее заданиеП. 11 (читать) + повторять
в тетради + воп. 3 стр. 62.
23
24.
СПАСИБО ЗА ВНИМАНИЕ!24












 chemistry
chemistry