Similar presentations:
2025 Фармакология боли лекция
1.
Фармакология болиКафедра фармации с циклом клинической фармакологии
Д.м.н. Воробьева В.В.
1
2. План лекции
• Чувствительность к боли – ноцицепция• Классификация анальгетиков
• Наркотические анальгетики
• Ненаркотические анальгетики НПВС
2
3. Классификация анальгетиков
• Анальгетики преимущественноцентрального действия
А. Опиоидные (наркотические) анальгетики
Б. Неопиоидные анальгетики
• Анальгетики преимущественно
периферического действия
Нестероидные противовоспалительные средства
(НПВС)
3
4. Наркотические (опиоидные) анальгетики
45. Наркотические анальгетики – вещества, способные при резорбтивном действии избирательно подавлять чувство боли благодаря влиянию
наЦНС, а при регулярном применении – вызывать
психическую и физическую зависимость
5
6. Классификация наркотических анальгетиков по химической структуре
• Производные пиперидинфенантрена• Морфин, Кодеин (алкалоиды опия)
• Омнопон (новогаленовый препарат опия)
• Бупренорфин (Бупранал)
• Производные фенилпиперидина
• Тримеперидин (Промедол),
• Пропионилфенилэтоксиэтилпиеридин (Проксидол)
• Фентанил
• Производные морфинана
• Налбуфин, Буторфанол
• Производные циклогексанола
• Трамадол (Трамал),
• Тапентадол (Палексия)
6
7. Фармакодинамика наркотических анальгетиков на молекулярном уровне
• При активации опиоидного рецептораингибируется аденилатциклаза, которая отвечает за
синтез вторичного посредника цАМФ, а также
осуществляется регулирование ионных каналов
• Закрытие потенциал-зависимых Ca2+ каналов
в пресинаптическом нейроне приводит к уменьшению
выброса возбуждающих нейромедиаторов (таких
как глутаминовая кислота),
• Активация К+ каналов в постсинаптическом нейроне
приводит к гиперполяризации мембраны
• Уменьшается чувствительность нейрона к
возбуждающим нейромедиаторам
7
8. Основные свойства µ1,2 опиатных рецепторов
• Ответственны за тормозной контроль проведения ивосприятия боли преимущественно на супраспинальном
уровне (µ1)
• Через стимуляцию µ1 опиоидных рецепторов возникают
эффекты эйфории, седации, психической и физической
зависимости, повышения тонуса гладких мышц, миоз
• Стимуляция µ2 рецепторов ответственна за угнетение
дыхания
• Тип µ1,2 рецепторов стимулируется морфином,
тримеперидином, фентанилом, трамадолом
• Налорфин и налоксон играют роль антагонистов µ
рецепторов
8
9. Основные свойства каппа, дельта, сигма опиатных рецепторов
• Каппа (k) рецепторы осуществляют контроль запроведением и восприятием боли на спинальном
уровне, дисфория
• Возбуждение сигма рецепторов вызывает дисфорию,
галлюцинации и тахикардию
• Возбуждение дельта (δ) рецепторов обеспечивают
анальгезию, угнетение дыхания, снижение моторики
ЖКТ
• Ноцицептивный рецептор (NОР) ответственен за
формирование толеранности к морфину
9
10. Классификация наркотических анальгетиков по действию на опиоидные рецепторы (ОР)
• Агонисты - вызывают стимуляцию опиоидныхрецепторов
• Антагонисты - вызывают блокаду опиоидных
рецепторов (Налоксон, Налтрексон), но без их
стимуляции и не оказывают обезболивающего эффекта,
снимают действие агонистов
• Частичные антагонисты (агонисты/антагонисты) –
активируют каппа- и сигма ОР и блокируют мю- и дельта
- ОР (Налорфин, Буторфанол)
10
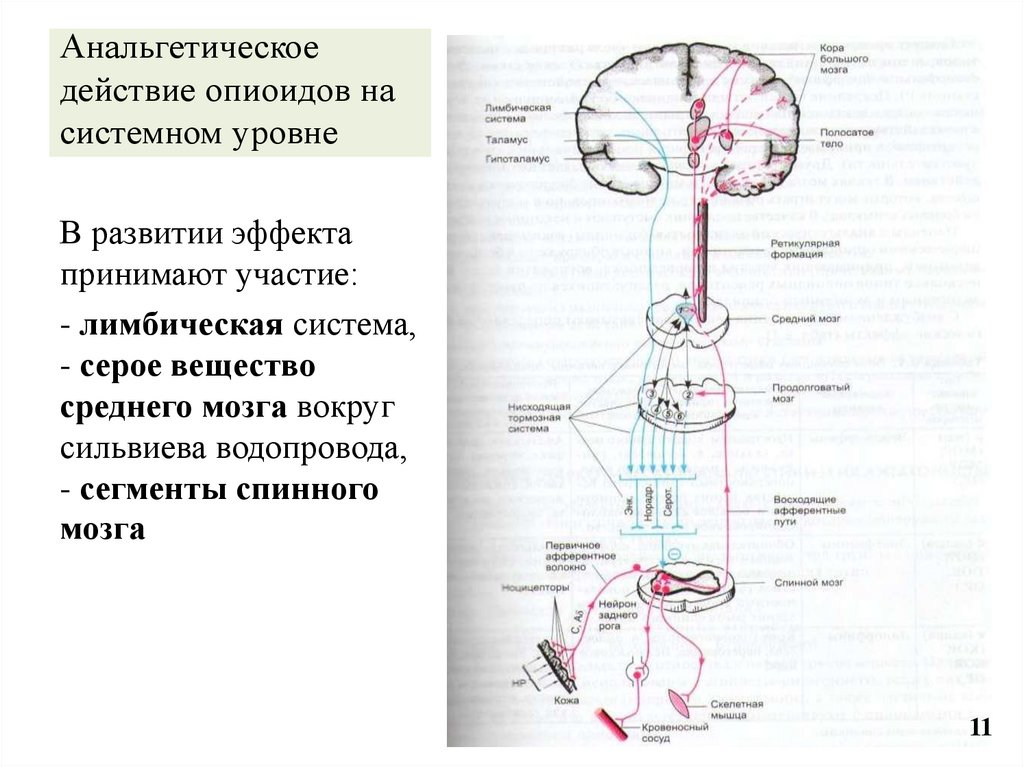
11. Анальгетическое действие опиоидов на системном уровне
В развитии эффектапринимают участие:
- лимбическая система,
- серое вещество
среднего мозга вокруг
сильвиева водопровода,
- сегменты спинного
мозга
11
12. Анальгетическое действие опиоидов (1)
• На уровне сегментов спинного мозга подавляетсяпереключение восходящих болевых импульсов
• Активация ОР лимбической системы мозга
вызывает торможение эмоциональной реакции на
боль. Пациент локализует боль, но она теряет
выраженный характер и деперсонифицируется!
• Воздействие на серое вещество среднего мозга
вокруг сильвиева водопровода активизирует
нисходящие пути, тормозящие болевое ощущение
12
13. Обезболивающее действие опиоидных анальгетиков (2)
• Повышение болевого порога в результате:• Торможения передачи
• Интеграции
• Интерпретации болевых импульсов,
проходящих через болевые пути
• Угнетение процессов суммации
подпороговых болевых раздражений на
всех уровнях проведения боли
• Противотревожное, эйфоризирующее действие
13
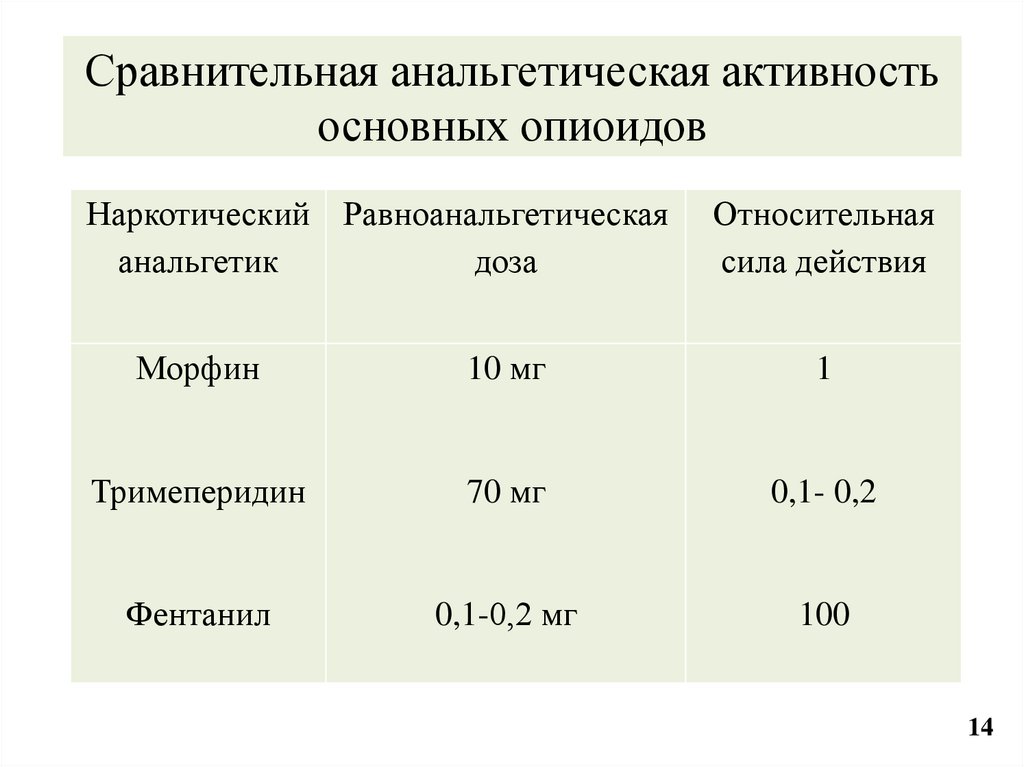
14. Сравнительная анальгетическая активность основных опиоидов
Наркотический Равноанальгетическаяанальгетик
доза
Относительная
сила действия
Морфин
10 мг
1
Тримеперидин
70 мг
0,1- 0,2
Фентанил
0,1-0,2 мг
100
14
15. Действие опиоидов на психическую сферу человека
• В обычных дозах вызывают седацию, апатию,сонливость, эйфорию с усилением чувства
собственного достоинства
• Снижают способность человека к сложным
мыслительным функциям, нарушают двигательную
координацию
• При первых введениях может появиться дисфория,
сопровождающаяся тревогой, беспокойством,
головными болями, головокружением, тошнотой,
рвотой
• Развитие пристрастия и толерантности!
15
16. Действие опиоидов на дыхание
• Все опиоиды угнетают дыхание пропорциональнодозе, воздействуя на респираторные центры
• Снижается чувствительность дыхательного
центра к CO2
• Опиоиды подавляют чувство недостатка воздуха,
уменьшается частота дыхания и, в случае
передозировки, происходит остановка дыхания
• Угнетают кашель за счет торможения кашлевого
рефлекса
16
17. Действие опиоидов на кровообращение
• Опиоиды оказывают минимальное действие накровообращение
• Опиоидные анальгетики не влияют на
сократимость миокарда
• Морфин и промедол расширяют сосуды, это
вазодиляторы (гистаминогенный эффект)
• Фентанил суживает сосуды, это вазоконстриктор
17
18. Действие опиоидов на ЖКТ
• Стимулируют хеморецепторную триггерную зонурвотного центра продолговатого мозга и вызывают
тошноту и рвоту
• Уменьшают выработку желудочного сока
• Снижают перистальтику кишечника и стимулируют
циркулярные мышечные волокна ЖКТ
(пилорический, илеоцекальный сфинктер) , что
ведет к абстипации
• Увеличивают тонус желчных и панкреатических
протоков
спазм сфинктера Одди
18
19. Показания к использованию опиоидных анальгетиков
• Тяжелые травмы и ожоги для предупреждениетравматического шока (морфин, тримеперидин,
буторфанол, трамадол)
• Медикаментозная премедикация
(тримеперидин, фентанил и др.)
• Острый инфаркт миокарда (морфин, фентанил)
• Отек легких кардиогенного генеза (морфин)
• Обезболивание родов (тримеперидин)
• Приступ почечной колики (тримеперидин)
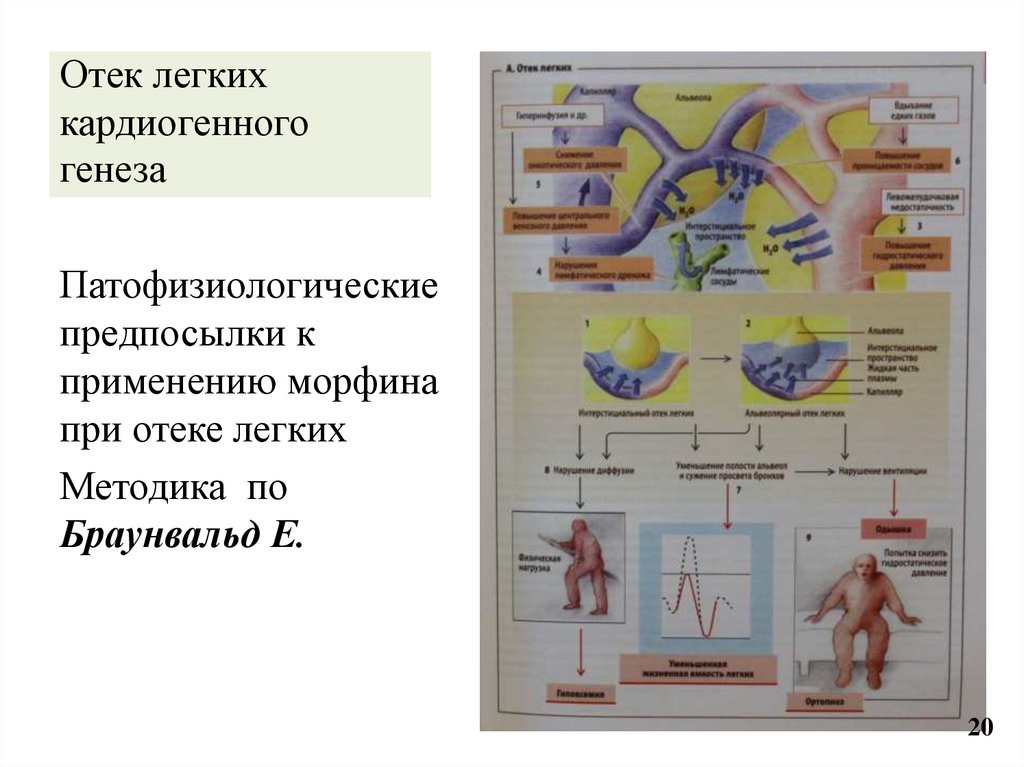
20. Отек легких кардиогенного генеза
Патофизиологическиепредпосылки к
применению морфина
при отеке легких
Методика по
Браунвальд Е.
20
21. Противопоказания к назначению опиоидных анальгетиков
• Угнетение дыхания• Острое заболевание органов брюшной полости до
решения вопроса об оперативном вмешательстве
• Черепно-мозговая травма (ЧМТ)
• Возраст до 2-х лет
• Бронхиальная астма
• Брадикардия
21
22. Центральные эффекты морфина
УгнетающиеВозбуждающие
Анальгезия
Седация
Подавление кашлевого
рефлекса
Угнетение дыхательного
центра
Эйфория
Галлюцинации
Возбуждение
окуломоторного центра
(миоз)
Тошнота
Возбуждение триггерной
зоны
Брадикардия (n.vagus)
22
23. Передозировка морфина
• Депрессия дыхания (редкое периодическое типаЧейн-Стокса или Биотта)
• Антидот – налоксон 0,04% раствор по 1 мл в
ампулах и вводить в/в медленно по 1 мл с
интервалом 3-5 мин до появления сознания и
восстановления спонтанного дыхания
• Не более 10 мг препарата
23
24. Тримеперидин
• Синтетический опиоид• В 10 раз слабее морфина по анальгетической
активности
• Обладает спазмолитическим действием, поэтому
применяют при почечной и кишечной колике
• Слабый депрессант дыхания
• При повторных введениях высоких доз может
спровоцировать судороги
24
25. Трамадол (Трамал)
• Не вызывает седации• Не угнетает дыхания
• Не вызывает кардиодепрессии
• Формы выпуска;
• капсулы по 0,05
• раствор для приема внутрь
• суппозитории по 0,1
• раствор для инъекций в ампулах (1 мл по
0,05 активного вещества)
25
26. Ненаркотические анальгетики Нестероидные противовоспалительные средства (НПВС)
2627.
• Неопиоидные анальгетики – синтетическиевещества, оказывающие умеренное
обезболивающее действие за счет торможения
образования тканевых биологически активных
веществ (простагландинов), участвующих в
возникновении боли при воспалении и
травматизации тканей
• Не вызывают лекарственной зависимости
27
28. Исторические предпосылки
• В 1971 году Джон Вейн обнаружил ЦОГ-1. Открытиепомогло объяснить механизм действия аспирина, который
активно использовали с 1899 года как обезболивающее и
противовоспалительное средство.
• В 1991 году Кси с соавт. в лаборатории Дэниеля Симмона
университета Бригама Янга открыли ЦОГ-2.
• Интересно, что структура фермента ЦОГ-2 значительно не
отличается от структуры ранее обнаруженной ЦОГ-1. Но,
несмотря на это, их клиническое значение различно.
• Наконец, в 2002 году Чандрасекхаран с соавт. обнаружили
у собак ЦОГ-3 и предположили, что ее экспрессия может
играть роль в жаропонижающем эффекте парацетамола.
Однако воздействие парацетамола на ЦОГ-3 недостаточно
для объяснения всех наблюдаемых эффектов.
28
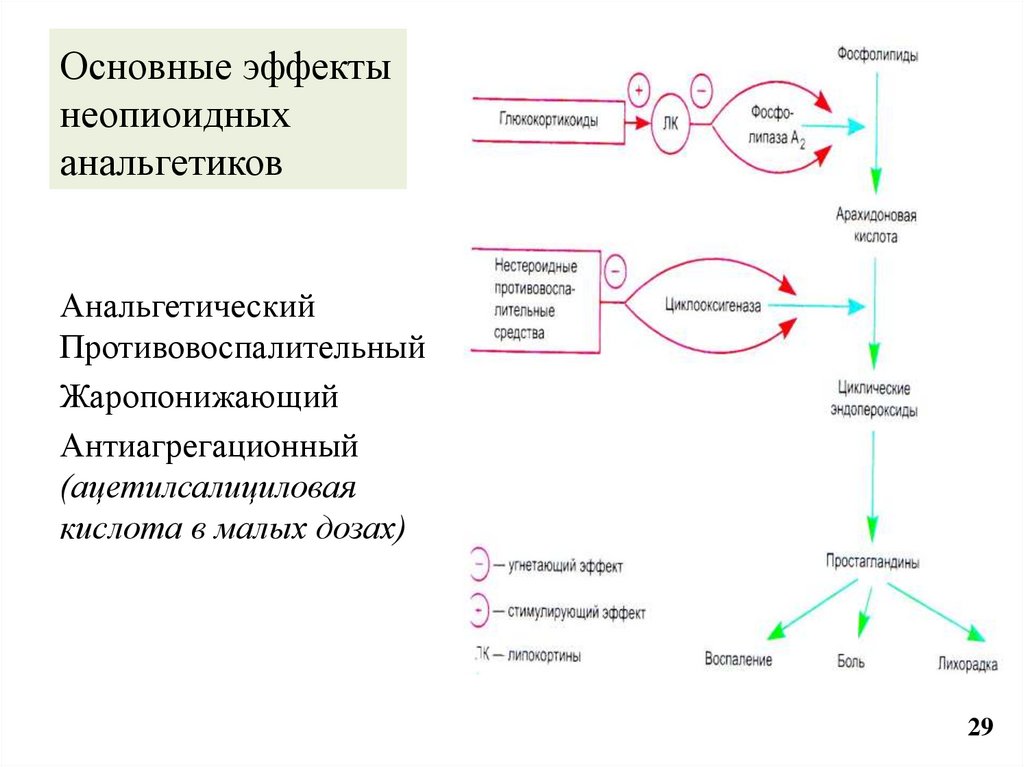
29. Основные эффекты неопиоидных анальгетиков
АнальгетическийПротивовоспалительный
Жаропонижающий
Антиагрегационный
(ацетилсалициловая
кислота в малых дозах)
29
30. Анальгетический эффект неопиоидных анальгетиков
• Подавляют боль средней интенсивности, зависимую отвыработки простагландинов (Pg)
• В ЦНС препараты тормозят облегчающее влияние
простагландинов на проведение болевых импульсов,
устраняют гиперальгезию
• В тканях устраняют повышенную чувствительность
болевых рецепторов к «альгогенам», уменьшают
• воспалительный отек
• внутриклеточное давление и
• растяжение капсул
30
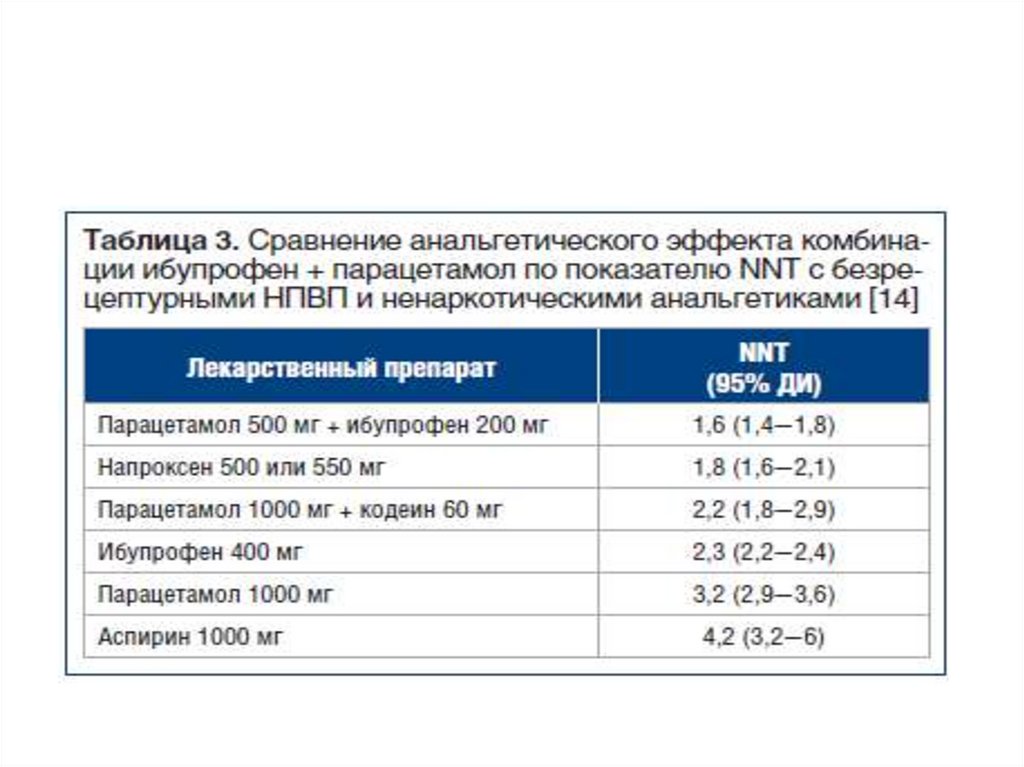
31. Анальгетическая активность неопиоидных анальгетиков
• По мере убывания анальгетического эффекта• кеторолак > диклофенак > индометацин >
метамизол > ибупрофен > парацетамол >
ацетилсалициловая кислота
• По анальгезирующей активности уступают ОА
примерно в 15-100 раз
31
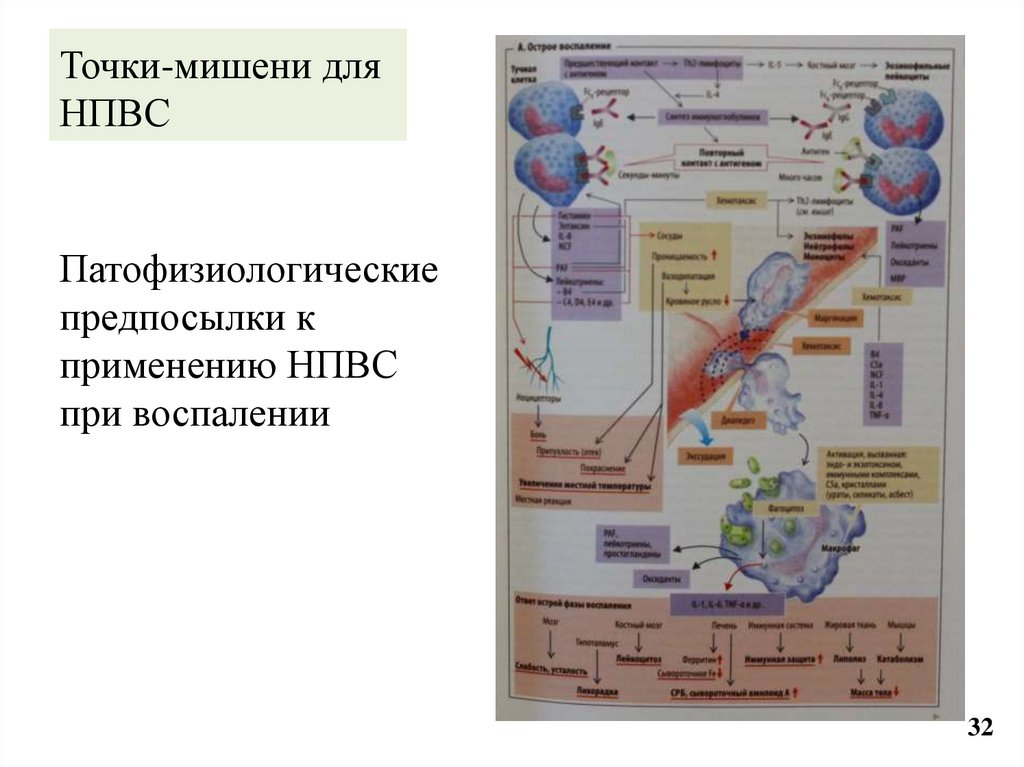
32. Точки-мишени для НПВС
Патофизиологическиепредпосылки к
применению НПВС
при воспалении
32
33. Механизмы противовоспалительного действия неопиоидных анальгетиков
• Снижение проницаемости капилляров• Стабилизация лизосомальных мембран
• Торможение выработки макроэргических соединений
• Ингибирование активности фермента
циклооксигеназы (ЦОГ- 2)
• Цитостатическое действие
• Торможение продукции и инактивация свободных
радикалов кислорода
• Подавление активации фактора транскрипции в Тлимфоцитах
33
34. Противовоспалительная активность неопиоидных анальгетиков
• По мере убывания противовоспалительногоэффекта
• индометацин > вольтарен > мелоксикам >
пироксикам > набуметон > бутадион >
ибупрофен > ацетилсалициловая кислота
• Неспецифичность противовоспалительного
действия
• Противовоспалительное действие фиксируется
через 36 и более ч, тогда как ослабление боли
наступает через 1 ч и длится 3-4 ч
34
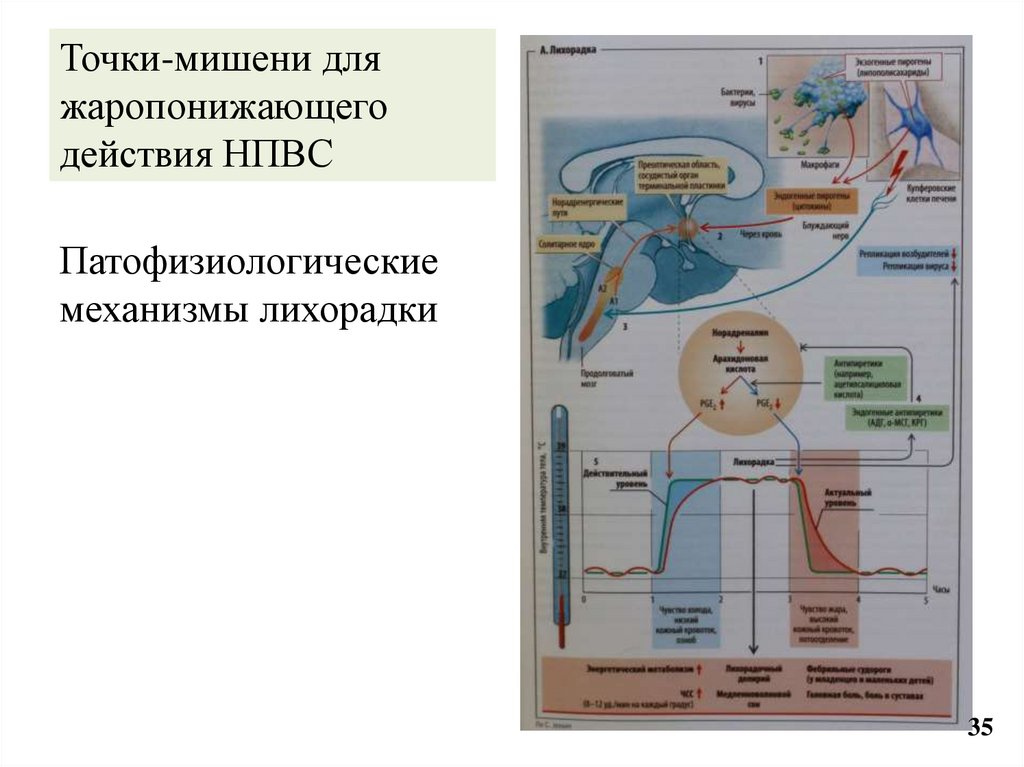
35. Точки-мишени для жаропонижающего действия НПВС
Патофизиологическиемеханизмы лихорадки
35
36. Механизм жаропонижающего действия неопиоидных анальгетиков
• Подавляют синтез Pg в клеткахтерморегулирующего центра
• Усиливают теплоотдачу радиацией через
расширение кожных сосудов и испарением через
усиление потоотделения
• Тормозят гиперпродукцию тепла в результате
мышечного дрожательного термогенеза (озноб) и
выделения тепла жировой тканью и внутренними
органами
36
37. Показания для назначения жаропонижающих средств
• Лихорадка на фоне тяжелого легочного илисердечно-сосудистого заболевания
• Лихорадка у больного с патологией ЦНС
(эпилепсия)
• Наличие в анамнезе фебрильных судорог
• Детский возраст до 1-3-х лет
37
38. Парацетамол (INN)
• Парацетамол – наименее токсичный из всехжаропонижающих средств и является
препаратом выбора для лечения лихорадочных
состояний
• В дозе 10-15 мг/кг массы тела в растворе
внутрь дает снижение температуры тела на 1-
1,50 С
• Действие парацетамола уже заметно через 30
мин, и сохраняется до 4 часов
38
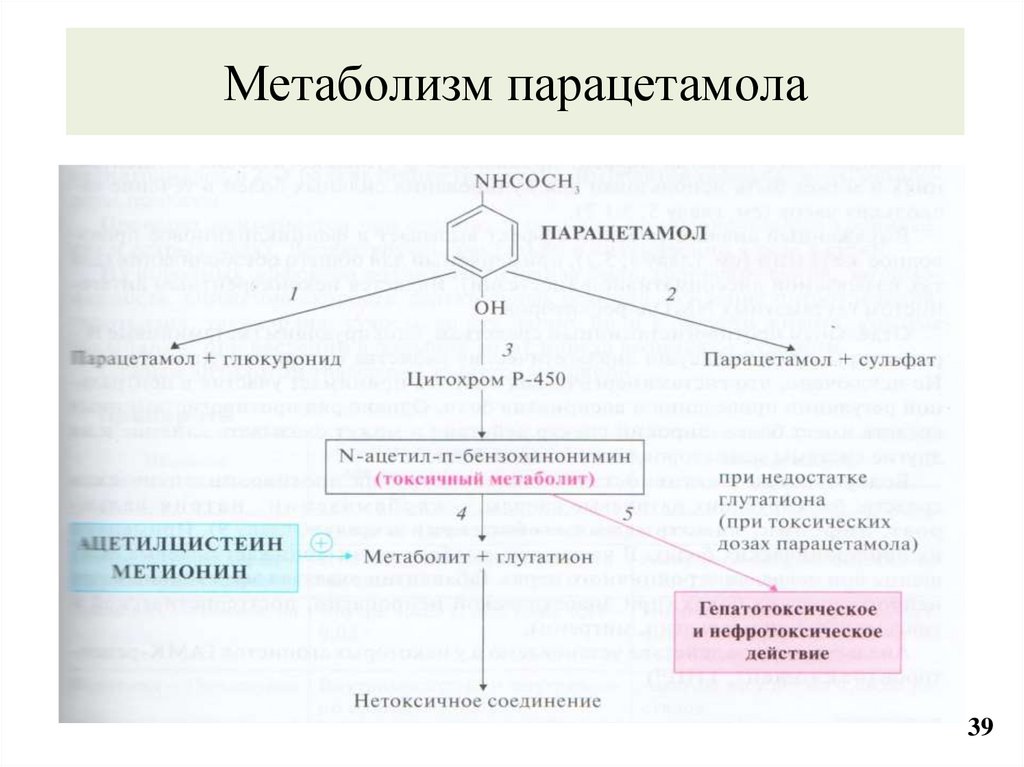
39. Метаболизм парацетамола
3940. Общие показания для НПВС
• Ревматизм, миокардит, кардит и диффузные заболеваниясоединительной ткани
• Травматическое воспаление мягких тканей и опорнодвигательного аппарата
• Миозиты, невралгии, радикулиты, подагра
• Послеоперационные боли средней интенсивности
• Головная боль
• Боль после стоматологических вмешательств
• Боль при почечной и желчной колике, панкреатите
• Гиперпиретические состояния при инфекционных
заболеваниях, инфузионной терапии, переливании компонентов
крови
40
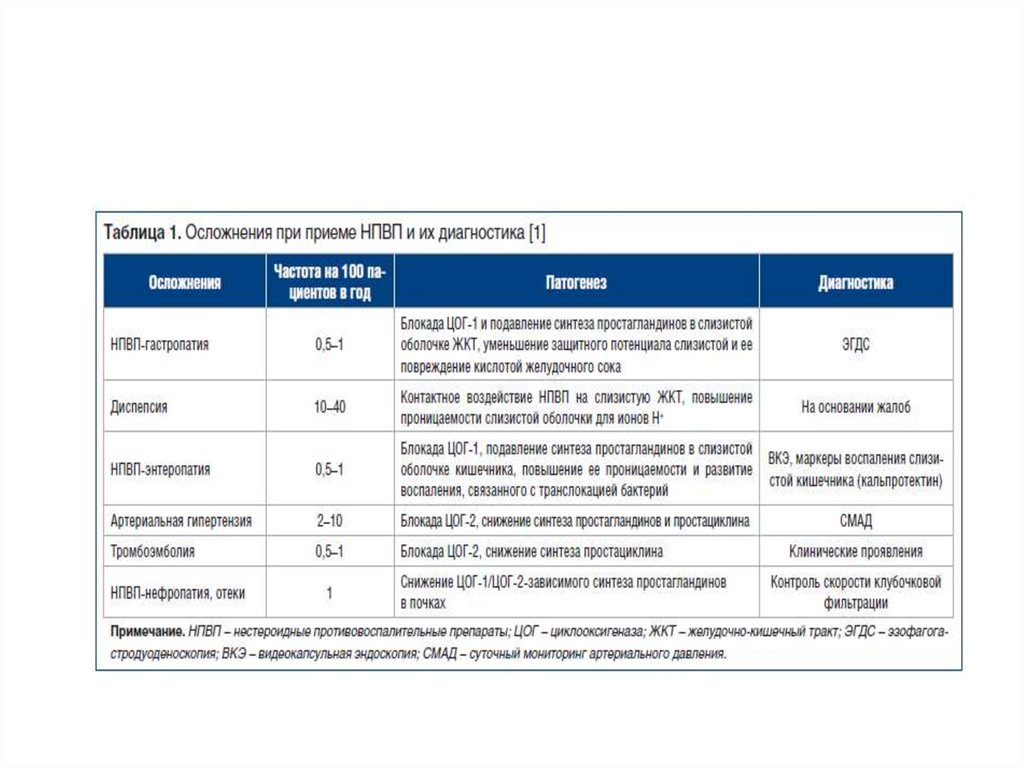
41. Осложнения на фоне приема НПВС (1)
• Желудочно-кишечные осложнения:- диспептический синдром
- кишечное воспаление
- язва желудка и двенадцатиперстной кишки
Профилактика
• Блокаторы Н2-гистаминовых рецепторов (фамотидин,
ранитидин)
• Блокаторы протонной помпы (омепразол)
• Гастропротекторы (де-нол, сукральфат)
• Антациды (альмагель, маалокс)
• Применение специфических ингибиторов ЦОГ-2 –
(мелоксикам, набуметон)
41
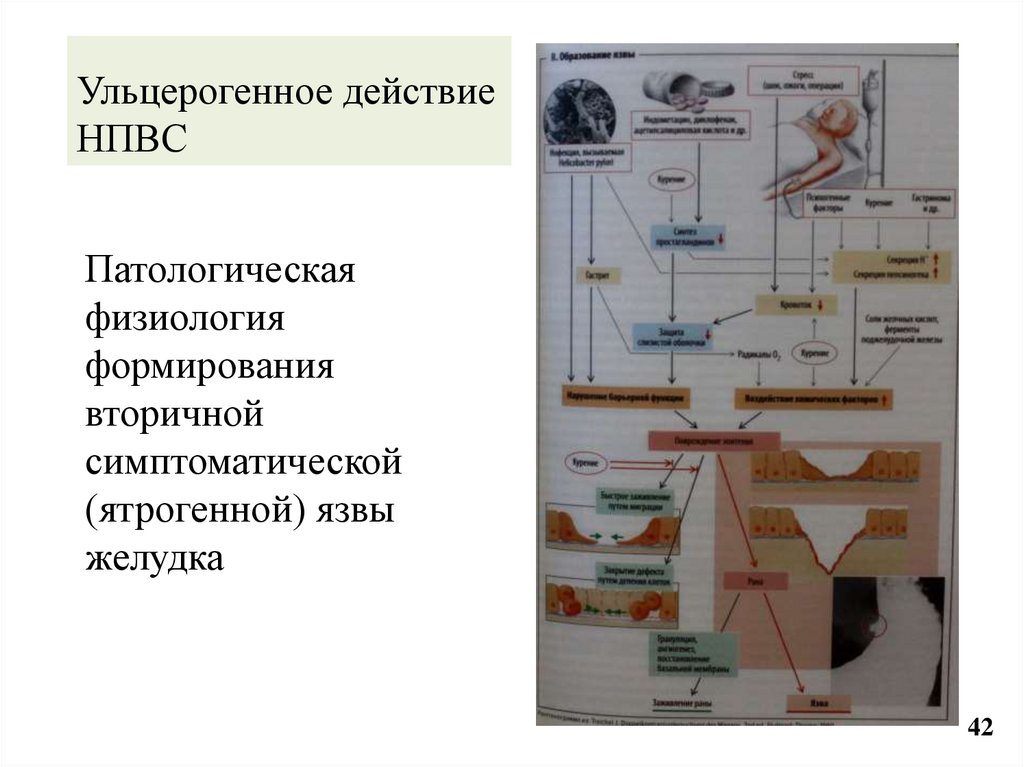
42. Ульцерогенное действие НПВС
Патологическаяфизиология
формирования
вторичной
симптоматической
(ятрогенной) язвы
желудка
42
43. Осложнения на фоне приема НПВС (2)
• Гиперчувствительность к НПВС(ацетилсалициловая кислота)
• Поражение печени и почек (пироксикам,
напроксен) носят иммунологичекий характер
• Поражение ЦНС (ибупрофен, индометацин)
• Гематологические нарушения (метамизол,
бутадион, индометацин)
• Синдром Рея! (ацетилсалициловая кислота)
• Поражение кожи и слизистых оболочек
43
44. Метамизол натрия (INN)
• Анальгин угнетает кроветворение ивызывает агранулоцитоз
• Запрещен к использованию в Австрии в
1965 году, в Норвегии – в 1976 году, в США
- в 1977 году
• Специальные рекомендации ВОЗ о запрете
использования метамизола выпущены в
1991 году
44
45. Синдром Рея
• Острое заболевание с токсическойэнцефалопатией и жировой дегенерацией
органов преимущественно печени и мозга
• Частота варьирует от 0,2 до 4,0% на 100 000
детей, больных простудными заболеваниями
(ОРВИ)
• Наиболее уязвимые возрастные группы – 6-9 и
11-14 лет
45
46. Этиология синдрома Рея
• Вирус гриппа, парагриппа, аденовирусная инфекция,энтеровирусы (Коксаки, ЕСНО), ветряной оспы,
герпеса, Эпштейн-Барр, риносинтициальный вирус
• Токсическая – органофосфаты, пестициды, афлотоксины
(продукты обмена штаммов грибков рода Aspergillus
flavus)
• Врожденные или приобретенные дефекты метаболизма
(матаболизма аммиака, карнитина)
• Применение аспирина на фоне вирусной инфекции
46
47. Клинические стадии синдрома Рея
ПерваяСонливость, заторможенность, неадекватная реакция
на вопросы, неукротимая рвота
Вторая
Ступор, затрудненная речь, атаксия, отсутствие
контакта с окружающими
Третья
Делирий, двигательное возбуждение,
гиперрефлексия, гипервентиляция, патологические
рефлекса, клонус стоп, зрачковые рефлексы и
дыхание сохранены
Четвертая
Кома, декортикционная ригидность, гиповентиляция,
угасание спонтанного дыхания и зрачковых
рефлексов
Пятая
Судороги, остановка дыхания
47
48. Тактика при отравлении салицилатами
• Промывание желудка и введениеактивированного угля (до 15,0)
• В/в инфузии полиионных, коллоидных
растворов и в/в введение петлевых диуретиков
(«метод форсированного диуреза»)
• При ацидозе – в/в раствор натрия
гидрокарбоната
• Физическое охлаждение
• Гемосорбция, гемодиализ
48
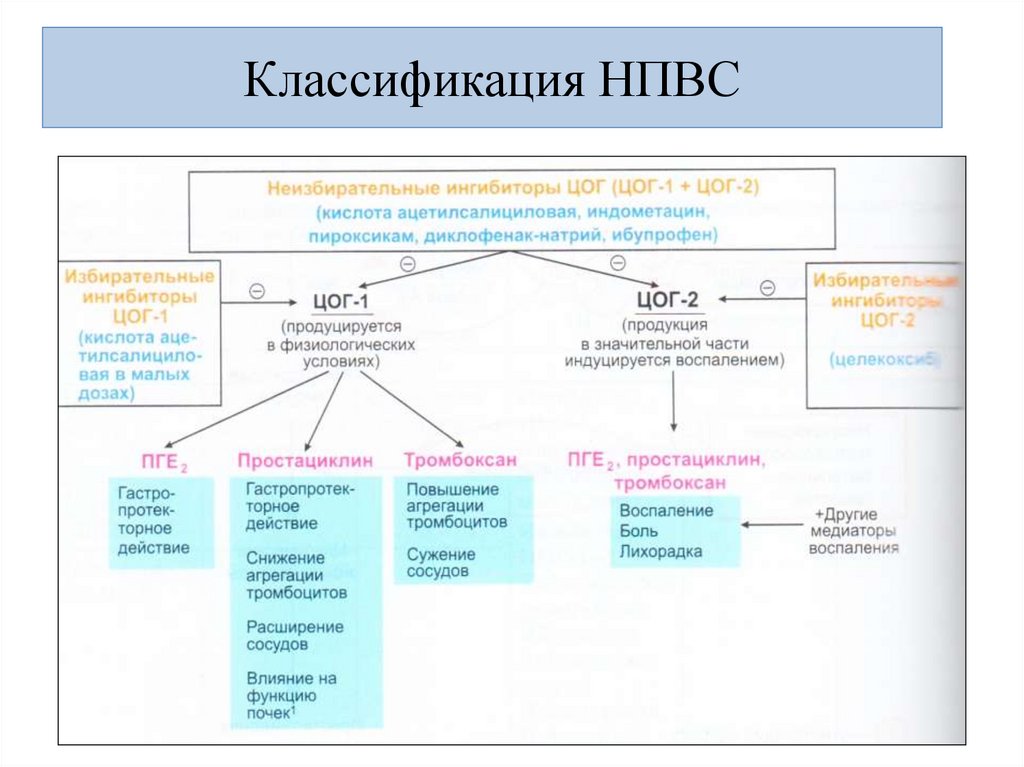
49. Физиологическая роль ЦОГ-1 и ЦОГ-2
ЦОГ1ЦОГ1
ЦОГ2
• Гастропротекция (ПГЕ2, простациклины )
• Нефропротекция, вазодилятация (простациклины)
• Вазоконстрикция (тромбоксан)
• Снижение агрегации тромбоцитов (простациклины)
• Повышение агрегации тромбоцитов (тромбоксан)
• Воспаление
• Боль
(ПГЕ2, простациклин, тромбоксан)
• Лихорадка
49
50. Избирательные ингибиторы ЦОГ-2
• Мелоксикам• Нимесулид
• Набуметон
• Целекоксиб
• Вальдекоксиб
• Эторикоксиб
50
51. Мелоксикам (INN)
• Селективный ингибитор ЦОГ-2 - подавляетсинтез только провоспалительных
простагландинов
• По противовоспалительной активности
мелоксикам не уступает индометацину,
вольтарену
• Биодоступность составляет 80%, Т1/2 - более 200
ч, что позволяет назначать препарат 1 раз в день
по 7,5 или 15 мг во время еды
51
52. Кардиотоксичность НПВС
• Следует соблюдать осторожность у пациентов сзаболеваниями:
• Артериальная гипертензия
• Сердечная недостаточность
• ИБС
• Гиперлипидемия
• Заболевания периферических сосудов
• Диабет
• Никотиновая зависимость
52
53.
СПб ГУ 2025 г.53












































 medicine
medicine








