Similar presentations:
№2_Жай,_бинарлы_және_күрделі_бейорганикалық_заттардың_қатысуымен
1.
2.
Сабақтың тақырыбы:Жай, бинарлы және күрделі
бейорганикалық заттардың
қатысуымен жүретін тотығутотықсыздану реакциялары.
3. https://twig-bilim.kz/kz/film/redox-reactions
https://twig-bilim.kz/kz/film/redoxreactions4.
Валенттілік электрондарыэлектртерістілігі кіші атомдардан
электр терістілігі үлкен
атомдарға ауысатын немесе
ығысатын процестер тотығутотықсыздану реакциялары
деп аталады.
5.
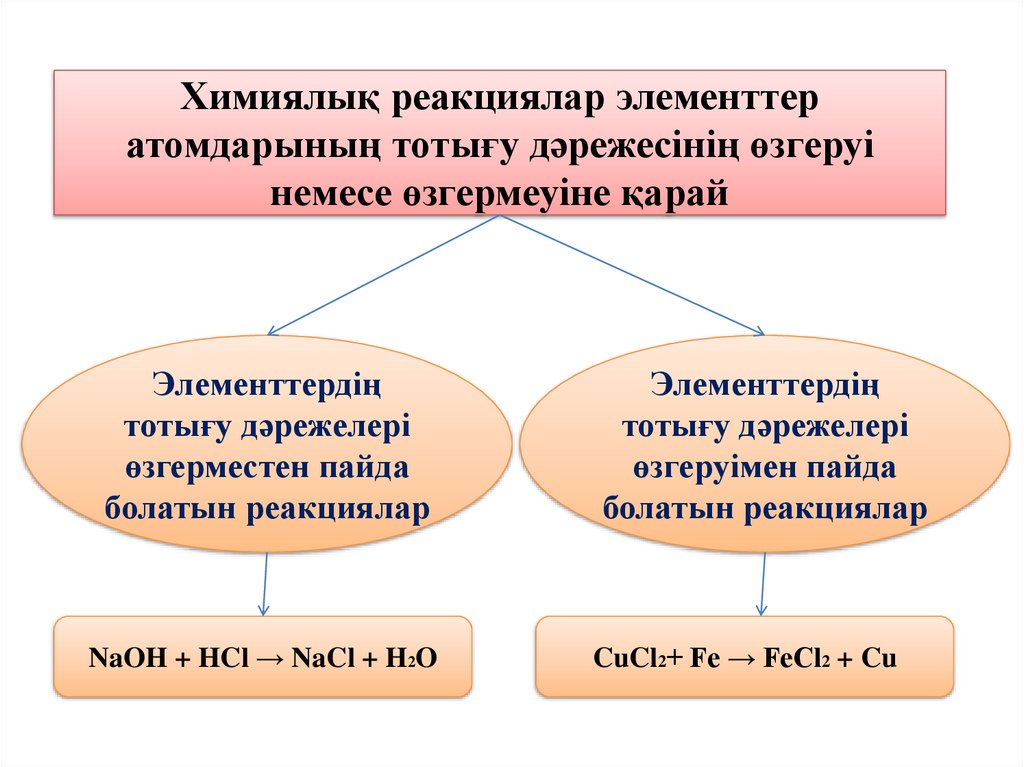
Химиялық реакциялар элементтератомдарының тотығу дәрежесінің өзгеруі
немесе өзгермеуіне қарай
Элементтердің
тотығу дәрежелері
өзгерместен пайда
болатын реакциялар
Элементтердің
тотығу дәрежелері
өзгеруімен пайда
болатын реакциялар
NaOH + HCl → NaCl + H2O
CuCl2+ Fe → FeCl2 + Cu
6.
Ормандағы өртC + O2 → CO2
7.
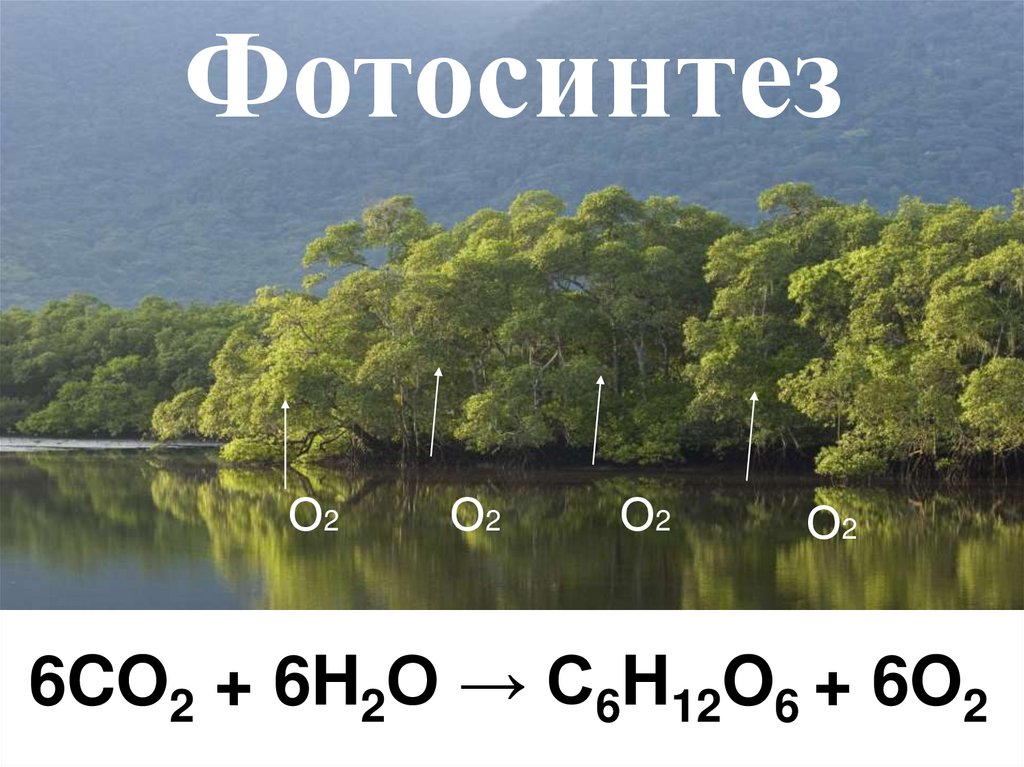
ФотосинтезО2
О2
О2
О2
6CO2 + 6H2O → C6H12O6 + 6O2
8.
Металдар коррозиясы4Fe +6H2O +3O2 → 4Fe(OH)3
9. Аккумуляторлар
Zn +H2SO4 → ZnSO4 + H2↑10. Вулкан жанарғысында
S + O2 → SO211. Глюкозаның ашуы
Ашу цехыC6H12O6 → 2C2H5OH + 2CO2
12. Тотығу дәрежесі
• Жай заттардың құрамына кіретін элементатомының тотығу дәрежесі нөльге тең.
Сутектің тотығу дәрежесі гидридтерден басқа
қосылыстарды +1 тең.
• Оттектің тотығу дәрежесі пероксидтер мен фтор
қосылыстарынан басқа қосылыстарында -2 тең.
• Қосылыстың құрамындағы барлық атомдардың
тотығу дәрежесінің қосындысының жиынтығы
нөльге тең.
• Иондағы атомдардың тотығу дәрежесінің
жиынтық қосындысы ион зарядына тең болады.
Mgº, Cl2º, O2º
+1
+1
-1
HCl, H2O, NaH
-2
-1
+2
H2O, Н2О2, OF2
+1 +6 -2
H2SO4
2(+1)+6+4(-2)=0
+6 -2
SO4
6+4(-2)=-2
13.
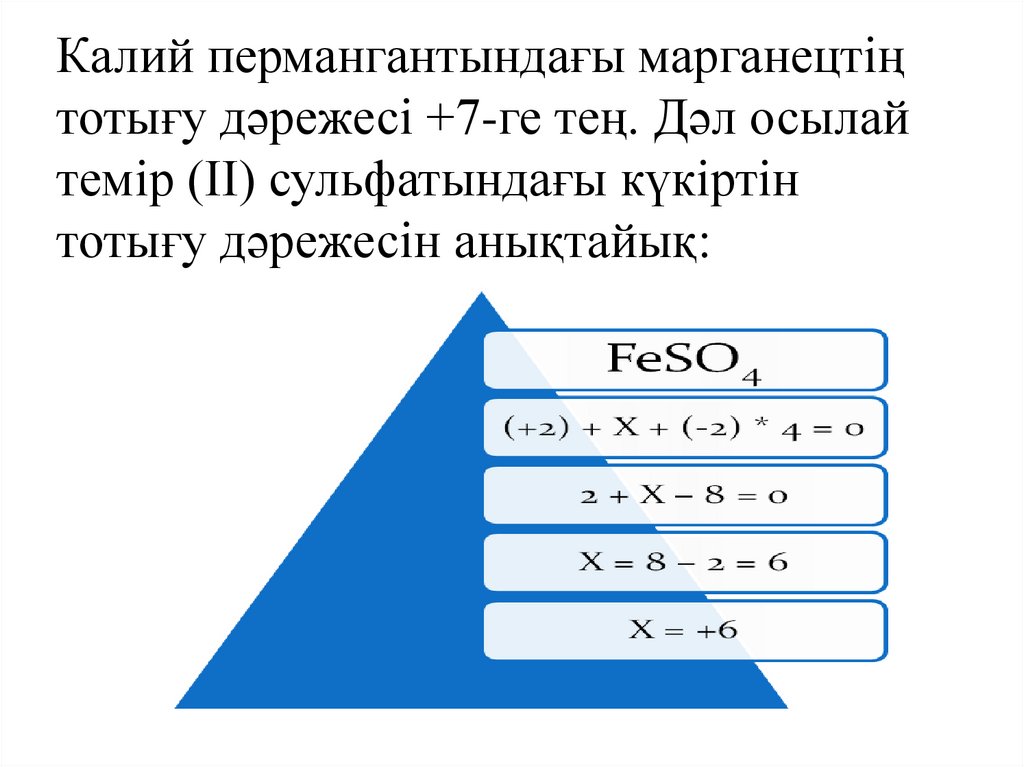
Калий пермангантындағы марганецтіңтотығу дәрежесі +7-ге тең. Дәл осылай
темір (ІІ) сульфатындағы күкіртін
тотығу дәрежесін анықтайық:
14.
Электрондарберу процесі –
тотығу, ал
қосып алу
процесі
тотықсыздану
деп аталады.
Электрондарды
қосып алатын
атомдар немесе
иондар
тотықтырғыш,
ал беретіндері
тотықсыздандырғыш
болады.
Тотықтырғыш
+nē
тотығу дәрежесі төмендейді
Тотықсыздандырғыш
- nē
тотығу дәрежесі артады
тотықсызданады
тотығады
15.
Ең маңыздытотықтырғыштар:
күштілері – F2, O2, O3, H2O2,
Cl2 (әсіресе сулы ерітіндісі),
HClO, HClO3, H2SO4 (тек
концентрлісі), патша арағы
(концентрлі HNO3 және HCl
қоспасы), HNO2, NO2,
KMnO4 (әсіресе қышқыл
ерітіндіде), MnO2, K2Cr2O2,
CrO3, PbO2 және т.б.;
әлсіздері – I2, бром суы
(Br2+H2O), SO2, Fe3+ және
т.б.
Маңызды
тотықсыздандырғыштар:
күштілері – сілтілік және
сілтілік жер металдар,
(әсіресе бөлінген күйінде),
HI және иодидтер, H2S және
сульфидтер, NH3, PH3,
H3PO3, C, CO, Fe2+, Cr2+
және т.б.; әлсіздері –
активтілігі төмен металдар
(Pb, Cu, Ag,Hg), HCl және
хлоридтер, SO2, HNO2 және
т.б.
16.
ТТР мынадай типтері бар:1) тотықтырғыш пен тотықсыздандырғыш әр
түрлі молекулалар құрамына кіретін
молекулааралық реакциялар;
2) тотықтырғыш пен тотықсыздандырғыш бір
молекуланың құрамына кіретін
молекулаішілік реакциялар;
3) бір элемент атомының бір мезетте тотығу
дәрежесінің әрі өсуі, әрі кемуі арқылы жүретін
диспропорциялану реакциялары.
17.
4ē1
2
4 Na O 2 Na O
0
0
2
тотықсыздандырғыш
(тотығады)
тотықтырғыш
(тотықсызданады)
2
2ē
1
2
2 Na S Na S
0
0
тотықсыздандырғыш
тотықтырғыш
(тотығады)
(тотықсызданады)
2
2ē
1
2 Na F2 2 Na F
0
тотықсыздандырғыш
(тотығады)
тотықтырғыш
(тотықсызданады)
1
18.
0-2
S + 2ē → S
Иә
19.
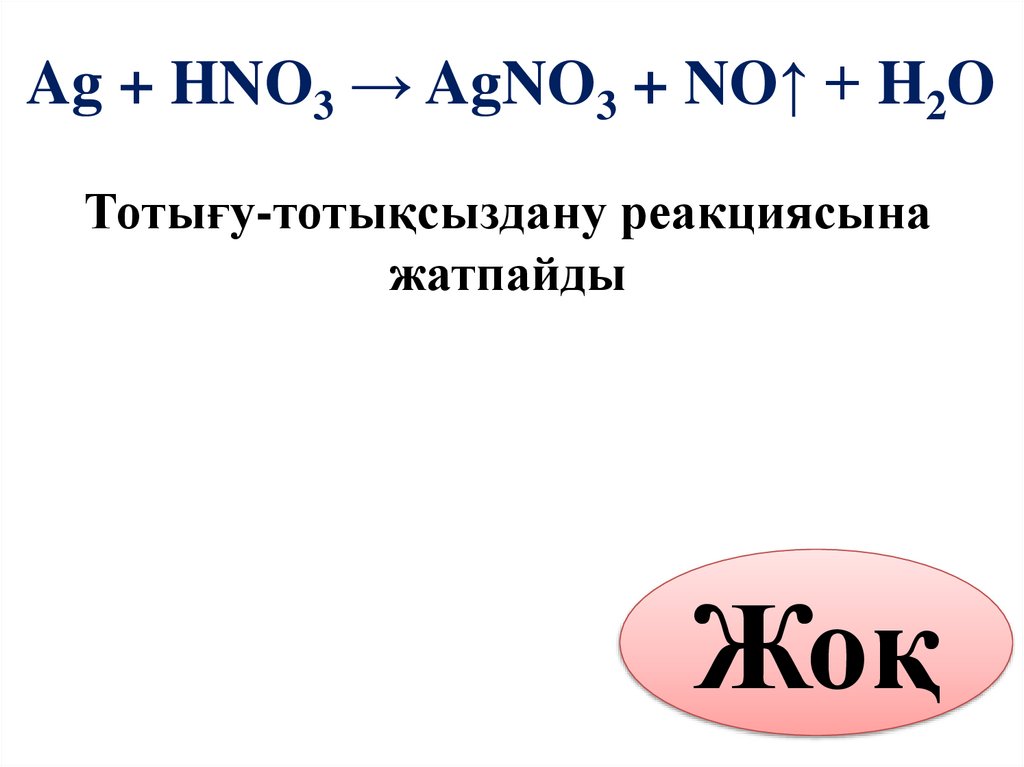
Ag + HNO3 → AgNO3 + NO↑ + H2OТотығу-тотықсыздану реакциясына
жатпайды
Жоқ
20.
0+3
Fe + 3ē → Fe
Иә
21.
+3+2
Fe + 1ē → Fe
Иә
22.
NaOH + HCl = NaCl + H2OТотығу-тотықсыздану реакциясына
жатады
Жоқ
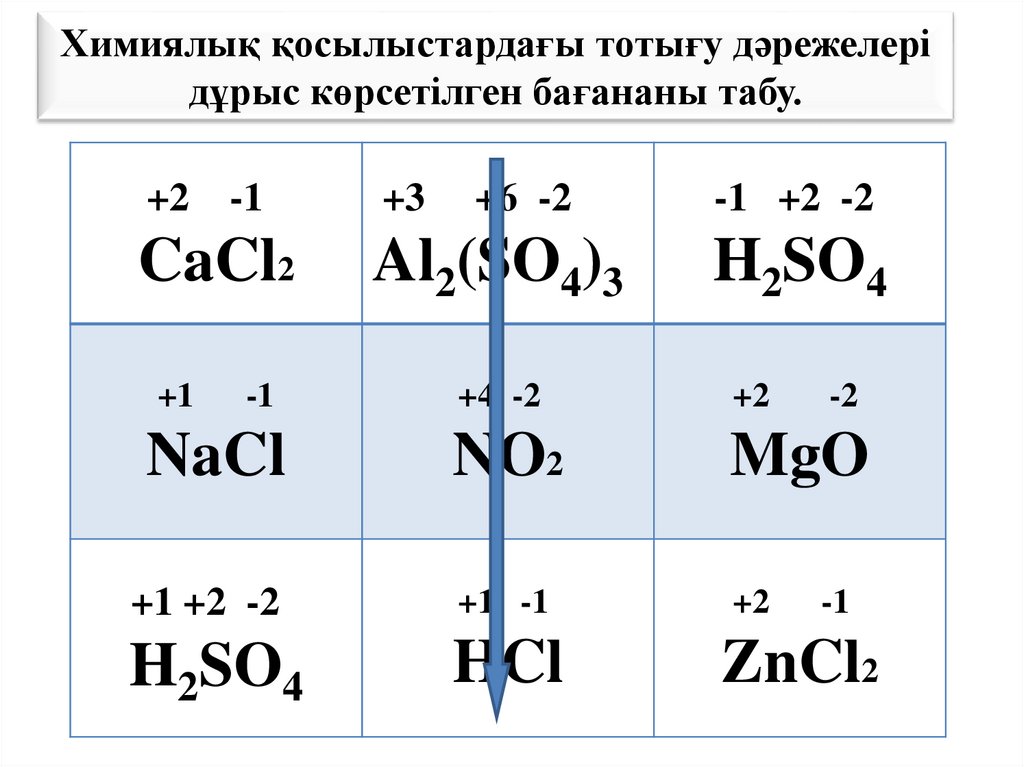
23.
Химиялық қосылыстардағы тотығу дәрежелерідұрыс көрсетілген бағананы табу.
+2
-1
CaCl2
+1
+3
+6 -2
-1 +2 -2
Al2(SO4)3
H2SO4
-1
+4 -2
+2
-2
NaCl
NO2
MgO
+1 +2 -2
+1 -1
+2
H2SO4
HCl
ZnCl2
-1
24.
Тапсырма №1.25.
Тапсырма№2. Жұптық жұмыс.26.
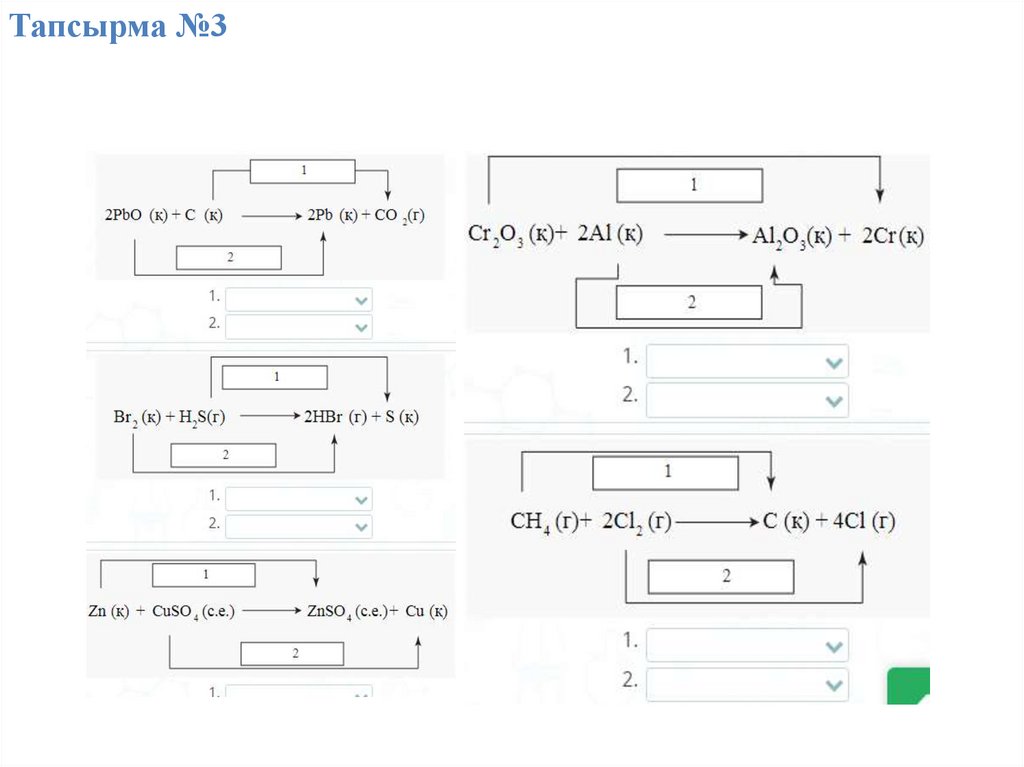
Тапсырма №327.
1211
18
683457129
10
13
15
17
30
14
16
23
20
19
22
21
24
26
25
27
28
29
12
11
18
682134579
10
13
15
17
30
14
16
23
20
19
22
21
24
26
25
27
28
29
12
11
18
682134579
10
13
15
17
30
14
16
23
20
19
22
21
24
26
25
27
28
29












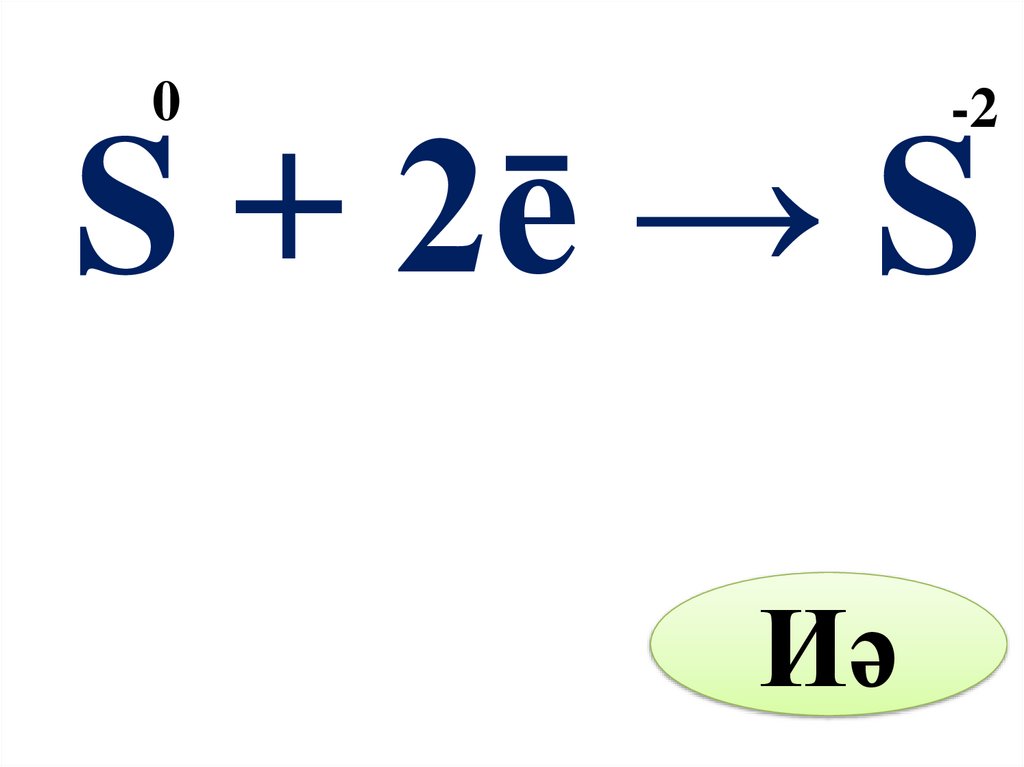
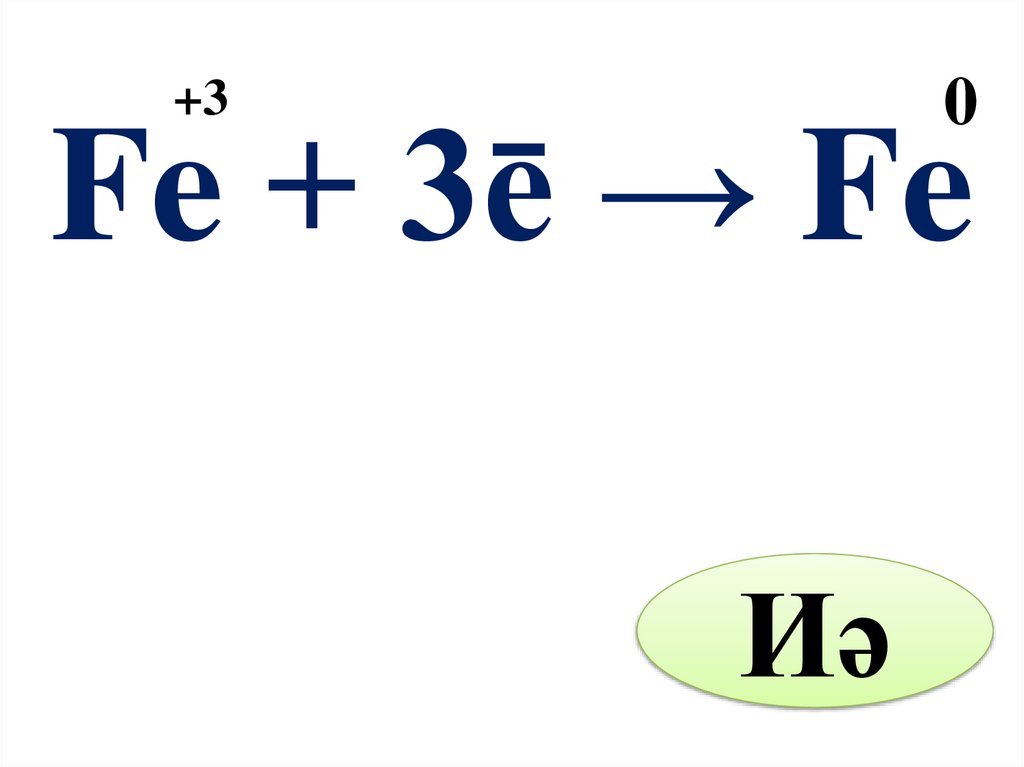
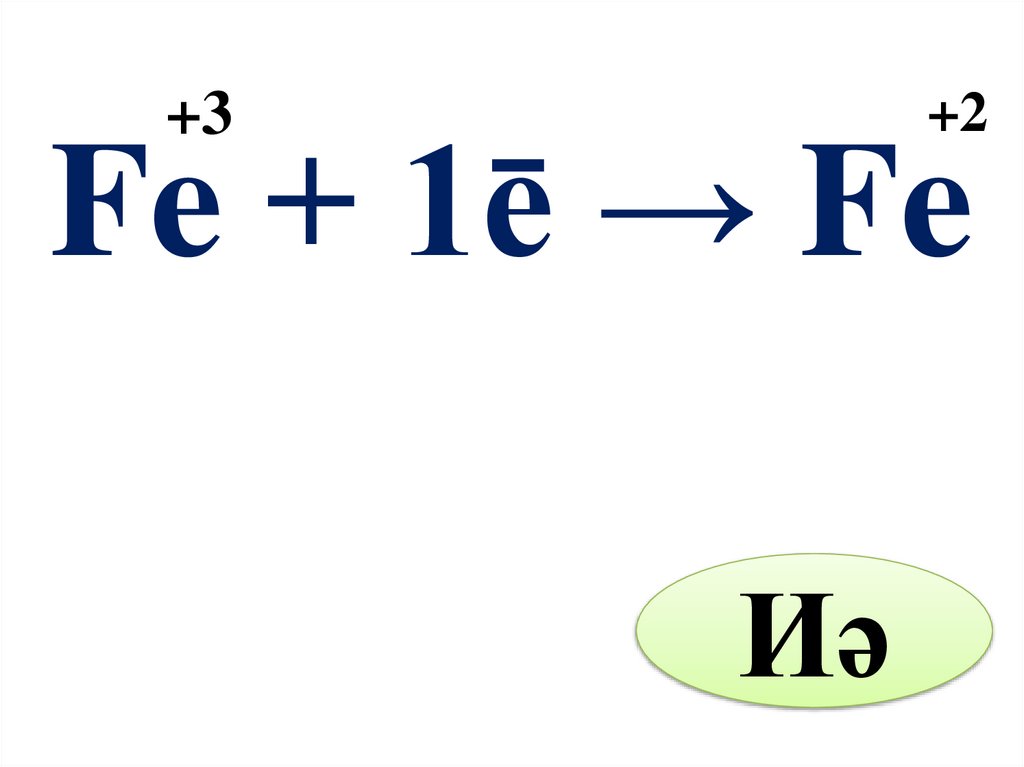




 chemistry
chemistry








