Similar presentations:
Химия элементов 15-16 группы. Лекция 8
1. Лекция 8. Химия элементов 15-16 группы
шцпм.интернатЛекция 8.
Химия элементов
15-16 группы
2.
Элементы 15 группы - пниктогеныN – азот
P – фосфор
As – мышьяк
Sb – сурьма
Bi – висмут
Mc - московий
2
3.
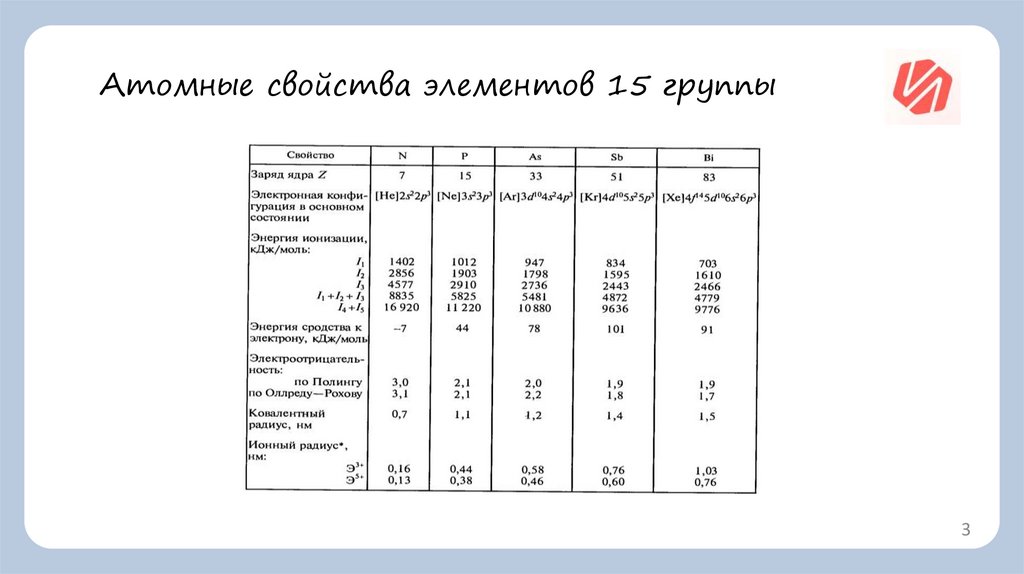
Атомные свойства элементов 15 группы3
4.
Этимология и картинкиАзот (англ. Nitrogen, франц. Azote) был
получен из воздуха в 1772 году Кавендишем.
Название «азот» (от греческой приставки «а» — без, и слова «зоэ» — жизнь, то есть
«безжизненный»).
Фосфор (англ. Phosphorus, франц. Phosphore)
в виде светящегося вещества был открыт в
1669 г. гамбургским алхимиком Брандом.
Название происходит от греч. «фос» – свет и
«феро» – несу, т.е. светоносец.
Мышьяк (англ. и франц. Arsenic, нем. Arsen)
известен с глубокой древности. Название
элемента происходит от греч. «арсеникон».
Русское название «мышьяк» появилось искажённо
от тюркского «маргумуш» (от «мар» — убить и
«муш» — мышь), что означает «мышиный яд».
4
5.
Этимология и картинкиСурьма (англ. Antimony) использовалась для
изготовления предметов и сплавов, а из Sb₂S₃ делали
черный порошок для косметики. Antimonium - «антимонах» (против монахов). Русское название «сурьма»
тюркского происхождения и изначально означало
«грим» или «мазь».
Висмут (англ. Bismuth, нем. Wismut) как металл был
известен в Центральной Европе с XV века, однако
вплоть до XVIII века его часто путали со свинцом,
оловом и сурьмой. Происхождение названия связано с
немецкими словами «wis» и «mat» (искажённое «weisse
Masse» — «белая масса»).
5
6.
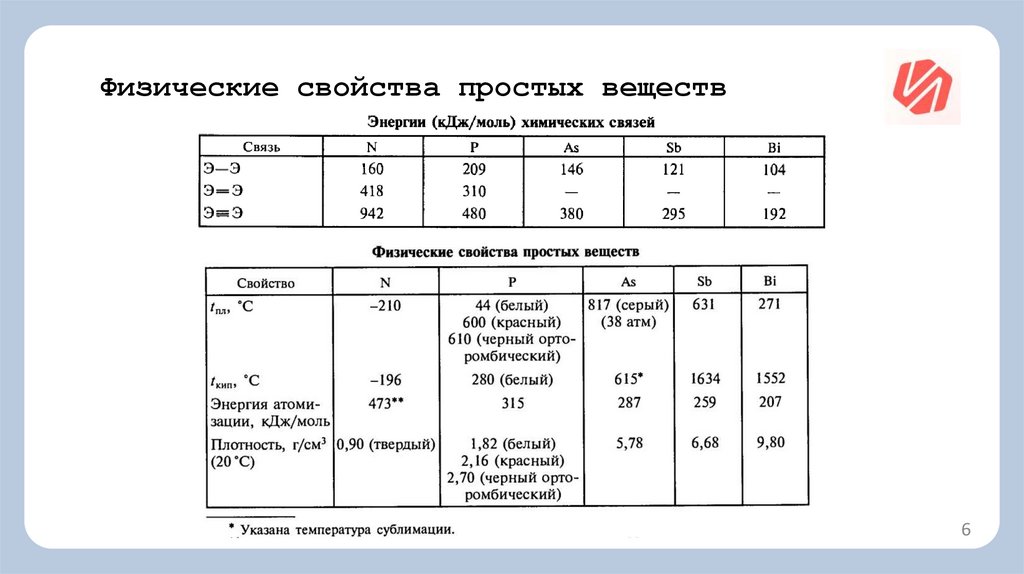
Физические свойства простых веществ6
7.
Простые вещества. АзотПолучение:
Фракционная перегонка жидкого воздуха
Сосуд Дьюара
Применение:
• Создание инертной атмосферы
• Синтез аммиака (процесс
Габера-Боша)
• Охлаждение
7
8.
Простые вещества. ФосфорПолучение (из апатитов):
Применение:
Белый
Красный
Фиолетовый
Чёрный
• Фосфорные удобрения
• Пищевая
промышленность
• Химический синтез
8
9.
Простые вещества. МышьякРеальгар As4S4
Аурипигмент As2S3
Получение:
Применение:
Легирование сплавов
Производство стёкол
Полупроводники (GaAs)
Медицина
Крысиный яд
9
10.
Простые вещества. СурьмаСурьмяный блеск Sb2S3
Получение:
Применение:
• Сплавы со свинцом (в
аккумуляторах)
• Полупроводники
• Фотоэлектроника
• Катализ
• Косметика
10
11.
Простые вещества. ВисмутПолучение:
Висмутин Bi2S3
Применение:
• Сплавы
• Нефтехимический
катализ
• Полупроводники
• Медицина
11
12.
Свойства азота12
13.
Свойства соединений азота13
14.
Свойства фосфораH3PO2 + 4FeCl3 + H2O = H3PO4 + 4FeCl2 + 4HCl
14
15.
Свойства мышьяка и сурьмы15
16.
Свойства висмута16
17.
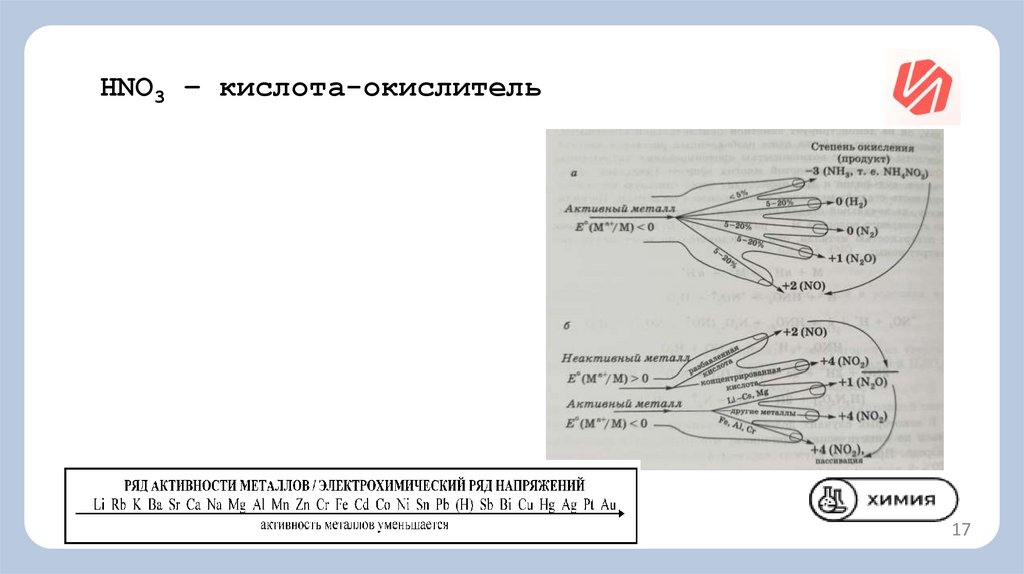
HNO3 – кислота-окислитель17
18.
Оксиды азота18
19.
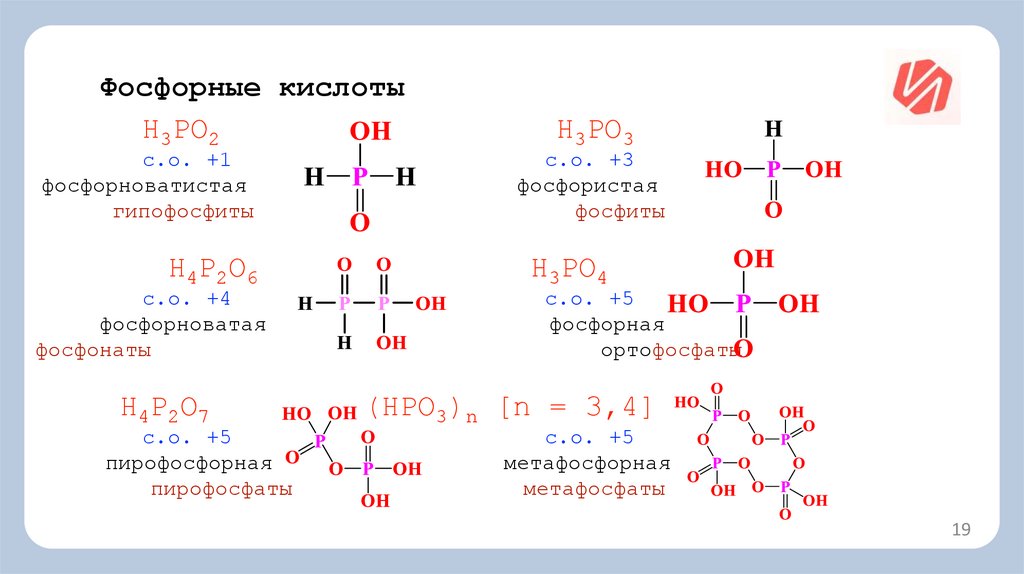
Фосфорные кислотыH3PO2
с.о. +1
фосфорноватистая
гипофосфиты
H 4 P2 O6
с.о. +4
фосфорноватая
фосфонаты
H4 P2 O 7
с.о. +5
пирофосфорная
пирофосфаты
H3PO3
с.о. +3
фосфористая
фосфиты
H3PO4
с.о. +5
фосфорная
ортофосфаты
(HPO3)n [n = 3,4]
с.о. +5
метафосфорная
метафосфаты
19
20.
Элементы 16 группы - халькогеныO – кислород
S – сера
Se – селен
Te – теллур
Po – полоний
Lv – ливерморий
20
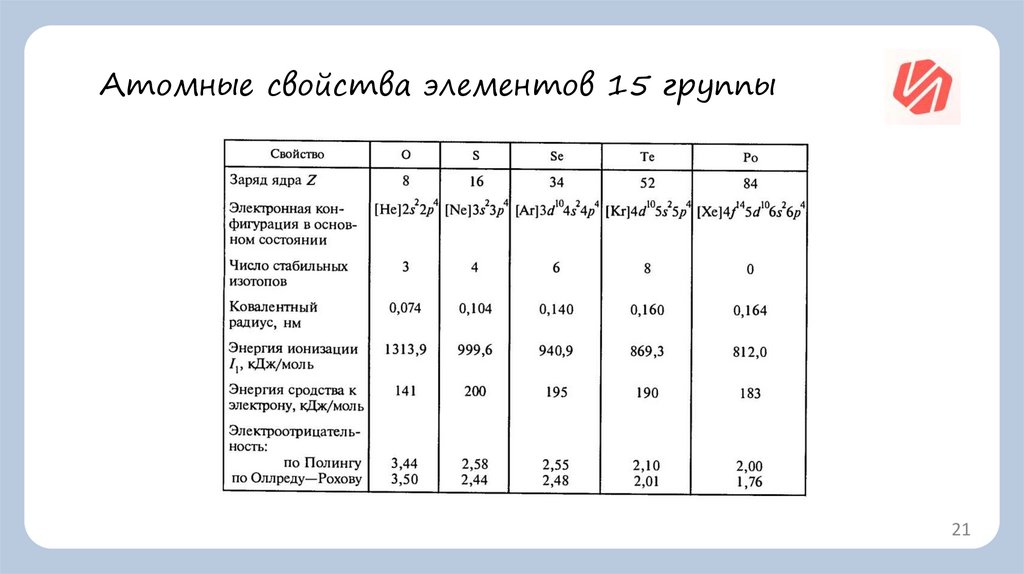
21.
Атомные свойства элементов 15 группы21
22.
Этимология и картинкиКислород (англ. Oxygen) был впервые получен нагреванием
оксида ртути. Ошибочно полагая, что этот газ является
обязательным началом всех кислот, Лавуазье ввёл для него
новое название от греческих слов «оксис» (кислый) и «генао»
(рождаю).
Сера (англ. Sulfur, нем. Schwefel) известна с
древнейших времен в самородном состоянии и в
виде соединений. Происхождение названия
«Sulfur» неясно. Древнерусское название
«сера», по-видимому, происходит от
санскритского слова «сirа» (светло-желтый).
Селен (англ. Selenium, франц. Selenium, нем.
Selen) был открыт при исследовании осадка
производства серной кислоты. Берцелиус ожидал
найти теллур, но открыл элемент, который назвал
селеном (от греч. «σελήνη» — Луна).
22
23.
Этимология и картинкиТеллур (англ. Tellurium, нем. Tellur) был открыт в конце
XVIII века. В 1782 году горный инспектор Франц Йозеф
Мюллер (фон Рейхенштейн), исследуя золотоносную руду из
Трансильвании, предположил, что выделил из неё новый
металл. Название «теллур» от латинского «tellus» (Земля).
Полоний (англ. Polonium) был открыт в 1898 году Марией
Кюри-Склодовской. Исследуя урановую смолку, она
обнаружила, что её радиоактивность значительно выше, чем у
чистого урана, и выделила две высокоактивные фракции. Из
фракции, содержащей соли висмута, был получен новый
химический элемент, активность которого в 400 раз
превышала активность урана. Кюри-Склодовская назвала его
полонием (Polonium) в честь своей родины — Польши (лат.
Polonia).
23
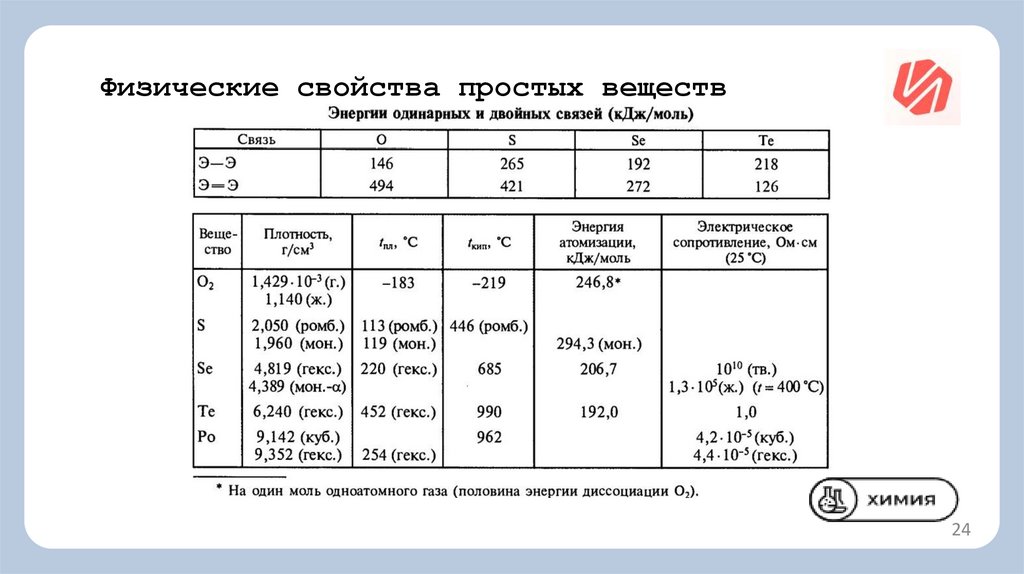
24.
Физические свойства простых веществ24
25.
Простые вещества. КислородПолучение:
Фракционная перегонка жидкого
воздуха
Кислород O2
Применение:
Озон O3
Металлургия
Космонавтика
Медицина
Промышленный синтез
Сельское хозяйство
25
26.
Простые вещества. СераПолучение:
Самородная S или из попутного H2S
Применение:
• Производство
аккумуляторов
• Сельское хозяйство
• Резина и текстиль
• Медицина
26
27.
Простые вещества. СеленПолучение:
Из сульфидных минералов Cu, Ag при
электролитическом рафинировании
металла (анодный шлам)
Применение:
• БАДы и удобрения
• Фотоэлектроника и
полупроводники
• Стёкла
• Пигменты
27
28.
Простые вещества. ТеллурПолучение:
Из сульфидных минералов Cu, Ag
при электролитическом
рафинировании металла (анодный
шлам)
Применение:
CdTe
• Металлургия
• Фотоэлектроника и
полупроводники
• Медицина
28
29.
Свойства кислорода29
30.
Свойства серы, селена и теллура1) С неметаллами:
2) Со щелочью:
3) С кислотами:
4) Халькогениды:
30
31.
Свойства серы, селена и теллура31
32.
H2SO4 – кислота-окислитель32
33.
Соединения серы с кислородом33
34.
Сравнение силы кислот. Магическая кислота34




























 chemistry
chemistry








