Similar presentations:
Алюминий. Группы элементов
1.
ПРЕЗЕНТАЦИЯ1
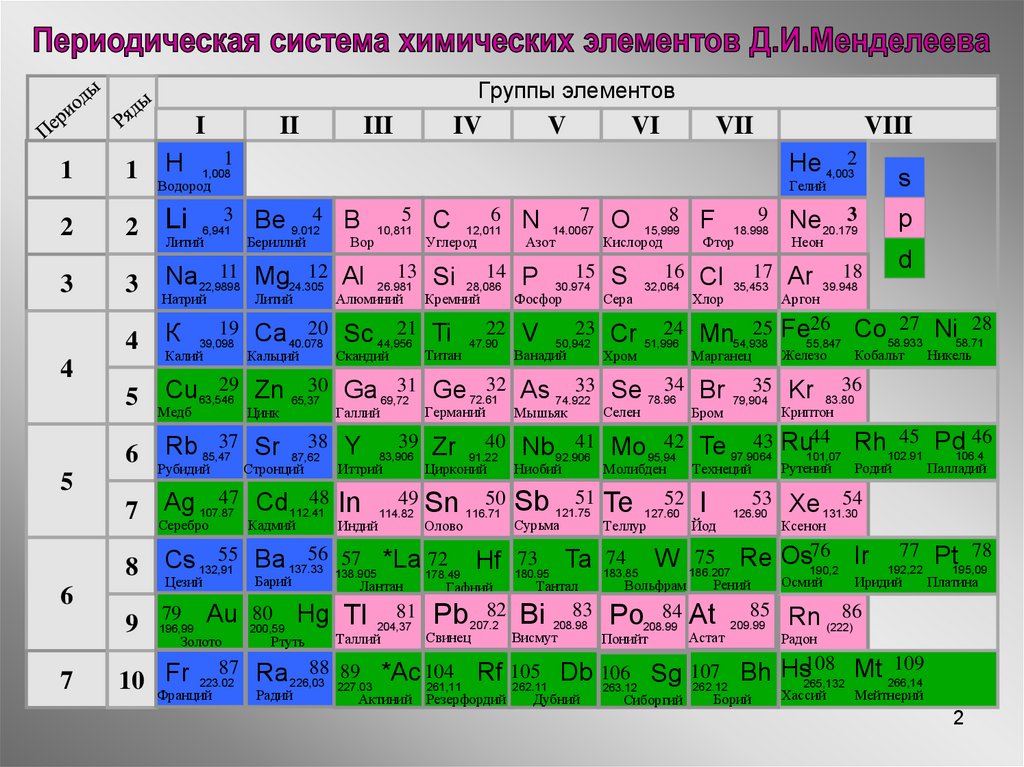
2.
Группы элементовI
1
1
2
2
3
3
4
4
5
6
5
7
8
6
9
7
Н
II
III
IV
V
VI
VII
VIII
1
1,008
Водород
Li
3
6,941
Литий
Be 9.0124 В
Бериллий
Вор
11 Mg 12 Al
Na22,9898
24.305
Натрий
К
Литий
19
39,098
Калий
5
10,811
13
26.981
Алюминий
С
Углерод
Si
Титан
Скандий
14
28,086
Кремний
20 Sc 21 Ti
Ca 40.078
44,956
Кальций
6
12,011
22
47.90
N
7
14.0067
Азот
P
15
30.974
Фосфор
V
23
50,942
Ванадий
О
8
15,999
Кислород
S
Сера
16
32,064
9
F
18.998
Фтор
17
Cl
35,453
Хлор
Цинк
Rb 85,4737 Sr
Рубидий
38
87,62
Стронций
Кадмий
39
Y
83,906
Иттрий
47 Cd 48 In
Ag 107.87
112.41
Серебро
Германий
Галлий
49
Индий
114.82
Zr
Мышьяк
40
91.22
Цирконий
Хром
55 Ba 56 57 *La 72 Hf
Cs 132,91
137.33 138.905
178.49
Барий
Цезий
79
196,99
Au
Золото
80
200,59
Лантан
Hg Tl
Ртуть
87 Ra 88
Fr 223.02
226,03
10 Франций
Радий
81
204,37
Таллий
89
227.03
Гафний
Резерфордий
Ne 20.1793
p
18
d
Неон
Ar
Аргон
39.948
Kr
Кобальт
Никель
36
83.80
Криптон
41 Mo 42 Te 43 Ru44 Rh 45 Pd 46
Nb 92.906
102.91
106.4
101,07
97.9064
95,94
Ниобий
Молибден
Сурьма
73
180.95
52
127.60
Теллур
Ta
Тантал
74
183.85
W
Вольфрам
Висмут
Понийт
*Ac 104
Rf 105
Db 106
Sg
261,11
262.11
263.12
Актиний
35
79,904
Бром
Дубний
Сиборгий
Рутений
Технеций
53
I
126.90
Йод
75
186.207
Астат
107
262.12
Родий
85
209.99
Палладий
54
Xe 131.30
Ксенон
76 Ir
Re Os190,2
Рений
83 Po 84 At
Pb 207.282 Bi 208.98
208.99
Свинец
s
Железо
Марганец
Селен
50 Sb 51 Te
Sn 116.71
121.75
Олово
Гелий
24 Mn 25 Fe26 Co 27 Ni 28
Cr 51,996
58.933
58.71
55,847
54,938
29 Zn 30 Ga 31 Ge 32 As 33 Se 34 Br
Cu 63,546
72.61
78.96
65,37
69,72
74.922
Медб
Не 4,0032
Осмий
77
192,22
Иридий
78
Pt195,09
Платина
Rn (222)86
Радон
108 Mt 109
Bh Hs265,132
266,14
Борий
Хассий
Мейтнерий
2
3.
Группы элементовI
1
1
2
2
3
3
5
7
IV
Аl
27
4
6
III
V
VI
+13
0
Открытие
элемента
Содержание в
земной коре
(масс.)
Важнейшие
минералы
8
6
9
7
VII
VIII
Подробнее
4
5
II
Радиус атома,
нм
1825 год Х.Эрстед
1827 год Ф.Велер
8,8%
Алюмосиликаты
Боксит
Корунд
Глинозем
0,143
10
3
4.
1. Из истории открытия2. Электронное строение
3. Строение простого вещества
4. Физические свойства
5. Свойства атома
6. Химические свойства
7. Нахождение в природе
8. Получение
9. Применение
4
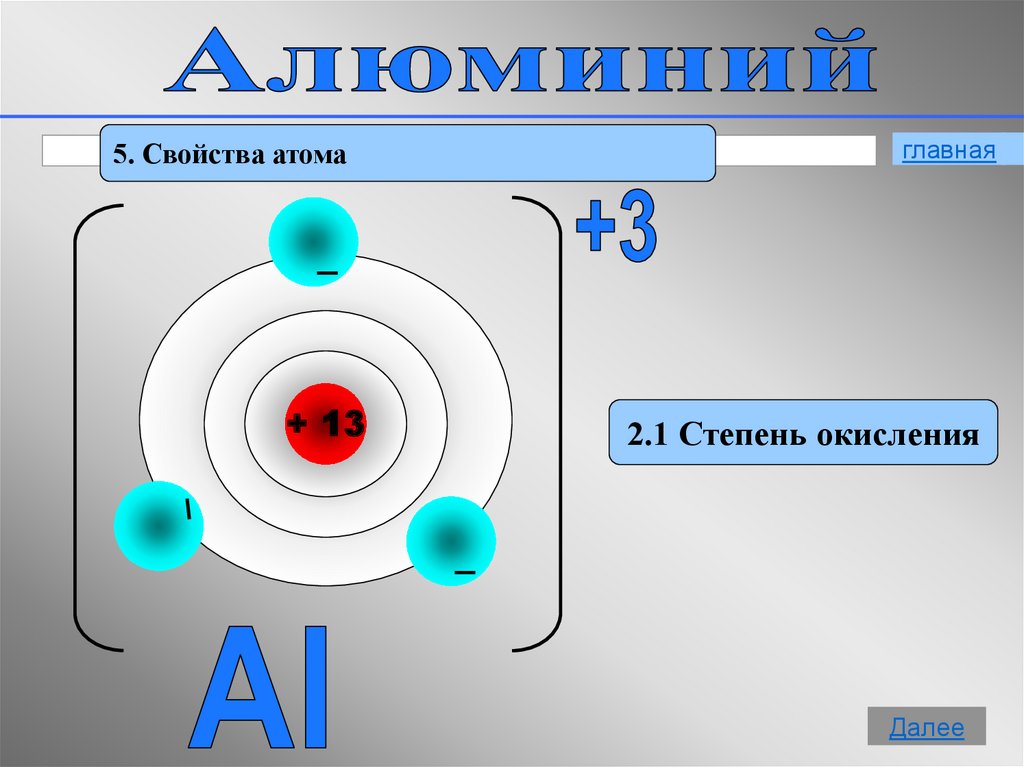
5.
1. Из истории открытияглавная
Впервые Al был получен датским физиком Эрстедом Х.
в 1825 г. Название элемента происходит от лат.
алюмен, так в древности называли квасцы,
которые использовали для крашения
тканей (KAl(SO4)2 . 12H2O).
Позже в 1827 г. немецкий химик
Фридрих Велер получил алюминий
следующим способом:
t
AlCl3+3K
3KCl + Al
Далее5
6.
1. Из истории открытияГлавная
В период открытия алюминия металл был дороже золота. Англичане
хотели почтить богатым подарком
великого русского химика Д.И
Менделеева, подарили ему
химические весы, в которых одна
чашка была изготовлена из золота,
другая - из алюминия. Чашка из
алюминия стала дороже золотой.
Полученное «серебро из глины»
заинтересовало не только учёных, но
и промышленников и даже
императора Франции.
Далее
Далее6
7.
2. Электронное строениеАl
27
+13
0
P+ = 13
e- = 13
n0 = 14
2e
8e
Порядок заполнения
3e
3s2
2s2
главная
3p1
2p6
1s2
Далее
Краткая электронная запись
7
8.
3.Строение простого веществаглавная
Металл
Связь - металлическая
Кристаллическая решетка металлическая,
кубическая
гранецентрированная
Далее8
9.
4. Физические свойстваглавная
Цвет – серебристо-белый
t пл. = 660°C.
t кип. ≈ 2450°C.
Электропроводный, теплопроводный
Легкий, плотность ρ = 2,6989 г/см3
Мягкий, пластичный.
Далее9
10.
5. Свойства атома+ 13
главная
2.1 Степень окисления
10
Далее
11.
5. Свойства атомаглавная
Группы элементов
I
II
III
IV
V
VI
VII
VIII
1
B
2
3
Na
Mg
Al
2.2 Восстановительные
4
Ga
Электрохимический ряд напряжений металлов
Li, K, Ca, Na, Mg, Al, Cr, Zn, Fe, Co, Pb,H2,Cu,Hg,Ag
5
Ослабление восстановительных свойств
11
Далее
12.
главная6. Химические свойства
C н е м е т а л л а м и (c кислородом, с серой)
C неметаллами (c галогенами, с углеродом)
C водой
C кислотами
Cо щ е л о ч а м и
C
оксидами
металлов
2Аl
3Cl
=
2AlCl
оксидную
пленку)
8Al (Снять
++ 3Fe
O
=
4Al
O
+
9Fe
4Аl
3O
=
2Al
O
2Al
6HCl
=
2AlCl
+
H
2
3
2Al + 6NaOH
++
6H
O
=
2Na
[Al(OH)
3
4
2
3
2
2
2]↑+ 3H2↑
2
3 3
6
t
2Al
++2NaOH
+
2H
O
=2NaAlO
+3H
↑
2Al
+
6H
O
=
2Al(OH)
+
H
↑
2
2
2
2Al
+
WO
=
Al
O
+
W
2Al
3H
SO
=
Al
(SO
)
+
H
↑
2Al
+
3S
=
Al
S
2
2
4Al
C
3
3
2 2 43C
22 2
4
3
2
3
4
12
Далее
13.
7. Содержание в земной кореглавная
Кислород - 49%
Кремний - 26%
Алюминий - 7%
Железо - 5%
Кальций - 4%
Натрий - 2%
Калий - 2%
Магний - 2%
Водород - 1%
Остальные - 2%
13
Далее
14.
7. Нахождение в природеглавная
Алюмосиликаты
Полевой шпат (ортоклаз) – K2O*Al2O3*6SiO2
Нефелин - Na2O * Al2O3 * 2SiO2
Каолин – Al2O3 * 2SiO2 * 2H2O
Корунд – Al2O3
Рубин (красный Cr+3)
Сапфир (синийTi+4, Fe+2, Fe+3)
Бокситы – Al2O3
Глинозем – Al2O3
14
Далее
15.
8. Получениеглавная
1825 год Х. Эрстед:
AlCl3 + 3K = 3KCl + Al :
Электролиз (t пл. = 2050°С) :
2Al2O3 = 4Al +3O2
Электролиз (в распл. криолите Na3AlF6, tпл.≈1000°С) :
2Al2O3 = 4Al +3O2
15
Далее
16.
главная9. Применение
Легкость
Теплопроводность
Электропроводность
Алюминий
Пластичность
Нетоксичность
16
Далее














 chemistry
chemistry








