Similar presentations:
Вычисление термодинамических характеристик конденсированной системы
1.
Расчетная работа 1Раздел: Углубленное математическое описание
изменений экстенсивных свойств
однокомпонентных и многокомпонентных систем
Тема: Вычисление термодинамических характеристик
конденсированной системы
2.
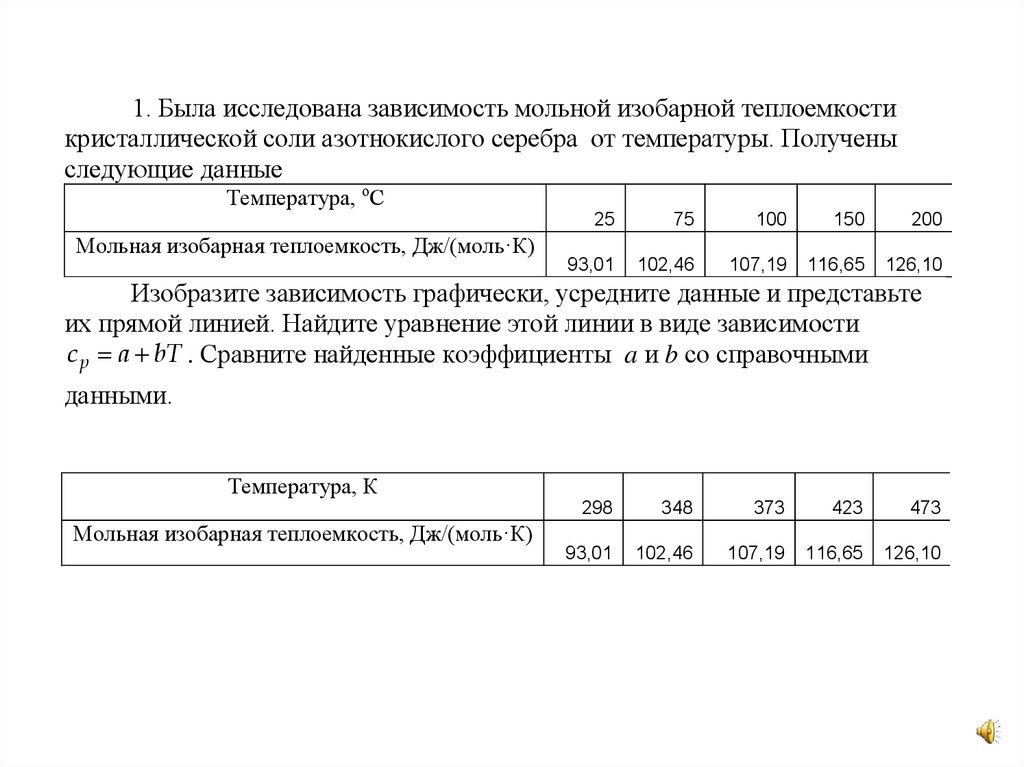
1. Была исследована зависимость мольной изобарной теплоемкостикристаллической соли азотнокислого серебра от температуры. Получены следующие
данные
Температура, оС
Мольная изобарная теплоемкость, Дж/(моль·К)
25
75
100
150
200
93,01
102,46
107,19
116,65
126,10
Изобразите зависимость графически, усредните данные и представьте их прямой
линией. Найдите уравнение этой линии в виде зависимости с p a bT .
Сравните найденные коэффициенты a и b со справочными данными.
2. Используя справочные данные по температурной зависимости теплоемкости,
определите изменение следующих термодинамических функций при переводе 1 моль
кристаллической соли от температуры 25 оС до температуры 150 оС при постоянном
давлении:
2.1. изменение энтропии;
2.2. изменение энтальпии;
2.3. изменение энергии Гиббса.
3. Вычислите при таком изобарическом переходе изменение мольного объема соли,
если коэффициент изобарической расширяемости не зависит от температуры и равен
0,000192 К-1 .
3.
1. Была исследована зависимость мольной изобарной теплоемкостикристаллической соли азотнокислого серебра от температуры. Получены
следующие данные
Температура, оС
Мольная изобарная теплоемкость, Дж/(моль·К)
25
75
100
150
200
93,01
102,46
107,19
116,65
126,10
Изобразите зависимость графически, усредните данные и представьте
их прямой линией. Найдите уравнение этой линии в виде зависимости
с p a bT . Сравните найденные коэффициенты a и b со справочными
данными.
Температура, К
Мольная изобарная теплоемкость, Дж/(моль·К)
298
348
373
423
473
93,01
102,46
107,19
116,65
126,10
4.
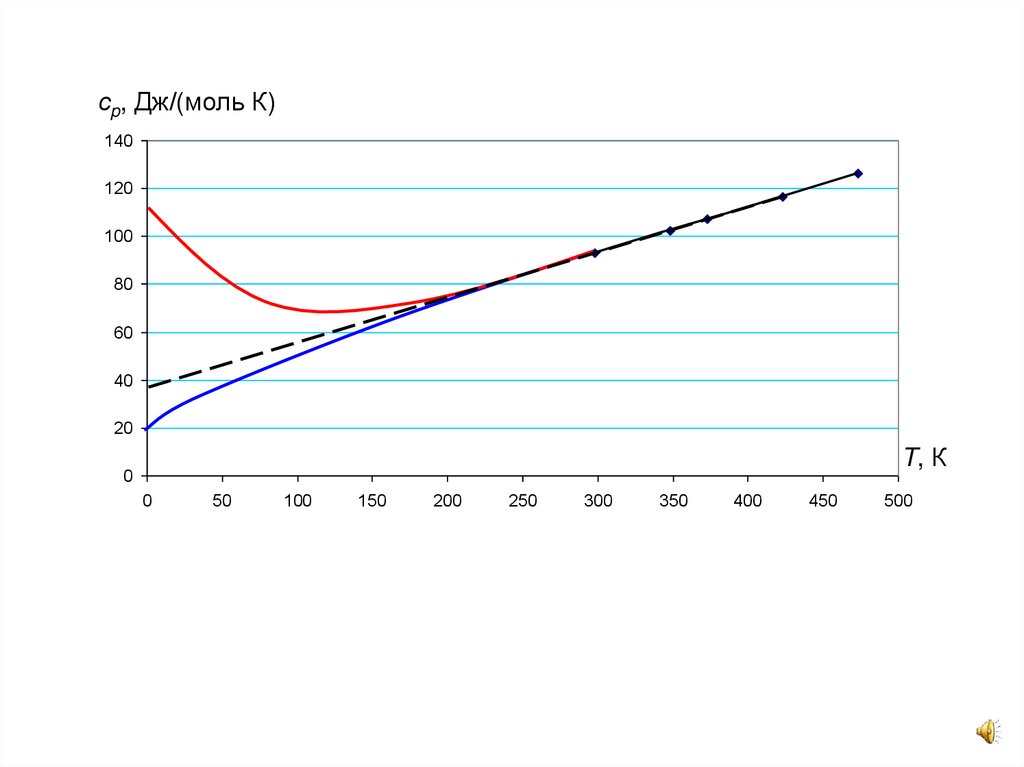
сp, Дж/(моль К)140
120
100
80
60
40
20
0
0
50
100
150
200
250
300
350
400
450
500
T, К
5.
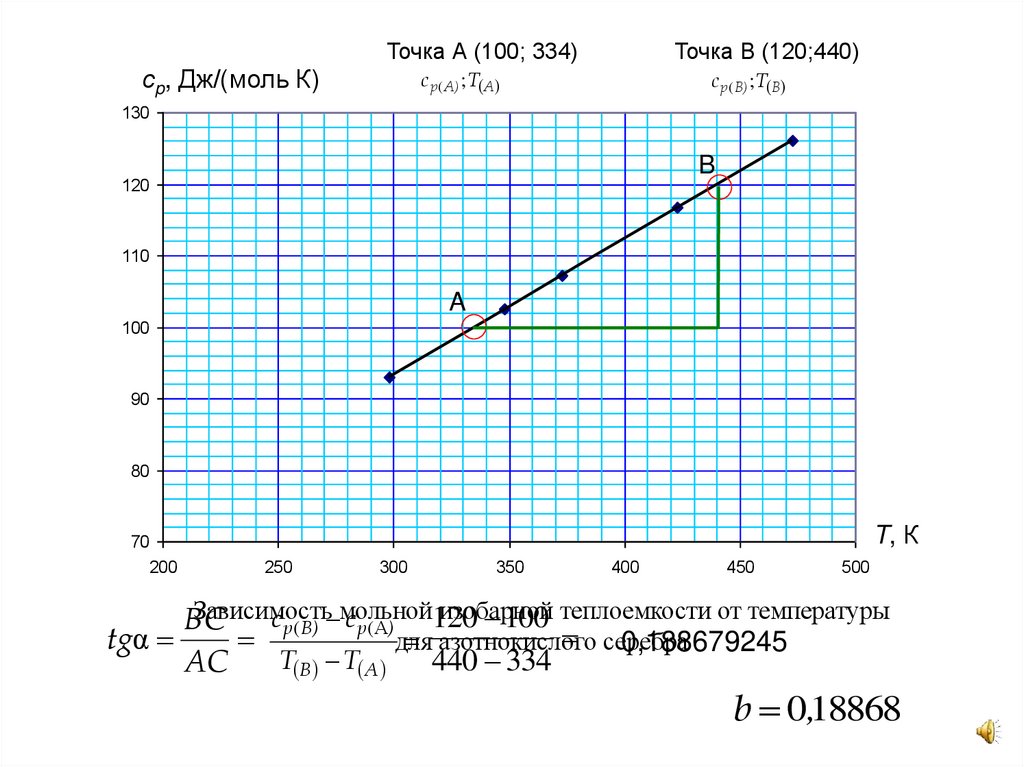
Точка А (100; 334)сp, Дж/(моль К)
Точка В (120;440)
с p ( A) ; T A
с p ( B) ; T B
130
B
120
110
A
100
90
80
70
200
T, К
250
300
350
400
450
500
Зависимость
изобарной
с p ( B) мольной
с p (А) 120
100 теплоемкости от температуры
BC
серебра
tgα
азотнокислого
для
0,188679245
T
T
440
334
AC
В
A
b 0,18868
6.
100100
90
90
80
80
70
200
250
300
70
0200
350
250
400
300
450
500
350
7.
сp, Дж/(моль К)140
120
100
80
60
40
20
T, К
0
0
50
100
150
200
250
300
350
400
450
500
8.
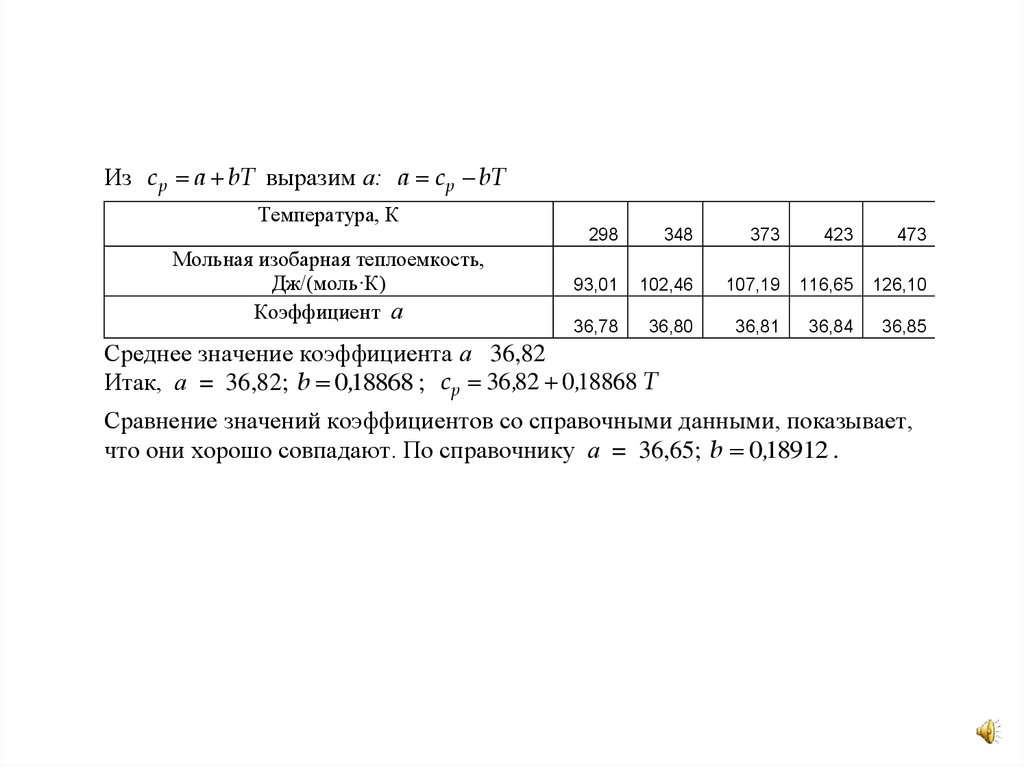
Из с p a bT выразим а: a c p bTТемпература, К
Мольная изобарная теплоемкость,
Дж/(моль·К)
Коэффициент а
298
348
373
423
473
93,01
102,46
107,19
116,65
126,10
36,78
36,80
36,81
36,84
36,85
Среднее значение коэффициента а 36,82
Итак, а = 36,82; b 0,18868 ; с p 36 ,82 0,18868 T
Сравнение значений коэффициентов со справочными данными, показывает,
что они хорошо совпадают. По справочнику а = 36,65; b 0,18912 .
9.
2. Используя справочные данные по температурной зависимоститеплоемкости, определите изменение следующих термодинамических
функций при переводе 1 моль кристаллической соли от температуры 25 оС до
температуры 150 оС при постоянном давлении:
2.1. изменение энтропии;
2.2. изменение энтальпии;
2.3. изменение энергии Гиббса.
В общем виде
e f T , p
e
e
de dT dp
T p
p T
e : s,h , g ,v
e
de dT
T p
10.
Изменение энтропииs
cp T
T p
T2
T2
T1
ds
c p T
ds T dT
T1
s
ds dT
T p
T2
s
T1
a bT dT
T
T2
T1
cp
T
dT
a
dT
T
T2
T1
T2
s aln b(T2 T1 )
T1
423
s 36,65 ln
0,18912 (423 298) 36,48 Дж/(моль К)
298
bT
dT
T
11.
hdh dT
T p
h
cp
T p
T2
dh c p dT
T2
dh cp T dT
T1
Изменение энтальпии
T1
h
T2
T2
T2
T1
T1
T1
a
bT
dT
adT
bTdT
b 2
h a(T2 T1 ) T2 T12
2
0,18912
h 36,65(423 298)
4232 2982
2
=13103,47 Дж/моль
12.
Изменение энергии Гиббсаg h Ts
g h T s
g g2 g1
g1 h1 T1s1
g2 h2 T2s2
g h2 h1 T1s1 T2s2
13.
s s2 s1s2 s s1
g h T1s1 T2s2 h T2 s s1 T2 T1
g h T2 s s1 T
s1 140 ,92
Дж/(моль К)
g 13103 ,47 423 36,48 140 ,92 125
= - 19942,57 Дж/моль
14.
3. Вычислите при таком изобарическом переходе изменение мольногообъема соли, если коэффициент изобарической расширяемости не зависит от
температуры и равен 0,000192 К-1 .
ln
v f ( p ,T )
v
dv dT
T p
1 v
α
v T p
dv αvdT
dv
α dT
v
dln v αdT
vT2
vT1
α (T2 T1 )
vT2 vT1 exp α(T2 T1 )
v vT2 vT1 vT1 exp α T2 T1 1
V VM M
v
n
m
ρ
15.
Критерии оценивания РР-1В отчете по РР-1 должны быть:
1) корректно оформленный график зависимости (на
миллиметровой бумаге, с линейкой и карандашом), правильное
оформление осей, название. Необходимые построения на
графике, корректные вычисления коэффициентов;
2) логика вычисления изменений энтропии и энтальпии,
расчетные формулы;
3) вычисления этих изменений с подстановкой чисел и
указанием в конце размерности полученных величин;
4) логика расчета изменения энергии Гиббса, вывод формулы,
нахождение необходимых справочных величин и расчет
изменения энергии Гиббса;
5) логика вычисления изменения мольного объема,
нахождение необходимых справочных величин, конечная
формула, расчет.






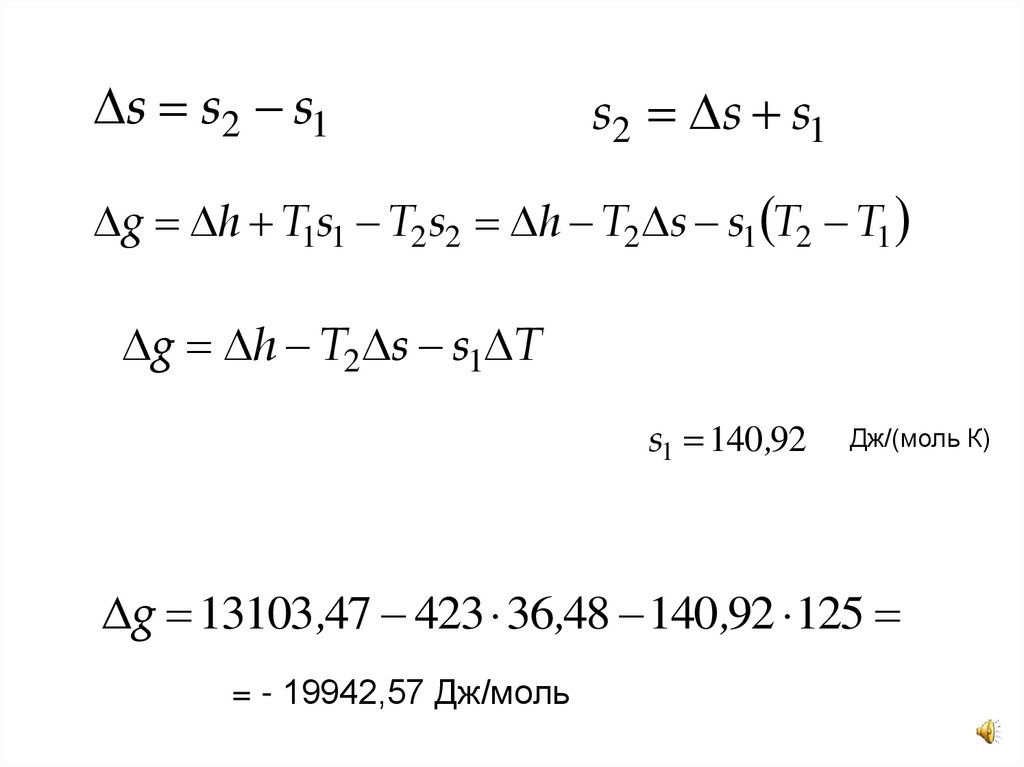


 physics
physics chemistry
chemistry








