Similar presentations:
Производство серной кислоты. Лекция 4-5
1.
ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫЛЕКЦИЯ 4-5
2.
План лекции:Общие сведения;
Сырьё для производства серной кислоты;
Основные
стадии
получения
серной
кислоты;
Особенности технологии получения серной
кислоты из колчедана, серы и сероводорода
и их физико-химические основы;
Пути усовершенствования сернокислотного
производства.
2
3.
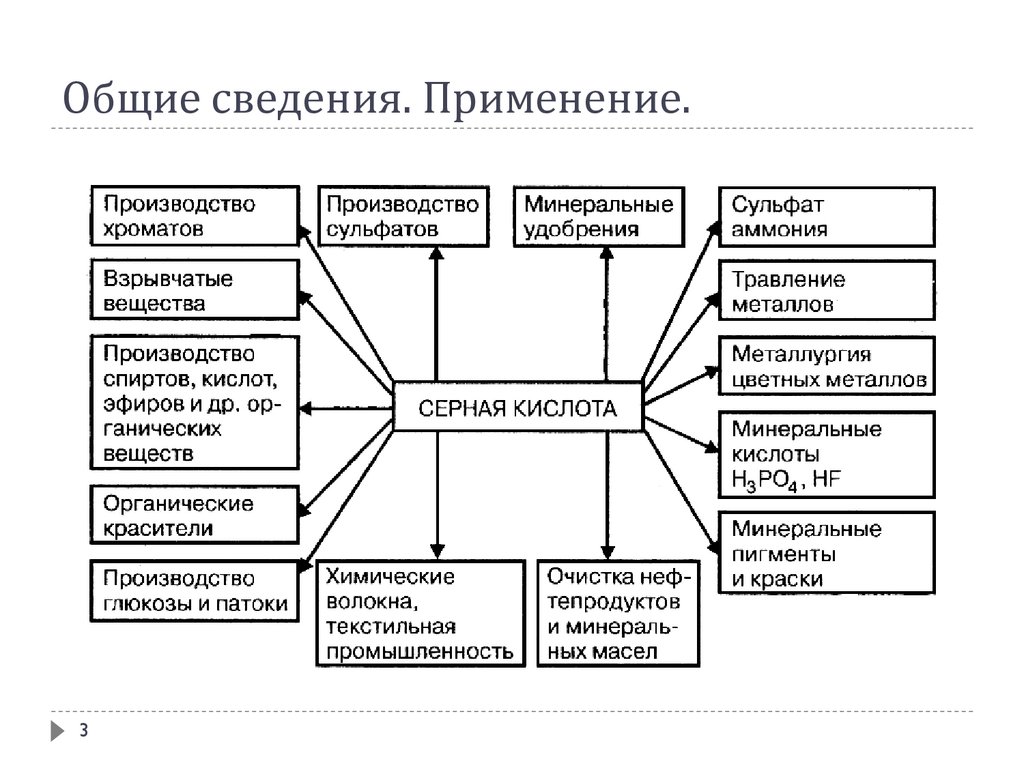
Общие сведения. Применение.3
4.
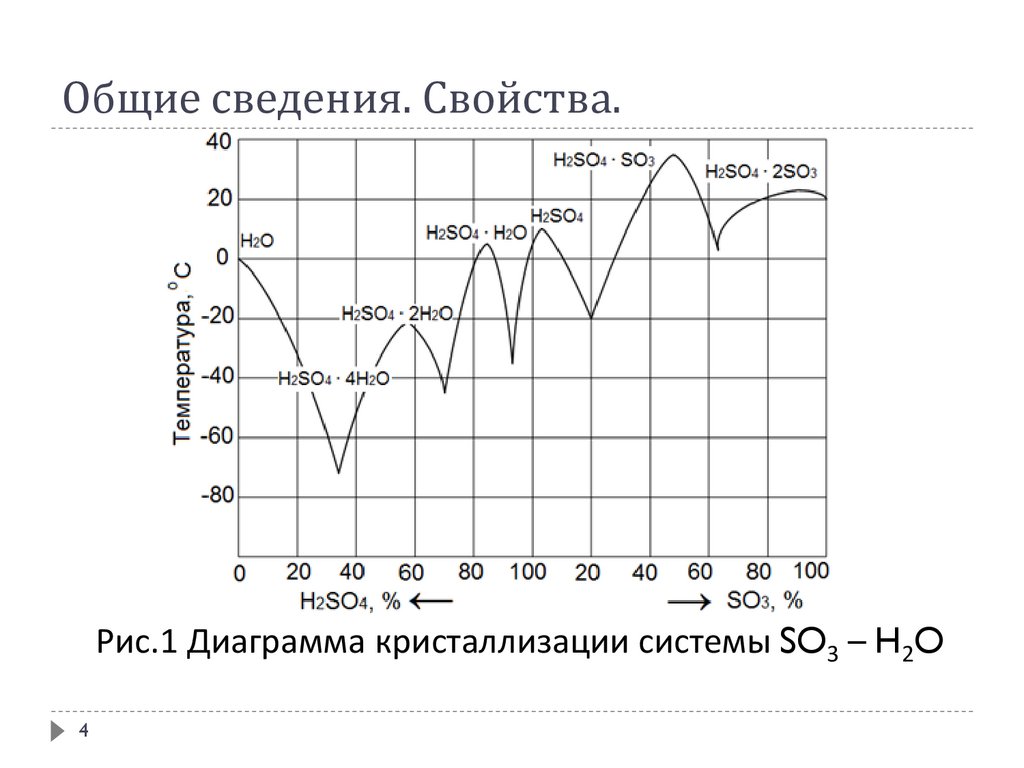
Общие сведения. Свойства.Рис.1 Диаграмма кристаллизации системы SO3 – H2O
4
5.
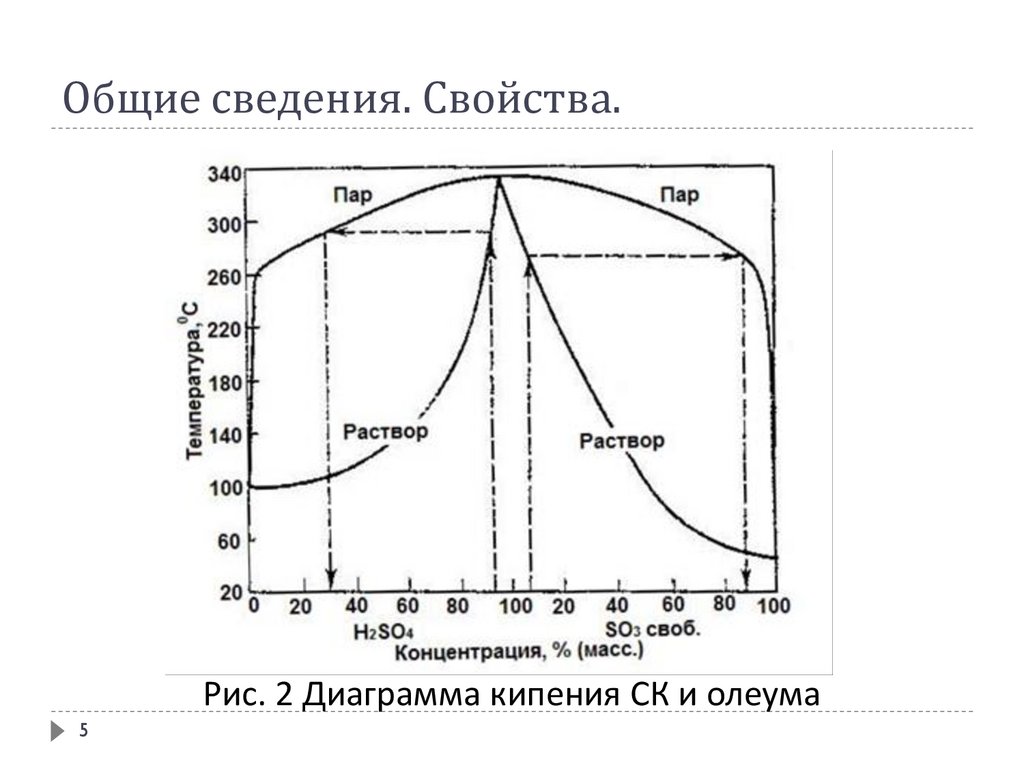
Общие сведения. Свойства.Рис. 2 Диаграмма кипения СК и олеума
5
6.
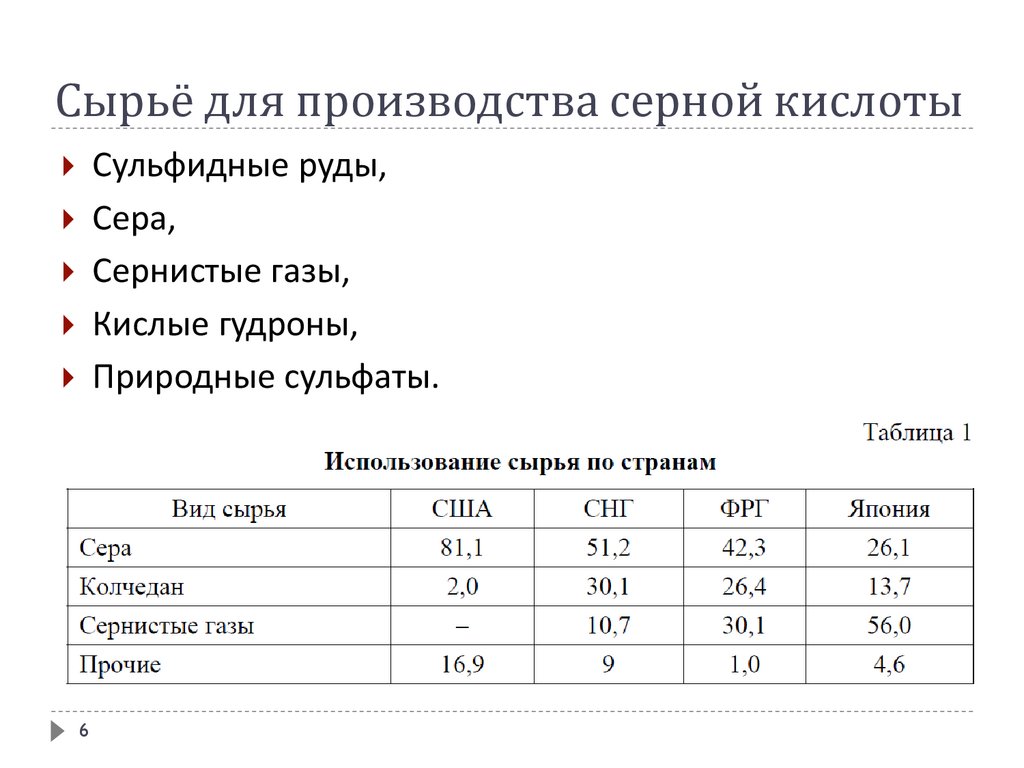
Сырьё для производства серной кислотыСульфидные руды,
Сера,
Сернистые газы,
Кислые гудроны,
Природные сульфаты.
6
7.
Сырьё для производства серной кислотыСерный колчедан
7
8.
Сырьё для производства серной кислотыСера
Сорта серы:
природная и
газовая.
Природная и
газовая сера
выпускаются в
виде: комовой,
молотой, жидкой.
8
9.
Основные стадии производства серной кислотыполучение SO2 (зависит от сырья);
4FeS2 + 11O2 = 2Fe2O3 + 8SO2;
(1)
S + O2 = SO2;
(2)
2Н2S + 3O2 = 2Н2О + 2SO2;
(3)
2Ме + nH2SO4 = Ме2(SO4)n + SO2 + nH2O (4)
2H2SO4 = 2SO2 + O2 +2H2O .
9
(5)
10.
Основные стадии производства серной кислотыокисление SO2 с целью получения SO3:
2SО2(г.) + О2(г.) ↔ SО3(г.)
абсорбция SO3 с образованием H2SO4:
SО3 + Н2О = Н2SО4
очистка отходящих газов.
10
11.
Получение сернистого газа из колчедана.Физико-химические основы.
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
(1)
FeS2 = FeS + S
S + О2 = SO2
4FeS + 7О2 = 2Fe2O3 +4SO2
(1а)
(1б)
(1в)
В результате реакции образуются обжиговый газ и огарок.
Состав обжигового газа:
оксид серы(IV) (12–15 %);
избыточный кислород воздуха;
азот воздуха;
газообразные соединения мышьяка, селена и теллура;
влага (колчедана и воздуха);
пыль.
11
12.
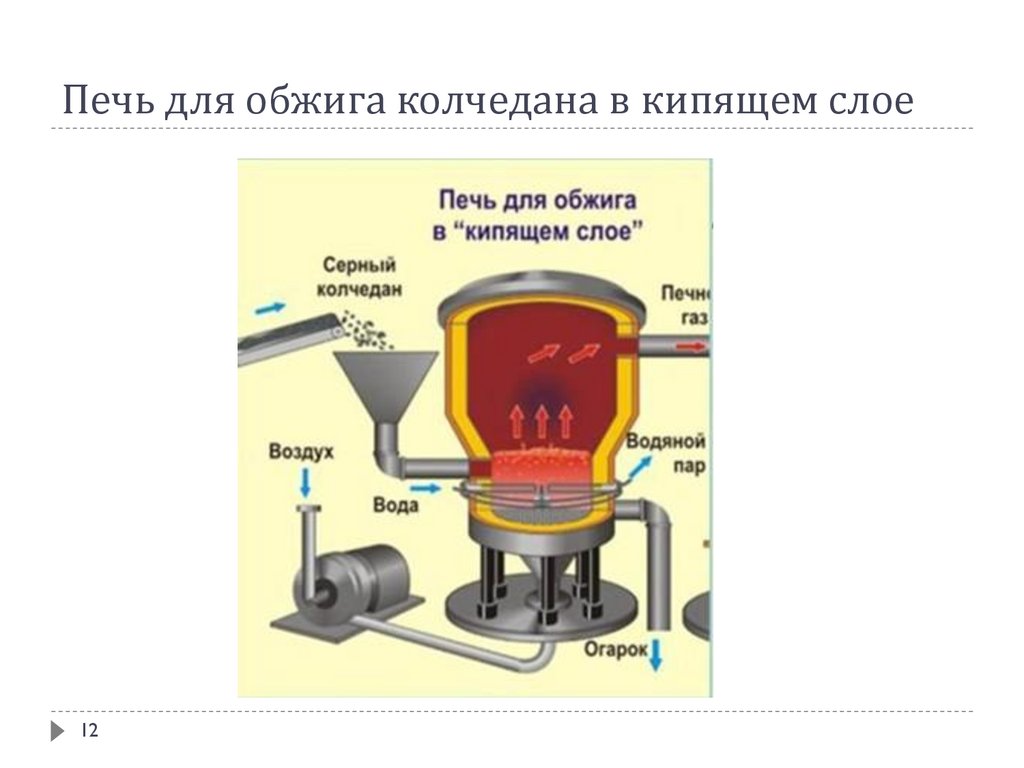
Печь для обжига колчедана в кипящем слое12
13.
Получение сернистого газа из серы.Физико-химические основы.
S + O2 = SO2; ∆Н = –295 кДж/моль
Механизм реакции, происходящей в капле расплавленной серы:
Sn → S8• + Sn–8;
Sn + S8• → S8 + Sn–8• + S8;
Sn–8• + Sn → Sn–8 + Sn–8 + S8•;
Sn–8 + S8• → S8 + Sn–16 + S8
13
14.
Печь для сжигания серы14
15.
Печь для сжигания серы15
16.
Окисление сернистого газа.Физико-химические основы.
2SО2(г.) + О2(г.) ↔ SО3(г.); ∆Н < 0
Равновесный выход SО3 зависит
следующих условий:
состава исходной газовой смеси;
температуры;
давления.
16
от
17.
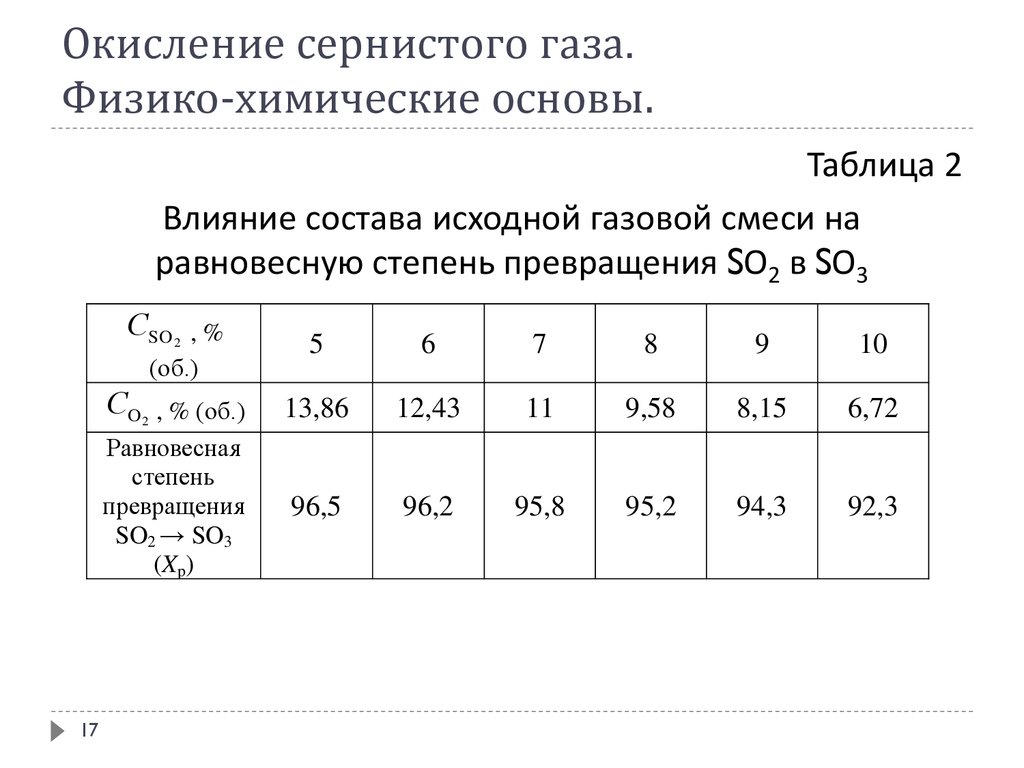
Окисление сернистого газа.Физико-химические основы.
Таблица 2
Влияние состава исходной газовой смеси на
равновесную степень превращения SО2 в SО3
СSO 2 , %
5
6
7
8
9
10
СO2 , % (об.)
13,86
12,43
11
9,58
8,15
6,72
Равновесная
степень
превращения
SO2 → SO3
(Xp)
96,5
96,2
95,8
95,2
94,3
92,3
(об.)
17
18.
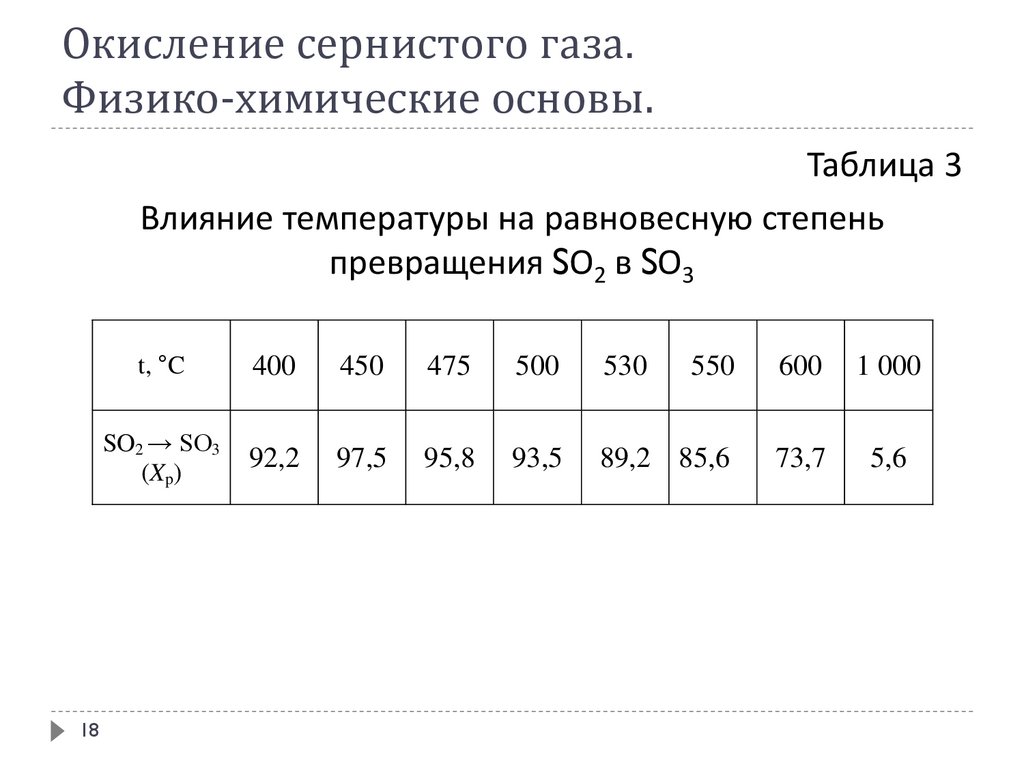
Окисление сернистого газа.Физико-химические основы.
Таблица 3
Влияние температуры на равновесную степень
превращения SО2 в SО3
18
t, °C
400
450
475
500
530
550
600
1 000
SO2 → SO3
(Xp)
92,2
97,5
95,8
93,5
89,2 85,6
73,7
5,6
19.
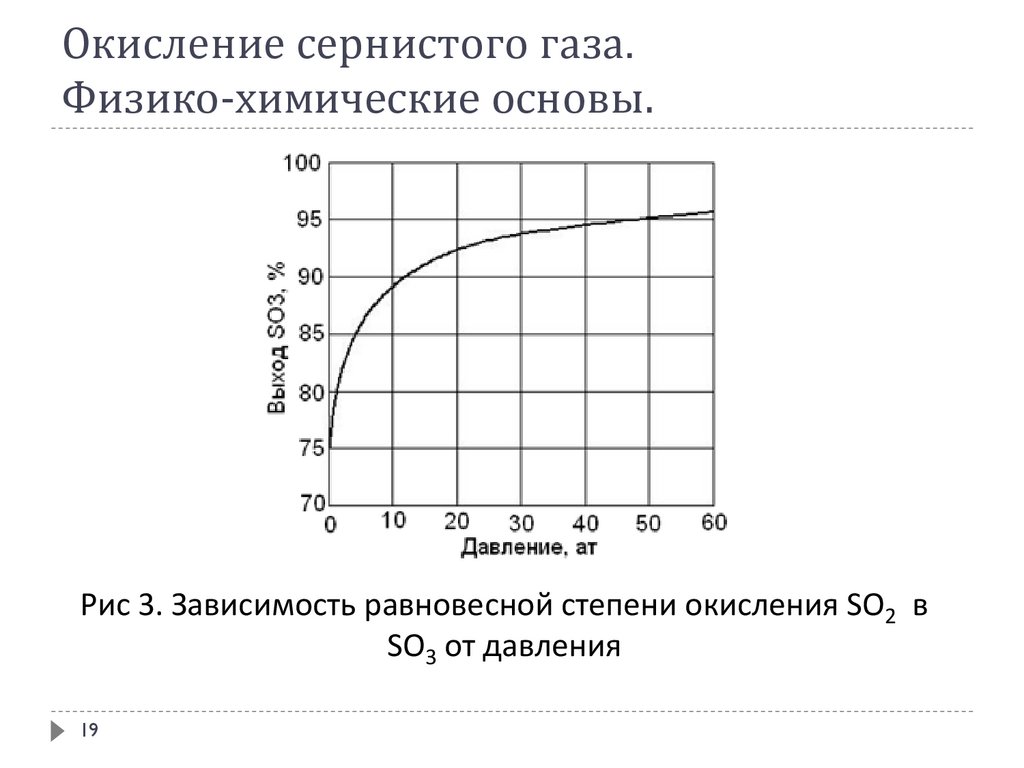
Окисление сернистого газа.Физико-химические основы.
Рис 3. Зависимость равновесной степени окисления SО2 в
SО3 от давления
19
20.
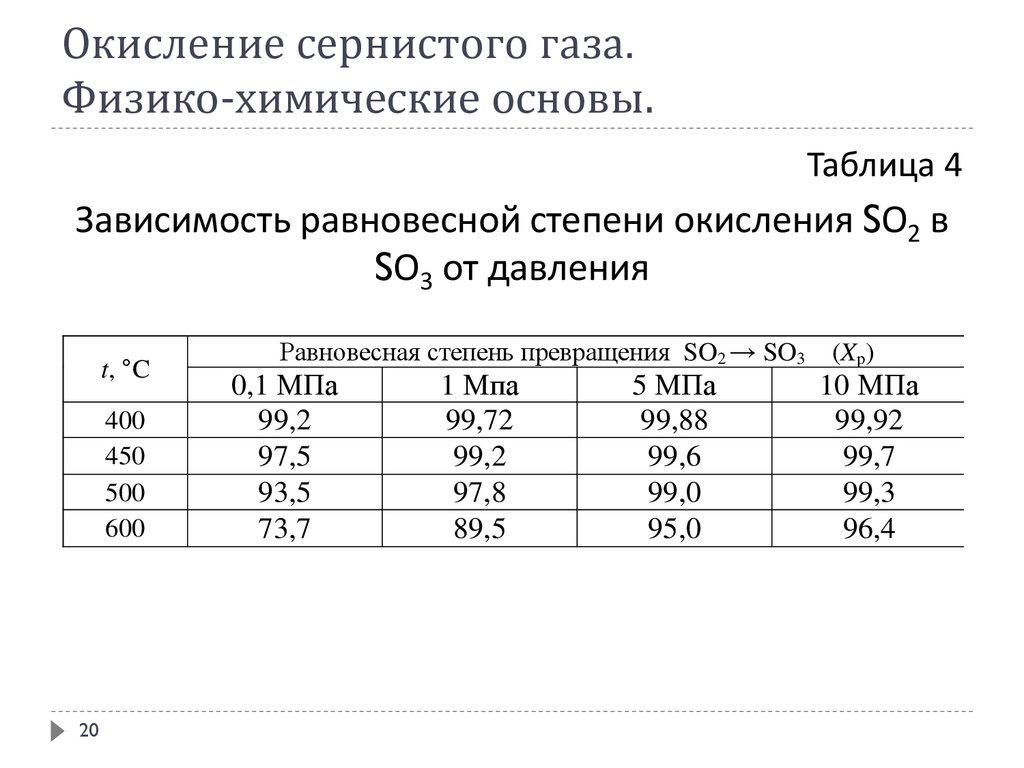
Окисление сернистого газа.Физико-химические основы.
Таблица 4
Зависимость равновесной степени окисления SО2 в
SО3 от давления
t, °C
400
450
500
600
20
Равновесная степень превращения SO2 → SO3
0,1 МПа
99,2
97,5
93,5
73,7
1 Мпа
99,72
99,2
97,8
89,5
5 МПа
99,88
99,6
99,0
95,0
(Xp)
10 МПа
99,92
99,7
99,3
96,4
21.
Окисление сернистого газа.Физико-химические основы.
Катализаторы:
Платина;
Оксид железа(III);
Оксид ванадия(V).
В промышленности применяют следующие типы ванадиевых
катализаторов:
БАВ – бариево-алюмованадиевый катализатор.
СВД – сульфо-ванадиевый на доломите.
СВС – сульфованадат на селикагеле.
СВНТ – сульфованадат низкотемпературный.
21
22.
Окисление сернистого газа.Физико-химические основы.
Высокими
показателями
обладают
отечественные катализаторы ИК 1-6, ТС и ЛТИ .
22
новые
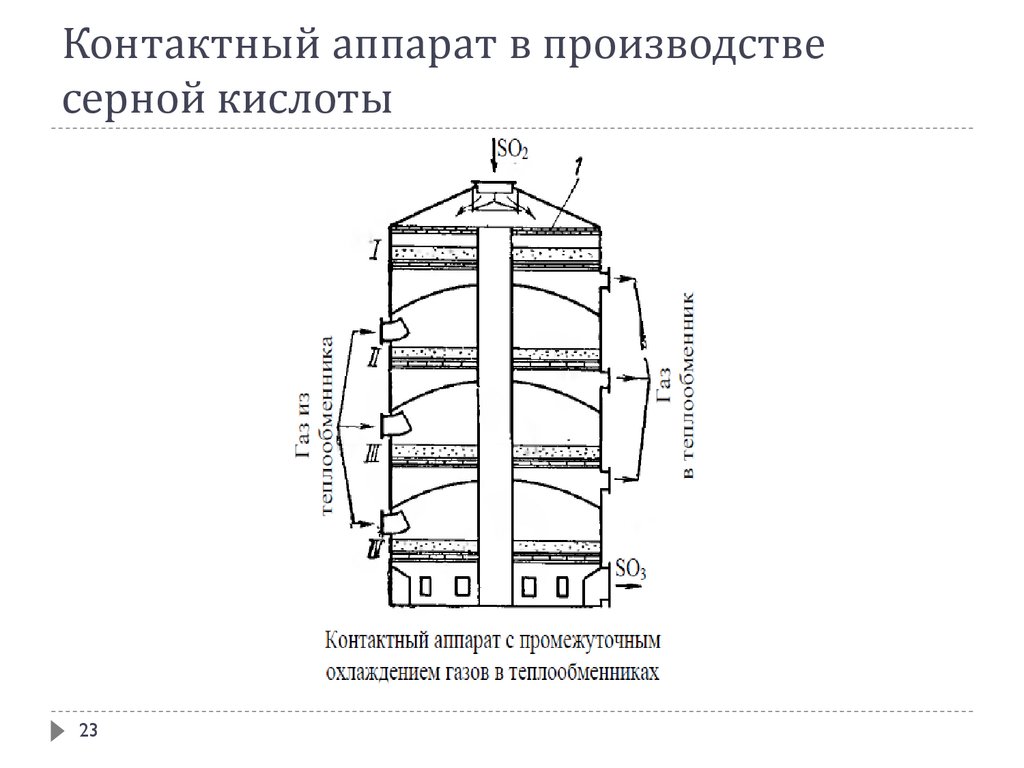
23.
Контактный аппарат в производствесерной кислоты
23
24.
Абсорбция серного ангидрида.Физико-химические основы.
Получение моногидрата:
SО3 + Н2О = Н2SО4;
∆H < 0
В промышленности моногидратом называют серную кислоту
с концентрацией несколько меньшей 100 % (98 %).
Дальнейшим насыщением получают олеум:
nSО3 + Н2SО4 = Н2SО4∙nSО3
24
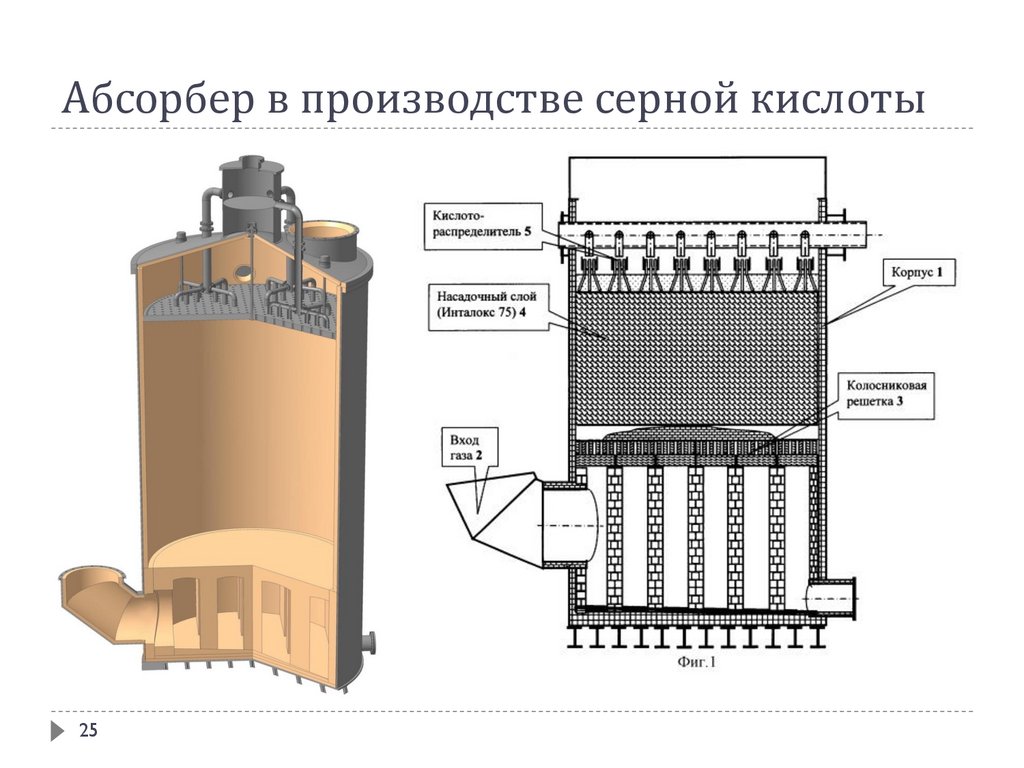
25.
Абсорбер в производстве серной кислоты25
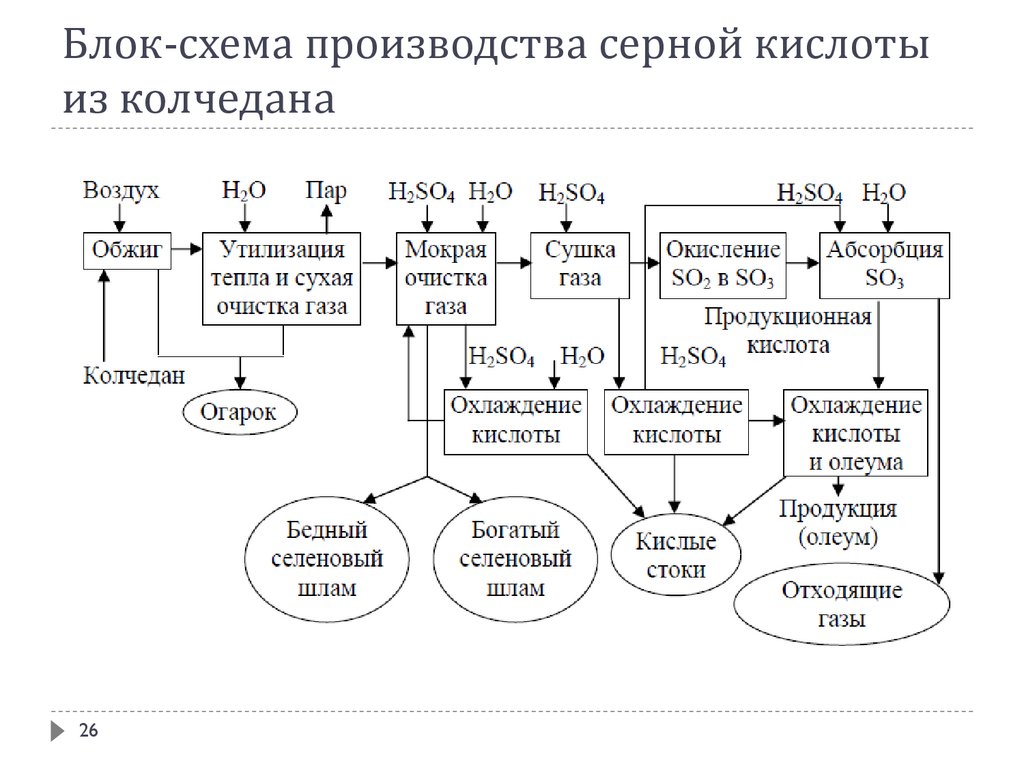
26.
Блок-схема производства серной кислотыиз колчедана
26
27.
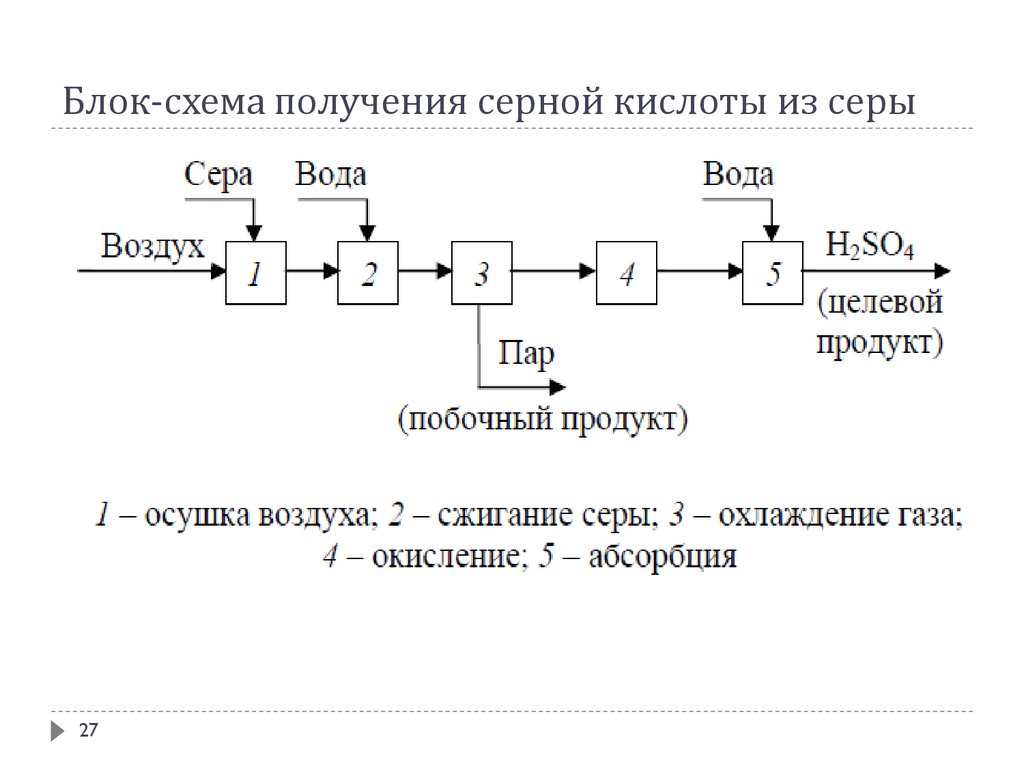
Блок-схема получения серной кислоты из серы27
28.
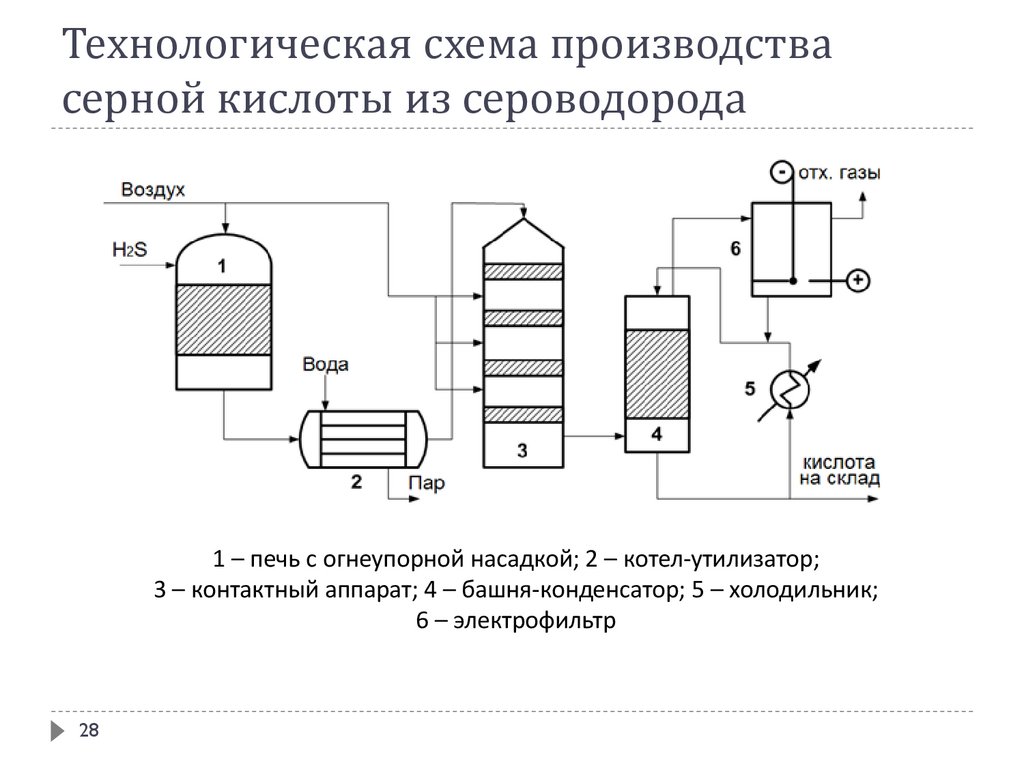
Технологическая схема производствасерной кислоты из сероводорода
1 – печь с огнеупорной насадкой; 2 – котел-утилизатор;
3 – контактный аппарат; 4 – башня-конденсатор; 5 – холодильник;
6 – электрофильтр
28
29.
Пути усовершенствованиясернокислотного производства
Расширение сырьевой базы;
Повышение единичной мощности установок,
например, за счёт улучшения конструкции
отдельных аппаратов или повышения давления в
системе в целом;
Применение новых катализаторов с повышенной
активностью и более низкой температурой
зажигания;
Использование тепловых эффектов химических
реакций на всех стадиях производства и для
выработки энергетического пара;
29
30.
Пути усовершенствованиясернокислотного производства
При повышении давления в системе обеспечиваются следующие положительные
факторы улучшения технологических показателей сернокислотных систем:
В соответствии с принципом Ле-Шателье увеличивается
выход SO3 при взаимодействии SO2 с O2 на катализаторе.
Возрастает степень использования сырья, уменьшаются
выбросы SO2 в атмосферу. При этом может быть достигнута
степень окисления SO2 99,95–99,99%.
Объемы
перерабатываемого
газа
уменьшаются
пропорционально давлению, что позволяет создать мощные
системы с малыми размерами аппаратов. Диаметры
аппаратов системы мощностью 700–750 тыс. т/год при
давлении 1,0–1,2 МПа не превышают 3,5–3,6 м (в обычных
системах мощностью 450–500 тыс. т/год диаметр контактного аппарата равен 13 м).
30
31.
Пути усовершенствованиясернокислотного производства
Удельная металлоемкость системы снижается в 2,5–3,0
раза. Сокращается производственная площадь, занятая
сернокислотной системой.
Резко снижается (в 6–7 раз) расход катализатора по
сравнению с обычной системой.
Увеличивается скорость горения серы, окисления SO2,
абсорбции SO3, что позволяет применять для этих
процессов новые аппараты.
Появляется возможность получать непосредственно в
производстве СК 100% SO3 и высококонцентрируемый
олеум с содержанием SO3 до 65%.
31
32.
Самостоятельно:Очистка обжигового газа при производстве СК из
колчедана;
Информация о новых катализаторах ИК 1-6, ТС и
ЛТИ;
Утилизация отходов и обезвреживание отходящих
газов в производстве СК.
32


















 chemistry
chemistry








